Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.63 no.4 Palmira Oct./Dec. 2014
https://doi.org/10.15446/acag.v63n4.42038
Doi: http://dx.doi.org/10.15446/acag.v63n4.42038
Ciencias del Suelo
Formas de hierro y aluminio en suelos con diferentes usos en la zona norte del departamento del Magdalena, Colombia
Iron and aluminium forms in soils with different uses in Magdalena, Colombia
José Rafael Vásquez Polo1*, Felipe Macías Vázquez2 y Juan Carlos Menjivar Flores3
1Universidad del Magdalena, Colombia; 2Universidad Santiago de Compostela, España; 3Universidad Nacional de Colombia sede Palmira, Colombia. Facultad de Ciencias Agropecuarias. Autor para correspondencia: jvasquez@unimagdalena.edu.co
Rec.:13.02.2014 Acep.: 21.04.2014
Resumen
En el estudio se evaluaron las diferentes formas de hierro (Fe) y aluminio (Al) presentes en suelos cultivados y en áreas de bosque de la zona norte del departamento del Magdalena (Colombia). Se seleccionaron seis zonas de muestreo localizadas entre 0 y 1000 m.s.n.m. Se utilizaron tres técnicas selectivas de extracción de Fe y Al con los agentes extractantes: pirofosfato de sodio, oxalato ácido de amonio, y ditionito citrato bicarbonato. Los contenidos totales de Fe y Al fueron determinados mediante un ataque ácido y cuantificación por absorción atómica. El análisis de varianza multivariado mostró diferencias significativas (P < 0.05) entre zonas y usos del suelo para todas las formas de Fe y Al extraídas, las cuales fueron mayores en suelos de bosques, en comparación con suelos de cultivo. Una alta proporción de Fe forma parte estructural de silicatos, en menor proporción de oxihidróxidos cristalinos y en una proporción muy baja se encuentra ligado a compuestos orgánicos; esto refleja una pobre evolución del humus en las zonas estudiadas. El Al extraído con oxalato amónico fue bajo (> 3% del Al total), lo que sugiere que un alto contenido de Al forma parte de estructuras cristalinas.
Palabras clave: Óxidos de hierro y aluminio, extracción química selectiva.
Abstract
Different forms of iron (Fe) and aluminum (Al) present in soils with different uses in the northern department of Magdalena (Colombia) were evaluated. Six sampling areas located between 0-1000 meters, including cultivated soils and soils of cultivated areas adjacent to forests were selected. Three selective extraction techniques Fe and Al were used as extracting agents used: sodium pyrophosphate, acid ammonium oxalate and dithionite citrate bicarbonate, the total content of Fe and Al were determined (t) by an acid attack and quantified by atomic absorption. The analysis of variance shows that there are significant differences (p < 0.05) between areas and land uses for all forms of Fe and Al extracted, which were higher for forest soils compared to agricultural soils, thus large proportion a structural part of Fe silicates in crystalline oxyhydroxides less content and a very low proportion, linked to organic compounds, this reflects a poor evolution of humus in the study areas. The Al extracted with ammonium oxalate was low (less than 3% of total Al), suggesting that a high Al content is part of crystal structures.
Key-words: Iron and aluminum oxides, selective chemical extraction.
Introducción
En Colombia, al igual que en otros países, la ampliación de las fronteras agrícola y pecuaria ha convertido extensas áreas de bosques en cultivos y pasturas, lo que ha acelerado la degradación de los suelos, especialmente en los ecosistemas de bosques secos tropicales que con frecuencia son objeto de colonización mediante tala y quema de la vegetación nativa (Ceballos, 1995).
En el departamento del Magdalena (Colombia) 46.74% del área es de vocación agrícola; 16.65% corresponde a zonas de manejo especial, en las que se incluyen reservas forestales, resguardos indígenas y parques naturales; 12.88% es de vocación agroforestal; 7.84% está dedicada a la ganadería; 5.30% es forestal; y sólo 3.03% corresponde a áreas de conservación y zonas urbanas. El área potencialmente cultivable en este departamento es de 1.084.860 ha, aproximadamente, que corresponden a 46.74% del área total (IGAC, 2009).
Los óxidos de hierro se emplean como indicadores de la pedogénesis y son minerales que se presentan en cristales muy pequeños que afectan las propiedades de suelos altamente meteorizados, ya que pueden agregar, dispersar o revestir otros minerales (Acevedo et al., 2004); El aluminio (Al) tiene un papel importante en la acidificación del suelo (Thomas y Hargrove, 1984). Los óxidos, hidróxidos y oxihidróxidos de Al adsorben grandes cantidades de metales en traza y tienen además una importante influencia en la sorción y disponibilidad de fosfatos (Zhang et al., 1997).
Procesos como la formación de agregados, la cementación, la formación de nódulos, entre otros, están directamente relacionados con la presencia de óxidos de hierro (Duiker et al., 2003). Wierzchos et al. (1992) encontraron que la remoción selectiva de óxidos de Fe y Al y de materia orgánica (M.O.) influyen en la microestructura del suelo, actuando como agentes floculantes. Percival et al. (2000) y Matus et al. (2008) sugieren que formas no cristalinas de Al, hidróxidos y complejos órgano alumínicos insolubles deben ser considerados como los parámetros clave para la estabilización de la M.O. en suelos Andicos, en lugar de alófano (o imogolita); por otra parte, los filosilicatos de arcillas, con sus grandes superficies, son considerados, con frecuencia, como parte importante en la estabilización de la M.O. en los suelos, protegiéndola del ataque microbiano.
Un procedimiento de extracción de una sola etapa usando un apropiado extractante permite la separación de una fracción caracterizada por propiedades particulares. Este procedimiento permite la evaluación cualitativa y la determinación cuantitativa de las fracciones solubles del metal, así como formas fácilmente intercambiables disponibles para las plantas, los animales y el hombre. El procedimiento de extracción de un solo paso es utilizado para el fraccionamiento del Al en los suelos agrícolas y forestales (Zhu et al., 2004, Takeda et al., 2006, Frankowski et al., 2013)
Existen varios métodos para la extracción selectiva de las fracciones de C, Al, Fe, especialmente cuando se consideran formas móviles y fracciones lábiles o reactivas; incluyendo Na2B4O7, CuCl2 , LaCl3, y KCl, entre otras (Jansen et al., 2011). No obstante, para Al y Fe en la actualidad se utilizan diferentes métodos de disolución selectiva (MDS), entre ellos extracciones con oxalato de amonio ácido, pirofosfato de Na o ditionito-citrato. La utilidad de estos métodos es limitada por el corto rango de ordenación y grado de cristalinidad de los componentes, así mismo, por la baja tendencia del Al en comparación con el Fe para formar oxihidróxidos.
Aunque los MDS utilizados no siempre son específicos para un grupo determinado de compuestos de Al, Si o Fe, algunos de ellos son razonablemente específicos para la mayoría de los suelos (García-Rodeja et al., 2007), no obstante, aún no está claro si el manejo de los suelos puede modificar el contenido de estos compuestos. Teniendo en cuenta estos interrogantes, la presente investigación tuvo como objetivo evaluar el efecto del uso del suelo sobre las formas extraíbles de Fe y Al determinados por diferentes métodos en la zona norte del departamento del Magdalena Colombia.
Materiales y métodos
La investigación se realizó en los municipios de Santa Marta, Ciénaga, Dibulla y Aracataca en la zona bananera, considerados a partir de estudios previos del IGAC (2009) como la mayor zona con cultivos de importancia económica al noreste del departamento del Magdalena y localizados entre las coordenadas 11° 36' 58" - 8° 56' 25" N y 73° 32' 50" - 74° 56' 45" O.
Mediante un muestreo aleatorio estratificado se seleccionaron seis zonas o estratos diferenciados por el tipo de uso del suelo. En cada una de ellas fueron seleccionados dos sitios de muestreo, uno de cultivo y otro en área de bosque, excepto en la zona 4 donde se seleccionaron tres (dos de cultivo y uno de bosque) para recolectar cuatro muestras de suelo entre 0 y 20 cm de profundidad (ICA, 1992). Las característica de clima y suelos en cada zona aparecen en el Cuadro 1.
La densidad aparente (Da) fue determinada por el método del cilindro (IGAC, 2006) y la textura de los suelos por el método del hidrómetro de Bouyoucos, el pH en agua (1:2.5) (IGAC, 2006), los minerales Ca, Mg, K y Na fueron extraídos por digestión ácida y determinados por espectrofotometría de absorción atómica, el N y el C total se determinaron mediante un analizador LECO (Modelo CHN-1000, LECO Corp., St Joseph, MI).
La extracción selectiva de Al y Fe se realizó por las metodologías siguientes: (1) Utilizando pirofosfato sódico (Na4P2O7.10H2O) 0.1 M (Smith, 1994) y filtrando los extractos en filtros Albert (0.45 µ) para minimizar errores en las determinaciones por la posible presencia en suspensión de partículas inorgánicas como ferrihidrita. Con este método se solubilizan los complejos orgánicos de Al (Alp) y Fe (Fep). (2) Extracción con oxalato amónico 0.2M tamponado a pH 3 (Blakemore, 1983); en este caso, el extractante es una mezcla de oxalato amónico 0.2M ((NH4)2C2O4.H2O) y oxalato ácido (H2C2O4.2H2O) en proporción 1:0.75 para la extracción de formas de Al y Fe ligadas a óxidos amorfos, óxidos hidratados, aluminosilicatos no cristalinos y a la M.O. (Alo y Feo, respectivamente). (3) Extracción con ditionito-citrato sódico 0.5M en medio reductor Holmgren (1967). Con esta metodología se solubilizan óxidos cristalinos de Fe, así como el Fe presente en compuestos inorgánicos no cristalinos y asociados con la M.O., además es un buen estimador de la cantidad de Fe y Al libre total (Fed y Ald, respectivamente). El Fe y Al total (Fet y Alt) se extrajeron por digestión ácida de la muestra con ácido perclórico y ácido fluorhídrico. En todos los casos, las concentraciones de Al y Fe fueron determinadas mediante espectrofotometría de absorción atómica (Perkin Elmer 2380, Norwalk, CT). Los datos fueron sometidos a correlación y análisis de varianza multivariado (arreglo factorial) utilizando el programa SPSS v20, con el objeto de establecer posibles diferencias estadísticas entre usos del suelo, zonas de muestreo y su interacción, para las diferentes formas de Fe y Al determinadas.
Resultados y discusión
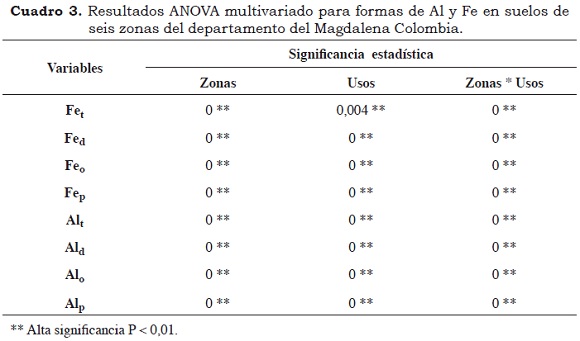
Los análisis mostraron correlación (P < 0.01) entre las diferentes formas de Fe y Al extraídas y las propiedades físico-químicas de los suelos (Cuadro 2), destacando las correlaciones negativas con el pH, lo que concuerda con los hallazgos de Bronick et al. (2005). El Nt mostró correlación positiva (P < 0.01) con todas las formas de Fe. El análisis multivariado mostró que existen diferencias significativas entre zonas, usos del suelo y su interacción para todas las formas de Fe y Al extraídas (Cuadro 3 y Cuadro 4), lo que contrasta con los resultados de Ramírez et al. (2009) quienes no encontraron diferencias en el contenido de Fet por efecto del uso del suelo.
En términos generales, los contenidos de las diferentes formas de Fe y Al presentaron una heterogeneidad moderada a alta, siendo mayores para los suelos de bosques, en comparación con los suelos de cultivo, destacando los mayores valores de Fet en la zona 1 (54.8 g/kg) y el menor valor en la zona 2 en el cultivo de palma africana (7.46 g/kg). En este sitio fue evidente un alto detrimento en los contenidos de Fe en relación con los suelos de bosques próximos.
Los valores de Fed (Fe libre extraído con ditionito) fueron más altos (P < 0.05) que los valores de Feo (Fe extraído con oxalato) y con pirofosfato (Fep), con valores promedio de 9.56 g/kg para suelos de bosque y de 6.93 g/kg en suelos cultivados. Estas diferencias muestran que el Fe se encuentra principalmente formando parte de los oxihidróxidos cristalinos.
Los bajos contenidos de Feo (2.27 g/kg) para suelos de bosque y 1.90 g/kg para suelos de cultivo, indican la presencia de pequeñas cantidades de Fe amorfo; sin embargo, son aún más pequeñas las cantidades de Fe relacionadas con los complejos orgánicos (Fep) que presentaron valores de 0.02 g/kg en suelos de bosque y 0.01 g/kg en suelos de cultivo (Cuadro 4).
El contenido de Fe libre extraído con ditionito representó, respectivamente, 22.8% y 29% del Fe total para suelos de cultivos y bosques. El Fe silicatado (Fet - Fed) presentó comportamientos similares en los diferentes usos del suelo, no obstante en las zonas 1 (Café), 3 (suelo arado) y 5 (frutales) los valores superaron a los encontrados en suelos de bosques (Cuadro 5). Esto se debe, posiblemente, a que en la medida que aumenta la intensidad de uso del suelo, incrementa el contenido de Fe-silicatado (Acevedo et al., 2008; Ramírez et al. 2009).
En el Cuadro 4 antes citado, se muestran los valores del Fe presente en los óxidos de hierro cristalinos (goethita y hematita) (Fed - Feo). Según Smith (1994) la presencia de estos minerales depende de una buena aireación, temperatura y humedad adecuadas, además de un alto potencial reductor-oxidante en el suelo; para los suelos de cultivo el valor promedio (5.03 g/kg) representó 16.36% del Fe total y para los suelos de bosques (7.29 g/kg) el 22.10%. En las zonas 5 y 6 los óxidos de Fe cristalinos representaron, aproximadamente, 5.6% del Fe total. Por otra parte, 77.14% y 71% del Fe total forma parte de la estructura de los silicatos (Fet - Fed) para los suelos de cultivos y bosques, respectivamente, llegando hasta 93% para los suelos de cultivo en la zona 6.
La relación Feo:Fed varió entre 0.2 y 0.62 g/kg en suelos de cultivo y entre 0.14 y 0.41 g/ kg en suelos de bosque con valores de medios a bajos en la concentración de Fe amorfos, resultados que concuerdan con los obtenidos por Acevedo et al. (2002). Los menores valores de la relación Fep:Fed (0.0037) y los valores bajos, entre 0.002 y 0.026, en la relación Fep/ Feo indican una muy limitada asociación de Fe con los compuestos orgánicos. Es posible que la escasa afinidad de este elemento con el tipo de M.O. se deba a la presencia de humus joven con baja capacidad para la formación de complejos o al poco aporte del elemento por el material parental que dio origen a estos suelos.
En relación con la extracción selectiva de Al, se presentaron valores mayores de Alo en relación con los extraídos con ditionitocitrato, debido posiblemente a que éste es menos eficiente para la extracción de Al y sólo sirve cuando existe mucho aluminio ligado a los óxidos de Fe cristalinos (García-Rodeja et al., 2007). Los valores medios de Ald en suelos de cultivo (0.51 g/kg), Ald en bosque (0.64 g/kg), Alo en cultivo (0.65 g/kg) y Alo en bosque (0.92 g/kg) son similares a los encontrados por Dahlgren y Ugolini (1991) en profundidades > 20 cm en Andosoles quienes atribuyeron esta diferencia (Alo > Ald) a la presencia de alumino-silicatos de bajo grado de cristalinidad.
El Al amorfo representó sólo 2.5% del Al total en suelos de cultivos y 3% en suelos de bosques, lo que sugiere un alto porcentaje del Al formando parte de estructuras cristalinas (Zysset et al., 1999). Los valores de oxalato ácido son un índice del grado de acumulación de los productos amorfos de reciente alteración, además la fracción amorfa de los suelos se relaciona con problemas de labranza como dispersión, floculación, agregación, infiltración, erosión y estabilidad de los suelos (Schcaefer et al., 1999). El Al extraído por oxalato ácido es considerado como indicativo de oxihidróxidos e hidróxidos de Al, los cuales pueden estar o no asociados con sustancias húmicas y alumino-silicatos amorfos (Paterson et al., 1993).
La extracción selectiva de Al con pirofosfato (complejos orgánicos de Al) fue muy baja, con valores menores que 0.3% del Al total, lo que unido a las bajas relaciones Alp:Alo (< 0.12), indica que el bajo Al activo presente en el suelo se encuentra unido a compuestos amorfos. Con el uso de oxalato ácido se extrajeron cantidades más altas que con pirofosfato, lo que marca la diferencia Alo - Alp e indica la presencia de Al paracristalino y no cristalino, aunque ésta es muy baja en relación con el total (Alt - Alo), de donde se puede deducir que 98% del Al pertenece a la estructura de los silicatos.
Aunque los datos indican diferencia entre los contenidos de las diferentes formas de Fe y Al en los suelos, cuando se analizan estos nutrientes en forma individual por zonas las diferencias son menores y es posible establecer un comportamiento común en todos los casos. El porcentaje de Fe total varió entre 0.8 y 5.5%, con una mayor ocurrencia entre 2% y 3%; lo que significa que las rocas son relativamente pobres en Fe, tal como corresponde a rocas intermedias o ácidas. De este contenido de Fe la mayor parte se encuentra en las redes silicatadas, sin ser liberado por alteración. El porcentaje de Fe cristalino extraíble con ditionito-citrato, que representa los compuestos de este elemento presentes como oxihidróxidos tanto cristalinos como amorfos, es bajo; siendo en la mayoría de las muestras < 30% del Fe total, con excepción de los suelos con bosque en la zona 2 (49.7%) y con cultivo de café en la zona 1 (35.5%). Estos bajos porcentajes de Fe libre se asocian siempre con suelos de alteración y evolución incipiente, lo que está de acuerdo con su clasificación como Entisoles o Inceptisoles. No se observaron procesos avanzados de edafogénesis propios de los sistemas tropicales con alteración y evolución intensa. El Fe extraíble con oxalato, que representa las formas de baja cristalinidad, presentó en la mayor parte de las muestras menos del 10% del Fe total, lo que indica que el Fe liberado de los silicatos es rápidamente cristalizado y se mantiene un pequeño porcentaje en forma de bajo grado de orden. Esto está relacionado con la existencia de períodos secos que favorecen la cristalización, respondiendo así al régimen ústico existente y dominante en toda la zona. Finalmente, el Fe extraíble con pirofosfato, atribuido a las formas complejadas prácticamente no existe, lo que indica que el Fe juega un papel importante en la floculación y meta-estabilización de la M.O. en estos suelos.
El contenido de Al total fue bajo y varió entre 0.7% y 4.4%. Las formas de mayor reactividad, que son extraídas con oxalato, representaron entre 1.6 y 5.9% del Al total, siendo los valores más elevados los correspondientes a los suelos de cultivo de café y bosque de las zonas de mayor precipitación con suelos clasificados como Typic Eutrudept. En estos suelos se alcanzaron los valores más altos para el índice ándico (Alo+1/2Feo, en porcentaje), siendo de 0.22% en el cultivo de café y 0.25% en el bosque, lo que pone de manifiesto la total ausencia de propiedades ándicas, incluso en las zonas de alta precipitación (2000 mm). Los resultados ponen de manifiesto que el Al se encuentra fundamentalmente en los minerales primarios y que sólo existe liberación de este elemento. Una situación similar ocurre si se analiza el Al extraíble con pirofosfato donde el valor máximo absoluto fue de 0.12% y la mayor parte de los resultados estuvieron alrededor de 0.01%. Por tanto, puede afirmarse que los suelos n en estudio son muy incipientes y que ni el Fe ni el Al representan papel relevante en la floculación y metaestabilización de la M.O., lo que debe ser atribuido exclusivamente a los elementos alcalinotérreos.
Conclusiones
- El uso y manejo de los suelos cultivados afectó los contenidos de las diferentes formas de Fe. Los contenidos medios con las diferentes extracciones de Fe evaluadas fueron mayores para suelos de bosques en relación con los suelos de cultivo, destacando la zona 1, donde las condiciones climáticas determinaron los mayores contenidos de Fe en sus diferentes formas.
- El manejo de los suelos de cultivo incrementó la proporción de formas no lábiles o silicatadas de Fe, en detrimento de la calidad de los mismos; así, los suelos estudiados presentan una limitada afinidad del Fe con la M.O., además del poco Fe lábil por el predominio de humus joven con una baja capacidad para la formación de complejos.
- El Al corresponde a la estructura de los silicatos, sin mucha influencia en las condiciones de los suelos estudiados, bien sean de bosque o de cultivo.
Agradecimientos
A la Universidad del Magdalena por los recursos aportados a través de su Fondo para la Investigación-Fonciencias. Al Departamento de Edafología y Química Agrícola de la Universidad de Santiago de Compostela (España) por su apoyo técnico y humano, claves para el normal desarrollo de la investigación.
Referencias
Acevedo-Sandoval, O.; Prieto-Garcia, F.; y Gordillo-Martínez, A. 2008). Identificar las fracciones de aluminio en un Andosol del Estado de Hidalgo, México. Rev. Soc. Geol. España 21(3 - 4):125 - 132. [ Links ]
Acevedo, S.; Ortiz, E.; Cruz, M.; y Cruz, E. 2004. Papel de los oxidos de hierro en suelos. Terra Latinoam 22:485 - 497. [ Links ]
Blakemore, L. C.; Searle, P. L.; y Daly, B. K.. 1981. Soil bureau laboratory methods: A methods for chemical analysis of soils. New Zealand Soil Bureau Scientific Report 10a. p. 44 - 45 [ Links ]
Bronick, C. J. y Lal, R. 2005. Soil structure and management: a review. Geoderma 124 (1 - 2):3 - 22 [ Links ]
Ceballos, G. 1995. Vertebrate diversity, ecology, and conservation in neotropical dry forest. En: Bullock, S.; E. Medina; y H. A. Mooney (eds.). ropical Deciduous Forest Ecosystems. Cambridge Univ. Press, Cambridge. pp. 195-222.
Dahlgren, R. A. y Ugolini, F. C. 1991. Distribution and characterization of short range order minerals in Spodosols from the Washington Cascades. Geoderma 48:391 - 413. [ Links ]
Duiker, S.; Rhoton, F.; Torrent, J.; Neil, E.; y Smeck, N. 2003. Iron (hydr)oxidecrystallinity effects on soil aggregation. Soil Sci. Soc. Amer. J. 67:606 - 611. [ Links ]
Frankowski, M.; Zio1a-Frankowska, A.; y Siepak, J. 2013. From soil to leaves e aluminum fractionation by single step extraction procedures in polluted and protected areas. J. Environ. Manag. 127:1 - 9. [ Links ]
García-Rodeja, E.; Nóvoa, J. C.; y Pontevedra, X. 2007. Aluminium and iron fractionation of european volcanic soils. Soils of Volcanic Regions in Europe. 2007. Springer. P. 325 - 351 [ Links ]
Holmgren, G. G. 1967. A rapid citrate-dithionite extractable iron procedure. Soil Sci. Soc. Am. Proc. 31:210 - 211. [ Links ]
ICA (Instituto Colombiano Agropecuario). 1992. Fertilización en diversos cultivos. Quinta Aproximación. Manual de Asistencia Técnica. 64 p. [ Links ]
Jansen, B.; Tonneijck, F.; y Verstraten, J. 2011. Selective extraction methods for aluminium, iron and organic carbon from montane volcanic ash soils. Pedosphere 21(5):549 - 565. [ Links ]
Matus, F.; Garrido, E.; Sepúlveda, N.; Cárcamo, I.; Panichini, M.; y Zagal, E. 2008. Relationship between extractable Al and organic C in volcanic soils of Chile. Geoderma 148:180 - 188. [ Links ]
Paterson, E.; Clark,L.; y Birnie, A. C. 1993. Sequential selective dissolution of iron, aluminium and silicon from soils. Communication. Soil Sci. Plant Anal. En: Periódico Oficial del Estado de Hidalgo. (2001):24(15-16). 2015 - 2023. [ Links ]
Percival, H. J.; Parfitt, R. L.; y Scott, N. A. 2000. Factors controlling soil carbon levels in New Zealand grassland: is clay content important? Soil Sci. Soc. Am. J. 64:1623 - 1630. [ Links ]
Ramírez, R.; Cardona, C. M., y Leiva, E. I.. 2009. El hierro y la estructura de un Andisol bajo labranza y barbechos. Suelos Ecuatoriales 39(2):157 - 162. [ Links ]
Smith, B. F. 1994. Characterization of poorly ordered minerals by selective chemical methods. Clay mineralogy spectroscopic and chemical determinative methods. p: 333 - 357. [ Links ]
Takeda, A.; Tsukada, H.; Takaku, Y.; Hisamatsu, S.; Inaba, J. y Nanzyo, M.2006. Extractability of major and trace elements from agricultural soils using chemical extraction methods: application for phy-toavailability assessment. Soil Sci. Plant Nutr. 52:406 - 417. [ Links ]
Thomas , G. W. y Hargrove, W. L.. 1984. The chemistry of soil acidity. En: F. Adam (ed.). Soil acidity and liming. Agronomy Monograph No. 9. American Society of Agronomy. Crop Science Society of America and Soil Science Society of America. [ Links ]
Vásquez, J. R.; Macías,F.; y Menjivar, J. C. 2010. Variabilidad espacial de propiedades físicas y químicas en suelos de la granja experimental de la Universidad del Magdalena (Santa Marta, Colombia). Acta Agronómica 59(4):449 - 456. [ Links ]
Vera, M. , Sierra,M.; Díez,M.; Sierra, C.; y Martínez, A. 2007. Deforestation and land use effects on micromorphological and fertility changes in acidic rainforest soils in Venezuelan Andes. Soil Tillage Res. (97):184 - 194. [ Links ]
Wierzchos , J.; Ascaso, C.; y García, M. 1992. Changes in microstructure of soils following extraction bonded metals and organic matter. Eur. J. Soil Sci. 43(3):505 - 515. [ Links ]
Zhang, M.; Alva, A. K; Li, Y C.; y Calvert, D. V. 1997. Fractionation of iron, manganese, Al an P in selected sandy soils under citrus production. Soil Sci. Soc. Amer. J. 61(3):794 - 801. [ Links ]
Zhu, M.; Jiang, X.; y Ji, G. 2004. Experimental investigation on aluminum release from Haplic Acrisols in southeastern China. Appl. Geochem. 19:981 - 990. [ Links ]
Zysset, M, Blaser, P.; Luster, J. ; y Gehring,U. 1999. Aluminium control in different horizons of a podzol. Soil Sci. Soc. Am. J.63(5):1106 - 1115 [ Links ]