Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.63 no.4 Palmira Oct./Dec. 2014
https://doi.org/10.15446/acag.v63n4.42035
Doi: http://dx.doi.org/10.15446/acag.v63n4.42035
Protección de cultivos
Detección por PCR de Colletotrichum lindemuthianum en cultivos y semillas de frijol en Antioquia, Colombia
PCR detection of Colletotrichum lindemuthianum in seeds and crops of common bean from Antioquia, Colombia
Leonardo Martínez Pacheco1, Katherin Vanegas Berrouet2, Mauricio Salazar Yepes2, Pablo Gutiérrez Sánchez1 y Mauricio Marín Montoya1
1 Universidad Nacional de Colombia sede Medellín, Facultad de Ciencias, Laboratorios de Microbiología Industrial y Biología Celular y Molecular, Colombia. 2 Universidad Nacional de Colombia sede Medellín, Museo Micológico-MMUNM. Autor para correspondencia: mamarinm@unal.edu.co
Rec.: 13.02.2014 Acep.: 05.06.2014
Resumen
Colletotrichum lindemuthianum, agente causal de la antracnosis del frijol, es uno de los patógenos más limitantes en la producción de este cultivo. La detección y correcta identificación de este hongo resulta fundamental para el manejo de la enfermedad, siendo las pruebas moleculares alternativas rápidas y sensibles para este fin. Mediante la técnica de PCR se evaluaron cuatro juegos de cebadores (CY1/CY2, CD1/CD2, ClF4/ITS4 y ClF432/ClR533) para la detección de C. lindemuthianum a partir de tejidos foliares, de vainas y de semillas procedentes de cultivos de frijol de Antioquia, Colombia. Los resultados indicaron que el par CD1/CD2, dirigido al pseudogen de permeasa de hierro Ftr1, fue el más efectivo para detectar el hongo en tejidos y semillas de frijol, así como para identificar aislamientos en cultivos microbiológicos. Para los cebadores CY1/CY2, dirigidos a los ITS del rDNA, se recomienda un esquema de PCR-RFLPs con MseI (=Tru1I) para la diferenciación con las especies C. orbiculare y C. trifolii. Estos cebadores generaron resultados consistentes cuando se utilizaron en combinación con ITS1 (ITS1/CY2) e ITS4 (CY1/ITS4). Finalmente, los cebadores ClF4/ITS4 resultaron en amplificaciones inespecíficas y ClF432/ClR533 en fragmentos de difícil resolución en electroforesis de agarosa. Este estudio servirá de apoyo para los programas de certificación de semilla y mejoramiento genético de frijol.
Palabras clave: DNA ribosomal, antracnosis, permeasa de hierro, Phaseolus vulgaris, RFLPs.
Abstract
Colletotrichum lindemuthianum, the causal agent of anthracnose in common bean, is one of the most important pathogens of this crop around the world. Accurate detection and identification of this fungus is of paramount importance for adequate management of this disease; in this respect, molecular tests are the fastest and most sensitive methods. In this work, the usefulness of four primer sets (CY1/CY2, CD1/CD2, ClF4/ITS4 and ClF432/ClR533) for PCR detection and identification of C. lindemuthianum was evaluated using leaf, pod and seed tissues of common bean crops from Antioquia, Colombia. The results suggest that primers CD1/CD2, targeting iron permease pseudogen Ftr1, were the most effective in detecting DNA from both microbiological isolates and infected bean tissues, including seeds. In the case of primers CY1/CY2 targeting the rDNA ITS region, a PCR-RFLP strategy is recommended using MseI (=Tru1I) to differentiate C. lindemuthianum from C. orbiculare and C. trifolii. These primers produced better results when combined with universal primers ITS1 (ITS1/CY2) and ITS4 (CY1/ITS4). Primers ClF4/ ITS4 were non-specific while ClF432/ClR533 result in bands with poor resolution in agarose gels. This study will serve as support of seed certification and genetic improvement programs in common bean.
Key words: Anthracnose, Iron permease, PCR, Phaseolus vulgaris, RFLPs, Ribosomal DNA.
Introducción
Colletotrichum lindemuthianum (Sacc. & Magnus Briosi & Cavara) causa la antracnosis del frijol (Phaseolus vulgaris L.), una de las enfermedades más limitantes en la producción de este cultivo en el mundo. Esta enfermedad ocasiona pérdidas de rendimientos de hasta el 95%, especialmente cuando se cultivan variedades de frijol susceptibles al patógeno en regiones con altos niveles de humedad, temperaturas moderadas y precipitaciones frecuentes. Esto ocurre en los Andes colombianos, donde se siembran principalmente las variedades Radical y Cargamanto (Pastor- Corrales y Tu, 1989; Fenalce, 2010). La siembra de frijol en Colombia se extiende a 120,000 ha, siendo el departamento de Antioquia uno de los principales productores con cerca de 26,000 ha (Santana y Mahuku, 2002; Fenalce, 2010).
El hongo afecta principalmente la calidad de las vainas de frijol, al inducir lesiones carnosas oscuras que se transforman en chancros hundidos con centros de color salmón; pero también afecta pecíolos y tallos (Chaves, 1989; Schwartz et al., 2005). Las semillas pueden presentar decoloración, aunque es frecuente que aun estando infectadas se presenten asintomáticas (Melotto et al., 2000).
El manejo de la antracnosis del frijol se fundamenta en la utilización de semilla certificada libre del patógeno, control químico con fungicidas sistémicos y protectantes y la siembra de variedades resistentes. Este último aspecto es fundamental para el manejo de la enfermedad, especialmente en sistemas de producción con pequeños productores, donde el acceso a semilla comercial y fungicidas es muy limitado por motivos económicos y ambientales. La generación de variedades de frijol con resistencia duradera a C. lindemuthianum es difícil de lograr, debido a los altos niveles de variabilidad genética y patogénica del hongo, del cual hasta el momento se han identificado más de 100 razas en el mundo (Apostolos et al., 2009; Pinto et al., 2012). Los estudios de diversidad genética de C. lindemuthianum han confirmado los altos niveles de variación intra-específica del patógeno, aunque es frecuente que se reporte la ausencia de relación entre los patotipos y genotipos identificados con marcadores moleculares como RAMS, RAPDS, Rep-PCR y AFLPs (Balardin et al., 1997; Mahuku y Riascos, 2004; Damasceno e Silva et al., 2007).
Ya que este hongo se dispersa principalmente por residuos de cosecha y semilla sexual (Melotto et al., 2000; Schwartz et al., 2005) es fundamental disponer de sistemas de detección altamente sensibles y específicos. Los métodos basados en PCR, convencional o en tiempo real, son ideales para este fin, ya que son rápidos, precisos y presentan altos niveles de sensibilidad (Chen et al., 2007; 2012; Wang et al., 2008).
Colletotrichum lindemuthianum es parte de un complejo de especies cercanas que incluyen a C. orbiculare (Berk. y Mont.) Arx y C. trifolii Bain (Liu et al., 2007) cuya relación filogenética fue recientemente confirmada por Cannon et al. (2012). Esto puede representar problemas para la detección molecular específica de los hongos pertenecientes a dichas especies, debido a que sus genomas pueden presentar secuencias idénticas en las regiones de unión de los cebadores utilizados en las pruebas de PCR. En este trabajo se evaluó la utilidad de cuatro juegos de cebadores para la detección específica de C. lindemuthianum a partir de tejidos foliares, vainas, semillas de frijol y aislamientos microbiológicos obtenidos en cultivos de frijol en el Departamento de Antioquia, Colombia.
Materiales y métodos
Obtención de muestras
Se realizaron recolecciones de tejidos foliares, vainas y semillas de frijol de la var. Cargamanto, con y sin síntomas de antracnosis (Foto 1C), provenientes de seis diferentes regiones cultivadoras de Antioquia, Colombia (Cuadro 1). En 10 de las muestras se realizó un aislamiento inicial de C. lindemuthianum, con el fin de evaluar los cebadores por PCR. Los tejidos se desinfestaron en una solución de hipoclorito de sodio al 1% durante 1 min, posteriormente se lavaron con agua destilada estéril y se procedió al aislamiento del agente causal en medio de cultivo Papa Dextrosa Agar (PDA) suplementado con penicilina y tetraciclina (100 mg/lt). Los cultivos se incubaron a temperatura ambiente (20 - 24°C) durante 5 - 7 días. En el momento en que se observaban colonias presumiblemente pertenecientes a C. lindemuthianum, se confirmó su identidad morfológica por microscopía y se realizaron repiques a nuevas cajas con medio PDA. Adicionalmente, se realizó una nueva salida de recolección a cultivos de frijol del municipio de El Carmen de Viboral con el fin de evaluar la utilidad de los cebadores en la detección directa del patógeno a partir de DNA de muestras foliares, vainas y de semillas procedentes de vainas con y sin síntomas de antracnosis.
Extracción de DNA
El DNA de cada aislamiento fue obtenido utilizando el método del CTAB 3X (Doyle y Doyle, 1990). También se utilizó el Kit comercial DNeasy Plant Mini kit (Qiagen, Alemania) para extraer el DNA directamente de tejidos de frijol. La integridad del DNA se determinó por electroforesis en gel de agarosa al 0.8%, suplementado con bromuro de etidio (10 mg/ ml). La concentración y pureza del DNA obtenido se determinó por lecturas a 260 nm y 280 nm (260 nm/280 nm) en un equipo Nanodrop 2000C (Thermo, EEUU).
PCR y secuenciación
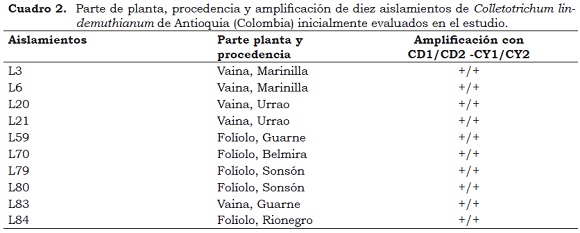
Inicialmente, se confirmó la identidad taxonómica de 10 aislamientos del hongo procedentes de las diferentes regiones cultivadoras de frijol en Antioquia (Cuadro 2). Para ello se realizó la amplificación por PCR y secuenciación posterior de las regiones ITS del rDNA, utilizando los cebadores universales ITS1 (5'-TCCGTAGGTGAACCTGCGG-3') e ITS4 (5'-TCCTCCGCTTATTGATATGC-3') y el procedimiento estándar descrito por White et al. (1990). Posteriormente, este grupo de aislamientos fue utilizado para evaluar por PCR los cebadores específicos para C. lindemuthianum: CY1âCY2 (CY1: 5'-CTTTGTGAACATACCTAACC-3'; CY2: 5'-GGTTTTACGGCAGGAGTG-3'), CD1 âCD2 (CD1: 5'-ACCTGGACACATAAGTCAAAG-3'; CD2: 5'-CAACAATGCCAGTATCAGAG-3') (Wang et al., 2008), ClF4/ITS4 (ClF4: 5'-TCCCCCCTGCCCCGCTCG-3') (Chen et al., 2007); ClF432/ Cl R533 (Cl F432: 5'-GGAGCCTCCTTTGCGTAGTAAC-3'; ClR533: 5'-ACCTGATCCGAGGTCAACCTTGTT-3') (Chen et al., 2012), siguiendo las condiciones descritas por sus autores. Los amplicones del tamaño esperado se purificaron directamente del gel mediante el kit QIAquick Gel Extraction (Qiagen) y se realizó su secuenciación directa en un secuenciador ABI Prism 3730XL (PE Applied Biosystems) en la compañía Macrogen (Corea del Sur). Las secuencias obtenidas con cada cebador fueron editadas y ensambladas para obtener los consensos con el programa Bioedit 6.0.6. (Hall, 1999), comparando con la base de datos GenBank del National Center For Biotechnology Information (NCBI), mediante el programa Blastn (http://www.ncbi.nlm.nih.gov/BLAST).
Las secuencias obtenidas con los cebadores ITS1/ITS4 y aquellas de referencia de diferentes especies de Colletotrichum, se utilizaron para realizar un alineamiento con el algoritmo Clustal W incluido en el software Bioedit 6.0.6. (Hall, 1999). La matriz obtenida fue empleada para realizar un análisis filogenético basado en el método de Neighbor Joining (NJ) con distancia genética calculada por el método dos-parámetros de Kimura y análisis de bootstrap con 1000 iteraciones, mediante el software Mega 5.0 (Tamura et al., 2011). Para el caso de las secuencias obtenidas con los cebadores CD1/CD2 se realizaron comparaciones con GenBank usando Blastx, determinando el marco de lectura correcto y la traducción respectiva con la herramienta translate del servidor Expasy (www.expasy.org). Los números de accesión de las secuencias depositadas en GenBank de este trabajo corresponden al rango KJ956028-KJ956037.
Evaluación de cebadores en la totalidad de aislamientos
Los pares de cebadores CY1/CY2 y CD1/CD2 que generaron los fragmentos del tamaño esperado en los 10 aislamientos inicialmente evaluados, fueron seleccionados para su utilización en reacciones de PCR dúplex a partir del DNA de otros 50 aislamientos de C. lindemuthianum obtenidos en el estudio. En adición, se evaluó la utilidad de los cebadores para la detección directa del patógeno en 15 muestras de tejidos foliares, 15 de tejidos de vainas y 30 de semillas de frijol. Las condiciones de PCR y electroforesis fueron similares a las descritas anteriormente, utilizando como controles positivos DNA de los aislamientos previamente secuenciados. Todas las reacciones de PCR incluyeron además un control negativo que carecía del DNA molde del patógeno.
PCR-RFLPs
Debido a los altos niveles de identidad de las regiones ITS del rDNA de C. lindemuthianum, C. orbiculare y C. trifolii, se diseñó una prueba basada en la amplificación de esta región, bien con los cebadores específicos CY1/ CY2 o con una combinación de estos y los cebadores universales ITS1 e ITS4 (ej. CY1/ ITS4, ITS1/CY2). Las secuencias obtenidas en este trabajo para dichos amplicones en C. lindemuthianum y aquellas depositadas en GenBank para las otras especies filogenéticamente afines de Colletotrichum fueron utilizadas para realizar un análisis in silico de RFLPs (polimorfismo en la longitud de los fragmentos de restricción) mediante el programa Webcutter (http://rna.lundberg.gu.se). Al final, dada su adecuada resolución en la separación de dichas especies, se seleccionaron las enzimas de restricción CfoI, MspI y MseI (=Tru1I) para confirmar su patrón de digestión sobre cinco amplicones de regiones ITS de C. lindemuthianum. Las reacciones consistieron de 10 µl, conteniendo 1 µl de buffer de enzima 10X, 1 U de cada enzima de restricción (Thermo), 5 µl del amplicon y 1 µl de agua. Las reacciones fueron incubadas al baño María a 37 °C durante 12 h. La separación y visualización se efectuó por electroforesis en gel de agarosa al 2.5%, tal como se indicó anteriormente.
Resultados y discusión
Aislamientos y extracciones de DNA
En total se obtuvieron 60 aislamientos de C. lindemuthianum en el estudio. En los aislamientos en los que se presentó esporulación fue posible confirmar morfológicamente su identidad, al presentar conidias hialinas, cilíndricas, no septadas, con terminaciones obtusas, de 13 - 18 µm x 3.75-5 µm (promedio ±SD: 15.75 ± 2.44 x 4.76 ± 0.46) (Foto 1A). Conidióforos no septados, hialinos y cilíndricos, micelio septado, inicialmente hialino pero rápidamente tornándose de color gris a negro oliva (Foto 1B), con colonias planas cubiertas de micelio aéreo esparcido y masas de esporas de color salmón producidas en el centro de los cultivos. Las metodologías de extracción basadas en los método del CTAB 3X y el kit comercial permitieron obtener DNA en cantidades suficientes y adecuada calidad, con concentraciones en el rango de 100 a 1500 ng/µl, promedio de 978 ng/µl (SD: ±354 ng/µl) y relaciones de 260 nm:280 nm de 1.7 a 2.1 (promedio: 1.9, SD ± 0.11). En el caso particular de las extracciones de DNA a partir de tejidos de frijol (incluyendo semillas), el uso del kit comercial fue muy efectivo en términos de la calidad del DNA obtenido para adelantar las reacciones de PCR posteriores.
Análisis filogenético de regiones ITS del rDNA
Las reacciones de PCR con los cebadores ITS1 e ITS4 generaron fragmentos de cerca de 600 pb a partir del DNA de los aislamientos bajo análisis, siendo evidente la uniformidad del tamaño de esta región en la especie C. lindemuthianum. La comparación de las secuencias con respecto al GenBank presentó como primeros 'hits' secuencias de C. lindemuthianum o de su estado sexual Glomerella lindemuthiana Shear (ej. accesiones EU400129, AJ301947 y AJ301958) con 100% de identidad y valores e de 0.0 (100% cobertura), lo que en conjunto con las observaciones coloniales y microscópicas, condujo inequívocamente a confirmar la identidad de los aislamientos.
En el árbol filogenético se observó la formación de cinco clados principales (1 a 5) con altos soportes de bootstrap (> 84%). El primero de ellos agrupó las 10 secuencias obtenidas en este estudio con aquellas de C. lindemuthianum de diferentes orígenes geográficos; además de secuencias de C. orbiculare y C. trifolii; aunque los representantes de dichas especies se presentaron en subclados individuales. El segundo clado presentó secuencias de C. dracaenophilum, C. yunnanense y C. tropicicola; mientras que el tercer grupo correspondió a C. gloeosporioides y C. fructicola. El cuarto clado incluyó aislamientos de C. coccodes y C. nigrum y finalmente el quinto grupo correspondió a C. acutatum (Figura 1).
Evaluación inicial de cebadores
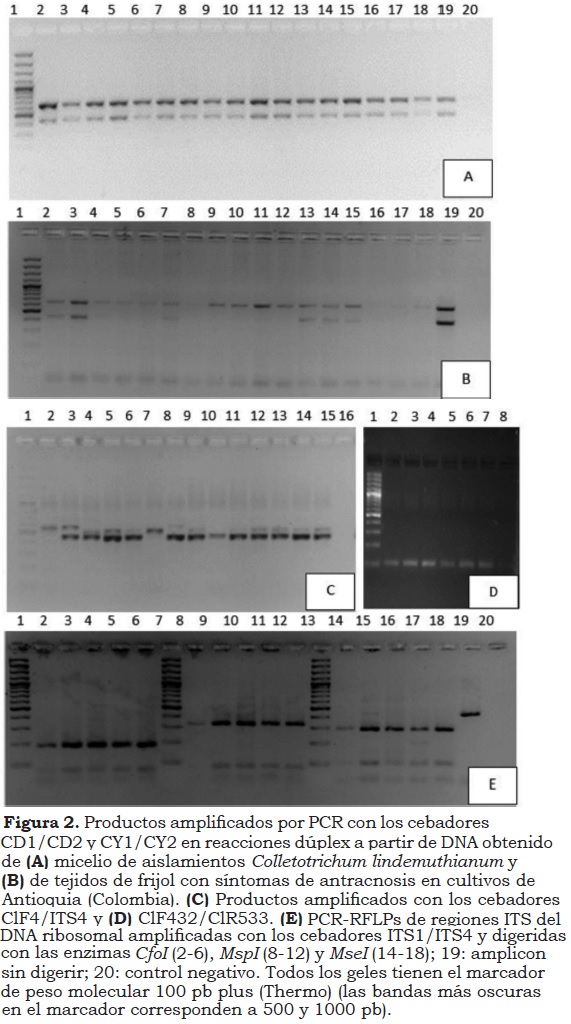
De los cuatro juegos de cebadores evaluados en el estudio, sólo dos (CD1/CD2 y CY1/CY2) demostraron ser útiles en la detección molecular de aislamientos de C. lindemuthianum en Antioquia, al generar fragmentos únicos de 638 pb y 442 pb, respectivamente (Figura 2A). Por otra parte, las amplificaciones con los cebadores ClF4/ITS4 fueron inespecíficas, aun cuando se variaron condiciones de PCR como la temperatura de anillamiento y las concentraciones de MgCl2, DNA y cebadores (Figura 2C). Para el caso de los cebadores ClF432/ClR533 se produjeron los fragmentos del tamaño esperado (101 pb) (Figura 2D), pero no fueron tenidos en cuenta por los problemas de separación y visualización de amplicones pequeños en esquemas de electroforesis estándar. Sin embargo, este resultado confirma su utilidad en sistemas de PCR en tiempo real, para lo cual fueron originalmente diseñados (Chen et al., 2012).
Evaluación de los cebadores en la totalidad de aislamientos y en tejidos vegetales
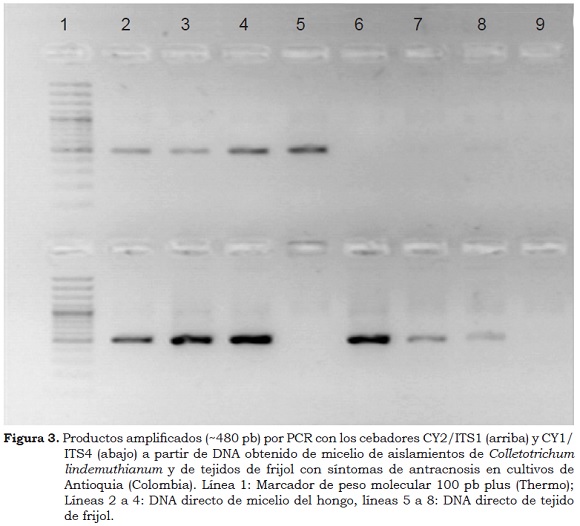
Los cebadores CD1/CD2 y CY1/CY2 permitieron obtener los amplicones del tamaño esperado en los aislamientos evaluados (Figura 2A), siendo confirmada su naturaleza como parte de la región ITS del rDNA de C. lindemuthianum (ej., 99% de identidad y cobertura, e = 0.0 con respecto a JX546806, EU400129). Sin embargo, cuando se probaron los cebadores CY1/CY2 sobre DNA total obtenido de tejidos de frijol, los resultados mostraron ser inconsistentes, ya que no siempre permitían la obtención del amplicon en muestras con síntomas de antracnosis (Figura 2B). Este resultado está acorde con lo reportado por Wang et al. (2008), quienes indican que dichos cebadores no resultaron completamente específicos, al amplificar también DNA de aislamientos de C. orbiculare. Por esto, se decidió la evaluación de las combinaciones de estos cebadores con los universales ITS1 e ITS4, con lo que se obtuvieron los fragmentos del tamaño esperado (∼480 pb) en ambas combinaciones (CY1/ITS4 e ITS1/CY2) (Figura 3). Para el caso del uso de los cebadores CD1/CD2 sobre DNA de tejidos de frijol, incluyendo semillas, nuevamente se obtuvieron los amplicones del tamaño esperado, aunque con variaciones en los niveles de intensidad, lo que es frecuente dadas las diferencias propias en la calidad del DNA obtenido de diversos tejidos vegetales. Ya que los autores de dichos cebadores (Wang et al., 2008) no reportaron sus regiones diana, se realizó su secuenciación y no fue posible encontrar por Blastn 'hits' significativos con respecto a la base de datos del GenBank (cobertura: 6%, y valores e: 3.7), por lo que se procedió a realizar búsquedas con la herramienta Blastx. En este caso los resultados indicaron 'hits' con niveles de identidad de 34 a 37% (valores e: 1x10-12,-14, coberturas: 71 - 74%) con respecto a secuencias de permeasas de hierro de hongos, incluyendo miembros del género Colletotrichum (ej., Accesiones EJP66635, EGX90976). Este resultado condujo a plantear que dicha región obtenida por SCARs (secuencias caracterizadas de regiones amplificadas al azar) por parte de Wang et al. (2008), correspondía a un pseudogen, siendo evaluada dicha hipótesis a partir del análisis de la traducción del fragmento secuenciado. En este caso se encontró que efectivamente la secuencia resultante presentaba codones de parada internos, altas tasas de variación y niveles de identidad inferiores que 0.38 con respecto a secuencias de otras permeasas de hierro. Estos hallazgos condujeron al grupo de investigadores a profundizar en el estudio de este pseudogen y de los genes funcionales que participan en las rutas de absorción y transformación del hierro en C. lindemuthianum, realizando una evaluación genómica mediante pirosecuenciación 454 (Roche), que confirmó la naturaleza de esta región SCAR como un pseudogen de Ftr1 (Gutiérrez et al., 2014). De gran interés resultará en el futuro obtener la secuencia del gen funcional de la permeasa de hierro de C. lindemuthianum, para realizar comparaciones con el pseudogen aquí reportado y con los genes encontrados en otras especies de Colletotrichum, de manera que se evalúe su utilidad como un posible marcador molecular en este género de hongos.
PCR-RFLPs
Debido a la agrupación en el primer clado del árbol filogenético de C. lindemuthianum con otras dos especies de Colletotrichum, se realizó un análisis de identidad genética, encontrando que los aislamientos en el presente estudio compartían niveles de identidad de 0.998 con respecto a los de C. lindemuthianum de otras regiones del mundo, y que dichos niveles disminuían a 0.986 y 0.981 con las especies C. orbiculare y C. trifolii, respectivamente, siendo inferiores que 0.90 en relación con las demás especies del género (matriz no incluida). Esto representó una oportunidad para utilizar la región ITS del rDNA como base para la detección molecular de C. lindemuthianum. Por esta razón se procedió a realizar un análisis in silico de RFLPs, que incluyó diferentes secuencias de referencia del género Colletotrichum, encontrando que efectivamente tres endonucleasas (CfoI, MspI y MseI (=Tru1I)) presentaban diferentes sitios de corte entre las secuencias de las especies más cercanas C. lindemuthianum y C. orbiculare. Además, dichas especies pueden ser fácilmente identificadas mediante RFLPs con respecto a C. trifolii usando MseI, ya que en la región ITS de C. lindemuthianum se presentan cuatro sitios de corte T/TAA (132, 177, 480, 523), mientras que en C. orbiculare tres (135, 180, 526) y en C. trifolii sólo dos sitios de corte (124, 169) (Cuadro 3). La confirmación in vitro de dichas predicciones se realizó utilizando cinco aislamientos de C. lindemuthianum obtenidos en este estudio y amplificación por PCR de la región ITS del rDNA con los cebadores ITS1/ITS4 (ver Figura 1E). En trabajos previos adelantados por Liu et al. (2007) se había propuesto una prueba de RFLPs para diferenciar las especies C. orbiculare, C. lindemuthianum, C. trifolii y C. malvarum utilizando RFLPs de un intron de 900 pb del gen glutamina sintetasa; sin embargo, dado el bajo número de copias de este gen, su detección resulta menos sensible que el uso de regiones ITS del rDNA, que puede tener de varios cientos a miles de copias por genoma (White et al., 1990), siendo preferible su utilización como prueba de diagnóstico molecular.
Se espera que las herramientas de detección molecular de C. lindemuthianum evaluadas en el presente estudio sean efectivamente incorporadas por los organismos de sanidad vegetal estatal, gremios de agricultores y productores de semillas, para mejorar los sistemas de certificación de semilla de frijol, fortalecer los programas de vigilancia cuarentenaria y apoyar estudios epidemiológicos y de mejoramiento genético por resistencia a este hongo que se adelantan en Colombia y otros países como Brasil, EE.UU. y México.
Conclusiones
- En esta investigación se evaluó el uso de cuatro grupos de cebadores (CY1/CY2, CD1/CD2, ClF4/ITS4 y ClF432/ClR533) para su utilización en pruebas de detección e identificación molecular de aislamientos de C. lindemuthianum obtenidos en diferentes subregiones cultivadoras de frijol del departamento de Antioquia (Colombia). Los cebadores CD1/CD2 resultaron en amplificaciones por PCR más robustas y específicas; sin embargo su utilización para la detección de C. lindemuthianum en otras regiones de Colombia y en diferentes países, requiere de una evaluación previa de las características genéticas de las poblaciones del hongo.
- Como prueba confirmatoria para la detección de C. lindemuthianum a partir de DNA de micelio y tejidos de frijol, en este trabajo se propone el uso de una prueba de PCR-RFLP de la región ITS del rDNA y la digestión con la enzima MspI que genera dos sitios de corte C/CGG en C. lindemuthianum, en contraste con tres en C. orbiculare y C. trifolii. En caso de ser requerido, dichas especies pueden, a su vez, ser diferenciadas por la digestión con CfoI que produce dos sitios de corte GCG/C en C. trifolii y un sólo corte en C. orbiculare.
- Como prueba confirmatoria a la amplificación con CD1/CD2 para la detección de C. lindemuthianum en tejidos de frijol (folíolos, vainas, semillas) se recomienda el empleo de los cebadores ITS1/CY2 o CY1/ITS4, que generan amplicones más robustos que aquellos logrados con CY1/CY2.
Agradecimientos
Este trabajo fue financiado por la Vicerrectoría de Investigaciones de la Universidad Nacional de Colombia, proyecto: 20101009932. Convocatoria Nacional para el fortalecimiento de los Grupos de Investigación y Creación Artística de la Universidad Nacional de Colombia. 2010-2012.
Referencias
Apostolos, B. J.; Koutita, O.; y Klonari, K. T. 2009. Molecular diversity and assessment of biological characteristics of Greek Colletotrichum lindemuthianum populations. J. Phytopath. 157:311 - 318. [ Links ]
Balardin, R. S.; Jarosz, A.M.; y Kelly, J. D. 1997. Virulence and molecular diversity in Colletotrichum lindemuthianum from South, Central, and North America. Phytopath. 87:1184 - 1191. [ Links ]
Cannon, P. F.; Damm, U.; Johnston, P. R.; y Weir, B. S. 2012. Colletotrichum - current status and future directions. Stud. Mycol. 73:181 - 213. [ Links ]
Chaves, G. 1989. Anthracnose. En: Schwartz, H. y Galvez, G. (eds.). Bean production problems. Centro Internacional de Agricultura Tropical (CIAT), Cali. p. 39 - 54. [ Links ]
Chen, Y. Y.; Conner, R. L.; Gillard, C. L.; Boland, G. J.; Babcock, C.; Chang, K. F.; Hwang, S. F.; y Balasubramanian, P. M. 2007. A specific and sensitive method for the detection of Colletotrichum lindemuthianum in dry bean tissue. Plant Dis. 91:1271 - 1276. [ Links ]
Chen, Y. Y.; Conner, R. L.; Gillard, C. L.; McLaren, D. L.; Boland, G. J.; Balasubramanian, P. M.; et al. 2012. A quantitative real-time PCR assay for detection of Colletotrichum lindemuthianum in navy bean seeds. Plant Pathol. 62:900 - 907. [ Links ]
Damasceno e Silva, K. J.; de Souza, E. A.; y Ishikawa, F. H. 2007. Characterization of Colletotrichum lindemuthianum isolates from the state of Minas Gerais, Brazil. J. Phytopath. 155:241 - 247. [ Links ]
Doyle, J. J. y Doyle, J. L. 1990. Isolation of plant DNA from fresh tissue. Focus 12:13 - 15. [ Links ]
Fenalce (Federación Nacional de Cereales). 2010. El cultivo de frijol. Historia e importancia. El cerealista, mayo-junio. p. 30. [ Links ]
Gutiérrez, P.; Salazar, M.; Alzate, J. F.; Vanegas, K.; y Marín, M. 2014. The CD1/CD2 marker for specific detection of Colletotrichum lindemuthianum is an iron transporter pseudogene. Trop. Plant Pathol. 39:275 - 283. [ Links ]
Hall, T. A. 1999. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucleic Acids Symp. Ser. 41:95 - 98. [ Links ]
Liu, B.; Walsiwa, L. A.; Morelock, T. E.; O'Neill, N. R.; y Carrell, J.C. 2007. Comparison of Colletotrichum orbiculare and several allied Colletotrichum spp. for mtDNA RFLPs, intron RFLP and sequence variation, vegetative compatibility, and host specificity. Phytopath. 97:1305 - 1314. [ Links ]
Mahuku, S. G. y Riascos, J. J. 2004. Virulence and molecular diversity within Colletotrichum lindemuthianum isolates from Andean and Mesoamerican bean varieties and regions. Eur. J. Plant Pathol. 110:253 - 263. [ Links ]
Melotto, M.; Balardin, R. S. y Kelly, J. D. 2000. Host-pathogen interaction and variability of Colletotrichum lindemuthianum. En: Prusky, D.; Freeman, S.; y Dickman, M. B. (eds.). Host specificity, pathology and host-pathogen interactions of Colletotrichum. APS Press, St Paul, p. 346 - 361. [ Links ]
Pastor-Corrales, M. A. y Tu, J.C. 1989. Anthracnose. En: Schwartz, H. y Galvez, G. (eds.). Bean production problems. Centro Internacional de Agricultura Tropical (CIAT), Cali. p. 77 - 104. [ Links ]
Pinto, J. M.; Pereira, R.; Mota, S. F.; Ishikawa, F. H.; y Souza, E. A. 2012. Investigating phenotypic variability in Colletotrichum lindemuthianum populations. Phytopath. 102:490 - 497. [ Links ]
Santana, E. G. y Mahuku, G. 2002. Diversidad de razas de Colletotrichum lindemuthianum en Antioquia y evaluación de germoplasma de frijol crema-rojo por resistencia a antracnosis. Agron. Mesoam. 13:95 - 103. [ Links ]
Schwartz, H. F.; Steadman, J. R.; Hall, R.; y Forster, R. L. 2005. Compendium of bean diseases. 2nd ed. St Paul: APS Press. 109 p. [ Links ]
Tamura, K., Peterson, D.; Peterson, N.; Stecher, G.; Nei, M.; y Kumar, S. 2011. MEGA5: Molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods. Mol. Biol. Evol. 28:2731 - 2739. [ Links ]
Wang, W.; Tang, J. H.; y Wang, Y. C. 2008. Molecular detection of Colletotrichum lindemuthianum by Duplex PCR. J Phytopath. 156:431 - 437. [ Links ]
White, T. J.; Bruns, T.; Lee, S.; y Taylor, J. 1990. Amplification and direct sequencing of fungal rRNA genes for phylogenetics. En: Innis A. M.; Gelfand, D. H.; Sninsky, J. J.; y White, T. J. (eds.). PCR Protocols: A guide to methods and applications. Academic Press, San Diego, p. 315 - 322. [ Links ]