Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.65 no.1 Palmira Jan./Mar. 2016
https://doi.org/10.15446/acag.v65n1.47994
http://dx.doi.org/10.15446/acag.v65n1.47994
Identificación molecular de aislamientos de Moniliophthora roreri en huertos de cacao de Norte de Santander, Colombia
Molecular identification of Moniliophthora roreri isolates from cocoa orchards in Norte de Santander, Colombia
Liliana Yanet Suárez Contreras
Universidad Francisco de Paula Santander. Avenida Gran Colombia No. 12E–96. Barrio Colsag, Cúcuta, Norte de Santander, Colombia. Autora para correspondencia: lilianayanethsc@ufps.edu.co
Rec.: 22.12.2014 Acep.: 27.01.2015
Resumen
El hongo fitopatógeno Moniliophthora roreri produce la moniliasis, una enfermedad que destruye la mazorca de cacao (Theobroma cacao L.) y, por tanto, reduce la producción del cultivo y los ingresos de los agricultores. En el departamento de Norte de Santander, Colombia, las pérdidas por esta enfermedad pueden alcanzar hasta 60% de la producción. El conocimiento sobre la biología del hongo es escaso y actualmente se están realizando estudios de identificación macroscópica, microscópica, y comportamiento in vitro frente a antagonistas como: Trichoderma asperellum, T. longibrachiatum, Paecilomyces sp. y Bacillus brevis. En ocho municipios y corregimientos del departamento (El Zulia, Cúcuta, Tibú, Sardinata, Bucarasica, Teorama, Agua clara y El Tarra) se obtuvieron 56 aislamientos de M. roreri con fines de extracción de ADN y análisis de PCR. El método de aislamiento se realizó a partir de mazorcas infectadas por M. roreri, las cuales fueron lavadas con agua destilada, fraccionadas en trozos de 2 × 2 cm y desinfestadas con hipoclorito de sodio (2.5%), y alcohol (60%), antes de la siembra en cajas de Petri con medio PDA e incubación por 10 días a 28 °C. Las regiones ribosomales, ITS, (espaciadores internos de transcritos) correspondientes al ADNr 18S, ITS1, 5.8S, ITS2 y 25S fueron amplificadas y secuenciadas. Amplicones de 600 pb (8 aislamientos), 740 pb (12 aislamientos) y de 750 pb, para los 36 aislamientos restantes. Los tamaños de los amplicones correspondieron a los esperados para la especie M. roreri y los análisis de BLAST confirmaron este nivel de caracterización.
Palabras clave: Moniliophthora roreri, Theobroma cacao, moniliasis, ITS.
Abstract
The plant pathogenics fungus Moniliophthora roreri, causes losses to cocoa farmers and it causes the “Moniliasis”, too. The disease destroys the cocoa pod and crop production decreases, the losses reach up to 60% in the department of Norte de Santander. Little is known of the biology of the fungus, studies are currently identifying macroscopic, microscopic, and behavior in vitro with antagonists such as Trichoderma asperellum, Trichoderma longibrachiatum, Paecilomyces sp. and Bacillus brevis. Fifty–six isolates of M. roreri were obtained from 8 municipalities and townships the department (El Zulia, Cucuta, Tibú, Sardinata, Bucarasica, Teorama, Agua clara, El Tarra) for the purpose of DNA extraction and PCR analysis. The method of isolation was performed from infected ears M. roreri, which were washed with distilled water, and cut into 2 × 2 cm, and were disinfected with hypochlorite, 2.5% sodium and 60% alcohol. Then sown in Petri dishes containing PDA medium and incubated for 10 days at 28 ° C. Ribosomal regions “ITS” (internal transcribed spacers) for the 18S rDNA, ITS1, 5.8S, ITS2 and 25S, were amplified and sequenced. Amplicons of 600 bp (8 isolates), 740 bp (12 isolates) and 750 bp for the remaining 36 isolates. The sizes of the amplicons corresponded to those expected for the species M. roreri, and analysis “BLAST” level confirmed this characterization.
Keywords: Moniliophthora roreri, Theobroma cacao, moniliasis, ITS.
Introducción
La moniliasis es una enfermedad del cacao (Theobroma cacao L.) producida por el hongo Moniliophthora roreri que se presentó en 1916 por primera vez en forma virulenta en la república del Ecuador (Barros, 1977), siendo actualmente un problema común para Colombia, Ecuador y Perú (Sánchez y Garcés, 2012). Según Rorer (1918) la moniliasis es un hongo patógeno nativo de Ecuador, que se encontró en especies como T. bicolor y T. baloensis (Barros, 1977). También se pensó que T. gireli era el huésped nativo de M. roreri al norte de Colombia en el departamento de Antioquia, donde se observó infectando plantas forestales al occidente de la cordillera andina de Colombia, zona rica en especies de Herrania y Theobroma. Evans (1985), considera que el hongo es nativo del Nororiente de esta parte de Sur América, ya que está presente en estas especies en Ecuador y Colombia.
Es probable que T. gileri represente un huésped coevolutivo de M. roreri, que se extendió del occidente de Ecuador al Noroccidente de Colombia, de esta forma se considera Ecuador como el centro de origen del patógeno. Sin embargo, algunos reportes sugieren que Colombia podría ser el primer lugar de origen del patógeno (Phillips, 2003).
En Colombia no existen registros precisos de la fecha de aparición de la enfermedad. En la literatura se reporta que de Ecuador pasó a Colombia y más tarde fue encontrada en el Perú, en plantaciones del occidente de Venezuela y al sur de Panamá (Barros, 1977). Existen reportes de 1969, donde se afirma que la primera inundación producida por el río Cauca afectó las plantaciones de 2 años de edad existentes en el dique, lo que produjo un ataque generalizado de cáncer o ‘chancro’ del tronco de los árboles causado por P. palmivora; más tarde, en 1971, se observó por primera vez la presencia de la moniliasis incidiendo levemente en las demás plantaciones de la región (Barros, 1980). Además, la primera detección del patógeno se hizo en el noreste de Colombia donde se describió la mayor diversidad genética del agente causal y se conoce la enfermedad desde hace 200 años, aproximadamente (Sánchez y Garcés, 2012).
En Colombia esta enfermedad fungosa es el factor más limitante para la producción de cacao (Sánchez y Garcés, 2012), ya que destruye la mazorca y reduce la producción en Norte de Santander y el resto del país, con pérdidas hasta de 60% de la cosecha (Suárez y Rangel, 2013). En esta región son escasos los estudios sobre los daños de este fitopatógeno, por lo tanto es necesario identificarlo no solo a nivel morfológico sino molecular. Los marcadores moleculares exhiben las características fisicoquímicas del ADN y su herencia se explica con las mismas leyes establecidas por la genética. Como consecuencia, han sido útiles para la detección de polimorfismos en animales, plantas superiores, patógenos y plagas (virus, hongos, insectos, nemátodos) (Rocha, 2003). Los ITS son algunos de los marcadores de ADN utilizados para la identificación molecular de M. roreri. Los espaciadores internos de transcritos son regiones no codificantes de la secuencia de ADN que separan los genes que codifican para los ARN ribosomales, altamente conservados a lo largo de los taxa, mientras que los nucleótidos entre ellos pueden ser específicos a nivel de especie. La conservación de los genes ARNr permite el fácil acceso a las regiones ITS con cebadores ‘versátiles’ para realizar la PCR. La variación en los espaciadores es una herramienta útil en la distinción entre una amplia diversidad de taxa difíciles de identificar. Para la detección de los ITS se hace uso de los cebadores en regiones conservadas de los genes de ARNr 28S, 5.8S y 18S (White, Bruns, Lee, y Taylor, 1990).
En la actualidad se realizan estudios del genoma de M. roreri que permitirán una imagen más completa de su evolución y mejorarán el conocimiento de su biología, para ayudar en el desarrollo de estrategias para un mejor control (Sánchez y Garcés, 2012). Igualmente se continúa con otras investigaciones para aislar microorganismos con potencial antagónico al fitopatógeno y observar su capacidad antagónica in vitro para el control biológico en Norte de Santander (Suárez y Cabrales, 2008).
Por lo tanto el objetivo de este trabajo fue estandarizar la técnica de espaciadores internos de transcritos (ITS) específicamente para aplicarlos en aislamientos de M. roreri y así determinar su variabilidad genética en Norte de Santander utilizando marcadores moleculares. Esto constituirá una de las estrategias para el posible control de la enfermedad y mejoramiento genético, la selección más adelante de genotipos de cacao resistentes a las variantes de M. roreri y en el futuro, mejorar las condiciones fitosanitarias del cultivo de cacao.
Materiales y métodos
Aislamientos. Los aislamientos de M. roreri fueron obtenidos de T. cacao tomados en fincas en diferentes municipios y corregimientos del Nororiente colombiano a partir de frutos con síntomas de la enfermedad. Así, en Zulia (8 aislamientos), Cúcuta (7), Tibú (5), Sardinata (6), Bucarasica (11), Teorama (5), Agua Clara (6) y El Tarra (8).
Los aislamientos se hicieron a partir de mazorcas infectadas por M. roreri, las cuales fueron lavadas externamente con agua destilada y cortadas en pequeñas secciones transversales. De estas secciones se tomaron trozos de 2 × 2cm, que fueron lavados y desinfectados con hipoclorito de sodio (2.5%) durante 2 minutos y alcohol al 60% durante 3 minutos. Posteriormente fueron sembrados en cajas Petri en medio papa dextrosa agar (PDA) con un tiempo de incubación de 10 días a 28 °C (Suárez, 2006).
Mantenimiento y preservación de los aislamientos. Los aislamientos de M. roreri crecieron en medio PDA mantenido durante el estudio en medios frescos. Dos réplicas de esta colección fueron conservadas en tubos y en cajas Petri en condiciones de oscuridad a temperatura ambiente (28 °C), mientras que otras fueron conservadas en refrigeración a 4 °C.
Producción de micelio. El ADN genómico de M. roreri fue extraído del micelio obtenido después de repiques de caja de Petri a tubo, donde creció entre 11 y 15 días. Los aislamientos fueron cultivados en PDB (Caldo de Papa Dextrosa) a 25°C.
Extracción y purificación del ADN genómico. El ADN fue extraído del micelio de M. roreri (0.5 – 0.75 g) que había crecido previamente en PDB. Cada muestra fue macerada en un microtubo de 2 ml con 500 µl de buffer de extracción, con ayuda de un motor y pistilo. Luego la muestra fue llevada a vortex por un minuto y centrifugada a 6000 × g por diez minutos. El sobrenadante se pasó a un microtubo donde se incubó a 70 °C por 15 minutos; seguido de una extracción con un volumen de fenol–cloroformo (1:1) y centrifugación a 10.000 x g por 10 minutos. La fase acuosa fue transferida a otro microtubo donde se agregó un volumen de isopropanol. Se dejó en frío (congelación) por 10 minutos y nuevamente se centrifugó a 10.000 x g, durante 10 minutos. El sobrenadante fue eliminado y el precipitado fue lavado en 150 µl de etanol a 70%, secado a 37 °C durante 3 minutos y resuspendido en 50 µl de buffer TE 1X pH: 8 con RNAasa (Suárez, 2005). Este protocolo de extracción se aplicó a las 56 cepas de M. roreri.
Cuantificación del ADN. La cantidad y la calidad del ADN extraído de cada muestra fue estimada en un gel de agarosa (0.9% (w/v)) teñido con bromuro de etidio (0.5 µg /ml) y visualizado bajo luz UV utilizando un transiluminador. Las concentraciones de ADN obtenidas variaron entre 1 y 2 µg/µl.
Amplificación por PCR. Las regiones ribosomales ITS fueron amplificadas utilizando los cebadores ITS4 (5'–TCCTCCGCTTATTGATATGC–3'), ITS5 (5'GGAAGTAAAAGTCGTAACAAGG–3') (White et al., 1990), los cuales se anclan en los ADNr 25 S y 18 S, respectivamente, por lo que incluyen también el 5.8 S.
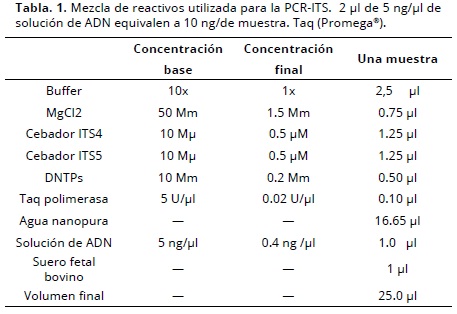
La amplificación por PCR fue realizada en un volumen final de 25 µl, constituido de un buffer 1x taq polimerasa; MgCl2: 1.5 mM, 0.5 µl de cada cebador, 0.2 mM de DNTPs (Promega®) y 10 (0.4) ng de ADN genómico total de M. roreri (Tabla1).
La reacción de PCR fue realizada en un termociclador (MJ. Research®) con las condiciones siguientes: un ciclo inicial a 94 °C por 1 minuto (denaturación); 35 ciclos de 94 °C por 1 minuto (denaturación), 52°C por 45 segundos (hibridación) y 72 °C por 1 minuto (extensión) y un ciclo final de 72°C por 7 minutos. Las amplificaciones fueron chequeadas en un gel de agarosa al 1.5% w/v (1xTAE buffer) teñidas con bromuro de etidio (0.5 µg/ml) y visualizado bajo luz UV en un transiluminador. Los fragmentos fueron determinados por comparación con un marcador de 1 Kb (Promega®). Y las bandas únicas obtenidas por PCR fueron posteriormente secuenciadas.
Secuenciación. Las bandas típicas obtenidas mediante ITS fueron secuenciadas por Macrogen Inc. en Corea del Sur. Se utilizó la química del kit ABI PRISM® BigDyeTM Terminator Cycle Sequencing usando electroforesis capilar y un secuenciador ABI PRISM® 3730XL Analyzer (96 capillary type) siguiendo los protocolos de los fabricantes. Se secuenciaron ambas hebras por amplicon.
En este trabajo se utilizaron herramientas microbiológicas y moleculares que se aplicaron al fitopatógeno. La técnica de ITS se estandarizó de la forma como se mencionó en materiales y métodos. Solo se hizo una modificación de la técnica propuesta por Phillips, en cuanto a adicionar suero fetal bovino 1 µl por muestra para evitar inhibición de la PCR y el número de ciclos en la PCR también se varió, aumentando 5 ciclos de 30 a 35 ciclos. Así: un ciclo inicial a 94°C por un minuto (denaturación); 35 ciclos de 94°C por un minuto (denaturación), 52°C por 45 segundos (hibridación) y 72 °C por 1 minuto (extensión) y un ciclo final de 72°C por 7 minutos; y así se mostraron buenos resultados en las amplificaciones.
Resultados y discusión
En total se obtuvieron 56 aislamientos de M. roreri a partir de los 8 municipios y corregimientos muestreados del departamento Norte de Santander (Tabla 2).
Amplicones
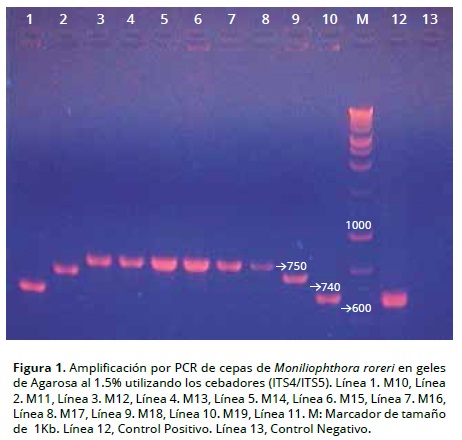
Se obtuvieron amplicones de 600 pb para 8 aislamientos, 740 pb para 12 aislamientos y de 750 pb para los 36 aislamientos restantes (Figura 1). Los tamaños de estos correspondieron a los esperados para la especie M. roreri y los análisis de ‘BLAST confirmaron este nivel de caracterización. Orozco, Osorio, Botero, Rivera, y López, (2011) encontraron resultados similares para M. roreri (amplicones de 710 pb), y por Phillips, Aime, y Wilkinson (2007) encontraron amplicones de 741 pb para este hongo.
El tamaño de los amplicones observados por ITS no coincidió con todos los fenotipos de los aislamientos (Tabla 3), corroborando así una diferencia a nivel molecular que no se puede apreciar en el fenotipo de cada aislamiento de M. roreri. El estudio de ADN ribosomal en numerosos basidiomicetos muestra que los ITS presentan una variación que las convierte en un marcador taxonómico muy útil para distinguir entre especies (Orozco et al., 2011). Los fenotipos de las muestras presentaron tres tamaños de amplicones ITS que en algunos casos son comunes. Un grupo está conformado por los aislamientos que tienen un amplicón de 750 pb y presentaron una gran variación fenotípica y la caracterizan 36 aislamientos de M. roreri; otro grupo de 12 aislamientos de M. roreri mostraron amplicones de 740 pb y un último grupo de 8 aislamientos exhibió amplicones de 600 pb (Figura 1). Los tres amplicones observados coincidieron con el tamaño de 760 pb reportado por Phillips (2003).
Aislamientos
Solo dos aislamientos de M. roreri compartieron igual morfología o fenotipo, grupo I, e igual tamaño de amplicón de 600 pb: la cepa M10 proveniente del municipio de Bucarasica y la cepa M19 del municipio de El Zulia; ambos geográficamente cercanos y localizados en la región central del departamento. Un aislamiento de M. roreri, M54 constituye el fenotipo del grupo II, con tamaño de amplicón de 740 pb y se encuentra en el municipio de Tibú, región nororiental del departamento. Doce aislamientos de M. roreri comparten el fenotipo del grupo III y el tamaño de amplicón de 750 pb. Estos se caracterizan por estar localizados en cuatro puntos geográficos diferentes: en la región central del departamento se encuentran los aislamientos: M2 (Cúcuta), M29, y M39 (El Zulia), M56 (Bucarasica); en la región noroccidental se encuentran los aislamientos M12 y M44 (Teorama); en la región nororiental los aislamientos M42, y M47 (El Tarra), M3, y M36 (Tibú); en la región oriental los aislamientos M40 y M45 (Agua Clara).
Los aislamientos del grupo I (M1, M4, M5, M10, M13, M15, M19, M26, M27, M30, M31, M32, M33, M34, M35, M38, M43, M46, M48, M49, M50, M51, M52, M55) presentaron un crecimiento disperso del micelio radial, con coloración parda clara y oscura e intercalada con filamentos cortos y entreverados, el color anverso de la colonia fue café claro y el reverso crema.
En el grupo II (M14, M16, M17, M20, M21, M25, M28, M41, M54) los aislamientos presentaron micelio más abundante, más compacto y con moteados de color salmón. El color anverso de las colonias fue café y salmón, el reverso fue crema. El grupo III (M2, M3, M6, M7, M8, M9, M11, M12, M18, M22, M23, M24, M29, M36, M37, M39, M40, M42, M44, M45, M47, M53, M56) se caracterizó por tener micelio abundante y más compacto que el de los dos grupos anteriores, con anverso de color café oscuro y reverso café claro. Todos los grupos presentaron aspecto pulverulento, plano con crecimiento radial, sin pigmentos difusibles en el medio, siendo similar a las observadas por Arbeláez (2010).
Regiones ITS
Se observó un bajo nivel de variación intraespecífica de los datos de las secuencias de los ITS para tamaño de bandas de algunas muestras analizadas para M. roreri, lo que posiblemente puede deberse a mutaciones producidas por deleción e inserción de bases como las reportadas por Phillips (2003).
La región ITS consiste de las variables no codificadas que están localizadas entre las repeticiones ADNr entre la altamente conservada pequeña subunidad, 5.8S, y los genes de la gran subunidad ARNr, ITS1 e ITS2 que tienen un papel funcional, el cual explica el alto nivel de variación de secuencia entre ellos. ITS es ahora la región más secuenciable del ADN del genoma en hongos y ha sido explotado para explicar o inferir en afinidades filogenéticas de grupos relacionados (Lee y Taylor, 1992). Para estudiar la relación genética de varias especies de Phytophthora que atacan cacao se utilizan también las secuencias de ambos, ITS1 e ITS2 (Phillips, 2003).
Según Bridge y Arora (1998) la región ITS es utilizada para estudios de caracterización molecular en hongos debido a que es una región relativamente corta (500 – 800 pb) y puede ser fácilmente amplificada por PCR utilizando solo pares de cebadores universales, que son complementarios para regiones conservadas entre los genes de la subunidad ARNr. La naturaleza multicopia del ADNr repetitivo hace que la región ITS sea fácil de amplificar, como se comprobó en este estudio al secuenciar algunas cepas de M. roreri, donde los rangos van de 762–787–827 pb.
Con la técnica PCR se comprobó que las tres bandas de ITS están en un rango relativamente corto de 600 – 780 pb. También esta región puede ser altamente variable entre especies distantes morfológicamente y los datos de restricción RFLPITS generados pueden ser usados para estimar la distancia genética y proveer características para análisis sistemático y filogenético. Asimismo, la PCR–ITS genera pruebas especie–específica que se pueden reproducir rápidamente, sin necesidad de producir una librería cromosomal, además, se pueden seleccionar secuencias de los ITS para pruebas especie–específicas, porque las secuencias ocurren en múltiples copias y guardan similitud entre ellas y son variables entre especies de hongos. Los análisis de los ITS no generan información suficiente en hongos (Bruns, White, y Taylor, 1991). Los cebadores diseñados por White et al. (1990) permiten la determinación de varias secuencias ITS de hongos que sirven para investigación taxonómica y relación filogenética entre especies de diferente género como Colletotrichum, Phytophthora y Penicillium (Edel, 1998). Además, han permitido desarrollar procedimientos rápidos y sencillos para la detección de especies de hongos fitopatógenos (Bridge y Arora, 1998; Edel, 1998).
Los análisis de secuencias ITS son de utilidad para reconstrucciones filogenéticas en una gran variedad de hongos, algas y plantas (Berbee y Taylor, 1999) En Colletotrichum y Alternaria se ha mostrado variación de secuencias a nivel interespecífico pero bajos niveles de variación intraespecifica en género de especies bien definidas (Cooke et al., 1997; Gardes et al., 1991). Por otra parte, se ha estimado variación en secuencias ITS entre especies de Laccaria y entre L. bicolor de 3–5% y de 1–2%, respectivamente. Además, esta variación en la información intraespecifica ha sido reportada para algunas especies de hongos tales como Fusarium oxysporum (Bridge y Arora, 1998) y Plerotus tuberregium (Isikhuemhen, Moncalvo, Nerud, y Vilgalys, 2000) Igualmente se ha demostrado por ITS que M. roreri está relacionada con C. perniciosa (Aime, 2005; Phillips, 2006).
Según Grisales y Afanador (2007) en Antioquia (Colombia) se ha observado que M. roreri, posee una gran similitud genética con bajos niveles de diversidad y diferenciación, indicando que la introducción de este patógeno en Antioquia es muy reciente. Estos estudios fueron realizados con los marcadores moleculares AP–PCR y RAPD. Información que ha sido relevante para continuar estudios con marcadores moleculares a partir de las muestras de M. roreri aisladas en Norte de Santander y que permitirán aclarar muchas dudas en cuanto al origen del fitopatógeno en este departamento y en Colombia. Según Arbeláez (2010), quien realizó caracterización molecular a través de la actividad de isoenzimas, Colombia es una de los países con mayor diversidad y posible origen de M. roreri.
Conclusiones
- En este trabajo se aisló e identificó molecularmente a Moniliophthora roreri extraído de Theobroma cacao en el departamento de Norte de Santander utilizando el marcador molecular ITS. El desarrollo de la técnica ITS permitió demostrar su aplicabilidad en M. roreri, siendo además una herramienta confiable para el estudio de variabilidad genética entre diferentes muestras y las relaciones existentes entre ellas.
- Los ITS fueron útiles para definir tres grupos subespecíficos. Una relativamente baja variación intraespecifica fue obtenida de los ITS analizados para los 56 aislamientos de M. roreri. Se observó la presencia de tres tamaños de amplicones de 600 pb, 740 pb, y 750 pb, distribuidos así: 600 pb para ocho aislamientos, 740 pb para doce aislamientos y 750 pb para los 36 aislamientos restantes.
Agradecimientos
Al Fondo de Investigaciones de la Universidad (FINU) de la Universidad Francisco de Paula Santander, por el apoyo financiero. A Fedecacao–Norte de Santander por facilitar las mazorcas infestadas de Moniliophthora roreri. A los Doctores Wilbert Phillips y Pedro Rocha por su valiosa colaboración y motivación para iniciar estudios con este hongo en Norte de Santander.
Referencias
Arbeláez, L. 2010. Análisis de la diversidad intraespecie de Moniliophthora roreri (Cif.) Evans et al. por medio de marcadores morfológicos y genéticos. Tesis de Magister en Biotecnología. Universidad Nacional de Colombia. Medellín, Colombia. 133 p. [ Links ]
Aime, M. C. y Phillips, W. 2005. The causal agents of witches' broom and frosty pod rot of cacao (chocolate, Theobroma cacao) form a new lineage of Marasmiaceae. Mycologia 97(5):10–12. [ Links ]
Barros, O. 1977. Investigaciones sobre el hongo Monilia roreri, Cif y Par, causante de la pudrición Acuosa de la mazorca del cacao: sus daños y su control. El Cacaotero Colombiano 3:42 – 43. [ Links ]
Barros, O. 1980. El control de la moniliasis en cacaoteras del Dique. El Cacaotero Colombiano15:31 – 44. [ Links ]
Berbee, M. L. y Taylor, J. W. 1999. Fungal phylogeny. UK. Cambridge University Press 21 – 71. [ Links ]
Brand, O. T. 2014. Estudio agronómico de las enfermedades escoba de bruja (Crinipellis perniciosa) y moniliasis (Moniliophthora roreri) en el cultivo de cacao (Theobroma cacao) en el departamento del Huila. Tesis de Ingeniería agronómica. Universidad Nacional Abierta y a Distancia. La Plata. Colombia. 68 p. [ Links ]
Bridge, P. D. y Arora, D. K. 1998. Interpretation of PCR methods for species definition. UK. CAB International 63 – 84 p. [ Links ]
Bruns, T. D.; White, T. J. y Taylor, J. W. 1991. Fungal molecular systematics. Ann. Rev. Ecol. Syst. (22):525 – 564. [ Links ]
Cooke, D. E. y Duncan, J. M. 1997. Phylogenetic analysis of Phytophthora species based on ITS1 and ITS2 sequences of the ribosomal RNA gene repeat. Mycol. Res. (101):667 – 677. [ Links ]
Edel, V. 1998. Polymerase Chain reaction in mycology. Applications of PCR in mycology. UK: CAB International 1 – 20 p. [ Links ]
Evans, H. C. 1981. Pod Rot of cacao caused by Moniliophthora (Monilia) roreri. Phytopath. Papers 24:7 – 49. [ Links ]
Gardes, M.; Mueller, G. M.; Fortin, J. A.; y Kropp, B. R. 1991. Mitochondrial DNA polymorphisms in Laccaria bicolor, L. laccata, L. proxima and L. amethystine. Mycol. Res. 95:206 – 216. [ Links ]
Grisales, S. y Afanador, L. 2007. Análisis de variabilidad genética en Moniliophthora roreri con AP–PCR y RAPD en Antioquia, Colombia. Rev. Col. Biot. 9(2):15 – 32. [ Links ]
Gutarra, B. A.; Silva, M. J.; Márquez, K. J.; y León, B. 2013. Análisis de la diversidad genética de 21 aislamientos del hongo Moniliophthora roreri basado en marcadores RAPD. Instituto de Cultivos Tropicales, San Martín, Perú. Apunt. Cienc. Soc. 03(02):100 – 110. [ Links ]
Isikhuemhen, O. S.; Moncalvo, J.M.; Nerud, F. y Vilgalys, R. 2000. Mating compatibility and phylogeography in Pleurotus tuberregium. Micol. Res. 104:732 – 737. [ Links ]
Lee, S. y Taylor, J. 1992. Phylogeny of five fungus–like protoctistan Phytophthora species, inferred from the internal transcribed spacer of ribosomal DNA. J. Mol. Biol. Evol. (9):636 – 653. [ Links ]
Mayes, S.; Jack, P.L.; Marshall, D. I.; y Corley, R. H. 1997. Construction of RFLP genetic link–age map for oil palm. (Elaeis guineensis Jacq.). Genome 40:116 – 122. [ Links ]
Orozco, C.; Osorio, C.; Botero, M. J.; Rivera, F. y López, G. 2011. Evaluación microbiológica y molecular de Moniliophthora perniciosa (Agaricales:Marasmiaceae). Museo de historia natural. Universidad de Caldas. Manizales. Colombia. Bol. Científico 15 (1):41 – 47. [ Links ]
Phillips, Wilbert. 2003. Origin, biogeography, genetic diversity and taxonomic affinities of the cacao (Theobroma cacao L.) fungus Moniliophthora roreri (Cif.) Evans et al. as determined using molecular, phytopathological and morpho–physiolofical evidence. Ph.D. Thesis 359 p. [ Links ]
Phillips, W. J.; Cawich, W.; Garnett y Aime, M. C. 2006. First report of frosty pod rot (moniliasis disease) caused by Moniliophthora roreri on cocoa in Belize. Plant Path. 55:584.
Phillips, W.A.; Cautiño, C.F. ; Ortiz, A.P. ; López, J.; Hernandez y Aime M.C. 2006. First report of frosty pod rot (moniliasis disease) caused by Moniliophthora roreri on cocoa in México. New Disease Reports (12):41.
Phillips, W.; Aime, M. y Wilkinson, M. 2007. Biodiversity and biogeography of the cacao (Theobroma cacao) pathogen Moniliophthora roreri in tropical America. Plant Pathol. 56:911 – 922. [ Links ]
Rocha, P. Marcadores moleculares, una herramienta útil para la selección genética de palma de aceite. 2003. Palmas 24(2):11 – 25. [ Links ]
Rorer, J. B. 1918. Enfermedades y plagas del cacao en el Ecuador y métodos modernos apropiados al cultivo de cacao. Guayaquil, Ecuador. Asociación de Agricultores. p. 17 – 40. [ Links ]
Sánchez, F. D. y Gárces, F. R. 2012. Moniliophthora roreri (Cif y Par) Evans et al. En el cultivo de cacao. Sci. Agrop. 3: 249 – 258. Disponible en: www.sci–agropecu.unitru.edu.pe. 1–10–2013. [ Links ]
Suárez, L. y Rangel, A. 2013. Aislamiento de microorganismos para control biológico de Moniliophthora roreri. Acta Agronómica 62(4):370 – 378. [ Links ]
Suárez, L. 2005. Extracción y purificación del ADN de Moniliophthora roreri, hongo que ataca el cacao, en Norte de Santander. Respuestas 10(2):3 – 7. [ Links ]
Suárez, L. 2006. Aislamiento e identificación de Moniliophthora roreri causante de la moniliasis en municipios del nororiente colombiano y ensayos preliminares para su control biológico. Respuestas 11(1):3 – 8. [ Links ]
Suárez, L. y Cabrales C. 2008. Identificación de especies nativas de Trichoderma sp, y Bacillus. Evaluación de su potencial antagonista in vitro frente al hongo fitopatógeno nativo Moniliophthora roreri en el departamento de Norte de Santander. Respuestas 13(1):45 – 56. [ Links ]
White, T. J.; Bruns, T.; Lee, S.; y Taylor, J.; 1990. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. San Diego, EE.UU. Academic Press 315 – 322 p. [ Links ]