Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.65 no.3 Palmira July/Sep. 2016
https://doi.org/10.15446/acag.v65n3.49771
http://dx.doi.org/10.15446/acag.v65n3.49771
Estimación de parámetros de calidad del fruto para segregantes interespecíficos de tomate de árbol (Solanum betaceum Cav.) en respuesta de resistencia a la Antracnosis (Colletotrichum acutatum J.H. Simmonds)
Estimation of fruit quality parameters for tree tomato (Solanum betaceum Cav.) interspecific segregating in response to Antracnose (Colletotrichum acutatum J.H. Simmonds) resistance
William Fernando Viera Arroyo 1*, Andrea Verónica Sotomayor Correa 1, María Viviana Tamba Sandoval 2, Wilson Arturo Vásquez Castillo1, Aníbal Martínez 1, Pablo Francisco Viteri Díaz 1 y Lenin Ron 2
1 Programa de Fruticultura, Estación Experimental Santa Catalina. Instituto Nacional de Investigaciones Agropecuarias (INIAP), Provincia de Pichincha, Mejía – Ecuador. 2 Universidad Central del Ecuador, Facultad de Ciencias Agrícolas, Jerónimo Leiton s/n y Av. La Gasca, Ecuador. *Autor para correspondencia: william.viera@iniap.gob.ec
Rec.: 24.03.2015 Acep.: 29.07.2015
Resumen
El tomate de árbol (Solanum betaceum Cav.) en el Ecuador, presenta una severa reducción en el rendimiento y producción, atribuida mayormente al ataque de la enfermedad antracnosis (Colletotrichum acutatum J.H. Simmonds). Con base a esta problemática, se ha optado por evaluar estratégicamente genotipos mejorados de tomate de árbol provenientes de la cruza [(S. unilobum x S. betaceum) x S. betaceum] x S. betaceum, con algún grado de resistencia a la antracnosis para generar una alternativa de manejo sostenible al ataque de esta enfermedad, la cual presenta una respuesta altamente detrimental en los cultivares comerciales tradicionalmente sembrados en la zona de estudio (Pelileo– Provincia del Tungurahua, Ecuador). Se encontraron diferencias significativas entre los grupos analizados tanto en variables de color de fruto y pulpa, así como en la variable cuantitativa de rendimiento, destacándose dos grupos (G1 y G5) por su bajo umbral de incidencia a la antracnosis; aunque en las variables productivas presentaron un menor avance. Un índice de selección basado en z–scores, permitió identificar individuos superiores en relación al grado de resistencia a la enfermedad y calidad del fruto. Los componentes genéticos de las variables fenotípicas evaluadas, demostraron que gran parte de la variabilidad genética observada se debe a los genotipos y muy poco a la variabilidad ambiental.
Palabras clave: Componente genético, fitomejoramiento para resistencia a enfermedades, modelo linear mixto, progenie.
Abstract
The tree tomato (Solanum betaceum Cav.) in Ecuador, performs a severe reduction in yield and production of tree tomato and it is mostly attributed to the attack of anthracnose disease (Colletotrichum acutatum J.H. Simmonds). We assessed an improved tree tomato genotypes, derived from the crossing [(S. betaceum unilobum x) x S. betaceum] x S. betaceum, showing some degree of resistance to generate an alternative of sustainable management to this disease on a site with a high degree of infection in commercial ecotypes (Pelileo– Province of Tungurahua, Ecuador). Significantly differences among the analyzed groups were found in fruit and flesh color, as well as in quantitative variables such as yield. Two groups (G1 and G5) were noted for their low incidence of anthracnose, although they showed less progress in terms of productive variables. A selection index based on z–scores, allowed identifying superior individuals in terms of resistance to the disease and fruit quality. The genetic component of phenotypic variables showed that most of the observed variability is due to the genotypes and not to the environmental variability.
Keywords: Genetic component, linear mixed model, plant breeding for disease resistance, progeny.
Introducción
El tomate de árbol (Solanum betaceum Cav.), es un frutal andino ampliamente cultivado en las regiones de clima frío moderado y subtropicales de Colombia, Ecuador y Perú. Particularmente en el Ecuador, la producción de tomate de árbol está confinada a pequeños y medianos productores de la Sierra y ha presentado grandes limitantes para expansión del cultivo y la exportación de la fruta como son: la falta de calidad y por la susceptibilidad a insectos plaga y enfermedades (Meza & Manzano, 2009; Carrillo et al., 2015).
Antracnosis ocasionada por el hongo Colletotrichum acutatum (Wharton & Diéguez, 2004; Falconí et al., 2013) es uno de los mayores limitantes del cultivo. Los síntomas ocasionados por esta enfermedad producen una disminución de la vida productiva de los árboles y en la mayoría de casos las pérdidas superan el 50% (Lobo, 2006; Alarcón y Chavarriaga, 2007). En Ecuador, investigaciones de antracnosis determinaron que tanto los cultivares comerciales anaranjados como morados son susceptibles al patógeno, y pueden alcanzar pérdidas entre el 60 y 100% de la producción, verificándose la poca resistencia genética a esta enfermedad en los cultivares más frecuentes como el 'Gigante Anaranjado', 'Anaranjado Puntón', 'Morado Gigante' y 'Redondo Anaranjado' (Falconí et al., 2013).
Factores ambientales como la lluvia y el viento, diseminan esta enfermedad en todo el cultivo (Peres et al. 2005). Estudios epidemiológicos señalan que el patógeno a más de atacar los frutos en cualquier edad o estado fenológico, también ataca hojas, ramas y el conjunto de órganos de la inflorescencia (Alarcón y Chavarriaga, 2007). Progresivamente, los frutos muestran pequeñas lesiones de apariencia aceitosa que se van convirtiendo a pardas o negras. En el centro de la lesión se va formando un polvillo de color rosado claro, que corresponde a la esporulación del hongo, y finalmente el fruto se seca hasta quedar momificado.
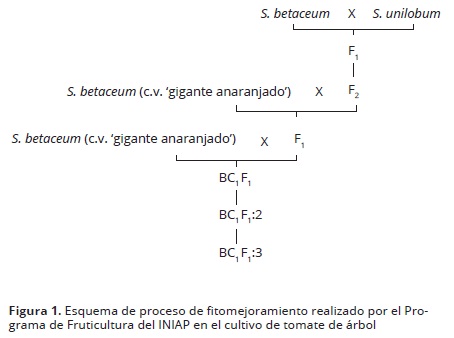
Las medidas de control para la enfermedad incluyen el manejo de la arquitectura del árbol, podas de follaje, remoción de frutos enfermos y el control químico del patógeno. El uso de fungicidas como benzimidazoles, han generado cada vez más tolerancia del patógeno, y en muchos casos se han vuelto prácticamente ineficientes. La demanda de alternativas de manejo de la enfermedad ha creado la necesidad de ampliar la base genética del tomate de árbol, mediante la hibridación interespecífica, a través de planes de mejoramiento que representen una solución y que haga posible el desarrollo productivo de este frutal (Acosta et al., 2011). Así mismo, en estudios realizados por el Programa Nacional de Fruticultura del INIAP (Instituto Nacional de Investigaciones Agropecuarias) en Ecuador, se han evaluado segregantes de cruzamientos interespecíficos entre el cultivar comercial S. betaceum por la especie silvestre S. unilobum, obteniéndose distintos niveles de resistencia, pero de deficiente calidad del fruto en cuanto a tamaño, color y sabor de pulpa, por lo que se han realizado retrocruzamientos hacia S. betaceum para recuperar dichas características. Posteriormente, se han seleccionado segregantes en función de la resistencia a la enfermedad, desempeño agronómico y calidad del fruto. De este modo, esta investigación tiene como objetivo evaluar segregantes de retrocruzas de (S. betaceum x S. unilobum) hacia S. betaceum (Figura 1), para identificar individuos con características de calidad de fruto y resistencia a antracnosis.
Materiales y métodos
Ubicación Geográfica. El trabajo de campo se llevó a cabo en la localidad de Sigualó Alto (Cantón Pelileo, Provincia de Tungurahua, Ecuador: 01°19' 57'' S; 78° 27' 49'' W), localizada a 2400 m.s.n.m., la precipitación anual de la zona es de 556 mm al año, la temperatura máxima es de 27.40°C, temperatura mínima de 3.90°C, y temperatura media de 15.30°C. La humedad relativa promedio durante el estudio fue de 78.11%. Este sitio presenta una fuerte incidencia de la enfermedad en los cultivares 'Gigante Anaranjado' y 'Puntón Anaranjado' de tomate de árbol que se cultivan con alta presencia de inóculo circulante.
Material biológico. Cinco grupos de segregantes (retrocruza con S. betaceum) más un control susceptible se utilizaron el estudio (Figura 1). Para todas las plantas evaluadas se utilizó tabaquillo (Nicotiana glauca) y palo blanco (Solanum auriculatum) como portainjertos debido a su tolerancia a nematodos (en particular Meloidogyne incognita) y hongos (Fusarium solani). Los segregantes evaluados provienen de cruzas interespecíficas y retrocruzas [[(S. unilobum x S. betaceum) x S. betaceum] x S. betaceum] mismos que fueron agrupados en función de características físicas del fruto como el color de cáscara, pulpa y mucílago, presencia y color de vetas en la cáscara, así como la forma del fruto considerando los descriptores morfológicos del fruto publicados por Bioversity International (2013) (Tabla 1). Adicionalmente se utilizó el cultivar 'Gigante Anaranjado' (S. betaceum) como testigo experimental por su susceptibilidad a antracnosis. Inicialmente se plantaron 120 plantas de cada grupo (720 plantas), con una sobrevivencia final total de 267 plantas (Tabla 1).
Manejo del cultivo. El experimento se llevó a cabo en junio de 2012. La distancia de plantación utilizada fue de 1.5 m entre plantas x 2 m entre hileras. Todas los segregantes y el grupo testigo se distribuyeron en cinco bloques. Inicialmente 24 plantas de cada grupo fueron asignadas para cada bloque. Las evaluaciones se realizaron cuando las plantas alcanzaron el estado adulto. En el proceso de crecimiento muchas plantas se perdieron por diferentes causas no atribuidas a la enfermedad en estudio. Las plantas que presentaron una mayor respuesta detrimental, fueron reemplazadas posteriormente para llenar los espacios vacíos con segregantes del mismo grupo. El área del ensayo ocupó una superficie de 850 m2. La cosecha de frutos se realizó en forma manual cuando los frutos presentaron el 75% del color característico a la madurez.
Inóculo de Colletotrichum acutatum J.H. Simmonds. El sitio escogido para implementar el estudio es una zona de alta incidencia de antracnosis, el patógeno se aisló de frutos afectados en medio de cultivo Papa Dextrosa Agar (PDA). El inóculo del hongo se preparó raspando con una espátula las conidias producidas en las colonias de crecimiento y colocando agua destilada. La suspensión de conidias se ajustó a 1.20 x 106 conidias/ml de agua, utilizando la cámara de Neubauer. Esta solución conidial del patógeno se aplicó en campo con el uso de una bomba de mochila (julio de 2013). Posteriormente a la inoculación se cubrieron los frutos con fundas plásticas por 15 días. Cabe recalcar que en los lotes colindantes en estado productivo se presentaba una severa incidencia de la enfermedad. Así mismo, en el agua de riego, frecuentemente había presencia frutos contaminados viajando a los distintos lotes.
Variables dependientes evaluadas
Porcentaje de frutos infectados con antracnosis. Se contabilizó el número de frutos que presentaron síntomas, así como el número de frutos sanos y se calculó el porcentaje de incidencia de la enfermedad. El conteo de frutos se realizó cada 15 días durante tres meses.
Severidad de antracnosis. Se evaluó como porcentaje de tejido afectado por el patógeno calificando visualmente el área afectada que presentaron los frutos de cada una de las plantas, considerando a un fruto sano como 0% y a uno momificado como 100% (Moral et al., 2008). Esta variable se registró en diez frutos enfermos (cosechados o caídos) por planta.
Rendimiento por árbol. En cada grupo de plantas se registró el peso total de los frutos (sanos y enfermos) cosechados por planta, expresado en gramos. Para la evaluación se utilizó una balanza tipo reloj Camry.
Color de la cáscara de los frutos. Se registró en base a la escala establecida por Biodiversity International (2013), donde los colores posibles para esta variable fueron rojo, anaranjado y amarillo.
Color de mucílago de las semillas. Se registró en base a la escala establecida por Biodiversity International (2013), donde los colores posibles para esta variable fueron anaranjado, rojo y morado.
Sólidos Solubles. Para la determinación de esta variable se utilizó el jugo de frutos de tomate de árbol en madurez de consumo. Con el uso de un refractómetro manual DY – T20 se registró los grados Brix presentes en un fruto/planta en todos los grupos. Esta evaluación se realizó una sola vez con frutos de las primeras cosechas.
Acidez titulable. Se utilizó 30 g de pulpa de fruta licuada y se aforó a un volumen de 200 ml con agua destilada. Se tomó una alicuota de 20 ml para realizar una titulación con hidroxido de sodio 0.1 N hasta que en medidor de pH marque el 8.2 (viraje del indicador de la fenolftaleína) y se expresó el resultado de acuerdo al ácido predominante en la muestra.
Análisis Estadístico. El análisis de la información se realizó en dos etapas: 1) El contraste entre las medias de los genotipos segregantes se determinó en base a contrastes pares generados entre ellos. Estas diferencias se realizaron utilizando la prueba de Holm para la serie de pruebas sin necesidad de combinar en una única varianza y la correspondiente corrección por la inflación del error de significación. La falta de homogeneidad dentro de los grupos de segregantes fue verificada tanto gráficamente así como a través de la prueba de Bartlett con una significación estadística del 5%. 2) Por otro lado, para el análisis de la información genética se utilizó un modelo lineal mixto separadamente por grupo de segregantes. De esta manera el único efecto ambiental debido a los bloques donde estuvieron cada grupo segregantes constituyó el único efecto aleatorio. La estimación de componentes de varianza se basó en el Método Máxima Verosimilitud Restringida (REML). El modelo estadístico para la evaluación fue el siguiente: . Donde Gi representa el efecto del bloque i. De esta manera, la covariación entre dos medidas del mismo bloque ; por lo es la varianza dentro de sujetos debido efectos netos del genotipo. La proporción que representa respecto de la variabilidad total () es la estimación proporcional de este componente (Componente genético) que se estimó, dado que se pretende hacer selección dentro de los segregantes. La estimación de los efectos fijos y aleatorios se realizó en el paquete estadístico R v.2.1.5., a través del paquete lme4 ®.
Selección de segregantes. Se realizó selección directa con base a los promedios alcanzados por cada uno de los segregantes. Para escoger los mejores individuos a ser reproducidos, se realizó un promedio ponderado de z–scores () para estimar un índice de selección dónde, la resistencia a la antracnosis recibió una ponderación de 0.50, los sólidos solubles de 0.05, total de frutos una ponderación de 0.25 y 0.20 para peso promedio de frutos. Finalmente, se estimó un promedio de z score de los individuos para cada genotipo.
Resultados y discusión
Porcentaje de frutos con antracnosis
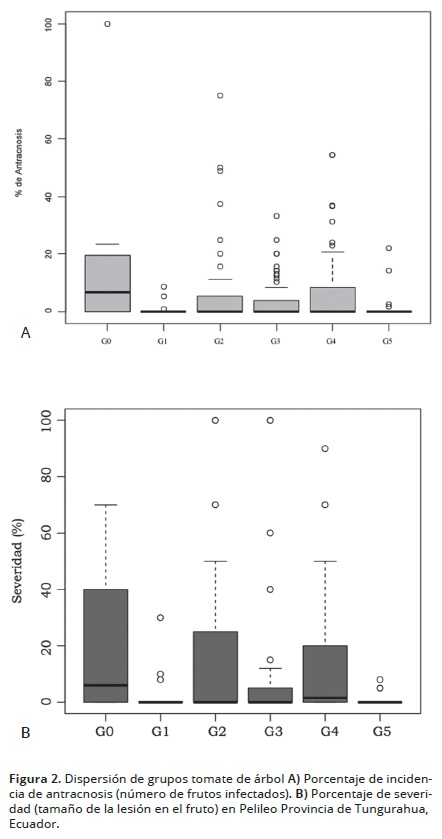
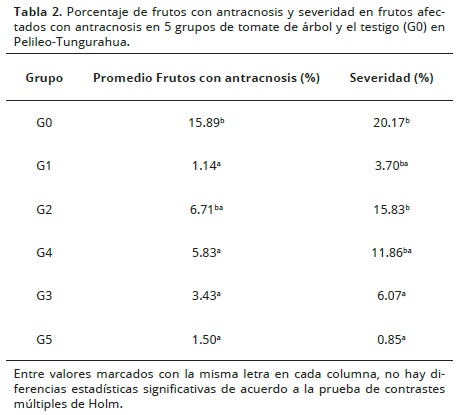
En el período evaluado (agosto–octubre 2013) se encontró un promedio de 15.89% de frutos con síntomas típicos de la enfermedad en las plantas testigo de tomate de árbol ('Gigante anaranjado'). El 60% de plantas del cultivar comercial presentaron frutos enfermos, y el 15% de éstas tuvieron el 100% de incidencia (Figura 2 A).
El grupo G1 constituido por 13 plantas, presentó un mínimo de ningún fruto enfermo y un máximo de 8.70%; de las cuales 11 plantas (84%) exhibieron porcentajes de infección de hasta 2.90%. La mayoría de plantas de este grupo muestran una infección comprendida entre 0 y 3%, solamente tres datos (puntos dispersos) se encuentran alejados de la respuesta general del genotipo (Figura 2 A). El grupo G2 conformado por 52 plantas, presentó un mínimo de ningún fruto enfermo y un máximo de 75%; de las cuales 45 plantas (87%) exhibieron porcentajes de infección < 15%. En el grupo G3 constituido por 73 plantas, presentó un mínimo de ningún fruto enfermo y un máximo de 33.33%; de las cuales 57 plantas (79%) mostraron porcentajes de infección < 5.56%. El grupo G4 conformado por 90 plantas, exhibió un mínimo de ningún fruto enfermo y un máximo de 54.55%; de las cuales 71 plantas (79%) exhibieron porcentajes de infección de hasta 9.09%. El grupo G5 constituido por 27 plantas, presentó un mínimo de ningún fruto enfermos y un máximo de 22.22%; de las cuales 25 plantas (92%) manifestaron porcentajes de infección comprendidos entre 0 y 5.56%. La mayoría de plantas de este grupo muestran una infección comprendida mayormente entre 0 y 3%. (Figura 2 y Tabla 2).
Severidad de antracnosis
La resistencia a antracnosis es un caracter que alcanza valores moderados de herencia en poblaciones provenientes de cruzamientos de padres resistentes (Stommel, 2001; Syukur et al., 2013). En el período de evaluación, se encontró que el testigo (G0) y los grupos segregantes G2 y G4, mostraron ser los grupos más afectados por la enfermedad con medias de 20.17, 15.83 y 11.86%, respectivamente (Figura 2 B). De acuerdo al análisis de varianza, las plantas de los grupos G1, G3 y G5 presentaron diferencias estadísticas, observándose menor severidad de antracnosis respecto de los grupos antes mencionados, siendo G5 el grupo con menor severidad menor al 1%. En las condiciones agroclimáticas en las que se desarrolló la presente investigación, la mayoría de plantas de los grupos evaluados presentaron una severidad promedio de 7.66%. En adición a lo anterior, cabe destacar que todas las plantas testigo fueron infectadas en mayor grado, a diferencia del material mejorado que expone intragrupalmente plantas libres de antracnosis.
Color del fruto (Cáscara)
El grupo testigo (G0) es el único que presentó 100% de frutos con cáscara de color anaranjado. Las plantas de los grupos G1 y G3 manifiestan homogeneidad respecto a este carácter con el 100% de frutos con cáscara de color amarillo. En los grupos G2, G4 y G5 se observa una segregación de este carácter, ya que los frutos de las diferentes plantas exhibieron colores distintos. El grupo G2, presentó 49 plantas (94%) con frutos de color anaranjado y 3 plantas (6%) fueron de color rojo. El grupo G4, presentó 75 plantas (83%) con frutos de color anaranjado, 9 plantas (10%) fueron de color rojo y 6 plantas (7%) de color amarillo. El grupo G5, presentó 26 plantas (96%) con frutos de color anaranjado y 1 planta (4%) fue de color amarillo. En función de lo anterior, en los grupos de segregantes G2, G4 y G5 habría que hacer selección para eliminar caracteres indeseables para el mercado, o a su vez intentar motivar la aceptación de otras coloraciones para la comercialización de esta fruta.
Esta característica ha demostrado ser altamente heredable en estudios realizados en varios frutales (Brown et al., 2009; Zaouay & Mars, 2014) ya que está controlado principalmente por pocos genes de carácter dominante.
Color del mucílago
Las plantas que conforman los grupos G0 (testigo) y G2 se destacan por presentar un 100% de coloración anaranjada. El grupo G1 exhibió 12 plantas (92%) con frutos de color de mucílago anaranjado y 1 planta (8%) con mucílago de color rojo. El grupo G5 presenta 25 plantas (92%) con frutos de color de mucílago anaranjado, una planta (4%) fue de color morado y una planta (4%) exhibió un color rojo. El genotipo G3 presentó un 66% de frutos con mucílago de color rojo, 12% de color anaranjado y 22% morado. En los segregantes G4, se presentaron un 52% de frutos con mucílago color rojo, 37% color anaranjado y un 11% morado. A pesar de que los grupos presentan alta variabilidad, y que el mercado de consumo en fresco en general acepta coloración anaranjada para el consumo, los grupos G3 y G4 se caracterizan por tener mucílago rojo y cualidad antioxidante.
El color rojo en el mucílago está relacionado con las cantidad de antocianinas, Dossett et al. (2008), reportaron valores moderados de heredabilidad de este compuesto. Sin embargo de acuerdo a nuestros resultados, el color anaranjado fue predominante en los segregantes evaluados.
Peso promedio de frutos
El grupo G2 presentó mayor peso promedio con 106.30 g por fruto (Tabla 3); en el mismo rango estuvieron el genotipo testigo G0 con 103.80 g, G4 con 98.78 g y G1 que compartió un segundo rango de clasificación junto con G3 y G5 que obtuvieron valores de 93.30, 82.75 y 72.67 g respectivamente. En el presente estudio, se observó que los segregantes que presentaron mucílago amarillo (grupo G2) mostraron el mayor peso promedio por fruto.
Los grupos G3 y G5 son los que presentaron menor peso promedio junto con G1; sin embargo, mostraron mayor resistencia a antracnosis, lo que podría inferir que tienen caracteres heredados de la accesión silvestre (S. unilobum), la misma que ha presentado resultados de resistencia a esta enfermedad (Rueda et al. 2005). Además Acosta et al. (2011), mencionan que frutos que presentan menor tamaño están relacionados con las especies silvestres de tomate de árbol.
Los grupos estudiados presentaron una media cercana a de 93 g, valor igual al reportado por Acosta et al. (2011), quienes evaluaron 24 accesiones de tomate de árbol, que en su mayoría (58,33%) eran de origen ecuatoriano. Sin embargo, el rango de variación entre accesiones en nuestro estudio fue menor, ya que el peso promedio mínimo y máximo registrado fue de 72.67 y 106.30 g respectivamente, mientras que en el estudio de Acosta et al. (2011), se reportaron valores entre 30.50 y 154.20 g, siendo un caracter de alta heredabilidad (0.96).
En el rendimiento de los grupos, el testigo G0 obtuvo un rendimiento de 3340 g/árbol, compartiendo rango con G1, G2 y G4, mientras que G3 y G5 presentaron menores rendimientos.
Grados brix y acidez titulable
Los grupos G2, G4 y G5 presentan diferencias estadísticas frente al grupo testigo (G0), en las variables de sólidos solubles (°brix) y acidez, destacándose G2 con 11.02 °brix y acidez de 1.66% (Tabla 3). En segregantes africanos de tomate de árbol estudiados por Mwithiga et al. (2007) se obtuvo un máximo de 10.90 °brix, resultado similar obtenido por Belén et al. (2004), quienes evaluaron segregantes venezolanos, reportando un porcentaje de grados brix de 10% y acidez de 1.35%. En estudios realizados en otros frutales, Ohtsuka et al. (2004) mencionan que existe un alto efecto genético aditivo en lo relacionado al contenido de azúcares. Sin embargo, la heredabilidad puede variar dependiendo del tipo de azúcar presente en el fruto (Viera et al., 2013).
Componente genético
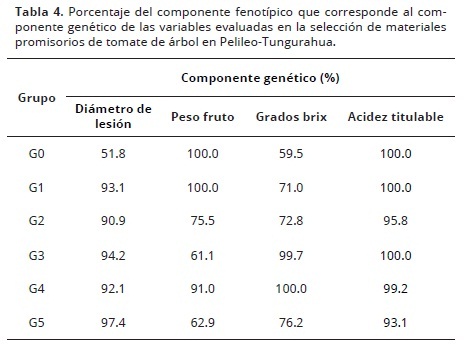
El componente genético (Tabla 4), para la variable sólidos solubles (grados brix), el grupo testigo (G0) tuvo un 59% de componente genético mientras que la diferencia fue debido a factores ambientales. En los grupos G1 y G5 estos valores fueron de 71 y 76%, mientras que en el grupo G4 toda la variabilidad se debió a la variación dentro de individuos. Ciertamente la variabilidad interna aún es muy fuerte respecto de la variabilidad ambiental, lo que demuestra que hay opciones para el establecimiento de un programa de mejoramiento genético vegetal.
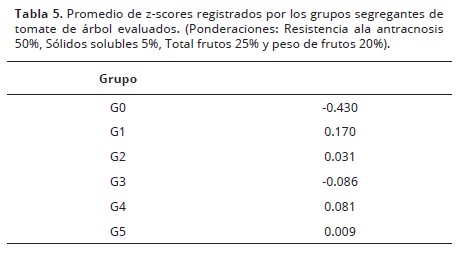
Los grupos analizados presentan diferencias en los z–scores promedios (Tabla 5). Aunque la selección es individual, los individuos que estuvieron sobre una desviación estándar sobre el promedio de la población fueron seleccionados. Así mismo, los valores de las ponderaciones para las cuatro variables involucradas en el análisis, consideró la resistencia a la antracnosis como el principal componente con un 50% del peso, la segunda variable en importancia fue el total de frutos por árbol con un 25% y el peso de los frutos con 20%. La intencionalidad de este índice es aportar información relevante respecto a la resistencia genética, pero además, propender por el mantenimiento de las características comerciales.
Conclusiones
- Los grupos G1 y G5, presentaron bajos niveles de infección por antracnosis, comparados con la variedad susceptible 'Gigante Anaranjado' (G0), por lo cual los segregantes dentro de estos grupos son considerados como promisorios para continuar con el proceso de mejoramiento de este frutal.
- Los análisis de los componentes genéticos, demuestran que en la mayoría de las variables analizadas los componentes genéticos son altos, siendo la variabilidad interna de los genotipos la que tiene supremacía respecto de la variabilidad ambiental.
Agradecimientos
A la Sra. Martha Sambache y su familia por el invaluable apoyo. A la Secretaría Nacional de Educación Superior, Ciencia, Tecnología e Innovación (SENESCYT) y al Instituto Nacional de Investigaciones Agropecuarias (INIAP), Ecuador, por el financiamiento de esta investigación.
Referencias
Acosta. P. Martinez. J. Prohens. J. (2011). Variation among tree tomato (Solanum betaceum Cav.) accessions from different cultivar groups: implications for conservation of genetic resources and breeding. Genet Resour Crop Ev, 58(6), 943–960. doi: 10.1007/s10722–010–9634–9. [ Links ]
Alarcón. J. & Chavarriaga. W. (2007). Diagnóstico precoz de la antracnosis (Colletotrichum gloeosporioides) (Penz) Penz & Sacc. en tomate de árbol mediante el empleo de infecciones quiescentes. Agron, 15(1), 89–102. [ Links ]
Belén. D. Sánchez. E. García. D. Moreno–Álvarez. M. Linares. O. (2004). Características fisicoquímicas y composición en ácidos grasos del aceite extraído de semillas de tomate de árbol (Cyphomandra betacea Sendt) variedades roja y amarilla. Grasas y Aceites, 55(4), 428–433. [ Links ]
Bioversity International. (2013). Descriptors for tree tomato (Solanum betaceum Cav.) and wild relatives. Bioversity International, Rome, Italy. 57p.http://www.bioversityinternational.org/uploads/tx_news/Descriptors_for_tree_tomato__Solanum_betaceum_Cav.__and_wild_relatives_1578.pdf. 06.04.2014. [ Links ]
Brown. J. Raymond. Schnell. R. Ayala. T. Moore. J. Tondo. C. Winterstein. M. (2009). Broad–sense heritability estimates for fruit color and morphological traits from open–pollinated half–sib mango families. Hort Sci, 44(6), 1552–1556.
Carrillo. E. Aller. A. Cruz. S. Giampieri. F. Álvarez. J. (2015). Andean berries from Ecuador: A review on Botany, Agronomy, Chemistry and Health Potencial. J Berry Res, 5(2), 49–69. doi: 10.3233/JBR–140093. [ Links ]
Dossett. M. Lee. J. Finn. C. (2008). Inheritance of phenological, vegetative, and fruit chemistry traits in black raspberry. J Amer Soc Hort Sci, 133(3), 408–417. [ Links ]
Falconí. C. Visser. R. Van Heusden. A. (2013). Phenotypic, molecular, and pathological characterization of Colletotrichum acutatum associated with Andean lupine and tamarillo in the Ecuadorian Andes. Plant Dis, 97(6), 819–827. doi:10.1094/PDIS–02–12–0175–RE. [ Links ]
Lobo. M. (2006). Recursos genéticos y mejoramiento de frutales andinos: una visión conceptual. Corpoica, 7(2), 40–54. [ Links ]
Mwithiga. G. Inzoberi. M. Shitanda. D. Nyota. P. (2007). Evaluation of the effect of ripening on the sensory quality and properties of tamarillo (Cyphomandra betaceae) fruits. J Food Eng, 79(1), 117–123. doi:10.1016/j.jfoodeng.2006.01.035. [ Links ]
Meza. N. Manzano. J. (2009). Características del fruto de tomate de árbol (Cyphomandra betaceae [Cav.] Sendtn) basadas en la coloración del arilo, en la Zona Andina Venezolana. UDO Agrícola, 9(2), 289–294. [ Links ]
Moral. J. Bouhmidi. K. Trapero. A. (2008). Influence of fruit maturity, wounding, inoculum density, inoculation method, and cultivars susceptibility on infection of olive fruit by Colletotrichum acutatum. Plant Dis, 92(10), 1421–1426. doi: 10.1094/PDIS–92–10–1421. [ Links ]
Ohtsuka. Y. Kibe. H. Hakoda. N. Shimura. I. Ogiwara. I. (2004). Heritability of sugar contents in strawberry fruit in the F1 populations using a common pollen parent. J Japan Soc Hort Sci, 73(1), 31–35. doi: 10.2503/jjshs.73.31. [ Links ]
Peres. N. Timmer. L. Adaskaveg. J. & Correll. J. (2005). Lifestyles of Colletotrichum acutatum. Plant Dis, 89(8), 784–796. doi: 10.1094/PD–89–0784. [ Links ]
Rueda. A. Echeverri. F. Torres. F. Gallego. A. Quiñones. W. Lobo. M. (2005). Perfil químico y microbiológico del tomate de árbol (Cyphomandra spp.) y su papel contra Colletotrichum gloeosporioides Penz agente causal de la antracnosis. Actual Biol, 27(1), 117–121. [ Links ]
Stommel. J. (2001). Selection influences heritability estimates and variance components for anthracnose resistance in populations derived from an intraspecific cross of tomato. J Amer Soc Hort Sci, 126(4), 468 – 473. [ Links ]
Syukur. M. Sujiprihati. S. Koswara. J. Widodo. (2013). Genetic analysis for resistance to anthracnose caused by Colletotrichum acutatum in chili pepper (Capsicum annuum L.) using diallel crosses. Sabrao J Breed Genet, 45(3), 400–408.
Viera. W. Alspach. P. Brewer. L. Johnston. J. Winefield. C. (2013). Genetic parameters for sugar content in an interspecific pear population. Europ J Hort Sci, 78(2), 56–66. [ Links ]
Wharton. P. Diéguez. J. (2004). The biology of Colletotrichum acutatum. Anales del Jardín Botánico de Madrid, 61(1), 3–22. doi:10.3989/ajbm.2004.v61.i1.61. [ Links ]
Zaouay. F. Mars. M. (2014). Phenotypic variation and estimation of genetic parameters to improve fruit quality in Tunisian pomegranate (Punica granatum L.) accessions. J Hort Sci Biot, 89(2), 221–228. [ Links ]