Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.65 no.4 Palmira Oct./Dec. 2016
https://doi.org/10.15446/acag.v65n4.50327
http://dx.doi.org/10.15446/acag.v65n4.50327
Compuestos de hierro para la fortificaciónde alimentos: El desarrollo de una estrategia nutricional indispensable para países en vía de desarrollo. – Una revisión
Iron compounds for food fortification: The development of an essential nutritional strategy for developing countries. A review
Angélica Maria Serpa Guerra, Lina Maria Vélez Acosta, Jaime Alejandro Barajas Gamboa, Cristina Isabel Castro Herazo y Robin Zuluaga Gallego*
Facultad de Ingeniería Agroindustrial. Grupo de Investigaciones Agroindustriales (GRAIN), Universidad Pontificia Bolivariana. Medellín, Antioquia–Colombia. *Autor para correspondencia: robin.zuluaga@upb.edu.co
Rec.: 30.04.2015 Acep.: 30.11.2015
Resumen
La deficiencia de hierro (Fe) ha sido reconocida como un problema de salud pública, debido a sus implicaciones económicas y en el bienestar de la población humana. Para países en desarrollo como Colombia, esta deficiencia afecta a gran parte de sus habitantes, especialmente a los niños y a las mujeres en estado de gestación. De allí la importancia de generar estrategias como la fortificación de alimentos con hierro, con el objetivo de mejorar los niveles de consumo en la población y contrarrestar las consecuencias que se generan con la carencia de este mineral, entre las que se incluyen fallas en el desarrollo mental y motor, y alteraciones del sistema inmune. Por lo anterior, en la presente revisión se plasman los principales conceptos sobre la fortificación de alimentos con hierro, incluyendo los factores que influyen en su aprovechamiento a nivel fisiológico, su importancia desde el punto de vista nutricional, las tecnologías aplicadas durante la fortificación de alimentos y las últimas tendencias de este tipo de productos, como la bio–fortificación y la nano–tecnología, con el fin de contribuir a los procesos de investigación y desarrollo de estrategias nutricionales cuyo eje central sea la prevención y el control de la deficiencia de hierro.
Palabras clave: alimentos funcionales, anemia, deficiencia, fortificación, nutrición, salud pública.
Abstract
Iron (Fe) deficiency has been recognized as a public health problem due to its health and economic implications. In developing countries like Colombia this deficiency still affects a large part of its population, especially children and pregnant women. Hence the importance of developing strategies such as food fortification with iron to improve the levels of consumption in the population and offset the consequences generated by the lack of this mineral, including mental and motor development, and immune system disorders. In this review, the main concepts of iron food fortification are developed, including the main factors which influence their physiological use, its importance from the nutritional point of view, the technologies used for food fortification and the latest trends in this type of products, such as biofortification and nanotechnology, all this in order to contribute to the research and development of nutritional strategies whose central point is iron deficiency as an strategy of prevention and control.
Keywords: anemia, deficiency, functional food, nutrition, public health
Introducción
El hierro es un mineral con gran importancia para el buen desarrollo del ser humano y el mantenimiento de su organismo (Nadadur, Srirama & Mudipalli, 2008), y a su vez, se utiliza como indicador para determinar el estado nutricional de las personas. Este mineral, hace parte de diversas enzimas y complejos moleculares que participan en los procesos metabólicos (Conrad & Umbreit, 2000). Sus principales funciones incluyen el transporte de oxígeno por medio de la hemoglobina (Hb) (Toxqui, De piero, Courtois, Bastida, Sánchez–Muniz y Vaquero, 2010) que se deriva en la producción de energía, su participación en la síntesis, degradación y almacenamiento de neurotransmisores (Suárez, Cimino & Bonilla, 1985), en la función eritropoyética y en la respuesta inmune de las células (Muñoz, García–Erce y Remacha, 2011).
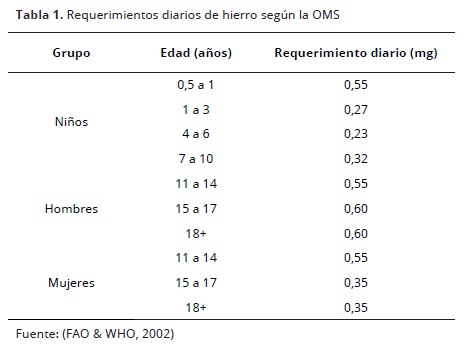
Debido a la importancia del hierro en el organismo, la Organización Mundial de la Salud (OMS) en el 2002, determinó los requerimientos diarios de este mineral para el cumplimiento de todos los procesos metabólicos en los que interviene, como se observa en la Tabla 1; lo anterior teniendo en cuenta la población de interés y su edad (FAO & WHO, 2002).
De igual manera, a partir de los requerimientos de hierro que el organismo necesita, se han establecido los porcentajes de valor diario recomendado (VDR) para este mineral, que se utilizan como referencia para los procesos de desarrollo, producción y etiquetado de producto. Es importante resaltar, que dichos valores cambian según la norma consultada para cada país, como se observa en la Tabla 2; además en Argentina, Estados Unidos y Venezuela, se tienen los valores diarios recomendados diferenciados para cada población, mientras que en países como Brasil, Ecuador, El Salvador y México, la normativa presenta un valor general, que en la mayoria de los casos es tomado directamente del reportado como valor de referencia en el Codex Alimentarius (14 mg).
Los valores de referencia son proporcionados por la FAO/OMS y tienen como base la evaluación reciente de los datos científicos, que luego van encaminados a reflejar las recomendaciones de ingesta para la población general; sin embargo, el Codex también establece las directrices para determinar los VDR para subgrupos específicos y que inician con la revisión de valores o intervalos que hayan sido establecidos por organismos científicos competentes (Codex Alimentarius, 1993).
Los requerimientos y valores diarios recomendados de hierro son un buen punto de partida a la hora de caracterizar nutricionalmente una población, si se tiene en cuenta que la deficiencia de este mineral está considerada como una de las problemáticas nutricionales más comunes a nivel mundial, afectando aproximadamente al 30 % de la población (WHO, 2006). Esta situación es más predominante en los países en desarrollo (Boccio et al. 2004) y Colombia no es la excepción a este escenario, ya que según la última Encuesta Nacional de la Situación Nutricional (ENSIN) de 2010, en el país, la prevalencia de anemia por deficiencia del mineral está entre un 7,6 % y un 27 % (ICBF, 2011). Este tipo de deficiencia es multifactorial, ya que su desarrollo está condicionado a aspectos culturales, sociales y económicos, cuya consecuencia es la alteración de la calidad de vida de las personas por efectos a nivel inmunológico, físico y digestivo. Además, se ha establecido que las pérdidas causadas por deficiencia de micronutrientes como el hierro, representan en incapacidades y muertes, un costo del 5% del Producto Interno Bruto (PIB), mientras que la implementación de estrategias nutricionales adecuadas como la fortificación de alimentos, tiene un costo menor al 0,3 % del PIB.
Entre las causas que pueden ocasionar una deficiencia de hierro, se pueden señalar la insuficiente ingesta del mineral debido a la baja bio–disponibilidad del hierro no hemítico presente en las dietas basadas en hortalizas; frutos secos y cereales, y a la baja ingesta de carne, fuente de hierro hemático o hémico (Gaitán et al. 2006). Por otro lado, la deficiencia de hierro también se presenta, por la baja absorción de este mineral, debido a las interacciones entre diversos componentes de la dieta que se convierten en factores sinérgicos e inhibidores de su absorción (Gaitán et al. 2006), de allí, la importancia de reconocer los mecanismos y las sustancias responsables de dicho comportamiento.
Por lo anterior, la obtención de alimentos fortificados, es decir productos con adición de micronutrientes, se presenta como una estrategia que busca contrarrestar la deficiencia de micronutrientes como el hierro en la población y a su vez, como uno de los métodos utilizados para la elaboración de productos funcionales, encaminados hacia la obtención de alimentos con alto valor agregado, teniendo en cuenta la creciente preocupación de la población por estilos de vida más saludables. Asi, la presente revisión, busca establecer las principales características de los procesos de fortificación de alimentos, especialmente con hierro, teniendo en cuenta los factores que influyen en el aprovechamiento de este mineral a nivel fisiológico, su importancia desde el punto de vista nutricional y las directrices que rigen dicho proceso. De igual manera, se abordan las metodologías y tendencias de mercado frente a este tipo de productos, presentando un acercamiento a las nuevas corrientes que tratan la fortificación de alimentos e incluyen la bio–fortificación y la nano–tecnología, todo esto con el fin de contribuir al acercamiento y entendimiento de la deficiencia de hierro como un problema de salud pública, que requiere especial atención y para el que la fortificación de alimentos, representa una de las mejores estrategias para su prevencion y control.
Bio–disponibilidad y absorción del hierro
La absorción del hierro no hemático en el tracto digestivo se da mediante diferentes mecanismos (Gaitán et al. 2006): a) por solubilización y reducción en el medio gástrico, b) por absorción en el duodeno proximal y c) por mecanismos de reducción del hierro férrico a ferroso en el borde cepillo del enterocito y co–transporte de hierro ferroso y H+ a través del transportador de metales divalentes (DMT1). Según las necesidades corporales del nutriente, éste se almacena en la proteína citoplasmática ferritina y se utiliza en los procesos metabólicos celulares o se transporta hacia la sangre (Miret, Simpson & Mckie, 2003).
En cuanto al hierro hemítico, se conoce que es solubilizado en el tracto gastrointestinal sin ser modificado, se transporta en compañía del anillo de protoporfirina hacia el duodeno (Forrellat Barrios et al. 2000), de allí que su absorción sea mayor al hierro no hemítico, ya que es la estructura hemo la que permite su entrada directa en las células de la mucosa del intestino en forma de complejo hierro–porfirina.
Por otro lado, se ha estudiado el efecto del índice de masa corporal de las mujeres sobre la absorción de hierro y aunque los resultados aún no permiten establecer una relación entre estos, se observó que las mujeres obesas presentaron una menor absorción de este mineral que aquellas con sobrepeso o peso normal, comportamiento atribuido a las inflamaciones subclínicas derivadas de la obesidad (Mujica–Coopman et al. 2015).
En cuanto a la bio–disponibilidad del hierro, es decir la porción de este mineral que el organismo absorbe y utiliza para las funciones corporales (Hurrel & Egli, 2010), se ha establecido que depende de las cantidades ingeridas, de la combinación de alimentos en una comida (ya que a un pH básico existe la tendencia de formar precipitados con componentes de la dieta) y por factores intraluminales; lo que disminuye su solubilidad y por lo tanto su absorción (Gaitán et al. 2006). A su vez, factores como el estado nutricional del hierro y algunos eventos que requieran modificar la movilización del mineral entre los tejidos o la absorción del mismo, como la eritropoyésis aumentada, la hipoxia y las infecciones, afectan también su bio–disponibilidad, incrementando su absorción durante la deficiencia del metal, las anemias hemolíticas y por la hipoxia, mientras que disminuye durante los procesos infecciosos o inflamatorios (Gaitán et al. 2006).
Antagonistas de la bio–disponibilidad del hierro
Como se mencionó anteriormente, existen varios factores que influyen en la absorción del hierro en el organismo. Entre los principales inhibidores de la bio–disponibilidad de este mineral, se encuentran los fitatos, compuestos presentes en las dietas basadas en frutas y vegetales (Hurrel, 1997), los cuales generan una inhibición entre un 51 y un 82 %. De igual manera se ha encontrado que los polifenoles presentes en el té negro y en el vino actúan como inhibidores de la absorción del hierro (Binaghi et al. 2011), ya que contribuyen a la formación de complejos insolubles que no son absorbidos por el organismo (Allen & Ahluwalia, 1997).
La presencia de calcio también influye negativamente en la absorción del hierro hemático y no hemático (Hurrell & Egli, 2010), aunque esta última afirmación está siendo estudiada, debido a los resultados contradictorios que han arrojado recientes investigaciones (Miranda et al. 2014).
Finalmente, algunos minerales también están siendo clasificados como antagonistas de la absorción del hierro, debido a diversos estudios in vivo e in vitro que han dado como resultado, la disminución de la absorción, debido a la interacción con otros minerales como cobre y zinc, y a la inhibición competitiva con el manganeso (Arredondo, Martínez & Nuñez, 2006; Olivares et al. 2007).
Sinergistas de la bio–disponibilidad del hierro
La presencia de vitamina C o ácido ascórbico, aumenta la bio–disponiblidad del hierro no hemítico (Gaitán et al. 2006). Este efecto se atribuye a su capacidad de reducir el ion férrico a su forma ferrosa (soluble), a su acción para formar quelatos solubles y absorbibles a pH alcalino (duodeno) y a su capacidad antioxidante (Trinidad et al. 2014).
La vitamina A también es reconocida por incrementar la bio–disponibilidad del hierro no hemítico al formar complejos solubles con iones férricos, además, se ha establecido que la concentración de esta vitamina es uno de los nutrientes responsables de modular el metabolismo del hierro y por ende su homeostasis (Gaitán et al. 2006).
Deficiencia de hierro
Como se mencionó anteriormente, la deficiencia de hierro se presenta porque la mayor parte del mineral se encuentra en forma férrica (no hemático), el cual es difícil de absorber y poco bio–disponible, comportamiento inverso al hierro hemático de origen animal, que presenta una bio–disponibilidad de 2 a 3 veces mayor que la del hierro no hemático (Alcaraz et al. 2006). Sin embargo, la escasez de proteína animal en la dieta actual, hace que la deficiencia de hierro sea responsable del 15 % de los casos de anemia en la población mundial, presentándose prevalencia del 10 % y 50 %, en países desarrollados y en desarrollo respectivamente, siendo los niños, los adolescentes y las mujeres, los más afectados (WHO, 2008).
De manera general, se establece que la deficiencia de hierro se debe a múltiples factores, tales como un inadecuado consumo, una baja absorción, un aumento de la demanda o una excesiva pérdida del mineral (Denic & Agarwal, 2007) y se caracteriza por una disminución de los depósitos de hierro, con baja concentración sérica y baja saturación de transferrina, lo que implica cambios en los niveles de la concentración de hemoglobina (De Paz & Fernández Navarro, 2005).
Enfermedades asociadas a la deficiencia
La anemia es una enfermedad que ha sido considerada como un problema de salud pública, debido a que afecta a un cuarto de la población mundial, principalmente a niños en edad preescolar (47,4 %), seguido de mujeres gestantes (41,8 %) y mujeres en edad fértil (30,2 %), siendo esta enfermedad un problema de salud severo característico de la población infantil en países Latinoamericanos como Brasil, Perú y Bolivia, y de las mujeres en período de gestación y en edad reproductiva en Perú (WHO, 2008). Esta enfermedad se caracteriza por la disminución de la concentración de hemoglobina (proteína que se encuentra dentro de los glóbulos rojos) en el organismo, y cuya función es el transporte de oxígeno a través de todos los tejidos del cuerpo humano. Su principal causa es la deficiencia de hierro, elemento fundamental, sin el cual no se puede obtener la movilización de dicha proteína (Moreira & López San Román, 2009).
Las manifestaciones de la deficiencia de hierro incluyen las causadas por una disfunción de las enzimas dependientes de este mineral, y de aquellas propias de la anemia, e incluyen alteraciones de la capacidad de trabajo físico y de la actividad motora espontánea, alteraciones de la inmunidad celular debido al papel de este mineral en diversas enzimas como la mielo–peroxidasa, la cual es requerida para la producción de radicales hidroxilo por los neutrófilos en respuesta a la presencia de bacterias (Soyano & Gómez, 1999). Otras implicaciones incluyen la alteración de la termogénesis, alteraciones funcionales e histológicas del tubo digestivo, falla en la movilización de la vitamina A hepática, menor transferencia de hierro al feto, disminución de la velocidad de crecimiento, mayor riesgo de parto prematuro y de morbilidad perinatal, y alteraciones conductuales (Allen, 2000). Todas las consecuencias derivadas de la deficiencia de hierro, principalmente del padecimiento de la anemia, generan un impacto importante en el desarrollo del individuo desde la edad temprana, que a su vez se traduce en efectos a nivel social y económicos, ya que a esta enfermedad se asocian los costos generados al estado por su tratamiento (costos directos) y costos indirectos por la reducción en la productividad y rendimiento actual y futuro de la población (Action Against Hunger, 2013).
Fortificación de alimentos
La adición o fortificación con micronutrientes de los alimentos que hacen parte de la canasta básica familiar, es una de las estrategias más empleadas para prevenir y corregir las deficiencias y enfermedades descritas anteriormente, gracias a que estos alimentos logran llegar a gran parte de una determinada población. Fue así como surgió en Suiza y Estados Unidos la fortificación de sal con yodo en 1920 (Burgi, Supersaxo & Selz, 1990), y se fue expandiendo a nivel mundial como una buena opción para controlar la deficiencia de este mineral, al igual que las fortificaciones de cereales realizadas en 1940 con tiamina, riboflavina y niacina (WHO, 2006), la fortificación de azúcar con vitamina A en algunos países de Centro y Sur América (Asamblea Legislativa de la República el Salvador, 1994; Ministerio de Salud, 1998) y la fortificación de harina de trigo con vitaminas y minerales (incluyendo el hierro) en América Latina y el Caribe (Muzzo, 2004).
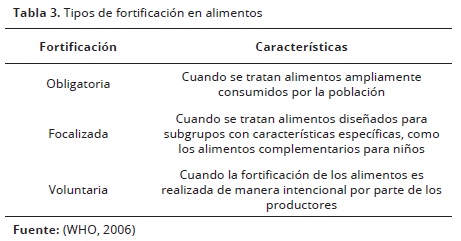
Al hablar de fortificación, se debe tener en cuenta que existen diferentes tipos (Tabla 3). Dentro de las fortificaciones obligatorias, se encuentran aquellas establecidas por mandatos gubernamentales, encaminadas a tratar problemas nutricionales identificados en la población y que incluyen las adiciones de micronutrientes en harina, azúcar y sal, mencionadas anteriormente. Ejemplo de ello, es la fortificación con hierro de maicena y harina decretada en Venezuela a partir 1993, que se tradujo en una reducción de la deficiencia de hierro del 37 % al 15 % en 1994 (Layrisse et al. 1996). Situación similar a la presentada en Chile después de decretar la adición de ácido fólico en la harina de trigo, que contribuyó a la disminución del 40 % en las tasas de defecto del tubo neural (Hertrampf & Cortés, 2004), y la fortificación de azúcar con vitamina A en Nicaragua a partir del 2000, que generó un aumento en la concentración plasmática de retinol de 0,97 a 1,17 mol.L-1 en tan solo un año (Ribaya et al. 2004).
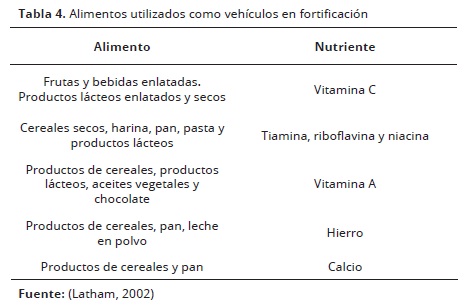
En cuanto a la fortificación voluntaria, es decir, aquella realizada por los productores de manera autónoma, se ha establecido, que en Colombia, las principales matrices utilizadas son los cereales para el desayuno, las pastas, y las bebidas, mientras que los nutrientes más adicionados son las vitaminas A, C y B1, y los minerales hierro, zinc y calcio. A nivel mundial, compañias como General Mills, Gerber Products, Kraft Foods, Unilever y The Procter and Gamble Co., poseen diversas patentes para desarrollos en alimentos fortificados, que incluyen técnicas y premezclas. De igual manera, la FAO, ha identificado los cereales, las frutas y los productos lácteos como los vehículos más utilizados en los procesos de fortificación (Tabla 4).
Fortificar alimentos con nutrientes es un asunto de gran importancia, su propósito va dirigido a beneficiar la salud de las personas, por ello debe hacerse de manera responsable y con conocimientos científicos y técnicos del tema, además, debe tener en cuenta los siguientes aspectos (Latham, 2002):
- La carencia (o riesgo) del micronutriente en la población debe estar demostrada en gran parte de la población.
- El alimento o matriz a fortificar debe ser de alto consumo en la población para la cual está dirigida la fortificación.
- Si se fortifica, la declaración de salud de un alimento funcional debe estar aceptada en la normativa existente, o se debe contar con los estudios científicos requeridos que demuestren que dicho nutriente genera cierto beneficio o disminución de riesgo de enfermedad.
- La interacción entre la matriz alimentaria y el nutriente que se va adicionar, no debe disminuir su absorción y bio–disponibilidad; o generar cambios organolépticos indeseados en el producto final.
- Se debe evaluar la factibilidad técnica para que a nivel industrial se pueda realizar la adición del nutriente, teniendo en cuenta costos operacionales.
- Tener en cuenta los valores diarios recomendados que se debe adicionar del nutriente, según la población a quien va dirigido el alimento.
Fortificación de alimentos con hierro
La fortificación de alimentos con hierro, surge como una estrategia nutricional que busca solucionar los problemas generados por la deficiencia de este mineral. En Colombia dicha fortificación es una de las más comunes, en gran parte, debido a los resultados obtenidos en la Encuesta Nacional de la Situación Nutricional en Colombia de los años 2005 y 2010, en las que se evidencia la deficiencia de hierro como uno de los indicadores con mayor prevalencia en la población del país, generando la necesidad de proveer mecanismos para evitar y disminuir la anemia, enfermedad asociada a esta deficiencia. En Colombia, gracias al Decreto 1994 de 1996, la fortificación de harina de trigo con hierro es una medida obligatoria en el territorio nacional, para todos los productores y comercializadores, ya sea para la venta directa al consumidor o para la fabricación de productos de panadería, pastelería, galletería entre otros (Ministerio de Salud, 1996). Esta situación es similar a lo ocurrido en otros 30 países de América Latina y el Caribe incluyendo Bolivia, Argentina, Brasil, Chile y Costa Rica, donde esta fortificación es obligatoria por declaración gubernamental (Muzzo, 2004).
Diferentes estudios han demostrado que el consumo de alimentos enriquecidos con hierro mejora la concentración de hemoglobina y ferritina en sangre. Este es el caso de un estudio realizado en Pontal, Brasil, con 50 niños entre 12 y 72 meses de edad con el fin de evaluar el consumo de un jugo de naranja fortificado con hierro, en el que se determinó la hemoglobina antes y después del estudio, cuya duración fue de 4 meses durante los cuales, de lunes a viernes, se suministró a cada niño dos porciones de 200 ml de jugo de naranja fortificado con 20 mg de sulfato ferroso (heptahidratado). Los resultados mostraron un incremento de la Hb de 10,45 mg.dl-1 a 11,60 mg.dl-1, y una disminución de la anemia (hemoglobina menor a 11,0 mg.dl-1) del 60 % al 20 % (Nogueira de Almeida et al. 2003). En Teresina, Brasil, se suministró un snack rico en proteína, vitaminas y hierro, a niños con anemia entre 32 y 72 meses de edad, el cual generó una reducción del 61,5 % al 11,5 % de prevalencia de la enfermedad (Moreira Araújo, Araújo & Areas, 2008).
En Vietnam se estableció que el consumo de salsa de pescado fortificado con etilendiaminotetraacetato ferrosódico (NaFeEDTA), puede mejorar el estado nutricional de hierro, incremetando los valores de ferritina de 13.6 mg.L–1 a 30.9 mg. ml –1 y minimizando la deficiencia en las mujeres anémicas de esta población (Thuy et al. 2003), mientras que en la India, un estudio llevado a cabo durante dos años, donde se le brindó a la población curry fortificado con hierro, mostró una reducción de la anemia por deficiencia de hierro del 22 % al 5 % en la población femenina y un aumento de los niveles de ferritina en la población masculina (Ballot et al. 1989).
De igual manera, se ha demostrado que la fortificación con hierro de bebidas como la avena (Trinidad et al. 2014) y las fórmulas para bebes (Maldonado Lozano et al. 2007) ofrecen un mecanismo para aumentar los niveles del mineral en niños y así minimizar la presencia de anemia.
Por otro lado, es importante tener en cuenta que el hierro también hace parte de los procesos de investigación que se llevan a cabo en bio–fortificación, y surge como una metodología para lograr la incorporación de nutrientes en alimentos vegetales durante su producción primaria, gracias a la importancia de los productos agrícolas en la canasta familiar, nuevamente como alternativa para dar solución a las deficiencias nutricionales de la población. Por ejemplo, se han realizado investigaciones que evalúan la posibilidad de incrementar la concentración de hierro en el arroz, a través de su adición en los suelos de cultivo del cereal, con el fin de aumentar la absorción desde las raíces de la planta, gracias a los mecanismos de reducción y solubilización que han surgido como respuesta evolutiva de los cultivos (Bashir et al. 2013). De igual manera, se ha utilizado la manipulación genética, para mejorar el almacenamiento del hierro en los granos de arroz, logrando la expresión de la ferritina, proteína encargada de dicho proceso (Masuda et al. 2012).
Compuestos de hierro utilizados para la fortificación de alimentos
Compuestos de alta solubilidad como el sulfato ferroso aportan hierro de alta bio–disponibilidad para ser adicionado, pero poseen la desventaja de permitir que el hierro libre iónico interactué con los componentes del alimento, produciendo cambios en las propiedades sensoriales del mismo, además este metal ayuda a la oxidación de los ácidos grasos insaturados y al enranciamiento de los lípidos ya que actúa como catalizador (Boccio & Bressan Monteiro, 2004). El proceso de oxidación afecta las vitaminas y las enzimas, disminuyendo el valor nutricional del alimento (Hurrel, 1997), sin embargo, estudios recientes están encaminados a la utilización de compuestos que ayuden a evitar la oxidación producida por el hierro orgánico empleado para la fortificación, es así como se ha establecido que el uso de palmitato ascorbilo, podría generar estabilidad oxidativa en productos de panificación, mientras que el ácido cítrico actúa como sustancia pro–oxidante (Alemán et al. 2014).
Otros compuestos como el fumarato ferroso y succinato ferroso, son de solubilidad media y presentan buena bio–disponiblidad. Sin embargo, poseen la restricción de ser utilizados en alimentos líquidos, ya que se precipitan en medios acuosos y la fracción del hierro interactúa con el alimento. Finalmente, compuestos como el orto–fosfato–férrico y el hierro elemental son de baja solubilidad y por lo tanto no producen cambios significativos en el alimento, pero presentan la desventaja de una reducida absorción y a su vez una baja bio–disponibilidad (Boccio & Bressan Monteiro, 2004).
La utilización de compuestos de hierro protegidos, surgen como una estrategia para fortificar los alimentos debido a la necesidad de la industria, por elementos con alta bio–disponibilidad y que no interactúen con el alimento. Uno de estos es el sulfato ferroso estabilizado o micro encapsulado, en el cual, la sal se encuentra protegida por una membrana de almidón/maltodextrina/goma arábiga (Gupta et al. 2015) o por fosfolípidos (Boccio et al. 1997), evitando la interacción del metal con el alimento. Sin embargo, es importante tener en cuenta, que los altos costos de procesamiento (micro encapsulación) se desplazan al producto final, lo que restringe su utilización. Otro ejemplo de un compuesto protegido es el hierro aminoquelado, que presentó mayor efectividad que el sulfato ferroso, y que corresponde a un estudio clínico en niños preescolares con deficiencia de hierro (sin anemia), llevado a cabo en la ciudad de Medellín Colombia, y que tenia como objetivo determinar la eficacia de la fortificación de leche con los dos compuestos. Se concluyó que aunque ambos compuestos aumentaron los niveles de ferritina en el organismo, el grupo de niños que consumió hierro amino–quelado logró un aumento mayor que los que consumieron sulfato ferroso (Rojas et al. 2013).
Finalmente, compuestos estabilizados como el EDTA–Fe, presentan una elevada bio–disponiblidad en presencia de inhibidores y son estables en los procesos industriales; no obstante, generan cambios de color en las matrices alimentarias en las que se adicionan (Boccio & Bressan Monteiro, 2004).
Métodos y técnicas aplicados a la fortificación de alimentos
Las metedologías que se utilizan para realizar los procesos de fortificación de alimentos, incluyen diversas técnicas que se aplican desde la producción primaria hasta el procesamiento, siendo la incorporación a granel, la más utilizada. Esta, consiste en la adición directa de los nutrientes en el producto durante su proceso, cuya cantidad dependerá del aporte establecido y de la fase de inclusión, ya que se deben tener en cuenta todos los factores de industrialización responsabes de las pérdidas de los nutrientes incorporados, y que requieren tratamientos térmicos como la pasteurización y diversas operaciones mecánicas (Cortés, Chiralt & Puente, 2005).
La impregnación al vacío, es un método relativamente nuevo, que busca reemplazar el gas ocluido en la microestructura celular de los alimentos, por solutos contenidos en un líquido de impregnación, mediante la acción capilar y de los gradientes de presión aplicados en el sistema (Ostos et al. 2012). Dicha metodología ha permitido obtener fresa fortificada con vitamina E (Restrepo, Cortés & Rojano, 2010) y mango adicionado con calcio (Ostos et al. 2012).
Por otro lado, la utilización de la ingeniería genética para la fortificación de alimentos, constituye una de las tecnologías con mayor controversia, debido a la importancia actual de los alimentos genéticamente modificados (GM), aún asi, se han desarrollado productos como el "Golden rice" o arroz dorado, que ha sido manipulado para producir beta–caroteno, al realizar una modificación del ADN utilizando información de la planta Narcissus pseudonarcissus (Beyer et al. 2002), o papas genéticamente modificadas para alterar su composición nutricional (Prescha et al. 2003). Otros métodos aplicados en la fortificación de alimentos, se llevan a cabo en los procesos de producción primaria, realizando modificaciones en las técnicas de cultivo y en la cría de animales, con el fin de generar cambios en la composición de los alimentos; ejemplos de esto, es el desarrollo de huevos fortificados con omega 3 y de leche con ácido linoleico (Cortés et al. 2005). Tanto la modificación genética como la fortificación por fertilización, hacen parte de lo que hoy se conoce como bio–fortificación, y que corresponde al mejoramiento agronómico del contenido de micronutrientes en los alimentos de origen vegetal de primera necesidad y que ha permitido desarrollar productos como cebollas fortificadas con zinc (Almendros et al. 2015), al igual que zanahorias y brócoli adicionados con selenio (Banuelos et al. 2015), todo esto, enfocado a las necesidades nutricionales de la población.
Las metodologías presentadas anteriormente, y que se resumen en la Tabla 5, permiten establecer los diferentes enfoques que ha tenido la investigación en torno a la fortificación de alimentos, y que incluyen desde procesos simples que han tenido su origen desde hace varios años, como la adición directa en el alimento, hasta métodos más complejos que aún se encuentran en estudio como la manipulación genética y el uso de la nano–tecnología para el desarrollo de compuestos dirigidos a mejorar las caracteristicas nutricionales de los alimentos.
La nanotecnología, es el término que define las áreas de la ciencia y la ingeniería en la que los fenómenos ocurren en escalas nanométricas y se utilizan para llevar a cabo procesos de diseño, caracterización y producción de materiales, estructuras y sistemas a niveles atómicos y moleculares (Scenihr, 2006). En cuanto a la fortificación de alimentos se refiere, las investigaciones y aplicaciones en nanotecnología apuntan al mejoramiento de la bio–disponibilidad de los nutrientes y por tanto al aumento de los beneficios nutricionales para las personas. En esta vía, se están desarrollando nano–partículas para la fortificación, que pueden ser adicionadas en los alimentos, y cuyo fin es controlar la liberación del micronutriente una vez ingerido en el alimento (Joye, Davidov–Pardo & McClements, 2014). Otra aplicación busca la generación de nano–emulsiones para encapsular y proteger los micronutrientes, evitando la interacción con las matrices alimentarias y por tanto la oxidación, solubilización y generación de malos sabores y olores en los alimentos (Fathi, Mozafari & Mohebbi, 2012).
Normativa para la fortificación de alimentos
Los alimentos fortificados fueron el punto de partida para el nacimiento de los alimentos funcionales y surgieron en Japón en 1984 con la búsqueda de una definición para los alimentos adicionados con constituyentes especiales, que presentaban efectos fisiológicos beneficiosos en quién los consume (Bigliardi & Galati, 2013). Así, la normativa que rige los procesos de fortificación de alimentos, incluyendo la fortificación de alimentos con hierro, está directamente relacionada con las directrices establecidas para el desarrollo, la producción y venta de alimentos funcionales a nivel mundial, que en muchos casos se relaciona a su vez con los requisitos para etiquetado nutricional.
Panorama internacional
En 1997, el Codex Alimentarius estableció "Las directrices para el uso de declaraciones nutricionales y saludables en el etiquetado", y que incluyen la declaración de propiedades nutricionales y las relativas al contenido de nutrientes, donde se establece la declaración de "Alto contenido" para vitaminas y minerales cuando en el producto se adiciona más del 30% del VDR por porción (Codex Alimentarius, 1997). Situación similar a la presentada en la Union Europea, donde se estableció que la declaración nutricional de vitaminas y minerales se debe realizar de acuerdo al aporte mínímo por porción. Aun así, en este territorio se ha creado una comisión de acción concertada sobre bromatología funcional (Functional Food Science in Europe– FUFOSE), con el fin de desarrollar y establecer las bases científicas sobre las evidencias que deben soportar el desarrollo de productos alimenticios que puedan tener un efecto beneficioso sobre una función fisiológica del organismo, mejorar el estado de salud de una persona o disminuir el riesgo de enfermedad. Por otro lado, es importante mencionar, que Japón, es el país que más ha profundizado en la normatividad para este tipo de productos, desarrollando un marco legal bajo el sello FOSHU (Foods for Specified Health Use), para el cual, se debe comprobar científicamente que el alimento, más no sus componentes aislados, ejercen un efecto saludable sobre el organismo cuando se consume como parte de una dieta normal (Moreno, 2012).
En Estados Unidos, la regulación de los alimentos funcionales, se encuentra relacionada directamente con las declaraciones permitidas en el etiquetado nutricional, y que incluyen las relacionadas con el contenido de nutriente, con la salud y las declaraciones de estructura/función, necesitando las dos últimas, la evaluación de la FDA antes de su uso en el etiquetado de los productos.
La situación en América Latina no difiere mucho de la presentada anteriormente, donde la normativa de los alimentos funcionales se aborda desde las declaraciones permitidas en los alimentos. Sin embargo, es importante destacar, la declaración aprobada en Chile, que permite establecer en el etiquetado de los alimentos que "Una ingesta adecuada de hierro es el principal factor de prevención de anemia nutricional por déficit de hierro", solo si el producto es una alta fuente de hierro y si el compuesto utilizado para la fortificación es de aceptable bio–disponibilidad como el sulfato ferroso, las formas protegidas, los aminoquelados, el NaEDTA o los microencapsulados (Ministerio de Salud, 2009).
Situación en Colombia
En Colombia la adición o fortificación de nutrientes, incluyendo el hierro, es regulado por medio de la Resolución 333 de 2011 del Ministerio de Salud y Protección Social, por la cual establece el "Reglamento técnico sobre los requisitos de rotulado o etiquetado nutricional que deben cumplir los alimentos" y donde se incluyen los valores diarios recomendados de los nutrientes, que constituyen el punto de partida para las fortificaciones alimentarias. A lo largo de la norma, se hace referencia a los diferentes tipos de declaraciones nutricionales asociadas al contenido de nutrientes en el alimento, y que inlcuyen:
- La declaración de las propiedades relacionadas con el contenido de nutriente, en la cual se describe el nivel de un determinado nutriente en un alimento, por ejemplo "Buena fuente de hierro" o "Alto contenido de fibra y bajo en grasa".
- La declaración de propiedades comparativas, en la cual se confronta los niveles de nutrientes y/o valor energético de dos o más alimentos, por ejemplo "Reducido en", "Fortificado con hierro".
Por otro lado, en el artículo 19 del capítulo V, la Resolución establece los términos o descriptores permitidos para las declaraciones de propiedades comparativas y que incluye en el numeral 19.3, las especificaciones para la declaración de "enriquecido/fortificado/adicionado", cuando al alimento se le ha adicionado por lo menos un 10 % y no más del 100 % del valor de referencia para las vitaminas, minerales, proteína y fibra, teniendo en cuenta que el término "enriquecido/adicionado/fortificado", debe aparecer en la etiqueta seguido de la preposición "con" y del nutriente (s) que ha sido añadido (Ministerio de la Protección Social, 2011).
Finalmente, se debe tener presente la clasificación establecida en la Resolución 719 del 11 de marzo de 2015 del Ministerio de Salud y Protección Social, para los productos fortificados y/o adicionados, como alimentos de alto riesgo en salud pública, especialmente para trámites y solicitud de notificación, permiso o registro sanitario ante el INVIMA (Ministerio de Salud y Protección Social, 2015).
Tendencias del mercado de los productos fortificados con hierro
Como se mencionó anteriormente, los alimentos fortificados fueron el punto de partida para el nacimiento de los alimentos funcionales (Bigliardi & Galati, 2013), razón por la cual, las tendencias actuales de la fortificación de alimentos, estan unidas a los nuevos desarrollos de alimentos funcionales. Particularmente, en la última decada, los requerimientos del consumidor han cambiado, debido a un mejor entendimiento de la relación que existe entre alimentación y salud, por esto, los alimentos se buscan para satisfacer el hambre y proveer los nutrientes necesarios, al igual que como parte fundamental para prevenir las enfermedades asociadas con la alimentación y mejorar la calidad de vida. Lo anterior, se ve reflejado en las estadísticas del mercado de los alimentos funcionales establecidas por Euromonitor, que alcanzaron para el 2011 los 691 billones de dólares y cuya proyección para finales del 2015 se espera sea de 862 billones de dólares (Tabla 6). De igual manera, se estableció un incremento en la venta de alimentos fortificados que pasó de 169,4 billones de dólares en 2007 a 230 billones en 2011 (Fresno, 2012), reflejando la importancia de este tipo de alimentos en las preferencias del consumidor.
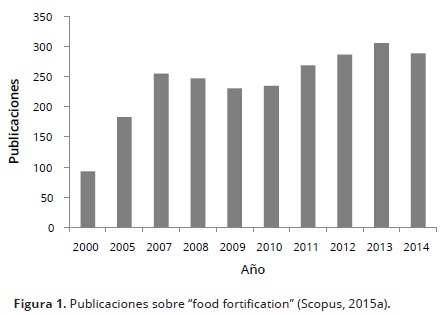
El incremento en las ventas de alimentos fortificados y funcionales, son una oportunidad de mercado que invita a los productores a llevar a cabo metodologías de innovación y desarrollo en productos, procesos y materias primas, con el fin de satisfacer las crecientes demandas que existen en este mercado, y que se ven reflejadas en el aumento de las publicaciones llevadas a cabo en los últimos años, como muestran los resultados arrojados por el portal Scopus, el cual se presenta en la Figura 1, al realizar la búsqueda de "Food fortification" .
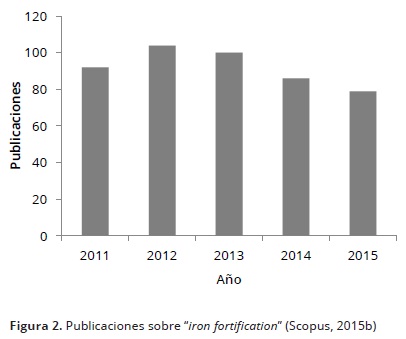
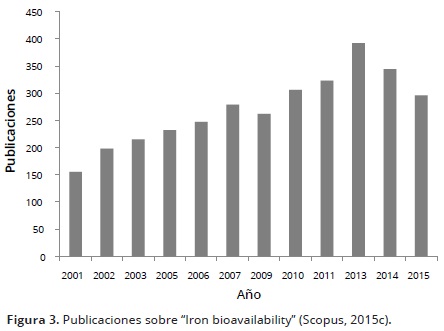
Por otro lado, al realizar la búsqueda de "Iron fortification" se observa una reducción de las publicaciones en los últimos 5 años como se observa en la Figura 2. Sin embargo, en el mismo portal, se evidencia un incremento en las publicaciones encaminadas hacia la biodisponibilidad de este mineral (Figura 3), donde se presentan las publicaciones correspondientes a la búsqueda de "Iron Bioavailability".
Dentro de dichas investigaciones, se encuentran resultados acerca de la evaluación de sinérgia entre las proteínas y la absorción del hierro, que han permitido establecer que proteínas de origen animal y productos generados durante su digestión no aumentan la absorción del hierro hemítico (Pizarro et al. 2016), situación similar a la observada con las protínas de origen vegetal que a excepción de la proteína de soya (que actúo como antagonista), no afectaron la absorción de este tipo de hierro (Weinborn et al. 2015). De igual manera, otro estudio evidenció a nivel in–vitro, que productos comerciales fortificados con hierro, presentaron mayor biodisponibilidad que las tabletas de sulfato de hierro, utilizadas tradicionalmente para tratar pacientes con anemia por deficiencia de este mineral (Christides et al. 2015). Por otro lado, algunos estudios encontrados en el portal Scopus, se refieren a la evaluación de nuevos compuestos para fortificar alimentos con hierro, dentro de los cuales se puede destacar que el sulfato de hierro estabilizado con maltodextrina y ácido cítrico permite desarrollar fórmulas lácteas para niños con alta biodisponibilidad (Pizarro et al. 2015); mientras que proteínas a partir de salvado de arroz desengrasado pueden incrementar la biodisponibilidad del hierro y ser utilizadas para el desarrollo de alimentos fortificados con este mineral (Foong, Imam & Ismail, 2015).
Los resultados anteriores, permiten establecer que el hierro como compuesto para fotificar, aún es de gran importancia en el mundo, y su principal interés en la actualidad radica en establecer y mejorar los métodos a través de los cuales nuestro organismo aprovecha biológicamente este compuesto, con el fin de mejorar e inclementar la efectividad de los procesos de fortificación de alimentos.
Por lo anterior, se presenta la fortificación de alimentos con hierro, como la estrategia de intervención nutricional más efectiva para contrarrestar la deficiencia de este mineral y todas las consecuencias que este padecimiento trae consigo, incluyendo enfermedades como la anemia y transtornos en el desarrollo y mantenimiento del organismo. Sin embargo, a la hora de realizar esta fortificación se deben tener en cuenta diversos factores para lograr que la intervención sea exitosa, como las características de la población objetivo, el tipo de matriz alimentaria y sus componentes, el compuesto químico a utilizar y la normativa nacional que rige dicho proceso. De allí, la importancia de las investigaciones que buscan generar nuevos productos y materias primas que permitan mejorar e incrementar la eficacia de los planes de intervención basados en la fortificación de alimentos. Por otro lado, es importante, plantear la necesidad que presentan algunos países como El Salvador y Ecuador, por establecer nuevos valores diarios recomendados (VDR) de hierro, según su población, y de esta manera contribuir al planteamiento de progrmas de intervención nutricional más específicos y efectivos.
De igual manera, se debe resaltar la importancia de los procesos tecnológicos a la hora de generar nuevos productos fortificados, si bien existen metodologías utilizadas de manera segura como la adición a granel o la impregnación al vacío, en la actualidad surgen también técnicas de manipulación genética o que involucran la nanotecnología en este campo, que deben ser investigadas a fondo, con el fin de evaluar los efectos a mediano y largo plazo que pueden generar este tipo de productos, no solo en la salud humana si no también en la dinámica de la producción agroindustrial a nivel mundial.
Agradecimientos
Los autores agradecen a la Gobernación de Antioquia, al Sistema General de Regalías de Antioquia y al Grupo de Investigaciones Agroindustriales (GRAIN) de la Universidad Pontificia Bolivariana, cuyo apoyo fue esencial para la realización de la presente revisión.
Referencias
Action Against Hunger. (2013). El problema de la anemia en Perú. http://www.accioncontraelhambre.org/files/file/informes/anemia_peru.pdf. 04.03.2015. [ Links ]
Alcaraz – López. G. M. Bernal Parra. C. Aristizábal– Gil. M. A. Ruiz – Villa. M. B. & Fox – Quintana. J. E. (2006). Anemia y anemia por déficit de hierro en niños menores de cinco años y su relación con el consumo de hierro en la alimentación. Invest Educ Enferm, 24, 16–29. [ Links ]
Alemán. M. Bou. R. Tres. A. Polo. J. Codony. R. & Guardiola. F. (2014). The effect of citric acid and ascorbyl palmitate in palm oil enriched with heme iron: A model for iron fortification in bakery products. Eur J Lipid Sci Tech, 116(3), 300–310. doi: 10.1002/ejlt.201300007. [ Links ]
Almendros. P. Obrador. A. Gonzales. D. & Alvarez. J.M. (2015). Biofortification of zinc in onions (Allium cepa L.) and soil Zn status by the aplication of different organic Zn complexes. Sci Hort, 186, 254–265. doi:10.1016/j.scienta.2015.02.023. [ Links ]
Allen. L. H. (2000). Anemia and iron deficiency: effects on pregnacy outcome. Am J Clin Nutr, 71(5), 1280–1284 [ Links ]
Allen. L.H. & Ahluwalia. N. (1997). Improving iron status throgh diet the application of knowledge concerning dietary iron bioavaibility in human populations. USAID, Estados Unidos. 13–16 p. [ Links ]
ANVISA (Agencia Nacional de Vigilancia Sanitária). (2003). Regulamento Técnico sobre Rotulagem Nutricional de Alimentos Embalados, tornando obrigatória a rotulagem nutricional. Resolução 360. Brasil: ANVISA.11p. [ Links ]
Arredondo. M. Martínez. R. & Nuñez. M. (2006). Inhibition of iron and copper uptake by iron, copper and zinc. Biol Res, 39(1),95–102. [ Links ]
Asamblea Legislativa de la República el Salvador. (1994). Ley de fortificación del azúcar con vitamina A. Decreto 843. El Salvador: Asamblea Legislativa de la República el Salvador.41p. [ Links ]
Ballot. D.E. MacPhail. A.P. Bothwell. T.H. & Mayet. F.G. (1989). Fortification of curry powder with NaFe(111)EDTA in an iron– deficient population: report of a controlled iron– fortification trial. Am J Clin Nutr, 49(1),162–169. [ Links ]
Banuelos. G.S. Arroyo. I. Pickering. I.J. Yang. S.Y. & Freeman. J.L. (2015). Selenium biofortification of broccoli and carrots grown in soil amended with Se– enriched hyperaccumulator Stanleya pinnata. Food Chem, 166(1), 603–608. doi:10.1016/j.foodchem.2014.06.071. [ Links ]
Bashir. K. Nozoye. T. Ishimaru. Y. Nakanishi. H. & Naokoko. N.K. (2013). Exploting new tools for bio–fortification of rice. Biotech Adv, 31(8), 1624–1633. doi:10.1016/j.biotechadv.2013.08.012. [ Links ]
Beyer. P. Al–Babili. S. Ye. X. Lucca. P. Schaub. P. Welsch. R. & Potrykus. I. (2002). Golden rice: introducing the B– carotene biosyntesis pathway into rice endosperm by genetic engineering to defeat vitamin A deficiency. J Nutr, 132(3),506S–510S. [ Links ]
Bigliardi. B. & Glati. F. (2013). Innovation trends in the food industry: the case of functional foods. Trends Food Sci Thech, 31(2), 118–129. doi:10.1016/j.tifs.2013.03.006. [ Links ]
Binaghi. M. Cagnasso. C. Pellegrino. N. Drago. S. González. R. Royaine. P. & Valencia. M. (2011). Disponibilidad potencial in vitro de hierro y zinc en una dieta infantil con pan fortificado con distintas fuentes de hierro o con agregado de promotores de la absorción. Arch Latinoam Nutr, 51(3), 316–322. [ Links ]
Boccio. J. Páez. M. C. Zubillaga. M. Salgueiro. J. Goldman. C. Barrado. D. & Weill. R. (2004). Causas y consecuencias de la deficiencia de hierro sobre la salud humana. Arch Latinoam Nutr, 54(2),165–173. [ Links ]
Boccio. J. & Bressan – Monteiro. J. (2004). Fortificación de alimentos con hierro y zinc: pro y contras desde un punto de vista alimenticio y nutricional. Rev Nutr, 17(1), 71–78. [ Links ]
Boccio. J. Zubillaga. M. Caro. R. Gotelli. C. Gotelli. M. & Weill. R. (1997). New procedure to fortify fluid milk and dairy products with high–bioavailable ferrous sulfate. Nutr Rev, 55(6): 240–246. [ Links ]
Burgi. H. Supersaxo. Z. & Selz. B. (1990). Iodine deficiency diseases in Switzerland one hundred years after Theodor Kocher's survey: a historical review with some new goitre prevalence data. Acta Endocrinol, 123, 577–590. [ Links ]
Christides. T. Wray. D. McBride. R. Fairweather. R. & Sharp. P. (2015). Iron bioavailability from commercially available iron supplements. Eur J Nutr, 54(8), 1345–1352. doi: 10.1007/s00394–014–0815–8.
Codex Alimentarius. (1997). Directrices para el uso de declaraciones nutricionales y saludables. CAC/GL 23–1997. Geneva: Codex Alimentarius. 9p. [ Links ]
Codex Alimentarius. (1993). Directrices sobre etiquetado nutricional. CAC/GL 2–1993. Geneva: Codex Alimentarius. 7p. [ Links ]
CONACYT (Consejo Nacional de Ciencia y Tecnología). (1993). Norma Directrices del Codex Alimentarius sobre etiquetado nutricional. CAC/GL 2–1993. El Salvador: CONACYT. 9p. [ Links ]
Conrad. M. & Umbreit. J. (2000). Iron absorption and transport– an update. Am J Hematol, 64, 287–289. [ Links ]
Cortés. M. Chiralt. A. & Puente. L. (2005). Alimentos funcionales: una historia con mucho presente y futuro. Vitae, 21(1), 5–14. [ Links ]
De Paz. R. & Fernandez Navarro. F. (2005). Manejo, prevención y control del sindrome anémico secundario a deficiencia férrica. Nutr Hosp, 20(5), 264–267. [ Links ]
Denic. S. & Agarwal. M. (2007). Nutritional iron deficiency: an evolutionary perspective. Nutrition, 23(7–8), 603–614. doi:10.1016/j.nut.2007.05.002. [ Links ]
FAO (Food and Agriculture Organization of the United Nations). & WHO(World Health Organization). (2002). Human Vitamin and Mineral Requirements. http://www.fao.org/docrep/004/y2809e/y2809e00.html. 04.03.2015. [ Links ]
Fathi. M. Mozafari. M.R. & Mohebbi. M. (2012). Nanoencapsulation of food ingredients using lipid based delivery systems. Trends Food Sci Tech, 23(1), 13–27. doi:10.1016/j.tifs.2011.08.003. [ Links ]
FDA (United States Food and Drug Administration). (2015). Guidance for Industry Nutrition Labeling of Standard Menu Items in Restaurants and Similar Retail Food Establishments. http://www.fda.gov/downloads/Food/GuidanceRegulation/GuidanceDocumentsRegulatoryInformation/UCM437566.pdf. 04.04.2015. [ Links ]
Foong. L. Imam. M. & Ismail. M. (2015). Iron–Binding Capacity of Defatted Rice Bran Hydrolysate and Bioavailability of Iron in Caco–2 Cells. J Agr Food Chem, 63(41), 9029–9036. doi: 10.1021/acs.jafc.5b03420. [ Links ]
Fresno. G.J. (2013). Las oportunidades para las empresas de Chile e los alimentos funcionales. http://www.agrimundo.cl/?publicacion=las–oportunidades–para–las–empresas–de–chile–en–los–alimentos–funcionales–y–nutraceuticos. 04. 03. 2015. [ Links ]
Forrellat Barrios. M. Gautier du Défaix Gómez. H. & Fernández Delgado. N. (2000). Metabolismo del hierro. Rev. Cubana Hematol Inmunol Hemoter, 16(3), 283–301. [ Links ]
Gaitán. D. Olivares. M. Arredondo. M. & Pizarro. F. (2006). Biodisponibilidad de hierro en humanos. Rev Chil Nutr, 33(2), 142–148. [ Links ]
García–Cascal. M. N. Landaeta. M. Adrianza de Baptista. G. Murillo. C. Rincón. M. Bou Rached. L. Bilbao. A. Anderson. H. García. D. Franquiz. J. Puche. R. García. O. Quintero. Y. & Peña–Rosas. J. P. (2013). Valores de referencia de hierro, yodo, zinc, selenio, cobre, molibdeno, vitamina C, vitamina E, vitamina K, carotenoides y polifenoles para la población venezolana. Arch. Latioam Nutr, 63(4), 338–361. [ Links ]
Gupta.C. Chawla. P. Arora. S. Tomar. S. K. & Singh. A. K. (2015). Iron microencapsulation with blend of gum arabic, maltodextrin and modified starch using modified solvent evaporation method – Milk fortification. Food Hydrocolloid, 43, 622–628. doi:10.1016/j.foodhyd.2014.07.021. [ Links ]
Hertrampf. E. & Cortés. F. (2004). Folic acid fortification of wheat flour: Chile. Nutr Rev, 62(6), S44–S48. [ Links ]
Hurrel. R. (1997). Preventing iron deficiency through food fortification. Nutr. Rev, 55(6), 210–222. [ Links ]
Hurrel. R. & Egli. I. (2010). Iron bioavailability and dietary reference values. Am J Clin Nutr, 91(5), 161–1467. doi: 10.3945/ajcn.2010.28674F. [ Links ]
ICBF (Instituto Colombiano de Bienestar Familiar). (2011). Encuesta Nacional de la Situacion Nutricional en Colombia 2010. http://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/ED/GCFI/Base%20de%20datos%20ENSIN%20–%20Protocolo%20Ensin%202010.pdf. 04.12.2014. [ Links ]
INEN (Instituto Ecuatoriano de Normalización). (2011). Rotulado de productos alimenticios para consumo humano– Parte 1. Norma Técnica Ecuatoriana 1334–2. Ecuador: INEN. 24p. [ Links ]
Joye. I.J. Davidov–Pardo.G. & McClements. J.D. (2014). Nanotechnology for incresed micronutrient bioavailability. Trends food sci Tech, 40(2), 168–182. doi:10.1016/j.tifs.2014.08.006. [ Links ]
Latham. M.C. (2002). Nutrición Humana en el Mundo en Desarrollo. FAO, Roma. 300p. [ Links ]
Layrisse. M. Chaves. J.F. Mendez–Castellano. H. Boscs. V. Tropper. E. Bastardo. B. & González. E. (1996). Early response to the effect of iron fortification in Venezuelan population. Am J Clin Nutr, 64(6), 903–907. [ Links ]
Maldonado Lozano. J. Baró. L. Ramírez–Tortosa. M. C. Gil. F. Linde. J. López–Huertas. E. Boza. J.J. & Gil. A. (2007). Ingesta de una fórmula láctea suplementada con hierro como medida preventiva del déficit de hierro en niños de 1 a 3 años de edad. An Pediatr, 66(6), 591–596. doi:10.1157/13107394. [ Links ]
Masuda. H. Ishimaru. Y. Aung. M.S. Kobayashi. T. Kakei. Y. Takahashi. M. Higuchi. K. Nakanishi. H. & Nichizawa. N.K. (2012). Iron biofortification in rice by the introduction of multiple genes involver in iton nutrition. Sci Rep, 2, 1–6. doi: 10.1038/srep00543. [ Links ]
Ministerio de Salud y Protección Social. (2015). Se establece la clasificación de los alimentos para consumo humano de acuerdo con el risgo en salud pública. Resolución 2674. Bogotá: Ministerio de Salud y Protección Social. 20 p. [ Links ]
Ministerio de la Protección Social. (2011). Reglamento técnico sobre los requisitos de rotulado o etiquetado nutricional que deben cumplir los alimentos envasados para consumo humano. Resolución Número 333. Bogotá: Ministerio de la Protección Social. 56p. [ Links ]
Ministerio de Salud. (2009). Normas técnicas sobre directrices nutricionales que indica, para la declaración propiedades saludables de los alimentos. Resolución Exenta Número 764/09. Santiago de Chile: Ministerio de Salud.10p. [ Links ]
Ministerio de Salud. (1998). Se reglamenta la fortificación de azúcar con vitamina A y se establecen las condiciones de comercialización, rotulado, vigilancia y control. Decreto 1324. Bogotá: Ministerio de Salud. 3p. [ Links ]
Ministerio de Salud. (1996). Se reglamenta la fortificacion de harina de trigo y se establecen las condiciones de comercilizacion, rotulado, vigilancia y control. Decreto 1944. Bogotá: Ministerio de Salud. 22p. [ Links ]
Miranda. M. Olivares. M. Brito. A. & Pizarro. F. (2014). Reducing iron deficiency anemia in Bolivian school children: Calcium and iron combined versus iron supplementation alone. Nutrition, 30(7–8), 771–775. doi:10.1016/j.nut.2013.12.008. [ Links ]
Miret. S. Simpson. R. & McKie. A. (2003). Physiology and molecular biology of dietary iron absorption. Annu Rev Nutr, 23, 283–301. [ Links ]
Moreira Araújo. R. S. Araújo. M. A. & Areas. J. A. (2008). Fortified food made by extrusion of a mixture of chickpea, corn and bovine lung controls iron deficiency anaemia in preschool children. Food Chem, 107(1),158–164. doi:10.1016/j.foodchem.2007.07.074. [ Links ]
Moreira. V. & López San Román. A. (2009). Anemia ferropenica. Tratamiento. Rev Esp Enferm Dig, 101(1), 70–70. [ Links ]
Moreno. C. (2012). Un tema complejo: Normativa y alimentos funcionales. Alimentos Argentinos, 55, 61–63. [ Links ]
Mujica–Coopman. M. F. Brito. A. López de Romaña. D. Pizarro. F. & Olivares. M. (2015). Body mass index, iron absorption and iron status in childbearing age women. J Trace Elem Med Biol, 30, 215–219. doi:10.1016/j.jtemb.2014.03.008. [ Links ]
Muñoz. M. García– Erce. J.A. & Remacha. A.F. (2011). Disorders of iron metabolism. Part 1: molecular basis of iron homeostasis. J Clin Pathol, 64, 281–286. doi: 10.1136/jcp.2010.079046. [ Links ]
Muzzo. B. (2004). Fortificación de harina de trigo en América Latina y Región del Caribe. Rev Chil Nutr, 31(3), 336–347. [ Links ]
Nadadur. S.S. Srirama. K. & Mudipalli. A. (2008). Iron transport & homeostasis mechanisms: their role in health & disease. Indian J Med Res, 128, 533–534. [ Links ]
Nogueira de Almeida. C. A. Crottr. G. C. Ricco. R. G. Del Ciampo. L. A. Dutra de Oliveira. J. E. & Cantolini. A. (2003). Control of iron deficiency anaemia in Brazilian preschool children usin iron fortified orange juice. Nutr Res 123(1), 27–33. doi:10.1016/S0271–5317(02)00487–6. [ Links ]
Olivares. M. Pizarro. F. Gaitán. D. & Ruz. M. (2007). Acute inhibition of iron absorption by zinc. Nutr Res, 27(5), 279–282. doi:10.1016/j.nutres.2007.04.006. [ Links ]
Ostos. S.L. Díaz. A.C. & Suarez. M. (2012). Evaluación de diferentes condiciones de proceso en la fortificación de mango (Tommy Atkins) con calcio mediante impregnación al vacio. Rev Chil Nutr, 39(2),181–190. [ Links ]
Pizarro. F. Olivares. M. Maciero. E. Krasnoff. G. Cócaro. N. & Gaitán. D. (2015). Iron absorption from two milk formulas fortified with iron sulfate stabilized with maltodextrin and citric acid. Nutrients, 7(11), 8952–8959. doi: 10.3390/nu7115448. [ Links ]
Pizarro. F. Olivares. M. Valenzuela. C. Britto. A. Weinborn. V. Flores. S. & Arredondo. M. (2016). The effect of proteins from animal source foods on heme iron bioavailability in humans. Food Chem, 196(1), 733–738. doi:10.1016/j.foodchem.2015.10.012. [ Links ]
Prescha. A. Biernat. J. Weber. R. Zuk. M. & Szopa. J. (2003). The influence of modified 14–3–3 protein synthesis in potato plants on the nutritional value of the tubers. Food Chem, 82(4), 611–617. doi:10.1016/S0308–8146(03)00018–9. [ Links ]
Restrepo. A.M. Cortés. M. & Rojano. B.A. (2010). Potencialización de la capacidad antioxidante de la fresa (Fragaria ananassa Duch.) por la incorporación de vitamina E utilizando la técnica de impregnación al vacio. Vitae, 17(2),135–140. [ Links ]
Ribaya Mercado. J.D. Solomons. N.W. Medrano. Y. Bulux. J. Dolnikowski. G.G. Russell. R.M. & Wallace. C.B. (2004). Use of the deuterated–retinol–dilution technique to monitor the vitamin A status of Nicaraguan schoolchildren 1 y after initiation of the Nicaraguan national program of sugar fortification with vitamin A. Am J Clin Nutr, 80(5), 1291–1298. [ Links ]
Rojas. M. L. Sánchez. J. Villada. O. Montoya. L. Díaz. A. Vargas. C. Chica. J. & Herrera. A. (2013). Eficacia del hierro amino–quelado en comparación con el sulfato ferroso como fortificante de un complemento alimentario en preescolares con deficiencia de hierro, Medellín, 2011. Biomédica, 33(3), 350–360. doi: 10.7705/biomedica.v33i3.775. [ Links ]
SCENIHR (Scientific Committee on Emerging and Newly Identified Health Risks). (2006). The appropriateness of existing methodologies to assess the potential risks associated with engineered and adventitious products of nanothechnologies. http://ec.europa.eu/health/ph_risk/committees/04_scenihr/docs/scenihr_o_003b.pdf. 04.04.2015. [ Links ]
Scopus. (2015a). Analyze search results "food fortification". http://www.scopus.com/term/analyzer.url?sid=856285D4A7F9E138C2AA122CFC02A8FF.FZg2ODcJC9ArCe8WOZPvA%3a690&origin=resultslist&src=s&s=TITLE–ABS–KEY%28food+fortification%29&sort=plf–f&st=b&sot=b&sl=33&count=4139&analyzeResults=Analyze+results&txGid=856285D4A7F9E138C2AA122CFC02A8FF.FZg2ODcJC9ArCe8WOZPvA%3a75. 04.04.2015. [ Links ]
Scopus. (2015b). Analyze search results "iron fortification". http://www.scopus.com/term/analyzer.url?sid=6677EFD1906471AC54F8280520DE771B.fM4vPBipdL1BpirDq5Cw%3a20&origin=resultslist&src=s&s=TITLE–ABS–KEY%28iron+fortification+%29&sort=plf–f&st=b&sot=b&sl=34&count=1579&analyzeResults=Analyze+results&txGid=6677EFD1906471AC54F8280520DE771B.fM4vPBipdL1BpirDq5Cw%3a7. 04.04.2015. [ Links ]
Scopus. (2015c). Analyze search results "iron bioavailability". http://www.scopus.com/term/analyzer.url?sid=6677EFD1906471AC54F8280520DE771B.fM4vPBipdL1BpirDq5Cw%3a20&origin=resultslist&src=s&s=TITLE–ABS–KEY%28iron+bioavailability+%29&sort=plf–f&st=b&sot=b&sl=36&count=5449&analyzeResults=Analyze+results&txGid=6677EFD1906471AC54F8280520DE771B.fM4vPBipdL1BpirDq5Cw%3a13. 04.04.2015. [ Links ]
Secretaria de Economía. (2010). Especificaciones generales de etiquetado para alimentos y bebidas no alcohólicas preenvasados. Norma oficial Mexicana NOM–051–SCFI/SAA1–2010. México: Secretaria de Economía. 18p. [ Links ]
Secretaría de Políticas, Regulación e Institutos & Secretaría de Agricultura, Ganaderia Pesca y Alimentos. (2008). Modificación del Código Alimentario Argentino. Resolución Conjunta 118/2008 y 474/2008.Argentina: Secretaría de Políticas, Regulación e Institutos & Secretaría de Agricultura, Ganaderia Pesca y Alimentos. 64p. [ Links ]
Soyano. A. & Gómez. M. (1999). Participación del hierro en la inmunidad y su relación con las infecciones. Arch Latinoam Nutr, 40(3), 40–46. [ Links ]
Suárez. H. Cimino. F. & Bonilla. E. (1985). Hierro en el sistema nervioso central: metabolismo y consideraciones fisiopatológicas. Invest Clin, 26, 247–322. [ Links ]
Thuy. P.V. Berger. J. Davidsson. L. Khan. N.C. Lam. N.T. Cook. J.D. Hurrell. R.F. & Khoi. H.H. (2003). Regular consumption of NaFeEDTA– fortified fish sauce improves iron status and reduces the prevalence of anemia in anemic Vietnamese women. Am J Clin Nutr, 78(2), 284– 290. [ Links ]
Toxqui. L. De Piero. A. Courtois. V. Bastida. S. Sánchez– Muniz. F.J. & Vaquero. P. (2010). Deficiencia y sobrecarga de hierro; implicaciones en el estado oxidativo y la salud cardiovascular. Nutr Hosp, 25(3), 350–365. [ Links ]
Trinidad. T.P. Kurilich. A.C. Mallillin. A.C. Walcyzk. T. Sagum. R.S. Singh. N.N. Harjani. Y. de Leon. M.P. Capanzana. M.V. & Fletcher. J. (2014). Iron absorption from NaFeEDTA– fortified oat beverages with or without added vitamin C. Int J Food Sci Nutr, 65(1), 124–128. doi: 10.3109/09637486.2013.836739. [ Links ]
Weinborn. V. Pizarro. F. Olivares. M. Brito. A. Arredondo. M. Flores. S. & Valenzuela. C. (2015). The effect of plant proteins derived from cereals and legumes on heme iron absorption. Nutrients, 7(11), 8977–8986. doi: 10.3390/nu7115446. [ Links ]
WHO (World Health Organization). (2006). Guidelines on food fortification with micronutrients. http://whqlibdoc.who.int/publications/2006/9241594012_eng.pdf?ua=1.04.04.2015. [ Links ]
WHO (World Health Organization). (2008). Worldwide pevalence of anaemia 1993– 2005: WHO global database of anaemia. http://whqlibdoc.who.int/publications/2008/9789241596657_eng.pdf. 04.04.2015. [ Links ]