Introducción
El cadmio (Cd) es reconocido como un factor de riesgo para la salud humana por los daños que ocasiona en diferentes órganos y en el sistema óseo (Zia-ur-Rehman et al., 2015), siendo el consumo de alimentos una de las formas frecuentes de contaminación para los humanos. Por su importancia tóxica, la Organización Mundial de la Salud (OMS) ha establecido como nivel máximo de tolerancia al cadmio en el cuerpo, la cantidad de 7 ^g/kg de peso corporal (Roberts, 2014). Este elemento es incorporado en el suelo en forma natural o por acciones antropogénicas, combustibles fósiles, residuos de minería, lodos de depuradores y aplicación de fertilizantes fosfatados (Guo et al., 2010).
El cacao producido en Latinoamérica tiene una alta demanda a nivel mundial para la elaboración de confitería o chocolates finos. En Colombia, es producido por pequeños agricultores, cuyas unidades productivas son de 3.3 ha, en promedio. En 2016 la producción fue estimada en 56,785 t de grano. La Organización Mundial del Cacao (ICCO) restringen las exportaciones cuando la concentración de Cd en granos supera el valor crítico de 0.6 mg/kg.
El proceso de fitoextracción es seguro y amigable con el ambiente, ya que permite extraer metales pesados como el cadmio (Ramírez et al., 2017). Este sistema es un componente promisorio en la rehabilitación de suelos contaminados, siendo su función principal extraer de forma segura un elemento tóxico por medio de varios procesos como la absorción, transporte, translocación y acumulación (Saad-Allah y Elhaak, 2015; Mahar et al., 2016).
La hiperacumulación hace referencia a la capacidad de los organismos vivos para capturar y almacenar elementos pesados en altas concentraciones. Esta habilidad le confiere a las plantas, con alta capacidad de translocación y alto coeficiente de acumulación, tolerancia a dichos metales (Sun et al., 2008; Wei et al., 2010). Wei et al. (2005) clasifican a S. nigrum L. dentro de las plantas hiperacumuladoras de cadmio, ya que con altas aplicaciones de Cd (25 mg/kg) encontraron concentraciones en tallos de 103.8 mg/kg y en hojas de 124.6 mg/kg, siendo éstas más altas que la encontradas en el suelo. El presente estudio tuvo como objetivo evaluar estrategias para la rehabilitación de suelos con altos contenidos de cadmio, entre ellas, el cultivo de hierba mora (Solanum nigrum L.) como especie fitoextractora en suelo con diferentes concentraciones de este metal.
Materiales y métodos
El ensayo se realizó en invernadero en la Universidad Nacional de Colombia, Sede Medellín (6° 15’ 44’’ N 75° 34’ 37’’ W), a 1526 m.s.n.m. con una temperatura, promedio anual, de 23 °C, 1397 mm de precipitación, humedad relativa de 66%, en la zona de vida bosque húmedo premontano (bh-PM/T-h) (Holdridge, 1966).
Las semillas de Solanun nigrum L. utilizadas fueron recolectadas dentro del campus de la Universidad Nacional Sede Medellín. Antes de la siembra fueron tratadas con ácido giberélico y germinadas en bandejas para ser trasplantadas a macetas de 1 kg de capacidad. El suelo era Inceptisol proveniente de una finca productora de cacao ubicada a N 7° 39' 2,5’’ W 76° 41’ 58’’, en la vereda Champitas, Chigorodó, Antioquia. A una altura de 40 m.s.n.m., 21.3-36.4 °C, 2747 mm de precipitación y humedad relativa de 83%.
Para el experimento de fitoextracción de cadmio, se evaluaron tres tratamientos correspondientes en concentraciones de Cd (mg/kg) de: 0 (T1), 5 (T2) y 10 (T3). Las unidades experimentales consistieron en las macetas que fueron dispuestas en un diseño completamente aleatorizado con cinco repeticiones por tratamiento.
Al momento de la cosecha (9 semanas después de la siembra), las plantas se encontraban en estado vegetativo. Para medir la biomasa se separaron la parte aérea (hojas y tallo) de las raíces, que fueron secadas por 3 días en horno (modelo 600, Memmert GmbH) hasta alcanzar un peso constante, que fue medido en una balanza analítica Explorer-pro. El área foliar se midió en el equipo LI-3100 AREA METER. Para medir la concentración de cadmio en la planta se hizo una adaptación a la norma NTC 5752 y GTC 189. Para el suelo se utilizó una adaptación a la norma ISO 11466 e ISO 11047. Para la digestión de las plantas y el suelo, se pesaron 0.5 y 0.1 g, respectivamente, y se colocaron en tubos de teflón, se agregó 4 ml de H2O2 al 30%, 4 ml de agua desionizada y 2 ml de HNO3 al 65%. Para la digestión se utilizaron microondas a 180°C por 1:30 h. Finalizada ésta, se agregaron dos gotas de fenolftaleína y naranja de metilo como indicadores de pH, se ajustó el pH por medio del equipo HandyLab 680 marca SI analytcs, agregando NaOH y HNO3. Las lecturas de cadmio absorbido se realizaron con un electrodo de Ion selectivo de Cd HI4104, marca Hanna Instruments. Equipo lector multipropósito HI98191, marca Hanna Instruments.
Lasmediciones de variables morfológicas se hicieron cada 15 días. La altura de planta se midió desde el nivel del suelo hasta el ápice del tallo. Se contó el número de hojas verdaderas y el número de entrenudos. El área foliar se midió con LI-3100 Area Meter.
Resultados
Las plantas de hierba mora (S. nigrum L) germinaron después de 4 días de sembradas y transcurridas 9 semanas, se observó un incremento por planta en el número de hojas (13) y entrenudos (11), en longitud del tallo (11.3 cm) y de raíz (13.1 cm) (Figura 1).
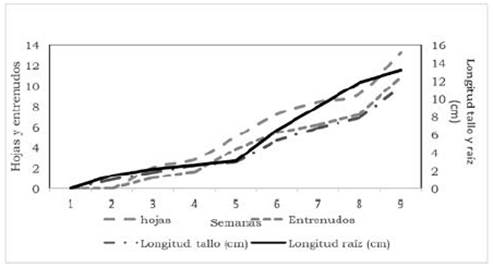
Figura 1 Promedios de crecimiento de Solanum nigrum L.: hojas, entrenudos, longitud del tallo y de raíz, durante las fases germinación y desarrollo.
Cuando las plantas recibieron las aplicaciones de cadmio presentaron una biomasa acumulada más alta (P < 0,05), incrementando su contenido a medida que se aumentó la concentración de Cd en el suelo (Figura 2a).
El área foliar fue mayor (P < 0.05) con el incremento de la concentración de cadmio en el suelo, con valores de 0.062, 0.095, 0.102 m2 para los T1, T2 y T3, respectivamente (Figura 2b).
La acumulación de cadmio en los distintos tejidos de la planta aumentó (P < 0.05) al aumentar la concentración de cadmio aplicada, esto muestra que la planta de hierba mora tiene la capacidad de extraer y acumular este elemento presente en el suelo sin afectar sus funciones (Figura 2c).
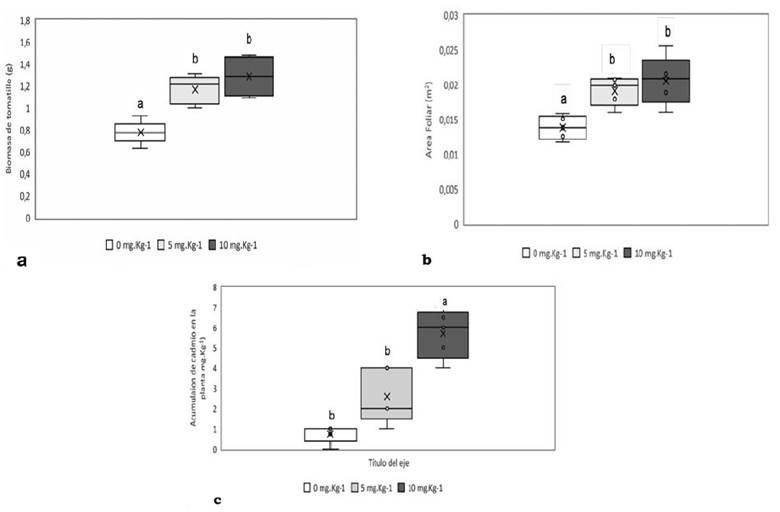
Figura 2. (a) Biomasa acumulada. (b) área foliar. (c) Cadmio acumulado en plantas de Solanum nigrum L. con aplicaciones de 0, 5, 10 y 10 mg/kg de cadmio. Letras distintas indican diferencias significativas de medias de tratamientos (P < 0.05).
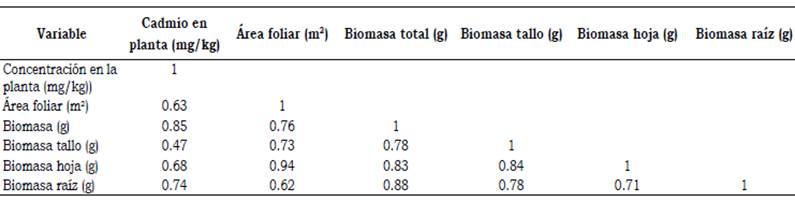
Las longitudes del tallo y la raíz presentaron una correlación lineal. La relación tallo: raíz al comienzo fue de 1.27 y a los 35 días de 0.96. Esta relación durante el crecimiento de la planta fue aproximadamente de 1, lo que significa un equilibrio entre la parte aérea y la raíz, que puede incidir en el área de exploración y absorción de cadmio por la planta. Se observó que al aumentar la cantidad de cadmio extraído por la planta incrementaron el área foliar (R2 = 0.63) y la biomasa de la planta (R2 = 0.63), tanto en raíces como en tallos y hojas de manera significativa (Tabla 1).
Discusión
Las plantas de S. nigrum durante el periodo experimental desarrollaron 3 hojas y una longitud de tallo entre 2 y 4 cm lo que coincide con los hallazgos de Sun et al. (2008) en condiciones de campo. Wei et al. (2006) encontraron que la duración del ciclo de vida de S. nigrum L. bajo condiciones de temperaturas cálidas (24°C y 700 mm/año) es variable entre 35 y 60 días.
La presencia de cadmio en el suelo estimula la acumulación de biomasa de S. nigrum, respuesta que puede atribuirse al efecto de este elemento sobre el crecimiento en la especie. No obstante es conocido que este metal en otras plantas inhibe el desarrollo, debido a la reacción en contra del oxígeno que bloquea la acumulación y transporte del NO3 - y disminuye la absorción de nutrientes (Fodor et al., 1995; Krantev et al., 2008).
El incremento de biomasa en Sorghum bicolor por efecto del cadmio fue demostrado por Pinto et al. (2004), quienes al aplicar en el suelo 1 mg/kg de este elemento encontraron aumentos significativos de la materia seca acumulada lo que atribuyeron al aumento en, la apertura estomática, el intercambio de gases, el metabolismo de los aminoácidos y la presencia de lignina en la biomasa de la raíz. Resultados similares encontraron Aibibu et al. (2010) en el pasto vetiver (Vetiveria zizanioides),
El incremento de cadmio en la biomasa por efecto de la mayor concentración de éste en el suelo es consistente con los hallazgos de Sun et al. (2008) en la misma especie evaluada en el presente trabajo, y con los de Jiang et al. (2001) en ajo y pasto guinea.
Las concentraciones de cadmio en S. nigrum fueron menores que las encontradas por Dahmani-Muller et al. (2000) para especies hiperacumuladoras (100 mg/kg). Las diferencias se deben al estado de desarrollo en que se encontraban las plantas al momento de las mediciones. Según Wei et al. (2006) la acumulación de cadmio en S. nigrum es más alta entre el estado de floración y la madurez de la planta cuando puede absorber hasta 85% del total.
En la etapa de floración se presenta una serie de comportamientos metabólicos, que indirectamente conllevan a la absorción, transporte y acumulación de cadmio. Liphadzi y Kirkham (2005) e Irfan et al. (2013) consideran que la acción fuente-sumidero contribuye a una alta actividad de translocación de nutrientes, en la cual intervienen componentes de función transportadora, incluyendo componentes como los canales y proteínas transportadoras no específicas, que pertenecen a los grupos IR y ZIP; canales como ZIPs, Nramps, LCT1, y Ca^ que permiten la absorción de cadmio hacia el citoplasma. Para Sheoran et al. (2016) la absorción de metales es afectada por su disponibilidad en el suelo, siendo esta última menor en suelos arcillosos y franco arcillosos que en suelos arenosos, donde hay menos densidad de cargas.
Conclusión
Se encontró alta correlación entre los contenidos de cadmio en el suelo y su acumulación en los tejidos de S. nigrum L. La mayor presencia de cadmio en el suelo favoreció el crecimiento de esta planta, incrementando el área foliar (r2 = 0.63) y la producción de hojas (r2 = 0.68), la biomasa de la planta (r2 = 0.63) y la biomasa tanto en raíz (r2 =0.74) como en tallo (r2 = 0.47).
Solanum nigrum es una especie con potencial para co-ayudar en la reducción de niveles nocivos de cadmio en suelos cultivados con cacao.