Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Colombian Journal of Anestesiology
versão impressa ISSN 0120-3347
Rev. colomb. anestesiol. v.33 n.1 Bogotá jan./mar. 2005
GUÍAS DE PRÁCTICA CLÍNICA - REUNIÓN DE CONCENSO
Terapia de fluidos en pacientes adultos críticamente enfermos
Rafael Mora, MD1, Alvaro Ruiz, MD2, Abraham Alí, MD3, Oswaldo Borraez, MD,4, José N. Carreño, MD5, Edgar Celis, MD6, Luis E. Cruz, MD7, Germán Gamarra, MD8, Alberto García, MD9, Marcela Granados, MD.10, Francisco Holguín, MD11, Jorge Mejía, MD12, Carlos Morales, MD13, Jesús Muñoz, MD14, Henry Oliveros, MD15, Guillermo Ruiz, MD16, Mauricio Sanabria, MD17, Ricardo Uribe, MD18, Juan P. Velásquez, MD19
1 Departamento de Cirugía, Coordinación de Postgrado, Facultad de Medicina, Universidad San Martín, Bogotá
2 Departamento de Medicina Interna, Unidad de Epidemiología Clínica y Bioestadística, Facultad de Medicina, Universidad Javeriana, Bogotá
3 Departamento de Medicina Interna, Unidad de Neumología, Fundación Cardioinfantil, Bogotá
4 Departamento de Cirugía , Hospital San Blas, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá
5 Departamento de Investigación Clínica , E. Lilly Company, Lima, Perú
6 Departamento de Medicina Crítica, Coordinación de la Unidad de Cuidados Intensivos, Clínica Fundación Santafé de Bogotá
7 Departamento de Fisiología, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá
8 Departamento de Medicina Interna, Unidad de Nefrología, Facultad de Medicina, Universidad Industrial de Santander, Bucaramanga
9 Departamento de Cirugía, Hospital Universitario del Valle, Facultad de Medicina, Universidad del Valle, Cali
10 Departamento de Medicina Crítica, Coordinación de la Unidad de Cuidados Intensivos, Clínica Fundación Valle de Lili, Cali
11 Departamento de Cirugía, Clínica Medihelp Services, Cartagena
12 Departamento de Cirugía, Coordinación de Anestesiología, Clínica Fundación Valle de Lili, Cali
13 Departamento de Cirugía, Hospital Universitario San Vicente de Paúl, Facultad de Medicina, Universidad de Antioquia, Medellín
14 Unidad de Nefrología, R.T.S. Ltda., Agencia Cardioinfantil,Bogotá
15 Departamento de Medicina Crítica, Hospital Militar Central, Hospital Universitario Clinica San Rafael, Facultad de Medicina, Universidad Militar Nueva Granada, Bogotá.
16 Departamento de Medicina Crítica, Coordinación de la Unidad de Cuidados Intensivos, Clínica San Pedro Claver, Bogotá
17 Unidad de Nefrología, R:T.S. Ltda.., Agencia Cardioinfantil, Bogotá
18 Departamento de Urgencias, Coordinación de Urgencias, Hospital Militar Central, Facultad de Medicina, Universidad Militar Nueva Granada, Bogotá
19 Departamento de Medicina Crítica, Coordinación de la Unidad de Cuidados Intensivos, Hospital Militar Central, Facultad de Medicina, Universidad Militar Nueva Granada, Bogotá
RESUMEN
La terapia de fluidos en el paciente críticamente enfermo ha venido experimentando una serie de cambios que buscan optimizar este manejo, varios de los cuales han sido motivo de controversia. Dentro de éstos se seleccionaron los siguientes tópicos para ser discutidos en la Reunión de Consenso, los cuales originaron estas Guías de Práctica Clínica: cristaloides versus coloides en el paciente crítico; uso de albúmina humana en resucitación; hipoalbuminemia y plasmaféresis; resucitación con fluidos y el desarrollo del síndrome de dificultad respiratoria aguda; fluidos en resucitación de pacientes con trauma craneoencefálico; acidosis metabólica como índice de resucitación insuficiente en el paciente crítico; accesos venosos en resucitación; utilidad de los signos clínicos en el diagnóstico y manejo del choque hipovolémico.
Los expertos participantes representan 10 disciplinas médicas relacionadas con este campo de la medicina crítica y una amplia diversidad de hospitales y facultades de medicina.
Palabras Claves:Fluidoterapia, choque, resucitación (Fuente: DeCS, BIREME).
SUMMARY
Fluid therapy in the critically ill patients has experienced a sequence of changes, looking for the optimization in the management. Some of those changes have provoked controversy. The next controversial topics has been selected to be discussed in a consensus conference, in order to produce the present Guidelines of Clinical Practice: colloids vs crystalloids in the critically ill patient; the use of human albumin in resuscitation; hypoalbuminemia and plasmapheresis; fluid resuscitation and the development of acute respiratory distress syndrome; fluid resuscitation in head injury; metabolic acidosis as a sign of insuficient resuscitation in the critically ill; venous access in resuscitation; utility of the clinical signs in the diagnosis and management of hypovolemic shock.
The experts participants represent 10 medical specialties involved in the area of critical medicine, as well as different hospitals and medicine faculties.
Key words:Fluid therapy, shock, resuscitation (Source: MeSH, NLM)
MÉTODOS
Los pasos para el establecimiento de las Guías de Práctica Clínica, producto del consenso de expertos fueron los siguientes:
1. Definición del tema, se hizo una evaluación del tema y una selección de las preguntas prioritarias, con base en el análisis hecho a través de cuestionarios estructurados que fueron respondidos por médicos a cargo de Unidades de Cuidado Intensivo en instituciones de atención terciaria.
2. Selección de un panel de expertos, a cada uno de sus integrantes se le asignó un tema en particular que fue revisado de manera exhaustiva y crítica y del cual se hizo un resumen final, a manera de revisión sistemática de la literatura, con recomendaciones finales.
3. Selección de un segundo grupo de expertos,; a cada uno de los cuales se le asignó el mismo tema que a un par del panel y cuyo papel fué actuar como evaluadores críticos de la revisión y de las recomendaciones en el área asignada.
4. Reunión final de consenso, en la cual cada experto presentó las recomendaciones, que fueron luego revisadas por el grupo de evaluadores y por el grupo general. La reunión se llevó a cabo en la ciudad de Bogotá el día 25 de septiembre de 2004.
5. Definición de las recomendaciones con base en la mejor evidencia disponible y por consenso.
6. Escritura del tema final, con revisión por cada uno de los participantes.
7. La revisión final fue actualizada hasta el 1 de enero de 2005.
Calificación de la información y graduación de las recomendaciones
Se utilizó la propuesta del GRADE Working Group
(1) que incluye los siguientes pasos:1. Calidad de la Información para cada resultado
2. Importancia relativa de los resultados
3. Calidad global de la información
4. Balance de los beneficios y daños
5. Balance de los beneficios netos y de los costos
6. Fortaleza de la recomendación
7. Implementación y evaluación
Para la evaluación de la Calidad de la Información (Evidencia) se utilizó la clasificación siguiente, específica para calificación de intervenciones:
Calidad de la Información disponible según la fuente de origen
a. Alta:Experimentos clínicos aleatorizados o metaanálisis
b. Baja:Estudios observacionales
c. Muy Baja:Cualquier otro origen
Para las recomendaciones finales, se escogió la propuesta del mismo grupo GRADE, que busca ser práctico y simple. Las recomendaciones en relación con la conducta que se debe tomar son:
1. "Hágalo.". En este caso, la información es suficiente para una recomendación formal, hay evidencia que sustenta la decisión y puede recomendarse con solidez. En la mayoría de los casos habrá metaanálisis o experimentos clínicos aleatorizados de alta calidad, sin defectos metodológicos ni fallas en análisis, así como con buena generalizabilidad.
2. "Probablemente hágalo". La información es bastante clara en apoyar la recomendación pero no es suficientemente sólida como para ser indiscutible. Puede haber defectos metodológicos menores en los estudios que apoyan el concepto, o no haber suficientes estudios, o haber información conflictiva. Puede haber también buena validez interna de los estudios (calidad apropiada) pero no suficiente información para garantizar la validez externa (generalizabilidad) por faltar, por ejemplo, estudios locales (cuando sean pertinentes) o en condiciones particulares.
3. "Probablemente no lo haga". Se trata de información que apunta claramente a una contraindicación, aunque falta solidez, bien por falta de estudios, por estudios conflictivos o por defectos metodológicos en los estudios. Sin embargo, el conjunto global de información hace más probable que se trate de una intervención que deba evitarse.
4. "No lo haga". Hay evidencia que apoya esta recomendación. La información es clara, coherente, sólida y justifica una contraindicación para la acción.
TEMAS Y RECOMENDACIONES
Se seleccionaron los siguientes temas:
- Cristaloides versus coloides en el paciente crítico
- Uso de albúmina humana en resucitación, hipoalbuminemia y plasmaféresis
- Resucitación con fluidos y el desarrollo del síndrome de dificultad respiratoria aguda.
- Fluidos en resucitación de pacientes con trauma craneoencefálico
- Acidosis metabólica como índice de resucitación insuficiente en el paciente crítico
- Accesos venosos en resucitación
- Utilidad de los signos clínicos en el diagnóstico y manejo del choque hipovolémico
CRISTALOIDES VERSUS COLOIDES EN EL PACIENTE CRÍTICO
Pregunta: Cuál es la indicación actual en el uso de cristaloides y coloides en pacientes críticamente enfermos?
Recomendación.
Se recomienda el empleo de cristaloides isotónicos en la resucitación con fluidos de los pacientes críticamente enfermos.
Evidencia : Alta Categoría de la recomendación : Hágalo
Resumen de la evidencia clínica
1- Los estudios clínicos revisados no demuestran diferencias significativas en la mortalidad de los pacientes críticamente enfermos por razón del uso de soluciones cristaloides versus coloides empleados en la resucitación.
La solución de albúmina, en particular, tampoco ofrece diferencias en mortalidad
2- Hay evidencia que sugiere ventaja de los cristaloides sobre los coloides en la resucitación de pacientes con trauma.
3- Al evaluar otros desenlaces menores en pacientes agudamente enfermos, hay evidencia que sugiere ventaja de la albúmina sobre los cristaloides.
4- Dadas las diferencias significativas en costo y la escasa evidencia en relación con diferencias en efectividad, la recomendación global de uso debe ser la de los cristaloides isotónicos.
Soporte de la recomendación
Contexto
Los cristaloides y los coloides, isotónicos e hipertónicos, son soluciones empleadas en la expansión del compartimento extracelular del organismo. Si son hipotónicos, también en la expansión del compartimiento intracelular.
Expansión del volumen vascular
La primera diferencia postulada entre cristaloides y coloides, es que estos últimos por contener moléculas de gran tamaño: albúmina, hidroxietilalmidón, gelatina, dextrano, etc., que se quedan en el espacio vascular al menos temporalmente, incrementan la presión oncótica de este espacio y aumentan su volumen más efectivamente y con una menor cantidad que los cristaloides.
Bajo condiciones ideales, de un litro de cristaloide isotónico infundido, 250 cc se quedan en el espacio vascular y 750 cc ocupan el espacio intersticial .
Clínicamente, 100-200ml de 1 litro de cristaloides isotónicos infundidos al espacio vascular, se quedan en éste2.
Después de la administración de 1 litro de solución de albúmina al 5% (isotónica), la expansión del volumen plasmático es de 500 a 1000ml (2), es decir, la mitad del volumen o más se quedan en el espacio vascular.
Si se infunde una solución de albúmina al 25% (hipertónica) se produce movilización del volumen extravascular (intersticial) hacia el vascular, de modo que la infusión de 100ml de albúmina al 25% puede producir un incremento de hasta 500 ml del volumen intravascular, después de 1 hora de la infusión2.
Una solución de 1 litro de hidroxietilalmidón al 6% en solución salina normal, con una presión oncótica de aproximadamente 30 mOsm/L, expande el volumen vascular entre 700 a 1000ml, persistiendo hasta el 40% de esta expansión vascular por 24 horas3.
En la práctica clínica lo que se ha encontrado es que cuando los cristaloides y los coloides son administrados para lograr las mismas presiones de llenado vascular, ambas clases de soluciones son igualmente efectivas en restaurar la perfusión tisular4.
La resucitación con soluciones isotónicas de cristaloides requerirán de 2 a 4 veces más volumen que los coloides y ligeramente más largos períodos para alcanzar las metas hemodinámicas5.
Edema tisular
La segunda ventaja teórica atribuida a los coloides sobre los cristaloides es el menor edema tisular.
En la formación del edema intervienen todos los factores que determinan el flujo de fluidos a través de la membrana capilar integrados en la Ecuación de Starling Figura 1 y que incluyen la presión hidrostática capilar e intersticial; la presión oncótica capilar e intersticial y la permeabilidad capilar.

En los pacientes críticamente enfermos todos los factores pueden estar alterados, en particular la permeabilidad capilar que está aumentada permitiendo el paso de moléculas de gran tamaño al intersticio, contrarrestando la osmolaridad efectiva que estas moléculas ejercen en condiciones normales en el espacio vascular y que evitan el edema intersticial o acúmulo aumentado del líquido en el espacio intersticial.
El edema es particularmente deletéreo en el pulmón, donde facilita el colapso alveolar y la oxigenación de la sangre se ve comprometida.
Algunos estudios, incluyendo una variedad de modelos de permeabilidad capilar incrementada, así como estudios clínicos en pacientes con choque séptico y síndrome de dificultad respiratoria aguda, no han encontrado evidencia de aumento del agua pulmonar o compromiso de la función pulmonar con coloides4-8.
Adicionalmente, el mantenimiento de presiones hidrostáticas capilares bajas, en modelos sépticos, evita el edema pulmonar sin importar que se empleen cristaloides o coloides9.
El edema sistémico en una complicación frecuente de la resucitación con fluidos.
El edema tisular puede reducir teóricamente la tensión de oxígeno al aumentar la distancia para la difusión de oxígeno a la célula.
Estudios experimentales9,10 han evaluado este efecto, al administrar grandes volúmenes de cristaloides en animales sépticos, sin que se encuentre impedimento en el metabolismo oxidativo a pesar del edema.
Otras tres condiciones deben ser adicionalmente analizadas en la evaluación del uso de cristaloides y coloides. La primera se refiere a los efectos adversos de sus componentes, la segunda al costo monetario y la tercera, la patología para la cual se están usando los cristaloides o los coloides.
Reacciones adversas
Existen reportes11,12 que sugieren que las moléculas de hidroxietilalmidón pueden afectar adversamente la función renal al causar lesión tubular. Esta molécula puede causar disminución en la actividad del factor VIII, con prolongación del tiempo de tromboplastina y aumento potencial del sangrado en pacientes quirúrgicos13.
La infusión de albúmina puede conducir a una reducción del calcio ionizado que se fija a la albúmina, lo que podrá ocasionar un trastorno de la contractilidad de la célula miocárdica, que puede llevar a una descompensación cardíaca al sumarse a la sobrecarga del volumen que la albúmina produce sobre el espacio vascular (14). Igualmente la albúmina puede ejercer efectos hipocoagulantes importantes al inhibir la agregación plaquetaria y acrecentar la inhibición del factor Xa por antitrombina III15.
Por otra parte, la administración de grandes cantidades de solución salina normal (0.9%) produce acidosis metabólica16.
Costos
Las soluciones coloides son mucho más costosas que los cristaloides. Las soluciones de albúmina cuestan el doble que las de hidroxietilalmidón y 30 veces más que la solución salina y el lactato de ringer5,19.
La tercera condición que debe ser analizada son las características fisiopatologícas de las entidades clínicas para las cuales está propuesto el uso de estas soluciones.
En efecto, el término "pacientes críticamente enfermos" abarca un sin número de condiciones clínicas, cada una con características diferentes, que no permiten agruparlas para comparar los resultados del uso de estas soluciones17,18.
Las revisiones sistemáticas de la literatura clínicamente relevante o metanálisis, han producido resultados conflictivos con respecto a mortalidad, cuando se comparan los grupos tratados con coloides versus cristaloides, probablemente por esta falla en categorizar los subgrupos de pacientes críticamente enfermos y no tener además en cuenta la multiplicidad de variables que afectan a estos estudios18.
Por otra parte debe tenerse en cuenta que los desenlaces fisiológicos intermedios no siempre se relacionan con la mortalidad.
Estudios clínicos
En 1998 el Cochrane Injuries Group Albumin Reviewers14 publicó un metanálisis comparando la mortalidad de pacientes críticamente enfermos que recibieron soluciones de albúmina o fracción protéica del plasma versus soluciones cristaloides.
El mismo grupo hizo una revisión del estudio inicial en el año 200319 con resultados similares. En esta revisión los hallazgos incluyeron 31 estudios aleatorizados con 1519 pacientes críticamente enfermos subdivididos en tres grupos: hipovolemia, quemaduras e hipoalbuminemia.
Los resultados globales muestran que el riesgo relativo de morir en el grupo tratado con albúmina en comparación con el de cristaloides fue de 1.52 (95%. Intervalo de confianza 1.17- 1.99) es decir, el grupo tratado con albúmina tuvo una mortalidad más alta que el tratado con cristaloides (14% VS 9%).
El mismo grupo evaluó en un metanálisis los efectos sobre la mortalidad del empleo de los coloides diferentes a albúmina versus cristaloides, en la resucitación de pacientes críticamente enfermos20 sin que se encontrara diferencia estadísticamente significativa entre las dos terapias. (2243 pacientes en 27 estudios)
Una comparación entre los diversos coloides entre sí en resucitación de pacientes críticamente enfermos no demostró diferencias estadísticamente significativas en mortalidad entre ellos, en un metanálisis realizado por el grupo anteriormente mencionado (21) (36 estudios con 2516 pacientes). Se compararon albúmina o fracción protéica del plasma versus hidroxietilalmidón; albúmina o fracción protéica del plasma versus gelatina; gelatina versus hidroxietilalmidón.
En 1999, Choi y colaboradores22 estudiaron en un metanálisis 17 trabajos con 814 pacientes y no encontraron diferencia en el grupo total cuando se compararon las soluciones de cristaloides y coloides en estos pacientes críticamente enfermos, ni en mortalidad ni en la incidencia de edema pulmonar. En este mismo análisis se encontró evidencia que el empleo de cristaloides en la resucitación de pacientes con trauma conlleva menor mortalidad que con el uso de coloides (riesgo relativo 0.39, 95 % intervalo de confianza 0.17-0.89).
Wilkes y colaboradores en el año 200123 en otro metanálisis de 55 estudios y 3500 pacientes, no encontraron diferencia significativa en mortalidad al comparar las soluciones de albúmina versus cristaloides.
El estudio SAFE (Saline versus Albumin Fluid Evaluation), en el que se compara albúmina al 4% y solución salina normal en la resucitación con fluidos en 6997 pacientes de cuidados intensivos, no encontró diferencia significativa en mortalidad a los 28 días de seguimiento entre estos dos grupos. Hubo 726 muertes en el grupo con albúmina comparado con 729 muertes en el grupo con salina (riesgo relativo de muerte 0.99% intervalo de confianza 0.91-1.09; P=0.87). En el subgrupo de pacientes con trauma, sin incluir trauma craneoencefálico, la mortalidad tampoco fue diferente (riesgo relativo 1.00; 95% intervalo de confianza, 0.56- 1.79; P= 1.00). Tampoco hubo diferencia significativa en la mortalidad en el subgrupo con sepsis severa ni en el subgrupo de pacientes con síndrome de dificultad respiratoria aguda.
Vincent y colaboradores25 analizaron en un metanálisis, la morbilidad y mortalidad de pacientes agudamente enfermos (71 estudios con 3782 pacientes), comparando el uso de albúmina en diversas concentraciones versus cristaloides y encontraron que la albúmina redujo la morbilidad y mortalidad, (riesgo relativo 0.92; 95% intervalo de confianza 0.86-0.98).
En los estudios en los que el grupo control no recibió nada de albúmina (32 estudios) los resultados a favor de la albúmina fueron más notorios (RR 0.77; Intervalo confianza: 0.67- 0.88).
USO DE ALBÚMINA HUMANA EN RESUCITACIÓN, HIPOALBUMINEMIA Y PLASMAFÉRESIS
Pregunta: Tiene alguna utilidad el empleo de albúmina humana parenteral en: resucitación, hipoalbuminemia, plasmaféresis?
Recomendaciones
Albúmina humana en resucitación
Se recomienda el uso de cristaloides isotónicos en la resucitación y manejo de pacientes críticamente enfermos. El empleo de albúmina humana es más costoso y no se han demostrado efectos benéficos significativos con su uso.
Evidencia: Alta Categoría de la recomendación: Hágalo
Albúmina humana en hipoalbuminemia.
No se recomienda el uso de albúmina humana para corregir hipoalbuminemia en enfermedades agudas.
Evidencia: Alta Categoría de la recomendación: No lo haga
El uso simultáneo de albúmina humana y furosemida puede ser efectivo en síndrome nefrótico para incrementar la diuresis y la excreción de sodio.
Evidencia: Intermedia Categoría de la recomendación: Probablemente hágalo
Está indicado el uso de albúmina humana asociada con paracentesis y diuréticos en cirróticos con ascitis de gran volumen y ascitis refractaria, así como asociada con vasopresores en el síndrome hepatorenal.
Evidencia: Intermedia Categoría de la recomendación: Probablemente hágalo
Albúmina humana en plasmaféresis
El uso de albúmina humana, para reemplazar volumen vascular en plasmaféresis, elimina la posibilidad de transmisión viral del plasma fresco congelado y produce menos complicaciones que éste.
Evidencia: Alta Categoría de la recomendación: Hágalo
Resumen de la evidencia clínica
1- En relación al tema Albúmina Humana en Resucitación, se remite al lector al tema Cristaloides versus Coloides en el Paciente Crítico
2- Hay evidencia significativa que el tratamiento de la hipoalbuminemia aguda con albúmina humana no modifica la morbilidad en estos pacientes.
3- Hay evidencia significativa que el tratamiento con furosemida y albúmina humana en síndrome nefrótico mejora la excreción de sodio y el volumen urinario
4- Existe información que sugiere que la albúmina es superior a otros expansores plasmáticos en la prevención de la disfunción circulatoria después de la paracentesis terapéutica en ascitis de gran volumen y ascitis refractaria.
5- Existe información que sugiere la utilidad de la albúmina humana en el tratamiento del síndrome hepatorenal asociado a vasopresores y agonistas alfa adrenérgicos.
6- Hay evidencia significativa que el empleo de albúmina humana para reemplazar el volumen vascular en plasmaféresis elimina la posibilidad de transmisión viral del plasma fresco congelado y produce menos complicaciones que éste.
SOPORTE DE LAS RECOMENDACIONES
Contexto
La albúmina humana es una proteína de alto peso molecular, 66.248 daltons.
En un adulto normal existen unos 300 gramos: 120 en el espacio vascular (42g/L) y 180 en el extravascular. En este último unos 70 gramos (30-40%) se localizan en la piel y el resto está distribuido en músculos y vísceras26.
La albúmina sérica representa la mayor fracción proteica del plasma: 42g/l de un total de 70g/L. Su sitio de síntesis es el hígado, a una tasa de 12g/día e igual cantidad se degrada, la mitad en el hígado y la otra mitad secretada al intestino26.
Por su tamaño molecular, la albúmina no difunde fácilmente hacia el espacio intersticial. La permeabilidad de la membrana capilar, en condiciones normales, es muy baja para la albúmina (Tabla 1)26.
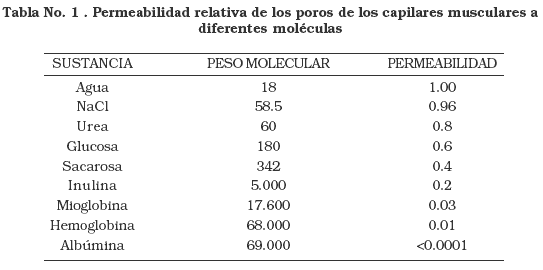
Esta condición hace que la albúmina, junto con las otras proteínas plasmáticas de gran peso molecular, ejerzan una presión osmótica efectiva (la dada por partículas que no atraviesan una membrana semipermeable), o tonicidad (denominada así la presión osmótica efectiva del compartimiento extracelular) que mantiene el volumen de este espacio vascular.26.
Esta presión osmótica de la albúmina y demás proteínas plasmáticas de gran tamaño es denominada también presión oncótica o presión coloidosmótica. Está incrementada por los cationes, principalmente sodio, que equilibran su carga eléctrica negativa26. Así, la presión coloidosmótica plasmática es de aproximadamente 28mmHg, 19 mmHg por las proteínas y 9mmHg por los cationes, el llamado efecto Donnan.26
A pesar de que 28mmHg es un bajo porcentaje de la presión osmótica total, su importancia en el mantenimiento de los volúmenes en cada compartimiento es definitiva.
Como la presión osmótica está dada por el número de partículas activas en la solución y no por el peso molecular, la albúmina ejerce la mayor presión osmótica de todas las proteínas plasmáticas, hasta el 75% 26.
Las propiedades descritas de la albúmina han motivado su uso en la terapia de fluidos, como expansor del volumen vascular en casos de hipovolemia y para corregir la hipoalbuminemia y restaurar la presión oncótica del plasma y en plasmaféresis para reemplazar el plasma.
La solución de albúmina humana al 4% es ligeramente hipooncótica, al 5% es isooncótica y al 25% hiperoncótica.
Las demás propiedades de la albúmina, como transportadora de otras moléculas endógenas o exógenas, su acción en el mantenimiento del equilibrio ácido-básico y su función anticoagulante y antioxidante, no han sido objeto de una evaluación tan extensa como la función osmótica.26-28
En condiciones patológicas que cursan con aumento de la permeabilidad capilar, como el síndrome de respuesta inflamatoria sistémica, la sepsis, las respuestas histamínicas, etc., la albúmina pierde parcialmente su capacidad osmótica ya que su paso al intersticio es facilitado por este trastorno de permeabilidad29.
Por otra parte, la síntesis de albúmina se reduce en el síndrome de respuesta inflamatoria, en la sepsis y en el trauma26.
En estas situaciones de trastorno de la permeabilidad capilar y reducción de la síntesis hepática que concurren en los "pacientes críticamente enfermos", el empleo de soluciones de albúmina como expansor plasmático, teóricamente no funcionaría como en las condiciones normales y podría favorecer la expansión del espacio intersticial o edema de este espacio29.
Estudios Clínicos
Albúmina humana en resucitación
Se refiere al lector a la sección: Cristaloides versus Coloides en el Paciente Crítico.
Albúmina humana en hipoalbuminemia.
Vincent y colaboradores30 condujeron un metanálisis sobre 90 estudios de cohortes, con un total de 291.433 pacientes para evaluar la hipoalbuminemia en enfermedad aguda como un factor de predicción de morbimortalidad y para evaluar la terapia con albúmina en pacientes hipoalbuminémicos en la disminución de la morbimortalidad.
En cuanto a los niveles séricos de albúmina como factor pronóstico, los hallazgos muestran que la hipoalbuminemia es un potente factor pronóstico, independiente. Por cada gramo por 100 ml de disminución en la concentración de albúmina sérica, se eleva significativamente el riesgo de mortalidad en 137%, de morbilidad en 89%, la estancia en la unidad de cuidados intensivos y en el hospital en 28% y 71% respectivamente y el aumento en la utilización de recursos en 66%.
En relación con la terapia de albúmina para corregir la hipoalbuminemia se analizaron 9 trabajos prospectivos, 7 de ellos aleatorizados, con 535 pacientes, que involucraron pacientes adultos y pediátricos.
No se encontraron diferencias en los dos grupos, odds-ratio de 0.74; I.C 95 % (0.36- 1.49), aunque este análisis sugiere la hipótesis que la administración de albúmina exógena para lograr un nivel sérico de más de 3.0g%, puede disminuir la morbilidad en pacientes hipoalbuminémicos.
En enfermedades crónicas que cursan con hipoalbuminemia importante, como síndrome nefrótico, cirrosis hepática y desnutrición de tipo Kwashiorkor, se ha evaluado la terapia con albúmina humana como a continuación se describe.
En el tratamiento del edema que se observa en el síndrome nefrótico se ha utilizado la albúmina, teniendo en cuenta que en el edema nefrótico se presenta hipovolemia como consecuencia de la reducción de la presión oncótica y que el uso de albúmina podría aumentar la presión oncótica y a su vez la excreción del sodio, produciendo disminución de edema. Dicha respuesta no se observa de manera uniforme en todos los individuos.
Un estudio que utilizó la combinación de albúmina más furosemida (60mgr más 200 ml de albúmina al 20%) produjo solo un modesto incremento en la excreción del sodio al compararla con furosemida sola31.
El incremento en la excreción del sodio puede ser equivalente a la cantidad de sodio contenida en el coloide y la expansión del volumen podría explicar el aumento de la natriuresis. Se observó una eficacia similar con la combinación albúmina-furosemida, cuando se utilizó en pacientes hipoalbuminémicos con cirrosis hepática32.
Es probable que la infusión de albúmina-furosemida sea efectiva en pacientes con edema refractario y severa hipoalbuminemia (< 2 Gr /dl) aunque no existe información concluyente al respecto.
En pacientes cirróticos con ascitis de gran volumen, que se define como una ascitis de gran magnitud que produce marcada incomodidad, que interfiere con las actividades diarias y que se acompaña de severa retención de sodio (con concentración urinaria de sodio < 10 mmol/L) y con filtración glomerular normal o moderadamente reducida, la terapia actual consiste en paracentesis de grandes volúmenes, expansores plasmáticos y diuréticos de mantenimiento33.
La remoción de grandes cantidades de fluido ascítico sin el uso de expansores del plasma se asocia con deterioro de la función circulatoria, caracterizada por una reducción del volumen sanguíneo arterial efectivo y la activación de factores vasoconstrictores y antinatruréticos33. Esta disfunción circulatoria que ocurre después de paracentesis de grandes volúmenes se asocia con una alta tasa de recurrencia de la ascitis, desarrollo del síndrome hepatorrenal o hiponatremia dilucional hasta en 20% de los casos y con sobrevida reducida33. Los expansores plasmáticos son efectivos en prevenir esta complicación34,35.
La albúmina es superior al dextrán 70 y a poligeline en la prevención de disfunción circulatoria posterior a una paracentesis que remueva más de 5 litros de fluido, pero los experimentos clínicos aleatorizados no han mostrado diferencias significativas en supervivencia entre los pacientes tratados con albúmina y aquellos tratados con otros expansores plasmáticos, por falta de estudios con un adecuado tamaño de muestra.35-37
La ascitis refractaria por cirrosis, definida como la pérdida de respuesta a altas dosis de diurético (400 mg de espironolactona por día más 160 mg de furosemida por día) o la recurrencia de efectos colaterales (ejemplo: encefalopatía hepática; hiponatremia; hipercalemia o azohemia) con dosis más bajas, se trata también con paracentesis y uso de expansores plasmáticos, especialmente albúmina33.
En el síndrome hepatorrenal, caracterizado por falla renal debida a vasoconstricción de la circulación renal, se utilizan medicamentos vasoconstrictores, como vasopresina o agentes alfa adrenérgicos, en combinación con albúmina, con buenos resultados en dos tercios de los pacientes.
Aunque este manejo es muy promisorio, la información es todavía limitada, pues está basada sólo en experimentos clínicos con tamaños de muestra pequeños38-43.
Albúmina humana en plasmaféresis
La plasmaféresis o extracción plasmática terapéutica es una técnica extracorpórea de purificación de la sangre que busca remover sustancias del plasma44.
Se realiza con mayor frecuencia en bancos de sangre, utilizando instrumentos de centrifugación que permiten la remoción selectiva de células (citoferesis) pero también se ha utilizado un eficiente método para separar el plasma por medio de filtros de hemodiálisis altamente permeables45.
El líquido removido por plasmaféresis requiere ser reemplazado para evitar la depleción de volumen; para tal fin se utiliza la albúmina humana, sola o con solución salina, y el plasma fresco congelado.
Las principales ventajas con el uso de albúmina son el menor riesgo de reacciones anafilácticas y la ausencia en la transmisión de infecciones virales46. Las principales complicaciones asociadas con el uso de albúmina se deben a anormalidades de la coagulación, hipocalemia que podría generar arritmias cardiacas, y reacciones anafilácticas en individuos que reciben inhibidores de la enzima convertidora de angiotensina (IECA), manifestadas por rubor e hipotensión como consecuencia del aumento de bradiquinina, que lleva a vasodilatación.
El plasma fresco congelado reemplaza a las proteínas normales que han sido removidas, no produce depleción de los factores de coagulación o de inmunoglobulinas; sin embargo, se presentan más complicaciones que con la albúmina como parestesias inducidas por el citrato (debido a la unión del calcio libre con critrato), calambres, urticaria y menos a menudo reacciones anafilácticas severas.
Se presentan complicaciones con mayor frecuencia con el uso de plasma fresco congelado que con albúmina (20% Vs 1.4%) , que pueden llegar a producir mortalidad entre 3 y 5 casos por 10.000 47.
El mayor costo de la albúmina puede limitar su uso.
RESUCITACIÓN CON FLUÍDOS Y EL DESARROLLO DEL SINDROME DE DIFICULTAD RESPIRATORIA AGUDA (SDRA)
Pregunta: Debe hacerse uso liberal o restringido de cristaloides en resucitación ante el riesgo de desarrollar SDRA?
Recomendación 1
En pacientes con sepsis severa o con choque séptico la resucitación debe ser temprana y agresiva con cristaloides, drogas vasoactivas, glóbulos rojos y oxígeno, dirigida a optimizar la respuesta hemodinámica a través de la obtención de los siguientes parámetros en las primeras 6 horas de resucitación: presión venosa central (PVC) de 8 a 12 mmHg, de 12 a 15 mmHg si está en ventilación mecánica o existe presión intrabdominal alta; presión arterial media (PAM) de 65 a 90 mmHg; gasto urinario > 0.5 ml/kg/min; saturación venosa central (ScvO2) >70%.
Evidencia: Alta Categoría de la recomendación: Hágalo
La resucitación de menor intensidad en esta fase, se considera inadecuada y conlleva mayor severidad de la disfunción orgánica múltiple y una mortalidad más elevada.
Evidencia: Alta Categoría de la recomendación: No lo haga
Recomendación 2
En pacientes críticamente enfermos la terapia de fluidos subsecuente al período de resucitación inicial de 6 horas debe estar dirigida a evitar la sobrecarga de líquidos y el edema pulmonar, a través de la obtención de presiones de llenado menos altas que en la resucitación inicial
Evidencia: Alta Categoría de la recomendación: Hágalo
El control secuencial radiológico de tórax para evaluar el ancho del pedículo vascular pulmonar se correlaciona bien con el balance de fluidos en estos pacientes.
Evidencia: Alta Categoría de la recomendación: Hágalo
Recomendación 3
En pacientes en choque hipovolémico por trauma, la resucitación debe ser temprana y agresiva con lactato de ringer hasta lograr la normalización de la tensión arterial, la frecuencia cardiaca, el gasto urinario y obtener una presión venosa central entre 8 y 15 mmHg . La resucitación debe ser, en lo posible, simultánea con el control vascular de la hemorragia.
Evidencia: Alta Categoría de la recomendación: Hágalo
Si se sospecha taponamiento cardíaco, la corrección quirúrgica es prioritaria antes que lograr los puntos finales de resucitación con administración masiva de fluidos.
Evidencia: Alta Categoría de la recomendación: Hágalo
Una vez los procedimientos quirúrgicos se han completado, la optimización de la resucitación debe guiarse por la obtención de un índice de entrega de oxígeno de 500 ml/min/m2.
Evidencia: Alta Categoría de la recomendación: Hágalo
La restricción de fluidos no reduce la disfunción pulmonar y en cambio aumenta la mortalidad.
Evidencia: Alta Categoría de la recomendación: No lo haga
Resumen de la evidencia clínica
1- Existe evidencia significativa de que la reanimación dentro de las primeras seis horas en pacientes con sepsis severa o choque séptico disminuye la mortalidad.
2- Existe evidencia significativa de que la reanimacion en pacientes con sepsis severa o choque séptico al guiarse por metas hemodinámicas definidas reduce la mortalidad.
3- No hay ninguna evidencia que soporte la restricción de líquidos en la reanimacion de pacientes sépticos o en choque séptico como método para prevenir la aparición del SDRA.
4- No hay ninguna evidencia que justifique la sobrecarga de volumen en el paciente en riesgo de desarrollar SDRA.
5- Existe evidencia clínica significativa que indica que una vez logradas las metas de reanimación con líquidos en el paciente con sepsis severa o choque séptico, el manejo de los líquidos debe guiarse por presiones de llenado, buscando los valores más bajos posibles.
6- Existe evidencia clínica significativa de que la reanimación precoz y agresiva con cristaloides en pacientes con trauma severo y choque hipovolémico reduce la mortalidad.
7- Hay evidencia clínica que sugiere que la reanimación en trauma con cristaloides produce menor mortalidad que cuando se usan coloides.
8- Existe evidencia clínica que sugiere que la corrección del taponamiento cardíaco debe preceder a la reanimación agresiva con fluidos para reducir la mortalidad en esta situación clínica.
9- Existe evidencia clínica significativa de que la optimización de la reanimación con fluidos en trauma, posterior al manejo inicial, debe guiarse por metas preestablecidas, específicamente la entrega de oxígeno (DO2).
10-Existe evidencia clínica significativa de que la reanimación agresiva con líquidos en el paciente con choque hemorrágico no conlleva una mayor incidencia de SDRA.
Soporte de la recomendación 1
Estudios clínicos
En el estudio de Rivers y colaboradores48, la resucitación inicial de pacientes con sepsis severa o choque séptico bajo las pautas dadas en la recomendación 1 (Tabla 2)48 redujo la mortalidad del grupo así tratado a 30.5% comparada con el 46.5% en el grupo manejado con terapia estándar (P=0.009). En esta reanimación inicial los cristaloides juegan un papel importante. El promedio de cristaloides recibidos para cumplir las presiones de llenado descritas fue de 4981+ 2984 ml en la resucitación inicial comparados con 3499 + 2438 ml (P< 0.001) en el grupo estándar, aunque al completar 72 horas de tratamiento los volúmenes de líquidos administrados fueron similares en ambos grupos. Igualmente el grupo con el tratamiento propuesto recibió en el período inicial más frecuentemente transfusiones de glóbulos rojos (P< 0.001) y soporte inotrópico (dobutamina) (P<0.001).
Los llamados puntos finales de resucitación que ayudan a valorar la hipoxia tisular global, a saber: la saturación venosa mixta de oxígeno; la concentración arterial de lactato, el déficit de base y el pH en sangre arterial49, mostraron que la reanimación inicial bajo las pautas propuestas corrigen oportunamente la hipoperfusion tisular.
Así, la reanimación temprana "agresiva" con cristaloides, inotrópicos, glóbulos rojos y oxígeno dirigida a obtener unos parámetros hemodinámicos preestablecidos, mejora la supervivencia en pacientes con sepsis severa y choque séptico al compararla con un tratamiento menos intensivo o restringido.
La mortalidad por falla multiorgánica fue similar en ambos grupos, sin que el estudio mencione incremento de mortalidad por SDRA en ninguno de los dos grupos48.
Dellinger y colaboradores50 quienes desarrollaron las "Guías para el manejo de la sepsis severa y el choque séptico: Campaña Sobreviviendo la Sepsis" y que representan 11 organizaciones internacionales, de cuidado intensivo e infectología, acogieron las pautas dadas en el trabajo de Rivers en el proceso de reanimación inicial en estos pacientes, resaltando la importancia de éste. Tabla No. 2.

Soporte de la recomendación 2
Estudios clínicos
En un estudio retrospectivo de 373 pacientes críticamente enfermos, Sakka y colaboradores51, demostraron que el contenido de agua pulmonar extravascular (APEV) medida en ml/kg o edema pulmonar, se correlaciona directamente con la mortalidad. Independientemente del diagnóstico, la mortalidad fue significativamente más alta en pacientes con un pico de APEV más alto de 15 ml/kg.
Foland y colaboradores52, en un estudio retrospectivo sobre 113 pacientes pediátricos con síndrome de disfunción orgánica múltiple, identificaron la sobrecarga de fluidos como un predictor de mortalidad, antes del inicio de hemofiltración continua.
En un estudio prospectivo, Mitchell y colaboradores53 aleatorizaron pacientes críticamente enfermos, un porcentaje de ellos con edema pulmonar, para recibir una terapia estándar de fluidos o un tratamiento restrictivo guiado por monitoría invasiva. Encontraron un menor edema pulmonar, menos días de ventilación mecánica y una tendencia hacia menor mortalidad en el grupo con restricción de líquidos.
La monitorización de la terapia de fluidos ha sido evaluada. Aunque parecería lógico que la monitoría invasiva con catéter de arteria pulmonar debería disminuir la mortalidad y la aparición de lesión pulmonar aguda (LPA) y síndrome de dificultad respiratoria aguda (SDRA), este concepto tampoco ha podido ser demostrado54-56.
Martín y colaboradores57, en un estudio prospectivo y ciego encontraron que la medición del ancho del pedículo vascular pulmonar en la radiografía portátil de tórax se correlaciona fuertemente con cambios en la presión de oclusión de la arteria pulmonar y la presión venosa central en pacientes con catéter en arteria pulmonar, siendo por consiguiente esta evaluación radiológica un procedimiento confiable y no invasivo para establecer el balance de fluidos en estos pacientes.
Soporte de la recomendación 3
Estudios clínicos
En pacientes con trauma severo y choque hipovolémico, la reanimación temprana ha demostrado mejorar la sobrevivencia en forma importante. Estas conclusiones se han obtenido al analizar la mortalidad durante la primera y segunda guerras mundiales, la guerra de Corea y la de Vietnam58.
La ausencia de reanimación con fluidos preoperatoriamente durante la primera guerra mundial se acompañó de gran mortalidad59.
Durante la segunda guerra mundial y durante el conflicto de Corea, la reanimación con coloides únicamente mejoró la sobreviviencia inicial, pero la mortalidad tardía por falla renal fue notoria59.
Durante el conflicto de Vietnam, con el reconocimiento de que el espacio intersticial y no solamente el vascular debía ser repletado, los cristaloides isotónicos se usaron en lugar de los coloides en la reanimación inicial, con lo cual la mortalidad se redujo aún más, así como la incidencia de falla renal aguda59.
Los trabajos de Shires, Moss y otros59 establecieron este concepto y además demostraron que la reanimación con grandes soluciones de cristaloides isotónicos ofrece la mejor supervivencia.
Un estudio reciente por Choi y colaboradores22 reafirma los resultados anteriores al mostrar que en trauma la reanimación con cristaloides tiene menos mortalidad que cuando se usan coloides (riesgo relativo 0.39, I.C. 95% (0.17- 0.89).
Se ha estudiado el tipo de solución cristaloide a usar en la reanimación.
Existen diferencias teóricas a favor del lactato de ringer59. El estudio de Healey y colaboradores60 mostró en animales que en hemorragia masiva la solución salina normal se asoció con un gran trastorno fisiológico (acidosis metabólica pH: 7.14+.06 vs 7.39+.04-P<0.01) y mayor mortalidad (50% vs 0%-P<0.05) comparada con el lactato de ringer.
Se están estudiando soluciones de cristaloides con características especiales, como la solución de ringer etil piruvato, la cual no solo expande el espacio intravascular intersticial sino que posee propiedades antiinflamatorias61.
En aquellos pacientes con hemorragia no controlada, existe controversia sobre si la administración de líquidos hasta normalizar la presión arterial y la frecuencia cardiaca antes del control vascular agraven la hemorragia y la mortalidad y si está indicado en estos casos iniciar la reanimación agresiva solo después de controlar la hemorragia.
El trabajo prospectivo de Bickell y colaboradores 62 sobre pacientes con trauma penetrante en el torso, mostró más baja sobrevivencia en los pacientes a quienes se repletó de volumen antes de que el control vascular fuera logrado (62% vs 70%-P<0.04), aunque el análisis de subgrupos mostró que este efecto fue solo significativo en aquellos pacientes con taponamiento cardiaco.
Un estudio de metanálisis de Kwan y colaboradores63 sobre el tiempo y el volumen de líquidos en reanimación de pacientes con shock hemorrágico no encontró evidencia significativa a favor de retrasar la reanimación hasta que el control vascular se haya logrado o el iniciar la reanimación en forma temprana en el período prequirúrgico.
Parece apropiado como se establece en la recomendación, iniciar la reanimación precozmente, iniciar el abordaje quirúrgico para control vascular tan pronto sea posible y, si se sospecha taponamiento cardiaco por el trauma, iniciar la corrección de éste antes de realizar una reanimación masiva con líquidos.
La optimización de la reanimación posterior al manejo inicial, cuyo objetivo final es la restauración del funcionamiento normal celular, debe estar orientada por la obtención de ciertos parámetros, que en la actualidad se centran en la adecuada entrega de oxígeno a los tejidos (DO2)64. Este parámetro integra tres variables importantes: concentración de hemoglobina, saturación arterial de O2 de la hemoglobina y gasto cardiaco.
McKinley y colaboradores65 en un estudio prospectivo encontraron el índice DO2 de 500 ml/min/m2 como adecuado para alcanzar las metas propuestas.
La posibilidad de que el tipo de reanimación propuesto, dirigido por unas metas hemodinámicas y fisiológicas y que implica el uso de altos volúmenes de cristaloides, pueda ser causa del síndrome de dificultad respiratoria aguda (SDRA) ha venido siendo estudiada desde la década de los años 70.
Se han realizado estudios prospectivos aleatorizados66-68 comparando cristaloides y coloides en reanimación, teniendo como punto prioritario de análisis la disfunción pulmonar. Los resultados han sido conflictivos por la metodología de los estudios, lo que ha llevado a estudios de metanálisis 22,69 que no han encontrado diferencia en la incidencia de disfunción pulmonar entre el uso de cristaloides y coloides, y volúmenes altos o reducidos de líquidos de reanimación.
Así, la carga temprana de volumen ha mostrado ser beneficiosa59, pero la reanimación agresiva en posteriores etapas no mejora los resultados59.
Se está estudiando la solución salina hipertónica al 7.5% con Dextran 70 al 6% en reanimación, a objeto de reducir la carga de fluidos iniciales. Un metanálisis (70) sugiere que este manejo podría ser mejor, especialmente en politraumatizados con trauma craneoencefálico cerrado severo71.
FLUIDOS EN RESUCITACIÓN DE PACIENTES CON TRAUMA CRANEOENCEFÁLICO
Pregunta: Debe hacerse uso liberal o restringido de cristaloides en resucitación de pacientes con trauma craneoencefálico ante el riesgo de desarrollar edema cerebral?
Recomendaciones
Evite la hipovolemia, que es un factor de riesgo en el desarrollo de edema cerebral, utilizando los líquidos necesarios para su corrección.
Evidencia: Alta Categoría de la recomendación: Hágalo
La restricción de líquidos no previene la aparición de edema cerebral, ni en la resucitación ni en el manejo posterior.
Evidencia: Alta Categoría de la recomendación: No lo haga
Use cristaloides isotónicos o hipertónicos en la resucitación.
Evidencia: Alta Categoría de la recomendación: Hágalo
Resumen de la evidencia clínica
1- Existe evidencia que favorece la reanimación liberal versus restringida de líquidos en pacientes con trauma craneoencefálico.
2- Existe evidencia que sugiere que la resucitación insuficiente ante la presencia de trauma o hemorragia de otros sistemas orgánicos incrementa la mortalidad
Soporte de las recomendaciones
Contexto
En la situación del trauma cráneo encefálico (TCE), la barrera hematoencefálica (BHE), que tiene un papel fundamental en el control del edema intersticial cerebral72, se altera transitoriamente y permite el paso de agua y electrolitos al parénquima cerebral; esta situación dura unos minutos y si se restablece el aporte de energía al encéfalo, la mayor parte de la BHE recupera parcialmente su función, y el daño persiste en las zonas en las que haya ruptura anatómica de la vasculatura (contusión y hematoma). Cuando al TCE se le adiciona un estado de mala perfusión (hipotensión arterial, choque), la disfunción de la BHE persiste por más tiempo y empeora el edema cerebral.
Se ha visto que el edema cerebral es el factor que más contribuye al aumento del volumen cerebral que ocurre después del trauma; el otro factor es el aumento del volumen sanguíneo cerebral, pero este último es responsable de solo una pequeña fracción del volumen total73.
En las guías norte-americanas de manejo del TCE (American Association of Neurological Surgeons-Brain Trauma Foundation)74 se sugiere que la terapia con líquidos endovenosos se debe guiar por la presión arterial (mantenerla por encima de 90 mmHg), y que el uso de cristaloides (isotónicos o hipertónicos) debe ser liberal en caso de hipotensión (recomendación de expertos). Otra revisión del tema sugiere que la restricción de líquidos no es mejor que la administración liberal, y que podría asociarse a mayor cantidad de episodios de hipotensión, con la consiguiente mala evolución de los pacientes75.
Estudios en animales
En un modelo de lesión criogénica76, se encontró que en animales con choque hipovolémico y lesión cerebral, el contenido de agua cortical cerebral no se correlacionaba con la presión venosa central (PVC), y de manera débil (29%) con la presión arterial media (PAM), sugiriendo que el estado circulatorio influye poco en la formación del edema cerebral y que lo hace a través de la presión hidrostática arterial. El mismo grupo77 con el mismo modelo animal, mostró que la cantidad de fluido administrada se correlaciona con la presión intracraneana, pero no con el contenido de agua cortical. En este estudio, la administración de agua libre y la disminución de la osmolaridad plasmática se asociaron a aumento de la presión intracraneana (PIC), pero no a aumento del edema cerebral. Estos hallazgos son reforzados por un estudio en ratas en el que se vió que la BHE se altera de manera transitoria por el TCE, y que a los 30 minutos la BHE ha recuperado su funcionamiento, pero si hay choque e hipoxia, la BHE tarda hasta 60 minutos en recuperar sus características78.
En otro estudio en ratas79, la administración de grandes volúmenes de solución salina (250 ml/Kg) no alteró la evolución del edema ni el desenlace después de trauma cerrado, pero la administración de DAD o SS1/2N empeoró el edema y el desenlace; posteriormente, el mismo grupo mostró que el factor más importante en esta diferencia en el aumento del agua cerebral es la administración de agua libre y no la hiperglicemia80.
Por otro lado, el aumento de la presión arterial con el clampeo de la aorta no produjo aumento de la PIC ni del edema cerebral81. En otro modelo de contusión cerebral, la utilización de Dopamina aumentó la PAM y por lo tanto el flujo Sanguíneo cerebral (FSC), pero aumentó el edema tanto en el hemisferio lesionado como en el contralateral82 y un modelo de hemorragia no controlada y lesión criogénica en cerdos mostró que el grupo reanimado con LR tuvo mejor el FSC y menos lesión secundaria que los grupos de reanimación retardada o fenilefrina83.
Un estudio en gatos, en 1976, mostró que la presión venosa influye en la presión tisular cerebral, pero no en el contenido de agua cerebral, a menos que la vasculatura se encuentre lesionada84. Algo similar mostró otro grupo con un modelo criogénico más choque hipovolémico en cerdos: la distensibilidad craneana disminuye en relación con el aumento de la PVC85, lo que sugiere que el aumento del volumen intracraneano está determinado en gran parte por el volumen sanguíneo.
Dos estudios más recientes con un modelo de hemorragia no controlada + lesión criogénica en cerdos, mostraron que con reanimación retardada (70 minutos) se obtenían mejores índices de aporte cerebral de oxígeno que con la reanimación temprana (solución de Hartmann 2 litros en esos 70 minutos), pero no se reporta el agua cerebral o la PIC86,87. Pero otro trabajo con seguimiento a 24 horas mostró que la asociación de choque más lesión cerebral produjo mayor edema y aumento de la PIC que la lesión cerebral sola88, mostrando que la agresión secundaria incide tardíamente en la evolución de la lesión.
Respecto al uso de lactato de Ringer (LR) ha existido mucha controversia, pues contiene una pequeña proporción de agua libre, pero en los estudios sobre el uso de solución salina hipertónica (SSH) se ha visto que la reanimación con LR se asocia a mayor PIC, pero el contenido de agua es similar89. De manera similar, usando el modelo de lesión criogénica en cerdos, la administración de LR no se asoció a mayor edema cerebral en el área lesionada, pero los líquidos hipertónicos mejoraron la distensibilidad cerebral al deshidratar el tejido no lesionado90.
En cuanto a la comparación de cristaloides contra coloides, se ha comparado la reanimación con LR vs Dextrán en un modelo de lesión criogénica + choque en cerdos adultos. Este estudio mostró que la PIC y el contenido de agua fue similar a 24 horas91, lo que sugiere que la presión coloido-oncótica no modifica la evolución del edema cerebral. En cambio un modelo de lesión criogénica en perros mostró que la administración de coloide (hetastarsh) se asoció a menor PIC que el cristaloide y sugiere que el edema cerebral podría ser menor92.
Estudios en humanos
Bouma evaluó 37 pacientes con TAC-Xe y encontró que la PIC se correlacionaba con el volumen sanguíneo cerebral (VSC) pero este no se correlaciona con el FSC93 ni con los signos de edema cerebral en la TAC, sugiriendo que otro factor (¿falla energética?) es la causa del edema y la vasodilatación.
Scalea y colaboradores94, estudiaron un cohorte de 30 pacientes con poli-trauma y TCE, sin indicación de craneotomía. Encontraron que la estabilización hemodinámica con líquidos (29 casos de los cuales 12 necesitaron inotrópicos), disminuyó la PIC de 15 a 13 mmHg (p=NS). La presencia de hemorragia subaracnoidea, edema cerebral y contusión en la TAC se asoció a mayor PIC inicial; en ellos la respuesta a la reanimación fue similar a la de los pacientes con TAC normal: la PIC tiende a disminuir. La mortalidad fue de 20% (6 pacientes) y no se relacionó con las variables hemodinámicas sino con la severidad (PIC elevada). La PIC no se correlacionó con la cantidad de líquidos, ni sangre infundida, ni con las variables hemodinámicas, pero si con el nivel sérico de lactato. Ésto llevó a los autores a proponer que había mala perfusión sistémica y regional en la génesis de la hipertensión endocraneana (HTEC).
York y colaboradores95, reportan un análisis secundario de 34 pacientes politraumatizados, con TCE, admitidos en un estudio de un fármaco neuroprotector. Ninguno requirió craneotomía y todos recibieron una reanimación agresiva con líquidos (17,9 litros en tres días en promedio). Reportan que la mortalidad fue de solo 6% y se obtuvo buena recuperación en 74% de los casos. Los autores atribuyen este resultado a que se evitaron las agresiones secundarias por hipotensión e hipoxemia en la mayoría de los casos, gracias a la reanimación agresiva, pero no hay análisis estadístico sobre el efecto atribuible a los líquidos.
Clifton96 reporta un análisis secundario de un cohorte de 392 pacientes de un estudio sobre hipotermia en TCE. En este trabajo examinaron la correlación entre varios niveles de balance de líquidos, PIC, PPC y PAM en el desenlace. Encontraron que los factores que se correlacionaron con un mal resultado (muerte, estado vegetativo o secuelas mayores) fueron en su orden: el puntaje de coma al ingreso, la edad, la PAM < 70 mmHg, el balance de líquidos _594 ml en los primeros 4 días y la PIC > 25 mmHg. No reportan ningún estimativo de edema cerebral. Los autores proponen evitar el balance negativo de líquidos en los primeros días de atención del paciente con TCE para mejorar el desenlace.
En contraposición a estas publicaciones, un pequeño estudio de casos y controles, no aleatorizado (97), mostró que la reanimación guiada por aporte de oxígeno (líquidos abundantes e inotrópicos para aumentar el gasto cardiaco, n=14) no llevó a resultados diferentes a los de la reanimación restringiendo líquidos (n=17). El bajo número de pacientes impide obtener una conclusión definitiva en este estudio.
Recientemente se ha evaluado el uso de soluciones salinas hipertónicas para reanimar a los pacientes con TCE, con la esperanza de contribuir al tratamiento del edema. Saltarini98 reportó que la infusión de SSH al 18% en un paciente con HTEC refractaria produjo una disminución del edema cerebral evaluado por RMN.
Cooper99 publicó un ensayo clínico controlado de inclusión aleatoria en el que se comparó la adición de SSH al 7,5 % contra LR en pacientes reanimados con LR + coloides en fase pre-hospitalaria. Este estudio no logró demostrar beneficio de la solución hipertónica. Hubo una tendencia a menor mortalidad en el grupo hipertónica (55% vs 47%) pero la potencia del estudio no permitió determinar la validez de esta conclusión.
Un estudio71 en el que se incluyeron los pacientes con TCE de ensayos clínicos previos controlados comparó 103 pacientes con TCE grave manejados con SSH + dextrán contra 119 casos con manejo estándar. Se encontró una mejoría significativa de la mortalidad en el grupo hipertónica 37.9% contra 26.9% (p = 0.080) .
ACIDOSIS METABÓLICA COMO ÍNDICE DE RESUCITACIÓN INSUFICIENTE EN EL PACIENTE CRÍTICO
Pregunta: La persistencia de acidosis metabólica es indicativa de resucitación insuficiente en el paciente críticamente enfermo?
Recomendaciones
La acidosis metabólica persistente en el paciente críticamente enfermo no necesariamente es debida a resucitación insuficiente.
Evidencia: Alta
La acidosis metabólica en pacientes críticamente enfermos es indicativa de resucitación insuficiente sólo en aquellos casos en que se demuestre hipoperfusión tisular.
Evidencia: Alta Categoría de la recomendación: Hágalo
La evaluación de hipoperfusión tisular debe incluir las mediciones hemodinámicas y de oxigenación usuales.
Evidencia: Alta Categoría de la recomendación: Hágalo
Considere la evaluación de la perfusión a través de capnografía sublingual, tonometría gástrica o similares en los casos de acidosis metabólica persistente con sospecha de hipoperfusión tisular en los que las mediciones usuales no la demuestren.
Evidencia: Alta Categoría de la recomendación: Probablemente hágalo
En el diagnóstico de acidosis metabólica no hay un método que sea superior a otro, para pronóstico o para sugerir intervenciones terapéuticas que permitan recomendarlo ampliamente para su uso clínico.
Evidencia: Alta
Resumen de la evidencia clínica
1.-Existe suficiente evidencia clínica de que la hipoperfusión tisular es la principal causa, aunque no la única, de acidosis metabólica persistente en el paciente críticamente enfermo.
2.-Existe evidencia clínica significativa de que la interpretación de los niveles de lactato sérico en el diagnóstico de acidosis metabólica es compleja, por cuanto la hiperlactatemia puede deberse al aumento en su producción en condiciones de hipoxia celular o hipermetabolismo, o a la disminución en el aclaramiento renal o en el metabolismo hepático, condiciones que coinciden con alta frecuencia en los pacientes críticos.
Por esta razón, el lactato sérico no es un indicador útil y práctico para establecer si la resucitación insuficiente es la causa de la acidosis metabólica, sobre todo en los pacientes sépticos.
3.- Hay evidencia clínica significativa que los parámetros clínicos, como presión arterial, frecuencia cardíaca, perfusión capilar y gasto urinario, así como los parámetros hemodinámicos y de oxigenación que evalúan globalmente el estado de repleción y funcionamiento vascular y oxigenación tisular, no son lo suficientemente precisos para establecer las condiciones de perfusión y oxigenación de importantes lechos vasculares como el esplácnico y el estado de la microcirculación en situaciones patológicas especiales como la sepsis.
Por consiguiente , su utilidad es limitada para diagnosticar los defectos de perfusión tisular y la acidosis metabólica dependiente de ésta.
4.- Existe evidencia clínica significativa de que las metodologías que evalúan la perfusión de lechos vasculares específicos, como la tonometría gástrica y la presión sublingual de CO2 y la microcirculación, como la técnica con luz polarizada ortogonal espectral, permiten diagnosticar los trastornos de perfusión más adecuadamente que los métodos tradicionales y deben incorporarse al arsenal diagnóstico, en la medida en que se perfeccionen y se haga más fácil su aplicación.
Soporte de las recomendaciones
Contexto
Uno de los desórdenes del equilibrio ácido-básico que se encuentra con mayor frecuencia en el paciente críticamente enfermo es la acidosis metabólica100. 165
La acidosis metabólica puede dividirse para efectos de definir si es debida a resucitación insuficiente en dos grupos: la debida a hipoxia celular y la debida a las demás causas (Tabla 3).
Hipoxia celular por hipoperfusión
Dentro del grupo de hipoxia celular, la perfusión sanguínea inadecuada de los tejidos ocupa un lugar importante.
La hipoperfusión en estos pacientes con frecuencia es debida a hipovolemia, falla cardiaca y trastornos en la microcirculación.
Las causas de hipovolemia intravascular incluyen la hemorragia; la deshidratación que reduce el agua extra e intracelular; la pérdida de fluido extracelular, agua y sodio, como ocurre en las pérdidas de líquidos a través del tracto gastrointestinal o en la traslocación de fluidos del compartimento vascular al intersticial por permeabilidad vascular incrementada, como en la respuesta inflamatoria 102.
Los trastornos en la microcirculación característicamente afectan a pacientes con sepsis, al punto que se ha calificado la sepsis como una enfermedad de la microcirculación103.
La sepsis altera los mecanismos autoregulatorios vasculares y las propiedades reológicas de la sangre104,105 causando de este modo maldistribución del flujo sanguíneo106. Esto resulta en unidades microcirculatorias, fundamentalmente a nivel capilar, sin suficiente flujo sanguíneo, impidiendo la adecuada oxigenación tisular107-109. La pérdida persistente de la perfusión capilar en sepsis es un indicador sensible de pobre pronóstico en estos pacientes 110.
La acidosis metabólica resultante de mala perfusión es explicada por hipoxia celular que lleva a :
- Impedimento en la fosforilación oxidativa. En condiciones aeróbicas esta vía metabólica forma ATP a partir de ADP con recaptura de un ión H+. En anaerobiosis este ión H+ libre aumenta la carga ácida del organismo111.
- La reducción en la formación de ATP mitocondrial activa la fosfofructokinasa (PFK), que es la principal enzima regulatoria de la vía glicolítica, con lo cual se incrementa la glicólisis, la producción de piruvato y su conversión a lactato112.
- El lactato acumulado en los tejidos, sin poder ser transformado en energía por falta de oxígeno, se convierte en ácido láctico ante la sobreoferta de iones H+102.
Así, la mala perfusión tisular lleva a hipoxia y ésta a acidosis metabólica por exceso de producción de ácido láctico y reducción en su consumo. Tabla No.3.
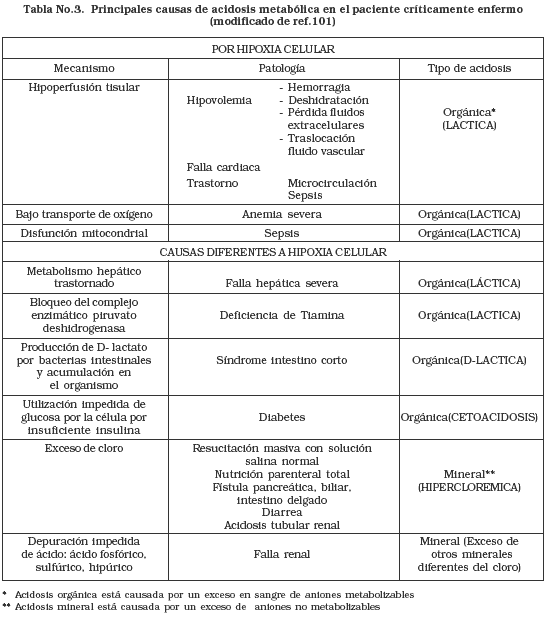
El hallazgo de niveles séricos elevados de lactato (>2 mmol/L ) sería un buen indicativo de hipoxia celular. Sin embargo la hipoxia celular no es la única causa de hiperlactatemia en estos pacientes.
En efecto, el hipermetabolismo que es parte de la respuesta al trauma y a las infecciones, cursa con una elevación de los niveles séricos de lactato que corren paralelos a la tasa metabólica y que no dependen de metabolismo anaeróbico sino de influencias hormonales y de citoquinas que incrementan su producción113.
Por esta razón el lactato sérico por si solo no es indicador de hipoxia celular.
Se ha postulado que la tasa lactato /piruvato permite discriminar la hiperlactatemia por hipermetabolismo (tasa no elevada: < 18 ) de la hiperlactatemia por hipoxia (tasa elevada: > 18 ) 113,114.
La interpretación de los niveles de lactato sérico es difícil por las razones expuestas. Independientemente de su utilidad diagnóstica, el lactato sérico tiene un valor pronóstico bien establecido115.
La evaluación de la hipoperfusión tisular e hipoxia consecuente, además del estudio del lactato sérico ya discutido, ha sido abordada por diversas metodologías .
Los medios tradicionales para evaluar la perfusión tisular como presión sanguínea, frecuencia cardíaca,gasto urinario y llenado capilar, así como las mediciones de oxigenación sistémica como entrega de oxígeno, consumo de oxígeno y saturación venosa central de oxígeno, aunque establecen el estado global de repleción vascular y de la oxigenación sistémica, no detectan importantes defectos de perfusión y oxigenación en lechos vasculares vitales ni tampoco el grado de recuperación de la homeostasis de éstos116,117.
Como ejemplos de estos trastornos de perfusión está el compromiso de la circulación esplácnica durante episodios de depleción de volumen vascular en la que ésta se compromete de forma más rápida y severa y se recupera más lentamente que otros sistemas orgánicos116,118-120, y los estados de sepsis, en los que los trastornos de la microcirculación descritos no pueden ser valorados por estas mediciones globales en forma adecuada.
Por esta razón, se han explorado nuevas alternativas para monitorizar el estado de perfusión y oxigenación de los diversos sistemas orgánicos.
El sistema esplácnico ha recibido especial atención por las características mencionadas.La detección temprana de hipoperfusión y de hipoxia en esta área, así como la monitorización de la recuperación de su homeostasis, dan una pauta acerca del estado de los demás lechos vasculares. Por otra parte, la rápida y completa corrección de la circulación mesentérica evita las complicaciones que van desde gastritis hemorrágica hasta falla multiorgánica118,119.
La tonometría gástrica es uno de los métodos propuestos para evaluar la perfusión y oxigenación del sistema esplácnico.
Dos datos pueden ser obtenidos por este método: el llamado PH intramucoso (PHi) y el gradiente de presión de CO2 gástrico-arterial sistémico. El PHi normal va de 7.35 a 7.45 y el gradiente de CO2 debe ser menor de 10 mmHg116.
El monitoreo sublingual del CO2 es otro método de evaluación de perfusión y oxigenación esplácnicas .Es menos invasivo y más fácil de aplicar y permite la medición continua del CO2 tisular 116,120. El gradiente de presión de CO2 sublingual - sistémico es mejor marcador de la perfusión tisular que la presión de CO2 sublingual únicamente121.
La aplicación de técnicas de espectroscopia infrarroja próxima a los tejidos podría avalar igualmente los trastornos de la microcirculación122.
El estudio de la microcirculación en sepsis a través de la técnica imagenológica de polarización ortogonal espectral110 es un método promisorio de evaluación y pronóstico en estos pacientes.
Hipoxia celular por anemia y disfunción mitocondrial
Dos condiciones adicionales a la hipoperfusión tisular pueden conducir a hipoxia celular, metabolismo anaeróbico y acidosis metabólica en los pacientes críticos: la anemia112 y la disfunción mitocondrial, demostrada en pacientes sépticos, que impide la utilización de oxígeno por la célula 123,124.
Las demás causas de acidosis metabólica descritas en la Tabla I no son debidas a resucitación insuficiente y obviamente deben ser tenidas en cuenta entre las causas de acidosis metabólica en el paciente crítico.
Estudios clínicos
Valoración de la perfusión tisular: patrones hemodinámicos clínicos. Se refiere al lector a la sección donde se trata este tema específico: "Utilidad de los Signos Clínicos en el Diagnóstico y Manejo del Choque Hipovolémico".
Valoración de la perfusión tisular: tonometría gástrica; monitoreo sublingual de CO2; técnica imagenológica de polarización ortogonal espectral.
Doglio y colaboradores125 en 1991 fueron los primeros en validar el uso de la tonometría gástrica. En cincuenta pacientes consecutivos admitidos a la unidad de cuidados intensivos, midieron el pHi gástrico a la admisión y 12 horas más tarde. Los pacientes fueron estratificados con un pHi normal (pHi >7.35) y con un pHi bajo. No había diferencia significativa en presión arterial, frecuencia cardíaca ni pH arterial entre los dos grupos.Sin embargo, aproximadamente el 30% de los pacientes tenía un bajo pHi. La mortalidad fue significativamente más alta en el grupo de pHi bajo (65.4% vs.43.6%). Los pacientes que fallaron en normalizar el pHi después de 12 horas tuvieron una mortalidad muy alta (87%) comparativamente con los que corrigieron el pHi (27%). Los autores concluyeron que el pHi fue un marcador tanto de la severidad del choque como de la adecuación de la resucitación.
Gutiérrez y colaboradores126 compararon la información obtenida de la tonometría gástrica con la del catéter arterial pulmonar. Los sobrevivientes fueron comparados con los no sobrevivientes. No hubo diferencia significativa entre las variables de edad, APACHE, signos vitales, y variables hemodinámicas al tiempo de la admisión a la unidad de cuidados intensivos .Durante el período de estudio los no sobrevivientes tuvieron más frecuentes elevaciones en el consumo de oxígeno, extracción de oxígeno, y acidosis mucosa gástrica. Estas diferencias alcanzaron significancia estadística. Sin embargo, solamente el pH venoso mixto y el pHi predijeron el desenlace.
Maynard y colaboradores127 corroboraron estos resultados. En su estudio de 83 pacientes críticamente enfermos, las variables hemodinámicas (índice cardíaco, entrega de oxígeno y extracción de oxígeno) fueron incapaces de predecir el desenlace. Mediciones globales tales como lactato sérico y déficit de base predijeron el desenlace. Sin embargo, el pHi tuvo una sensibilidad del 88% para predecir la muerte y una tasa de probabilidad de 2.32, mucho mejor que cualquier otra variable al tiempo de la admisión a la unidad de cuidados intensivos.
Dos estudios prospectivos aleatorizados han usado el pHi como un punto final de resucitación después de trauma severo. En el primero, Ivatury y colaboradores128 aleatorizaron pacientes a un punto final de pHi por encima de 7.30, comparado con el grupo manejado con parámetros de trasporte de oxígeno (entrega de oxígeno, 600mL/m/M2; índice de consumo de oxígeno de 150 mL/m/M2 ). No hubo diferencias significativas en la severidad del trauma, el déficit de base o el lactato sérico entre los dos grupos. Las metas de resucitación fueron alcanzadas dentro de las primeras 24 horas en virtualmente todos los pacientes. En el grupo de pHi (n=11) la sobrevivencia fue de 82%, y la sobrevida excedió el 90% entre los pacientes que tenían persistentemente un pHi normal. En el grupo de mediciones de trasporte de oxígeno (n=16), la sobrevida fue de 69%. Estos resultados no alcanzaron significancia estadística por el tamaño de la muestra. Es de anotar, sin embargo, que el 80% de los no sobrevivientes tenían acidosis mucosa. El pHi bajo fue el primer signo de bacteremia, isquemia mesentérica e hipertensión intraabdominal.
En un estudio similar, Ivatury y colaboradores 129 encontraron resultados similares. Sólo 7% de los pacientes con pHi por encima de 7.3 a las 24 horas experimentaron falla orgánica múltiple, comparados con más del 50% de los pacientes cuyo pHi no se normalizó. La cantidad de tiempo necesario para que variables como lactato, déficit de base y transporte de oxígeno se normalizaran no fue diferente entre sobrevivientes y no sobrevivientes. Solamente el tiempo de optimización del pHi predijo la mortalidad.
Creteur y colaboradores130 evaluaron el gradiente de CO2 mucosa-arterial en pacientes sépticos y encontraron que este gradiente no se correlaciona con los índices globales de oxigenación del intestino.
La tonometría gástrica no es un procedimiento práctico de realizar. Requiere un largo período de entrenamiento, que el paciente tenga un tubo de decompresión gástrica y que se retire la nutrición enteral. La medición acuciosa del pHi es dependiente del completo bloqueo de la secreción gástrica de iones H+(120) Por otra parte, la tonometría gástrica descansa en la premisa que los niveles de bicarbonato arteriales y de la mucosa son los mismos lo cual no es el caso en condiciones patológicas120.
Weil y colaboradores (131) fueron los que reportaron primero el uso clínico de la medición del CO2 sublingual en 45 pacientes críticos. Las medidas fueron reportadas cada treinta minutos por 6 horas. Los pacientes en choque circulatorio, definido como una presión sistólica menor a 100 mmHg y una concentración de ácido láctico >2.5 mmol/L, tenían una presión de CO2 sublingual estadísticamente más alta que los pacientes que no estaban en choque. Fue demostrado que la presión de CO2 sublingual tenía un valor predictivo positivo para choque de 100%. Al tiempo de la admisión, la presión sublingual de CO2 estaba significativamente más alta en los no sobrevivientes que en los sobrevivientes, reflejando los resultados de los niveles séricos de lactato.
Marik y colaboradores132 compararon la presión sublingual de CO2 y el PCO2 gástrico en un grupo de 22 pacientes críticamente enfermos con choque séptico o cardiogénico. La mortalidad global fue de 40%.Hubo una buena correlación entre estas dos mediciones. La presión inicial sublingual de CO2 fue de 43.5 ± 10.4 mmHg,y la PCO2 gástrica fue de 42.8± 10.9 mmHg (coeficiente de correlación, 0.86; p<0.001).
Baron y colaboradores133 usaron la presión sublingual de CO2 en 75 pacientes con trauma penetrante del torso. Los pacientes fueron estratificados en grupos representando un mínimo, moderado o gran volumen de sangre perdida, basados en hallazgos operatorios y requerimientos transfusionales. No hubo diferencias significativas en presión arterial o frecuencia cardíaca entre los tres grupos, de nuevo demostrando la falta de especificidad de los signos vitales. A la admisión, la presión sublingual de CO2 fue capaz de predecir la pérdida de sangre con precisión. Una presión sublingual de CO2 po debajo de 45 mmHg predijo con exactitud la estabilidad hemodinámica con un intervalo de confianza del 90%.
Marik y colaboradores (121) encontraron que el PCO2 sublingual inicial y el gradiente mucoso-arterial de CO2 fueron altamente predictivos del desenlace.(p=0.004 p=0.0004) en 58 pacientes en sepsis severa o choque séptico, por encima de detrminaciones tradicionales y globales de hipoxia tisular como lactato arterial y saturación venosa mixta de oxígeno.
Matura y colaboradores134 validaron el empleo de un aparato para la evaluación no invasiva de la microcirculación en humanos a través de la técnica de imagen de polarización espectral ortogonal al compararlo con la microscopía convencional.
Sakr y colaboradores110 en un estudio prospectivo observacional estudiaron 46 pacientes con choque séptico, utilizando esta técnica y encontraron que la perfusión de los pequeños vasos mejoró con el tiempo en los sobrevivientes (análisis de varianza, p< 0.05 entre sobrevivientes y no sobrevivientes) pero no en los que fallecieron.
A pesar de perfiles hemodinámicos y de oxigenación similares y el uso de vasopresores al final del choque, los pacientes que fallecieron después de la resolución del choque en falla multiorgánica tenían un porcentaje más bajo de capilares prefundidos que los sobrevivientes (Densidad vascular: 57.4 vs. 79.3 % ;p=0.02).
Concluyeron que las alteraciones microcirculatorias mejoran rápidamente en los sobrevivientes de choque séptico pero no en los pacientes que fallecen con falla multiorgánica, a pesar de que el choque se haya resuelto. Sugieren que alteraciones en la perfusión de la microcirculación pueden estar involucrados en el proceso de desarrollo de falla orgánica múltiple y muerte.
Enfoque diagnóstico de la acidosis metabólica
Tradicionalmente la ecuación de Henderson Hasselback (100) que describe la relación entre pH, HCO3- y PCO2 ha sido usada conjuntamente con la base exceso estandar y el cálculo de la brecha aniónica para delinear el estado ácido _ básico y las causas potenciales de la acidosis metabólica.
Dos factores limitan potencialmente este enfoque:
a) las variables de la ecuación de Henderson _ Hasselback están influenciadas por varios factores no considerados en la ecuación
b) la interpretación de la brecha aniónica es dependiente de la composición normal del plasma y con frecuencia en los pacientes críticamente enfermos se encuentran desviaciones de lo normal en relación a los aniones , primariamente albúmina pero también gelatinas infundidas y fosfato y en menor extensión constituyentes catiónicos como K+, Ca++, Mg++ y litio lo que puede resultar en que la brecha aniónica sea imprecisa y poco sensible en presencia de acidosis metabólica100.
Para obviar estos problemas se desarrolló un enfoque diferente, desarrollado por Stewart que fue modificado posteriormente por Figge, Fencl y Watson100. Este enfoque se basó en los principios de la electroneutralidad y conservación de masa.
Stewart mostró que tres variables independientes (diferencia de iones fuertes, ácidos no volátiles débiles y PCO2) independientemente alteran el pH por medio de su efecto sobre la disociación de la molécula de H2O en H+ y OH-. Las fuerzas electroquímicas cambian la concentración de H+. La aplicación de este enfoque permite el cálculo de la brecha de iones fuertes(100).
Algunos estudios han examinado si el enfoque de Stewart ofrece ventajas clínicas sobre los enfoques tradicionales, y los resultados son controversiales (100).(165)
ACCESOS VENOSOS EN RESUCITACIÓN
Pregunta: En resucitación cuál es el acceso venoso de elección: las líneas centrales o las líneas periféricas?
Recomendaciones
Los accesos venosos de elección para resucitación en pacientes adultos son las venas periféricas de los miembros superiores, como la antecubital y otras del antebrazo.
Evidencia: Alta Categoría de la recomendación: Hágalo
Se deben canalizar al menos dos venas periféricas por venipunción con catéteres cortos y de grueso calibre, 14 o 16 G.
Evidencia: Alta Categoría de la recomendación: Hágalo
Cuando no sea posible utilizar las venas periféricas de los antebrazos, y si se cuenta con experiencia, la selección en orden decreciente es:
- vena safena a nivel del maléolo medial, por venipunción
- vena subclavia o yugular interna por venipunción con técnica de Seldinger y si es posible apoyada por ultrasonido
- vena femoral por venipunción con técnica de Seldinger.
Evidencia: Alta Categoría de la recomendación: Hágalo
La venodisección de la vena cefálica, la vena basílica o la vena safena en su desembocadura a la femoral son la última opción y requieren experiencia.
Evidencia: Alta Categoría de la recomendación: Probablemente hágalo
En la resucitación de pacientes con sepsis severa o con choque séptico se debe canalizar una vena central (subclavia o yugular interna), además de las venas periféricas, para la administración de vasopresores.
Evidencia: Alta Categoría de la recomendación: Hágalo
Soporte de las recomendaciones
Estudios clínicos
Las mejores vías de acceso venoso periférico en el adulto son las venas antecubitales, otras del antebrazo y la safena interna. El acceso es exitoso en la mayoría de las situaciones por parte del personal paramédico y no se requiere un adiestramiento especializado135,136.
En casos de dificultad, cuando la situación impide que se utilicen venas periféricas, (por ejemplo, severa vasoconstricción, trauma de extremidades superiores, obesidad) y si se cuenta con el entrenamiento específico, se debe considerar la colocación de vías venosas centrales utilizando la técnica de Seldinger. Las vías de acceso son las venas subclavia, yugular o femoral. El acceso a la vena subclavia es tan exitoso como la canalización de venas periféricas; se logra en más del 90% de las veces137,138. El porcentaje de complicaciones al cateterizar la vena subclavia es bajo (7,8%-10%) cuando la realiza personal experto137,139. El acceso de la vena femoral tiene menor porcentaje de éxitos que el acceso a la vena subclavia (77% vs 94% p<0,05)140. El procedimiento de cateterización de venas centrales puede ser difícil de realizar en las circunstancias propias de resucitación del paciente traumatizado. También se debe considerar la disección quirúrgica de venas del antebrazo o de la safena interna135,136. Sin embargo, la cateterización percutánea de la vena femoral en pacientes con pulso palpable se puede realizar más rápidamente que la disección de la vena safena, logrando una velocidad mayor del flujo141. En todo caso, deberá elegirse aquella en cuya técnica se tenga más experiencia, siendo preferible la canalización de la subclavia, debiéndose elegir la subclavia del hemitórax lesionado en caso de traumatismo torácico.
Se pueden presentar complicaciones con la colocación de catéteres centrales. Pueden ser mecánicas, infecciosas y trombóticas. La complicación más común de la cateterización de la vena subclavia es el neumotórax el cual ocurre entre el 1,5% y el 2,8%142,143. Las complicaciones infecciosas son mayores cuando se canaliza la vena femoral que la vena subclavia (20 infecciones por 1.000 días catéter para la vena femoral vs 3,7 por 1.000 días catéter de vena subclavia)143. La incidencia de trombosis es mayor en la vena femoral (20%-25%) que en la vena subclavia (10%-15%)144,145. La canalización de la vena femoral sólo deberá considerarse si se fracasa en las punciones percutáneas o en el acceso a la vena subclavia o yugular. El uso de ultrasonido en la cateterización venosa central ha elevado el éxito en la cateterización y reducido las complicaciones146,147.
La canalización de una vena central es requerida para la administración de vasopresores que forman parte de la terapia de resucitación en choque séptico y sepsis severa50.
UTILIDAD DE LOS SIGNOS CLÍNICOS EN EL DIAGNÓSTICO Y MANEJO DEL CHOQUE HIPOVOLÉMICO
Pregunta: Presión arterial, frecuencia cardíaca y llenado capilar son parámetros suficientes para la valoración de la hipovolemia y la resucitación adecuada en el choque hipovolémico?
Recomendaciones
El diagnóstico del choque hemorrágico es eminentemente clínico.
Evidencia: Alta Categoría de la recomendación: Hágalo
No existe un parámetro único, clínico hemodinámico o de laboratorio, que permita diagnosticar o excluir el choque hemorrágico.
Evidencia: Alta
La presencia de hipotensión, taquicardia o lentitud del llenado capilar en el contexto clínico adecuado confirman la presencia de hipovolemia. Su ausencia, sin embargo no la excluyen.
Evidencia: Alta Categoría de la recomendación: Hágalo
La medición de la presión arterial por técnicas no invasivas está sujeta a riesgo de imprecisión, por factores del paciente, de la técnica, del equipo y de quien la ejecuta.
Evidencia: Alta
Lleve a cabo revisiones periódicas de la técnica de la medición de presión arterial y del estado de los equipos.
Evidencia: Alta Categoría de la recomendación: Hágalo
Haga medición de la presión arterial con un catéter intraarterial en los pacientes hipovolémicos críticos.
Evidencia: Alta Categoría de la recomendación: Hágalo
La valoración clínica del paciente en choque hipovolémico que está siendo reanimado debe ser dinámica y complementada por evaluaciones de variables de perfusión tisular.
Evidencia: Alta Categoría de la recomendación: Hágalo
Soporte de las recomendaciones
Estudios clínicos
Confiabilidad de la presión arterial medida con técnicas no invasivas
La presión arterial medida con la técnica de manguito está sujeta a imprecisiones relacionadas con la técnica, el dispositivo empleado para efectuar la medición y el paciente148,149.
La correlación entre la presión medida manualmente y la medida directamente muestra una buena correlación (r =0.94 _ 0.98). Sin embargo en pacientes individuales pueden ocurrir diferencias muy significativas149.
La presión medida automáticamente resulta en valores más altos que la medida manualmente (150).
En un estudio en el que se compararon la presión medida automáticamente con método no invasivo con la presión medida por canulación de una arteria radial se encontraron coeficientes de regresión de 0.91 para la PAS, de 0.76 para la media y de 0.84 para la diastólica. La presión medida indirectamente se apartó entre un 3 y 5% de la medida directamente150.
El método no invasivo sobreestimó la presión cuando esta era inferior a 80 mm Hg y la subestimó cuando era superior a esta cifra151.Confiabilidad de la presión arterial, la frecuencia cardiaca y llenado capilar en la detección del choque hemorrágico
McGee y colaboradores152 publicaron una revisión sistemática de la literatura, acerca de la utilidad de los signos clínicos para detectar hipovolemia. En voluntarios sanos sometidos a flebotomía encontraron que el hallazgo de un incremento de la frecuencia cardíaca superior a 30 latidos por minuto, después de hacer poner al paciente de pies, durante un minuto o más, o la incapacidad para hacerlo, tuvo una sensibilidad de 20% para detectar pérdidas de 450 a 630 c.c. y del 97% (IC 95% de 91- 100%) cuando la pérdida sanguínea osciló entre 630 y 1150 c.c. La especificidad fue del 98% (IC del 95% de 97% - 100%). Los signos persisten entre 12 y 72 horas si no se instituye terapia. La sensibilidad disminuye (39% a 78% para detectar pérdidas de 1000 c.c.) cuando las determinaciones se hicieron con el voluntario sentado en lugar de parado.
La hipotensión postural definida como la disminución de la presión arterial mayor de 20 mm Hg, después de hacer parar al voluntario, tuvo una sensibilidad baja en hemorragias de 450 a 630 c.c. y no pudo ser evaluada en pérdidas sanguíneas mayores.
La taquicardia supina (FC>100/min), tuvo una especificidad de 96%, pero una sensibilidad baja (12%, (IC 95% de 5 _ 24%) para pérdidas sanguíneas grandes.
La hipotensión en supino mostró una sensibilidad de 13% (0- 50%) para hemorragias pequeñas de 32% (IC 95% 21- 47%) para hemorragias grandes y una especificidad de 97% (IC 95% 90- 100%) para hemorragias grandes.
El cuadro clínico de hipotensión y taquicardia no está presente siempre en sujetos traumatizados con choque hemorrágico. Existe una proporción de pacientes hipotensos que se presentan bradicárdicos. 29% en una serie de 750 pacientes 153 y 35% en otra de 489(154); en esta última el 3% de los sujetos normotensos presentaban taquicardia. La mortalidad fue del 29% en los individuos hipotensos y taquicárdicos y del 22% en los hipotensos bradicárdicos en la primera serie y del 15% y el 2%, respectivamente, en la segunda. En esta última ocurrió pérdida de más de 1 L de sangre intraoperatoria en el 79% de los taquicárdicos y en el 21% de los bradicárdicos. Se encontró necesidad de transfundir >4u de GRE en 84% de los taquicárdicos y en el 16% de los bradicárdicos.
La determinación del llenado capilar se hace comprimiendo el dedo anular posicionado a nivel del corazón, durante 5 segundos, midiendo posteriormente el tiempo invertido para que el color regrese a lo normal. El tiempo límite es de 2 segundos para niños y hombres adultos, 3 para mujeres y 4 para ancianos155.
El llenado capilar ha sido evaluado solamente en una investigación, para determinar su desempeño en la detección de hemorragia. Empleando el límite de 2 segundos, la sensibilidad para detectar una pérdida sanguínea de 450 c.c. fue de 6%, la especificidad de 93% y el LR de 1.0.
Cuando se usó en la detección de hipovolemia de causas diferentes a la hemorragia, tuvo una sensibilidad del 34%, una especificidad del 96% y unos LR (+) de 6.9 y LR (-) 0.7 156.
En población pediátrica se ha encontrado correlación con el índice sistólico, la presión venosa central y el volumen latido, sin que se pueda predecir en forma significativa en pacientes intubados157, en valoración de urgencias 158 o en triage159.
La eliminación del llenado capilar de un índice que mide la intensidad de la alteración fisiológica presente en la revisión inicial de pacientes traumatizados, no modificó el desempeño del índice en la predicción de mortalidad o sobrevida160.
La presión arterial, la frecuencia cardiaca y llenado capilar como únicos parámetros de reanimación en pacientes con choque hemorrágico.
En un estudio observacional prospectivo que incluyó 126 pacientes quirúrgicos los terapeutas fueron instados a predecir las variables hemodinámicas antes de insertar un catéter de arteria pulmonar 161. El desempeño en la predicción de una presión de cuña pulmonar baja mostró una sensibilidad del 63%, una especificidad de 63%, un VPP de 25% y un VPN de 90%. El desempeño en la predicción de un gasto cardíaco bajo mostró una sensibilidad del 66%, una especificidad del 80%, un VPP de 22% y un VPN de 97%. Los hallazgos encontrados después de la inserción del catéter de arteria pulmonar motivaron cambios en el 50% de los casos. Estos fueron más comunes en los pacientes de cirugía vascular (63%) que en los de trauma (38%).
La observación prospectiva de pacientes en choque, ha permitido establecer que la frecuencia cardíaca no difiere entre los individuos que sobreviven y los que no, durante ninguna de las fases del choque y la reanimación. Por otra parte, la presión arterial media no difirió durante las fases iniciales y fue significativamente mayor en los sobrevivientes en las fases tardías de la reanimación. Los valores se superpusieron a tal grado, que fue imposible separar los sobrevivientes de los no sobrevivientes, con base en esta parámetro162. En este mismo estudio se encontró que el gasto cardíaco de los pacientes con hipotensión moderada y severa no difirió significativamente. Algunas determinaciones hemodinámicas invasivas, o las variables de transporte y consumo de oxígeno discriminaron a los sobrevivientes de los no sobrevivientes162.
En pacientes críticamente traumatizados se encontraron signos de hipoperfusión en más del 80% de los sujetos en quienes se había alcanzado la normalidad de los signos vitales163.
La presión arterial fue escogida como objetivo de la reanimación en un ensayo clínico controlado, en el que pacientes traumatizados que ingresaron hipotensos fueron aleatorizados para ser manejados hacia un objetivo de presión sistólica de 70 mm Hg y otros hacia una presión sistólica de 100 mm Hg. La mortalidad fue semejante 164.
Subvención de la Reunión de Consenso
La Reunión de Consenso fue subvencionada en su totalidad por los Laboratorios Baxter S.A.
AGRADECIMIENTOS
Los autores agradecen a los Laboratorios Baxter por su apoyo a estas actividades académicas y en particular al Doctor Víctor Pedroza y a las señoras Alexandra Orjuela y Carmen Sofía Alvarez, Gerente General y Ejecutivas respectivamente de esta empresa por su especial soporte en el desarrollo de este proyecto.
BIBLIOGRAFÍA
1- GRADE Working Group: Grading quality of evidence and strength of recommendations.BMJ, 328: 1, 2004.
2- Shoemaker, W.C.: Comparisons of the relative effectiveness of whole blood transfusions and various types of fluid therapy in resuscitation. Crit Care Med, 4:71, 1976.
3- Lamke, L.O., Liljedahl, S.O.: Plasma volume changes after infusion of various plasma expanders. Resuscitation, 5:93, 1976.
4- Rackow, E.C., Falk, J.L., Fein, I.A.: Fluid resuscitation in shock: A comparison of cardiorespiratory effects of albumin, hetastarch and saline solutions in patients with hypovolemic shock. Crit Care Med, 11: 839 , 1983.
5- Hollenberg, S.M, T.S., Ahrens, D., Astiz, M.E., et al: Practice parameters for hemodynamic support of sepsis in adult patients: 2004 update. Crit Care Med, 32 (9): 1928, 2004.
6- Nylander, W.A.J., Hammon, J.W.J., Roselli, R.J., et al: Comparison of the effects of saline and homologous plasma infusion on lung fluid balance during endotoxemia in unanesthetized sheep. Surgery, 90:221, 1981.
7- Metildi, L.A., Shackford, S.R., Virgilio, R.W., et al: Crystalloid versus colloid in fluid resuscitation of patients with severe pulmonary insufficiency. Surg Gynecol Obstet, 158: 207, 1984.
8- Appel, P., Shoemaker, W.L.: Evaluation of fluid therapy in adult respiratory failure. Crit Care Med, 9:862, 1981.
9- Rackow, E.C., Astiz, M.E., Schumer, W. ,et al: Lung and muscle water after crystalloid and colloid infusion in septic Rats: Effect on oxygen delivery and metabolism. J Lab Clin Med, 113: 184, 1989.
10- Baum. T.D., Wang, H., Rothschild, H.R., et al: Mesenteric oxygen metabolism, ileal mucosal hydrogen ion concentration and tissue edema after crystalloid or colloid resuscitation in porcine endotoxic shock: comparison of Ringer's lactate and 6% hetastarch. Cir Shock , 30: 385, 1990.
11- Cittanova, M.L., Leblanc, I., Legendre, C., et al: Effect of hydroxiethyl starch in brain dead kidney donors on renal function in kidney-trasplant recipients. Lancet, 348: 1620, 1996.
12- Schortgen, F., Lacherade, J.C., Bruneel, F., et al: Effects of hydroxiethyl starch and gelatin on renal function in severe sepsis: a multicentre randomised study. Lancet, 357: 911, 2001.
13- De Jorge, E Levi, M: Effects of different plasma substitutes on blood coagulation: A comparative review. Crit Care Med, 29: 1261, 2001.
14- Cochrane Injuries Group Albumin Reviewers: Human albumin administration in critically ill patients: systematic review of randomized controlled trials. BJM, 317: 325, 1998.
15- Tobias, M.D., et al: Differential effects of serial hemodilution with hydroxiethyl starch, albumin and 0.9 saline on whole blood coagulation. J Clin Annesth, 8:366, 1998.
16- Napolitano, L.M., et al: Life threatening Acid Base Disorders, In: ASC Surgery Principles and Practice Wilmore, D. et al (eds) Web MD Corporation. New York 2002. pp. 108 - 116.
17- Herbert, P.C., Cook, D.J., Wells, G., et al: The design of randomized clinical trials in critically ill patients. Chest, 121: 1290, 2002.
18- Weil, M.H., Tang, W.: Albumin versus crystalloid solutions for the critically ill and injured. Crit Care Med, 32 (10): 2154, 2004.
19- The Albumin Reviewers (Alderson, P., Bunn, F., Lefebre, C., LiWan Po A., Li, L., Roberts, I., Schierhout, G.) Human albumin solution for resuscitation and volume expansion in critically ill patients. (Cochrane Review) In: The Cochrane Library, Issue 2,2004, Chichester, U.K.: John Wiley & Sons, Ltd.
20- Alderson, P., Shierhout G., Robert, I., Bunn, F., Colloids versus crystalloids for fluids resuscitation in critically ill patients (Cochrane Review) In: The Cochrane Library Issue 2, 2004, Chichester, U.K.: John Wiley & Sons, Ltd.
21- Bunn, F., Alderson, P., Hawkins, V.: Colloid solutions for fluid resuscitation (Cochrane Review). In: the Cochrane Library, Issue 2, 2004. Chichester, U,K: John Wiley & Sons, Ltd.
22- Choi, P.T., Yip, G., Quiñonez, L.G., et al: Crystalloids VS Colloids in fluid resuscitation: a systemic review. Crit Care Med, 27: 200, 1999.
23- Wilkes, M.M., Navickis, R.J.: Patients survival after human albumin administration: A metaanalysis of randomized, controlled trials. Ann Intern Med, 135: 149, 2001.
24- Finfer, S., et al: SAFE Study Investigators: A comparison of albumin and saline for fluid resuscitation in the Intensive Care Unit N Eng J Med 350: 2247, 2004.
25- Vincent, J.L., Navickis, R.J.,Wilkes, M.M.: Morbidity in hospitalized patients receiving human albumin: a meta-analysis of randomized controlled trials. Crit Care Med,32(10): 2029,2004.
26- Mora, R., La albúmina. En: Soporte Nutricional Especial. Mora, R. (ed.) Editorial Médica Panamericana. Bogotá. Tercera Edición. 2002. pp. 110-117.
27- Powers, K.A., Capuz, A., Khadaroo, R.G., et al: Twenty five percent albumin prevents lung injury following shock/ resuscitation. Crit Care Med, 31 (9): 2355,2003.
28- Quinlan, G.J., Mumby, S., Martin, G.S., et al: Albumin influences total plasma antioxidant capacity favorably in patientes with acute lung injury. Crit Care Med, 32(3): 755, 2004.
29- Morissette, W., Weil, H.W., Shubin, H.,: Reduction in colloid osmotic pressure associated with fatal progression of cardio pulmonary failure. Crit. Care Med, 3:115, 1975.
30- Vincent, J.L., Dubois, M.J., Navickis, R,J., Wilkes, M.M.: Hypoalbuminemia in acute illness: is there a rationale for intervention?: A meta-analysis of cohort studies and controlled trials. Ann Surg, 237(3): 319,2003.
31- Fliser, D., Zurbruggen, I., Mustchler, E., et al: Coadministration of albumin and furosemide in patients with the nephrotic. Kidney Int, 55:629, 1999.
32- Chalasani, N.,Gorsky, J.C.,Horlander, J.C.,et al: Effects of albumin/furosemide mixtures on responses to furosemide in hypoalbuminemic patients J Am Soc Nephrol, 12:1010, 2001.
33- Ginés, O., Cárdenas, A., Arroyo, V., Rodás, J.: Management of cirrhosis and ascites. N. Eng J Med, 350(16): 1646, 2004.
34- Ginés, O., Tito, L., Arroyo. V., et al: Randomized comparative study of therapeutic paracentesis with and without intravenous albumin in cirrhosis. Gastroenterology, 94: 1493-1502, 1988.
35- Ginés, A., Fernández _ Esparrach, G., Monescillo A., et al: Randomized trial comparing albumin, dextran 70, and polygeline in cirrhotic patients with ascites treated by paracentesis. Gastroenterology, 111: 1002, 1996.
36- Salerno, F., Badalamenti, S., Lorenzo, E., Moser, P., Incerti, P.: Randomized comparative study of hemaccel versus albumin infusion after total paracentesis in cirrhotic patients with refractary ascitis. Hepatology, 13: 707, 1991.
37- Fassio, E. ,Terg, R., Landeira, G., et al: Paracentesis with dextran 70 vesus paracentesis with albumin in cirrhosis with tense ascites: results of a randomized study. J. Hepatol, 14: 310, 1992.
38- Duvoux , C., Zanditenas, D., Hezode, C., et al;: Effects of noradrenalin and albumin in pacients with type I hepatorenal sndrome. A pilot study. Hepatology, 36: 374. 2002.
39- Angeli, P., Volpin, R., Gerunda, G., et al.: Reversal of type 1 hepatorenal syndrome with de administration of midorine and octreotide. Hepatology, 29: 1690. 1999.
40- Uriz, J., Ginés, P., Cárdenas, A., et al. :Terlipressin plus albumin infusión: an effective and safe therapy of hepatorenal syndrome. J Hepatol;33:43. 2000.
41- Moreau, R., Durand ,F., Poyrand, T., et al.;: Terlipressin in patients with cirrhosis and type 1 hepatorenal syndrome: a retrospective multicenter study. Gastroenterology, 122: 923. 2002.
42- Mulkay, J.P., Louis, H., Donckier, V., et al.;: Long-term terlipressin administration improves renal function in cirrhotic patients with type 1 hepatorrenal syndrome: a pilot study. Acta Gastroenterol Belg, 64: 15. 2001.
43- Ortega ,R., Ginés, P., Uriz ,J., et al. :Terlipressin therapy with and without albumin for patients with hepatorenal syndrome: results of a prospective, nonrandomized study. Hepatology, 36: 941. 2002.
44- Kaplan, A.A.,: Towards a rational prescription of plasma exchange: the kinetics of immunoglobulin removal. Semin Dial , 5:227, 1992.
45- Gurland, H.J.,, Lysaght, M.H.,, Samtleben ,W.,, Schmidt, B.A.: Comparison of centrifugal and membrane base apheresis fomats. Int J Artif. Organs, 7:35; 1984.
46- Tabor, E.: The epidemiology of virus transmission by plasma derivatives clinical studies verifying the lack of transmission of hepatic B and C viruses and HIV type I. Transfusion, 39:1160, 1999.
47- Mokrzycki, M.H., Kaplan, A.A.: Therapeutic plasma exchange: complications and management.Am Kidney Dis,23:817.1994.
48- Rivers, E., et al: Early goal- directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med, 345 (19): 1368, 2001.
49- Elliot, D.C.: An evaluation of the end points of resucitation. J Am Coll Surg, 187: 5, 1998.
50- Dellinger, R.P., et al: Surviving Sepsis Campaign guidelines for management of severe sepsis and septic shock. Crit Care Med, 32(3): 858, 2004.
51- Sakka, S.G., et al: Prognostic value of extravascular lung water in critically ill patients. Chest, 122: 2080, 2002.
52- Foland, J.A., et al: Fluid overload before continuous hemofiltration and survival in critically ill children: A retrospective analysis. Crit Care Med ,32: 1771, 2004.
53- Mitchell, J.P., et al: Improved outcome based on fluid management in critically ill patients requiring pulmonary artery catheterization. Ann Rev Respir Dis, 145: 990, 1992.
54- Connors, A.F., et al: The effectiveness of right heart catheterization in the initial care of critically ill patientes. JAMA, 276: 889, 1996.
55- Sandham, J.D., et al: A randomized controlled trial of the use of pulmonary artery catheters in high-risk surgical patients. N Engl J Med, 348: 5, 2003.
56- Richard, C., et al: For the French Pulmonary Artery Catheter Study Group: Early Use of the Pulmonary Artery Catheter and Outcomes in Patients with Shock and Acute Respiratory Distress Syndrome: A Randomized Controlled Trial. JAMA, 290 (20): 2713, 2003.
57- Martin. G.S., et al. Findings on the portable chest radiograph correlate with the fluid balance in critically ill patients. Chest, 122: 2087, 2002.
58- Moore, F.A., More, E.E.: Trauma resuscitation. In: Wilmore, D.W, et al (eds) American College of Surgeons. ACS Surgery. New York: Web MD Corporation, 2002, pp. 31-37.
59- Moore, F.A., et al: The next generation in shock resuscitation. Lancet, 363: 1988, 2004.
60- Healey, M.A., et al: Lactated Ringer's is superior to normal saline in a model of massive hemorrhage and resuscitation. J. Trauma, 45: 894, 1998.
61- Sims, C.A., et al: Ringer's ethyl pyruvate solution ameliorates isquemia/ reperfusion-induced intestinal mucosal injury in rats. Crit Care Med, 29: 1513, 2001.
62- Bickell, W.H., et al: Immediate versus delayed fluid resuscitation for hypotensive patients with penetrating torso injuries. N Engl J Med, 331:1105, 1994.
63- Kwan, I., et al: Timing and volume of fluid administration for patients with bleeding. Cochrane Database Syst Reo 3: CD 002245, 2003.
64- McKinley, B.A., et al: Goal- oriented shock resuscitation for mayor torso trauma: what are we learning. Curr Opin Crit Care, 9(4): 292, 2003.
65- McKinley, B.A., et al: Normal versus supranormal oxygen delivery goals in shock resuscitation: the response is the same. J. Trauma, 53(5): 825, 2002.
66- Skilman, J.J., et al: Randomized trial of albumin vs electrolyte solutions during abdominal aortic operations. Surgery, 78: 291, 1975.
67- Holcroft, J.W., et al: Extravascular lung water following hemorrhagic shock en the baboon: comparison between resuscitation with Ringer's lactate and plasmanate. Ann Surg, 180: 408, 1974.
68- Velanovich, V.: Crystalloid versus collois fluid resuscitation: a meta analysis of mortality. Surgery, 105: 65, 1989.
69- Schierhout, G., et al: Fluid resuscitation with colloid or crystalloid solutions in critically ill patients: a systematic review of randomised trials. BMJ, 316: 961, 1998.
70- Wade, C.E., et al: Efficacy of hypertonic 7.5% saline and 6% dextran- 70 in treating trauma: a meta-analysis of controlled clinical studies. Surgery, 122: 609, 1997.
71- Wade, C.E., et al: Individual patient cohort analysis of the efficacy of hipertonic saline/dextran in patients with traumatic brain injury and hypotension J. Trauma, 42 (5 suppl): S 61, 1997.
72- Papadopoulos, M.C., Krishna, S., Verkman ,A.S. : Aquaporin Water Channels and Brain Edema. Mount Sinai J. Medicine, 69(4):242,2002.
73- Marmarou ,A., Fatouros , P.P., Barzo, P., Portella, G., Yoshihara, M., Tsuji, O., Yamamoto, T., Laine, F., Signoretti, S., Ward, J.D., Bullock, M.R., Young, H.F.: Contribution of edema and cerebral blood volume to traumatic brain swelling in head-injured patients. J Neurosurg, 93(2):183,2000.
74- American Association of Neurological Surgeons _ Brain Trauma Foundation. Estabilización de la presión arterial y oxigenación, en Guías para el manejo y pronóstico del trauma craneoencefálico severo, traducido por la Fundación Colombiana para el Manejo del Trauma Cerebral. Cali 2003, p 37 a 49.
75- Zornow, M.H., Prough, D.S.: Fluid management in patients with traumatic brain 76-Trevisani, G.T., Shackford ,S.R., Zhuang, J., Schmoker, J.D.: Brain edema formation after brain injury, shock, and resuscitation: effects of venous and arterial pressure. J Trauma,37(3):452, 1994.
76- Ramming, S., Shackford, S.R., Zhuang, J., Schmoker, J.D. : The relationship of fluid balance and sodium administration to cerebral edema formation and intracranial pressure in a porcine model of brain injury. J Trauma, 37(5):705, 1994.
77- Barzo ,P., Marmarou, A., Fatouros, P., Corwin, F., Dunbar ,J. : Magnetic resonance imaging-monitored acute blood-brain barrier changes in experimental traumatic brain injury. J Neurosurg, 85(6):1113,1996.
78- Shapira ,Y., Artru, A.A., Qassam, N., Navot, N., Vald, U. : Brain edema and neurologic status with rapid infusion of 0.9% saline or 5% dextrose after head trauma. J Neurosurg Anesthesiol, 7(1):17,1995.
79- Talmor, D., Shapira ,Y., Artru ,A.A., Gurevich, B., Merkind, V., Katchko, L., Reichenthal, E.: 0.45% saline and 5% dextrose in water, but not 0.9% saline or 5% dextrose in 0.9% saline, worsen brain edema two hours after closed head trauma in rats. Anesth Analg, 86(6):1225,1998.
80- Shackford, S.R., Walsh ,J.C., Davis, J.W. : The effects of aortic crossclamping and resuscitation on intracranial pressure, cerebral blood flow, and cerebral water content in a model of focal brain injury and hemorrhagic shock. J Trauma, 30(7):768-74; discussion 774-5,1990.
81- Beaumont, A., Hayasaki, K., Marmarou, A., Barzo, P., Fatouros, P., Corwin, F.: Contrasting effects of dopamine therapy in experimental brain injury. J Neurotrauma, 18(12):1359,2001.
82- Alspaugh, D.M., Sartorelli, K., Shackford ,S.R., Okum, E.J., Buckingham, S., Osler ,T.: Prehospital resuscitation with phenylephrine in uncontrolled hemorrhagic shock and brain injury. J Trauma , 48(5):851,2000.
83- Cuypers, J., Matakas, F., Potolicchio ,S.J. Jr. : Effect of central venous pressure on brain tissue pressure and brain volume. J Neurosurg, 45(1):89,1976.
84- Hariri, R.J., Firlick, A.D., Shepard ,S.R., Cohen, D.S., Barie ,P.S., Emery, J.M .3rd, Ghajar ,J.B.: Traumatic brain injury, hemorrhagic shock, and fluid resuscitation: effects on intracranial pressure and brain compliance. J Neurosurg, 79(3):421,1993.
85- Bourguignon, P.R., Shackford, S.R., Shiffer, C., Nichols, P., Nees ,A.V. : Delayed fluid resuscitation of head injury and uncontrolled hemorrhagic shock. Arch Surg,133(4):390, 1998.
86- Novak, L., Shackford, S.R., Bourguignon, P., Nichols, P., Buckingham, S., Osler, T., Sartorelli, K.: Comparison of standard and alternative prehospital resuscitation in uncontrolled hemorrhagic shock and head injury. J Trauma, 47(5):834,1999.
87- Schmoker, J.D., Zhuang, J., Shackford, S.R.: Hemorrhagic hypotension after brain injury causes an early and sustained reduction in cerebral oxygen delivery despite normalization of systemic oxygen delivery. J Trauma, 32(6):714-20; discussion 721-2,1992.
88- Anderson, J.T., Wisner ,D.H., Sullivan, P.E., Matteucci, M., Freshman, S., Hildreth, J., Wagner, F.C .Jr. : Initial small-volume hypertonic resuscitation of shock and brain injury: short- and long-term effects. J Trauma, 42(4):592-600; discussion 600-1,1997.
89- Shackford, S.R., Zhuang, J., Schmoker, J.: Intravenous fluid tonicity: effect on intracranial pressure, cerebral blood flow, and cerebral oxygen delivery in focal brain injury. J Neurosurg, 76(1):91, 1992.
90- Zhuang, J., Shackford, S.R., Schmoker, J.D., Pietropaoli, J.A. Jr.: Colloid infusion after brain injury: effect on intracranial pressure, cerebral blood flow, and oxygen delivery. Crit Care Med, 23(1):140,1995.
91- Tranmer, B.I., Iacobacci, R.I., Kindt ,G.W.: Effects of crystalloid and colloid infusions on intracranial pressure and computerized electroencephalographic data in dogs with vasogenic brain edema. Neurosurgery, 25(2):173-8; discussion 178-9. 1989.
92- Bouma ,G.J., Muizelaar, J.P., Fatouros, P. : Pathogenesis of traumatic brain swelling: role of cerebral blood volume. Acta Neurochir Suppl (Wien), 71:272, 1998.
93- Scalea, T.M., Maltz, S., Yelon, J., Trooskin, S.Z., Duncan, A.O., Sclafani, S.J.: Resuscitation of multiple trauma and head Injury: role of crystalloid fluids and inotropes. Crit Care Med, 22:1610, 1994.
94- York, J., Arrillaga, A., Graham, R., Miller, R.: Fluid resuscitation of patients with multiple injuries and severe closed head injury: experience with an aggressive fluid resuscitation strategy. J Trauma, 48(3):376-9; discussion 379,2000.
95- Clifton, G.L., Miller, E.R., Choi, S.C., Levin ,H.S.: Fluid thresholds and outcome from severe brain injury. Crit Care Med, 30(4):739, 2002.
96- Young ,J.S., Meredith, J.W.: Does oxygen delivery-directed resuscitation worsen outcome of head injured patients with multisystem injuries? Am Surg, 61(5): 419,1995.
97- Saltarini, M., Massarutti, D., Baldassarre, M., Nardi, G., De Colle ,C., Fabris, G.;: Determination of cerebral water content by magnetic resonance imaging after small volume infusion of 18% hypertonic saline solution in a patient with refractory intracranial hypertension. Eur J Emerg Med, 9(3):262,2002.
98- Cooper, D.J., Myles ,P.S., McDermott, F.T., Murray ,L.J., Laidlaw, J., Cooper, G., Tremayne, A.B., Bernard, S.S., Ponsford ,J.: Prehospital Hypertonic Saline Resuscitation of Patients With Hypotension and Severe Traumatic Brain Injury A Randomized Controlled Trial. JAMA, 291:1350,2004.
99- Carreira, F., Anderson, R.J: Assessing metabolic acidosis in the intensive care unit: does the method make a difference? (Editorials) Crit Care Med, 32 (5): 1227, 2004.
100- Levraut, J., Grimaud, D.: Treatment of metabolic acidosis. Current Opinion in Critical Care, 9 (4): 260, 2003.
101- Mullins, R.J. Fluids, Electrolytes and Shock. In: Sabiston Textbook of Surgery. The biological basis of modern surgical practice. Sixteenth Edition. Townsend, Courtney, M,. et al (eds) W.B. Saunders Company. Philadelphia, 2001. pp. 45-67.
102- Ince, C.: Microcirculation in distress: A new resuscitation end point? Crit Care Med, 32(9): 1963, 2004.
103- Vincent, J.L: Hemodynamic support in septic shock. Intensive Care Med. 27 (Suppl 1): S80,2001.
104- Piagnerelli, M., Boudjeltia, K.Z., Vanhaeverbeek, M. et al: Red blood cell rheology in sepsis. Intensive Care Med, 29: 1052, 2003.
105- Groerneveld, A.B., van Lambalgen, A.A., van den Bos, G.C., et al: Maldistribution of heterogeneous coronary blood flow during canine endotoxin shock. Cardiovas Res, 25: 80, 1991.
106- Ince, C. Sinoasappel, M.: Microcirculatory oxygenation and shunting in sepsis and shock. Crit Care Med, 27: 1369, 1999.
107- De Backer, D., Creteur, J., Preiser, J.C., et al: Microvascular blood flow is altered in patients with sepsis. Am J Respir Crit Care Med, 166:98, 2002.
108- Spronk, P.E., Ince, C., Gardien, M.J., et al: Nitroglycerin in septic shock after intravascular volume resuscitation. Lancet, 360: 1395, 2002.
109- Sakr, Y., Dubois, M-J., De Baker, D., et al: Persistent microcirculatory alterations are associated with organ failure and death in patients with septic shock. Crit Care Med, 32: 1825, 2004.
110- Halkerston, I.D.K.: Oxidative phosphorylation. In: Biochemistry. Halkerston, I.D.K .(ed). John Wiley & Sons. New York, 1984. pp. 195-204.
111- Halkerston, I.D.K.: Glycolysis. In: Biochemistry. Halkerston, I.D.K. (ed) John Wiley & Sons. New York, 1984 pp. 165-174.
112- Mizock, B.A.: Significance of hyperlactatemia without acidosis during hypermetabolic stress. Crit Care Med, 25 (11): 1780, 1997.
113- Suistoma, M., Roukonen, E., Kari, A., Takala, J.: Time-pattern of lactate and lactate to pyruvate ratio in the first 24 hours of intensive care emergency admissions. Shock, 14 (1): 8, 2000.
114- De Backer, D.: Lactic acidosis. Minerva Anestesiologica, 69 (4): 281, 2003.
115- Rufolo, D.C., Headley, J: Regional Carbon Dioxide Monitoring: A different look a tissue perfusion. AACN Clinical Issues, 14 (2): 168, 2003.
116- Scalea, T.M., Holman, M., Fuortes, M. et al: Central venous blood oxygen saturation: an early accurate meassurement of volume status during hemorrhage. J.Trauma, 28: 725, 1988.
117- Ceppa, E.P., Fuh, K.C., Bulkley, G.B.: Mesenteric hemodynamic response to circulatory shock. Current Opinions in Critical Care, 9(2): 127, 2003.
118- Stephan, M.J. :Clinical review: Splanchnic ischaemia. Crit Care, 6(4): 306, 2002.
119- Boswell, Sh.A, Sealea, T.M.: Sublingual Capnometry: An alternative to gastric tonometry for the management of shock resuscitation. AACN Clinical Issues. 14(2): 176, 2003.
120- Marik, P.E., Bankov, A.: Sublingual Capnometry versus traditional markers of tissue oxygenation in critically il patients. Crit Care Med, 31: 818, 2003.
121- Hameed, S.M., Cohn, S.M.: Gastric tonometry: The role of mucosal PH measurement in the management of trauma. Chest, 123(5) supplement: 475 S, 2003.
122- Brealey, D., Brand, M., Hargreaves, I., et al: Association between mitochondrial dysfunction and severity and outcome of septic shock. Lancet, 360: 219,2002.
123- Fink, M.P.: Bench to bedside review: Cytopathic hipoxia. Crit Care, 6: 491, 2002.
124- Doglio, G., Pusajo, J., Egurrola, M. et al: Gastric mucosal PH as a prognostic index of mortality in critically ill patients. Crit Care Med, 19: 1037, 1991.
125- Gutiérrez, G., Bismar, H., Dantzker, D.R., et al;: Comparison of gastric intramucosal pH with measures of oxygen transport and consumption in critically ill patients. Crit Care Med, 20: 451,1992.
126- Maynard, N., Bihari, D., Beale, R., et al;: Assessment of splanchnic oxygenation by gastric tonometry in patients with acute circulatory failure. JAMA, 270: 1203,1993.
127- Ivatury ,R.R., Simon, R.J., Havriliak, D., et al;: Gastric mucosal pH and oxygen delivery and oxygen consumption indices in the assessment of adequacy of resuscitation after trauma: a prospective, randomized study. J. Trauma, 39:128,1995.
128- Ivatury, R.R., Simon, R.J., Islam, et al;: A prospective randomized study of end points of resuscitation after major trauma: global oxygen transport indices versus organ-specific gastric mucosal pH. J Am Coll Surg, 183: 145,1996.
129- Creteur, J., De Backer, D., Vincent, J.L: Does gastric tonometry monitor splanchnic perfusion? Crit Care Med, 27 (11) 2480, 1999.
130- Weil, M.H., Nakagawa,Y., Tang, W., et al;: Sublingual capnometry: a new noninvasive measurement for diagnosis and quantitation of severity of circulatory shock. Crit Care Med, 27: 1225,1999.
131- Marik, P.E.: Sublingual capnography: a clinical validation study. Chest, 120: 923, 2001.
132- Baron, B.J., Sinert, R., Zehtabchi, et al;: Diagnostic utility of sublingual PCO2 for detecting hemorrhage in patients with penetrating trauma. Acad Emerg Med, 9:492,2002.
133- Matura, K.R.,Vollebregt, K.C., et al: Comparison of OPS imaging and conventional microscopy to study the human microcirculation. J Appl Physiol, 91:74,2001.
134- Advanced Trauma Life Support. American Collage of Surgeons. Committee on Trauma. Instructor Course Manual. 6ª ed. Chicago; 1995: 97 -117.
135- htp:// usuarios.lycos.es/urgenhospitalarias/ProtocolosEmerg/1-plt.pdf 13/VII/2004.
136- Arrighi, D.A., Farnell, M.B., Mucha, P.Jr, Iistrup, D.M., Anderson ,D.L.: Prospective, randomized trial of rapid venous access for patients in hypovolemic shock. Ann Emerg Med , 18(9): 927, 1989.
137- Scalea, T.M., Sinert ,R., Duncan, A.O., Rice, P., Austin, R., Kohl, Trooskin, S., Talbert, S.: Percutaneous central venous access for resuscitation in trauma. Acad Emerg Med , 16: 525, 1994.
138- Pappas, P., Brathwaite ,C.E., Ross, S. E.: Central venous catheterization during resuscitation of trauma patients. Am Surg , 58: 108, 1992.
139- Emerman, C.L., Betton, E.M., Lukens, T.W., May, T.E., Effron, D.: A prospective study of femoral versus subclavian vein catheterization during cardiac arrest. Ann Emerg Med ,19: 26, 1990.
140- Westfall, M.D., Price, K.R., Lambert ,M., Himmelman, R., Kacey, D., Dorovitcht ,S., Mathews, J.: Intravenous access in the critically ill trauma patient: a multicentered, prospective, randomized trial of saphenous cutdown and percutaneous femoral access. Ann Emerg Med , 23(3): 541, 1994.
141- Mansfield, P.F., Hohn, D.C., Fornage, B., Gregurich, M.A., Ota, D.M.: Complicationes and failures of subclavian-vein catheterization. N Engl J Med 331: 1.735, 1994.
142- Merrer, J., De Jonghe, B., Golliot, F., Lefran, J., Raffy, B., Barre, E., et al: Complications of femoral and subclavian venous catheterization in critically ill patients: A randomized controlled trial. JAMA , 286(6): 700, 2001.
143- Trottier ,S.J., Veremakis, C., O,Brien, J., Auer, A.I.: Femoral deep vein thrombosis associated with central venous catheterization: results from a prospective, randomized trial. Crit Care Med , 23(1): 52, 1995.
144- Joynt, G.M., Kew, J., Gomersall, C.D., Leung ,V.Y., Liu, E.K.: Deep´venous thrombosis caused by femoral venous catheters in critically ill adult patients. Chest,117(1): 178, 2000.
145- Randolph, A.G., Cook, D.J., González, C.A., Pribble, C.G., et al: Ultrasound guidance for placement of central venous catheters: a meta-analysis of the literaure. Crit Care Med ,24 (12): 2053, 1996.
146- Mind. D., et al: Ultrasound locating devices for central venous cannulation: meta-analysis BJM, 327:361, 2003.
147. Pickering, T.G.: Principles and techniques of blood pressure measurement. Cardiol Clin , 20:207, 2002.
148. Reeves ,R.A.: Does this patient have hypertension?: How to Measure Blood Pressure. JAMA , 273:1211, 1995.
159. Davis, R.F.: Clinical comparison of automated auscultatory and oscillometric and catheter-transducer measurements of arterial pressure. J Clin Monit , 1:114,1985.
151. Gordeau, M., Martin, R., Lamarche ,Y., Tetreault ,L.: Oscillometry and direct blood pressure: a comparative clinical study during deliberate hypotension. Can Anaesth Soc J , 33:300,1986.
152. McGee, S., Abernethy ,W.B. 3rd, Simel, D.L.: The rational clinical examination. Is this patient hypovolemic? JAMA , 281:1022,1999.
153. Demetriades, D., Chan, L.S., Bhasin, P., Berne ,T.V., Ramicone ,E., Huicochea ,F., Velmahos, G., Cornwell, E.E., Belzberg, H., Murray, J., Asensio, J.A. :Relative bradycardia in patients with traumatic hypotension. J Trauma , 45:534,1998.
154. Victorino, G.P., Battistella, F.D., Wisner, D.H.: Does tachycardia correlate with hypotension after trauma? J Am Coll Surg , 196:679,2003.
155. Schriger, D.L., Baraff, L. :Defining normal capillary refill: variation with age, sex, and temperature. Ann Emerg Med , 17:932, 1988.
156. Schriger, D.L., Baraff, L.: Capilary refill: is it a useful predictor of hypovolemic states? Ann Emerg Med , 20:601,1991.
157. Tibby, S.M., Hatherill, M., Murdoch ,I.A.: Capillary refill and core-peripheral temperature gap as indicators of haemodynamic status in paediatric intensive care patients. Arch Dis Child ,80:163,1999.
158. Pamba, A., Maitland, K.: Capillary refill: prognostic value in Kenyan children. Arch Dis Child , 89:950,2004.
159. Leonard ,P.A., Beattie ,T.F. : Is measurement of capillary refill time useful as part of the initial assessment of children?[. Eur J Emerg Med , 11:158,2004.
160. Champion, H.R., Sacco, W.J., Copes, W.: A revision of the trauma score. J Trauma , 29:623,1989.
161. Celoria ,G., Steingrub, J.S., Vickers-Lahti ,M., Teres, D., Stein, K.L., Fink, M., Friedmann, P.: Clinical assessment of hemodynamic values in two surgical intensive care units. Effects on therapy. Arch Surg , 125:1036, 1990. v
162. Shoemaker, W.C., Appel, P.L., Kran, H.: Physiologic patterns in surviving and nonsurviving shock patients. Arch Surg , 106:630, 1973.
163. Abou-Khalil, B., Scalea ,T.M., Trooskin, S.Z.: Hemodynamic responses to shock in young trauma patients: Need for invasive monitoring. Crit Care Med, 22:633, 1994.
164. Dutton, R.P., Mackenzie ,C.F., Scalea ,T.M.: Hypotensive resuscitation during active hemorrhage: impact on in-hospital mortality. J Trauma ,53:7,2002.
165. Oliveros , H.,Dennis, R., Rodríguez, N.: Cálculo de aniones no medibles como predictor de disfunción orgánica múltiple. Acta Colombiana de Cuidado Intensivo , 6(2): 129, 2003.













