Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.36 no.1 Bogotá Jan./Mar. 2008
ARTÍCULO DE INVESTIGACIÓN CLÍNICA
Analgesia preventiva en mujeres programadaspara esterilización definitiva con electrofulguración de trompas uterinas por laparoscopia
Experimento clínico controlado, aleatorizado, con doble enmascaramiento
J. Ricardo Navarro1, Gabriel Barragán2, David A. Rincón3, Javier H. Eslava4
1 MD. Anestesiólogo. Presidente de la Sociedad Cundinamarquesa de Anestesiología (SCA), Miembro del Comité de Reanimación de la Sociedad Colombiana de Anestesiología y Reanimación (SCARE). Profesor Asociado. jrnavarrov@unal.edu.co2 Interno Especial de Anestesiología. gbarraganb@unal.edu.co
3 MD Anestesiólogo.
4 MD Anestesiólogo. Maestría en Dirección Universitaria y en Epidemiología Clínica. PhD en Salud Pública. Profesor Asociado. Universidad Nacional de Colombia. Unidad de Anestesiología y Reanimación, Departamento de Cirugía, Facultad de Medicina.
Recibido para publicación marzo 28 de 2008, Aceptado para publicación abril 9 de 2008.
RESUMEN
Antecedentes: La analgesia preventiva continúa siendo fuente de discusión y desacuerdo entre los especialistas que manejan el dolor. Hay resultados contradictorios, incluidos algunos metaanálisis, sobre la efectividad de la analgesia preventiva con ketamina.
Objetivo: Evaluar la eficacia de la ketamina preventiva en la cirugía ambulatoria de mujeres programadas para esterilización definitiva con electrofulguración por laparoscopia, en la disminución del dolor postoperatorio, comparada contra ketamina administrada de manera no preventiva.
materiales y métodos: Entre diciembre de 2007 y enero de 2008 se incluyeron 130 mujeres de la Clínica Piloto de Profamilia, en Bogotá (Colombia), que deseaban planificar mediante ligadura de trompas. Fueron asignadas de manera aleatoria simple a dos grupos: a 71 pacientes se les administró ketamina antes de la incisión quirúrgica (0.25 mg/kg) y a 59 pacientes se les administró ketamina a la misma dosis al fnal del procedimiento. La administración de ketamina y la evaluación de los desenlaces se realizaron de manera enmascarada.
Resultados: El nivel de dolor medido mediante la Escala Visual Análoga (EVA) fue similar para ambos grupos, aunque hubo una mayor proporción de pacientes con dolor al minuto 15 en el grupo de ketamina preventiva (19.7% vs. 6.8%, p=0.03). El grupo de ketamina no preventiva presentó más náusea (15% vs 10%) y mareo (46% vs. 37%), aunque esto no fue significativo (p>0,05)
Conclusión: La eficacia de la ketamina preventiva para el alivio del dolor postoperatorio no fue diferenre a la de la ketamina no preventiva.
Palabras Clave: Analgesia Preventiva, Ketamina, Ligadura de Trompas, Cirugía por Laparoscopia.
SUMMARY
Background: The pre-emptive analgesia keeps being a source of discussion and discord between the spe-cialists in the pain management. There are contradictory results, even in meta-analysis, about effectiveness of preemptive analgesia with ketamine.
Objective: To evaluate effectiveness of ketamine as preemptive analgesia in women under laparoscopic electrofulguration of Falopio tubes, in control of postoperative pain, compared with ketamine administered in a non preemptive way.
material and methods: 130 women who wanted a defnitive contraceptive method as laparoscopic tubal ligation were included with the diagnosis of satisfed parity, from the Clínica Piloto de Profamilia, in Bogotá (Colombia), between december 2007 and january o2008. They were randomly assigned in two groups: 71 received preemptive ketamine (before initiating the surgical procedure, dose of 0,25 mg/kg) and the other 59 patients received ketamine, the same doses, at the end of the procedure. Both, administration of ketamine and evaluation of patients outcomes, were made in blinded form.
Results: Patients were similar at the start of the study. The level of pain measured with a visual analog scale (VAS) was similar for both groups, there was a higher proportion of patients with pain in the preemp-tive ketamine group to the minute 15 (29.7% vs 6.8%) Ketamine non preemptive group, felt more nauseous (25% vs. 10% and seasickness (46% vs 37%), this was not signifcative (p>0.05)).
Conclusions: The preemptive ketamine wasnt different in effectiveness to ketamine administered in non preemptive way for the relief of postoperative pain.
Key words: Preemptive Analgesia, Ketamine, Laparoscopic Tubal Ligation.
INTRODUCCIÓN
La analgesia preventiva (que en inglés se refere como preemptive analgesia) es un concepto reciente que comprende la aplicación de un régimen analgésico antes del estímulo quirúrgico, con el objetivo de prevenir la sensibilización central y periférica causada inicialmente por la incisión quirúrgica y posteriormente por la lesión infamatoria, en forma amplifcada1-3. A diferencia de la analgesia anticipada (en inglés preventive), que busca asegurar niveles óptimos de un analgésico antes de que se presente el dolor, la analgesia preventiva como dice su nombre, previene y reduce el desarrollo de una memoria del estímulo doloroso en el sistema nervioso central, obteniendo una disminución de los requerimientos de analgésicos en el postoperatorio con menores efectos colaterales y de esta forma se evita la presencia del dolor patológico como hipe-ralgesia, alodinia e hiperpatía4,5.
La ketamina a través de los años ha probado ser además de un agente anestésico, un medicamento analgésico potente. Sin embargo, sus efectos colaterales (especialmente la disociación córtico-límbica) y la aparición de nuevos medicamentos, en teoría más seguros, han sido determinantes en relegarlo a un puesto secundario en la actualidad6,7.
Son múltiples los sitios de interacción de la ketamina: receptores N-metil-D-aspartato (NMDA), receptores glutamato no NMDA, receptores colinérgicos y muscarínicos, receptores de opioides y monoaminérgicos y además interacciones con iones de canales voltaje-dependientes tales como calcio tipo L y canales de sodio8-12. Todas estas interacciones hacen parte del espectro clínico y farmacológico de la ketamina, sin embargo el antagonismo sobre el receptor NMDA juega el papel principal en sus efectos de analgesia preventiva.
El objetivo de este estudio se dirige a evaluar si la ketamina tiene efecto analgésico preventivo en cirugía de trompas uterinas por vía laparoscópica, cuando se compara con la administración de ketamina a dosis similares, al fnal del procedimiento quirúrgico.
MÉTODOS
Este estudio fue aprobado por el comité de investigaciones de la Unidad de Anestesiología y Reanimación del Departamento de Cirugía de La Facultad de Medicina de la Universidad Nacional de Colombia, por la Dirección Médica de Profamilia y por el Comité de Ética de la Clínica Piloto de Profamilia en Bogotá (Colombia). Se obtuvo consentimiento informado de cada una de las pacientes.
Antes del procedimiento quirúrgico se explicó en detalle el objetivo del estudio, teniendo en cuenta la colaboración de las pacientes para responder a las preguntas en el postoperatorio sobre dolor (Escala Visual Análoga (EVA)), y demás síntomas que pudieran presentar.
Se trató de un experimento, doble ciego, controlado y aleatorizado, en el cual los criterios de inclusión utilizados fueron las pacientes en edad fértil con paridad satisfecha, con prueba de embarazo negativa reciente que deseaban ser llevadas a técnica defnitiva de esterilidad por medio de la ligadura de trompas con técnica de laparoscopia; con clasifcación de ASA I o II, quienes frmaron el consentimiento informado y aceptaron entrar a la investigación.
Se excluyeron pacientes que no aceptaron entrar en el protocolo de investigación; que presentaban alergias conocidas a alguno de los medicamentos utilizados en el protocolo de manejo anestésico de Profamilia para este tipo de cirugía por vía laparoscópica. Igualmente, aquellas pacientes con Hipertensión arterial, glaucoma, síndrome convulsivo de cualquier etiología, vértigo e hipertiroidismo.
El método que se llevó a cabo para la realización del estudio consistió en la secuencia protocolaria de información del procedimiento y recomendaciones postoperatorias por parte del personal de enfermería, cuando la paciente estaba con vestido quirúrgico en el área de espera prequirófano; posteriormente, los investigadores reinterrogaron a las pacientes para la lista de chequeo de los criterios de exclusión e inclusión; les explicaron el objetivo del trabajo de investigación, y solicitaron su consentimiento, y luego de firmar que entendían y aceptaban la incorporación al estudio, se realizaba la aleatorización mediante balotas, las cuales estaban numeradas del 1 al 10; los números impares se asignaron al grupo que se le daría ketamina en forma preventiva y los números pares el grupo al cual se le daría ketamina al final del procedimiento. Tanto la paciente como el anestesiólogo de la sala eran ciegos con respecto al grupo asignado por el azar. Un médico diferente del encargado de la paciente en la sala de cirugía, envasaba en forma estéril la mezcla de solución a inyectar, según el grupo asignado, y se la entregaba al anestesiólogo de la sala de cirugía.
Se estimó un tamaño de muestra de 123 pacientes, para encontrar diferencias de 1.6 +/- 3 en la escala visual análoga de dolor, con un error alfa del 5% y un poder del 80%, y unas pérdidas estimadas al seguimiento del 10%
Las pacientes en la sala de de cirugía, se monitorizaron con cardiovisoscopio, oxímetro de pulso, tensiómetro y capnógrafo. Se inició la inducción con meperidina 0.4-0.5 mg/kg (dosis máxima de 25 mg), remifentanil 1 μg/kg y fentanyl 1 μg/kg en una jeringa de 3ml, y propofol 0.7 mg/kg más lidocaina 20 mg como dosis única, en una jeringa de 5ml. Una vez aplicados los medicamentos, se administró de manera enmascarada para el anestesiólogo 0.25 mg/ Kg de ketamina en el grupo de las pacientes aleatorizadas para recibir el fármaco en el estudio de forma preventiva, o solución salina (SSN) para las pacientes que no recibirían la ketamina de forma preventiva. Se aplicó a todas las pacientes como anestésico local preincisional, 5cc de lidocaina al 2% en piel. Todas las pacientes recibieron oxígeno al 100%.
Al final del procedimiento las pacientes que por el azar fueron asignadas a analgesia preventiva recibieron SSN y las demás (grupo de no analgesia preventiva) recibieron 0.25 mg/kg de ketamina intravenosa.
En el postoperatorio se les aplicó analgésicos de acuerdo a la EVA: si ésta refejaba un dolor menor de 6 sobre 10, se aplicaba una ampolla de 20 mg IV de Butil bromuro de hioscina, si el dolor era mayor de 6, se aplicaba tramadol 25 mg IV o diclofenaco 75 mg IM.
En ocasiones además de estos medicamentos si se requería más de una dosis de tramadol (25 mg IV), se aplicaba meperidina 20 mg a 30 mg IV. Una vez la paciente toleraba la vía oral se le administraba acetaminofén 1 g. VO.
En el postoperatorio se cuantifco el dolor con la EVA al minuto 1, 15, 30 y 60. Se tuvieron en cuenta los requerimientos de AINES y opioides. Se realizó una encuesta de satisfacción similar a la programada previamente13, donde se evaluó si presentaron náuseas, vómito, mareo, excitación, disnea, vértigo, etc. y se les preguntó ¿cómo se sentían en la sala de recuperación tardía? y para dar de alta se tuvo en cuenta la escala de recuperación de Aldrete para paciente ambulatorio14.
La base de datos se digitó en Excel® y para el análisis estadístico se utilizó metodología no paramétrica no paramétrica dado que la mayoría de variables no tuvieron distribución normal con la prueba de Shapiro Wilks. Para diferencia de medianas se utilizó la prueba de Mann Whitney y para datos categóricos la prueba de Chi2 y la prueba exacta de Fisher con eventos poco frecuentes. El análisis se realizó con STATA 10.0.
RESULTADOS
Los criterios de inclusión fueron cumplidos por 137 pacientes, de las cuales cuatro se excluyeron por presentar Hipertensión arterial, diagnosticada en la sala de espera pre-quirófanos, ya que habían referido no tener este antecedente en evaluaciones médicas previas. Ninguna paciente rehusó participar en el estudio.
Se realizó la asignación aleatoria en 133 mujeres que deseaban planifcar con el método de ligadura de trompas, de las cuales 72 se asignaron al grupo de ketamina preventiva y 61 pacientes al grupo de analgesia no preventiva. 3 pacientes se excluyeron por infltración de la vena en el momento de la cirugía, 1 paciente asignada a analgesia preventiva y 2 pacientes del grupo de analgesia no preventiva. (Figura 1).

Se realizó el análisis con 71 pacientes del grupo de analgesia preventiva y 59 pacientes del grupo de analgesia no preventiva; no existieron pérdidas de seguimiento de las pacientes mientras se desarrollaba el experimento.
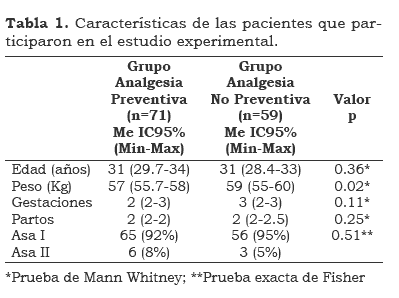
Al evaluar sus características de base (edad, peso, gestaciones, partos y tipo de ASA) no se encontraron diferencias estadísticamente signifcativas entre ambos grupos. (Tabla 1)
Al evaluar el desenlace primario se encontró que el dolor medido mediante la escala EVA fue muy parecido para ambos grupos, dando como resultado que la ketamina preventiva no se diferencia en el manejo del dolor postoperatorio al compararse con la ketamina administrada de forma no preventiva, aunque en el minuto 15 se encontró una mayor proporción de pacientes con dolor en el grupo de analgesia preventiva que en el grupo de analgesia no preventiva (Tabla 2)
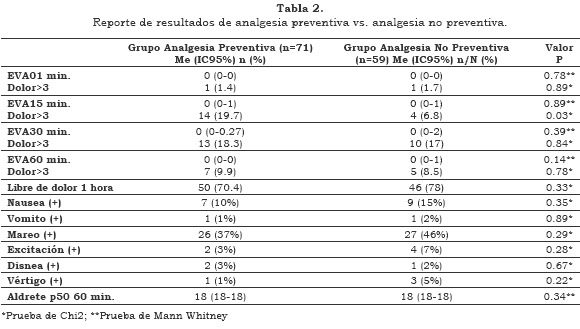
Se evaluaron efectos secundarios como náuseas, vómito, mareo, excitación, disnea y vértigo (Tabla 2); y se encontró que las náuseas se habían presentado un 5% en el grupo de la analgesia no preventiva, al igual que el vómito, con una incidencia del un 1%; el mareo, la exitación y el vértigo estubieron presentes con un 4% mayor en la analgecia no preventiva; por otro lado la apnea observada ocurrió en un 1% en el grupo de analgesia preventiva.
Otra variable que se evaluó fue la escala de recuperación de Aldrete para paciente ambulatoria, la cual se midió al minuto 1, 15, 30 y 60; se encontró que no existía una diferencia estadísticamente signifcativa, y que los valores fueron similares para ambos grupos.
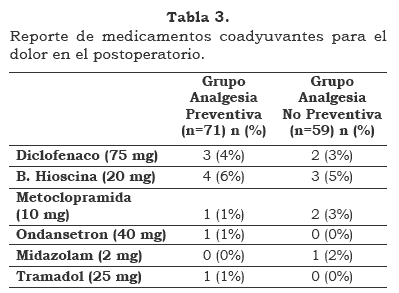
La necesidad de analgésicos postoperatorios se valoró para ambos grupos y se encontró que la dosis de diclofenaco y de Bromuro de hioscina fueron similares desde el punto de vista porcentual; también se observó que hubo una ligera tendencia a usar más metoclopramida en el grupo de analgesia no preventiva dado por una diferencia entre los grupos del 2%. (Tabla 3)
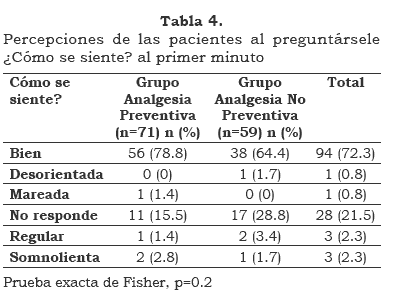
Con respecto a la percepción sensorial del paciente al primer minuto, hubo una mayor proporción de pacientes que no respondieron en el grupo de analgesia no preventiva que en el grupo de analgesia preventiva (Tabla 4). Estas diferencias fueron clínicamente más no estadísticamente diferentes. Al fnal de la hora, todos los pacientes de ambos grupos reportaron sentirse bien.
DISCUSIÓN
El término de analgesia preventiva se popularizó, como una intervención que precede al procedimiento quirúrgico para prevenir o disminuir el dolor posquirúrgico, previniendo la sensibilización central.
Este tipo de sensibilización y la estimulación electrofsiológica repetida a baja frecuencia de las fbras C en la medula espinal, disminuye el umbral de activación neuronal y prolonga las descargas luego de que se produzca un estímulo corto (wind up)18. Estos dos mecanismos dependen de la activación del receptor N-metil-D aspartato (NMDA). Esto en términos sencillos se puede comprender como que existe una memoria en el sistema nervioso central (SNC) que se dispara por la activación del receptor NMDA produciendo hiperalgesia19. De aquí surge la posibilidad clínica de prevenir el dolor posqui-rúrgico, bloqueando estos nociceptores con anestesia epidural (anestésicos locales) o con analgesia epidural (opioides). Experimentos en animales han bloqueado la sensibilización central y el wind up, si se bloquean los nociceptores antes del evento nociceptivo20.
La razón de ser de la técnica anestésica para ligadura de trompas en nuestra institución, es precisamente aplicar estos conceptos traducidos en los tres principios de la analgesia preventiva: 1. Profundidad sufciente para bloquear los estímulos nociceptores. 2. Amplitud sufciente para cubrir (bloquear) el estímulo quirúrgico. 3. Duración suiciente no solo para el acto quirúrgico sino también para el postoperatorio inmediato17,21.
Se inicia con la explicación del procedimiento enfatizando que es ambulatorio, para pacientes de bajo riesgo, de corta duración y realizado por personal con amplia experiencia. Se utiliza anestesia local previo a la incisión quirúrgica y una mezcla que consiste en medicamentos opioides (remifentanil, meperidina), hipnóticos y sedantes (propofol) y un bloqueador de receptores NMDA, como la ketamina en dosis bajas, para evitar efectos colaterales.
La analgesia exclusiva con AINES no brinda sufciente profundidad para bloquear el estímulo nociceptivo. La infltración de anestésico local previo a la incisión no es sufcientemente amplia para cubrir estos estímulos, ya que el trocar del laparoscopio va más allá de la piel. Cuando hay múltiples áreas de inervación, se requiere de dosis adecuadas de opioides sistémicos (o una combinación de ellos)17. La ketamina es anestésico o analgésico según la dosis. No bloquea los impulsos primarios aferentes al tálamo, por lo tanto no tiene acción medular. Su efecto se produce a nivel central y a nivel de dolor talámico. Su acción es supraespinal como un analgésico y se le ha encontrado una acción espinal y supraespinal de agente anti-hiperalgésico22.
El dolor visceral va por vía del nervio vago a la medula e inicia la sensibilización central. Por lo tanto se requiere una combinación de opioides, sedantes y dosis bajas de ketamina endovenosas23 para que actúen a nivel heterosegmental, de esta forma se potencia el efecto de la ketamina y se disminuyen los efectos colaterales de los opioides (sedación profunda, depresión respiratoria). Para que haya una buena analgesia se requiere la administración intermitente (cada 3-5 minutos) de la mezcla si el procedimiento se extiende más allá de los 5 minutos.
Si se aprecia la evaluación de la escala EVA, el efecto analgésico es satisfactorio, sin embargo no hubo diferencias en la percepción al dolor en las pacientes a quienes se les administró ketamina preventivamente respecto a las pacientes a quienes se les administró ketamina en forma no preventiva. Lo anterior se evidencia claramente al comparar los valores que se obtuvieron en ambos grupos según la escala de dolor ya mencionada; de esta manera, la administración de la ketamina antes o después del estímulo quirúrgico se comporta como un analgésico efcaz, lo que está de acuerdo con la literatura 15, 16, se puede colocar en cualquier momento de la cirugía y no alterará el resultado (Tabla 2)
De acuerdo con lo anterior, la técnica permite una menor tasa de efectos colaterales, que en este trabajo fueron principalmente náusea y mareo; se demostró una ligera tendencia a ser más frecuentes en las pacientes a quienes se les administró analgesia no preventiva, por lo cual administrar la ketamina en forma preventiva podría reducir estos efectos secundarios.
Las dosis de los medicamentos realmente son bajas con lo cual se puede obtener una recuperación precoz, de acuerdo al tipo de procedimiento quirúrgico. Al analizar los valores obtenidos en la escala de Aldrete, se infere que el tiempo de permanencia de las pacientes, no se ve afectado estadísticamente a favor ni en contra de la analgesia preventiva. Los resultados de esta variable no son exactos, ya que no se registró el tiempo de salida de la paciente.
Solamente una paciente presentó un estado de excitación postoperatoria, la cual pertenecía al grupo de analgesia no preventiva, indicando que la ketamina en dosis analgésicas no tiene mayores efectos sicomiméticos, caso que se presenta según la literatura como un evento posible con dosis mayores, indicadas para inducir anestesia.
CONCLUSIÓN
En este trabajo se encontró que la efcacia de la ketamina para el alivio del dolor postoperatorio, no fue diferente cuando se administró en forma preventiva como no preventiva. Es decir, que no fue mejor la ketamina antes del estímulo quirúrgico que después del mismo. Los análisis registrados y las respuestas de las pacientes no mostraron en forma signifcativa, un menor respuesta al dolor en los grupos comparativos de Ketamina preventiva y al fnal de la intervención.
AGRADECIMIENTOS
Los investigadores agradecen la valiosa colaboración del personal de enfermería, ginecólogos y colegas anestesiólogos de la Clínica Piloto de Profamilia Bogotá. Igualmente a los doctores César Rubiano y Francisco Valero gestores del protocolo de esta investigación.
REFERENCIAS
1. Cliff K. S. Ong, Philipp Lirk, Robin A. Seymour, and Brian J. Jenkins. The Effcacy of Preemptive Analgesia for Acute Postoperative Pain Management: A Meta-analysis. Anesth Analg 2005; 100: 757-773. [ Links ]
2. Moiniche S, Kehlet H, Dahl JB. A qualitative and quantitative systematic Review of preemptive analgesia for postoperative pain relief. Anesthesiology. 2002; 96: 725-741. [ Links ]
3. Collin J. L. McCartney. A Qualitative Systematic Review of the Role of N-Methyl-D Aspartate Receptor Antagonists in preventive analgesia. Anesthesia and Analgesia. 2004; 98:1385-1400. [ Links ]
4. Dionne R.Preemptive vs preventive analgesia: which appro-ach improves clinical outcomes?. Compend Contin Educ Dent. 2000 jan; 21(1) 48, 51-4, 56. [ Links ]
5. Kelly DJ, Ahmad M, Brull SJ: Analgesia I: Physiological Pathways and pharmacological modalities. Can J. Anaesth. 2001; 48: 1000-1010 [ Links ]
6. Martín Redmond, B. Florence, P. Glass. Effective analgesic modalities for ambulatory patients. Anesthesiology Clinics of North America: june 2003. [ Links ]
7. Kohrs R, Rainer, Durieux ME. Ketamine: Teaching an old drug new tricks. Anesth and analg. November 1998; 87: 1186-1193. [ Links ]
8. Hirota, K.; Lambert, D.G. Ketamine: its mechanisms of action and unusual clinical uses. British Journal of Anesthesia. October 1996 [ Links ]
9. Karl G. Henriksson., J Sörensen. The promise of N-methyl-D-aspartate receptor antagonists in fbromyalgia. Rheum Dis Clin North Am (2002) 28: 343-51 [ Links ]
10. Petrenko, Andrei B. The Role of N-methyl-D-aspartate (NMDA) Receptors in pain: a review. Anesth and Analg. October 2003. Vol 97 (4). Pag. 1108 – 1116. [ Links ]
11. Alan D. Kaye. Pulmonary vasodilation by ketamine is media-ted in part by L-type Calcium channels. Anesth and analg. 1998; 87: 956 – 62 [ Links ]
12. Kakinohana M, Higa Y, Sasara T, Saikawa S, Miyata Y, Tomiyama H, Sugahara K: Addition of ketamina to propofoly fentanyl anaesthesia can reduce postoperative pain and epidural analgesic consumption in upper abdominal surgery. Acute Pain. 2004; 5:75-79 [ Links ]
13. Navarro J.R, Gutiérrez M, Restrepo F: Cirugía laparoscópica en Profamilia. Implicaciones en la paciente ambulatoria. Rev. colomb. anestesiol. 2003; 31: 21 [ Links ]
14. Aldrete J.A. Criterios para dar de alta. El puntaje de recuperación postanestésica. Rev. Col Anest. 1996. 24: 305-312 [ Links ]
15. Allan Gottschalk, David S. Smith. New concepts in Acute Pain therapy: preemptive analgesia. American Family Physician: May 2001. [ Links ]
16. Igor Kissin. Clinical Concepts and Commentary: Preemptive Analgesia. Anesthesiology. October 2000. [ Links ]
17. Aida S. The Challenge of preemptive analgesia. Pain. Clinical Updates. IASP. June, 2005. Vol. XIII, No. 2: 1-40 [ Links ]
18. Woolf CJ, Chong MS. Preemptive analgesia treating postoperative pain by preventing the establishment of central sensitization. Anesth Analg 1993; 77: 362-379 [ Links ]
19. Song SO, Carr DB. Pain and memory. Pain Clinical Updates. IASP 1999; VII (1): 1-4 [ Links ]
20. Coderre TJ, Katz J, Vaccarino AL, Melzac R. Pain mecha-nisms Laboratory, Clinical Research Institute of Montreal, Montreal - Canada. Pain. 1993; 52: 259-285 [ Links ]
21. Katz J, Kavanagh B, Sandler A, Nierenberg H, Boylan J, Friedlander M, Shaw B. Preemptive analgesia clinical evidence of neuroplasticity contributing to postoperative pain. Anesthesiology. 1992; 77(3): 439- 446 [ Links ]
22. Kondo E, Koichi I, Ogawa A, Tashiro A, Tsuboi Y, Fukuoka T, Yamanaka H, Morimoto T, Noguchi K. Involvement of gluta-mate receprtors on hyperexcitability of Wide dynamic range neurons in the gracile nucleus of the rats with experimental mononeuropathy. Pain. 2002; 95: 153-163 [ Links ]
23. Michl T, Jocic M, Heinemmann A, Schuligoi R, Holtzer P. Vagal afferent signaling of a gastric mucosal acid insult to medullary, pontine, thalamic, hypothalamic and limbic, but not cortical, nuclei of the rat brain. Pain. 2001; 92: 19-27. [ Links ]













