Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Colombian Journal of Anestesiology
versión impresa ISSN 0120-3347
Rev. colomb. anestesiol. v.36 n.3 Bogotá jul./sep. 2008
ARTÍCULO DE INVESTIGACIÓN TECNOLÓGICA
Realización de un procedimiento con anestesia total intravenosa ordenada por computador, utilizando un programa diseñado en la Universidad de Antioquia
Francisco Javier Gómez1, Pedro Arango2, Jorge Andrés Ruiz3, Juan Manuel Fernández4
1 Profesor asociado, Servicio de Anestesia, Universidad de Antioquia; anestesiólogo, IPS Universitaria, Medellín, Colombia fajago@une.net.co
2 Anestesiólogo, Universidad de Antioquia, Medellín, Colombia
3 Bioingeniero, Universidad de Antioquia, Medellín, Colombia
Recibido para publicación agosto 14 de 2008, Aceptado para publicación septiembre 22 de 2008
RESUMEN
Una infusión controlada por concentración objetivo, es un sistema guiado por ordenador que permite administrar fármacos de tal manera que se alcance y mantenga una concentración definida en un compartimento tisular, generalmente el plasma o el cerebro, basado en un modelo farmacocinético y farmacodinámico.
En este artículo se presenta el caso de una paciente a la que se le aplicó anestesia total intravenosa controlada por concentración objetivo en sitio efectivo, utilizando un programa desarrollado conjuntamente por el Departamento de Anestesiología y el programa de Bioingeniería de la Universidad de Antioquia. Luego de haber sido validado con otros programas similares como el Stanpump®, se procedió a realizar una prueba clínica. Los resultados fueron satisfactorios y se alcanzaron profundidades de anestesia adecuadas para el procedimiento quirúrgico, acordes con las concentraciones en sitio efectivo reportadas a nivel mundial. Además, el comportamiento hemodinámico del paciente fue estable y su recuperación fue satisfactoria.
Palabras clave: propofol, farmacocinética, farmacodinamia, anestesia total intravenosa.
SUMMARY
An infusión controlled by a target concentratiuon is a system guided by a computer that allows the administration of pharmachologycal drugs in Duch way that a defined concentration is reached and maintained in a tissue compartment; generally, plasma or the brain, based on a pharmachodynamic and pharmacokinetic model.
In this article, the case of a patient to whom total intravenous anesthesia was applied, controlled by target concentration in effective site, using a program developed together by the anesthesiology department and the bioengineering program of the Universidad de Antioquia is presented. After being validated with other similar programs like the Standpump, a clinical test was made. The results were satisfactory and the adequate anesthesia depths were reached for the surgical procedure, in accordance with the concentrations in the effective site reported worldwide. Additionally, the homodynamic behavior of the patient was stable and his recovery was satisfactory as well.
Key words: Propofol, pharmacokinetic, pharmachodynamica, total intravenous anesthesia.
INTRODUCCIÓN
William T. G. Morton realizó la primera demostración pública de anestesia en octubre de 1846. Administró éter en forma inhalada a Gilbert Abbott en el Massachusetts General Hospital.1 Durante el siglo siguiente, la inducción y el mantenimiento anestésico generalmente se realizaban por inhalación.
Aunque la idea de inyectar fármacos intravenosos no era nueva (el opio se inyectaba por vía intravenosa en 1665), la inducción intravenosa sólo se practicó en 1930 después del descubrimiento de los barbitúricos. Por lo tanto, la inducción y el mantenimiento de la anestesia por vía intravenosa es una alternativa reciente como técnica anestésica.
El tiopental y el metohexital son de utilidad en la inducción anestésica pero no se usan en infusión para el mantenimiento de la anestesia. En el caso del tiopental, su acumulación puede producir inestabilidad cardiovascular y la recuperación del paciente es muy lenta. El metohexital se ha asociado con fenómenos de excitación y cambios epileptiformes en el electroencefalograma (EEG).
El descubrimiento del propofol ha revolucionado la anestesia intravenosa. Se utilizó por primera vez en 1977 y es el único agente intravenoso hipnótico disponible tanto para la inducción como para el mantenimiento de la anestesia.
El descubrimiento reciente de analgésicos opiáceos de corta acción, tipo alfentanilo y remifentanilo, los cuales tienen un inicio de acción rápido y son rápidamente metabolizados, permiten que se utilicen en infusiones intravenosas mediante los desarrollos tecnológicos de bombas de perfusión confables. Esto ha llevado a un mejor entendimiento de los principios farmacocinéticos y al desarrollo de la anestesia total intravenosa(TIVA), en la cual el anestésico es administrado exclusivamente por esta vía.2
La técnica intravenosa total basada en la administración de propofol tiene muchas ventajas, entre las que podemos incluir la rápida recuperación tanto de la conciencia como de la función motora del paciente, que permite un tránsito rápido por la unidad de cuidados postanestésicos.3,4 El propofol posee, además, un efecto antiemético6, el cual está demostrado por una menor frecuencia de náuseas y vómito postoperatorios asociados a su utilización.5,7,8 Los agentes intravenosos no causan contaminación ambiental y no producen efectos adversos en el personal que labora en el quirófano.
CASO CLÍNICO
Se trata de una paciente de 21 años de 55 kg de peso, programada para rinoseptoplastia en la Unidad de Cirugía Ambulatoria en la IPS Universitaria de la Universidad de Antioquia. Como antecedentes de importancia, se encontró que fue sometida a una cesárea sin complicaciones y que sufre de migraña. En el examen físico, se encontró una paciente en buenas condiciones generales, con signos vitales y examen físico dentro de rangos normales, con presión arterial de 120/70 mm Hg, frecuencia cardiaca de 72 por minuto y frecuencia respiratoria de 12 por minuto.
La vía aérea se clasificó como Mallampati 1, con buena apertura oral y distancia tiromentoniana mayor de 6 cm.
La paciente se clasificó como ASA 1 con clase funcional de I según la clasificicación de la New York Heart Association (NYHA).
La paciente se sometió a ayuno completo y fue premedicada con midazolam, 3 mg por vía endovenosa. Se instaló monitoreo ASA básico (Monitor Poet plus 8100, Criticare Systems Inc.) que incluye pulsoximetría, cardioscopio, monitor de presión no invasiva, capnografía y analizador de gases, y para la medición de la profundidad de anestesia, el monitor BIS Vista (Biespectral Index System).
En la inducción se administraron por vía endovenosa: 100 µg de fentanilo y 100 mg de lidocaína, y se programó el computador al cual estaba conectada la jeringa con propofol a una infusión sérica de 3 µg/ml en cerebro; la concentración pico se alcanzó en 3,1 minutos, como se muestra en la figura 1. Luego se administraron por vía endovenosa 0,6 mg/kg de rocuronio, 8 mg de dexametasona y una infusión de remifentanilo a 0,1 µg/kg por minuto.
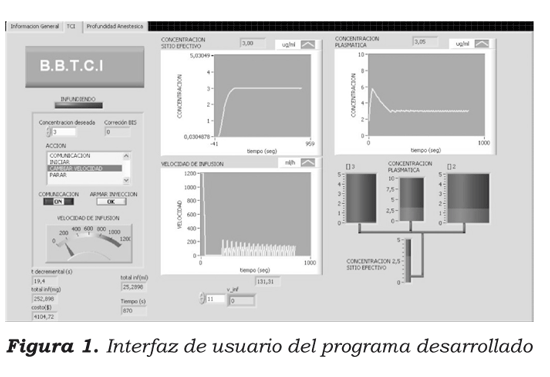
Se manejó la vía aérea mediante intubación orotraqueal con un tubo de diámetro interno de 7,0 mm. Se conectó a la máquina de anestesia y se inició asistencia respiratoria mecánica, con una mezcla de gases (50% aire y 50% oxígeno) sin productos halogenados; el mantenimiento se hizo con técnica endovenosa basada en propofol y remifentanilo.
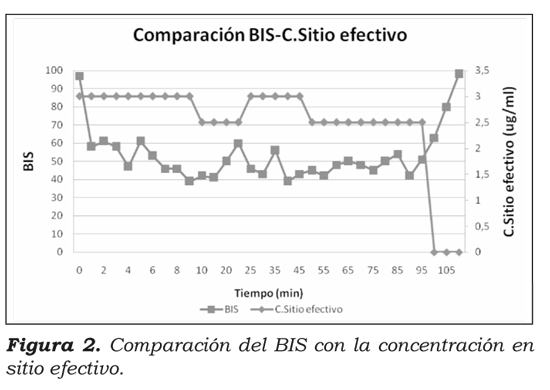
En la figura 2 se observa que al programar en el sistema una concentración objetivo de 3ug/ml, se alcanzó en menos de 2 minutos una medición en el BIS de 60. En las figuras 3 y 4 se observa un descenso en la frecuencia cardiaca y en la presión arterial. A los 8 minutos, el BIS alcanzó un valor de 40 y se disminuyó la concentración objetivo a 2,5 ug/ml.
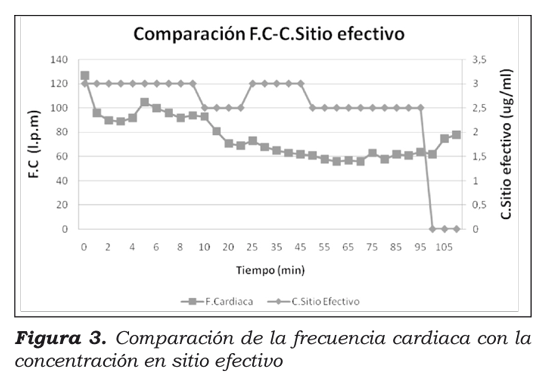
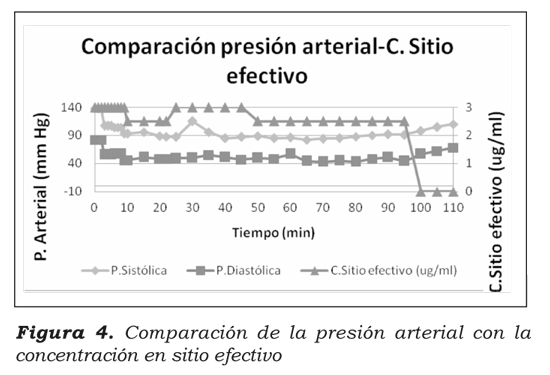
El comportamiento hemodinámico del paciente fue estable, como se puede apreciar en las figuras 3 y 4.
Durante todo el procedimiento fueron infundidos 108 ml de propofol. Se suspendió la infusión de propofol 10 minutos antes de terminar la cirugía, según lo calculado en el programa (por la función del tiempo decreciente), y el remifentanilo, al terminar la cirugía. Se registraron los signos vitales de la paciente y el programa se siguió ejecutando para determinar la concentración estimada a la que la paciente se despertaría. Esta concentración fue de 1 µg/ml, aproximadamente, lo cual es coherente con lo reportado en la literatura.
Al alcanzar esta concentración, la paciente se encontraba completamente conciente y atendiendo comandos verbales simples. Fue llevada a recuperación y se le dio el alta posteriormente sin evidencia alguna de complicaciones.
DISCUSIÓN
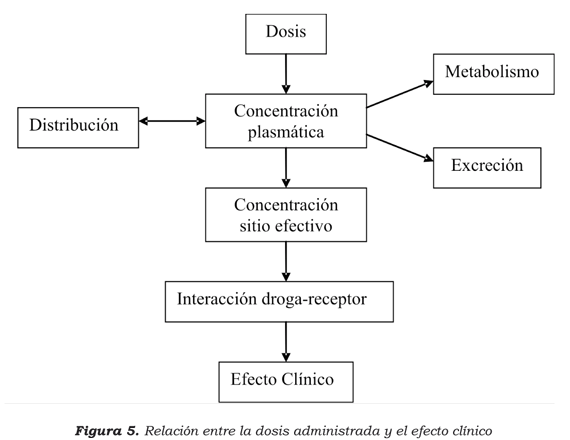
Cuando se administra una dosis de un fármaco, el objetivo principal es alcanzar la concentración necesaria en el sitio de acción para producir un efecto clínico específco. Esta relación dosis-respuesta (figura 5) puede dividirse en tres partes: la relación entre la dosis administrada y la concentración sérica (fase farmacocinética), la concentración en el órgano blanco y el efecto clínico (fase farmaco-dinámica), y el acople entre la farmacocinética y la farmacodinámica.
Hace más de 40 años, el concepto de concentración alveolar mínima (MAC) fue definido para agentes inhalados. Esta es la concentración alveolar mínima de un agente halogenado a una atmósfera, que produce inmovilidad durante la incisión de la piel en el 50% de los pacientes.9 Este concepto se ha usado en la práctica anestésica desde entonces. La determinación de la concentración efectiva se ha extendido a los agentes intravenosos mediante los programas de infusión ordenada por computador.
Antes de estar disponibles los aparatos TCI (target controlled infusión), se tenía en cuenta la velocidad de infusión y se utilizaba una velocidad mínima de administración.
Antes de la aparición de los algoritmos en la aplicación de anestesia controlada por concentración objetivo, la selección de la dosis de los agentes por vía intravenosa se calculaba teniendo en cuenta únicamente el peso del paciente.2
Hace más de 30 años, Kruger y colaboradores desarrollaron un esquema para la administración continua de fármacos intravenosos10,11, que consistía en un algoritmo complejo que entregaba una serie rudimentaria, pero útil, de velocidades de infusión. Sin embargo, sólo en la era actual, se han han podido incorporar estos esquemas o vectores de velocidad a la cotidianidad de los servicios de anestesia, gracias al desarrollo de nuevas tecnologías en la física del estado sólido y en la electrónica. Los algoritmos propuestos son demasiado complejos para ser resueltos manualmente y requieren de procesadores para su utilización. Hace, aproximadamente, 20 años se han venido desarrollando en las universidades y centros de investigación de Sudáfrica, Europa, Australia y Estados Unidos, sistemas para la administración de fármacos asistidos por computador y sólo hasta 1996 el primer dispositivo denominado Diprifusor® fue aprobado y distribuido comercialmente.11
El algoritmo que inicialmente utilizó el Diprifusor®, conocido como BET (bolo transfer elimination), ha sido perfeccionado9,12-15 y los modelos farmaco-cinéticos se han ampliado para diferentes tipos de población, como adultos mayores y niños.16 Lamentablemente, estos estudios no se han desarrollado en Latinoamérica y, aunque en varias clínicas y hospitales de nuestro país se utilizan el Diprifusor® y otros dispositivos que incorporan modelos farmacocinéticos, aún no se ha encontrado ninguna investigación que evalúe el comportamiento de estos modelos en la población latinoamericana. Aunque es bien sabido entre los expertos en anestesia intravenosa en el país que la población latina tiene una tendencia a requerir menor cantidad de algunos fármacos que la reportada en la bibliografía, nunca se ha documentado formalmente, dejando así una inquietud para futuras investigaciones.
Para la implementación del programa desarrollado en la Universidad de Antioquia, se usó el modelo farmacocinético de Marsh, desarrollado para el propofol. Este agente anestésico es un hipnótico de uso cotidiano en el quirófano y es un medicamento con uno de los modelos farmacocinéticos más aceptados a nivel mundial, el cual es implementado en un dispositivo de uso comercial, el Diprifusor®.
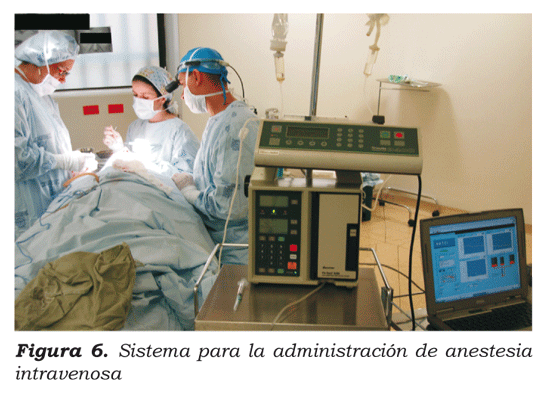
Utilizando este modelo se implementó el algoritmo desarrollado por Shafer y colaboradores, para el cálculo de las velocidades de infusión con el fin de mantener una concentración constante de fármaco en el cerebro.14 Luego, analizando el protocolo de comunicación entre un programa para el control de bombas de infusión denominado Stanpump® y la bomba de infusión Graseby 3400®, nuestro trabajo consistió en desarrollar un protocolo de comunicación que permitiera controlar la velocidad de infusión de la bomba de perfusión, a partir de las velocidades de infusión calculadas previamente por el algoritmo. En la figura 6 se presenta el sistema completo.
REFERENCIAS
1. Lee JA. History of anaesthesia. In: Atkinson RS, Rushman GB, Davies NHJ, editors. Lees Synopsis of Anaesthesia. 11th edition. London: Butterworth Heinemann; 1996. p. 875-915. [ Links ]
2. Absalom AR, Struys M. Overview of target controlled infusions and total intravenous anaesthesia. Gent: Academic Press; 2007. p. 108. [ Links ]
3. Doze VA, Shafer A, Whiste PF. Propofol-nitrous oxide versus thiopental-isoforane-nitrous oxide for general anesthesia. Anesthesiology. 1988;69:63-71. [ Links ]
4. Lim BL, Low TC. Total intravenous anaesthesia versus inhalational anaesthesia for dental day surgery. Anaesth Intensive Care. 1992;20:475-8. [ Links ]
5. Suttner S, Boldt J, Schmidt C, Piper S, Kulme B. Cost analysis of target controlled infusion-based anesthesia compared with standard anesthesia regimens. Anesth Analg. 1999;88:77-82. [ Links ]
6. Borgeat A, Wilder-Smith OH, Saiah M, Rifat K. Subhipnotic doses of propofol posses direct antiemetic properties. Anesth Analg. 1992;74:539-41. [ Links ]
7. Eriksson H, Korttila K. Recovery profle after desfurane with or without ondansetron compared with propofol in patients undergoing outpatient gynecological laparoscopy. Anesth Analg. 1996;82:533-8. [ Links ]
8. Smith I, Terhoeve PA, Hennart D, Feiss P, Harmer M, Pourriat JL, et al. Multicentre comparison of the costs of anaesthesia with sevofuorane or propofol. Br J Anaesth. 1999;83:564-70. [ Links ]
9. Kruger-Theimer E. Continuous intravenous infusion and multicompartmental accumulation. Eur J Pharmacol. 1968;4:317-24. [ Links ]
10. Vivian X, Leone M. Induction and maintenance of intravenous anaesthesia using target-controlled infusion systems. Baillieres Best Pract Res Clin Anaesthesiol. 2001;15:19-33. [ Links ]
11. Schraag S. Theoretical basis of target controlled anaesthesia: history, concept and clinical perspectives. Baillieres Best Pract Res Clin Anaesthesiol. 2001;15:1-17. [ Links ]
12. Schwilden H. A general method for calculating the dosage scheme in linear pharmacokinetics. Eur J Pharmacol. 1981;20:379-86. [ Links ]
13. Jacobs JR. Algorithm for optimal linear model-based control with application to pharmacokinetic model-driven drug delivery. IEEE Transactions on Biomedical Engineering. 1990;37:107-9. [ Links ]
14. Shafer SL, Gregg KM. Algorithm to rapidly achieve and maintain stable drug concentrations at the site of drug effect with a computer-controlled infusion pump. J Pharmacokinet Biopharm. 1992;20:147-69. [ Links ]
15. Jacobs JR, Williams EA. Algorithm to control effect compartment drug concentrations in pharmacokinetic modeldriven drug delivery. IEEE Transactions on Biomedical Engineering. 1993;40:993-9. [ Links ]
16. Dyck JB, Shafer SL. Effects of age on propofol pharmacokinetics. Semin Anesth. 1992;11:2-4. [ Links ]













