Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Colombian Journal of Anestesiology
versão impressa ISSN 0120-3347
Rev. colomb. anestesiol. v.38 n.2 Bogotá abr./jun. 2010
Investigación Científica y Tecnológica
Eficacia de la asociación dipirona-meperidina en disminuir la necesidad de opioide en dolor agudo posterior a cirugía abdominal
Héctor J. Meléndez*, José Rafael Ramos**
* Médico anestesiólogo, MSc, profesor asociado de postgrado de Anestesiología, Universidad Industrial de Santander, Bucaramanga, Colombia. melendez@uis.edu.co
** Médico anestesiólogo, Universidad Industrial de Santander, Bucaramanga, Colombia.
Recibido: febrero 13 de 2009. Enviado para modificaciones: enero 27 de 2010. Aceptado: marzo 15 de 2010.RESUMEN
Introducción. La principal preocupación de los pacientes que van a ser intervenidos es el dolor agudo postoperatorio, en cuyo manejo los opioides son los fármacos más recomendados, aunque sus efectos secundarios han limitado su uso. En nuestro medio, su manejo lo realizan los médicos generales o los cirujanos, con uso prevalente de la dipirona y resultados subóptimos. Una alternativa segura sería la adición a la dipirona de meperidina, obteniéndose así una adecuada alternativa para su manejo por parte de médicos no especialistas, sin los efectos adversos.
Objetivo. Determinar si la adición de dipirona a la meperidina disminuye en 50 % las necesidades del opioide en el manejo eficaz del dolor agudo postoperatorio.
Métodos. Se llevó a cabo un ensayo clínico controlado con 107 pacientes distribuidos en dos grupos. Se usaron dosis de 0,5 mg/kg de meperidina más 2,5 g de dipirona (n = 57), comparadas con la dosis usual de meperidina de 1 mg/kg (n = 50). El dolor agudo postoperatorio se evaluó según escala visual análoga.
Resultados. La incidencia del dolor agudo postoperatorio fue de 28 % en el grupo intervenido y de 26,32 % en el control. El riesgo relativo (RR) fue mayor en el grupo intervenido (RR = 1,06; IC95 % 0,57-1,98), sin diferencias entre ellos. La incidencia de efectos secundarios presentó mayores riesgos absolutos en el grupo control, con una diferencia significativa (p = 0,0055).
Conclusiones. La mezcla de dipirona más meperidina nos permite disminuir en 50 % la necesidad de opioide, con menos efectos adversos, sin que el control del dolor agudo postoperatorio sea eficaz.
Palabras clave: Dolor postoperatorio, meperidina, dipirona, ensayos clínicos como asunto (Fuente: DeCS, BIREME)
INTRODUCCIÓN
En 57 % de los pacientes que van a ser intervenidos quirúrgicamente, su principal preocupación es el dolor agudo postoperatorio (1). Este dolor presenta complicaciones respiratorias, cardiovasculares y digestivas, entre otras, prolonga la estancia hospitalaria y aumenta los costos.
A escala mundial, los opioides, y en especial la morfina, son los fármacos más usados para el control del dolor agudo postoperatorio, pero los efectos secundarios, tipo depresión respiratoria, náuseas, vómito, estreñimiento y retención urinaria, han limitado su uso (2). En Colombia no se puede decir lo mismo, pues agregadas a lo anterior tenemos la falta de disponibilidad y oportunidad de la morfina, y la poca disponibilidad de personal idóneo en las salas de recuperación, que refieren temor al usarlo (3).
En la actualidad, el manejo del dolor agudo postoperatorio con tratamiento multimodal, mezclando opioides con no opioides, ha demostrado disminución de la necesidad de los opioides; no obstante, los estudios con este tipo de terapia han sido controversiales en cuanto a la disminución significativa de los efectos adversos derivados de su uso, aunque sí han logrado reducir en forma importante los costos del tratamiento (4).
En nuestro medio, el manejo del dolor agudo postoperatorio lo realizan, en su mayoría, médicos generales o cirujanos, lo cual ha llevado a un manejo subóptimo del dolor, y sólo cuando éste se vuelve de difícil manejo consultan al especialista.
Motivados por lo anterior y el uso prevalente de la dipirona (5,6,7), su bajo costo y un estudio piloto realizado por nosotros, en el cual la asociación de dipirona (2,5 g) con meperidina (0,5 mg/ kg) mostró una efectividad de 75 % y una disminución de 60 % de los efectos adversos, como náuseas y vómito, nos propusimos llevar a cabo este ensayo clínico controlado con el objetivo de probar su eficacia y, además, tener una adecuada alternativa para el manejo del dolor agudo postoperatorio por médicos no especialistas, sin el temor a efectos adversos.
MATERIALES Y METODOS
Se realizó un ensayo clínico controlado doblemente enmascarado. Se incluyeron pacientes entre 15 y 75 años, con puntaje I-II de la American Society of Anesthesiologists (ASA), sometidos a laparotomía por cirugía general o ginecológica bajo anestesia regional o general. Se excluyeron personas con alteraciones de la comunicación, inestables, con catéter peridural, con contraindicaciones para los fármacos propuestos o con historia previa de adicción a opiáceos.
El dolor se midió por medio de la escala visual análoga, que ya ha sido ampliamente validada, en la cual se considera como dolor agudo postoperatorio cuando se encuentran valores de 4 o mayores (8).
La muestra se calculó con base en un estudio previo en nuestro medio que mostró una incidencia de dolor agudo postoperatorio de 37 % (3) y bajo la hipótesis de la bioequivalencia para proporciones, utilizando los siguientes parámetros: con 0,5 mg/kg de meperidina más 2,5 g de dipirona, se obtiene igual eficacia en el control del dolor agudo postoperatorio que utilizando 1 mg/kg de meperidina; calculando un error tipo I de 5 % (significancia de 95 %) y un error tipo II de 10 % (poder de 90 %); si se considera una diferencia de 50 % en el consumo del opiáceo para considerar los tratamientos como clínicamente equivalentes y una diferencia verdadera de 10 % entre los dos tratamientos equivalentes, se requerían de 58 pacientes por grupo.
Se hizo una distribución aleatoria por bloques, con el fin de garantizar homogeneidad en el tamaño de los grupos. Se generó una tabla de números aleatorios y se hizo la asignación mediante una central.
El auxiliar de la investigación preparaba la medicación y, utilizando una jeringa protegida con igual volumen (20 ml) con el fin de garantizar el enmascaramiento, la entregaba al anestesiólogo de la sala (igualmente, enmascarado) y lo administraba al momento de iniciar el cierre de la piel. Seguidamente, se ordenaba y dejaba la dosis correspondiente según el protocolo, para ser administrada cada 6 horas hasta cumplir 24 horas. Estos medicamentos fueron preparados y entregados a la jefe de la clínica del dolor encargada de administrar los medicamentos y realizar el seguimiento.
Antes de administrar las dosis subsiguientes, se evaluaba la intensidad del dolor y los posibles efectos secundarios de los fármacos. Si el paciente refería dolor antes de corresponderle la nueva dosis, se manejaba según el protocolo de rescate analgésico, utilizando dosis de 0,25 mg/kg de meperidina; si a los 15 minutos persistía el dolor, se administraba una dosis similar de meperidina; si el dolor agudo postoperatorio era persistente, se solicitaba valoración por la clínica de dolor.
Todos los pacientes recibieron (si no tenían contraindicación) 4 mg de dexametasona combinados con 20 mg de metoclopramida o 4 mg de ondansetrón, con el objetivo de disminuir la incidencia de náuseas o vómito, efecto adverso muy frecuente de la meperidina. La elección de estos medicamentos estuvo sujeta a su disponibilidad, y su administración u omisión se registró en el instrumento diseñado para tal fin.
Los datos registrados en el instrumento se digitaron en una base de datos previamente codificada en el programa Excel 2007. Las variables cuantitativas se describieron con medidas de tendencia central y de dispersión; se agruparon y se construyeron tablas de frecuencia. Las variables cualitativas se describieron en porcentajes, con su intervalo de confianza; las cuantitativas se describieron utilizando promedios, mediana, desviación estándar y su respectivo intervalo de confianza (9).
Se analizaron las características de base y clínicas de los individuos de los diferentes grupos, para verificar si eran comparables; luego, se verificó la distribución normal de cada una. Se plantearon pruebas de hipótesis para evaluar las diferencias tanto para las variables continuas como para las dicotómicas o cualitativas.
Las características clínicas de las pacientes se describieron usando medias y proporciones, y su respectivo intervalo de confianza al 95 % (IC95 %). La prueba exacta de Fischer y la de la t de Student, con su significancia al 0,05, se usaron para evaluar las diferencias entre las variables dicotómicas y continuas, respectivamente. Las diferencias entre más de dos subgrupos se evaluaron con la prueba de ANOVA. Se hizo un análisis bivariado y multivariado, calculando el riesgo relativo (RR) como medida de impacto. Se asumieron como diferencias estadísticamente significativas aquéllas en las cuales el valor de p era inferior a 0,05 (10,11). El análisis se hizo con el paquete estadístico Stata 9.0 (12).
RESULTADOS
El presente estudio se llevó a cabo en el Hospital Universitario de Santander; fue aprobado por el comité de ética interinstitucional de Universidad Industrial de Santander-Hospital Universitario de Santander y fue autorizado mediante el consentimiento firmado por todos los participantes.
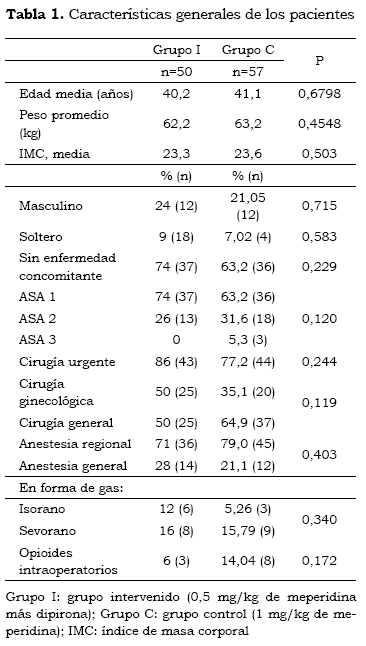
Se incluyeron 107 pacientes distribuidos en los dos grupos (intervenido, n = 50, y control, n = 57), lo cual equivalió a 91 % de la muestra calculada; se presentó una pérdida de seguimiento del 5 % 12 horas después de la cirugía. Estas pérdidas se dieron por falta de seguimiento del protocolo, vómito persistente o retiro voluntario. Los dos grupos no presentaron diferencias estadísticamente significativas en sus características basales. La edad promedio fue de 40 años, el peso promedio fue de 62 kg y la media del índice de masa corporal fue de 26 (tabla 1).
La incidencia del dolor agudo postoperatorio, a las 6 horas, fue de 28 % en el grupo intervenido y de 26,32 % en el control. El riesgo relativo fue mayor en el grupo intervenido (RR = 1,06; IC95 % 0,57-1,98), sin diferencias entre ellos (tabla 2).
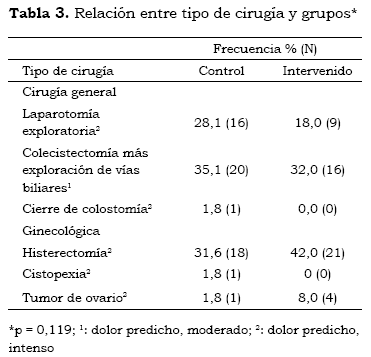
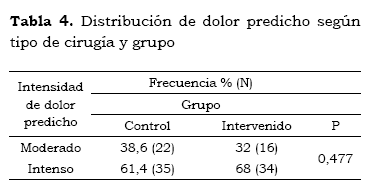
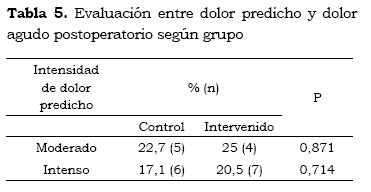
A pesar de no haberse encontrado diferencias significativas en las características basales (p = 0,119), se analizaron la relación del dolor agudo postoperatorio según el tipo de cirugía realizada y su intensidad esperada (moderada o grave)(13), sin evidenciarse diferencias significativas (p = 0,477). El análisis según la intensidad del dolor agudo postoperatorio esperado (según tipo de cirugía, moderado a grave) y el observado a las 6 horas tampoco evidenciaron diferencias significativas (p = 0,871 y 0,714) (tablas 3, 4 y 5).
Durante los periodos evaluados, el riesgo absoluto y RR de dolor agudo postoperatorio fueron mayores en las primeras 18 horas en el grupo intervenido, pero sin diferencias significativas entre los dos grupos. Los valores de dolor agudo postoperatorio máximo fueron mayores en las primeras 6 horas en el grupo intervenido, en los siguientes intervalos fue igual y a las 24 horas no se presentó en el grupo intervenido (tabla 6).
El tiempo promedio de rescate fue de 125 y 94 minutos en los grupos intervenido y control, respectivamente, sin diferencias significativas (p = 0,449). En las primeras 6 horas, el grupo intervenido presentó mayor riesgo absoluto de rescate analgésico (26 % vs. 24,56 %) y RR (1,05) pero sin diferencias significativas (p = 0,861) (tabla 7).
La incidencia de efectos adversos presentó mayor riesgo absoluto en el grupo control, con diferencia significativa (p = 0,0055). El mareo fue el efecto secundario de mayor incidencia en el grupo intervenido, aunque sin diferencias significativas. Los demás efectos presentaron RR mayores y significativos en el grupo control, exceptuando la depresión respiratoria (tabla 8).
DISCUSIÓN
Es necesario resaltar que la mayoría de los estudios que existen en el mundo sobre el dolor agudo postoperatorio se realizan a través de analgesia controlada por el paciente (PSA) lo cual aumenta los costos. Sin embargo, la literatura reporta incidencias altas de este tipo de dolor, con valores que oscilan entre 46 % y 53 % (14,15).
Los resultados de nuestros estudios nos permiten afirmar que la adición de dipirona a la meperidina, permite disminuir en 50 % la necesidad de opioides para el control del dolor agudo postoperatorio, valor superior a los hallazgos de Aubrun et al. (16), realizados en París, con paracetamol más morfina, quienes reportaron una disminución de 37 % de dicho dolor en pacientes con dolor moderado, y con mejores resultados que los obtenidos en el estudio realizado en el Hospital San Vicente de Paúl de Medellín, donde el fármaco más utilizado fue la dipirona, con resultados desfavorables en el 69 % de los pacientes (6). Así, este ahorro significativo del opioide nos permite incentivar su uso combinado en el manejo del dolor agudo postoperatorio.
A pesar de no tener un control efectivo del dolor agudo postoperatorio (27 %, en promedio), éste sí fue menor que el reportado por Camacho en 1995 (3). Este dato no nos puede dejar satisfechos pues, a pesar de disminuir en 30 % la incidencia, aún tenemos un valor alto de dolor y tenemos que uno de cada cuatro pacientes lo presenta, y el objetivo es un dolor agudo postoperatorio de cero a tres; y ahí debemos enfocar nuestra atención.
La seguridad de dosis menores con menos efectos adversos es muy conocida y esto fue lo que pudimos corroborar en el presente estudio. La mayor incidencia de mareo podría darse por el efecto aditivo de la dipirona y la meperidina a nivel central, sin descartar la influencia del tipo de anestesia. La literatura mundial reporta hasta 73 % de efectos adversos con opioides (6) y otros estudios presentan resultados controversiales en los que no se observa diferencia en la analgesia multimodal (14).
La incidencia de 26,3 % y 28 % de dolor agudo postoperatorio en los dos grupos (control e intervenido) nos hace pensar que, a pesar de no existir diferencias, su control no fue el óptimo, pues es muy diferente un control eficaz en los dos grupos a la falta de diferencia entre ellos, dado que la incidencia de dolor agudo postoperatorio no fue la ideal.
Es importante aclarar que pueden existir interpretaciones diferentes en el cálculo del tamaño de la muestra y, según el software que se utilice, podemos llegar a concluir que pudimos estar expuestos a cometer errores de tipo II por falta de poder. Por ejemplo, si recalculamos la muestra con los parámetros de proporciones para bioequivalencia a una o dos colas, tomando como base la disminución del dolor en 50 % (del 37 % al 18,5 %) con diferencia máxima del 0,05, el tamaño de la muestra sería de 3,283 y 9,659 pacientes por grupo, respectivamente (software de la Pontifica Universidad Javeriana) y si recurrimos al cálculo de la muestra según proporciones con EpiInfo, con iguales parámetros, este tamaño sería de sólo 101 pacientes.
REFERENCIAS
1. Pogatzki-Zahn E, Zahn PK, Brennan TJ. Postoperative pain-clinical implications of basic research. Best Pract Res Clin Anaesthesiol. 2007;21(1):3-13. [ Links ]
2. Buvanendran A, Reuben S, Kroin J. Recent advances in nonopioid analgesics for acute pain management. Tech Reg Anesth Pain Manag. 2007;11(1):19-26. [ Links ]
3. Camacho N. Incidentes en la unidad de recuperación posquirúrgica Hospital Universitario Ramón González Valencia (tesis). Bucaramanga: Universidad Industrial de Santander; 2006. [ Links ]
4. Elia N, Lysakowski C, Tramèr MR. Does multimodal analgesia with acetaminophen, nonsteroidal antiinflammatory drugs, or selective cyclooxygenase- 2 inhibitors and patient-controlled analgesia morphine offer advantages over morphine alone? Meta-analyses of randomized trials. Anesthesiology. 2005;103(6):1296-304. [ Links ]
5. McQuay H. Opioids in pain management. Lancet. 1999;353(9171):2229-32. [ Links ]
6. Cardona E, Castaño ML, Builes AM, Castro G. Manejo del dolor postquirúrgico en el Hospital Universitario San Vicente de Paúl de Medellín. Rev Colomb Anestesiol. 2003;31(2):111-7. [ Links ]
7. Arcila-Herrera H, Barragán-Padilla S, Barbolla-Escoboza J, Canto-Solís A, Castañeda-Hernández G, León-González M, et al. Consenso de un grupo de expertos mexicanos. Eficacia y seguridad del metamizol (dipirona). Gac Méd Méx. 2004;140(1):99-101. [ Links ]
8. Loeser J, Butler S, Chapman C, Turk D. Bonica, terapéutica del dolor. 3ª ed. México: Mc Graw-Hill Interamericana; 2003. [ Links ]
9. Fleiss JL. Determining sample sizes needed to detect a difference between two proportions. In: Fleiss JL, Levin BA, Cho Paik M. Statistical methods for rates proportions. 2nd ed. New York: John Wiley & Sons; 1981. p. 33-49. [ Links ]
10. Greenland S. Introduction to regression modeling. In: Rothman K, Greenland S, Lash T. Modern epidemiology. 2nd ed. Buenos Aires: Lippincott; 1998. p. 401-32. [ Links ]
11. Rothman K, Greenland S, Lash T. Precision and validity of studies. In: Modern epidemiology. 2nd ed. Philadelphia: Lippincott; 1998. p. 119-33. [ Links ]
12. StataCorp. Stata Stadistical Software: Release 9.0. College Station: Stata Corporation; 2006. [ Links ]
13. Puebla F. Tipos de dolor y escala terapéutica de la OMS. Dolor iatrogénico. Oncología. 2005;28(3):139- 43. [ Links ]
14. Bustos M, González E, Gallego J, Mayo M, Pallares J. Estudio comparativo de la eficacia analgésica del tramadol versus morfina-metamizol tras histerectomía abdominal. Rev Soc Esp Dolor. 2003;10(7):411-8. [ Links ]
15. Macintyre P. Safety and efficacy of patient controlledanalgesia. Br J Anaesth. 2001;87(1):36-46. [ Links ]
16. Aubrun F, Kalfon F, Mottet P, Bellanger A, Langeron O,Coriant P, et al. Adjunctive analgesia with intravenous propacetamol does not reduce morphine related adverse effects. Br J Anaesth. 2003;90(3):314-9. [ Links ]











 texto em
texto em