Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.38 no.3 Bogotá July/Sept. 2010
Paciente embarazada con enfermedad cardiaca *
Manejo periparto basado en la estratificación del riesgo. Serie de casos 2005-2009
Germán A. Monsalve**, Catalina M. Martínez***, Tatiana Gallo***, María Virginia González***, Gonzalo Arango***, Alejandro Upegui***, Juan Manuel Castillo***, Juan Guillermo González***, Jorge Rubio****, Leonardo Mojica*****
* El resumen de este artículo fue aceptado y presentado como póster en el 42° Congreso de la Sociedad Americana de Anestesia Obstétrica y Perinatologia (SOAP), en San Antonio, Texas, Estados Unidos.12 de mayo de 2010.
** Médico Anestesiòlogo, Coordinador Unidad de Alta Dependencia Obstétrica Clinica del Prado. Medellín, Colombia. gerafomejia@yahoo.com.
*** Anestesiòlogos Unidad de Alta Dependencia Obstétrica Clinica del Prado. Medellín, Colombia.
**** Anestesiòlogo cardiovascular Unidad de Alta dependencia Obstétrica Clinica del Prado. Medellín, Colombia.
***** Anestesiòlogo intensivista Unidad de Alta dependencia Obstétrica Clinica del Prado. Medellín, Colombia.
Recibido: mayo 29 de 2010. Enviado para modificaciones: junio 30 de 2010. Aceptado: julio 14 de 2010.
RESUMEN
Objetivo. Reportamos nuestra experiencia en el manejo de una serie de pacientes obstétricas con enfermedad cardiaca de diferentes etiologías, utilizando una estrategia de estratificación del riesgo, para elaborar un plan de manejo periparto en el que está incluido el manejo anestésico.
Métodos. Serie de casos. Revisión retrospectiva de 37 pacientes embarazadas con diagnóstico de enfermedad cardiaca de diferentes etiologías, ingresadas a la Unidad de Alta Dependencia Obstétrica de la Clínica del Prado, de Medellín, Colombia entre 2005 y 2009.
Resultados. Del total de 37 pacientes, 15 presentaron enfermedad cardiaca congénita; 13, enfermedad cardiaca valvular; 5, cardiomiopatía periparto, y las 4 restantes, trastornos del ritmo y enfermedad isquémica. Se estratificó el riesgo según la clasificación de lesiones anatómicas y el riesgo de eventos cardiacos basados en el CARPREG. Se identificaron ocho pacientes en el grupo de alto riesgo y el resto, en riesgo intermedio y bajo. La mayor parte de las pacientes fueron manejadas con técnicas anestésicas conductivas (89,2 %). La decisión de cesárea (35 %) se dio por indicación obstétrica. Se presentaron complicaciones maternas de origen cardiovascular en el 10,8 % de los casos. No se presentaron muertes maternas.
Conclusión. La implementación de un protocolo de estratificación del riesgo de muerte y de la aparición de complicaciones cardiovasculares en la paciente embarazada con cardiopatía le permite al anestesiólogo hacer parte integral del grupo interdisciplinario de manejo y, así, tener impacto en la obtención de un mejor resultado materno y perinatal en este grupo de pacientes.
Palabras clave: Cardiopatía, complicaciones del embarazo, riesgo, anestesia (Fuente: DeCS, BIREME)
INTRODUCCIÓN
La enfermedad cardiaca complica entre 1 % y 4 % de los embarazos en los Estados Unidos, y es la principal causa de morbilidad y mortalidad materna de causa no obstétrica en el Reino Unido (1). La enfermedad reumática ha sido la principal causa de enfermedad cardiaca en el embarazo en países en vía de desarrollo, pero con el incremento en el cuidado perinatal de los recién nacidos con enfermedad cardiaca congénita (ECC) y el desarrollo de la cirugía cardiovascular, la ECC es ahora la causa más importante de cardiopatía en el embarazo (2,3).
Además, las mujeres con más frecuencia posponen el embarazo hasta la cuarta y quinta décadas de la vida (4,5), cuando las comorbilidades, como hipertensión, diabetes e hipercolesterolemia, hacen que aumente la incidencia de otras enfermedades cardiacas, como la enfermedad isquémica.
MÉTODOS
Se realizó una revisión retrospectiva de los reportes clínicos de 37 pacientes consecutivas con diagnóstico de enfermedad cardiaca, incluyendo enfermedad cardiaca valvular (ECV), ECC y cardiomiopatía periparto (CMP), que se presentaron en la Unidad de Alta Dependencia Obstétrica (UADO), de la Clínica del Prado, en Medellín (Colombia), entre 2005 y 2009. El objetivo del estudio es describir datos demográficos, como edad, paridad, edad gestacional, clase funcional según New York Heart Association (NYHA), vía del parto, tipo de cardiopatía, grado de severidad —según clasiicaciones de riesgo, como Clark y colaboradores (6), CARPREG (7,8) y El Colegio Americano de Cardiología/Asociación Americana del corazón (ACC/AHA), en el 2006, y la Sociedad Europea de Cardiología en el 2007 (ESC) (9,10)—, desenlace obstétrico, técnicas anestésicas utilizadas en el periparto, monitoría, cuidado posparto y morbilidad y mortalidad asociados.
Aspectos éticos: El trabajo fue aprobado por el comité de ética de la Clínica del Prado.
RESULTADOS
El promedio de edad de las pacientes fue 26,9 años (de 18 a 42); la paridad, 1,9 (1-8); la edad gestacional, 36 semanas (de 9 a 40), y 97 % de ellas tenían control prenatal. En nuestra serie, 15 pacientes tuvieron ECC, 13 ECV, 5 CMP, y las 4 restantes presentaron otras patologías, como taquicardiomiopatía, bloqueo aurículo-ventricular completo y enfermedad cardiaca isquémica. Todas las pacientes fueron admitidas a la institución antes del parto, y de aquéllas con control prenatal asistieron al menos a dos consultas; estas mismas pacientes tenían, al menos, una evaluación por cardiología ordenada en el control prenatal.
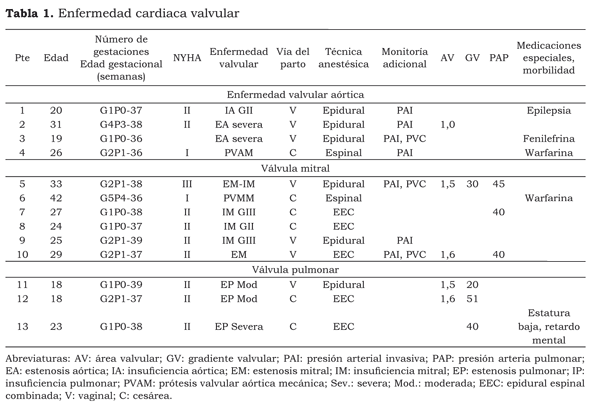
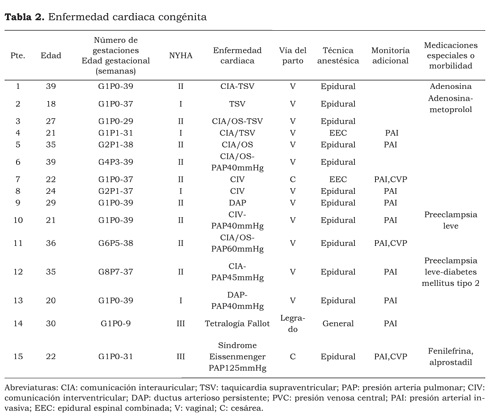
Las causas de ECV se ilustran en la Tabla 1. Aquí se incluyen pacientes con estenosis aórtica severa, estenosis mitral, y tres pacientes con enfermedad valvular pulmonar aislada. Dentro del grupo de pacientes con ECC destacamos dos pacientes catalogadas como alto riesgo: una paciente con diagnóstico de enanismo no acondroplásico y síndrome de Eissenmenger, asociado con comunicación interauricular (CIA), con hipertensión pulmonar severa suprasistémica, disfunción severa del ventrículo derecho e insuficiencia valvular pulmonar severa, quien no realizó ningún control prenatal ni evaluación ecocardiográica durante su embarazo, y una paciente con tetralogía de Fallot no corregida con estenosis pulmonar y disfunción ventricular derecha severas, quien tampoco realizó control prenatal. Los datos más relevantes de las pacientes con ECC se ilustran en la Tabla 2.
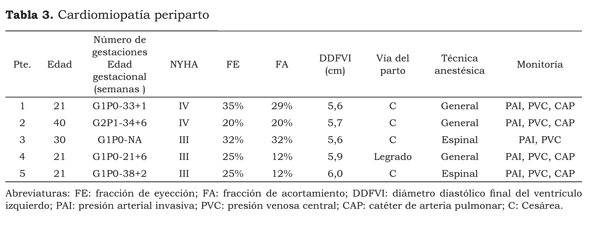
Se presentaron cinco casos de CMP, todas ingresadas en clase funcional NYHA III-IV, con cuadros de edema pulmonar. En la evaluación ecocardiográica se evidenció en todas ellas disfunción ventricular izquierda severa, con FE < 30 % y dilatación marcada del ventrículo izquierdo > 5,5 cm de diámetro diastólico final del ventrículo izquierdo (DDFVI). Una de las pacientes desarrolló un cuadro de muerte súbita por taquicardia ventricular, tipo torsade de pointes, que requirió manejo por electroisiología con cardiodesfibrilador implantable. Los datos más importantes de este grupo se ilustran en la Tabla 3.
La vía de terminación del embarazo fue decidida en conjunto con el servicio de obstetricia. El 35 % fueron llevadas a cesárea; de éstas, el 23 % bajo anestesia general (AG), 30 % bajo anestesia espinal (AE), 39 % bajo anestesia epidural/espinal combinada (EEC) y el 8 % restante bajo anestesia epidural (AEP). El 60 % de las pacientes terminaron su embarazo por parto vaginal, todas bajo analgesia epidural. Las dos pacientes restantes corresponden a gestaciones tempranas que necesitaron legrado y extracción de restos placentarios bajo anestesia general. Durante el trabajo de parto o la cesárea, el 64 % de las pacientes requirieron algún tipo de monitoría hemodinámica invasiva, principalmente monitoría invasiva de la presión arterial. Cuatro de las cinco pacientes con diagnóstico de CMP requirieron catéter de arteria pulmonar dentro de su manejo periparto.
Dentro de las complicaciones, en el grupo de pacientes con CMP se presentaron cuatro casos de edema pulmonar, dos de estas pacientes requirieron ventilación mecánica prolongada por más de 72 horas. La paciente que desarrolló muerte súbita por arritmia ventricular se incorporó al protocolo de enfriamiento posparo cardiaco, y al ser destetada de la ventilación mecánica, 72 horas después, no presentó secuelas neurológicas de importancia. Una de las pacientes con CMP debió ser manejada en conjunto con el grupo cardiología con levosimendan, debido a falla cardiaca persistente, a pesar del uso de dobutamina más milrinona. Una paciente presentó falla renal aguda oligúrica que no requirió terapia de reemplazo renal. Todas las pacientes de CMP recibieron anticoagulación y cuatro de ellas fueron trasladadas a unidades de cuidado intensivo cardiológico en el periodo posparto, para evaluación por parte del grupo de trasplante, debido a disfunción ventricular severa persistente.
En el seguimiento a un año ninguna de ellas ha requerido trasplante cardiaco. La paciente con diagnóstico de síndrome de Eissenmenger fue manejada en un centro cardiovascular por el alto riesgo de su patología; se obtuvo un resultado periparto favorable, con cuidado posquirúrgico en UCI cardiovascular.
No se presentaron muertes maternas.
DISCUSIÓN
La enfermedad cardiaca en el embarazo impone un riesgo que debe ser evaluado de manera interdisciplinaria e instaurar de manera secuencial un protocolo de diagnóstico y manejo basado en la estratificación del riesgo, cuyo objetivo es evitar desenlaces fatales debidos a un manejo no planeado. La aplicación de esta aproximación podría impactar en una posible reducción de las complicaciones cardiovasculares asociadas en este grupo de pacientes. Los aspectos más importantes de esta aproximación se describen a continuación.
Estratificación del riesgo
Múltiples sistemas de estratificación del riesgo han sido diseñados; el primero de ellos, escrito por Clark y colaboradores (6), define la severidad anatómica de las lesiones como el único modo de estratificación; es decir, pacientes con estenosis aórtica severa, hipertensión pulmonar de cualquier etiología y enfermedad de la aorta, como las lesiones con mayor mortalidad (50 %). El problema de esta clasificación es que sólo tiene en cuenta la lesión sin darles importancia a los datos clínicos o los eventos cardiacos previos. El índice de riesgo desarrollado por el estudio canadiense, conocido como CARPREG (7,8), fue publicado con el fin de predecir complicaciones cardiacas relacionadas con el embarazo en pacientes con cardiopatías, teniendo en cuenta no sólo la lesión anatómica, sino los datos del estado clínico.
Para el desarrollo de eventos cardiacos, como edema pulmonar, arritmias, enfermedad cerebrovascular, paro de origen cardiaco y muerte, se identificaron cuatro predictores:
• Pobre clase funcional ( NYHA III o IV) o cianosis.• Antecedente de evento cardiaco o arritmia.
Obstrucción del corazón izquierdo (área válvula mitral < 2 cm2, área válvula aórtica < 1,5 cm2, gradiente de salida pico del ventrículo izquierdo > 30 mmHg).
• Disfunción sistólica del ventrículo izquierdo (fracción de eyección < 40 %).
El Colegio Americano de Cardiología-Asociación Americana del Corazón (ACC/AHA, por sus siglas en inglés), en el 2006, y la Sociedad Europea de Cardiología (ESC), en el 2007, publicaron las guías para enfermedad cardiaca valvular, en las que consideran que son de alto riesgo materno y fetal durante el embarazo las mujeres con una de las siguientes lesiones (9,10):
• Estenosis aórtica severa con o sin síntomas.
• Estenosis mitral sintomática (NYHA II a IV).
Insuficiencia aórtica o mitral con NYHA III o IV.
Enfermedad valvular aórtica o mitral con disfunción ventricular izquierda severa (definida como fracción de eyección < 40%) o severa hipertensión pulmonar (presión arterial sistólica arteria pulmonar > 75 mmHg).
Síndrome de Marfán con o sin insuficiencia aórtica (11).
Válvula protésica mecánica que requiere anticoagulación.
En la evaluación aislada de la ECC, la presencia de insuiciencia valvular pulmonar severa, de disfunción ventricular derecha severa y de síndrome de Eissenmenger se asociaron con eventos de muerte materna por falla cardiaca y arritmias en un 4,8 % y 4,5 %, respectivamente (8,12). Por definición, CMP se diagnostica cuando se desarrolla falla cardiaca en el último mes de embarazo o en los siguientes cinco meses posparto, en ausencia de otras causas conocidas de falla cardiaca asociada con los siguientes criterios: fracción de eyección (FE) < 45 %, fracción de acortamiento (FA) < 30 % y un diámetro de in de diástole ventricular izquierdo (DDFVI) > 2,7 cm (13,14). Aquellas pacientes que en el momento del diagnóstico tienen FE < 25 % y DDFVI > 5,0 cm presentan pobre pronóstico y altas tasas de necesidad de trasplante en caso de una nueva gestación (15).
En nuestro reporte, las pacientes con ECC y alto riesgo, según lo esbozado anteriormente, fueron la paciente con síndrome de Eissenmenger y la paciente con tetralogía de Fallot no corregida. Llama la atención que éstas no tenían control prenatal, hecho que se ha identiicado en la literatura como marcador aislado de morbimortalidad (16). La paciente con enfermedad valvular aórtica severa quien ingresó con clase funcional NYHA mayor de II también está en dicha categoría de alto riesgo.
Nuestras pacientes con CMP entran en el grupo de mayor riesgo para eventos de muerte y necesidad de trasplante (2), por lo cual su manejo impone un reto difícil con alto riesgo de complicaciones periparto y diicultad para el manejo anestésico; estas pacientes fueron manejadas con anestesia general, monitoría con catéter de Swan Ganz y cuidado posparto, en centros cardiovasculares con capacidad de realizar trasplante.
Vía del parto
La vía del parto debe ser decidida por las condiciones obstétricas; en general, está permitido el parto vaginal. En nuestro reporte, el 60 % de las pacientes terminaron su embarazo por parto vaginal, todas bajo analgesia conductiva. Las únicas indicaciones de cesárea por causa cardiaca son: la aortopatía con raíz aórtica > 4 cm o crecimiento progresivo de ésta, disección aórtica o aneurisma de aorta torácica y anticoagulación con warfarina en las pacientes con prótesis valvulares mecánicas, por el riesgo de hemorragia intraventricular cerebral en el feto (6).
Los grandes centros de referencia de enfermedades cardiacas en el embarazo (17) están recomendando recientemente la posibilidad de cesárea programada en pacientes con enfermedad cardiaca con muy alto riesgo de muerte o de desarrollo de complicaciones cardiovasculares graves, como en el caso de pacientes con hipertensión pulmonar severa de cualquier etiología, debido a la posibilidad de realizar el proceso de terminación del embarazo en un ambiente "controlado", que permita evitar complicaciones relacionadas con la presencia de personal no familiarizado con la patología o la falta de recursos en escenarios no planeados, principalmente, ines de semana y turnos nocturnos.
Técnica anestésica
No existe en este momento en la literatura la posibilidad de definir si la mortalidad de este grupo de pacientes está influenciada por la elección de una técnica anestésica en particular. Los grupos de anestesia obstétrica se inclinan, recientemente, por el uso de técnicas conductivas (18). En nuestro reporte, las pacientes de riesgo alto, como tetralogía de Fallot, y las pacientes con CMP que tenían disfunción ventricular severa fueron manejadas con anestesia general; el resto, con técnicas conductivas basadas en lo que denominamos "metas hemodinámicas". Es decir, mantener normovolemia e incremento en las resistencias vasculares en pacientes catalogadas como de alto riesgo.
La aplicación de técnicas conductivas que permitan la titulación del grado anestésico deseado han sido descritas en el caso de pacientes con lesiones estenóticas severas del corazón izquierdo, como estenosis aórtica severa (19) o lesiones asociadas con hipertensión pulmonar severa (20), lo cual reporta seguridad con su utilización.
Monitoría
En pacientes de bajo riesgo utilizamos monitoria ASA básico y monitoría fetal continua. En nuestro centro, en las pacientes de riesgo moderado y alto utilizamos siempre una línea arterial para el control estricto de la presión (64 % de ellas), catéter venoso central para medir la tendencia en las presiones de llenado, más que un valor absoluto, ya que en pacientes con enfermedad cardiaca es conocido que no son el reflejo de un verdadero estado de volemia (21). El catéter de arteria pulmonar lo reservamos para casos de disfunción ventricular severa en pacientes con CMP; en este caso, en cuatro de las cinco pacientes. En nuestra paciente con síndrome de Eissenmenger definimos no usar catéter de arteria pulmonar, ya que en este grupo existe mucha controversia acerca de su uso, debido al riesgo de desarrollar arritmias ventriculares y ruptura de la arteria pulmonar (22).
Profilaxis para endocarditis bacteriana
En cuanto a la profilaxis antibiótica para endocarditis bacteriana, el Colegio Americano de Ginecología y Obstetricia (ACOG) determinó, en el 2007, no suministrar ninguna profilaxis en caso de parto vaginal o cesárea en ausencia de infección (23). En pacientes con lesiones de alto riesgo con infecciones establecidas que puedan causar bacteriemia, la infección debe ser tratada y el régimen antibiótico debe cubrir gérmenes causantes de endocarditis.
Las guías de adulto con enfermedad cardiaca congénita en el 2008 publicadas por ACC/AHA consideran que es recomendable administrar proilaxis antes del parto vaginal, al momento de la ruptura de membranas en pacientes de alto riesgo, como son los que tienen válvulas cardiacas protésicas o material protésico usado para reparar válvulas, o en paciente con enfermedad cardiaca cianosante con cirugía paliativa o no corregida (24,25).
Sin embargo, debido a la simplicidad, lo inocuo de la proilaxis y lo impredecible de las complicaciones del parto, como desgarros grado IV, cateterización uretral en pacientes con bacteriuria inadvertida, etc., nosotros hacemos profilaxis en pacientes con lesiones valvulares, presencia de cortocircuitos por defectos septales y aquellas pacientes con materiales protésicos valvulares y cortocircuitos artiiciales (cirugías paliativas en enfermedad congénita) (26).
CONCLUSIONES
La implementación de un protocolo universal de estratiicación del riesgo de muerte y de eventos cardiovasculares mayores en el grupo de pacientes obstétricas con enfermedad cardiaca y la creación de grupos interdisciplinarios en los que el anestesiólogo hace parte fundamental del manejo de estas pacientes, podría permitir que el manejo periparto sea enfocado a minimizar la posibilidad de complicaciones y a mejorar los resultados. En nuestra serie no se presentó ningún evento de mortalidad y se evidenció una baja incidencia de complicaciones cardiovasculares asociada. El uso racional de técnicas anestésicas con las cuales el anestesiólogo esté más familiarizado, y basado en "metas hemodinámicas", permitiría un manejo óptimo que se correlacione con un buen desenlace materno y perinatal.
AGRADECIMIENTOS
Los autores agradecen a todo el personal de enfermería de la Unidad de Alta Dependencia de la Clínica del Prado, en Medellín, Colombia.
REFERENCES
1.Lewis G. The Confidential Enquiry into Maternal and Child Health (CEMACH). Saving Mothers. Lives: reviewing maternal deaths to make motherhood safer-2003-2005. (internet) London: CEMACH; 2007 Dic. (citado 20/02 2010). 12 p. Disponible en: http://www.cmace.org.uk/getattachment/05f68346-816b-4560-b1b9-af24fb633170/Saving-Mothers%E2%80%99-Lives-2003-2005_ExecSumm.aspx. [ Links ]
2.Van Mook WN, Peeters L. Severe cardiac disease in pregnancy, part II: impact of congenital and acquired cardiac diseases during pregnancy. Curr Opin Crit Care. 2005;11(5):435-48. [ Links ]
3.Perloff JK. Congenital heart disease and pregnancy. Clin Cardiol. 1994;17(11):579-87. [ Links ]
4.Fretts RC, Schmittdiel J, McLean FH, Usher RH, Goldman MB. Increased maternal age and the risk of fetal death. N Engl J Med. 1995;333(15):953-7. [ Links ]
5.Cunningham FG, Leveno KJ. Childbearing among older women--the message is cautiously optimistic. N Engl J Med. 1995;333(15):1002-4. [ Links ]
6.Dildy GA. Critical care obstetrics. 4th Ed. Malden: Blackwell; 2004. [ Links ]
7.Siu SC, Sermer M, Colman JM, Alvarez AN, Mercier LA, Morton BC, et al. Prospective multicenter study of pregnancy outcomes in women with heart disease. Circulation. 2001;104(5):515-21. [ Links ]
8.Khairy P, Ouyang DW, Fernandes SM, Lee-Parritz A, Economy KE, Landzberg MJ. Pregnancy outcomes in women with congenital heart disease. Circulation. 2006;113(4):517-24. [ Links ]
9.Bonow RO, Carabello BA, Chatterjee K, de Leon AC Jr, Faxon DP, Freed MD, et al. 2008 Focused update incorporated into the ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): endorsed by the Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. Circulation. 2008;118(15):e523-661. [ Links ]
10.Vahanian A, Baumgartner H, Bax J, Butchart E, Dion R, Filippatos G, et al. Guidelines on the management of valvular heart disease: The Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology. Eur Heart J. 2007;28(2):230-68. [ Links ]
11.Elkayam U, Ostrzega E, Shotan A, Mehra A. Cardiovascular problems in pregnant women with the Marfan syndrome. Ann Intern Med. 1995;123(2):117-22. [ Links ]
12.Drenthen W, Pieper PG, Roos-Hesselink JW, van Lottum WA, Voors AA, Mulder BJ, et al. Outcome of pregnancy in women with congenital heart disease: a literature review. J Am Coll Cardiol. 2007;49(24):2303-11. [ Links ]
13.Pearson GD, Veille JC, Rahimtoola S, Hsia J, Oakley CM, Hosenpud JD, et al. Peripartum cardiomyopathy: National Heart, Lung, and Blood Institute and Office of Rare Diseases (National Institutes of Health) workshop recommendations and review. JAMA. 2000;283(9):1183-8. [ Links ]
14.Hibbard JU, Lindheimer M, Lang RM. A modified definition for peripartum cardiomyopathy and prognosis based on echocardiography. Obstet Gynecol. 1999;94(2):311-6. [ Links ]
15.Habli M, O'Brien T, Nowack E, Khoury S, Barton JR, Sibai B. Peripartum cardiomyopathy: prognostic factors for long-term maternal outcome. Am J Obstet Gynecol. 2008;199(4):415.e1-5. [ Links ]
16.Karnad DR, Lapsia V, Krishnan A, Salvi VS. Prognostic factors in obstetric patients admitted to an Indian intensive care unit. Crit Care Med. 2004;32(6):1294-9. [ Links ]
17.Kiely DG, Condliffe R, Webster V, Mills GH, Wrench I, Gandhi SV, et al. Improved survival in pregnancy and pulmonary hypertension using a multiprofessional approach. BJOG. 2010;117(5):565-74. [ Links ]
18.Langesaeter E, Dragsund M, Rosseland LA. Regional anaesthesia for a Caesarean section in women with cardiac disease: a prospective study. Acta Anaesthesiol Scand. 2010;54(1):46-54. [ Links ]
19.Ioscovich AM, Goldszmidt E, Fadeev AV, Grisaru-Granovsky S, Halpern SH. Peripartum anesthetic management of patients with aortic valve stenosis: a retrospective study and literature review. Int J Obstet Anesth. 2009;18(4):379-86. [ Links ]
20.Bonnin M, Mercier FJ, Sitbon O, Roger-Christoph S, Jais X, Humbert M, et al. Severe pulmonary hypertension during pregnancy: mode of delivery and anesthetic management of 15 consecutive cases. Anesthesiology. 2005;102(6):1133-7;discussion 5A-6A. [ Links ]
21.Mittnacht AJ, Fanshawe M, Konstadt S. Anesthetic considerations in the patient with valvular heart disease undergoing noncardiac surgery. Semin Cardiothorac Vasc Anesth. 2008;12(1):33-59. [ Links ]
22.Amgad N. Makaryus AF, Johnson M. Pregnancy in the patient with Eisenmenger's Syndrome. Mt Sinai J Med. 2006;73(7):1033-6. [ Links ]
23.ACOG Committee Opinion No. 421, November 2008: antibiotic prophylaxis for infective endocarditis. Obstet Gynecol. 2008 Nov;112(5):1193-4. [ Links ]
24.Warnes CA, Williams RG, Bashore TM, Child JS, Connolly HM, Dearani JA, et al. ACC/AHA 2008 Guidelines for the Management of Adults with Congenital Heart Disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to develop guidelines on the management of adults with congenital heart disease). Circulation. 2008;118(23):e714-833. [ Links ]
25.Wilson W, Taubert KA, Gewitz M, Lockhart PB, Baddour LM, Levison M, et al. Prevention of infective endocarditis: guidelines from the American Heart Association: a guideline from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee, Council on Cardiovascular Disease in the Young, and the Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and the Quality of Care and Outcomes Research Interdisciplinary Working Group. Circulation. 2007;116(15):1736-54. [ Links ]
26.Pijuan Domenech A, Gatzoulis MA. Pregnancy and heart disease. Rev Esp Cardiol. 2006;59(9):971-84. [ Links ]
Conflicto de intereses: ninguno declarado. Este estudio fue financiado por los autores. No se recibió financiación externa.











 text in
text in