Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Colombian Journal of Anestesiology
versão impressa ISSN 0120-3347
Rev. colomb. anestesiol. vol.41 no.2 Bogotá abr./jun. 2013
https://doi.org/10.1016/j.rca.2013.03.002
http://dx.doi.org/10.1016/j.rca.2013.03.002
Investigación científica y tecnológica
Manejo de la temperatura en el perioperatorio y frecuencia de hipotermia inadvertida en un hospital general
Temperature management during the perioperative period and frequency of inadvertent hypothermia in a general hospital
Caridad Greta Castillo Monzóna,*, César Augusto Candia Aranaa, Hugo Antonio Marroquín Valzb, Fernando Aguilar Rodrígueza, Jairo Julián Benavides Mejíac y José Antonio Alvarez Gómeza
a Especialista en Anestesiología y Reanimación, Seruicio de Anestesiología y Reanimación, Complejo Hospitalario Universitario de Cartagena, Cartagena, Murcia, España
b Médico de Urgencias, Seruicio de Urgencias, Magister en Administración, Seruicio de Urgencias, Complejo Hospitalario Uniuersitario de Cartagena, Cartagena, Murcia, España
c Médico Residente de tercer año de Anestesiología, Seruicio de Anestesiología y Reanimación, Complejo Hospitalario Uniuersitario de Cartagena, Cartagena, Murcia, España
* Autor para correspondencia: Calle Vicenza n.° 29, Polígono Santa Ana, 30310 Cartagena, Murcia, España. Correo electrónico: gretacastillo9@hotmail.com (C.G. Castillo Monzón).
© 2012 Sociedad Colombiana de Anestesiología y Reanimación. Publicado por Elsevier España, S.L. Todos los derechos reservados.
INFORMACION DEL ARTICULO
Historia del artículo: Recibido el 20 de noviembre de 2012 Aceptado el 14 de febrero de 2013
On-line el 11 de abril de 2013
Resumen
Introducción: La hipotermia perioperatoria está asociada con mayor morbimortalidad, por lo que la temperatura del paciente quirúrgico debería ser una preocupación fundamental; sin embargo, es el parámetro fisiológico menos valorado.
Objetivos: Evaluar el manejo de la temperatura en el perioperatorio, determinar la frecuencia de hipotermia inadvertida y los factores relacionados.
Material y métodos: Estudio prospectivo observacional en pacientes adultos programados para procedimiento quirúrgico con tiempo > 30 min de anestesia. La hipotermia se definió como una temperatura de la piel de la frente <35,9°C. Se planteó la hipótesis nula de no diferencia entre los pacientes con normotermia e hipotermia. La comparación de las variables cuantitativas fue analizada con la prueba t de Student y las cualitativas con la prueba del Chi cuadrado, y después se realizó un análisis de regresión logística. Resultados: Se incluyeron 167 pacientes consecutivos; la monitorización intraoperatoria de la temperatura se usó en el 10% de los pacientes, el uso de líquidos intravenosos tibios y calentamiento con aire forzado en el 78 y el 63%, respectivamente. La frecuencia de hipotermia inadvertida fue del 56,29%, asociada a edad > 65 años, sexo femenino e índice de masa corporal >30kg/m2. Esta última variable podría estar influenciada por el método de medición de la temperatura.
Conclusiones: Las medidas de calentamiento sin monitorización de la temperatura no tienen el efecto esperado. La frecuencia elevada de hipotermia inadvertida hace necesaria una guía de actuación de prevención y manejo en especial en pacientes de riesgo, que en este estudio fueron edad > 65 años y sexo femenino.
Palabras clave: Anestesia, Hipotermia, Regulación de la temperatura corporal, Periodo perioperatorio.
© 2012 Sociedad Colombiana de Anestesiología y Reanimación. Publicado por Elsevier España, S.L. Todos los derechos reservados.
Abstract
Introduction: Perioperative hypothermia is associated with increased morbidity and mortality. Consequently, surgical patient temperature should be the fundamental concern but, nonetheless, it is still the least valued physiological parameter.
Objectives: To assess temperature management during the perioperative period and determine the frequency of inadvertent hypothermia and related factors.
Material and methods: Prospective observational study in adult patients scheduled for surgical procedure with anesthesia time ≥30 minutes. Hypothermia is defined as a forehead skin
temperature ≤35.9 ◦C. The null hypothesis of no difference between patients with normothermia and hypothermiawas proposed. Comparison of quantitative variableswas analyzed
with the Student “t” test, and the Chi square was used for the qualitative variables. The analysis was followed by a logistic regression analysis.
Results:We included 167 consecutive patients; intraoperative monitoring of temperaturewas used in 10% of patients, and the use ofwarm intravenous fluids and forced air heating in 78%
and 63%, respectively. The frequency of inadvertent hypothermia was 56.29%, associated with age ≥65 years, female gender and BMI≥30 kg/m2. This last variable might have been influenced by the method of temperature measurement.
Conclusion:Warming measures without temperature monitoring do not result in the desired effect. The high frequency of inadvertent hypothermia requires action guidelines for prevention
and management, especially in high-risk patients who, in this study, were patients≥65 years of age and females.
Keywords: Anesthesia, Hypothermia, Body temperature regulation, Perioperative period
© 2012 Sociedad Colombiana de Anestesiología y Reanimación. Published by Elsevier España, S.L. All rights reserved
Introducción
Hay evidencia que la hipotermia se asocia a complicaciones sistémicas1"6 y altera la farmacocinética y la farmacodi-namia de los agentes anestésicos7"11. La alteración de la termorregulación perioperatoria más frecuente es la hipotermia inadvertida12. La incidencia reportada tiene un amplio rango de variación (del 6 al 90%13"17), dependiendo del tipo de cirugía, y presenta un alto potencial de complicaciones1 que incluyen el aumento de la pérdida sanguínea2'3, episodios cardiacos mórbidos4, compromiso con la cicatrización e infección de las heridas5'6, y aumento de la mortalidad18.
La monitorización de la temperatura en el intraoperatorio comenzó a hacerse popular a inicios de los años sesenta. Han pasado más de 50 años y este parámetro fisiológico no está aún rigurosamente monitorizado ni manejado por el anestesió logo a pesar de conocerse que, correctamente tratada, mejora el resultado final del paciente quirúrgico19'20.
Son pocas las recomendaciones que se han dado en relación a la temperatura. Las guías del Colegio Americano de Cardiología de 2007 sobre el cuidado y la evaluación cardiovascular perioperatorios para cirugía no cardiaca recomiendan, como clase i (nivel B), el mantenimiento de la normotermia perioperatoria21. La guía de la Sociedad Americana de Aneste-siólogos (ASA)22 se refiere a la temperatura en forma escueta: «La temperatura debe ser periódicamente valorada durante la recuperación anestésica». En Inglaterra, el Instituto Nacional para la Salud y la Excelencia Clínica (NICE) publicó en 2008 unas guías para el manejo de la hipotermia inadvertida en el perioperatorio haciendo recomendaciones para su adecuado manejo tanto en el preoperatorio como en el intraoperatorio y el postoperatorio23.
El objetivo del estudio fue evaluar cómo es el manejo de la temperatura en el perioperatorio, determinar la frecuencia de la hipotermia inadvertida y los factores relacionados con su presencia.
Material y métodos
El protocolo de este estudio prospectivo observacional fue aprobado por el Comité de Ética e Investigación Clínica del Complejo Hospitalario Universitario de Cartagena (Murcia, España). Se incluyeron de forma consecutiva los pacientes adultos programados para algún tipo de cirugía y sometidos a diferentes técnicas anestésicas con duración mayor a 30 min. Se excluyeron las pacientes obstétricas y la población pediátrica.
Los datos registrados para el estudio fueron los siguientes: sexo, edad en años, peso en kilogramos, talla en centímetros, índice de masa corporal (IMC), clasificación ASA, la especialidad quirúrgica, el tiempo y el tipo de anestesia, el uso de monitorización de la temperatura, el uso de líquidos tibios intravenosos y el uso de sistemas de calentamiento de aire forzado en el intraoperatorio, y las manifestaciones clínicas de hipotermia presentadas por el paciente en la unidad de reanimación. La edad se clasificó en 2 grupos etarios: menor de 65 años y mayor o igual a 65 años; el IMC se clasificó como menor de 30 kg/m2 y mayor o igual a 30 kg/m2. La temperatura de la superficie de la piel de la frente se registró inmediatamente al ingreso del paciente en la unidad de reanimación y una hora después; esto en relación con el tiempo de permanencia del paciente en la unidad de reanimación, que suele ser superior a la hora pero menor de 2 h. El uso o no de la moni-torización intraoperatoria de la temperatura y/o las técnicas empleadas para mantener la temperatura fue a criterio del anestesiólogo; esta información se recogió verbalmente del equipo de anestesia a la llegada del paciente a la unidad de reanimación. Durante el estudio, para controlar el sesgo o error sistemático se tomó la medida de no notificar a los anestesiólogos del seguimiento realizado en la unidad de reanimación, con el fin de que ningún anestesiólogo cambiara su conducta en cuanto a la monitorización y a las estrategias empleadas para el manejo de la temperatura. Se registraron las manifestaciones clínicas de hipotermia durante su permanencia en la unidad de reanimación.
Cuando se usó la medición intraoperatoria de la temperatura se realizó con sensores reusables o descartables de la máquina de anestesia Ohmeda Aestiva 3000, con registro esofágico inferior o nasofaríngeo. En su caso, el sistema de calentamiento de aire forzado utilizado (manta/colchón) fue Bair Hugger unidades 750 y 775. Los líquidos intravenosos fueron calentados en baños termostáticos para agua (Precisterm P Selecta) a temperatura de 40°C.
La medición de la temperatura se hizo a 5 cm de la superficie de la piel de la frente, en la unidad de reanimación, y se utilizó el termómetro infrarrojo PCE-FIT 10 (PCE Deutschland GmbH, precisión ± 0,2 °C en el rango de 36 a 39 °C y de ± 0,3 °C de 32 a 35,9°C, rango de medición de 32 a 42,4°C), que es el equipo del cual se dispone en esta área. El equipo fue mantenido y calibrado con las instrucciones del fabricante para obtener una lectura equivalente a la temperatura central.
La hipotermia se definió como una temperatura igual o menor a 35,9°C en 3 niveles: hipotermia leve, 35-35,9°C; hipotermia moderada, 34-34,9°C, e hipotermia severa, < 33,9°C17.La muestra se seleccionó por conveniencia. En las pruebas estadísticas se planteó la hipótesis nula de no diferencia entre los pacientes normotérmicos y los que presentaron hipotermia a su llegada a la unidad de reanimación. La comparación de las variables cuantitativas fue realizada con la prueba t de Student y de las variables cualitativas con la prueba de Chi cuadrado. Realizada esta comparación, se procedió a aplicar un análisis multivariado (regresión logística binaria), en el que se incluyeron las variables en las que se obtuvo un valor de p < 0,08, y además se convirtieron a forma dicotómica las variables politómicas. El análisis de los datos se realizó con el paquete estadístico SPSS versión 12 (SPSS Inc., Chicago, IL) y la hoja de cálculo Excel versión 12 (Microsoft Corporation). Se consideró en todas las pruebas un valor de p < 0,05 como estadísticamente significativo.
Resultados
Se obtuvieron los datos de 200 pacientes consecutivos. Treinta y tres pacientes fueron excluidos por tener información incompleta, incluyéndose para el análisis estadístico 167 pacientes.
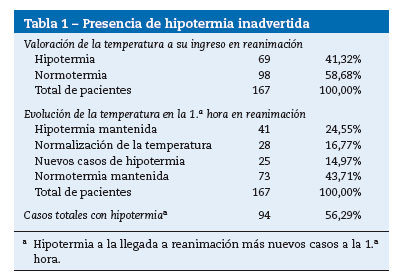
La hipotermia se presentó en el 56,29% de los pacientes (94/167); en el 41,32% fue detectada a su llegada a la unidad de reanimación y en el 14,97%, a la hora de su permanencia en esta área. En la tabla 1 se muestra la evolución de la temperatura. De los pacientes que presentaron hipotermia a su llegada a reanimación, el 40,72% (68 pacientes) presentaron hipotermia leve y el 0,6% (un paciente, de 89 años), hipotermia moderada. El rango de edad fue de 17 a 89 años. Cuando se compararon las características de los pacientes (análisis biva-riable), se encontraron diferencias significativas (p < 0,02) entre el grupo de normotermia e hipotermia en grupo etario, sexo, obesidad (IMC > 30) y clasificación ASA. Se incluyeron, además, para la regresión logística la especialidad quirúrgica y el tipo de anestesia por tener un valor p = 0,08 (tabla 2).
En el análisis de regresión logística binaria fueron encontrados como factores independientes relacionados a la hipotermia (tabla 3): grupo etario >65 años, IMC>30kg/m2 y sexo femenino, los 3 con valor de p < 0,03.
En cuanto al manejo de la temperatura en el intraoperato-rio, se encontró que se monitorizó la temperatura en el 10% de los pacientes, y los métodos de calentamiento usados fueron los líquidos intravenosos tibios en el 78% y un sistema de calentamiento de aire forzado en el 63% de los pacientes, sin que se encontraran diferencias estadísticamente significativas entre los pacientes normotérmicos y los que presentaron hipotermia (tabla 2). Ningún paciente con anestesia neuroa-xial fue monitorizado en el intraoperatorio. No se encontró relación entre medidas para manejar la temperatura con la presencia de factores de riesgo de hipotermia como el ASA y/o la edad extrema, ni con el uso de líquidos calientes y/o calentamiento con aire forzado.
Durante su permanencia en la unidad de reanimación, el 9% (15/167) de los pacientes manifestó tener frió y/o se objetivó la presencia de escalofríos, lo cual fue manejado con el uso de la manta de calentamiento de aire forzado; en un paciente se usó este sistema por encontrarse hipotérmico, aunque sin manifestación clínica.
Discusión
En este estudio encontramos un alto porcentaje de hipotermia inadvertida (56,29%), cifra que está dentro del amplio rango de variación de la incidencia reportada en la literatura, del 6 al 90%13"17. De las variables consideradas para el estudio solamente se encontraron asociadas a la hipotermia la edad > 65 años, el sexo femenino y el IMC > 30.
En el análisis bivariable no se encontró relación entre la hipotermia y el tipo de anestesia, el tiempo anestésico, la especialidad quirúrgica, el uso de monitorización intraoperatoria de la temperatura, el uso de líquidos intravenosos tibios y el uso de sistema de calentamiento de aire forzado. Además, con la regresión logística se excluyó la clasificación ASA. Es necesario mencionar que algunos de estos factores son considerados en las recomendaciones a tener en cuenta para la prevención de la hipotermia inadvertida23.
Sabemos que la temperatura del cuerpo no es homogénea y que la temperatura central es el mejor indicador del estado térmico en los humanos. Su determinación en la arteria pulmonar es el gold standard, aunque tiene el inconveniente de ser invasiva. En el intraoperatorio los sitios de monitoriza-ción semiinvasivos aceptables son la nasofaringe, el esófago y la vejiga urinaria19. En la revisión sistemática de la literatura se encuentra que la medida oral no invasiva es válida y segura para la determinación de la temperatura central19, por lo que sería la mejor alternativa en el paciente despierto. Langham et al.24 encontraron que la temperatura oral electrónica era la más adecuada para el uso en el postoperatorio, seguida por la temperatura axilar. Höcker et al.25 demostraron que la medida de la temperatura sublingual es una modalidad buena y práctica para monitorizar la temperatura periopera-toria en los pacientes anestesiados y despiertos.
En este estudio se usó un termómetro infrarrojo de piel y se midió la temperatura a nivel de la región frontal por ser el equipo con el que contamos. Sabemos que la temperatura de los tejidos periféricos depende de la exposición, de la temperatura central y de la termorregulación vasomotora12.La temperatura axilar y de la piel es propensa a artefactos26, por lo que podría no ser la mejor opción. No se realizó ninguna corrección de la medición con la temperatura central, como sugieren varios autores27-29 (piel de la frente 0,7 °C menor que la temperatura central) por haber sido calibrado el equipo en su primer uso con una medición de la temperatura central como lo recomienda el fabricante; además, esta calibración es estable por periodos de uno a 3 años.
Se han reportado como factores de riesgo para la hipotermia perioperatoria, basados en evidencia débil (nivel B, clase IIa o IIb), la edad mayor de 60 años, el sexo femenino y el nivel alto del bloqueo espinal. Factores de riesgo con evidencia insuficiente (nivel C, clase IIa o IIb) son el IMC por debajo de lo normal, el IMC normal, la duración del procedimiento, el área de superficie no cubierta, la duración de la anestesia y la diabetes mellitus30. De los factores asociados a la hipotermia encontrados en este estudio, la variable IMC > 30 no se correlaciona con lo publicado. Se ha reportado que el mayor peso corporal es un factor protector contra la hipotermia central31,32. Los individuos obesos tienen grasa corporal con baja conductividad termal que reduce la pérdida de calor por la piel y minimiza la hipotermia32. Además, en el paciente obeso el umbral vasoconstrictor a una temperatura ambiental baja es alto33. Teniendo en cuenta lo previamente mencionado, el resultado encontrado en este estudio podría estar en relación con el método de medición usado, dado que la disminución de la pérdida cutánea de calor sería un mecanismo especialmente acentuado en el paciente obeso.
Por otro lado, el NICE23 ha definido como pacientes de alto riesgo a los que presentan 2 o más de los siguientes factores: ASA mayor de i, temperatura preoperatoria menor de 36 °C, anestesia combinada, cirugía intermedia o mayor y los pacientes con antecedentes cardiovasculares. Recomiendan medir la temperatura una hora antes de la inducción, en el intraoperatorio cada 30min, en el postoperatorio al ingreso en reanimación y cada 15min hasta que alcance los 36 ° C, y luego cada hora hasta que alcance los 36,5 °C.
En este estudio ningún paciente fue precalentado. El preca-lentamiento es una recomendación actual15,23,34,35 que atenúa considerablemente la disminución inicial en la temperatura del paciente anestesiado al impedir la pérdida de calor por redistribución. Mientras esta técnica no se implemente, el calentamiento activo intraoperatorio seguirá siendo la principal táctica para combatir la hipotermia. Podemos señalar que la falta de precalentamiento del paciente y el bajo porcentaje de uso de la monitorización intraoperatoria de la temperatura podría explicar por qué no encontramos diferencia estadísticamente signiicativa entre los pacientes que presentaron hipotermia y los normotérmicos, a pesar del uso de líquidos intravenosos tibios y de sistemas de calentamiento con aire forzado. Cuando no se precalienta, las técnicas de calentamiento intraoperatorio incluyendo las de calentamiento con aire forzado fallan en eliminar la caída inicial de la temperatura34.
La hipotermia inadvertida debe ser prevenida. Es más fácil mantener la normotermia intraoperatoria que recalentar a los pacientes en el postoperatorio36. En el intraoperatorio el paciente esta vasodilatado y la transferencia termal es más fácil que cuando se realiza con el paciente en vasoconstricción, que es lo que ocurre en el postoperatorio. La vasoconstricción periférica limita el flujo de calor hacia el compartimiento periférico, lo que aumenta el gradiente debido a la acumulación del calor generado por el metabolismo tisular en el compartimiento central37.
Los 2 mecanismos más importantes que causan pérdida de calor en el quirófano en orden de importancia son la radiación y la convección. La radiación produce el 60% de las pérdidas, y por ello debe mantenerse en las salas de operaciones una humedad relativa >45% con una temperatura entre 21 y 24 °C en pacientes adultos y 24-26 °C en pediatría. Las guías del NICE dicen en relación a este punto: «La temperatura del quirófano debe ser al menos de 21 °C mientras el paciente está expuesto». ASPAN recomienda mantener la temperatura en el quirófano entre 20 y 25 °C (clase i, nivel C). En este estudio no se consignaron la temperatura ni la humedad de los quirófanos, y este podría ser un factor importante en la presentación de hipotermia asociada al tipo de cirugía que se encuentra29.
El calentamiento con aire forzado, disponible desde 1980, funciona mediante la infusión de aire caliente que escapa por pequeños orificios que se dirigen hacia el paciente. Ha demostrado ser el único método eficiente para mantener la temperatura y calentar a los pacientes en el perioperatorio38-40. La eicacia del sistema se refuerza cubriendo la manta con una sábana de algodón, y tiene la ventaja de ser flexible, lo que posibilita el recubrimiento óptimo de la supericie cutánea, cualquiera que sea la posición quirúrgica. Las complicaciones reportadas al uso de los sistemas Bair Hugger son escasas: un caso de quemadura de tercer grado41 y un caso de ablandamiento térmico del tubo traqueal42.
Se ha encontrado que la administración de fluidos pre-calentados versus el calentamiento en línea son igualmente efectivos para prevenir la hipotermia perioperatoria43. El calentamiento de fluidos no calienta al paciente, pero minimiza la incidencia de hipotermia perioperatoria44. En los equipos que permiten calentamiento en línea los sueros se calientan a 38 °C, y cuando se calientan en gabinetes deben alcanzar los 41 °C; en ambos casos, cuando llegan al paciente están a 37 °C. En el presente estudio ningún paciente recibió fluidos calentados en línea a pesar de contarse con el recurso. El Colegio Americano de Cirujanos, en su manual Advanced Trauma Life Support (ATLS) recomienda calentar los fluidos de resucitación en microondas a 39 °C. Las bolsas de 500 mi se pueden calentar a 400 W durante 100 s o a 800 W durante 50 s, por lo que una alternativa que no acarrea costo es calentar los sueros en microondas45.
Está ampliamente justificada la implementación sistemática del manejo perioperatorio de la temperatura. La evidencia apoya el inicio del calentamiento activo antes de la operación y la monitorización durante todo el periodo perioperatorio para prevenir la hipotermia. El uso de métodos de calentamiento está soportado por la evidencia, pero solo se optimiza su empleo cuando se monitoriza la temperatura, pues ¿cómo vamos a manejar este parámetro si no lo hemos medido?46.
En conclusión, las medidas de calentamiento sin monitorización de la temperatura no tienen el efecto esperado de disminuir la presencia de hipotermia. Dada la elevada incidencia de hipotermia inadvertida encontrada a pesar de contar con los recursos adecuados para la monitorización y el manejo de la temperatura, es necesario estandarizar e implemen-tar una guía de actuación para su prevención y manejo, la cual debe incluir, entre otras medidas, el precalentamiento, la monitorización de la temperatura antes, durante y después de la anestesia para todos los pacientes con énfasis en los grupos en riesgo, que en este estudio fueron la edad > 65 años y el sexo femenino.
Financiación
Recursos propios de los autores.
Conflictos de intereses
Los autores declaran no tener ningún conflicto de intereses.
REFERENCIAS
1. Roth JV. Some unanswered questions about temperature management. Anesth Analg. 2009;109:1695-9. [ Links ]
2. Rajagopalan S, Mascha E, Na J, Sessler DI. The effects of mild perioperative hypothermia on blood loss and transfusion requirement. Anesthesiology. 2008;108:71-7. [ Links ]
3. Tse EY, Cheung WY, Ng KF, Luk KD. Reducing perioperative blood loss and allogeneic blood transfusion in patients undergoing major spine surgery. J Bone Joint Surg Am. 2011;93:1268-77. [ Links ]
4. Frank SM, Fleisher LA, Breslow MJ, Higgins MS, Olson KF, Kelly S, et al. Perioperative maintenance of normothermia reduces the incidence of morbid cardiac events. A randomized clinical trial. JAMA. 1997;277:1127-34. [ Links ]
5. Melling AC, Ali B, Scott EM, Leaper DJ. Effects of preoperative warming on the incidence of wound infection after clean surgery: a randomised controlled trial. Lancet. 2001;358:876-80. [ Links ]
6. Mauermann WJ, Nemergut EC. The Anesthesiologist's role in the prevention of surgical site infections. Anesthesiology. 2006;105:413-21. [ Links ]
7. Heier T, Caldwell JE. Impact of hypothermia on the response to neuromuscular blocking drugs. Anesthesiology. 2006;104:1070-80. [ Links ]
8. Heier T, Caldwell JE, Sessler DI, Miller RD. Mild intraoperative hypothermia increases duration of action and spontaneous recovery of vecuronium blockade during nitrous oxide-isofluorane anesthesia in humans. Anesthesiology. 1991;74:815-9. [ Links ]
9. Leslie K, Sessler DI, Bjorksten AR, Moayeri A. Mild hypothermia alters propofol pharmacokinetics and increases the duration of action of atracurium. Anesth Analg. 1995;80:1007-14. [ Links ]
10. Vitez TS, White PF, Eger E. Effects of hypothermia on halothane MAC and isoflurane MAC in the rat. Anesthesiology. 1974;41:80-1. [ Links ]
11. Sessler DI. Complications and treatment of mild hypothermia. Anesthesiology. 2001;95:531-43. [ Links ]
12. Sessler DI. Temperature monitoring and perioperative thermoregulation. Anesthesiology. 2008;109:318-38 [review] [ Links ].
13. Harper CM, Andrzejowski JC, Alexander R. Nice and warm. Br J Anaesth. 2008;101:293-5. [ Links ]
14. Knaepel A. Inadvertent perioperative hypothermia: a literatura review. J Perioper Pract. 2012;22:86-90. [ Links ]
15. Moola S, Lockwood C. Effectiveness of strategies for the management and/or prevention of hypothermia within the adult perioperative environment. Int J Evid Based Healthc. 2011;9:337-45. [ Links ]
16. Ross-Anderson DJ. A NICE idea or a high price to pay? Local assessment of national guidelines. Anaesthesia. 2009;64:330-1. [ Links ]
17. De Mattia AL, Barbosa MH, De Mattia Rocha A, Farias HL, Santos CA, Santos DM. Hipotermia en pacientes en el período perioperatorio. Rev Esc Enferm USP. 2012;46:60-6. [ Links ]
18. Karalapillai D, Story DA, Calzavacca P, Licari E, Liu YL, Hart GK. Inadvertent hypothermia and mortality in postoperative intensive care patients: retrospective audit of 5050 patients. Anaesthesia. 2009;64:968-72. [ Links ]
19. Torossian A. Thermal management during anaesthesia and thermoregulation standards for the prevention of inadvertent perioperative hypothermia. Best Pract Res Clin Anaesthesiol. 2008;22:659-68. [ Links ]
20. Hannenberg AA, Sessler DI. Improving perioperative temperature management. Anesth Analg. 2008;107:1454-7. [ Links ]
21. Fleisher LA, Beckman JA, Brown KA, Calkins H, Chaikof E, Fleischmann KE, et al., ACC/AHA. Guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery. J Am Coll Cardiol. 2007;50:1707-32. [ Links ]
22. American Society of Anesthesiologist Task Force on Postanesthetic Care. Practice guidelines for postanesthetic care: a report by the American Society of Anesthesiologists Task Force on Postanesthetic Care. Anesthesiology. 2002;96:742-52. [ Links ]
23. National Institute for Health and Clinical Evidence. Clinical practice guidelines: The management of inadvertent perioperative hypothermia in adults. Available from: www.nice.org.uk/CG65 [ Links ]
24. Langham GE, Maheshwari A, Contrera K, You J, Mascha E, Sessler DI. Noninvasive temperature monitoring in postanesthesia care units. Anesthesiology. 2009;111:90-6. [ Links ]
25. Höcker J, Bein B, Böhm R, Steinfath M, Scholz J, Horn EP. Correlation, accuracy, precision and practicability of perioperative measurement of sublingual temperature in comparison with tympanic membrane temperature in awake and anaesthetised patients. Eur J Anaesthesiol. 2012;29:70-4. [ Links ]
26. de Silva A. Anesthetic monitoring. In: Basic of anesthesia. 6th ed. Philadelphia: Elsevier Saunders Inc.; 2011. p. 817. [ Links ]
27. American Society of Anesthesiologists. Standards for basic anesthetic monitoring; 2010. http://asahq.org/For-Healthcare-Professionals/~/media/For%20Members/documents/Standards %20Guidelines%20Stmts/Basic%20Anesthetic%20Monitoring %202011.ashx [accessed 13.01.11] [ Links ].
28. Manuel Blanco-Pajón. ¿Es recomendable el monitoreo de la temperatura en los pacientes bajo anestesia? Implicaciones clínicas y anestésicas. Rev Mex Anestesiología. 2010;33:S70-5. [ Links ]
29. Modell JG, Katholi CR, Kumaramangalam SM, Hudson EC, Graham D. Unreliability of the infrared tympanic thermometer in clinical practice: a comparative study with oral mercury and oral electronic thermometers. South Med J. 1988;91:649-54. [ Links ]
30. Hooper VD, Chard R, Clifford T, Fetzer S, Fossum S, Godden B, et al. ASPAN's evidence-based clinical practice guideline for the promotion of perioperative normothermia: second edition. J Perianesth Nurs. 2010;25:346-65. [ Links ]
31. Kongsayreepong S, Chaibundit C, Chadpaibool J, Komoltri C, Suraseranivongse S, Suwannanonda P, et al. Predictor of core hypothermia and the surgical intensive care unit. Anesth Analg. 2003;96:826-33. [ Links ]
32. Fernandes LA, Braz LG, Koga FA, Kakuda CM, Módolo NS, de Carvalho LR, et al. Comparison of peri-operative core temperature in obese and non-obese patients. Anaesthesia. 2012;67:1364-9. [ Links ]
33. Kasai T, Hirose M, Matsukawa T, Takamata A, Tanaka Y. The vasoconstriction threshold is increased in obese patients during general anaesthesia. Acta Anaesthesiol Scand. 2003;47:588-92. [ Links ]
34. Hart SR, Bordes B, Hart J, Corsino D, Harmon D. Unintended perioperative hypothermia. Ochsner J. 2011;11:259-70. [ Links ]
35. Andrzejowski J, Hoyle J, Eapen G, Turnbull D. Effect of prewarming on post-induction core temperature and the incidence of inadvertent perioperative hypothermia in patients undergoing general anaesthesia. Br J Anaesth. 2008;101:627-31. [ Links ]
36. Díaz M, Becker DE. Thermoregulation: physiological and clinical considerations during sedation and general anesthesia. Anesth Prog. 2010;57:25-32. [ Links ]
37. Matsukawa T, Sessler DI, Sessler AM, Schroeder M, Ozaki M, Kurz A, et al. Heat flow and distribution during induction of general anesthesia. Anesthesiology. 1995;82:662-73. [ Links ]
38. Torrie JJ, Yip P, Robinson E. Comparison of forced-air warming and radiant heating during transurethral prostatic resection under spinal anaesthesia. Anaesth Intensive Care. 2005;33:733-8. [ Links ]
39. Leung KK, Lai A, Wu A. A randomised controlled trial of the electric heating pad vs forced-air warming for preventing hypothermia during laparotomy. Anaesthesia. 2007;62:605-8. [ Links ]
40. Fanelli A, Danelli G, Ghisi D, Ortu A, Moschini E, Fanelli G. The efficacy of a resistive heating under-patient blanket versus a forced-air warming system: a randomized controlled trial. Anesth Analg. 2009;108:199-201. [ Links ]
41. Truell KD, Bakerman PR, Teodori MF, Maze A. Third-degree burns due to intraoperative use of a Bair Hugger warming device. Ann Thorac Surg. 2000;69:1933-4. [ Links ]
42. Ayala JL, Coe A. Thermal softening of tracheal tubes: an unrecognized hazard of the Bair Hugger active patient warming system. Br J Anaesth. 1997;79:543-5. [ Links ]
43. Andrzejowski JC, Turnbull D, Nandakumar A, Gowthaman S, Eapen G. A randomised single blinded study of the administration of pre-warmed fluid vs. active fluid warming on the incidence of peri-operative hypothermia in short surgical procedures. Anesthesia. 2010;65:942-5. [ Links ]
44. Insler SR, Sessler DI. Perioperative thermoregulation and temperature monitoring. Anesthesiol Clin. 2006;24: 823-37. [ Links ]
45. Lindhoff GA, Mac G, Palmer JH. An assessment of the thermal safety of microwave warming of crystalloid fluids. Anaesthesia. 2000;55:251-4. [ Links ]
46. Nierman DM. Tools that we use: if you can't measure it, you can't manage it. Crit Care Med. 2007;35:312-3. [ Links ]











 texto em
texto em