Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.42 no.4 Bogotá Oct./Dec. 2014
https://doi.org/10.1016/j.rca.2014.05.007
http://dx.doi.org/10.1016/j.rca.2014.05.007
Revisión
Un resumen de la investigación en tromboelastografía
An overview of thrombelastography research
b Instructor Asociado, Anestesiología y Reanimación, Fundación Universitaria de Ciencias de la Salud, Hospital de San José, Bogotá, Colombia
c Profesor Titular, Anestesiología y Reanimación, Fundación Universitaria de Ciencias de la Salud, Hospital de San José, Bogotá, Colombia
d División de Investigaciones, Fundación Universitaria de Ciencias de la Salud, Anestesiología y Reanimación, Hospital de San José, Bogotá, Colombia
*Autor para correspondencia: División de Investigaciones, Fundación Universitaria de Ciencias de la Salud, Carrera 19 No. 8a - 32, Bogotá DC, Colombia. Correo electrónico: jarevalo@fucsalud.edu.co (J.J. Arevalo).
Recibido el 9 de octubre de 2013 - Aceptado el 27 de mayo de 2014
Resumen
Introducción: La tromboelastografía (TEG) es un método para valorar las características de la formación y destrucción del coágulo. Una variedad de aplicaciones han sido sugeridas en la literatura.
Objetivo: Proporcionar un resumen acerca del conocimiento actual de las aplicaciones de la TEG.
Métodos: Se realizó una búsqueda en la base de datos PubMed hasta julio de 2012 con el término «Thrombelastography [MeSH Terms]». Se analizaron artículos de estudios retrospectivos y prospectivos, revisiones y guías conteniendo información acerca de las aplicaciones de la TEG escritos en inglés y español.
Resultados: La búsqueda arrojó 3.139 artículos desde 1962. Se clasificaron en 8 categorías: 862 (27,6%) asociados a enfermedades no quirúrgicas, 294 (9,4%) a trasplante hepático, 711 (22,6%) a investigación básica, 174 (5,5%) a obstetricia, 228 (7,3%) a cirugía cardiovascular, 177 (5,6%) a otras cirugías, 234 (7,4%) a técnicas anestésicas y 459 (14,6%) a fármacos.
Conclusión: La TEG como herramienta diagnóstica y para guiar terapia transfusional está en aumento. La TEG aún continúa en estudio en diferentes áreas del conocimiento clínico y aún falta definir adecuadamente los alcances de esta técnica diagnóstica. Es evidente que se debe hacer un uso racional de la TEG, conocer a fondo sus fortalezas y debilidades y continuar explorando nuevas aplicaciones.
Palabras clave: Tromboelastografía, Cirugía General, Diagnóstico, Coagulación Sanguínea, Hemostasis.
Abstract
Introduction: Thrombelastography (TEG) is a method to assess clot formation and destruction. Various applications have been suggested in the literature.
Objective: To provide an overview of the current knowledge about TEG applications.
Methods: Adatabase search in PubMed was performed up to July 2012 using the term "Thrombelastography [MeSH Terms]". We analysed retrospective and prospective studies, reviews and guidelines with information about the applications of TEG written in English and Spanish.
Results: The search resulted in 3139 papers since 1962. These were classified in 8 categories: 862 (27.6%) in non-surgical diseases, 294 (9.4%) in liver transplant, 711 (22.6%) in basic research, 174 (5.5%) in obstetrics, 228 (7.3%) in cardiovascular surgery, 177 (5.6%) in other types of surgery, 234 (7.4%) in anaesthetic techniques, and 459 (14.6%) in relation with medications.
Conclusion: The application of TEG as a diagnostic tool and as a guide in transfusion therapy is increasing. Its use is still in development in different clinical fields and the advantages and limitations of this technique still have to be defined. It is evident that thrombelastography should be used with caution, and its strengths and weaknesses as well as new applications must continue to be explored.
Keywords: Thrombelastography, General Surgery, Diagnosis, Blood Coagulation, Hemostasis.
Introducción
La tromboelastografía (TEG) es la representación gráfica de la formación y destrucción del coágulo sanguíneo, así como de sus características de viscosidad y elasticidad1. Ha sido usada en la práctica clínica para detectar y cuantificar hipercoagulabilidad, hipocoagulabilidad, fibrinólisis, fuerza del coágulo y efectos de la terapia anticoagulante2. Recientemente este método diagnóstico es utilizado también en cirugía cardiovascular con circulación extracorpórea, neurocirugía, trauma y otras intervenciones quirúrgicas que comprometen el sistema hematológico3. Existen en el mercado varios métodos que valoran las propiedades viscoelásticas de la sangre junto con la TEG convencional (Haemosope Corporation, Niles, Illinois EE. UU.), que es la más referenciada en publicaciones nacionales1,4-6 y la cual es el objeto de este escrito. Dentro de las otras propuestas se destacan el ROTEM (Pentapharm GMBH, Munich, Alemania) y el Sonoclot Analyzer (Sienco Inc., Arvada, Colorado, EE. UU.). En la primera, la polimerización de la fibrina es detectada por la restricción a la oscilación de la copa en la que se deposita la muestra; en la segunda, por la restricción de la oscilación de un perno sumergido en la muestra, y en la tercera, por la restricción de la oscilación vertical de una sonda7.
En nuestro medio la TEG está tomando vigor en el uso clínico y quirúrgico. Muestra de ello es la existencia de publicaciones relacionadas con el entendimiento de la fisiología de la coagulación y principios de la TEG en la Revista Colombiana de Anestesiología1,4,5.
A pesar del aumento del acceso a las publicaciones que describen las nuevas implementaciones de la TEG, nuestra literatura carece de una revisión que las englobe desde sus inicios hasta el presente. El objetivo del presente artículo es proporcionar un resumen del conocimiento actual acerca de aplicaciones clínicas de la TEG.
Métodos
En esta revisión, los estudios fueron identificados mediante una búsqueda electrónica en la base de datos PubMed desde enero de 1962 hasta julio de 2012. Con el fin de hacer la búsqueda lo más sensible posible se empleó el Medical Subject Heading (término MeSH) «Thrombelastography». No se aplicó límite de idioma. Las listas de referencias de los artículos descargados fueron revisadas para la identificación de artículos adicionales por 3 investigadores (OMS, CCC y GAP). Se realizó una lectura de los títulos, resúmenes o textos completos de artículos en inglés o espa nol (nñ= 3.139) para realizar una clasificación según el tipo de uso sugerida por el estudio (fig. 1).
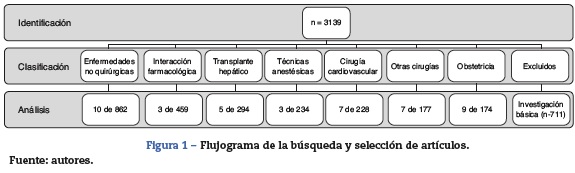
Las categorías de clasificación surgieron a medida que se hacía la revisión, según el objeto de estudio principal de cada artículo. Para el propósito de este estudio se aceptó la descripción de un uso de la TEG si los autores del artículo la describían como tal, en relación con una patología médica, una patología quirúrgica, un procedimiento diagnóstico o un procedimiento terapéutico. En la clasificación surgió una categoría que no correspondía a un uso de la TEG en seres humanos, principalmente artículos reportando resultados de investigación en ciencias básicas8,9, que fueron excluidos del análisis.
Para el análisis de cada categoría se seleccionaron las publicaciones más relevantes según el siguiente criterio (n = 44): revisiones sistemáticas y metaanálisis, artículos originales (experimentales o descriptivos), revisiones literarias. Con esa selección se extrajeron las conclusiones relacionadas con los usos y áreas de investigación de la TEG; estas son descritas por categoría en forma resumida. Las tendencias fueron analizadas a partir del número de publicaciones por año.
Resultados
Los primeros artículos identificados fueron publicados en el año 1963 (n= 84). A partir de esa fecha se observó una tendencia al aumento en el número de publicaciones por año hasta 1975 (n = 62). Posteriormente se observa una disminución constante en el número de publicaciones, hasta llegar al mínimo de publicaciones anual en el a no 1988 (n= 7). No se observaron cambios importantes en el número de publicaciones hasta el año 2004, cuando se inicia una tendencia al aumento en el número de publicaciones, con un pico final en el año 2010 (n= 174) (fig. 2).
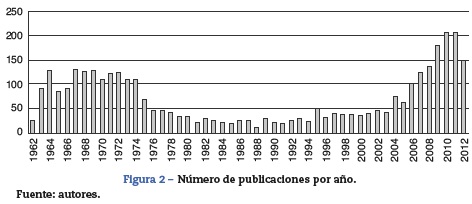
Usos de la tromboelastografía
Enfermedades no quirúrgicas
La TEG refleja la eficacia clínica del uso de concentrados de complejo protrombínico y factor VIIa recombinante7,10, al igual que guiando el manejo en la terapia de reposición de fibrinógeno11. El uso de la TEG es una alternativa en diferenciar patrones de coagulación anómalos, discrasias sanguíneas (en el seguimiento de pacientes sometidos a accidente ofídico o toxinas con potencial aparición de episodios hemorrágicos)12, en la detección de estados de hipercoagulabilidad y la capacidad de diferenciar patologías (accidente cerebrovascular isquémico y hemorrágico, neoplasias, síndrome urémico y tromboembolismo pulmonar)10,13-15, y para evaluar el estado de coagulación en neonatos16.
Interacción farmacológica
El uso de enoxaparina prolonga el tiempo R y se correlaciona con el pico de la actividad anti-Xa17. Algunos artículos demuestran un aumento de la actividad coagulante medida por TEG que ocurre a niveles leves y moderados de hemodilución con algunos cristaloides y coloides en trabajos in vitro18. En más del 40% de dilución disminuye la hipercoagulabilidad, y en el caso del dextran y el hydroxyethylstarch se convierte a un estado de hipocoagulación. La dilución con cristaloides y albúmina tiene que ser más de 5018.
A pesar de que dosis bajas de anticonceptivos orales (ACO) han sido asociados a trombosis venosa profunda a través de estudios epidemiológicos y cambios en varios factores de la cascada de la coagulación, bajas dosis de ACO no se han asociado a cambios significativos en los parámetros de la TEG hacia la hipercoagulabilidad en mujeres sin otros factores de riesgo19. Cabe resaltar que estos hallazgos no fundamentan el uso rutinario de la TEG en este tipo de pacientes.
Trasplante hepático
Los cambios en la hemostasia más marcados ocurren durante la fase anhepática y la fase inmediatamente posterior a la reperfusión del órgano, mayormente hiperfibrinólisis resultado de la acumulación de activador tisular de plasminógeno asociado a una depuración hepática inadecuadayala liberación de sustancias similares a la heparina (heparin-like substances)20. El algoritmo básico que se empleó para reponer productos sanguíneos se resume de la siguiente manera: el tiempo R aumentado indica el uso de plasma fresco congelado, la disminución en la amplitud máxima (MA) indica el uso de plaquetas y la disminución en el ángulo indica el uso de crioprecipitados21.
Además, se ha evaluado el uso de factor vii recombinante con TEG que se asoció a mejoría en la velocidad de formación y las características físicas del coágulo durante trasplante hepático.
Técnicas anestésicas
Kettner et al.22 reportan los cambios en los diferentes parámetros para evaluar la coagulación, incluyendo TEG en pacientes con hipotermia inducida aislada a 36, 34 y 32 ° C. Se evidenció que el PTT y el hematocrito no cambiaron, mientras que el PT y el recuento de plaquetas disminuyeron durante el enfriamiento. Las mediciones con TEG mostraron un retraso de la formación del coágulo a temperatura ajustada de la medición (es decir, que las temperaturas durante la medición del TEG se ajustaron a las temperaturas de los pacientes en el momento de la toma de la muestra), pero no mostraron ningún cambio cuando la temperatura de ensayo fue de 37 ° C. Esto indica que la hipotermia reduce la coagulación plasmática y la reactividad plaquetaria. Sin embargo, la fuerza del coágulo no se ve alterada por la hipotermia. Todas las variables de coagulación permanecieron dentro de los rangos normales, lo que demuestra que la hipotermia en las condiciones descritas solo tiene efectos adversos menores en los seres humanos sanos y se correlaciona con otros estudios en pacientes llevados a cirugía hepática y cardiaca23,24.
Al evaluar los efectos de propofol vs. isoflurano en los cambios en la TEG, Law et al.25 no demostraron cambios significativos en los parámetros de la misma ni tampoco diferencias en las pérdidas sanguíneas durante cirugía (resección de tumores de cabeza y cuello). Tampoco se han observado cambios significativos en la agregación plaquetaria con el uso de enflurano, opiáceos y anestésicos locales26.
Cirugía cardiovascular
En relación con la cirugía cardiovascular se encontraron un total de 228 artículos. Se enfocan en metas de terapia transfusional según los resultados de la TEG en las diferentes etapas del procedimiento quirúrgico con el objetivo de reducir así los requerimientos de sangre y hemoderivados27. Comparan la TEG con estudios rutinarios de coagulación buscando identificar el mejor predictor para sangrado excesivo posterior a bypass cardiocirculatorio y la necesidad de reintervención de pacientes28-30, monitorización de reversión de heparina, efecto de antiagregantes plaquetarios y heparinas de bajo peso molecular (HBPM) para cirugía programada y no programada que requiera cirugía cardiovascular31,32. La conclusión de estos artículos es que la TEG es un método diagnóstico útil como predictor de hemorragia postoperatoria al compararse con métodos de rutina posterior a bypass cardiocirculatorio30. Además, sugieren el uso de la TEG en la reversión de heparina debido a la rápida disponibilidad de resultados que permitan guiar la terapia efectiva y disminuir así el número de transfusiones innecesarias31.
La TEG se ha usado en conjunto con la monitorización de la función plaquetaria (platelet mapping) como una herramienta de valoración prequirúrgica y posquirúrgica para pacientes que van a ser sometidos a cirugía o procedimientos invasivos cardiovasculares y han sido tratados previamente con terapia de anti-agregación plaquetaria. Aunque los documentos revisados muestran buenos resultados en cuanto a guía para terapia de trasfusión y predicción de complicaciones, estas técnicas aún cuentan con algunas limitaciones, como la correlación de estas con las propiedades farmacocinéticas y farmacodinámicas de los medicamentos, lo cual no permite entregar recomendaciones generales para el uso de rutina de estas técnicas en la actualidad33-35.
Otros procedimientos quirúrgicos
En la categoría de otros procedimientos quirúrgicos se encontraron un total de 177 artículos, de los cuales la mayoría se enfocan en el manejo de coagulopatías en neurocirugía, cirugía ortopédica mayor, trasplante renal y cirugía para paciente con múltiples traumatismos36.
En neurocirugía los artículos apoyan la TEG como técnica de cribado para el diagnóstico de trastornos hemostáticos en pacientes neuroquirúrgicos con factores de riesgo como: trastornos de la coagulación detectados a partir de pruebas de laboratorio de rutina, la administración de anticoagulantes y antiagregantes crónicos, el uso de anticonvulsivos provocando alteraciones en el sistema hemostático, en enfermedades hematológicas y en intervenciones intraoperatorias como grandes volúmenes de cristaloides, coloides y soluciones hipertónicas.
En comparación con las pruebas de laboratorio de rutina, la TEG puede ser útil en la monitorización de la coagulación en pacientes neuroquirúrgicos con precisión y rápidamente; ayuda a identificar pacientes con alto riesgo de sangrado o episodios tromboembólicos intra y postoperatorios, y a guiar la terapia transfusional permitiendo una reducción de la transfusión de hemoderivados, sin deterioro de los resultados del tratamiento37-39.
En cirugías ortopédicas mayores de cadera, rodilla y columna, la TEG no solo mostraba las alteraciones coagulopáticas por sangrados significativos y su uso para guiar la terapia transfusional, sino que también los resultados sugerían que artroplastias completas de rodilla y caderas llevaban a un estado hipercoagulable en el posoperatorio temprano, aumentando la morbimortalidad secundaria a episodios tromboembólicos40.
Obstetricia
En este campo la TEG se focaliza en el diagnóstico del estado de coagulación de la materna desde los estudios para tener rangos de normalidad en población gestante41 y la evaluación de trastornos de hipertensión del embarazo y de la hemorragia posparto. Sharma et al. demostraron que el embarazo es un estado de hipercoagulabilidad que permanece así hasta 24 h posparto, y en otros estudios hasta 3 semanas21,42, que se correlaciona con los niveles de factores procoagulantes aumentados43, al igual que las pacientes con abortos a repetición y que en ellas se asocia una amplitud máxima (MA) elevada en la TEG44. En pacientes con preeclampsia el grado de trombocitopenia se correlaciona con tiempo KyMA disminuidos45. La concentración de fibrinógeno se correlaciona con la severidad del sangrado posparto43. La TEG ha servido para guiar la transfusión de fibrinógeno durante la hemorragia posparto46, detectar y corregir exitosamente estados de hiperfibrinólisis con ácido tranexámico47.
Discusión
La presente revisión de usos de la TEG muestra que la mayoría de los usos, basándose en el número de publicaciones encontradas, se centran en enfermedades no quirúrgicas, en especial enfermedades hematológicas y trastornos inmunológicos e interacciones farmacológicas. Un considerable número de publicaciones ha surgido del ámbito quirúrgico, por lo cual este fue dividido en 3 grupos: trasplante hepático, cirugía cardiovascular y otras cirugías (trauma, cirugía abdominal, cirugía torácica y neurocirugía). En menor grado se encontraron estudios sobre el uso de la TEG en técnicas anestésicas y obstetricia.
Las publicaciones en el campo de enfermedades no quirúrgicas han estado relacionadas con enfermedades hematológicas como hemofilias, mayormente la tipo A (en donde los niveles de factor ocasionalmente no se correlacionan con la clínica), y al parecer no solo la falta de ese factor está implícito en la patogenia10,48,49. En términos generales, el uso de la TEG en esta área está aún en continua exploración y creciendo a grandes pasos. En un metaanálisis realizado por Afshari et al.50 no se evidenció mejoría en la morbimortalidad en pacientes con hemorragia severa, de diversa índole, guiando el tratamiento con TEG. Por ello se ha sugerido que hace falta estandarizar el método para las diferentes patologías y su manejo respecto a los resultados de la TEG. Aún no está claro qué patologías son susceptibles de ser analizadas correctamente con este método.
La interacción con fármacos se ha centrado en los que tienen un mecanismo de acción relacionado con la coagulación. Por ejemplo, se ha evaluado el uso de la TEG con la administración de heparina no fraccionada (HNF), HBPM y antiagregantes plaquetarios. Los resultados de los artículos demuestran que los parámetros de la TEG son modificados por las concentraciones de HNF y HBPM, y que no tienen ningún efecto sobre pruebas convencionales basadas en fibrina como son el PT y PTT. Cálculos de la diferencia entre las pruebas estándar y la TEG han aumentado en gran medida la sensibilidad para valorar los efectos de la HNF y la HBPM.
El sangrado es una complicación frecuente del trasplante hepático51, dado el trauma quirúrgico y debido a que en el hígado se producen la mayoría de factores de la coagulación3. En un metaanálisis realizado por Gurusamy et al.18 yenuna revisión sistemática conducida por Wikkelsoe et al.52 se mostró que la TEG disminuye el uso de hemocomponentes durante el procedimiento.
Un tema importante en la práctica anestésica es el manejo de pacientes con trastornos de la coagulación hereditarios. Múltiples artículos demuestran que el tiempo R prolongado es compatible con PTT prolongado observado en pacientes con trastornos de la coagulación hereditarios conocidos, así como los valores de fuerza del coágulo (tiempo K y ángulo α) y valoración de la función plaquetaria con la MA son medidos en la enfermedad de Von Willebrand, que pudieran ser útiles en el manejo intraoperatorio. Estos resultados demuestran que la TEG puede ser un monitor de la coagulación útil para el anestesiólogo manejando pacientes quirúrgicos con hemofilia, enfermedad de Von Willebrand o con deficiencias de factores aislados. Además, ha servido para diferenciar entre sangrado de origen operatorio o por coagulopatía53.
En cirugía cardiaca la atención se ha centrado en los trastornos de coagulación secundarios al sangrado intraoperatorio, a la circulación extracorpórea, a la hipotermia inducida, al uso de heparinasyala monitorización postoperatoria del estado de coagulación del paciente3,31. En la actualidad se continúa usando la TEG como método diagnóstico en el pre, peri y posoperatorio de cirugía cardiovascular. Se ha demostrado que los signos tromboelastográficos de fibrinólisis son claramente detectables en la importante fase de circulación extracorpórea en cirugía cardiaca29,30,54.
En trauma, el uso de productos sanguíneos es empírico y «ciego», especialmente en pacientes que requieren transfusión masiva36. A menudo se afirma que valorar el estado de coagulación es la indicación más fiable para mejorar resultados clínicos en pacientes con lesiones traumáticas y se debe utilizar para dirigir la transfusión de componentes sanguíneos55. La mayoría de los artículos demuestran que la TEG rápida (RapidTEG) proporciona parámetros que pueden servir como una indicación fiable del estado de coagulación en pacientes que presentan de traumas múltiples56.
La TEG en el ámbito obstétrico se está abriendo paso dada su versatilidad y rapidez con la que se obtienen resultados. La evidencia de su uso para detectar sangrado asociado con anomalías en los niveles de fibrinógeno cada vez es más importante. Aún falta estandarizar el método con estudios posteriores para varios escenarios clínicos, como en preeclampsia y estados coagulopáticos, estandarizar puntos de corte43,57 y entrenamiento al personal disponible para así configurar el verdadero potencial de la técnica.
En conclusión, esta búsqueda nos muestra la tendencia de los usos de la TEG desde su introducción a la práctica clínica, la cual ha aumentado en la última década. Aún falta profundización en algunos temas valorados y quedan tópicos que no han sido estudiados en relación con la TEG. Aún no existe un método que valore en su totalidad el sistema de coagulación, pero la TEG, en combinación con otros estudios, puede mejorar nuestra visión del sistema hemostásico58. Igualmente, falta personal entrenado para obtener muestras y análisis de calidad con el uso de esta herramienta43,59. Esta revisión nos demuestra la alta y diversa aplicabilidad de la TEG en todas las especialidades clínicas y quirúrgicas, en todos los grupos etarios, y su alto poder como prueba diagnóstica, la cual muchas veces es subestimada e infrautilizada.
Financiación
Ninguna.
Conflicto de intereses
Los autores declaran que no existe ningún conflicto de intereses.
Referencias
1. Gempeler F, Perea A, Díaz L. Tromboelastografía: evaluación global de la coagulación. Aplicaciones en el periodo perioperatorio. Rev Colomb Anestesiol. 2011;39:410-23. [ Links ]
2. Dai Y, Lee A, Critchley LA, White PF. Does thromboelastography predict postoperative thromboembolic events? A systematic review of the literature. Anesth Analg. 2009;108:734-42. [ Links ]
3. Salooja N, Perry DJ. Thrombelastography. Blood Coagul Fibrinolysis. 2001;12:327-37. [ Links ]
4. Galvez K, Cortes C. Tromboelastografía: nuevos conceptos en la fisiología de la hemostasia y su correlación con la coagulopatía asociada al trauma. Rev Colomb Anestesiol. 2012;40:224-30. [ Links ]
5. Oliveros H. Tromboelastografía. Rev Colomb Anestesiol. 2012;40:173-4. [ Links ]
6. Raffán F, Ramírez F, Cuervo J, Sánchez L. Tromboelastografía. Rev Colomb Anestesiol. 2005;33:181-6. [ Links ]
7. MacDonald SG, Luddington RJ. Critical factors contributing to the thromboelastography trace. Semin Thromb Hemost. 2010;36:712-22. [ Links ]
8. Taggart R, Austin B, Hans E, Hogan D. In vitro evaluation of the effect of hypothermia on coagulation in dogs via thromboelastography. J Vet Emerg Crit Care (San Antonio). 2012;22:219-24. [ Links ]
9. Wohlauer MV, Moore EE, Harr J, Gonzalez E, Fragoso M, Silliman CC. A standardized technique for performing thromboelastography in rodents. Shock. 2011;36:524-6. [ Links ]
10. Sørensen B, Ingerslev J. Tailoring haemostatic treatment to patient requirements - an update on monitoring haemostatic response using thrombelastography. Haemophilia. 2005;11 Suppl 1:1-6. [ Links ]
11. Lang T, Johanning K, Metzler H, Piepenbrock S, Solomon C, Rahe-Meyer N, et al. The effects of fibrinogen levels on thromboelastometric variables in the presence of thrombocytopenia. Anesth Analg. 2009;108:751-8. [ Links ]
12. Hadley GP, McGarr P, Mars M. The role of thromboelastography in the management of children with snake-bite in Southern Africa. Trans R Soc Trop Med Hyg. 1999;93:177-9. [ Links ]
13. Handa A, Platts A, Tone S, Hamilton G. Vascular surgical society of Great Britain and Ireland: Thrombelastography can differentiate ischaemic from haemorrhagic stroke. Br J Surg. 1999;86:691. [ Links ]
14. Wegner J, Popovsky MA. Clinical utility of thromboelastography: One size does not fit all. Semin Thromb Hemost. 2010;36:699-706. [ Links ]
15. Pivalizza EG, Abramson DC, Harvey A. Perioperative hypercoagulability in uremic patients: A viscoelastic study. J Clin Anesth. 1997;9:442-5. [ Links ]
16. Kettner SC, Pollak A, Zimpfer M, Seybold T, Prusa AR, Herkner K, et al. Heparinase-modified thrombelastography in term and preterm neonates. Anesth Analg. 2004;98: 1650-2. [ Links ]
17. Klein SM, Slaughter TF, Vail PT, Ginsberg B, el-Moalem HE, Alexander R, et al. Thromboelastography as a perioperative measure of anticoagulation resulting from low molecular weight heparin: A comparison with anti-Xa concentrations. Anesth Analg. 2000;91:1091-5. [ Links ]
18. Gurusamy KS, Pissanou T, Pikhart H, Vaughan J, Burroughs AK, Davidson BR. Methods to decrease blood loss and transfusion requirements for liver transplantation. Cochrane Database Syst Rev. 2011;7(12):CD009052. [ Links ]
19. Zahn CM, Gonzalez DI, Suto C, Kennedy S, Hines JF. Low-dose oral contraceptive effects on thromboelastogram criteria and relationship to hypercoagulability. Am J Obstet Gynecol. 2003;189:43-7. [ Links ]
20. Ganter MT, Hofer CK. Coagulation monitoring: Current techniques and clinical use of viscoelastic point-of-care coagulation devices. Anesth Analg. 2008;106:1366-75. [ Links ]
21. Luddington RJ. Thrombelastography/thromboelastometry. Clin Lab Haematol. 2005;27:81-90. [ Links ]
22. Kettner SC, Sitzwohl C, Zimpfer M, Kozek SA, Holzer A, Spiss CK, et al. The effect of graded hypothermia (36 degrees C-32 degrees C) on hemostasis in anesthetized patients without surgical trauma. Anesth Analg. 2003;96:1772-6. [ Links ]
23. Douning LK, Ramsay MA, Swygert TH, Hicks KN, Hein HA, Gunning TC, et al. Temperature corrected thrombelastography in hypothermic patients. Anesth Analg. 1995;81:608-11. [ Links ]
24. Kettner SC, Kozek SA, Groetzner JP, Gonano C, Schellongowski A, Kucera M, et al. Effects of hypothermia on thrombelastography in patients undergoing cardiopulmonary bypass. Br J Anaesth. 1998;80:313-7. [ Links ]
25. Law NL, Ng KF, Irwin MG, Man JS. Comparison of coagulation and blood loss during anaesthesia with inhaled isoflurane or intravenous propofol. Br J Anaesth. 2001;86:94-8. [ Links ]
26. Kozek-Langenecker SA. The effects of drugs used in anaesthesia on platelet membrane receptors and on platelet function. Curr Drug Targets. 2002;3:247-58. [ Links ]
27. Shore-Lesserson L, Manspeizer HE, DePerio M, Francis S, Vela-Cantos F, Ergin MA. Thromboelastography-guided transfusion algorithm reduces transfusions in complex cardiac surgery. Anesth Analg. 1999;88:312-9. [ Links ]
28. Moulton MJ, Creswell LL, Mackey ME, Cox JL, Rosenbloom M. Reexploration for bleeding is a risk factor for adverse outcomes after cardiac operations. J Thorac Cardiovasc Surg. 1996;111:1037-46. [ Links ]
29. Dorman BH, Spinale FG, Bailey MK, Kratz JM, Roy RC. Identification of patients at risk for excessive blood loss during coronary artery bypass surgery: Thromboelastography versus coagulation screen. Anesth Analg. 1993;76:694-700. [ Links ]
30. Tuman KJ, Spiess BD, McCarthy RJ, Ivankovich AD. Comparison of viscoelastic measures of coagulation after cardiopulmonary bypass. Anesth Analg. 1989;69:69-75. [ Links ]
31. Woodman RC, Harker LA. Bleeding complications associated with cardiopulmonary bypass. Blood. 1990;76:1680-97. [ Links ]
32. Mongan PD, Hosking MP. The role of desmopressin acetate in patients undergoing coronary artery bypass surgery. A controlled clinical trial with thromboelastographic risk stratification. Anesthesiology. 1992;77:38-46. [ Links ]
33. Kaur J, Jones N, Mallett S. Thrombelastography Platelet Mapping is a useful preoperative tool in surgical patients taking antiplatelet medication. Br J Anaesth. 2009;103:304, author reply 305. [ Links ]
34. Collyer TC, Gray DJ, Sandhu R, Berridge J, Lyons G. Assessment of platelet inhibition secondary to clopidogrel and aspirin therapy in preoperative acute surgical patients measured by Thrombelastography Platelet Mapping. Br J Anaesth. 2009;102:492-8. [ Links ]
35. Pivalizza EG, Melnikov V, Guzman-Reyes S, Marasigan B. Thrombelastograph platelet mapping in a patient receiving antiplatelet therapy. Liver Transpl. 2010;16:919, author reply: 920. [ Links ]
36. Tieu BH, Holcomb JB, Schreiber MA. Coagulopathy: Its pathophysiology and treatment in the injured patient. World J Surg. 2007;31:1055-64. [ Links ]
37. Palmer JD, Francis DA, Roath OS, Francis JL, Iannotti F. Hyperfibrinolysis during intracranial surgery: Effect of high dose aprotinin. J Neurol Neurosurg Psychiatry. 1995;58: 104-6. [ Links ]
38. Kunio NR, Differding JA, Watson KM, Stucke RS, Schreiber MA. Thrombelastography-identified coagulopathy is associated with increased morbidity and mortality after traumatic brain injury. Am J Surg. 2012;203:584-8. [ Links ]
39. Windeløv NA, Welling KL, Ostrowski SR, Johansson PI. The prognostic value of thrombelastography in identifying neurosurgical patients with worse prognosis. Blood Coagul Fibrinolysis. 2011;22:416-9. [ Links ]
40. Brenn BR, Theroux MC, Dabney KW, Miller F. Clotting parameters and thromboelastography in children with neuromuscular and idiopathic scoliosis undergoing posterior spinal fusion. Spine (Phila Pa 1976). 2004;29:E310-4. [ Links ]
41. Macafee B, Campbell JP, Ashpole K, Cox M, Matthey F, Acton L, et al. Reference ranges for thromboelastography (TEG®) and traditional coagulation tests in term parturients undergoing caesarean section under spinal anaesthesia. Anaesthesia. 2012;67:741-7. [ Links ]
42. Sharma SK, Philip J, Wiley J. Thromboelastographic changes in healthy parturients and postpartum women. Anesth Analg. 1997;85:94-8. [ Links ]
43. Solomon C, Collis RE, Collins PW. Haemostatic monitoring during postpartum haemorrhage and implications for management. Br J Anaesth. 2012;109:851-63. [ Links ]
44. Rai R, Tuddenham E, Backos M, Jivraj S, el-Gaddal S, Choy S, et al. Thromboelastography, whole-blood haemostasis and recurrent miscarriage. Hum Reprod. 2003;18:2540-3. [ Links ]
45. Orlikowski CE, Rocke DA, Murray WB, Gouws E, Moodley J, Kenoyer DG, et al. Thrombelastography changes in pre-eclampsia and eclampsia. Br J Anaesth. 1996;77:157-61. [ Links ]
46. Huissoud C, Carrabin N, Audibert F, Levrat A, Massignon D, Berland M, et al. Bedside assessment of fibrinogen level in postpartum haemorrhage by thrombelastometry. BJOG. 2009;116:1097-102. [ Links ]
47. Annecke T, Geisenberger T, Kürzl R, Penning R, Heindl B. Algorithm-based coagulation management of catastrophic amniotic fluid embolism. Blood Coagul Fibrinolysis. 2010;21:95-100. [ Links ]
48. Shima M, Matsumoto T, Ogiwara K. New assays for monitoring haemophilia treatment. Haemophilia. 2008;14 Suppl 3:83-92. [ Links ]
49. Sørensen B, Ingerslev J. Whole blood clot formation phenotypes in hemophilia A and rare coagulation disorders. Patterns of response to recombinant factor VIIa. J Thromb Haemost. 2004;2:102-10. [ Links ]
50. Afshari A, Wikkelsø A, Brok J, Møller AM, Wetterslev J. Thrombelastography (TEG) or thromboelastometry (ROTEM) to monitor haemotherapy versus usual care in patients with massive transfusion. Cochrane Database Syst Rev. 2011;16(3):CD007871. [ Links ]
51. Hendriks HG, Meijer K, de Wolf JT, Porte RJ, Klompmaker IJ, Lip H, et al. Effects of recombinant activated factor VII on coagulation measured by thromboelastography in liver transplantation. Blood Coagul Fibrinolysis. 2002;13: 309-13. [ Links ]
52. Wikkelsoe AJ, Afshari A, Wetterslev J, Brok J, Moeller AM. Monitoring patients at risk of massive transfusion with thrombelastography or thromboelastometry: A systematic review. Acta Anaesthesiol Scand. 2011;55:1174-89. [ Links ]
53. Afshari A. Evidence based evaluation of immuno-coagulatory interventions in critical care. Dan Med Bull. 2011;58: B4316. [ Links ]
54. EMSALT Study Group Porte RJ, Molenaar IQ, Begliomini B, Groenland TH, Januszkiewicz A, Lindgren L, et al. Aprotinin and transfusion requirements in orthotopic liver transplantation: A multicentre randomised double-blind study. Lancet. 2000;355:1303-9. [ Links ]
55. Levrat A, Gros A, Rugeri L, Inaba K, Floccard B, Negrier C, et al. Evaluation of rotation thrombelastography for the diagnosis of hyperfibrinolysis in trauma patients. Br J Anaesth. 2008;100:792-7. [ Links ]
56. Jeger V, Zimmermann H, Exadaktylos AK. Can RapidTEG accelerate the search for coagulopathies in the patient with multiple injuries? J Trauma. 2009;66:1253-7. [ Links ]
57. De Lange NM, Lancé MD, de Groot R, Beckers EA, Henskens YM, Scheepers HC. Obstetric hemorrhage and coagulation: An update. Thromboelastography, thromboelastometry, and conventional coagulation tests in the diagnosis and prediction of postpartum hemorrhage. Obstet Gynecol Surv. 2012;67:426-35. [ Links ]
58. Weber CF, Zacharowski K. Perioperative point of care coagulation testing. Dtsch Arztebl Int. 2012;109:369-75. [ Links ]
59. Levy JH, Dutton RP, Hemphill JC, Shander A, Cooper D, Paidas MJ, et al. Multidisciplinary approach to the challenge of hemostasis. Anesth Analg. 2010;110:354-64. [ Links ]











 text in
text in 

