Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.43 no.1 Bogotá Jan./Mar. 2015
https://doi.org/10.1016/j.rcae.2014.11.001
http://dx.doi.org/10.1016/j.rca.2014.10.008
Guías y consensos
Manual de práctica clínica basado en la evidencia: Controles posquirúrgicos
Evidence-based clinical practice manual: Postoperative controls
Cristina Alexandra Benavides Caroa, Franklyn Edwin Prieto Alvaradob,*, Marcela Torresc, Giancarlo Buitragod, Hernando Gaitán Duartee, Cecilia Garcíae y Luz María Gómez Buitragof
a Médica Anestesióloga, Especialista en Bioética, Clínica Universitaria Colombia, Bogotá, Colombia
b Médico Epidemiólogo, MSc Salud Pública, MSc Bioética, Universidad Nacional de Colombia, Bogotá, Colombia
c Química Farmacéutica, MSc Epidemiología Clínica, Gerente Editorial, Cochrane Sexually Transmitted Infections Group, Universidad Nacional de Colombia, Bogotá, Colombia
d Médico, MSc Epidemiología Clínica, Magíster Economía, IECAS, Universidad Nacional de Colombia, Bogotá, Colombia
e Médico Especialista, MSc Epidemiología Clínica, Grupo de Evaluación de Tecnologías y Políticas en Salud, Universidad Nacional de Colombia, Bogotá, Colombia
f Médica, Anestesióloga, MSc en Epidemiología, Jefe Departamento Asesoría Médica Especializada S.C.A.R.E., Investigadora Centro de Desarrollo Tecnológico (S.C.A.R.E.), Bogotá, Colombia
* Autor para correspondencia: Calle 22B, No. 66-46 Consultorios 403-404, Clínica Universitaria Colombia, Bogotá, Colombia.
Correo electrónico: franklyn.prieto@gmail.com (F.E. Prieto Alvarado).
Información del artículo
Historia del artículo: Recibido el 10 de octubre de 2014 Aceptado el 19 de octubre de 2014
Resumen
Introducción: El cuidado postanestésico disminuye las complicaciones y la mortalidad postoperatorias inmediatas relacionadas con la anestesia, acorta la estancia en las unidades de cuidado postoperatorio y mejora la satisfacción de los pacientes.
Objetivo: Establecer un conjunto de recomendaciones para el cuidado postanestésico inmediato de los pacientes que recibieron anestesia general/regional o sedación profunda/moderada en las unidades de cuidado postoperatorio.
Metodología: Es un proceso de adaptación «rápida» de guías de práctica clínica, que incluyó búsqueda sistemática. Se calificaron las guías elegibles a adaptar, mediante AGREE II. La guía seleccionada para su adaptación como manual de práctica clínica fue Practice Guidelines for Postanesthetic Care, de la American Society of Anesthesiologists. El manual fue evaluado por un grupo de anestesiólogos y epidemiólogos mediante Delphi, en términos de implementabilidad, actualización, pertinencia, consideraciones éticas y seguridad del paciente.
Resultado: El manual mantuvo las recomendaciones sobre evaluación y monitorización, manejo farmacológico de náuseas y vómito postoperatorio, antagonismo de los efectos de sedantes, analgésicos y agentes de bloqueo neuromuscular, el manejo de la emergencia y recuperación anestésica, y los criterios para egreso de la unidad. Se incluyeron indicaciones sobre condiciones y requisitos de la unidad y el ingreso del paciente a esta.
Conclusiones: Este manual es una guía básica sobre el manejo primario de los pacientes en la unidad de cuidado postoperatorio, y puede ser modificado o adaptado según los institucionales y para grupos específicos de pacientes; no pretende reemplazar los protocolos existentes en cada institución ni puede definir desenlaces ni pronósticos.
Palabras clave: Cuidados Postoperatorios, Anestesia, Manuales como Asunto, Medicina Basada en Evidencia, Periodo de Recuperación de la Anestesia.
Abstract
Introduction: Post-anesthetic care reduces the anesthesia-related postoperative complications and mortality, shortens the length of stay at the postoperative care units and improves patient satisfaction.
Objective: To establish a set of recommendations for immediate post-anesthetic care of patients that received general/regional anesthesia or profound/moderate sedation at the postoperative care units.
Methodology: This is a process of ‘rapid' clinical practice guidelines adaptation, including systematic search. The illegible guidelines for adaptation were rated using AGREE II. The guideline selected to be adapted as the clinical practice handbook was Practice Guidelines for Post-anesthetic Care of the American Society of Anesthesiologists. The manual was evaluated in terms of implementation ability, up-to-date information, relevancy, ethical considerations and patient safety by the group of anesthesiologists and epidemiologists based on Delphi. Result: The manual kept the recommendations on evaluation and monitoring, pharmacological management of postoperative nausea and vomiting, antagonistic actions for sedatives and analgesics and neuromuscular block agents, emergency management and anesthesia recovery, as well as the criteria for discharge from the unit. Indications about the conditions and requirements of the unit and patient admission were also included.
Conclusions: This handbook comprises the basic guidelines for primary management of patients at the postoperative care unit. It may be amended or adapted according to the institutional requirements and for specific patient groups and is not intended to replace the existing protocols at the particular institution and does not define outcomes or prognosis.
Keywords: Postoperative Care, Anesthesia, Manuals as Topic, Evidence-Based Medicine, Anesthesia Recovery Period.
Introducción
La práctica de la anestesiología ha avanzado en la seguridad del paciente. La disminución en la mortalidad relacionada con la cirugía, la anestesia y el cuidado perioperatorio ha sido posible por mecanismos como el mejoramiento de las técnicas de monitorización, el desarrollo y difusión de las guías de práctica clínica y otros enfoques sistemáticos encaminados a reducir errores1.
Un metaanálisis de 87 estudios que midieron la mortalidad en más de 3.000 pacientes -de 21,4 millones que recibieron anestesia general para una cirugía- encontró que la mortalidad atribuible a la anestesia ha disminuido de 357 por millón (IC 95%: 324-394) en el periodo 1960-1969 a 52 por millón en la primera década de este siglo. El aporte de la anestesia a la mortalidad perioperatoria fue del 3,4% antes de 1980 y disminuyó al 2,9% entre 2000-2009. Los países con menor índice de desarrollo humano tienen 5,49 veces el riesgo de morir por anestesia2. Otro metaanálisis reportó una disminución en la mortalidad perioperatoria entre 1954 y 2006 y, al comparar esta mortalidad entre Brasil y los países desarrollados, no encontró diferencias3.
En el estudio del registro de 1,37 millones de cirugías electivas en Alemania (ASA I y II), del periodo 1999-2010, 26,2 pacientes de cada millón operados tuvieron una complicación grave o murieron (IC 95%: 19,4-34,6). De estos últimos, 7,3 de cada millón podrían relacionarse con la anestesia o con problemas por el cuidado del anestesiólogo (IC 95%: 3,912,3). Solo un caso de 80 sucedió por problemas en el cuidado postanestésico4.
Las complicaciones más comunes en las unidades de cuidado postoperatorio son las náuseas y el vómito, con incidencias entre el 10 y el 30%5. Un estudio retrospectivo de 18.473 pacientes detectó un 23% de complicaciones: 6,9% de problemas del tracto respiratorio superior; 2,7% de hipotensión; 1,4% de disritmias; 1,1% de hipertensión; 0,6% de estatus mental alterado y 0,6% de eventos cardiacos mayores6.La desaturación de oxígeno es uno de los problemas mayores más frecuentes7.
Las complicaciones postoperatorias afectan la supervivencia tanto para las personas con cirugía mayor como para los adultos mayores8,9. En los primeros días posteriores a la cirugía se pueden detectar complicaciones pulmonares, infarto agudo de miocardio, sangrado, insuficiencia cardiaca aguda y delirio10. Se ha reportado que el 19,3% de las admisiones no planeadas a las UCI tienen que ver con el proceso anestésico y el 5,4% serían prevenibles; sin embargo, se ha encontrado que el 52% de dichas admisiones podrían deberse a la anestesia y que entre el 74 y el 92% serían prevenibles11.
Un adecuado abordaje postoperatorio aumenta significativamente la supervivencia, así como disminuye los eventos adversos y las admisiones no planeadas a las UCI. Este Manual incluye los aspectos clave a considerar para ese abordaje adecuado. La implementación de protocolos de cuidado postanestésico contribuye a reducir la estancia hospitalaria, las complicaciones, la mortalidad y el acceso no planeado a las unidades de cuidado crítico12.
Los cuidados postoperatorios o postanestésicos se definían como aquellos proporcionados durante la estadía en una unidad de cuidado postoperatorio. Estos cuidados deben mejorarse para que la persona inicie su recuperación o para un tránsito adecuado hacia unidades de mayor complejidad13.La prevención de complicaciones en esta unidad puede significar el egreso temprano y la disponibilidad de camas para recibir pacientes de las salas de cirugía. Si las complicaciones suceden, los pacientes requieren de una intervención oportuna o la determinación de manejo en unidades de mayor complejidad.
Una de las condiciones clave para una mayor eficacia es el balance entre el cuidado de los pacientes que necesitan más atención y los que no. El Manual de controles posquirúrgicos incluye un conjunto de recomendaciones con base en lo definido por la Asociación Americana de Anestesiología14, mediante un proceso de adaptación de guías de práctica clínica. Inicialmente se mencionarán algunas consideraciones posteriores a la anestesia; luego se indicarán los aspectos principales del ingreso del paciente a la unidad de cuidado postoperatorio, su evaluación y su monitorización. En la segunda parte, el Manual se centrará en la profilaxis o tratamiento de las náuseas y el vómito; el tratamiento durante la emergencia y la recuperación anestésica, y la producción del antagonismo de los efectos de medicamentos sedantes, analgésicos y de bloqueo neuromuscular. Al finalizar, se establecerán los procedimientos para dar salida al paciente de la unidad de cuidado postoperatorio.
Definiciones
Cuidado postanestésico. Actividades emprendidas para el manejo del paciente después de completar el procedimiento que requirió anestesia para su realización y la anestesia concomitante.
Recuperación anestésica. Periodo posterior a la anestesia durante el cual se disminuye paulatinamente, en el paciente, el efecto de la misma. La valoración de la recuperación, acorde al tipo de anestesia, define el egreso del paciente de la unidad de cuidado postoperatorio.
Unidad de cuidado postoperatorio. Espacio físico en las salas de cirugía con la infraestructura y la dotación necesarias para la recuperación del paciente que ha recibido anestesia general, regional o sedación.
Evaluación y monitorización postanestésicas. Valoración y seguimiento periódico de las funciones vitales y condiciones especiales del paciente en postoperatorio, encaminadas a su optimización, que permiten el posterior traslado del paciente de forma segura fuera de las salas de cirugía.
Metodología
Fue un proceso dividido en 3 fases. Cada fase utilizó técnicas y procedimientos estandarizados para el desarrollo de guías y protocolos basados en la evidencia.
1. Conformación del grupo elaborador
Se conformó un grupo de expertos en anestesiología y en epidemiología, encargado de las directrices metodológicas para el desarrollo del Manual, basado en la evidencia. Los miembros del grupo elaborador aceptaron la participación en el proceso y declararon o no conflicto de intereses.
2. Revisión sistemática de literatura secundaria
Se realizó una revisión sistemática para identificar los protocolos y guías de práctica clínica con indicaciones o recomendaciones sobre el manejo por anestesiología. La unidad de análisis fueron artículos publicados en revistas científicas o documentos técnicos encontrados como literatura gris publicados desde 2011, en inglés o español.
Estrategia de búsqueda
Se diseñó una estrategia de búsqueda electrónica sensible de documentos que cumplieran con los criterios establecidos. La primera búsqueda fue efectuada el 19 de agosto de 2014.
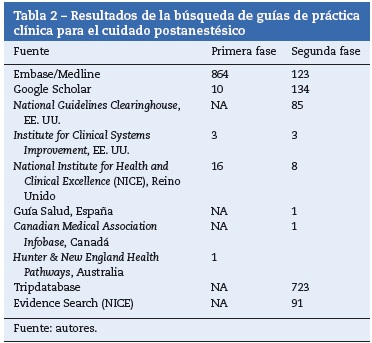
En una segunda búsqueda se incluyeron bases de datos de organismos compiladores de protocolos y metabuscadores. Se realizaron búsquedas adicionales de guías en los sitios web de asociaciones nacionales e internacionales de anestesiología y de los 10 mejores hospitales de Estados Unidos para 201415. En estas fuentes no se identificaron nuevas guías de práctica clínica. Las fuentes de información son presentadas en la tabla 1.
Diseño e implementación de las estrategias de búsqueda
Para la primera búsqueda se identificaron términos clave (lenguaje natural) correspondientes a la condición de salud o área de interés (anestesia, cuidado perioperatorio y protocolos clínicos). Posteriormente se construyó una estrategia de búsqueda de base compuesta por vocabulario controlado (términos MeSH, Emtree y DeCS) y lenguaje libre (variaciones ortográficas, plurales, sinónimos, acrónimos y abreviaturas).
A partir de la estrategia base se adaptaron búsquedas en los diferentes recursos, empleando (cuando fue posible) expansión de términos, identificadores de campo (título y resumen), truncadores y operadores booleanos y de proximidad.
Se buscó en los repositorios de protocolos clínicos, rastreando palabras clave mediante la herramienta «buscar» del navegador de Internet, así como una búsqueda reproducible en Google y Google Scholar, sin restricción de idioma o límite en la fecha de publicación.
Para la segunda búsqueda se modificaron los términos clave (anestesia, cuidado postoperatorio, cuidado postanestésico, protocolos clínicos, guías de práctica clínica), manteniendo el proceso integral de la primera búsqueda.
Para cada búsqueda se generó una bitácora o reporte que garantizara su reproducibilidad y transparencia. Las referencias fueron consolidadas en una base de datos en Microsoft Excel.
Las búsquedas fueron realizadas por personal entrenado, con la auditoría de un Trials Search Coordinator de la Colaboración Cochrane.
Resultados de las estrategias de búsqueda
Los resultados de las 2 fases de la estrategia de búsqueda se evidencian en la tabla 2.
Selección de evidencia
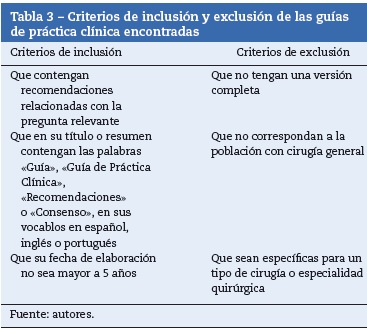
A partir de la primera fase de búsqueda se identificaron 193 referencias que corresponderían al propósito del Manual, aunque no fuesen guías de práctica clínica. Durante la depuración de las 2 fases de búsqueda se determinó que 12 documentos eran guías de práctica clínica sobre cuidado postoperatorio.
Los 12 documentos fueron revisados por 2 expertos: uno temático (anestesiólogo) y uno metodológico (epidemiólogo). Los expertos corroboraron que las guías cumplieran con los criterios de inclusión o exclusión y que tuvieran un enfoque basado en la evidencia. De los 12 documentos, 4 cumplían con los criterios. En la tabla 3 se presenta la información de los criterios utilizados.
Evaluación de la calidad
Se utilizó el instrumento AGREE II (por sus siglas en inglés Appraisal of Guidelines for Research and Evaluation) para evaluar la calidad de la evidencia seleccionada16. Este análisis de la calidad se realizó de forma pareada. Se identificaron los documentos que cumplieran con los requisitos de elegibilidad como documentos fuentes para este Manual. En los Anexo se encuentra el resumen de este proceso.
De acuerdo con la calificación, la guía de práctica clínica a adoptar corresponde a la Asociación Americana de Anestesiología14, que es una actualización de la Guía desarrollada en 200217. Por concepto del anestesiólogo experto, las recomendaciones sobre las condiciones de la sala de cuidado postoperatoria, del ingreso y egreso del paciente a la sala se complementaron a partir de las guías de The Association of Anaesthetists of Great Britain and Ireland18 y de la Scottish Intercollegiate Guidelines Network19.
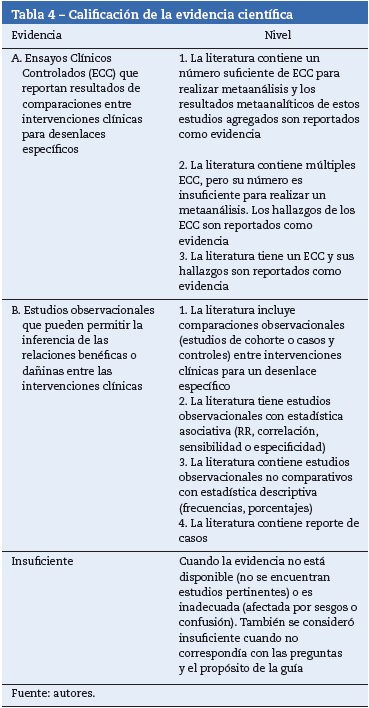
Disponibilidad y fuerza de la evidencia en la guía de práctica clínica base
La guía de práctica clínica base tuvo en cuenta tanto la evidencia científica como la opinión de expertos. En la tabla 4 se resume la calificación de la evidencia científica publicada en revistas. La categoría nivel de evidencia se refiere a la fuerza y validez del diseño de investigación. Los niveles se relacionan con la fuerza y la calidad de los hallazgos resumidos de cada estudio (por ejemplo, hallazgos estadísticos, tipo de datos y número de estudios que reportan o replican los hallazgos) en las 2 categorías de evidencia.
De acuerdo con los desenlaces, la intervención se consideró benéfica (B), dañina (H) o equívoca (E), cuando no significó diferencias estadísticas.
3. Método participativo
Se utilizó una modificación del método Delphi20. El grupo elaborador escogió los expertos y los convocó a una reunión, el 18 de septiembre de 2014, en las instalaciones de la SCARE. Participaron 28 expertos en anestesiología y epidemiología.
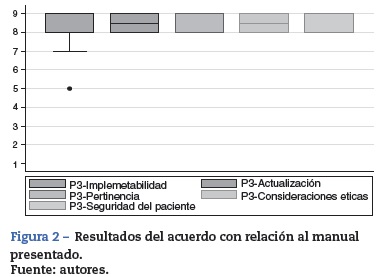
Luego de presentar el contenido clínico del manual y de la discusión por los expertos, se evaluó en relación a si cumplía con las siguientes características:
- Implementabilidad. Posibilidad de que el manual sea fácilmente utilizado en las diferentes instituciones.
- Actualización. Si las indicaciones corresponden a la evidencia actual.
- Pertinencia. Si las indicaciones serían pertinentes para el contexto de la mayoría de las áreas quirúrgicas.
- Consideraciones éticas. Si sería ético utilizar este manual.
- Seguridad del paciente. Si existe un riesgo elevado al utilizar este Manual para los pacientes.
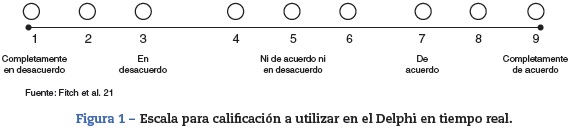
Se utilizó una escala ordinal de 9 categorías para calificar el acuerdo con cada una de las características mencionadas. Cada una de las indicaciones propuestas se calificó como recomendada (apropiada), contraindicada (inapropiada) o dentro de un nivel de incertidumbre21.
La figura 1 muestra los resultados del acuerdo logrado por los participantes del consenso.
Preparación y escritura del documento final
Se diseñó un modelo final de Manual en el que se incluyó la justificación, la metodología y la adaptación de la guía de práctica clínica base, según las recomendaciones de los expertos en el método participativo. El documento final fue desarrollado por el equipo que elaboró el Manual.
Conflicto de intereses
Todos los participantes del grupo elaborador y del consenso de expertos declararon, diligenciaron y firmaron el documento sobre conflictos de intereses.
Derechos de autor
Se realizaron las consultas y solicitud de permisos para la utilización y traducción de parte del contenido de las guías para la construcción del manual. La traducción y reproducción parcial se realizó con permiso de Lippincott Williams and Wilkins/ Wolters Kluwer Health, Association of Anaesthetists of Great Britain & Ireland & the AAGBI Foundation e Institute of Clinical Systems Improvement. Los derechos de autor pertenecen a los autores de las guías y protocolos base, los cuales son referenciados adecuadamente en el documento.
Contenido clínico
Enfoque
El manual tiene su eje en el manejo postoperatorio del paciente y se enfoca en la reducción de los eventos adversos mediante una evaluación uniforme del proceso de recuperación. Así se mejora la calidad de vida en el estado postanestésico, racionalizando el cuidado postoperatorio y los criterios de salida.
Este manual aplica para pacientes que recibieron anestesia general, regional o sedación profunda o moderada y podría ser modificado (o podría diseñarse un protocolo complementario) para adecuarlo a las necesidades de cierto tipo de pacientes y población tales como niños y adultos mayores. No aplica para pacientes con anestesia local sin sedación, para sedación mínima o para aquellos que requieren UCI.
Este manual no pretende reemplazar el manejo individualizado de cada paciente ni los protocolos de cada institución. Tampoco puede ni busca definir desenlaces de los pacientes.
La figura 2 presenta el esquema de la secuencia de actividades de este Manual.
Condiciones o requisitos de la unidad de cuidado postoperatorio
La unidad de cuidado postoperatorio deberá, preferiblemente, ocupar un lugar central en las salas de cirugía, con fácil acceso y movilización en y hacia la unidad. Deberá contar con monitores, medicamentos, equipos y personal de enfermería suficiente y entrenado para el manejo de los pacientes en periodo postoperatorio y sus complicaciones18.
Debe existir un anestesiólogo responsable por los pacientes entregados en la unidad de cuidado postoperatorio18.
Debe existir un sistema de comunicación y de alarmas de fácil funcionamiento. El recurso humano debe estar entrenado para usarlo racionalmente18.
Ingreso del paciente a la unidad de cuidado postoperatorio
El anestesiólogo responsable del paciente debe entregar personalmente al paciente al personal a cargo de la unidad de cuidado postoperatorio18.
El anestesiólogo debe realizar un reporte verbal de la historia clínica prequirúrgica y quirúrgica del paciente, incluyendo cualquier evento adverso que se hubiera presentado durante la cirugía18.
El anestesiólogo debe informar de las indicaciones generales del cuidado postoperatorio de acuerdo con la historia clínica, el tipo de cirugía y de la anestesia del paciente.
Indicaciones
Debe existir un anestesiólogo responsable de la entrega del paciente en la unidad de cuidado postoperatorio, UCI o cualquier unidad encargada de aceptar el paciente en su postoperatorio inmediato.
Si se presenta alguna complicación anestésica durante la fase intraquirúrgica o en la recuperación anestésica, el anestesiólogo a cargo del acto anestésico, el anestesiólogo a cargo de la unidad de cuidado postoperatorio o, en su defecto, el anestesiólogo al cual se le entregó formalmente el cuidado del paciente debe informar del tipo de complicación y de su manejo al pacienteoasurepresentante.
Si se presenta una complicación quirúrgica debe ser informada por el cirujano responsable del acto quirúrgico.
Es altamente deseable que el equipo quirúrgico, anestesiólogo y cirujano informen sobre el resultado quirúrgico al pacienteoasu acompañante en la institución.
Debe existir un anestesiólogo responsable de la recuperación del paciente en la unidad de cuidado postoperatorio.
El equipo de profesionales y auxiliares a cargo de la unidad de cuidado postoperatorio deben registrar toda valoración a partir de la monitorización, observaciones clínicas, lectura de exámenes diagnósticos de seguimiento, intervención, orden o prescripción terapéutica o profiláctica realizadas como parte del cuidado durante la emergencia y la recuperación anestésica, incluyendo la prevención y el tratamiento de complicaciones22.
Evaluación y monitorización del paciente en la unidad de cuidado postoperatorio
Función respiratoria
La evaluación periódica y la monitorización de la permeabilidad de la vía aérea, la frecuencia respiratoria y la saturación de oxígeno (SpO2) deben realizarse durante la recuperación de la anestesia, para disminuir los desenlaces adversos (evidencia A2-B).
Función cardiovascular
Los expertos de la ASA17 consideraron que el monitorización de la presión arterial, el pulso y el electrocardiograma detectan complicaciones, reducen desenlaces adversos y deben ser realizados durante la recuperación de la anestesia (evidencia insuficiente). Consideraron que la monitorización mediante electrocardiografía puede ser innecesaria en ciertos tipos de pacientes o según el procedimiento anestésico.
Función neuromuscular
Se considera que la evaluación de la función neuromuscular reduce desenlaces adversos y debe ser realizada en la recuperación postanestésica.
La evaluación neuromuscular se inicia con un examen físico y ocasionalmente puede incluir la monitorización del bloqueo neuromuscular (evidencia B2-B).
Estado mental
En opinión de los expertos17, cada institución debe contar con una escala que permita la evaluación del estado mental en la unidad de cuidado postoperatorio. Esto permitiría disminuir las complicaciones postanestésicas (evidencia insuficiente).
Temperatura
Los expertos están de acuerdo en que la evaluación de la temperatura del paciente está relacionada con la disminución de complicaciones postoperatorias y debe realizase durante la recuperación postanestésica (evidencia insuficiente).
El paciente idealmente debe ser llevado a la normotermia teniendo en cuenta los cambios en la autorregulación de la temperatura secundarios a la anestesia y la cirugía.
Dolor
Los expertos consideran que la valoración del dolor durante la recuperación disminuye algunos eventos adversos postoperatorios (evidencia insuficiente).
Este manejo puede iniciarse en la cirugía y formar parte del manejo anestésico elegido para el paciente. Puede ser seguido y evaluado en el periodo postoperatorio.
Náuseas y vómito
La opinión de expertos es ambigua sobre la efectividad de la evaluación de las náuseas y vomito para disminuir efectos adversos; sin embargo, indican que esta debería ser realizada en la recuperación de la anestesia (evidencia insuficiente).
Fluidos
Los expertos están de acuerdo con los beneficios de la monitorización del estado de hidratación y del manejo de fluidos. Esto disminuye los efectos adversos y mejora el bienestar y la satisfacción del paciente (evidencia insuficiente).
Gasto urinario y micción
La evaluación del gasto urinario detecta la retención urinaria (evidencia B3-B) pero la evidencia es ambigua para otras complicaciones (evidencia insuficiente). En opinión de los expertos17, la evaluación del gasto urinario detecta complicaciones y reduce efectos adversos. Esta evaluación puede no ser rutinaria, dependiendo de cada caso.
Hay evidencia insuficiente y opiniones ambiguas de los expertos sobre la evaluación de la micción para la detección de eventos adversos, aunque consideran que puede ser evaluada durante la recuperación.
Drenaje y sangrado
Los expertos están de acuerdo en que la evaluación de sangrado y drenaje detecta complicaciones, reduce los efectos adversos y puede ser una rutina en el cuidado de los pacientes postoperatorios (evidencia insuficiente).
Indicaciones
La evaluación periódica de la vía aérea, la frecuencia respiratoria, la saturación de oxígeno, el pulso, la frecuencia cardiaca y la presión arterial deben realizarse durante la recuperación anestésica.
La monitorización mediante electrocardiografía debe estar disponible en las unidades de cuidado postoperatorio para los pacientes que la requieran.
La evaluación de la función neuromuscular se debe realizar, durante la recuperación postanestésica, a aquellos pacientes que recibieron bloqueo neuromuscular con agentes no despolarizantes o que tienen condiciones médicas relacionadas con disfunción neuromuscular.
El estado de hidratación debe ser evaluado de acuerdo con el paciente, en especial para aquellos procedimientos con una significativa pérdida de sangre o fluidos y que requirieron manejo adicional de fluidos.
El gasto urinario y la micción deben ser evaluados para determinados pacientes y procedimientos.
El estado mental, la temperatura corporal, el dolor, la náusea, el vómito, el drenaje y el sangrado pueden ser evaluados durante la recuperación.
Manejo farmacológico en la unidad de cuidado postoperatorio
Náuseas y vómito
Los grupos de medicamentos evaluados fueron antieméticos 5-HT3, tranquilizantes y neurolépticos, metoclopramida y dexametasona.
Antieméticos 5HT3
Un metanálisis de los nuevos ECC confirmó que los medicamentos 5HT3, comparados con placebo, son efectivos en la profilaxis postoperatoria de náusea y vómito y reducen el uso de rescate antiemético (evidencia A1-B). Los medicamentos específicos son: dolasetrón (reduce el vómito)23-27, granisetrón (reduce el vómito)28-32 y ondansetrón (reduce el vómito y rescates antieméticos)28-30,33-45.
Tranquilizantes
El metaanálisis de los nuevos ECC corrobora que el droperidol reduce las náuseas y el vómito postoperatorio y el uso de rescate antiemético (evidencia A3-B)38,46-50. Varios ECC evidenciaron que el haloperidol es también efectivo (evidencia A2-B)34,47,49,51.
Metoclopramida
Los metaanálisis de ECC que compararon metoclopramida (10 mg) con placebo no reportan diferencias estadísticamente significativas en náusea y vómito en el periodo postoperatorio inmediato (evidencia A1-E), pero indican eficacia en la reducción del vómito durante las primeras 24 h del periodo postoperatorio (evidencia categoría A1-B)35,39,44,52-55.
Dexametasona
El metaanálisis de ECC reporta que este antiemético es efectivo en la profilaxis del vómito postoperatorio (reduce el uso de antieméticos de rescate) y como profilaxis de náusea (se observó efectividad a mayores dosis) (evidencia categoría A1-B)29,33,45,48,49,51,52,54-67.
Combinaciones
La combinación de 2 medicamentos antieméticos es efectiva en la profilaxis de náusea y vómito postoperatorio (evidencia categoría A2-B), sin diferencias en los efectos secundarios como cefalea, mareo, somnolencia e inquietud24,31,32,48,53,56,68-77.
Actualización
Una revisión sistemática78 sobre el tratamiento de las náuseas y el vómito postoperatorio considera una evidencia similar sobre los medicamentos que pueden ser eficaces para la profilaxis y el tratamiento de estos eventos. La revisión considera como primera elección farmacológica al ondansetrón.
Indicaciones
La profilaxis con antieméticos de las náuseas y el vómito asociado con la anestesia mejora la satisfacción y el bienestar del paciente, reduciendo los tiempos de salida de la unidad de cuidado postoperatorio.
La profilaxis y el tratamiento de las náuseas y el vómito asociados con la anestesia mejora con ondansetrón, droperidol o dexametasona, que también disminuyen el rescate antiemético.
Se considera como medicamento de primera línea al ondansetrón.
No se tiene evidencia concluyente sobre el uso de múltiples fármacos para el tratamiento de las náuseas y el vómito en recuperación.
Antagonismo de los efectos de sedantes, analgésicos y agentes de bloqueo neuromuscular
Antagonismo de las benzodiacepinas
Un nuevo ECC79 corroboró los hallazgos de la Guía 200217 sobre la eficacia del flumazenil para antagonizar los efectos residuales de las benzodiacepinas luego de anestesia general, comparado con placebo (evidencia A3-B). En la Guía 200217 se mencionaba que el flumazenil reducía el tiempo para emergencia después de sedación (evidencia A1-B).
Los expertos17 están en desacuerdo con el uso de rutina del flumazenil para reducir los eventos adversos o mejorar la comodidad o satisfacción del paciente.
Antagonismo de los opiáceos
La Guía 200217 indicaba que la naloxona reducía el tiempo para la emergencia y recuperación de la respiración espontánea (evidencia A3-B). Los expertos no están de acuerdo con el uso rutinario de naloxona para reducir los eventos adversos o mejorar la comodidad o satisfacción de los pacientes.
Reversión de los agentes relajantes neuromusculares
La Guía 200217 indicaba que la neostigmina es efectiva para antagonizar el efecto residual de los relajantes musculares (evidencia A1-B), aunque demostraba un aumento de los episodios de emesis postoperatoria (evidencia A1-H).
No hay consenso de los expertos en que los regímenes anestésicos diseñados para evitar el uso de antagonismo del bloqueo neuromuscular reducen los desenlaces adversos y mejoran la satisfacción y el bienestar del paciente.
Indicaciones
El flumazenil no debería ser administrado rutinariamente, aunque podría proporcionarse cuando se evidencie depresión respiratoria y sedación en pacientes a quienes se les puede atribuir el uso de benzodiacepinas como causa. Posterior al uso del antagonismo farmacológico, los pacientes deben ser observados por largo tiempo para asegurar que la depresión respiratoria no recurra.
No se recomiendan los antagonistas opiáceos (naloxona) para su uso rutinario. Sin embargo, pueden ser administrados cuando se presenta depresión respiratoria de causa atribuible al uso de opiáceos. Después del antagonismo farmacológico, el paciente debe ser observado por un largo periodo para evitar la recurrencia en la depresión respiratoria. El antagonismo agudo de los opiáceos puede desencadenar dolor, hipertensión, taquicardia y edema pulmonar.
Los antagonistas específicos deben ser administrados para revertir el bloqueo neuromuscular residual cuando esté indicado.
El flumazenil, la naloxona o los antagonistas del bloqueo neuromuscular deben estar disponibles para ser administrados en caso de ser necesarios.
Los antagonistas específicos del bloqueo neuromuscular deben estar disponibles para revertir el bloqueo cuando está indicado.
Tratamiento en la unidad de cuidado postoperatorio
Administración de oxígeno suplementario
Un ECC80 demostró que la administración de oxígeno suplementario durante el transporte y en la unidad de cuidado postoperatorio reduce la incidencia de hipoxemia (evidencia A3B).
Temperatura
La Guía 200217 incluía evidencia de que el calentamiento activo del paciente está asociado con la normalización de su temperatura (evidencia A2-B). Existe evidencia de que el uso de dispositivos de calentamiento por aire a presión normaliza la temperatura del paciente (evidencia categoría A3-B). Este último hallazgo se corrobora en un reciente ECC, pero no evidencia disminución de los escalofríos (evidencia A3-E)81.
Uso de agentes farmacológicos para la reducción del escalofrío postoperatorio
En la Guía 200217 se describe que la meperidina es efectiva para el manejo del escalofrío postoperatorio comparada con otros agonistas opiáceos y contra placebo (evidencia A1-B).Un nuevo ECC82 encontró que la meperidina disminuyó el escalofrío cuando se comparó con fármacos (evidencia A3-B).
Se han demostrado los efectos de la dexmedetomidina para el control de los escalofríos en niños (evidencia B3) y el relacionado con anestesia regional (evidencia A3)83-84.
Indicaciones
La administración de oxígeno suplementario durante el traslado y el cuidado anestésico postoperatorio debe ser realizada en los pacientes con riesgo de hipoxemia.
La normotermia debería ser uno de los objetivos durante el cuidado postoperatorio. Cuando están disponibles, los dispositivos de calentamiento por aire a presión deben ser usados.
La meperidina puede ser usada para el manejo del escalofrío en el postoperatorio cuando está clínicamente indicada y no tiene contraindicaciones.
Salida o alta de los pacientes de la unidad de cuidado postoperatorio
Requisito que el paciente presente orina espontánea antes de la salida
Puede incrementar el tiempo de salida y debería ser obligatorio solamente en pacientes seleccionados. No se considera un requisito indispensable para el egreso de los pacientes.
Requisito que el paciente tome líquidos claros antes de la salida
Puede alargar la estancia del paciente en la unidad. No se considera imperativo que el paciente tome líquidos claros antes de la salida. En la Guía 2002 se consideró una evidencia A2-E. Los expertos no consideran que mejore la comodidad o la satisfacción del paciente17.
Requisito que el paciente cuente con un acompañante responsable antes de la salida a casa
Se considera que la necesidad de tener un acompañante responsable al momento de la salida del paciente ambulatorio disminuye el riesgo de complicaciones e incrementa la satisfacción y el bienestar del paciente. Debe ser obligatorio, de acuerdo con las opiniones de los expertos. La evidencia científica es insuficiente.
Necesidad de un tiempo mínimo de estadía en la unidad de cuidado postanestésico
La evidencia es insuficiente y los expertos no consideran que se requiera un mínimo de estadía. Esta debe ser determinada para cada caso. No hay consenso si una estancia mínima disminuye los eventos adversos o complicaciones.
Evaluación de la actividad motora posterior a anestesia regional
Según las normas mínimas de seguridad en anestesia de la SCARE 201385, se sugiere utilizar una escala que permita medir el retorno de la actividad motora; la más usada es la escala de Bromage86 (tabla 5).
Evaluación de criterios para salida
En una revisión sistemática se considera que toda valoración para el egreso debe incluir estado de conciencia, presión arterial, situación de dolor y náusea/vómito87. La escala de Aldrete incluye estos aspectos, por lo que se podría considerar la escala seleccionada para este fin88 (tabla 6).
Actualización
El grupo de consenso considera como una práctica deseable que un funcionario de la institución acompañe al paciente hasta la salida física de la institución.
Indicaciones
Los requisitos de orinar o tomar líquidos antes de la salida podrían ser obligatorios en pacientes específicos.
Como parte de los protocolos de salida de cada institución, todos los pacientes con egreso hospitalario deben tener un acompaÁante responsable al momento de la salida.
No se recomienda un tiempo mínimo en la unidad de cuidado postoperatorio, de manera rutinaria. Este tiempo de estancia debe ser establecido para cada paciente.
Considerar chequear la disponibilidad de vía permeable, drenajes y catéteres de ser necesario.
Verificar los registros completos.
Debe valorarse, mediante una escala de criterios para egreso tipo Aldrete, a cada uno de los pacientes antes de su alta de la unidad de cuidado postoperatorio.
Información para trabajar con los pacientes
En el caso de egreso de la unidad de cuidado postoperatorio a casa deben entregarse por escrito las recomendaciones relacionadas con la cirugía, los signos de alarma y los eventos adversos inesperados19-20.
Financiación
Este proyecto fue financiado por la Sociedad Colombiana de Anestesiología y Reanimación (SCARE) en convenio colaborativo con la Facultad de Medicina de la Universidad Nacional de Colombia.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Anexo. Material adicional
Se puede consultar material adicional a este artículo en su versión electrónica disponible en http://dx.doi.org/10.1016/j.rca.2014.10.008.
Referencias
1. Kohn L, Corrigan JM, Donaldson M, editors. Committee on Quality of Health Care in America, Institute of Medicine, To err is human: building a safer health system. Washington, DC: National Academy Press; 2000. [ Links ]
2. Bainbridge D L, Martin J, Arango M, Cheng D, Evidence-based Peri-operative Clinical Outcomes Research (EPiCOR) Group. Perioperative and anaesthetic-related mortality in developed and developing countries: a systematic review and meta-analysis. Lancet. 2012;380:1075-81. [ Links ]
3. Braz LG, Braz DG, Cruz DS, Fernandes LA, Módolo NS, Braz JR. Mortality in anesthesia: a systematic review. Clinics (Sao Paulo). 2009;64:999-1006. [ Links ]
4. Schiff JH, Henn-Beilharz A, Welker A, Fohr B, Bothner U, Van Aken H, et al. Major incidents and complications in otherwise healthy patients undergoing elective procedures: results based on 1.37 million anaesthetic procedures. Br J Anaesth. 2014;113:109-21. [ Links ]
5. Apfel CC, Korttila K, Abdalla M, Kerger H, Turan A, Vedder I, et al. A factorial trial of six interventions for the prevention of postoperative nausea and vomiting. N Engl J Med. 2004;350:2441. [ Links ]
6. Hines R, Barash PG, Watrous G, O'Connor T. Complications occurring in the postanesthesia care unit: a survey. Anesth Analg. 1992;74:503. [ Links ]
7. Frost EA. Complications in the postanesthetic care unit. Middle East J Anesthesiol. 1992;11:525-47. [ Links ]
8. Khuri S, Henderson W, DePalma R, Mosca C, Healey N, Kumbhani D. Determinants of long-term survival after major surgery and the adverse effect of postoperative complications. Ann Surg. 2005;242:326-41. [ Links ]
9. Manku K, Bacchetti P Leung J. Prognostic significance of postoperative in-hospital complications in elderly patients. I. Long-term survival. Anesth Analg. 2003;96:583. [ Links ]
10. Thompson JS, Baxter BT, Allison JG, Johnson FE, Lee KK, Park WY, et al. Temporal patterns of postoperative complications. Arch Surg. 2003;138:596-603. [ Links ]
11. Annemie V, Verelst S, Bekkering GE, Schrooten W, Hellings J, Claes N. Incidence and preventability of adverse events requiring intensive care admission: a systematic review. J Eval Clin Pract. 2012;18:485-97. [ Links ]
12. Eichenberger A, Haller G, Cheseaux N, Lechappe V, Garnerin P, Walder B. A clinical pathway in a post-anaesthesia car unit to reduce length of stay, mortality and unplanned intensive care unit admission. Eur J Anaesthesiol. 2011;28: 859-66. [ Links ]
13. Falk SA. Postoperative care. Anesthesiol Clin. 2012;30:xi-ii. [ Links ]
14. Apfelbaum JL. Task Force on Postanesthetic Care. Practice guidelines for postanesthetic care: an updated report by the American Society of Anesthesiologists Task Force on Postanesthetic Care. Anesthesiology. 2013;118: 291-307. [ Links ]
15. U.S. news best hospitals 2014-15. Available from: http://health.usnews.com/best-hospitals/rankings?int=a01008 [accessed 28.08.14] [ Links ].
16. Cluzeau FA, Burgers JS, Brouwers M, Grol R, Mákelá M, Littlejohns P, et al. The AGREE Collaboration Writing Group: development and validation of an international appraisal instrument for assessing the quality of clinical practice guidelines: the AGREE project. Qual Saf Health Care. 2003;12:18-23. [ Links ]
17. American Society of Anesthesiologists Task Force on Postanesthetic Care. Practice guidelines for postanesthetic care: a report by the American Society of Anesthesiologists Task Force on Postanesthetic Care. Anesthesiology. 2002;96:742-52. [ Links ]
18. Whitaker DK, Booth H, Clyburn P, Harrop-Griffiths W, Hosie H, Kilvington B, et al. Immediate post-anaesthesia recovery 2013: Association of Anaesthetists of Great Britain and Ireland. Anaesthesia. 2013;68:288-97. [ Links ]
19. Scottish Intercollegiate Guidelines Network. Postoperative managemen in adults. Edimburgo: SIGN; 2004. [ Links ]
20. Williams PL, Webb C. The Delphi technique: a methodological discussion. J Adv Nurs. 1994;19:180-6. [ Links ]
21. Fitch KB, Bernstein SJ, Aguilar MD, Burnand B, La Calle JR, Lazaro P, et al. The RAND/UCLA appropriateness method. Santa Monica: RAND; 2001. [ Links ]
22. Vimlati L, Gilsanz F Goldik Z. Quality and safety guidelines of postanaesthesia care: Working Party on Post Anaesthesia Care (approved by the European Board and Section of Anaesthesiology, Union Européenne des Médecins Spécialistes). Eur J Anaesthesiol. 2009;26: 715-21. [ Links ]
23. Burmeister MA, Standl TG, Wintruff M, Brauer P, Blanc I, Schulte am Esch J. Dolasetron prophylaxis reduces nausea and postanaesthesia recovery time after remifentanil infusion during monitored anaesthesia care for extracorporeal shock wave lithotripsy. Br J Anaesth. 2003;90:194-8. [ Links ]
24. Eberhart LH, Morin AM, Hoerle S, Wulf H, Geldner G. Droperidol and dolasetron alone or in combination for prevention of postoperative nausea and vomiting after vitrectomy. Ophthalmology. 2004;111: 1569-75. [ Links ]
25. Iatrou CA, Dragoumanis CK, Vogiatzaki TD, Vretzakis GI, Simopoulos CE, Dimitriou VK. Prophylactic intravenous ondansetron and dolasetron in intrathecal morphine-induced pruritus: a randomized, double-blinded, placebo-controlled study. Anesth Analg. 2005;101: 1516-20. [ Links ]
26. Sukhani R, Pappas AL, Lurie J, Hotaling AJ, Park A, Fluder E. Ondansetron and dolasetron provide equivalent postoperative vomiting control after ambulatory tonsillectomy in dexamethasone-pretreated children. Anesth Analg. 2002;95:1230-5. [ Links ]
27. Wagner D, Pandit U, Voepel-Lewis T, Weber M. Dolasetron for the prevention of postoperative vomiting in children undergoing strabismus surgery. Paediatr Anaesth. 2003;13:522-6. [ Links ]
28. Dua N, Bhatnagar S, Mishra S, Singhal AK. Granisetron and ondansetron for prevention of nausea and vomiting in patients undergoing modified radical mastectomy. Anaesth Intensive Care. 2004;32:761-4. [ Links ]
29. Erhan Y, Erhan E, Aydede H, Yumus O, Yentur A. Ondansetron, granisetron, and dexamethasone compared for the prevention of postoperative nausea and vomiting in patients undergoing laparoscopic cholecystectomy: a randomized placebo-controlled study. Surg Endosc. 2008;22: 1487-92. [ Links ]
30. Jain V, Mitra JK, Rath GP, Prabhakar H, Bithal PK, Dash HH. A randomized, double-blinded comparison of ondansetron, granisetron, and placebo for prevention of postoperative nausea and vomiting after supratentorial craniotomy. J Neurosurg Anesthesiol. 2009;21:226-30. [ Links ]
31. Moussa AA, Oregan PJ. Prevention of postoperative nausea and vomiting in patients undergoing laparoscopic bariatric surgery - granisetron alone vs granisetron combined with dexamethasone/droperidol. Middle East J Anesthesiol. 2007;19:357-67. [ Links ]
32. Tseng LH, Liou SC, Chang TC, Tsai SC, Soong YK, Wong SY. A randomized blinded study of the incidence of postoperative nausea and vomiting in women after major gynecologic laparoscopic surgery. J Minim Invasive Gynecol. 2006;13: 413-7. [ Links ]
33. Alghanem SM Massad IM, Rashed EM, Abu-Ali HM, Daradkeh SS. Optimization of anesthesia antiemetic measures versus combination therapy using dexamethasone or ondansetron for the prevention of postoperative nausea and vomiting. Surg Endosc. 2010;24:353-8. [ Links ]
34. Aouad MT, Siddik-Sayyid SM, Taha SK, Azar MS, Nasr VG, Hakki MA, et al. Haloperidol vs. ondansetron for the preventio of postoperative nausea and vomiting following gynaecological surgery. Eur J Anaesthesiol. 2007;24: 171-8. [ Links ]
35. Ekinci O, Malat I, Iitmangil G, Aydin N. A randomized comparison of droperidol, metoclopramide, tropisetron, and ondansetron for the prevention of postoperative nausea and vomiting. Gynecol Obstet Invest. 2011;71:59-65. [ Links ]
36. Elhakin M, Nafie M, Mahmoud K, Atef A. Dexamethasone 8 mg in combination with ondansetron 4 mg appears to be the optimal dose for the prevention on nausea and vomiting after laparoscopic cholecystectomy. Can J Anaesth. 2002;49: 922-6. [ Links ]
37. Grove VK, Mathew PJ, Hedge H. Efficacy of orally disintegrating ondansentron in preventing postoperative nausea and vomiting after laparoscopic cholecystectomy: a randomised, double blind placebo controlled study. Anaesthesia. 2009;64:595-600. [ Links ]
38. Kathirvel S, Dash HH, Bhatia A, Subramaniam B, Prakash A, Shenoy S. Effect of prophylactic ondansentron on post-operative nausea and vomiting after elective craniotomy. J Neurosurg Anesthesiol. 2001;13: 2007-12. [ Links ]
39. Pan PH, Moore CH. Comparing the efficacy of prophylactic metoclopramide, ondansetron, and placebo in cesarean section patients given epidural anesthesia. J Clin Anesth. 2001;13:430-5. [ Links ]
40. Peixoto AJ, Celich MF, Zardo L, Peixoto Filho AJ. Ondansetron or droperidol for prophylaxis of nausea and vomiting after intrathecal morphine. Eur J Anaesthesiol. 2006;23:670-5. [ Links ]
41. Pirat A, Tuncay SF, Torgay A, Candan S, Arslan G. Ondasentron, orally disintegrating tablets versus intravenous injection for prevention or intrathecal morphine-induced nausea, vomiting, and pruritus in young males. Anesth Analg. 2005;101:1330-6. [ Links ]
42. Tzeng JI, Chu KS, Ho ST, Cheng KI, Liu KS, Wang JJ. Prophylactic iv ondansentron reduces nausea, vomiting and pruritus following epidural morphine for postoperative pain control. Can J Anaesth. 2003;40:1023-6. [ Links ]
43. Wig J, Chandrashekharappa KN, Yaddanapudi LN, Nakra D, Mukherjee KK. Effect of prophylactic ondansentron on post-operative nausea and vomiting in patients on preoperative steroids undergoing craniotomy for supratentorial tumors. J Neurosurg Anesthesiol. 2007;19:239-42. [ Links ]
44. Wilson EB, Bass CS, Abrameit W, Roberson R, Smith RW. Metoclopramide versus ondansetron in prophylaxis of nausea and vomiting for laparoscopic cholecystectomy. Am J Surg. 2001;181:138-41. [ Links ]
45. Yuksek MS, Alici HA, Erdem AF, Cesur M. Comparison of prophylactic anti-emetic effects of ondansetron and dexamethasone in women undergoing day-case gynaecological laparoscopic surgery. J Int Med Res. 2003;31:481-8. [ Links ]
46. Apfel CC, Cakmakkaya OS, Frings G, Kranke P, Malhotra A, Stader A, et al. Droperidol has comparable clinical efficacy against both nausea and vomiting. Br J Anaesth. 2009;103:359-63. [ Links ]
47. Chu CC, Shieh JP, Tzeng JI, Chen JY, Lee Y, Ho ST, et al. The prophylactic effect of haloperido plus dexamethasone on postoperative nausea and vomiting in patients undergoing laparoscopically assisted vaginal hysterectomy. Anesth Analg. 2008;106:1402-6. [ Links ]
48. Ho ST, Wang JJ, Tzeng JI, Liu HS, Ger LP, Liaw WJ. Dexamethasone for preventing nausea and vomiting associated with epidural morphine: a dose-ranging study. Anesth Analg 2001;92:745-8 [ Links ]
49. Wang TF, Liu YH, Chu CC, Shieh JP, Tzeng JI, Wang JJ. Low-dose haloperidol prevents post-operative nausea and vomiting after ambulatory laparoscopic surgery. Acta Anaesthesiol Scand. 2008;52:280-4. [ Links ]
50. Wu JI, Lo YChia YY, Liu K, Fong WP, Yang LC, et al. Prevention of postoperative nausea and vomiting after intrathecal morphine for Cesarean section: a randomized comparison of dexamethasone, droperidol, and a combination. Int J Obstet Anesth. 2007;16:122-7. [ Links ]
51. Parlow JL, Costache I, Avery N, Turner K. Single-dose haloperidol for the prophylaxis of postoperative nausea and vomiting after intrathecal morphine. Anesth Analg. 2004;98:1072-6. [ Links ]
52. Huang JC, Shieh JP, Tang CS, Tzeng JI, Chu KS, Wang JJ. Low-dose dexamethasone effectively prevents postoperative nausea and vomiting after ambulatory laparoscopic surgery. Can J Anaesth. 2001;48:973-7. [ Links ]
53. Nesek-Adam VGrizelj-Stojcic E, Mrsic V,Smiljanic A, Rasic Z, Cala Z. Prophylactic antiemetics for laparoscopic cholecystectomy: droperidol, metoclopramide, and droperidol plus metoclopramide. J Laparoendosc Adv Surg Tech A. 2004;14:212-8. [ Links ]
54. Nesek-Adam V. Grizelj-Stojcic: E, Rasic: Z, Cala Z, Mrsic V, Smiljanic A. Comparison of dexamethasone, metoclopramide, and their combinatio in the prevention of postoperative nausea and vomiting after laparoscopic cholecystectomy. Surg Endosc. 2007;21:607-12. [ Links ]
55. Tzeng JI, Hsing CH, Chu CC, Chen YH, Wang JJ. Low-dose dexamethasone reduces nausea and vomiting after epidural morphine: a comparison of metoclopramide with saline. J Clin Anesth. 2002;14:19-23. [ Links ]
56. Eberhart LH, Buning EK, Folz B, Maybauer DM, Kastner M, Kalder M, et al. Anti-emetic prophylaxis with oral tropisetron and/or dexamethasone. Eur J Clin Invest. 2006;36:580-7. [ Links ]
57. Ang JJ, Ho ST, Uen YH, Lin MET, Chen KT, Huang JC, et al. Small-dose dexamethasone reduces nausea and vomiting after laparoscopic cholecystectomy: a comparison of tropisetron with saline. Anesth Analg. 2002;95:229-32. [ Links ]
58. Bianchin A, De Luca A, Caminiti A. Postoperative vomiting reduction after laparoscopic cholecystectomy with single dose of dexamethasone. Minerva Anestesiol. 2007;73:343-6. [ Links ]
59. Coloma M, Duffy LL, White PF, Kendall Tongier W, Huber PJ Jr. Dexamethasone facilitates discharge after outpatient anorectal surgery. Anesth Analg. 2001;92:85-8. [ Links ]
60. Feo CV, Sortini D, Ragazzi R, De Palma M, Liboni A. Randomized clinical trial of the effect of preoperative dexamethasone on nausea and vomiting after laparoscopic cholecystectomy. Br J Surg. 2006;93:295-9. [ Links ]
61. Gómez-Hernández J, Orozco-Alatorre AL, Domínguez-Contreras M, Oceguera-Villanueva A, Gómez-Romo S, Alvarez Villaseñor AS, et al. Preoperative dexamethasone reduces postoperative pain, nausea and vomiting following mastectomy for breast cancer. BMC Cancer. 2010;10:692. [ Links ]
62. Koç S, Memis D, Sut N. The preoperative use of gabapentin, dexamethasone, and their combination in varicocele surgery: a randomized controlled trial. Anesth Analg. 2007;105:1137-42. [ Links ]
63. Lee Y, Lai HY, Lin PC, Lin YS, Huang SJ, Shyr MH. A dose ranging study of dexamethasone for preventing patient-controlled analgesia-related nausea and vomiting: a comparison of droperidol with saline. Anesth Analg. 2004;98:1066-71. [ Links ]
64. Lee Y, Lin PC, Lai HY, Huang SJ, Lin YS, Cheng CR. Prevention of PONV with dexamethasone in female patients undergoing desflurane anesthesia for thyroidectomy. Acta Anaesthesiol Sin. 2001;39:151-62003, 90:665-70. [ Links ]
65. Nortcliffe SA, Shah J, Buggy DJ. Prevention of postoperative nausea and vomiting after spinal morphine for Caesarean section: comparison of cyclizine, dexamethasone and placebo. Br J Anaesth. 2003;90:665-70. [ Links ]
66. Nazar CE, Lacassie HJ, López RA, Muñoz HR. Dexamethasone for postoperative nausea and vomiting prophylaxis: effect on glycaemia in obese patients with impaired glucose tolerance. Eur J Anaesthesiol. 2009;26:318-21. [ Links ]
67. Sánchez-Rodríguez PE, Fuentes-Orozco C, González-Ojeda A. Effect of dexamethasone on postoperative symptoms in patients undergoing elective laparoscopic cholecystectomy: randomized clinical trial. World J Surg. 2010;34: 895-900. [ Links ]
68. Awad IT, Murphy D, Stack D, Swanton BJ, Meeke RI, Shorten GD. A comparison of the effects of droperidol and the combination of droperidol and ondansetron on postoperative nausea and vomiting for patients undergoing laparoscopic cholecystectomy. J Clin Anesth. 2002;14:481-5. [ Links ]
69. Chaparro LE, Gallo T, Gonzalez NJ, Rivera MF, Peng PW. Effectiveness of combined haloperidol and dexamethasone versus dexamethasone only for postoperative nausea and vomiting in high-risk day surgery patients: a randomized blinded trial. Eur J Anaesthesiol. 2010;27:192-5. [ Links ]
70. Coloma M, White PF, Markowitz SD, Whitten CW, Macaluso AR, Berrisford SB, et al. Dexamethasone in combination with dolasetron for prophylaxis in the ambulatory setting: effect on outcome after laparoscopic cholecystectomy. Anesthesiology. 2002;96:1346-50. [ Links ]
71. Dagtekin O, Wiese P, Wolter K, Hermann MM, Pietruck C, Kampe S. Haloperidol versus haloperidol plus ondansetron for the prophylaxis of postoperative nausea and vomiting after ophthalmologic surgery. Pharmacology. 2009;83: 205-10. [ Links ]
72. Grecu L, Bittner EA, Kher J, Smith SE, Rosow CE. Haloperidol plus ondansetron versus ondansetron alone for prophylaxis of postoperative nausea and vomiting. Anesth Analg. 2008;106:1410-3. [ Links ]
73. Jones S, Strobl R, Crosby D, Burkard JF, Maye J, Pellegrini JE. The effect of transdermal scopolamine on the incidence and severity of postoperative nausea and vomiting in a group of high-risk patients given prophylactic intravenous ondansetron. AANA J. 2006;74:127-32. [ Links ]
74. Panda NB, Bharadwaj N, Kapoor P, Chari P, Panda NK. Prevention of nausea and vomiting after middle ear surgery: combination of ondansetron and dexamethasone is the right choice. J Otolaryngol. 2004;33:88-92. [ Links ]
75. Splinter WM. Prevention of vomiting after strabismus surgery in children: dexamethasone alone versus dexamethasone plus low-dose ondansetron. Paediatr Anaesth. 2001;11:591-5. [ Links ]
76. Szarvas S, Chellapuri RS, Harmon DC, Owens J, Murphy D, Shorten GD. A comparison of dexamethasone, ondansetron, and dexamethasone plus ondansetron as prophylactic antiemetic and antipruritic therapy in patients receiving intrathecal morphine for major orthopedic surgery. Anesth Analg. 2003;97:259-63. [ Links ]
77. Wallenborn J, Gelbrich G, Bulst D, Behrends K, Wallenborn H, Rohrbach A, et al. Prevention of postoperative nausea and vomiting by metoclopramide combined with dexamethasone: randomised double blind multicentre trial. BMJ. 2006;333:324. [ Links ]
78. Gan TH, Diemunsch P, Habib AS, Kovac A, Kranke P, Meyer TA, et al. Consensus Guidelines for the management of postoperative nausea and vomiting. Anesth Analg. 2014;118:85-111. [ Links ]
79. Araki H, Fujiwara Y, Shimada Y. Effect of flumazenil on recovery from sevoflurane anesthesia in children premedicated with oral midazolam before undergoing herniorrhaphy with or without caudal analgesia. J Anesth. 2005;19:204-7. [ Links ]
80. Mathes DD, Conaway MR, Ross WT. Ambulatory surgery: room air versus nasal cannula oxygen during transport after general anesthesia. Anesth Analg. 2001;93:917-21. [ Links ]
81. Person K, Lundberg J. Perioperative hypothermia and postoperative opioid requirements. Eur J Anaesthesiol. 2001;18:679-86. [ Links ]
82. Schwarzkopf KR, Horr H, Hartmann M, Fritz HG. A comparison between meperidine, clonidine and urapidil in the treatment of postanesthetic shivering. Anesth Analg. 2001;92: 257-60. [ Links ]
83. Blaine Easley R, Brady KM, Tobias JD. Dexmedetomidine for the treatment of postanesthesia shivering in children. Paediatr Anaesth. 2007;17:341-6. [ Links ]
84. Usta B, Gozdemir M, Demircioglu RI, Muslu B, Sert H, Yaldiz A. Dexmedetomidine for the prevention of shivering during spinal anesthesia. Clinics (Sao Paulo). 2011;66:1187-91. [ Links ]
85. Galindo Arias M, Carrillo Cifuentes R, Giraldo JC, Ibarra Murcia P, Niño de Mejía C, Robledo B. Normas mínimas de seguridad en Anestesiología CLASA - SCARE 2006. Rev Colomb Anestesiol. 2006;34:185-90. [ Links ]
86. Bromage PR, editor. Epidural analgesia. Philadelphia: WB Saunders; 1978. p. 144. [ Links ]
87. Phillips NM, Haesler E, Street M, Kent B. Post-anaesthetic discharge scoring criteria: a systematic review. JBI Library Syst Rev. 2011;9:1679-713. [ Links ]
88. Aldrete JA. The post anesthesia recovery score revisited. J Clin Anesth. 1995;7:89-91. [ Links ]











 text in
text in