Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Colombian Journal of Anestesiology
versão impressa ISSN 0120-3347
Rev. colomb. anestesiol. vol.43 no.1 Bogotá jan./mar. 2015
https://doi.org/10.1016/j.rcae.2014.11.004
http://dx.doi.org/10.1016/j.rca.2014.10.009
Guías y consensos
Manual de práctica clínica basado en la evidencia: preparación del paciente para el acto quirúrgico y traslado al quirófano
Evidence-based clinical practice manual: Patient preparation for surgery and transfer to the operating room
David A. Rincón-Valenzuelaa,* y Bibiana Escobarb
a Médico Anestesiólogo, Magister en Epidemiología Clínica, Profesor de Anestesiología, Universidad Nacional de Colombia; Anestesiólogo, Clínica Universitaria Colombia, Bogotá, Colombia
b Médica Anestesióloga, PhD en Ciencias Médicas, Profesora de Anestesiología, Universidad Nacional de Colombia, Instituto Nacional de Cancerología, Bogotá, Colombia
* Autor para correspondencia: CI 23B 66-46 Consultorio 403, Bogotá, Colombia.
Correo electrónico: darinconv@unal.edu.co (D.A. Rincón-Valenzuela).
Información del artículo
Historia del artículo: Recibido el 8 de octubre de 2014 Aceptado el 25 de octubre de 2014
Resumen
Introducción: La preparación del paciente para el acto quirúrgico y el traslado del paciente al quirófano son 2 procesos prioritarios definidos dentro de los procedimientos y condiciones de habilitación de servicios de salud por parte del Ministerio de Salud y la Protección Social en Colombia.
Objetivos: El objetivo de esta iniciativa fue desarrollar un manual de manejo clínico basado en la evidencia sobre la preparación del paciente para el acto quirúrgico y traslado al quirófano.
Materiales y métodos: Se realizó un proceso dividido en 4 fases (conformación del grupo elaborador, revisión sistemática de literatura secundaria, método participativo de consenso, y preparación y escritura del documento final). Cada una de ellas usó técnicas y procedimientos estandarizados para el desarrollo de manuales basados en la evidencia. Resultados: Se realizaron recomendaciones basadas en la evidencia sobre valoración preanestésica, manejo preoperatorio de condiciones médicas, educación y comunicación con los pacientes, consentimiento informado, traslado del paciente al área quirúrgica, marcación del sitio quirúrgico, estrategias para la prevención de infecciones, y lista de chequeo preoperatorio.
Conclusiones: Se espera que con el uso de este manual se minimice la incidencia de eventos que produzcan morbimortalidad en pacientes sometidos a procedimientos quirúrgicos.
Palabras clave: Quirófanos, Medicina Basada en la Evidencia, Anestesia, Infección de Herida Operatoria, Lista de Verificación.
Abstract
Introduction: Patient preparation for surgery and transfer to the operating room are two priority processes defined within the procedures and conditions for authorization of health care services by the Ministry of Social Protection in Colombia.
Objectives: The aim of this initiative was to develop a manual of clinical management based on the evidence on patient preparation for surgery and transfer to the operating room.
Materials and methods: A process divided into four phases (conformation of the development group, systematic review of secondary literature, participatory consensus method, and preparation and writing of the final document) was performed. Each standardized techniques and procedures used to develop evidence-based manuals.
Results: Evidence-based recommendations on pre-anesthetic assessment, preoperative management of medical conditions, education and patient communication, informed consent, patient transfer to the surgical area, surgical site marking, strategies for infection prevention and checklist were performed.
Conclusion: It is expected that with the use of this manual the incidence of events that produce morbidity and mortality in patients undergoing surgical procedures will be minimized.
Keywords: Operating Rooms, Evidence-Based Medicine, Anesthesia, Surgical Wound Infection, Checklist.
Introducción
Los protocolos tienen un papel fundamental en la práctica clínica, particularmente para garantizar la seguridad en la atención de los pacientes. Esto se debe a que su adopción minimiza la variabilidad de procedimientos, registros, tratamientos y tareas realizados rutinariamente. Los protocolos facilitan la estandarización e incrementan la confiabilidad en el cuidado de la salud del paciente, reduciendo el error humano en la ejecución de procesos complejos1. La posibilidad de seguir protocolos expande la generación de datos cada vez más robustos, permite medir desenlaces e indica-dores y retroalimenta los procesos. El reconocimiento de la existencia de procesos que son críticos dentro de la atención del paciente quirúrgico ha llevado a implementar códigos y técnicas efectivas de comunicación, y a disminuir las distracciones y variaciones durante la realización de los mismos. Lo anterior da soporte a cumplir, cambiar y mejorar las acciones emprendidas para disminuir los riesgos que amenazan la vida y el bienestar de los pacientes dentro del ambiente quirúrgico. Actualmente, en todos los países la seguridad del paciente es un campo de estudio e investigación del cual se han derivado conocimientos y prácticas de indudable beneficio, como la conocida WHO Surgical Safety Checklist2. Los eventos de los que más evidencia se dispone incluyen los llamados «eventos que nunca deben ocurrir» (en inglés, never events):
La realización de un procedimiento quirúrgico al paciente equivocado.
La realización de un procedimiento equivocado al paciente.
La realización de un procedimiento quirúrgico en el sitio equivocado.
La permanencia de cuerpo extraño olvidado después de la cirugía3.
También se cuentan otros, como la infección del sitio operatorio y la hipotermia.
En Colombia, el Ministerio de Salud y Protección Social ha establecido los procedimientos y condiciones de habilitación de servicios de salud y ha definido los procesos prioritarios dentro de las condiciones de habilitación de los servicios quirúrgicos. Dos de estos procesos son la preparación del paciente para el acto quirúrgico y el traslado del paciente al quirófano. Este protocolo establece los pasos ineludibles de aplicación constante y sistemática por parte de un equipo interdisciplinario informado y comprometido con el cuidado y bienestar del paciente quirúrgico.
Si bien será aplicado antes del procedimiento quirúrgico (periodo preoperatorio), su ejecución obliga al equipo a anticipar medidas diagnósticas o terapéuticas durante la cirugía (período intraoperatorio) o después de la cirugía (período postoperatorio). Por todo esto, en ciertos apartados el protocolo hace referencia al perioperatorio (pre, intra y postoperatorio).
El fin del uso de este manual es minimizar la incidencia de eventos que produzcan morbimortalidad en pacientes sometidos a procedimientos anestésicos.
Justificación
La elaboración de este manual está justificada en el cumplimiento de los requisitos de la resolución 2003 de 2014 del Ministerio de Salud, por la cual se definen los procedimientos y condiciones de inscripción de los Prestadores de Servicios de Salud y de habilitación de servicios de salud. En dicha resolución se estableció como un proceso prioritario estándar que las instituciones que prestan servicios quirúrgicos en todos los niveles de complejidad deben contar con un protocolo, manual o procedimiento para la preparación del paciente para el acto quirúrgico y traslado del paciente al quirófano, entre otros.
El objetivo de esta iniciativa fue desarrollar un manual de manejo clínico basado en la evidencia sobre la preparación del paciente para el acto quirúrgico, incluyendo el manejo de complicaciones posquirúrgicas y los controles posquirúrgicos.
MetodologíaSe realizó un proceso dividido en 4 fases. Cada una de ellas usó técnicas y procedimientos estandarizados para el desarrollo de guías y protocolos basados en la evidencia:
Conformación del grupo elaborador.
Revisión sistemática de literatura secundaria.
Método participativo.
Preparación y escritura del documento final.
Conformación del grupo elaborador
Se conformó un grupo de expertos en anestesiología y en epidemiología, quienes establecieron las directrices metodológicas y técnicas en el marco del desarrollo del protocolo. El grupo fue conformado por 2 coordinadores metodológicos con experiencia en el desarrollo de guías de práctica clínica y protocolos de manejo basados en la evidencia, quienes realizaron la coordinación metodológica del proceso. Además se conformaron 3 grupos, cada uno compuesto por un médico especialista en anestesiología y un epidemiólogo con experiencia en análisis crítico de evidencia científica. Todos los miembros del grupo elaborador aceptaron la participación en el proceso y diligenciaron y firmaron el formato de conflicto de intereses, el cual cumple con la normatividad vigente dentro del desarrollo de guías y protocolos basados en la evidencia.
Revisión sistemática de literatura secundaria
Se realizó una revisión sistemática con el propósito de identificar los protocolos clínicos y guías de práctica clínica que abordarán el tema del protocolo. La unidad de análisis de dicha revisión fueron los artículos publicados en revistas científicas o documentos técnicos encontrados como literatura gris:
Protocolos de manejo (o eventualmente guías de práctica clínica) basados en la evidencia que presentaran indicaciones o recomendaciones con relación al manejo clínico por parte del grupo de anestesiología, en el tema del protocolo.
Publicados desde el año 2011 hasta la actualidad.
Publicados en inglés o en español.
Estrategia de búsqueda
Las búsquedas de la literatura fueron diseñadas por el coordinador de búsquedas del grupo Cochrane de Infecciones de Transmisión Sexual. Se diseñó una estrategia de búsqueda digital sensible (anexo 1) con el fin de encontrar los documentos que cumplieran con los criterios antes descritos. La búsqueda se extendió hasta el 24 de agosto de 2014.
Las fuentes de información fueron las bases de datos de literatura científica biomédica Medline, Embase, Lilacs y fuentes de literatura gris: Google Scholar.
>Niv
Selección de evidencia
A partir de los resultados de las estrategias de búsquedas diseñadas se conformó una base de datos de posibles documentos que cumplieran con los criterios antes mencionados. Esta base fue entregadaa2revisores, que de forma independiente, a través de la lectura de títulos y resumen, realizaron la identificación de los documentos que cumplieran con los requisitos. En el caso de que hubiera desacuerdo, los 2 revisores lo dirimieron a través de comunicaciones. Los documentos seleccionados fueron descargados en texto completo y luego se les realizó una tamización final.
Evaluación de la calidad
Se utilizó el instrumento AGREE II como herramienta para la evaluación de la calidad de la evidencia encontrada en el paso anterior (anexo 2). Este análisis de la calidad se realizó de forma pareada4.
Finalmente se identificó un protocolo que cumplió con los requisitos de elegibilidad y que sirvió de documento fuente para la adaptación del protocolo de manejo clínico en el contexto mencionado. La identificación final del documento fuente se realizó con base en el criterio clínico de los expertos, actualidad (vigencia), exhaustividad en las indicaciones (recomendaciones) y calidad del documento.
Calificación de la calidad de la evidencia y fuerza de la recomendación
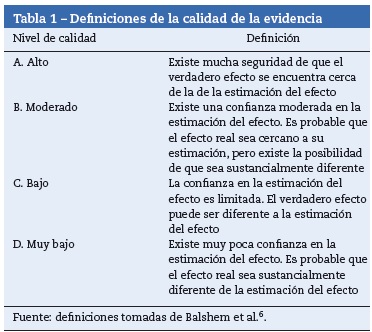
Se usó la estrategia Grade para informar la calidad de la evidencia de la fuente y la fuerza de la recomendación5,6 (tablas 1 y 2).
Método participativo
Se utilizó una modificación del método Delphi. El grupo elaborador escogió a los expertos que participaron en el Delphi. La reunión fue realizada el jueves 18 de septiembre en las instalaciones de la SCARE y contó con la participación de 28 expertos en anestesiología y epidemiología.
La reunión tuvo la siguiente agenda:
i. Presentación de proyecto.
ii. Metodología de la reunión.
iii. Resultados de la evidencia.
iv. Contenido clínico del manual.
v. Votación.
Después de la presentación del contenido clínico del manual y de la discusión por parte de los expertos, se realizó una evaluación del acuerdo que tenían los expertos con relación a si el protocolo cumplía con las siguientes características:
Implementabilidad: evalúa la posibilidad de que el manual sea fácilmente utilizado en las diferentes instituciones.
Actualización: evalúa si las indicaciones están actualizadas con relación a la evidencia actual.
Pertinencia: evalúa si las indicaciones son pertinentes para el contexto de la mayoría de las áreas quirúrgicas.
Consideraciones éticas: evalúa si es ético utilizar este manual.
Seguridad del paciente: evalúa si existe un riesgo elevado en la utilización de este protocolo para los pacientes.
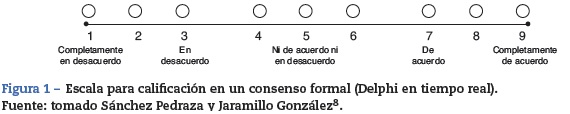
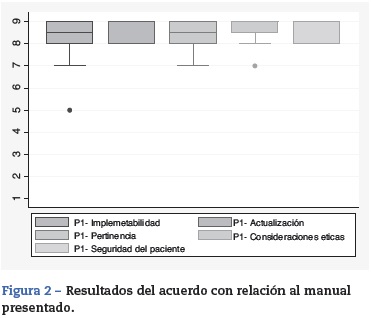
Se utilizó una escala ordinal de 9 categorías para calificar el acuerdo con cada una de las características antes mencionadas (fig. 1). Teniendo en cuenta esto, cada una de las indicaciones propuestas se calificó como recomendada (apropiada), contraindicada (inapropiada) o dentro de un nivel de incertidumbre. Esta calificación se basó en el método Rand (2004), que es citado por Sánchez Pedraza y Jaramillo González8. La figura 2 muestra los resultados del acuerdo por parte de los participantes del consenso.
Preparación y escritura del documento final
Finalmente se estructuró el modelo del documento de protocolo final que incluyera justificación de la realización del documento, metodología utilizada y adaptación del protocolo propuesto y que acogiera las recomendaciones de los expertos sobre el método participativo. El documento final fue desarrollado por el equipo elaborador del protocolo.
La figura 2 muestra los resultados del acuerdo por parte de los participantes del consenso.
Conflicto de intereses
Todos los participantes del grupo elaborador y del consenso de expertos diligenciaron y firmaron el formato de conflicto de intereses de acuerdo con el formato y la recomendación del grupo Cochrane.
Derechos de autor
Se solicitaron los permisos necesarios para la utilización y traducción del contenido de las guías contenidas en esta serie de manuales. La traducción y reproducción parcial se realizó con permiso de Lippincott Williams and Wilkins/Wolters Kluwer Health, Association of Anaesthetists of Great Britain & Ireland & the AAGBI Foundation, Institute of Clinical Systems Improvement.
Contenido clínico
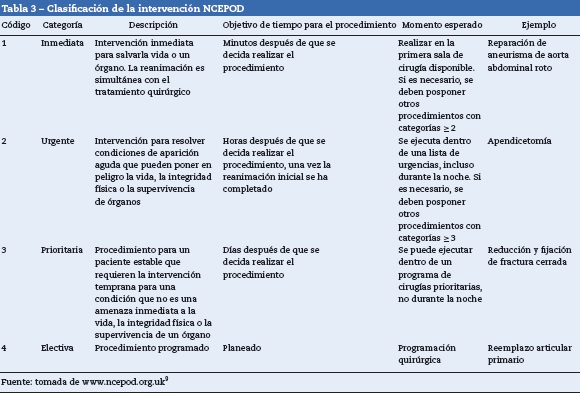
Preparar al paciente para un procedimiento quirúrgico es el resultado de varios subprocesos que habitualmente son ejecutados en serie. Estos subprocesos deben ejecutarse de manera secuencial, pues es un prerrequisito para la ejecución del siguiente subproceso. Sin embargo, se debe ajustar al contexto de cada paciente la aplicación completa y el intervalo de tiempo requerido para cada una de las etapas, especialmente en la categoría de la intervención. En este protocolo se adoptará la clasificación National Confidential Enquiry into Patient Outcome and Death (NCEPOD)9 (tabla 3).
Valoración preanestésica
La historia médica y el examen físico son la mejor estrategia para identificar problemas preoperatorios. El tiempo asignado a la consulta de la valoración preanestésica se puede optimizar mediante el uso de cuestionarios (tabla 4) que no sustituyen la valoración del anestesiólogo sino que facilitan la identificación de puntos importantes y que documentan las respuestas de los pacientes10.
Idealmente, la valoración preanestésica se debe realizar por lo menos una semana antes de un procedimiento quirúrgico programado con el fin de hacer una adecuada educación del paciente. Es importante señalar que este intervalo de tiempo se puede adaptar a las características específicas de cada paciente y al tipo de procedimiento quirúrgico a realizar7.
Los pacientes, familiares o cuidadores deben ser advertidos de que la valoración preanestésica no es un sustituto de los programas de promoción y prevención o detección temprana de enfermedades.
- La valoración preanestésica se debe realizar a todos los pacientes que se someten a procedimientos diagnósticos o terapéuticos, exceptuando pacientes sin enfermedades sistémicas severas que requieran anestesia tópica o local [GRADE C1].
Historia médica y examen físico
La valoración preanestésica debe incluir como mínimo:
Procedimiento programado.
- Motivo del procedimiento quirúrgico.
- Riesgo quirúrgico estimado (tabla 5)11.
Historia médica.
- Antecedentes y complicaciones quirúrgicas.
- Antecedentes y complicaciones anestésicas.
- Alergias e intolerancias a medicamentos y otras sustancias (especificando el tipo de reacción).
- Uso de medicamentos (prescritos, de venta libre, herbales, nutricionales, etc.).
- Antecedentes patológicos.
- Estado nutricional.
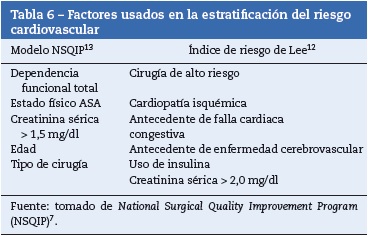
- Estado cardiovascular (tabla 6)12,13.
- Estado pulmonar.
- Clase funcional14-16.
- Estado hemostático (historia personal y familiar de sangrado anormal).
- Posibilidad de anemia sintomática.
- Posibilidad de embarazo (mujeres en edad fértil).
- Historia personal y familiar de complicaciones anestésicas.
- Tabaquismo, consumo de alcohol y otras sustancias.
- Identificación de factores de riesgo para infección del sitio quirúrgico (tabaquismo, diabetes, obesidad, desnutrición, enfermedades crónicas de la piel).
Examen físico.
- Peso, talla e índice de masa corporal.
- Signos vitales: presión arterial, pulso (frecuencia y regularidad), frecuencia respiratoria.
- Cardiaco.
- Pulmonar.
- Probabilidad de vía aérea difícil.
Los modelos de riesgo no deben determinar las decisiones de manejo, pero deben ser considerados como una pieza del rompecabezas y deben ser evaluados en conjunto con la información tradicional con la que cuenta el médico17.
Paraclínicos preoperatorios. El paradigma sobre la solicitud de exámenes paraclínicos ha cambiado en las últimas décadas en todoel mundo18. Los exámenes paraclínicos que no se sustenten en hallazgos de la historia médica o del examen físico no son costo-efectivos, no confieren protección médico-legal y pueden llegar a ser peligrosos para los pacientes19-21. Abarcar las indicaciones respecto a la solicitud de la extensa lista de exámenes paraclínicos disponible en el ejercicio clínico se sale del objetivo de este protocolo.
Para pacientes sometidos a cirugía no cardiaca se recomienda
ajustar la solicitud de paraclínicos de evaluación cardiovascular a alguna de las guías actuales de uso internacional17,22.
Electrocardiograma
Se puede considerar obtener un electrocardiograma preoperatorio a pacientes con 65 año previo al procedimiento quirúrgico [GRADE C2].
El electrocardiograma preoperatorio no se recomienda en pacientes que serán sometidos a otros procedimientos de bajo riesgo, a menos de que en la historia médica o el examen físico se indique que se trata de un paciente de alto riesgo [GRADE A1].
El electrocardiograma no está indicado -sin importar la edad- en pacientes que serán sometidos a cirugía de cataratas. [GRADE A1].
Hemograma
- La obtención de un hemograma preoperatorio se debe hacer con base en los hallazgos de la historia médica y del examen físico de los pacientes y de la pérdida sanguínea potencial del procedimiento programado [GRADE C1].
Electrólitos
- Se recomienda obtener de pacientes con consumo crónico de digoxina, diuréticos, inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina (ARA) [GRADE D2].
Radiografía de tórax
- Se debe obtener una radiografía de tórax (en proyecciones anteroposterior y lateral) en pacientes con signos o síntomas sugestivos de enfermedad cardiopulmonar no diagnosticada o crónica inestable [GRADE D2].
Prueba de embarazo
- Se debe obtener en mujeres en edad fértil y que tengan la posibilidad de estar en embarazo dado por un retraso menstrual, por una sospecha explícita de embarazo por parte de la paciente o por una posibilidad incierta de embarazo (por ejemplo, menstruación irregular) [GRADE C1].
Condiciones médicas
Enfermedades cardiovasculares
En todos los pacientes se debe evaluar la presencia de factores de riesgo para complicaciones cardiovasculares perioperatorias17 [GRADE A1].
La terapia con betabloqueadores se debe continuar en el perioperatorio en paciente que cuente con una historia de uso permanente de este tipo de medicamentos [GRADE A1].
Se debe considerar el inicio de la terapia con betabloqueadores en pacientes con alto riesgo de complicaciones cardiacas (tabla 5) que sean sometidos a cirugía vascular [GRADE C2].
Se debe considerar el inicio de la terapia con betabloqueadores en pacientes con enfermedad coronaria o riesgo cardiaco alto (2 o más factores de riesgo) que sean sometidos a cirugía de riesgo cardiovascular intermedio (tablas 5 y 6) [GRADE C2].
La terapia con betabloqueadores se debe iniciar entre una y 2 semanas antes de la cirugía, y la dosis se debe titular para obtener una frecuencia cardiaca entre 60 y 80 latidos por minuto [GRADE A1].
Los pacientes con uso permanente de estatinas deben continuar con su uso durante el perioperatorio [GRADE 1].
Se debe considerar el inicio de la terapia perioperatoria con estatinas en pacientes sometidos a cirugía vascular o de riesgo intermedio [GRADE C2].
Enfermedades hematológicas y anticoagulación
- Si la historia médica sugiere la posibilidad potencial de problemas de coagulación, se deben obtener pruebas de coagulación [GRADE C1].
Enfermedad coronaria y stent coronarios
La cirugía debe ser evitada por lo menos 6 semanas después de la implantación de un stent metálico [GRADE C1].
La cirugía debe posponerse por lo menos un año después de la implantación de un stent medicado [GRADE C1].
Si la cirugía no puede ser pospuesta durante los periodos de tiempo recomendados, la antiagregación plaquetaria dual debe continuarse en el perioperatorio a menos de que esté contraindicado (cirugía con alto riesgo de sangrado, cirugía intracraneal, etc.) [GRADE C1].
Si se considera necesario suspender clopidogrel / prasugrel / ticlopidina antes de la operación, la aspirina debe continuarse -si es posible- en el periodo perioperatorio para reducir el riesgo cardiaco [GRADE C1].
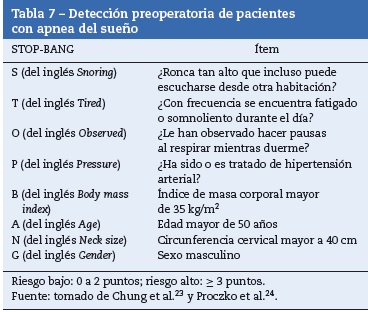
Apnea del sueño
En los pacientes se debe evaluar la posibilidad de apnea del sueño (tabla 7) y comunicar los resultados de la evaluación al equipo quirúrgico [GRADE C1].
Los pacientes con diagnóstico de apnea del sueño que reciban tratamiento con presión positiva continua en la vía aérea (CPAP) deben llevar con ellos el dispositivo para su uso en el postoperatorio inmediato [GRADE B2].
Diabetes mellitus
El control de la glucemia se debe dirigir para lograr concentraciones de glucemia entre 140 y 180 mg/dl y no a rangos más estrictos (por ejemplo, entre 80 y 110 mg/dl) [GRADE A1].
Se debe hacer una evaluación individualizada para generar instrucciones que eviten los cambios extremos de la glucemia [GRADE C1].
La dosis de insulina de acción prolongada (glargina, NPH, etc) se debe disminuir hasta el 50% en el preoperatorio [GRADE C1].
Agentes diabéticos orales e insulinas de acción corta no deben tomarse antes de la operación [GRADE C1].
Los esquemas móviles de insulina durante el perioperatorio se deben usar para tratar la hiperglucemia en pacientes con diabetes mellitus de difícil manejo [GRADE C1].
Los agonistas GLP-1 (exenatide, liraglutide, pramlintide) se deben suspender en el perioperatorio [GRADE C1].
Los inhibidores DPP-4 (sitagliptin) se puede seguir usando en el perioperatorio [GRADE C2].
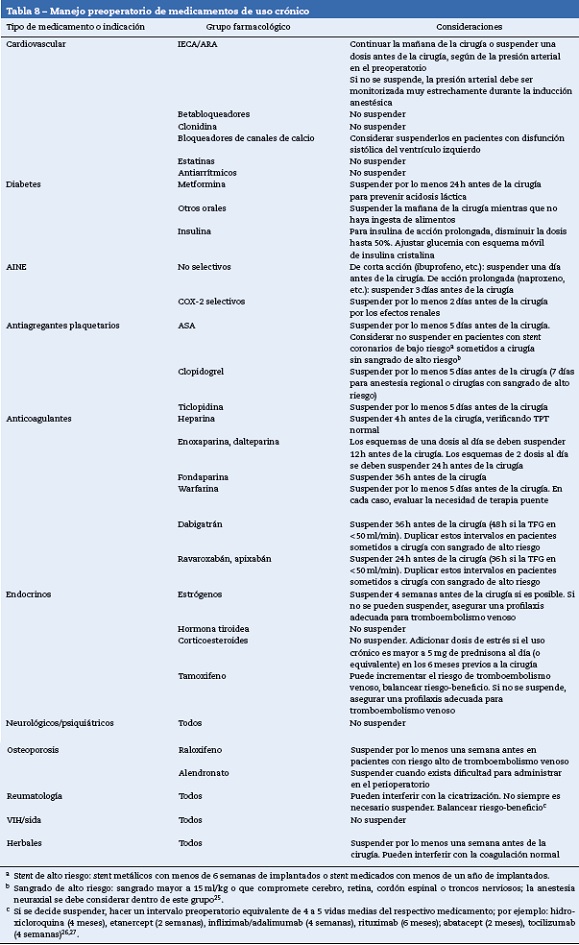
Medicamentos de uso crónico (tabla 8)
Se debe realizar una revisión a fondo de los medicamentos usados por el paciente (medicamentos formulados, no formulados, herbales y suplementos nutricionales) por lo menos una semana antes de una cirugía programada [GRADE C1].
En general, los medicamentos que contribuyan a mantener la homeostasis se deben continuar durante el perioperatorio, excepto los medicamentos que puedan aumentar la probabilidad de eventos adversos (AINE, IECA/ARA, insulina e hipoglucemiantes, anticoagulantes, productos biológicos, medicamentos para la osteoporosis, terapia hormonal, etc.) [GRADE C1].
En general, se deben suspender todos los medicamentos que no contribuyan a mantener la homeostasis de los pacientes (medicamentos no prescritos, herbales o naturistas, suplementos nutricionales, etc.) [GRADE C1].
Suspensión del tabaquismo
- Se debe fomentar en los pacientes suspender el tabaquismo [GRADE C1].
Profilaxis para tromboembolismo (tabla 9)
- Esta se debe obtener en todos los pacientes con una cuantificación del riesgo perioperatorio de tromboembolismo venoso, y dicha cuantificación se debe consignar en la historia clínica. Se recomienda discutir las medidas apropiadas para la prevención de estas complicaciones tromboembólicas con otros miembros del equipo quirúrgico28.
Educación y comunicación con los pacientes
Recomendaciones de ayuno preoperatorio
Las recomendaciones sobre ayuno preoperatorio (nada por vía oral) han sido revisados y simplificados considerablemente en la última década. Se han publicado guías de manejo que establecen la regla «2, 4, 6, 8 horas», y se aplica a pacientes de todas las edades29,30.
Los pacientes deben ser educados e informados de los requisitos de ayuno con suficiente antelación.
Se recomienda que el período de ayuno para líquidos claros, como agua, jugos de fruta sin pulpa, bebidas carbonatadas, té claro y café sea de 2 h o más antes de la cirugía [GRADE B1].
Se recomienda que el período de ayuno para leche materna debe ser de 4 h o más antes de la cirugía [GRADE B1].
Se recomienda que el período de ayuno para leche de fórmula, leche no humana y comidas ligeras (como pan tostado) debe ser de 6 h o más antes de la cirugía [GRADE B1].
El período de ayuno para los alimentos fritos y grasos o carne debe ser de 8 h o más, ya que estos alimentos pueden prolongar el tiempo de vaciamiento gástrico [GRADE B1].
Baño y afeitado preoperatorio
Para el propósito de prevenir infecciones, los pacientes deben ser alentados a bañarse el día del procedimiento quirúrgico. Ellos deben ser alertados de no afeitarse ni eliminar cualquier pelo en o cerca del sitio quirúrgico. Cada centro debe establecer directrices específicas para su población de pacientes y los procedimientos específicos que se realizan (ver Preparación de la piel).
Comunicación con pacientes y cuidadores
Se debe establecer un mecanismo fiable para comunicar el resultado de la valoración preanestésica, incluidos los resultados de las pruebas paraclínicas y las instrucciones para la marcación del sitio quirúrgico, además de la identificación del paciente antes del procedimiento (tabla 10)7.
- En el caso de procedimientos electivos se recomienda entregar a los pacientes o cuidadores material impreso en el que estén las indicaciones más importantes respecto al proceso de preparación para el procedimiento quirúrgico [GRADE D2].
Consentimiento informado
A pesar de los retos únicos que implican obtener el consentimiento informado para procedimientos anestésicos, a los pacientes, padres o cuidadores se les debe proporcionar información respecto a los riesgos anestésicos generales y específicos previstos, y sobre el cuidado anestésico. Se deben adoptar estrategias que permitan mejorar la comprensión de la información con el fin de asegurar que los encargados de tomar las decisiones están adecuadamente informados31,32.
- Se debe obtener consentimiento informado anestésico para todos los pacientes (firmado por ellos mismos, por los padres o cuidadores) que sean sometidos a procedimientos diagnósticos o terapéuticos [GRADE A1].
Traslado del paciente al área quirúrgica (salas de cirugía o quirófanos)
Los pacientes deben ser trasladados al quirófano de acuerdo con su estado clínico. Este traslado implica necesariamente que los pacientes sean cuidados en diferentes áreas de una institución prestadora de servicios de salud y, por tanto, existen procesos de entrega y recepción de pacientes. En la actualidad existe un consenso generalizado de que los procesos de entrega robustos y estructurados son críticos para una atención segura al paciente. Las listas de verificación y herramientas de software para facilitar el proceso de traslado pueden mejorar la fiabilidad y aliviar la presión sobre el personal de salud. Los procesos de traslado y entrega de pacientes se deben adaptar a cada ambiente clínico específico33.
Teniendo en cuenta lo anterior, se pueden definir 2 grupos de pacientes a los que se les debe tener algunas consideraciones específicas:
En pacientes ambulatorios y hospitalizados no críticos:
- Con la finalidad de prevenir lesiones por caídas, los pacientes no se pueden trasladar mediante deambulación. Deben trasladarse en silla de ruedas o en camilla.
- Según las necesidades específicas de cada paciente, se debe disponer de los dispositivos para asegurar un transporte seguro (por ejemplo, oxígeno de transporte, bombas de infusión, etc.).
- Debe participar por lo menos un paramédico en el transporte.
En pacientes críticamente enfermos, además de lo anterior:
- Transportar monitorizado, por lo menos con presión arterial no invasiva, electrocardiografía continua y oximetría de pulso.
- De acuerdo con las indicaciones clínicas, se debe contar con dispositivos para soporte ventilatorio invasivo con la posibilidad de administrar presión positiva al final de la espiración (PEEP).
- El grupo de traslado debe ser liderado por al menos un médico, con la asistencia de personal paramédico.
El traslado de los pacientes al quirófano se debe adaptar al estado clínico del paciente (crítico o no crítico). El proceso de entrega y recepción se debe registrar en la historia clínica [GRADE C1].
Marcación del sitio quirúrgico
Una cirugía incorrecta se puede dar como resultado de desinformación del equipo quirúrgico o mala percepción de la orientación del paciente. La clave para la prevención de este evento es tener múltiples controles independientes de información. Las discrepancias entre la valoración preanestésica, el consentimiento informado y el registro del cirujano de la historia y examen físico deben ser resueltas, idealmente, antes de iniciar cualquier tipo de proceso prequirúrgico34. Antes de marcar el lugar de la cirugía se debe verificar la identidad del paciente y el sitio correcto del procedimiento quirúrgico mediante:
- La información del consentimiento informado.
- La información contenida en la historia clínica.
- Los estudios diagnósticos.
- El interrogatorio al paciente, padre o cuidador [GRADE A1].
Prevención de infección
La infección posoperatoria es una complicación grave. Es la fuente más frecuente de morbilidad hospitalaria para los pacientes sometidos a procedimientos quirúrgicos y está asociada a un aumento de la estancia hospitalaria, mayor riesgo de mortalidad y disminución de la calidad de vida35,36.
Esta puede ocurrir por el procedimiento quirúrgico, y también por los procedimientos anestésicos. Se han descrito varias estrategias que, desde el punto de vista del anestesiólogo, disminuyen el riesgo de infección posoperatoria. Estas incluyen:
Profilaxis antibiótica.
Normotermia perioperatoria.
- Preparación adecuada de la piel, entre otras37-39.
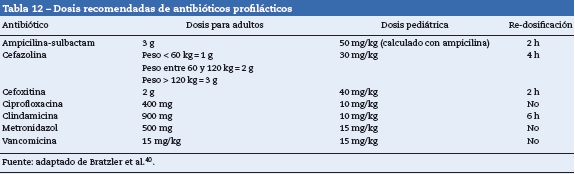
Manejo antibiótico
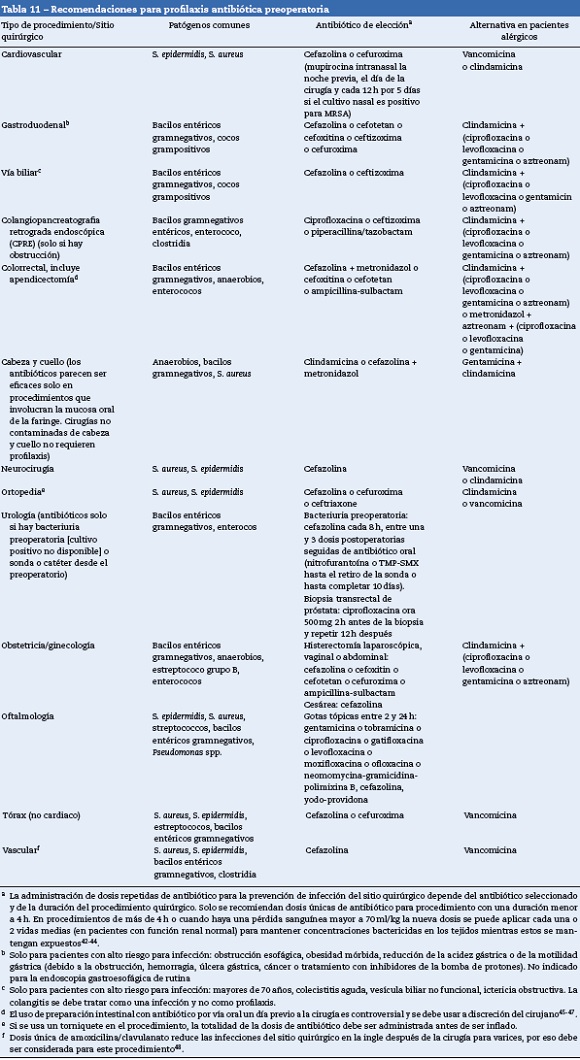
El uso de antibióticos profilácticos preoperatorios ha demostrado disminuir el riesgo de infección postoperatoria del sitio quirúrgico. Se han publicado recomendaciones respecto al tipo de antibióticos (tabla 11) y a las dosis (tabla 12) que se deben usar como profilaxis preoperatoria de acuerdo con el tipo de procedimiento quirúrgico40. Los antibióticos preoperatorios se deben administrar con el fin de obtener concentraciones bactericidas en los tejidos al momento de la incisión. Para la mayoría de antibióticos esta concentración se logra 30 min después de la administración. La vancomicina y las fluoroquinolonas se deben iniciar dentro de los 120 min previos a la cirugía porque requieren un tiempo de infusión más prolongado40. En los casos en los que no se pueda administrar el antibiótico dentro de los intervalos recomendados (por ejemplo, en no acceso este debe aplicar tan pronto se resuelva el impedimento. La administración tardía de la profilaxis antibiótica no disminuye su efectividad41.
Todos los pacientes deben ser evaluados respecto a alergias conocidas a medicamentos [GRADE C1].
Se debe administrar un adecuado antibiótico profiláctico, según la cirugía, entre 30 min y 2 h antes. Este tiempo depende del antibiótico usado [GRADE C1].
Los antibióticos profilácticos, en cirugía no cardiaca, se deben suspender antes de que pasen 24 h de finalizado el procedimiento [GRADE C1].
Los antibióticos profilácticos, en cirugía cardiaca, se deben suspender antes de que pasen 48 h de finalizado el procedimiento [GRADE C1].
Prevención de endocarditis
- Pacientes con diagnóstico de patologías valvulares cardiacas que se sometan a procedimientos quirúrgicos deben recibir profilaxis antibiótica adecuada [GRADE C1].
Procedimientos en pacientes con antecedente de reemplazo articular
- Pacientes con prótesis articulares no deben recibir profilaxis antibiótica para prevenir infección en la prótesis [GRADE C1].
Preparación intestinal en cirugía colorrectal
No se recomienda el uso de preparación intestinal mecánica para disminuir el riesgo postoperatorio de infección del sitio quirúrgico [GRADE A1].
Al momento de la cirugía todos los pacientes deben recibir una dosis profiláctica de antibióticos efectivos contra la flora del colon y la piel [GRADE A1].
Planeación de la normotermia y el manejo de la temperature
La temperatura se debe monitorizar en todos los pacientes que reciben anestesia y que se espera sufran cambios significativos de la temperatura central49,50 SMD. Existen muchos medios y sitios para medir la temperatura central con diferentes niveles de precisión, exactitud y facilidad de uso (oral, timpánico, esofágico, axilar, cutáneo, vesical, rectal, traqueal, nasofaríngeo y mediante un catéter de arteria pulmonar). La elección del sitio depende del acceso y del tipo de cirugía51.
- Se deben establecer estrategias para disminuir el riesgo de hipotermia intraoperatoria con el fin de disminuir complicaciones asociadas (infección del sitio quirúrgico, complicaciones cardiacas, aumento del sangrado, etc.) [GRADE A1].
Preparación de la piel
La mayoría de las infecciones del sitio quirúrgico se producen por la flora normal de la piel. El sitio quirúrgico debe ser evaluado antes de la preparación de la piel.
La piel debe ser evaluada por la presencia de:
Lunares.
Verrugas.
Erupciones.
Otras condiciones de la piel.
La eliminación inadvertida de lesiones puede proporcionar una oportunidad para la colonización de la herida52. Las recomendaciones respecto a la preparación de la piel también se deben aplicar tanto para procedimientos anestésicos como para la inserción de accesos vasculares centrales53.
Aplicación de soluciones antisépticas
Varios agentes antisépticos están disponibles para la preparación preoperatoria de la piel en el sitio de la incisión (tabla 13). Existe evidencia limitada para recomendar el uso de alguna sustancia antiséptica sobre otra para la preparación de la piel54. Se debe hacer una consideración cuidadosa con el fin de elegir la sustancia ideal de acuerdo con cada grupo de pacientes. Algunos agentes antisépticos pueden lesionar las mucosas, y otros son altamente inflamables.
El área preparada debe ser lo suficientemente grande como para permitir la extensión de la incisión o la inserción de drenes. El personal debe tener conocimiento de las técnicas de preparación de la piel, incluyendo el mantenimiento de la integridad de la piel y prevenir la lesión en la piel52.Elproceso de preparación debe contar con algunas consideraciones especiales:
Las áreas con un alto conteo microbiano se deben preparar a lo último.
Aislar las colostomías mediante una gasa impregnada en antiséptico para prepararlas al final del proceso.
Se recomienda el uso de solución salina normal para preparar áreas de piel quemadas o traumatizadas.
Se debe evitar el uso de productos con base en clorhexidina y alcohol en las mucosas.
Permitir suficiente tiempo de contacto para los antisépticos antes de aplicar los campos estériles.
Permitir el tiempo suficiente para la evaporación completa de agentes inflamables.
Prevenir que los antisépticos se acumulen debajo del paciente o los equipos.
La preparación de la piel se debe documentar en la historia clínica del paciente. Las políticas y procedimientos de preparación de la piel deben ser revisados periódicamente para evaluar nueva evidencia.
Eliminación del pelo
El afeitado con una rasuradora puede producir cortes y abrasiones en la piel, y por tanto no debe ser utilizado. El método de recorte utiliza máquinas de cortar con los dientes finos para cortar el pelo cerca de la piel del paciente. Deja el pelo normalmente de un milímetro de longitud. Una recortadora (clipper) normalmente tiene una cabeza desechable o cabezas reutilizables que se desinfectan entre pacientes. Estas máquinas cortadoras no entran en contacto con la piel del paciente, disminuyendo así los cortes y abrasiones. El uso de cremas depilatorias es un método en el que los productos químicos disuelven el pelo. Este es un proceso más lento que dura entre5y20 min. Los depilatorios químicos pueden irritar la piel o provocar reacciones alérgicas. El proceso de eliminación del pelo debe contar con algunas consideraciones especiales:
Se debe evitar la eliminación del pelo a menos de que este pueda interferir con el procedimiento55.
La eliminación del pelo debe ser la excepción, no la regla.
La eliminación del pelo, cuando sea necesario, debe realizarse lo más cerca posible de la hora del procedimiento quirúrgico. No hay evidencia que indique un tiempo específico cuando se abstengan de eliminación del pelo en o cerca del sitio quirúrgico. Afeitar más de 24 h antes del procedimiento aumenta el riesgo de infección56.
La eliminación del pelo en el campo estéril podría contaminar el sitio quirúrgico y los campos estériles debido a los pelos sueltos.
Para algunos procedimientos quirúrgicos, la depilación puede no ser necesaria. Los pacientes que requieren procedimientos inmediatos pueden no tener tiempo para la depilación.
El personal encargado de efectuar la depilación al paciente debe ser instruido para usar la técnica adecuada.
Las políticas y procedimientos deben indicar cuándo y cómo quitar el pelo en el lugar de la incisión. La eliminación del pelo debe ocurrir bajo las órdenes del médico o siguiendo el protocolo de determinados procedimientos quirúrgicos.
Si se realiza la eliminación del pelo, se debe documentar en la historia clínica. La documentación debe incluir la condición de la piel en el sitio quirúrgico, quién ha realizado la eliminación, el método de eliminación, la zona de depilación y el momento en el que se hizo.
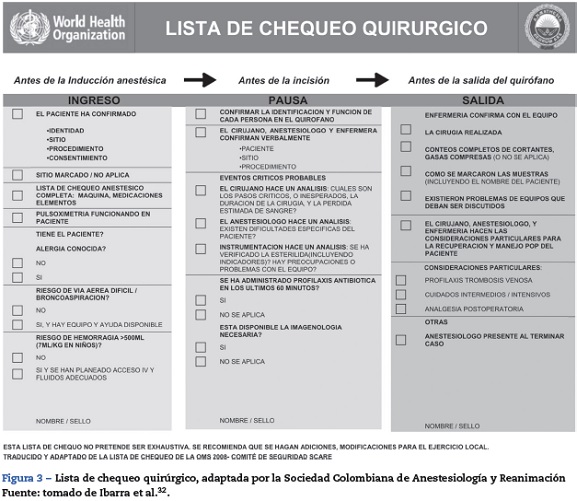
Lista de chequeo preoperatorio
Las listas de chequeo se han convertido en un lugar común en la práctica de la salud, como una estrategia para mejorar la seguridad del paciente. La Organización Mundial de la Salud (OMS) ha implantado una propuesta de lista de chequeo en más de 120 países (fig. 3). Se hace énfasis en el uso de estas listas en los procesos más importantes para la seguridad del paciente:
Anestesia segura y riesgo de vía aérea difícil.
Sitio quirúrgico correcto.
Prevención de infecciones.
Trabajo en equipo.
La intención de una lista de chequeo como una herramienta de seguridad es estandarizar y hacer más predecible el rendimiento del equipo quirúrgico a través de una diversa gama de personas, situaciones y entornos clínicos57. Así, las listas de comprobación se han convertido en sinónimo de la mejor práctica en áreas de alto riesgo, como en anestesiología, y se han adoptado en Colombia como una norma mínima de seguridad en anestesiología32,58.
- En todos los pacientes sometidos a procedimientos quirúrgicos, una vez dentro del quirófano, se debe verificar el cumplimiento de los procesos prequirúrgicos y la disponibilidad del personal y de los dispositivos requeridos mediante la lista de chequeo de la OMS [GRADE A1].
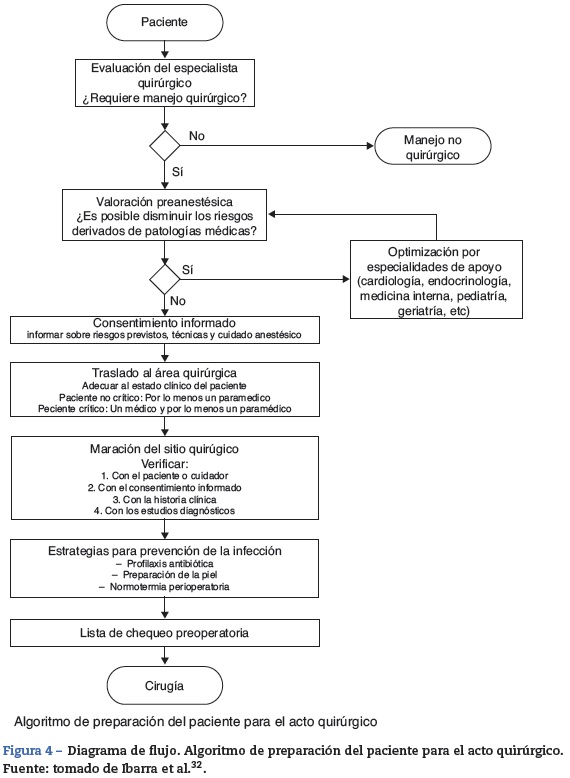
Diagrama de flujo
El diagrama de flujo del protocolo de preparación del paciente para el acto quirúrgico muestra varios subprocesos dispuestos en serie, en los que cada uno se constituye en un prerrequisito para el siguiente subproceso (fig. 4).
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Anexo 1. Búsqueda sistemática de protocolos clínicos para Protocolos Clínicos de Manejo de Anestesia pre, intra y postoperatoria
Se puede consultar material adicional a este artículo en su versión electrónica disponible en http://dx.doi.org/10.1016/j.rca.2014.10.009.
Referencias
1. Smith A, Alderson P. Guidelines in anaesthesia: support or constraint? Br J Anaesth. 2012;109:1-4. [ Links ]
2. Mahajan RP. The WHO surgical checklist. Best Pract Res Clin Anaesthesiol. 2011;25:161-8. [ Links ]
3. Michaels RK, Makary MA, Dahab Y, Frassica FJ, Heitmiller E, Rowen LC, et al. Achieving the National Quality Forum's "Never Events": prevention of wrong site, wrong procedure, and wrong patient operations. Ann Surg. 2007;245:526-32. [ Links ]
4. Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, et al. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182:E839-42. [ Links ]
5. Andrews JC, Schünemann HJ, Oxman AD, Pottie K, Meerpohl JJ, Coello PA, et al. GRADE guidelines: 15 going from evidence to recommendation-determinants of a recommendation's direction and strength. J Clin Epidemiol. 2013;66:726-35. [ Links ]
6. Balshem H, Helfand M, Schünemann HJ, Oxman AD, Kunz R, Brozek J, et al. GRADE guidelines: 3 rating the quality of evidence. J Clin Epidemiol. 2011;64:401-6. [ Links ]
7. Card R, Sawyer M, Degnan B, Harder K, Kemper J, Marshall M, et al. Perioperative protocol. Inst Clin Syst Improv. 2014. [ Links ]
8. Sánchez Pedraza R, Jaramillo González LE. Metodología de calificación y resumen de las opiniones dentro de consensos formales. Rev Colomb Psiquiatr. 2009;38:777-85. [ Links ]
9. National confidential enquiry into patient outcome and death [Internet]. [cited 27.09.14]. Available from: http://www.ncepod.org.uk/. [ Links ]
10. Muckler VC, Vacchiano CA, Sanders EG, Wilson JP, Champagne MT. Focused anesthesia interview resource to improve efficiency and quality. J Perianesth Nurs. 2012;27:376-84. [ Links ]
11. Glance LG, Lustik SJ, Hannan EL Osler TM, Mukamel DB, Qian F, et al. The Surgical Mortality Probability Model: derivation and validation of a simple risk prediction rule for noncardiac surgery. Ann Surg. 2012;255:696-702. [ Links ]
12. Lee TH, Marcantonio ER, Mangione CM, Thomas EJ, Polanczyk CA, Cook EF, et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery. Circulation. 1999;100:1043-9. [ Links ]
13. Gupta PK, Gupta H, Sundaram A, Kaushik M, Fang X, Miller WJ, et al. Development and validation of a risk calculator for prediction of cardiac risk after surgery. Circulation. 2011;124:381-7. [ Links ]
14. Myers J, Do D, Herbert W, Ribisl P, Froelicher VF. A nomogram to predict exercise capacity from a specific activity questionnaire and clinical data. Am J Cardiol. 1994;73:591-6. [ Links ]
15. Myers J, Bader D, Madhavan R, Froelicher V. Validation of a specific activity questionnaire to estimate exercise tolerance in patients referred for exercise testing. Am Heart J. 2001;142:1041-6. [ Links ]
16. Hlatky MA, Boineau RE, Higginbotham MB, Lee KL, Mark DB, Califf RM, et al. A brief self-administered questionnaire to determine functional capacity (the Duke Activity Status Index). Am J Cardiol. 1989;64:651-4. [ Links ]
17. Kristensen SD, Knuuti J, Saraste A, Anker S, B0tker HE, De Hert S, et al. ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management: The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesth. Eur J Anaesthesiol. 2014;35:2383-431. [ Links ]
18. Smetana GW, Macpherson DS. The case against routine preoperative laboratory testing. Med Clin North Am. 2003;87:7-40. [ Links ]
19. Michota FA, Frost SD. The preoperativ evaluation: use the history and physical rather than routine testing. Cleve Clin J Med. 2004;71:63-70. [ Links ]
20. Hepner DL. The role of testing in the preoperative evaluation. Cleve Clin J Med. 2009;76 Suppl. 4:S22-7. [ Links ]
21. Johansson T, Fritsch G, Flamm M, Hansbauer B, Bachofner N, Mann E, et al. Effectiveness of non-cardiac preoperative testing in non-cardiac elective surgery: a systematic review. Br J Anaesth. 2013;110:926-39. [ Links ]
22. Fleisher LA, Fleischmann KE, Auerbach AD, Barnason SA, Beckman JA, Bozkurt B, et al. ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2014, http://dx.doi.org/10.1016/j.jacc.2014.07.944. Aug 1, pii: CIR.0000000000000105, [Epub ahead of print] [ Links ].
23. Chung F, Yegneswaran B, Liao P, Chung SA, Vairavanathan S, Islam S, et al. STOP questionnaire: a tool to screen patients for obstructive sleep apnea. Anesthesiology. 2008;108:812-21. [ Links ]
24. Proczko MA, Stepaniak PS, de Quelerij M, van der Lely FH, Smulders JF, Kaska L, et al. STOP-Bang and the effect on patient outcome and length of hospital stay when patients are not using continuous positive airway pressure. J Anesth. 2014, http://dx.doi.org/10.1007/s00540-014-1848. May 29, [Epub ahead of print] [ Links ].
25. Fenger-Eriksen C, Münster A-M, Grove EL. New oral anticoagulants: clinical indications, monitoring and treatment of acute bleeding complications. Acta Anaesthesiol Scand. 2014;58:651-9. [ Links ]
26. González Naranjo LA, Ramírez Gómez LA. Manejo perioperatorio de la terapia antirreumática. Iatreia. 2011;24:308-19. [ Links ]
27. Polachek A, Caspi D, Elkayam O. The perioperative use of biologic agents in patients with rheumatoid arthritis. Autoimmun Rev. 2012;12:164-8. [ Links ]
28. Pannucci CJ, Laird S, Dimick JB, Campbell DA, Henke PK. A validated risk model to predict 90-da VTE events in postsurgical patients. Chest. 2014;145:567-73. [ Links ]
29. Apfelbaum JL, Caplan RA, Connis RT, Epstein BS, Nickinovich DG, Warner MA. Practice guidelines for preoperative fasting and the use of pharmacologic agents to reduce the risk of pulmonary aspiration: application to healthy patients undergoing elective procedures: an updated report by the American Society of Anesthesiologists Committee on Standards and Practice Parameters. Anesthesiology. 2011;114:495-511. [ Links ]
30. Rincón-Valenzuela DA. Guía de práctica clínica basada en la evidencia para la prevención de aspiración pulmonar en pacientes que requieren manejo de la vía aérea. Rev Colomb Anestesiol. 2011;39:277-8. [ Links ]
31. Tait AR, Teig MK, Voepel-Lewis T. Informed consent for anesthesia: a review of practice and strategies for optimizing the consent process. Can J Anaesth. 2014;61:832-42. [ Links ]
32. Ibarra P, Robledo B, Galindo M, Nino C, Rincón DA. Normas mínimas 2009 For ejercicio de la anestesiología en Colombia. Rev Colomb Anestesiol. 2009;37:235-53. [ Links ]
33. Kalkman CJ. Handover in the perioperative care process. Curr Opin Anaesthesiol. 2010;23:749-53. [ Links ]
34. Clarke JR, Johnston J, Blanco M, Martindell DP. Wrong-site surgery: can we prevent it? Adv Surg. 2008;42:13-31. [ Links ]
35. Anthony T, Murray BW, Sum-Ping JT, Lenkovsky F, Vornik VD, Parker BJ, et al. Evaluating an evidence-based bundle for preventing surgical site infection: a randomized trial. Arch Surg. 2011;146:263-9. [ Links ]
36. Murray BW, Huerta S, Dineen S, Anthony T. Surgical site infection in colorectal surgery: a review of the nonpharmacologic tools of prevention. J Am Coll Surg. 2010;211:812-22. [ Links ]
37. Gifford C, Christelis N, Cheng A. Preventing postoperative infection: the anaesthetist's role. Contin Educ Anaesthesia, Crit Care Pain. 2011;11:151-6. [ Links ]
38. Mauermann WJ, Nemergut EC. The anesthesiologist's role in the prevention of surgical site infections. Anesthesiology. 2006;105:413-21. [ Links ]
39. Forbes SS, McLean RF. Review article: the anesthesiologist's role in the prevention of surgical site infections. Can J Anaesth. 2013;60:176-83. [ Links ]
40. Bratzler DW, Dellinger EP, Olsen KM, Perl TM, Auwaerter PG, Bolon MK, et al. Clinical practice guidelines for antimicrobial prophylaxis in surgery. Am J Health Syst Pharm. 2013;70:195-283. [ Links ]
41. Hawn MT, Richman JS, Vick CC, Deierhoi RJ, Graham LA, Henderson WG, et al. Timing of surgical antibiotic prophylaxis and the risk of surgical site infection. JAMA Surg. 2013;148:649-57. [ Links ]
42. Zanetti G, Giardina R, Platt R. Intraoperative redosing of cefazolin and risk for surgical site infection in cardiac surgery. Emerg Infect Dis. 2001;7:828-31. [ Links ]
43. Bratzler DW, Houck PM, Richards C, Steele L, Dellinger EP, Fry DE, et al. Use of antimicrobial prophylaxis for major surgery: baseline results from the National Surgical Infection Prevention Project. Arch Surg. 2005;140:174-82. [ Links ]
44. Fonseca SNS, Kunzle SRM, Junqueira MJ, Nascimento RT, de Andrade JI, Levin AS. Implementing 1-dose antibiotic prophylaxis for prevention of surgical site infection. Arch Surg. 2006;141:1109-13. [ Links ]
45. Zmora O, Pikarsky AJ, Wexner SD. Bowel preparation for colorectal surgery. Dis Colon Rectum. 2001;44:1537-49. [ Links ]
46. Jimenez JC, Wilson SE. Prophylaxis of infection for elective colorectal surgery. Surg Infect (Larchmt). 2003;4: 273-80. [ Links ]
47. Nichols RL, Choe EU, Weldon CB. Mechanical and antibacterial bowel preparation in colon and rectal surgery. Chemotherapy. 2005;51 Suppl. 1:115-21. [ Links ]
48. Mekako AI, Chetter IC, Coughlin PA, Hatfield J, McCollum PT. Randomized clinical trial of co-amoxiclav versus no antibiotic prophylaxis in varicose vein surgery. Br J Surg. 2010;97: 29-36. [ Links ]
49. Horosz B, Malec-Milewska M. Methods to prevent intraoperative hypothermia. Anaesthesiol Intensive Ther. 2014;46:96-100. [ Links ]
50. Sajid MS, Shakir AJ, Khatri K, Baig MK. The role of perioperative warming in surgery: a systematic review. Sao Paulo Med J. 2009;127:231-7. [ Links ]
51. Sessler DI. Temperature monitoring and perioperative thermoregulation. Anesthesiology. 2008;109:318-38. [ Links ]
52. AORN. Recommended practices for skin preparation of patients. AORN J. 2002;75:184-7. [ Links ]
53. Moureau N, Lamperti M, Kelly LJ, Dawson R, Elbarbary M, van Boxtel a JH, et al. Evidence-based consensus on the insertion of central venous access devices: definition of minimal requirements for training. Br J Anaesth. 2013;110:347-56. [ Links ]
54. Dumville JC, McFarlane E, Edwards P, Lipp A, Holmes A. Preoperative skin antiseptics for preventing surgical wound infections after clean surgery. Cochrane Database Syst Rev. 2013;3:CD003949. [ Links ]
55. Sebastian S. Does preoperative scalp shaving result in fewer postoperative wound infections when compared with no scalp shaving? A systematic review. J Neurosci Nurs. 2012;44:149-56. [ Links ]
56. Mangram AJ, Horan TC, Pearson ML, Silver LC Jarvis WR. Guideline for prevention of surgical site infection, 1999 Centers for Disease Control and Prevention (CDC) Hospital Infection Control Practices Advisory Committee. Am J Infect Control. 1999;27:97-132. [ Links ]
57. Weiser TG, Berry WR. Review article: perioperative checklist methodologies. Can J Anaesth. 2013;60:136-42. [ Links ]
58. Schleppers A, Prien T, Van Aken H. Helsinki Declaration on patient safety in anaesthesiology: putting words into practice - experience in Germany. Best Pract Res Clin Anaesthesiol. 2011;25:291-304. [ Links ]











 texto em
texto em