Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.44 no.2 Bogotá Apr./June 2016
http://dx.doi.org/10.1016/j.rca.2016.01.007
Reporte de caso
Informe de caso: anestesia subdural en la paciente obstétrica
Case report: Subdural anesthesia in the obstetric patient
Carlos Andrés Palacio-Garcíaa,* y Juan Manuel Gómez-Menéndezb
a MD residente de tercer año de anestesiología, Universidad del Valle, Cali Colombia
b MD anestesiólogo, Centro Médico 1MBANACO, Docente Universidad del Valle, Cali Colombia
* Autor para correspondencia. Departamento de Anestesiología. Edificio 112. Hospital Universitario del Valle, piso 4. Campus San Fernando. Calle 5, N.° 36-08. Universidad del Valle. Cali, Colombia.
Correo electrónico: cpalacio65@gmail.com (C.A. Palacio-García).
Historia del artículo: Recibido el 10 de octubre de 2015 Aceptado el 28 de enero de 2016 On-line el 7 de abril de 2016
Resumen
Introducción: La anestesia subdural es una complicación de la anestesia neuroaxial relativamente frecuente pero poco reconocida; tiene un espectro de presentación bastante amplio, que va desde un bloqueo sensitivo inesperadamente alto con poco bloqueo motor hasta un compromiso hemodinámico y respiratorio importante.
Presentación del caso: Mujer de 22 años a la que se realiza cesárea con anestesia epidural, con evidencia de bloqueo sensitivo más alto de lo esperado, de larga duración y con dificultad respiratoria.
Conclusión: La anestesia neuroaxial es un conjunto de técnicas versátiles y seguras, aunque no exentas de complicaciones, como lo es la anestesia subdural. En la práctica clínica debemos estar atentos a esta posibilidad, y conocer los factores de riesgo y los criterios diagnósticos.
Palabras clave: Espacio subdural, Anestesia epidural, Cesárea, Bloqueo nervioso autónomo, Factores de riesgo.
Abstract
Introduction: Subdural anesthesia is a relatively frequent complication though seldom recognized. It has a broad spectrum of presentations ranging from an unexpectedly high sensory block with limited motor block, to substantial hemodynamic and respiratory involvement.
Case presentation: A 22-year old woman undergoing cesarean section under epidural anesthesia with evidence of long-lasting higher than expected sensory block and respiratory distress.
Conclusion: Neuraxial anesthesia comprises a number of versatile and safe techniques, though not exempt from complications including subdural anesthesia. We should be aware of this possibility in our clinical practice, and know the risk factors and the diagnostic criteria.
Keywords: Subdural space, Anesthesia epidural, Cesarean section, Autonomic nerve block, Risk factors.
Introducción
La anestesia subdural es una complicación de la anestesia neuroaxial relativamente frecuente pero poco reconocida1, con un espectro de presentación y de gravedad variable. Se estima de manera global, según trabajos de Lubenow, una incidencia de 0,87%2 para la población general; para las pacientes obstétricas sometidas a anestesia epidural es de 0,024%3. Sin embargo, en estudios que usan medio de contraste, se ha encontrado que puede llegar a valores tan altos como 7-11%1,4-6. En el presente caso se ilustra la manera inusual como puede presentarse, los factores de riesgo y las medidas preventivas que se pueden realizar.
Clásicamente se ha descrito el espacio subdural como un espacio virtual ocupado por líquido seroso, localizado entre la duramadre y la aracnoides. En concordancia con esta denominación anatómica, estaría constituido de manera similar a otras cavidades serosas como el pericardio o las pleuras; es decir, 2 láminas en contacto, con una serosidad que favorece el roce, sin ningún tipo de unión intercelular entre ellas. Sin embargo, estudios recientes en cadáveres y por microscopia electrónica demuestran que este espacio no existe como tal, y que su presencia se debe a factores patológicos o iatrogénicos7-10.
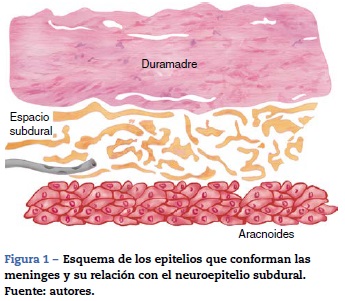
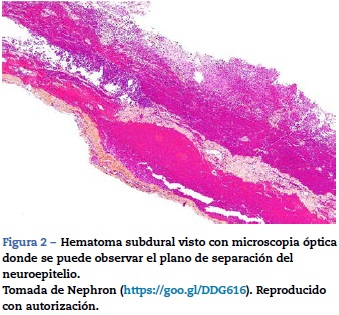
Desde el punto de vista histológico, el «espacio subdural» está constituido por un neuroepitelio compuesto de células alargadas, fusiformes y ramificadas con uniones intercelulares laxas, rodeado por escasas fibras colágeno y algunos vasos sanguíneos, lo cual le confiere una baja resistencia mecánica11,12 (figs. 1 y 2). Está localizado entre la porción más interna de la duramadre, un tejido de gran resistencia formado por 80 capas principalmente compuestas por fibras colágeno que forman una red con orientación en múltiples direcciones, y la lámina aracnoidea, que está formada por varios planos celulares unidos entre sí por uniones intercelulares estrechas, especializadas, tipo desmosoma, que la convierten en la principal barrera al paso de sustancias12. El neuroepitelio subdural tiene una orientación concéntrica alrededor del saco dural y, a diferencia del espacio epidural, no está limitado por el agujero magno. Dentro de las meninges, este es el tejido de menor resistencia, y cuando se rompe se origina un espacio patológico cuya orientación, forma y tamaño estará en función de la fuerza que lo genera. Esto es determinante en cuanto a la dirección y el patrón de distribución que pueden tomar las sustancias allí aplicadas, y en el caso de los anestésicos locales, es lo que explica la gran variabilidad en la presentación clínica2,5,6. Finalmente, la presentación clínica del bloqueo anestésico estará dada por las estructuras meníngeas atravesadas. Si no se atraviesa la duramadre, las características serán las de una anestesia epidural; si hay disrupción de la duramadre, pero se preserva la aracnoides, la presentación clínica será la de una anestesia subdural. Por último, si se atraviesa la aracnoides y se deposita el anestésico en el espacio subaracnoideo (intratecal), la anestesia será espinal o subaracnoidea13,14.
Reporte de caso
Se trata de una paciente de 22 años, primigestante de 39 semanas, 80 kg de peso, previamente sana, programada para cesárea por podálica, antecedentes negativos, signos vitales: presión arterial: 110/70, frecuencia cardiaca: 80/min, frecuencia respiratoria: 18/min, temperatura corporal: 37 °C, saturación arterial de oxígeno: 99.
Se decidió aplicar anestesia epidural, y previo consentimiento informado escrito y monitorización no invasiva, siguiendo estricta técnica aséptica, se puncionó en L3-L4 con aguja Tuohy 18 G, un intento, y mediante la técnica de pérdida de la resistencia con aire se ubicó el espacio epidural, y se dejó el catéter 3 cm dentro de este.
Dosis de prueba con 3 cc de lidocaína al 2% +100 mcg de fentanilo; no hubo signos de aplicación intratecal o intravenosa.
Se completó el volumen de anestésico con 7 cc de lido caína al 2% y 10 cc de bupivacaína al 0,5%, obteniendo un nivel sensitivo T6, y se dio inicio a la intervención quirúrgica sin incidentes.
A los 12min nació neonato masculino con un Apgar 9-10.
Tras 20 min de intervención la paciente presentó parestesias en los miembros superiores y dificultad respiratoria, y se tornó ansiosa; en ese momento la monitoria mostraba los siguientes signos vitales: PA 90/60 mmHg; P 54/min, SaO2 94.
Se evidenció bloqueo sensitivo con compromiso hasta miembros superiores nivel C5, sin bloqueo motor. Se manejó con bolo de lactato de Ringer 1.000 cc y aumento de la FiO2; posteriormente, no hubo mayores complicaciones. A la paciente se le pudo terminar el procedimiento, sin mayor deterioro, no se suministraron dosis adicionales de anestésico por el catéter epidural y este fue retirado al terminar la cirugía. El bloqueo sensitivo fue de 6 h de duración.
Discusión
Respecto a los mecanismos que producen una anestesia sub-dural, se pueden dar distintos escenarios:
La aguja espinal o epidural puede perforar la duramadre y la aracnoides, y el orificio de esta, quedar ubicado entre los 2 espacios; en este contexto debemos tener en cuenta la diferencia de presiones, que es subatmosférica en el tejido subdural y positiva en el líquido cefalorraquídeo, lo que va a dar lugar a una aspiración de líquido cefalorraquídeo positiva, pero la inyección del anestésico va a tomar el camino de menor resistencia, es decir, al espacio subdural; este mecanismo explica anestesias subaracnoideas fallidas8.
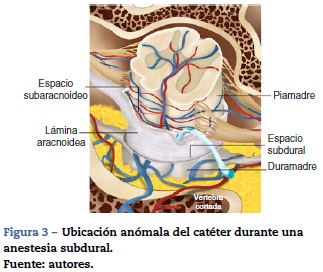
La aguja espinal o epidural puede perforar la dura sin comprometer la aracnoides; en este caso, la aspiración de líquido cefalorraquídeo será negativa y la prueba de pérdida de resistencia con aire o agua será positiva y se podrá ubicar fácilmente un catéter en este tejido (fig. 3). Este mecanismo explica el cuadro de anestesia subdural8.
Hay otros mecanismos menos comunes, como es el caso de los catéteres multiorificio, cuyo extremo distal puede quedar ubicado subdural y los orificios proximales en el espacio epidural; esto da lugar a una presentación normal con infusiones de baja velocidad, en las cuales se ha demostrado que la perfusión se da a través de los extremos proximales, pero si se suministra un bolo aparecerá el cuadro clínico de anestesia subdural15. Otro mecanismo es la migración del catéter8,15.
Se han encontrado ciertos factores que se asocian a anestesia subdural; todos tienen en común el daño físico a la duramadre, estos son:
Posterior a punción lumbar, inyección subdural previa, procedimiento difícil, rotación de la aguja epidural, antecedente de cirugía de columna, intentos repetidos en el mismo espacio y no hay relación con el nivel de experiencia5,6,8.
El cuadro clínico es bastante variable y va desde una presentación normal de anestesia epidural, pasando por bloqueos unilaterales, en parches o comprometiendo algunos dermato mas, hasta un bloqueo sensitivo muy alto en relación con un bloqueo motor mínimo o inexistente1,2,14,16.
La heterogeneidad del cuadro se explica por las características previamente descritas. El predominio sensitivo sobre el motor ocurre porque dado que el espacio es creado y el acceso es posterior habrá cierta selectividad sobre las raíces dorsales y a esto se le suma el hecho de que la duramadre y la aracnoides tienden a estar fusionadas en la raíz anterior, lo que limita la difusión a este nivel11,12. Además, según el volumen y la presión aplicados se pueden explicar la aparición de bloqueos extensos o los bloqueos en parches o unilaterales, según el plano de disección que tome el líquido inyectado en el «espacio subdural»11,12.
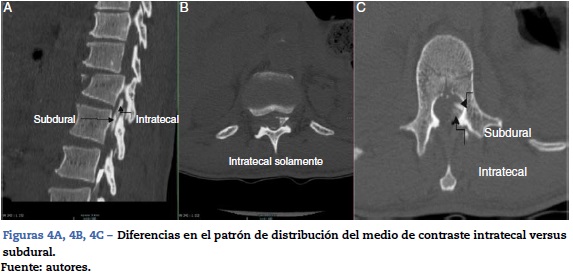
El diagnóstico de certeza se realiza mediante la inyección de 6 cc de medio de contraste y la obtención de radiografías AP y lateral, o mediante fluoroscopia o tomografía, obteniendo un patrón característico de distribución subdural1,4 (figs. 4 A, 4B, 4C).
Hay ciertos signos o síntomas que permiten sospechar la localización subdural del catéter o aguja, que son: la ausencia de pérdida clara de la resistencia, cefalea frontal o dolor tras la aplicación. Ante cualquiera de estos, lo que se recomienda es confirmar la posición radiológicamente, cambiar de espacio o, como último recurso, si no es factible lo anterior, abandonar la técnica5,6.
En cuanto a la dosis de prueba que clásicamente se ha usado, esta no tiene utilidad para la detección de la anestesia subdural8,9,17,18, pero se ha planteado la conveniencia del uso del neuroestimulador, en donde con una intensidad menor a 1 mA, si se está en el espacio subdural se obtendrá una respuesta difusa comprometiendo múltiples dermatomas, y si se está en el espacio epidural, con estímulos entre 1 y 10 mA se obtendrán respuestas correspondientes al dermatoma donde se encuentra la aguja16,19.
Recientemente, Hoftman y Ferrante1 han desarrollado unos criterios diagnósticos para anestesia subdural sin ima ginología, en los cuales plantean como criterios mayores, en el caso de la técnica epidural, la salida de líquido cefalorraquídeo negativa asociada a la sensación táctil por pérdida de resistencia, y plantean 2 escenarios: bloqueo excesivo o restringido; para cada uno de estos proponen los siguientes criterios menores, entre los cuales solo uno basta para hacer el diagnóstico:
- En el caso de bloqueo excesivo (sensibilidad 93%) son un inicio mayor de 20 min, estabilidad cardiovascular, compromiso sensitivo con motor mínimo o ausente, diseminación en parches o asimétrica, falla respiratoria y anestesia de cabeza o cara.
- En el caso de bloqueo restringido (sensibilidad 100%) son un inicio mayor de 20 min y compromiso sensitivo con motor mínimo o ausente.
En el caso de la técnica subaracnoidea, Hoftman y Ferrante1 plantean que ante la sensación táctil de punción subaracnoi dea y la salida de líquido cefalorraquídeo como criterio mayor, con solo uno de los siguientes criterios se hace el diagnóstico: excesivo (no se reportaron casos), restringido (sensibilidad 100%), inicio mayor de 20 min, compromiso sensitivo con motor mínimo o ausente y bloqueo fallido.
No hay muertes reportadas por bloqueo subdural. El manejo es de soporte, controlando la bradicardia con atropina, la hipotensión con bolos de cristaloides o coloides, posición en Trendelenburg y vasopresores si se requieren. Puede ser necesario el soporte ventilatorio, y a pesar de que algunos catéteres subdurales pueden tener un comportamiento normal, dada su naturaleza impredecible se recomienda retirarlos5.
Aunque no se encontraron en la paciente síntomas como cefalea o dolor tras el avance del catéter, ni fue reportada como «poco clara» la pérdida de la resistencia durante la identificación del espacio epidural, son todos estos signos y síntomas muy sutiles; por otro lado, se debe procurar que la identificación del espacio epidural sea con solución salina en lugar de aire, ya que esta técnica de identificación del espacio se ha asociado con menos cefalea pospunción y menor número de intentos según un metaanálisis reciente20, y debemos recordar que el número de intentos y la cefalea pospunción están relacionados con lesión de las meninges, que a su vez es un evento fundamental en la anestesia subdural11,12.
Conclusión
Aunque el diagnóstico de bloqueo subdural se confirma radiológicamente con los criterios previamente mencionados, hay evidencia de que se puede tener una buena sensibilidad para su diagnóstico con base en criterios clínicos; en nuestro caso, según los criterios de Hoftman y Ferrante teníamos una sensibilidad del 93%. No se presentó ningún incidente durante la inserción del catéter que nos alertara sobre la ubicación subdural. Sin embargo, se debe estar alerta a estos signos y síntomas y, ante la duda, proceder a la comprobación radiológica, al uso del neuroestimulador, al cambio de espacio intervertebral, o de técnica anestésica o analgésica si ninguna de las anteriores está disponible.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Financiamiento
Los autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
Al Dr. Fabián Valdés, residente de radiodiagnóstico en el Hospital Universitario del Valle Evaristo García.
A Stéphany Santanilla Arana, diseñadora gráfica, por la elaboración de las ilustraciones.
Referencias
1. Hoftman NN, Ferrante FM. Diagnosis of unintentional subdural anesthesia/analgesia: analyzing radiographically proven cases to define the clinical entity and to develop a diagnostic algorithm. Reg Anesth Pain Med. 2009;34:12-6. [ Links ]
2. Lubenow T, Keh-Wong E, Kristof K, Ivankovich O, Ivankovich AD. Inadvertent subdural injection: a complication of an epidural block. Anesth Analg. 1988;67:175-9. [ Links ]
3. Jenkins JG. Some immediate serious complications of obstetric epidural analgesia and anaesthesia: a prospective study of 145,550 epidurals. Int J Obstet Anesth. 2005;14:37-42. [ Links ]
4. Mehta M, Salmon N. Extradural block. Confirmation of the injection site by X-ray monitoring. Anaesthesia. 1985;40:1009-12. [ Links ]
5. Hoftman N. Unintentional subdural injection: a complication of neuraxial anesthesia/analgesia. Anesthesiol Clin. 2011;29:279-90. [ Links ]
6. Agarwal D, Mohta M, Tyagi A, Sethi AK. Subdural block and the anaesthetist. Anaesth Intensive Care. 2010;38:20-6. [ Links ]
7. Haines DE. On the question of a subdural space. Anat Rec. 1991;230:3-21. [ Links ]
8. Fettes PDW, Jansson J-R, Wildsmith JAW. Failed spinal anaesthesia: mechanisms, management, and prevention. Br J Anaesth. 2009;102:739-48. [ Links ]
9. Reina MA, De Leon Casasola O, López A, De Andrés JA, Mora M, Fernández A. The origin of the spinal subdural space: ultrastructure findings. Anesth Analg. 2002;94:991-5. [ Links ]
10. Haines DE, Harkey HL, al-Mefty O. The "subdural" space: a new look at an outdated concept. Neurosurgery. 1993;32:111-20. [ Links ]
11. Reina MA, Collier CB, Prats-Galino A, Puigdellívol-Sánchez A, Machés F, De Andrés JA. Unintentional subdural placement of epidural catheters during attempted epidural anesthesia. Reg Anesth Pain Med. 2011;36:537-41. [ Links ]
12. Reina MA, Pulido DP. El saco dural humano. Origen del espacio subdural espinal. Rev Argentina Anestesiol. 2007;65:167-84. [ Links ]
13. Hogan QH, Mark L. Subdural injection. Reg Anesth Pain Med [Internet]. 2009;34:10-1. [ Links ]
14. Singh B, Sharma P. Subdural block complicating spinal anesthesia? Anesth Analg. 2002;94:1007-9. [ Links ]
15. Toledano RD, Tsen LC. Epidural catheter design. Anesthesiology. 2014;121:9-17. [ Links ]
16. Tsui BC, Gupta S, Emery D, Finucane B. Detection of subdural placement of epidural catheter using nerve stimulation. Can J Anaesth. 2000;47:471-3. [ Links ]
17. Camorcia M. Testing the epidural catheter. Curr Opin Anaesthesiol. 2009;22:336-40. [ Links ]
18. Galindo Gualdrón LA. Dosis de prueba para anestesia regional. Rev Colomb Anestesiol. 2014;42:47-52. [ Links ]
19. Moore AR, Siddiqui N, Kassel EE, Carvalho JCA. Unintentional subdural catheter placement during labor analgesia shows typical radiological pattern but atypical response to the Tsui test. Int J Obstet Anesth. 2010;19:111-4. [ Links ]
20. Schier R, Guerra D, Aguilar J, Pratt GF, Hernandez M, Boddu K, et al. Epidural space identification: a meta-analysis of complications after air versus liquid as the medium for loss of resistance. Anesth Analg. 2009;109:2012-21. [ Links ]











 text in
text in