Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Colombian Journal of Anestesiology
versión impresa ISSN 0120-3347
Rev. colomb. anestesiol. vol.45 no.1 Bogotá ene./jun. 2017
http://dx.doi.org/10.1016/j.rca.2016.09.004
Eventos adversos en pacientes pediátricos sometidos a resonancia magnética bajo sedación o anestesia
Adverse events in pediatrics patients subject to magnetic resonance imaging under sedation or anaesthesia
Carlos Eriel Largo-Pineda*, Iván Darío Arenas-Correa, Gabriel Jaime Ángel-González, Jorge Mario Vélez-Arango, Victor Daniel Calvo-Betancur y Andrés Nahúm Arango-Zapata
* Instituto de Alta Tecnología Médica (IATM), Medellín, Colombia
** Autor para correspondencia. Instituto de Alta Tecnología Médica (IATM). Carrera 81 No. 30A-99, Medellín, Colombia.
Correo electrónico: cegopimed@gmail.com (C.E. Largo-Pineda).
Historia del artículo:
Recibido el 25 de enero de 2016 Aceptado el 1 de septiembre de 2016 On-line el 8 de diciembre de 2016
Resumen
Introducción: La resonancia magnética es una técnica en la que se requieren apneas o periodos de inmovilidad considerables para la adquisición de imágenes. Inmovilidad que por condiciones de los pacientes pediátricos es difícil mantener, requiriendo administración de sedación o anestesia, lo que genera riesgos adicionales a los existentes en otras áreas. Objetivo: Describir la incidencia de eventos adversos en pacientes pediátricos en el servicio de resonancia magnética bajo asistencia por anestesiólogo.
Materiales y métodos: Estudio observacional descriptivo donde se valoró la incidencia de eventos adversos en 4.786 pacientes menores de 15 arios que fueron llevados a resonancia bajo asistencia por anestesiólogo para sedación o anestesia en el Instituto de Alta Tecnología Médica entre los años 2010-2014.
Resultados: Se presentaron 12 eventos adversos, con un índice de 2,5 por cada 1.000 pacientes pediátricos, de los cuales 6 eventos adversos fueron graves, 4 moderadosy2leves. La proporción de mortalidad fue del 0,04%.
Conclusión: Realizar estudios de resonancia magnética bajo sedación o anestesia por anestesiólogo en pacientes menores de 15 años es seguro. Sin embargo, en pacientes hospitalizados o descompensados debe hacerse un análisis riesgo-beneficio y valorar la mejor opción.
Palabras clave: Anestesia, Sedación, Pediatría, Imagen por resonancia magnética, Niño.
Abstract
Introduction: Nuclear magnetic resonance is a technique requiring breath holding or staying still for long periods of time for image acquisition. For this reason, paediatric patients need to be given sedation or anaesthesia, creating additional risks to those found in other areas.
Objective: To describe the incidence of adverse events in paediatric patients in the magnetic resonance service with the presence of an anaesthetist.
Materials and methods: Descriptive observational study to assess the incidence of adverse events in 4786 patients under 15 years of age taken to magnetic resonance imaging with an attending anaesthetist for sedation or anaesthesia at Instituto de Alta Tecnología Médica between 2010 and 2014.
Results:There were 12 adverse events with a rate of 2.5 for every 1000 paediatric patients. Of these, there were 6 serious, 4 moderate and 2 mild adverse events. The proportion of mortality was 0.04%.
Conclusion: Performing magnetic resonance imaging studies under sedation or anaesthesia given by an anaesthetist in patients under 15 years of age is safe. However a risk-benefit analysis is required in hospitalized or decompensated patients, in order to assess the best option.
Keywords: Anesthesia, Sedation, Pediatrics, Magnetic resonance imaging, Child.
Introducción
La resonancia magnética (RM) es una técnica diagnóstica en continuo desarrollo con la que se busca obtener estudios de mayor calidad, diagnóstico de patologías más complejas y en periodos de tiempo más cortos1,2. A pesar de estos avances, aún se requieren periodos de inmovilidad relativamente prolongados, inclusive en algunos estudios de cortos periodos de apnea, para la adquisición de las imágenes3. Inmovilidad que en pacientes menores de 15 años es infrecuente, haciendo necesario administrar sedación y ocasionalmente anestesia para alcanzar las condiciones requeridas3.
La sedación en RM conlleva riesgos adicionales a los existentes en otros sitios1,4. Riesgos derivados del potente campo electromagnético, ondas electromagnéticas de alta frecuencia, alto nivel de ruido, baja luminosidad, entre otros1.El campo electromagnético es la condición que más restricciones impone, dado que contraindica la utilización de muchos de los dispositivos de uso habitual en anestesia, ante el riesgo de que por sus características ferromagnéticas se conviertan en proyectiles al interior del resonador1,5. Este hecho obliga a instaurar medidas de seguridad para disminuir la incidencia de eventos adversos en el área de resonancia1.
La literatura mundial1,5,6 describe como medidas de seguridad para disminuir la incidencia de eventos adversos las siguientes consideraciones:
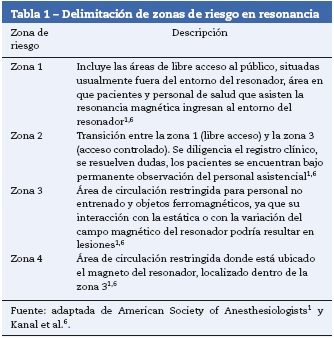
Zonas de riesgo: el área de resonancia está delimitada por zonas de riesgo (tabla 1).
En pacientes menores de 15 años o de alto riesgo la sedación (moderada o profunda) y la anestesia la realiza el médico especialista en anestesiología1.
Los equipos que ingresan a la zona 4 deben ser avalados por el fabricante antes de poder ser utilizados allí, incluyendo la máquina de anestesia y todos los dispositivos de vía aérea1. Debe contarse con área de reanimación en la zona 2, equipada con los dispositivos para reanimación cardiovascular básica y avanzada1.
Es así como en la búsqueda de mejorar continuamente la seguridad y la eficiencia de las medidas implantadas en la Fundación Instituto de Alta Tecnología Médica (IATM), ubicada en Medellín, Colombia, en la institución se realizó un estudio que describió la incidencia de eventos adversos en los últimos 5años en menores de 15 años sometidos a RM bajo sedación o anestesia guiada por anestesiólogo.
Materiales y métodos
Selección de pacientes para sedación o anestesia
Se llevó a cabo un estudio observacional descriptivo de carácter retrospectivo en pacientes menores de 15 años a quienes se les realizó RM (equipos de 1,5 y 3,0 teslas) bajo sedación o anestesia administrada por médico especialista en anestesiología, en el periodo comprendido entre el año 2010-2014 en el IATM.
Los pacientes se clasificaron de acuerdo a grupos de edad mutuamente excluyentes7; neonato (1-30 días), lactante menor (más de 1 mes-menos de 1año), lactante mayor (1-2años), preescolar (3-4 años), escolar (5-10 años) y adolescente (11-14 años).
Registro y verificación de información
La información fue tomada del registro clínico diligenciado por enfermería y del registro del médico anestesiólogo. El registro de enfermería incluye identificación, consentimiento informado para ingresar al resonador, interrogatorio del paciente (antecedentes, resumen de historia clínica y orden del médico tratante) y datos antropométricos. La información fue verificada por el médico radiólogo.
El registro de anestesia diligenciado por el médico anestesiólogo incluye la identificación del paciente, fecha, clasificación de riesgo anestésico (clasificación ASA)8, antecedentes personales y examen físico. Durante el acto anestésico se realizó monitorización ASA básica (o avanzada, de acuerdo a la condición clínica) y se dejó registro de las variables (presión arterial, oximetría, frecuencia cardiaca y capnografía) en formato físico, donde se incluyen también la hora y la dosificación de los medicamentos, los cuales fueron administrados en dosis terapéuticas recomendadas por la literatura9.
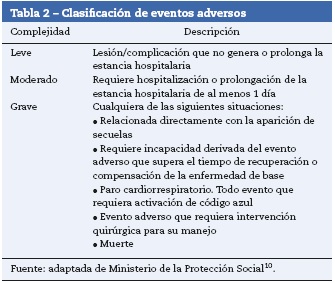
Una vez se obtuvo la información, se describió la población estudiada, identificando los eventos adversos, clasificándolos de acuerdo a la complejidad del desenlace (leve, moderado o grave), y además fueron caracterizados por sexo, edad, tipo de estudio realizado, duración del procedimiento y nivel de ASA. El presente estudio incluyó todos los desenlaces adversos de origen alérgico y los desenlaces moderados a graves de origen no alérgico (tabla 2).
Luego del evento adverso, a todos los pacientes se les hizo seguimiento por vía telefónica a las 48 h a través de sus familiares (padres o acompañantes) o con personal de enfermería en pacientes hospitalizados.
Plan de análisis
Para el análisis descriptivo se utilizaron distribuciones absolutas y porcentuales. De igual manera se usó el indicador de índice de eventos adversos, donde el numerador corresponde al número de casos de eventos adversos en el periodo y el denominador al número de pacientes pediátricos, multiplicado por una constante de 1000.
Consideraciones éticas
Previa revisión, aprobación y autorización del Comité de Ética en Investigación del IATM, la información del registro clínico se recopiló del Sistema de Información Radiológico (RIS) institucional. Acorde con la Declaración de Helsinki, el Informe Belmont y la resolución colombiana 8430 de 1993, esta investigación se clasificó sin riesgos, por lo cual el consentimiento informado no fue obtenido previo a la inclusión de los pacientes en ella.
Resultados
Aspectos generales
Se identificaron 4.786 pacientes menores de 15 años a quienes se les realizaron estudios de RM que requirieron asistencia de un médico anestesiólogo para sedación profunda o anestesia general, durante el periodo 2010-2014.
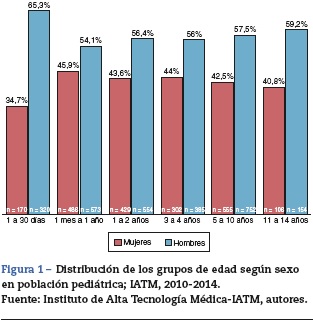
El 57,2% de los pacientes fueron hombres. Los grupos de edad según el sexo se pueden ver en la figura 1.
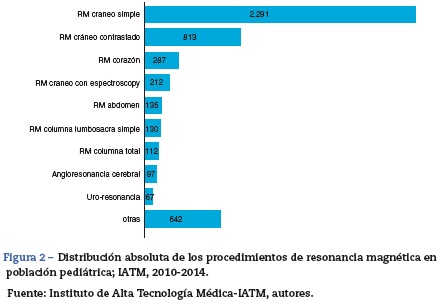
Los estudios realizados con más frecuencia fueron: RM de cráneo simple (47%; n = 2.291), RM de cráneo con medio de contraste (16%; n = 813) y RM de corazón (6%; n = 287) (fig. 2).
Eventos adversos
En este estudio, en un periodo de 5 años se identificaron 12 eventos adversos (0,25%), de los cuales 6 fueron graves (0,12%), 4 moderados (0,08%)y2 leves(0,04%).
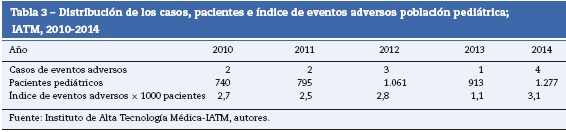
La distribución absoluta de los casos y el índice de eventos adversos se puede ver en la tabla 3.
Se presentaron 6 eventos adversos graves. Los pacientes con presencia de paro cardiorrespiratorio recibieron todas las medidas de reanimación cardiopulmonar básica y avanzada, siendo exitosas y retornando la circulación en 4 pacientes y no exitosas en 2 pacientes (fallecieron). Los eventos adversos graves se clasificaron como ASA II (n = 1), ASA III (n = 4) y ASA IV (n=1).
Los 4 eventos adversos graves que presentaron paro cardiorrespiratorio y que recuperaron circulación y respiración espontánea por medio de reanimación cardiopulmonar previamente habían sido clasificados como ASA II (n = 1) y ASA III (n = 3). Dos de estos eventos se presentaron en neonatos con diagnóstico de síndrome dismó un tercer evento ocurrió en una RM de cráneo (8 meses de edad) por encefalopatía hipóxica y el último evento (36 meses de edad) se presentó en un estudio para cardiomiopatía dilatada.
Respecto a los eventos adversos moderados, se hallaron 3 eventos de laringoespasmo; el primer evento fue en una paciente de 8 años clasificada como ASA II durante la RM de cráneo, el segundo evento fue en paciente de 7 meses, ASAIII durante angiorresonancia de cráneo, y el tercer evento se presentó en paciente de 2 años, ASA II durante la RM de corazón. El último evento moderado fue una extubación accidental, sin repercusión en el estado basal del paciente (este fue el único evento clasificado como prevenible) (tabla 4).
Se evidenció el registro de 2 eventos alérgicos leves por rash cutáneo que no requirieron hospitalización ni escalamiento en la terapia. Uno de estos eventos fue durante una RM de cráneo simple clasificado ASA II, quien recibió hidrato de cloral; al otro evento de rash clasificado ASA I se le realizó RM de cráneo contrastada y se le administraron lidocaína, midazolam, ketaminay propofol; ambos episodios se presentaron una vez dejaron las instalaciones de la institución, y estos pacientes solicitaron indicaciones por vía telefónica. En seguimiento a las 48 h se reportaron asintomáticos, sin requerir manejo hospitalario.
En los casos de eventos adversos se utilizaron medicamentos de uso frecuente en anestesia, incluyendo lidocaína, midazolam, ketamina, propofol, fentanilo e hidrato cloral.
Discusión
El rendimiento diagnóstico de la RM depende en gran parte de rfico, la calidad de imagen generada, requiriendo periodos prolongados libres de movimiento por parte del paciente, condición que en la mayoría de la población pediátrica no es posible dada la necesidad del uso de medicamentos a dosis sedantes o incluso anestésicas, situación que conlleva riesgos, lo que hace preciso que dichos procedimientos sean realizados por médico anestesiólogo.
En Colombia son pocos los estudios que describen la incidencia de eventos adversos relacionados con ayudas diagnósticas de alta complejidad como la RM. Delgado et al.2 realizaron una revisión sobre el uso de la sedación profunda por médico anestesiólogo en pacientes pediátricos (< 15 años) durante el año 2009, donde incluyeron 113 pacientes con una incidencia del 4,4% de eventos adversos no graves. La frecuencia de eventos adversos en la población pediátrica internacional está reportada entre el 0,3 y el 20,1% para el servicio de imágenes diagnósticas11-18.
Rangamani et al.15 reportan una incidencia de eventos adversos en RM del 8%; de estos, el 0,69% fueron eventos adversos graves en estudios de angiorresonancia o RM de corazón para pacientes menores de 120 días de nacidos en un periodo de 10 años. Dorfman et al.17 encontraron 22 eventos adversos entre 1.334 estudios de RM cardiovascular (1,6%); 14 (63,5%) menores, 7 (32%) moderados y uno (4,5%) grave. Por su parte, Kannikeswaran et al.14 reportaron incidencia de eventos adversos del 11,9% en pacientes pediátricos con alteraciones del neurodesarrollo y del 7,9% para pacientes sin alteraciones en el neurodesarrollo; sin embargo, se excluyeron pacientes que tuvieran ASA > III o requirieron anestesia general. En el presente estudio la incidencia de eventos adversos fue del 0,25%, sin incluir los eventos adversos leves no alérgicos; la mayoría de los eventos adversos graves ocurrieron en los pacientes con mayor nivel de riesgo (ASAIII y IV), lo que está acorde con lo descrito por Metzner y Domina18 y otros autores en la literatura15,19,20 en el sentido de que los pacientes con mayor nivel de riesgo tienen mayor frecuencia de complicaciones graves. En relación con los eventos adversos en pacientes pediátricos hospitalizados, el presente estudio mostró una proporción del 66%, cifra mayor a lo reportado por Dorfman et al.17, quienes encontraron un 32% de eventos adversos en pacientes hospitalizados.
Frente a la mortalidad, en este estudio se presentaron 2 muertes: la primera en el año 2012, en paciente femenina de 37 meses de edad, ASA III, con falla cardiaca de base, con paro cardiaco a los 35 min del inicio del procedimiento anestésico de la RM de corazón; el segundo caso de muerte se presentó en el año 2013 en paciente femenina de 48 meses de edad, clasificada como ASA IV, con tumor de fosa posterior, quien asistió para resonancia de cráneo contrastada y presentó paro cardiorrespiratorio a los 10 min del inicio anestésico. Ambos casos recibieron todas las medidas de reanimación cardiopulmonar básica y avanzada dirigidas por médico especialista en anestesiología. Es difícil hallar información acerca de la mortalidad en los estudios de eventos adversos en población pediátrica atendida en servicios de imagenología; una de las pocas investigaciones que reporta este hecho es el estudio de Vitiello et al.20, en el cual se evaluaron 4.952 pacientes, donde se presentaron 7 muertes asociadas a cateterización cardiaca en pacientes pediátricos críticamente enfermos.
Si bien algunos estudios de RM requieren mayor profundidad anestésica, inclusive de periodos cortos de apnea para minimizar los artefactos de movimiento por desplazamiento diafragmático, en la presente investigación no se evidenció una relación entre la complejidad del estudio y la presentación de eventos adversos graves. Dichos eventos ocurrieron durante la realización de 4 RM de cráneo (requiere menor profundidad anestésica)y2RMdecorazón (tiene la mayor exigencia desde el punto de vista anestésico). Cabe resaltar que las 2 muertes se presentaron en estudios de RM diferentes (uno RM de cráneo y otro RM de corazón).
Dentro de los desenlaces moderados en el presente estudio se presentaron 3 laringoespasmos (0,06%), de los cuales a 2 se les colocó dispositivo supraglótico; el evento se presentó durante el periodo de emergencia de la anestesia. El tercer caso no tuvo dispositivo en la vía aérea asociado y ocurrió en un paciente bajo sedación superficial. Todos los casos se resolvieron con la ventilación a través del uso de máscara facial con presión positiva,y 2 de ellos requirieron administración adicional de propofol. Durante el estudio no se presentaron secuelas secundarias a este tipo de desenlace. Malviya et al.16, en un estudio con 922 pacientes, encontraron una incidencia de laringoespasmo del 0,1%.
A diferencia de lo reportado por Malviya et al.21, con una reacción previa al alta, la presente investigación halló 2 reacciones alérgicas posteriores a la prestación del servicio; por su parte, Delgado et al.22 no reportan reacciones de este tipo en su estudio. Estos eventos fueron clasificados como leves, en ambos casos solo con rash cutáneo, sin requerimiento de hospitalización posterior. El primer caso tuvo relación con hidrato cloral, medicamento con poca predictibilidad y larga vida media, actualmente en desuso en nuestro medio. El segundo evento tuvo administración concomitante de medio de contraste con gadolinio, lo que dificultó identificar el agente causal.
Schulte-Uentrop y Goepfert23 reportaron la anestesia general como la técnica de preferencia para realizar RM en el contexto de pacientes menores de 3 años o con comorbilidades mayores y que requirieran algún tipo de sedación, factores que asociaron con mayor riesgo al realizar el estudio diagnóstico. En nuestra práctica únicamente se ha presentado mayor cantidad de eventos adversos en pacientes con comorbilidades mayores presentes al momento del estudio, sin encontrar una asociación con la edad (pacientes menores de 3 años); sin embargo, para hacer una valoración adecuada se requiere realizar un estudio de causalidad, lo cual está fuera del alcance de este estudio.
En el presente estudio el grupo completo de eventos adversos incluyó 12 pacientes (10 mujeres y 2 hombres): la mayoría de los eventos adversos se presentaron en mujeres. En los eventos adversos graves, 4 eventos fueron en mujeresy2en hombres. Por el diseño del estudio no es posible determinar relación causal; sin embargo, cabe señalar que la mayoría de los eventos adversos se presentaron en las mujeres.
Limitaciones
La información obtenida en este estudio proviene de bases de datos. Ya que en los eventos adversos leves no alérgicos hay evidencia de subregistro, estos desenlaces no fueron considerados. Tal es el caso de eventos como la extravasación ocasional de un acceso venoso que se identifica al administrar la prueba de solución salina sin llegar a administrar medicamentos, desaturación por periodo corto de tiempo (< 1 min) o bradicardia que mejora rápidamente según su causa (< 3 min), sin la administración de medicamentos.
Conclusión
El estudio de resonancia magnética asistida bajo sedación o anestesia por anestesiólogo en pacientes pediátricos menores de 15 años es un procedimiento seguro, con un riesgo mínimo del 0,25% de eventos adversos. Sin embargo, como se encuentra en la literatura en pacientes hospitalizados o con patologías descompensadas, debe hacerse un análisis profundo riesgo-beneficio y valorar la mejor opción para cada paciente.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Financiamiento
El Instituto de Alta Tecnología Médica (IATM) financió con recursos propios la creación de la base de datos y el tiempo dedicado por los investigadores. No se recibió ningún aporte externo.
Conflicto de intereses
Los autores declaran que no tienen conflicto de intereses.
Referencias
1. American Society of Anesthesiologists. Practice advisory on anesthetic care for magnetic resonance imaging: an updated report by the American Society of Anesthesiologists task force on anesthetic care for magnetic resonance imaging. Anesthesiology. 2015;122:495-520. [ Links ]
2. Delgado JA, Abad P.Angel GJ, Llano JF, Gómez FJ, Calvo VD. Uso de sedación profunda asistida por un anestesiólogo en resonancia magnética para población pediátrica. Rev Colomb Anestesiol. 2011;38:487-97. [ Links ]
3. Jain R, Petrillo-Albarano T, Parks WJ, Linzer JF, Stockwell JA. Efficacy and safety of deep sedation by non-anesthesiologists for cardiac MRI in children. Pediatr Radiol. 2013;43:605-11. [ Links ]
4. American Academy of Pediatrics, American Academy of Pediatric Dentistry, Coté CJ, Wilson S, Work Group on Sedation. Guidelines for monitoring and management of pediatric patients during and after sedation for diagnostic and therapeutic procedures: an update. Paediatr Anaesth. 2008;18:9-10. [ Links ]
5. Kanal E, Barkovich AJ, Bell C, Borgstede JP, Bradley WG Jr, Froelich JW, et al. ACR Guidance Document on MR Safe Practices: 2013. J Magn Reson Imaging. 2013;37:501-30. [ Links ]
6. Kanal E, Barkovich AJ, Bell C, Borgstede JP, Bradley WG Jr, Froelich JW, et al. ACR Blue Ribbon Pane on MR safety: ACR guidance document for safe MR practices: 2007. AJR Am J Roentgenol. 2007;188:1447-74. [ Links ]
7. Williams K, Thomson D, Seto I, Contopoulos-Ioannidis DG, Ioannidis JP, Curtis S, et al. Standard 6: age groups for pediatric trials. Pediatrics. 2012;129 Suppl. 3:S153-60. [ Links ]
8. Connis R, Nickinovich D, Caplan R, Apfelbaum J. Evaluation and classification of evidence for the ASA Clinical Practice Guidelines. In: Miller RD, editor. Miller's anesthesia. 8th ed. Philadelphia: Elsevier; 2015. p. 3257-70. 2017;45(1):8-14 [ Links ]
9. Vuyk J, Sitsen E, Reekers M. Intravenous anesthetics. In: Miller RD, editor. Miller's anesthesia. 8th ed. Philadelphia: Elsevier; 2015. p. 821-63. [ Links ]
10. Ministerio de la Protección Social. Herramientas para promover la estrategia de la Seguridad del Paciente en el Sistema Obligatorio de Garantía de Calidad de la Atención en Salud. Bogotá; Editorial Fundación FITEC. 2007 [Cited 2015 Ago 14]. Available at: https://www.minsalud.gov.co/sites/rid/1/Herramientas%20para%20la%20Seguridad%20del %20Paciente.pdf. [ Links ]
11. Sanborn PA, Michna E, Zurakowski D, Burrows PE, Fontaine PJ, Connor L, et al. Adverse cardiovascular and respiratory events during sedation of pediatric patients for imaging examinations. Radiology. 2005;237:288-94. [ Links ]
12. Cutler KO, Bush AJ, Godambe SA, Gilmore B. The use of pediatric emergency medicine-staffed sedation service during imaging: a retrospective analysis. Am J Emerg Med. 2007;25:654-61. [ Links ]
13. Bluemke DA, Breiter S. Sedation procedures in MR imaging: safety, effectiveness, and nursing effect on examinations. Radiology. 2000;216:645-52. [ Links ]
14. Kannikeswaran N, Mahajan PV, Sethuraman U, Groebe A, Chen X. Sedation medication received and adverse events related to sedatio for brain MRI in children with and without developmental disabilities. Paediatr Anaesth. 2009;19: 250-6. [ Links ]
15. Rangamani S, Varghese J, Li L, Harvey L, Hammel JM, Fletcher SE, et al. Safety of cardiac magnetic resonance and contrast angiography for neonates and small infants: a 10-year single-institution experience. Pediatr Radiol. 2012;42: 1339-46. [ Links ]
16. Malviya S, Voepel-Lewis T, Eldevik OP, Rockwell DT, Wong JH, Tait AR. Sedation and general anaesthesia in children undergoing MRI and CT: adverse events an outcomes. Br J Anaesth. 2000;84:743-8. [ Links ]
17. Dorfman AL, Odegard KC, Powell AJ, Laussen PC, Geva T. Risk factors for adverse events during cardiovascular magnetic resonance in congenital cardiac disease. J Cardiovasc Magn Reson. 2007;9:793-8. [ Links ]
18. Metzner J, Domino KB. Risks of anesthesia or sedation outside the operating room: the role of the anesthesia care provider. Curr Opin Anaesthesiol. 2010;23:523-31. [ Links ]
19. Odegard KC, DiNardo JA, Tsai-Goodman B, Powell AJ, Geva T, Laussen PC. Anaesthesia considerations for cardiac MRI in infants and small children. Paediatr Anaesth. 2004;14: 471-6. [ Links ]
20. Vitiello R, McCrindle BW, Nykanen D, Freedom RM, Benson LN. Complications associated with pediatric cardiac catheterization. J Am Coll Cardiol. 1998;32:1433-40. [ Links ]
21. Malviya S, Voepel-Lewis T, Prochaska G, Tait AR. Prolonged recovery and delayed side effects of sedation for diagnostic imaging studies in children. Pediatrics. 2000;105:E42. [ Links ]
22. Delgado J, Toro R, Rascovsky S, Arango A, Angel GJ, Calvo V, et al. Chloral hydrate in pediatric magnetic resonance imaging: evaluation of a 10-year sedation experience administered by radiologists. Pediatr Radiol. 2015;45:108-14. [ Links ]
23. Schulte-Uentrop L, Goepfert MS. Anaesthesia or sedation for MRI in children. Curr Opin Anaesthesiol. 2010;23:513-7. [ Links ]











 texto en
texto en