Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.46 no.3 Bogotá July/Sept. 2018
https://doi.org/10.1097/cj9.0000000000000067
Investigación científica y tecnológica
Análisis de resultados después de la implementation de protocolos de recuperación acelerada en cirugía hepatopancreatobiliar
a Clínica CES, Medellín, Colombia
b Residente de Anestesiología, Universidad CES, Medellín, Colombia.
Introducción:
La cirugía Hepatopancreatobiliar (HPB) ha logrado reducir la morbi-mortalidad en los últimos 30 años gracias a avances tecnológicos, centros de alto volumen, implementación de grupos multidisciplinarios y protocolos de recuperación acelerada.
Objetivos:
Comparar el impacto en la implementación de guías de recuperación acelerada en pacientes llevados a cirugía HPB.
Métodos:
Se realizó un estudio observacional retrospectivo donde se recolectaron historias clínicas de pacientes HPB entre julio 2012 - enero 2017. Se analizaron datos demográficos, diagnósticos más frecuentes, fluidoterapia, necesidad de transfusiones, estancia hospitalaria, necesidad de reintervención y mortalidad a 30 días. Se identificaron dos grupos: grupo A (julio 2012 - diciembre 2014) y grupo B (enero 2015 - enero 2017) en el cual se implementaron las guías de recuperación acelerada.
Resultados:
Un total de 364 pacientes, 145 para el grupo A y 219 para el grupo B. Los diagnósticos más frecuentes fueron cáncer de páncreas, metástasis hepáticas, colangiocarcinoma y lesión de vía biliar. Se evidenció sangrado menor a 600 ml (OR = 12,88 IC95%:5,31-31,23), menor necesidad de transfusión (OR=0,16 IC95%:0,068-0,418) y fluidoterapia menor a 5000 ml en el grupo B (OR = 4,23 IC95%:1,76-10,11). La estancia hospitalaria fue 3 días (rango intercuartílico 2-5; p < 0,001) y la mortalidad a 30 días fue menor para el grupo B (p=0,012).
Conclusiones:
La implementación de guías de recuperación acelerada mostró disminución en el sangrado intraoperatorio, cantidad de líquidos intravenosos administrados, estancia hospitalaria y mortalidad a 30 días.
Palabras clave: Pancreatectomía; Hepatectomía; Mortalidad; Morbilidad; Periodo de Recuperación de la Anestesia
Background:
Hepatopancreatobiliary surgery (HPB) has been able to reduce morbidity and mortality over the past 30 years, as a result of technological breakthroughs, high-volume centers, and the implementation of multidisciplinary groups with fast recovery protocols.
Objective:
To compare the impact of implementing fast recovery guidelines in patients undergoing HPB surgery.
Methods:
We conducted an observational retrospective study collecting medical records of patients undergoing HPB surgery from July 2012 to January 2017. An analysis was done of the demographic data, frequent diagnoses, fluid therapy, need for transfusions, length of hospital stay, need for reintervention, and 30-day mortality. Two groups were identified: group A (July 2012-December 2014) and group B (January 2015-January 2017) in which fast recovery protocols were implemented.
Results:
A total of 364 patients were included, 145 in group A and 219 in group B. The most frequent diagnoses were pancreatic cancer, liver metastasis, cholangiocarcinoma, and bile duct injury. Bleeding was less than 600 mL (OR = 12,88, CI 95%(5,3131,23)), the transfusion requirements dropped (OR=0.16; 95% CI: 0.068-0.418), and fluid therapy was below 5000 mL in group B (OR = 4.23; 95% CI: 1.76-10.11). Length of hospital stay was 3 days (interquartile range 2-5; p<0.001), and mortality at 30 days was lower in group B (p = 0.012).
Conclusion:
The implementation of fast recovery protocols showed a decrease in intraoperative bleeding, intravenous fluids therapy, length of hospital stay, and 30-day mortality.
Keywords: Pancreatectomy; Hepatectomy; Mortality; Morbidity; Anesthesia Recovery Period
Introducción
Desde sus inicios en 1880 la cirugía HPB ha presentado grandes desafíos para el grupo quirúrgico, con una morbilidad entre 30-40% y una mortalidad entre S-9%.1 Con los años se han desarrollado estrategias para disminuir los riesgos perioperatorios y mejorar los desenlaces. Estas estrategias incluyen un manejo anestésico avanzado, instrumentos diagnósticos más especializados, mayores herramientas en la elección del paciente, técnicas quirúrgicas menos invasivas y sobre todo protocolos enhanced recovery after surgery (ERAS) que disminuyen estancia hospitalaria, morbilidad y costos.2-4
En nuestro centro se ha conformado un grupo para el manejo quirúrgico de estas patologías, dentro del cual se resalta a los cirujanos hepatopancreatobiliares, anestesiólogos hepatobiliares, soporte nutricional, cuidado intensivo, oncología y radiología.
En el siguiente estudio queremos mostrar nuestra experiencia, realizando un análisis retrospectivo de 364 casos en los cuales se realizaron diferentes cirugías HPB, tanto abierta como laparoscópica; y se evaluó el impacto al implementar protocolos de recuperación acelerada en términos de sangrado intraoperatorio, cantidad de líquidos intraoperatorios, reintervención, estancia hospitalaria y mortalidad a 30 días.
Materiales y métodos
Se realizó un estudio observacional retrospectivo de casos y controles anidado a una cohorte de pacientes, donde se revisaron los pacientes llevados a cirugía de hígado, páncreas y vía biliar realizados por el equipo de cirugía HPB desde julio 2012 hasta enero 2017. La recolección y el análisis de los datos fueron aprobados por el comité de ética; y de acuerdo con las disposiciones legales por las cuales se establecen las normas científicas, técnicas y administrativas para la investigación en salud dadas en la resolución 8430, se consideró esta como una investigación sin riesgo.
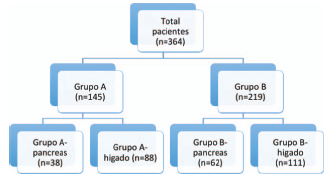
Se identificaron inicialmente dos grupos: el grupo A que comprendió los pacientes llevados a cirugía entre julio 2012 a diciembre 2014 y el grupo B en el cual se implementaron los protocolos de recuperación acelerada entre enero 2015 a enero 2017. Posteriormente se realiza un análisis por subgrupos en el cual, tanto para el grupo A, como para el grupo B se subdividieron dos grupos; el primero de ellos corresponde a cirugías hepáticas y el segundo a cirugías pancreáticas. En este análisis se excluyeron los diagnósticos correspondientes a colecistectomías laparoscópicas y los diagnósticos que no tienen relación directa con el páncreas o el hígado. Todos los procedimientos recolectados durante el estudio fueron realizados por el mismo equipo quirúrgico, dos cirujanos hepatobiliares y dos anestesiólogos hepatobiliares. (Ver Figura 1).
El manejo anestésico para el Grupo A se realizó sin ningún tipo de protocolo de trabajo. Todos los pacientes eran llevados a cirugía con ayuno de 8 horas para sólidos y líquidos, sin administrar cargas de carbohidratos; no se realizó asesoramiento ni educación prequirúrgica. Todos los pacientes fueron llevados a cirugía bajo anestesia general, el manejo de líquidos se realizó sin protocolo utilizando lactato de ringer o solución salina 0,9% de forma liberal. El uso de vasopresores se realizó según criterio del anestesiólogo, así como el manejo analgésico.
Para el grupo B tomando como referencia las guías recomendadas por la sociedad ERAS (www.erassociety.org) se creó un protocolo de manejo desde el preoperatorio hasta el alta. Este protocolo incluye:
Evaluación 14 días previo a la cirugía por nutrición donde se inicia manejo con ecoinmunonutrición (pre-bióticos y suplementos de arginina), evaluación preanestésica donde se brinda asesoramiento y educación prequirúrgica, ayuno manejado con 8 horas para sólidos y 2 horas para líquidos, ofreciendo carga de carbohidratos orales (maltodextrinas) 2 horas antes de la cirugía.
Todos los pacientes fueron llevados a cirugía bajo anestesia general con tubo orotraqueal, la anestesia fue balanceada con remifentanil por Target Control Infusión (TCI) entre 3-5ng/ml y sevoflurano para mantener 0.8 MAC en el gas espirado. La relajación neuromuscular se realizó con rocuronio o cisatracurio. El flujo de gases fue ajustado para mantener fracciones inspiradas de oxigeno del 70%. La ventilación mecánica se realizó con volumen corriente (VC) 6-8ml/kg, frecuencia respiratoria 12-14/minuto y PEEP 5mmhg para ajustar ETCO2 de 35mmhg. Según el diagnóstico y el tipo de cirugía se decidía si el paciente requería monitorización con catéter venoso central y línea arterial. En caso de ser cirugía hepática se mantuvo la PVC menor de 5mmhg. Para el manejo de líquidos perioperatorios se utilizó monitor de gasto cardiaco (EV1000, Edwards Lifescience) y se mantenía como metas variación volumen sistólico (VVS) menor 13%, índice cardiaco (IC) mayor de 2,5lt/min/m2 y delta CO2 menor 6mmhg. Se mantuvo infusión de líquidos a 2cc/kg/h y en caso de requerir terapia con volumen se administraba un bolo de 3cc/kg hasta normalizar metas de trabajo. En todos los casos se utilizaron soluciones balanceadas (Isofundin, Bbraun). En caso de persistir con presiones sistólicas menores de 90mmhg y tener metas de líquidos en rangos normales se iniciaba infusión de norepinefrina en dosis titulables la cual se retiraba al finalizar el procedimiento en caso de no ser requerida por más tiempo.
Para la analgesia se utilizó en caso de ser cirugía abierta técnicas epidural torácica (T7-T8), iniciando con bolo de bupivacaína 0.25% entre 10-15cc y continuando una infusión de bupivacaína 0,125% entre 6-8cc/h. En caso de ser cirugía laparoscópica se utilizó analgesia espinal (L4-L5) con aguja 27 Quincke y morfina a dosis de 2 mcg/kg, o analgesia intravenosa con dipirona 2gr e hidromorfona 0,01mg/kg. Según criterio de anestesiólogo tratante en cirugías laparoscópicas se realizaba un bloqueo Transverse Abdominal Plane (TAP) al finalizar el procedimiento con bupivacaina 0,25% 12cc en cada lado. Durante el transoperatorio fueron medidos gases arteriales, electrolitos y lactato.
Los datos fueron recolectados de forma retrospectiva, todas las variables fueron estandarizadas por el grupo, se tomaron datos sociodemográficos, diagnóstico preoperatorio, fluidoterapia medida como necesidad de líquidos menores a 5000ml, necesidad de transfusiones, sangrado intraoperatorio mayor de 600ml, estancia hospitalaria, necesidad de reintervención y mortalidad a 30 días.
Se realizó un análisis teniendo en cuenta las características de las variables, y usando para el procesamiento de la información el software SPSS versión 21.0 (IBM SPSS Statistics). Para las variables cuantitativas se tuvo en cuenta las medidas de tendencia central y de dispersión correspondientes, para las variables cualitativas la descripción se realizó en frecuencias absolutas y relativas. En el análisis bivariado se realizó comparación de proporciones para las variables cualitativas a través de la prueba Chi cuadrado de independencia de Pearson, y se calcularon odd ratios(OR) crudos con sus respectivos intervalos de confianza al 95%(IC 95%). Para las variables cuantitativas, la diferencia de medianas a través de la prueba U de Mann Whitney. Se consideró estadísticamente significativo un valor de alfa de 0.05.
Resultados
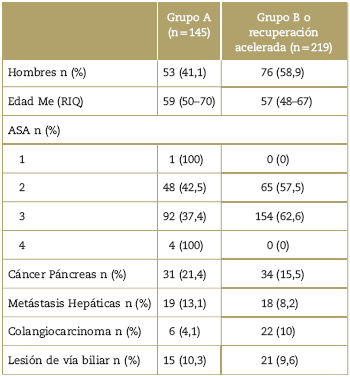
La cohorte inicial tenía un total de 364 pacientes recolectados desde julio 2012 a enero 2017. Para el grupo A (julio 2012 a diciembre 2014) se identificaron 145 pacientes y para el grupo B (enero 2015 a enero 2017) 219 pacientes. En el análisis por subgrupos se clasificaron en el grupo A-páncreas 38 pacientes y en el grupo B-páncreas 62 pacientes. En el grupo A-hígado 88 pacientes y en grupo B-hígado 111 pacientes. Del total de la muestra se excluyeron 65 pacientes debido a que en ellos no se realizaron cirugías directamente relacionadas con páncreas o hígado. Los datos demográficos se pueden observar en la tabla 1.
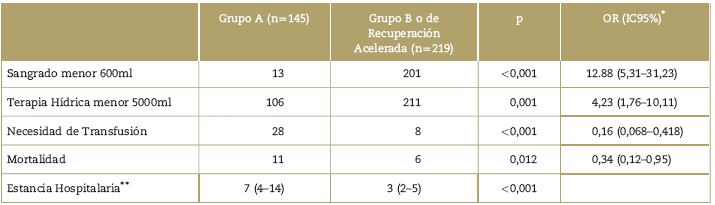
El riesgo de tener sangrado por encima de 600ml fue mayor en el grupo A, al igual que la necesidad de transfusión y la administración de más de 5000ml de fluidoterapia. La estancia hospitalaria fue menor en el grupo B, así como menor mortalidad a 30 días (Ver Tabla 2).
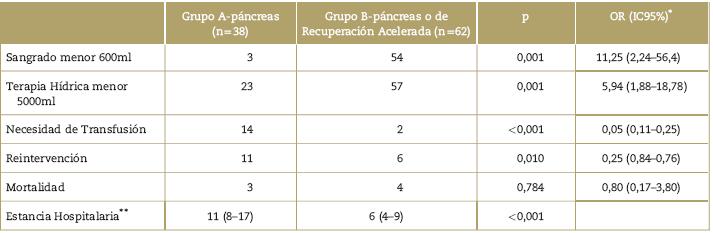
En el subgrupo pancreático el riesgo de sangrado por encima de 600 ml fue mayor en el grupo A-páncreas, así como la necesidad de fluidoterapia mayor a 5000 ml, mayor necesidad de transfusiones y mayor necesidad de reintervención. La estancia hospitalaria fue menor en el grupo B-páncreas (Ver Tabla 3). La mortalidad fue mayor en el grupo B-páncreas, aunque la diferencia entre los grupos no fue estadísticamente significativa. (Ver Tabla 3).
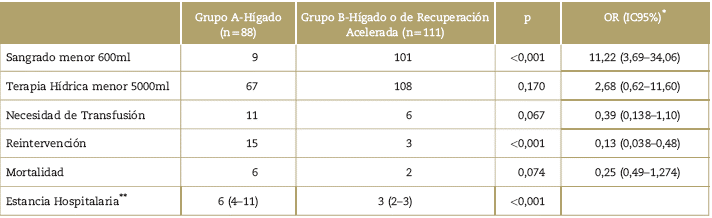
En el subgrupo hígado el riesgo de sangrado por encima de 600 ml fue mayor en el grupo A-hígado, la necesidad de fluidoterapia mayor a 5000 ml fue superior, mayor necesidad de transfusiones, y mayor necesidad de reintervención (Ver Tabla 4); aunque vale la pena mencionar que la terapia hídrica y la necesidad de transfusiones no mostraron diferencias estadísticamente significativas. La estancia hospitalaria fue menor en el grupo B-hígado. La mortalidad fue mayor en el grupo A-hígado, pero la diferencia entre los grupos no fue estadísticamente significativa. (Ver Tabla 4).
Discusión
En los 70's la mortalidad hepática era 20% y era causada principalmente por hemorragia o insuficiencia hepática. Gracias a los avances tecnológicos durante las últimas décadas, una gran cantidad de factores han contribuido a la reducción en la mortalidad a valores menores del 5%; dentro de estos factores están formación de grupos de trabajo, centros de alto volumen quirúrgico, cirugía laparoscópica, perfeccionamiento en las técnicas de volumetrías hepáticas y mejorías en las técnicas de transeccion hepática con métodos más selectivos de control vascular.5,6 Sin embargo la morbilidad permanece alrededor de 15-35%; es por esta razón, que la optimización en las variables perioperatorias y la creación de protocolos de recuperación acelerada juegan un papel importante en el cuidado de estos pacientes.7-10 Recientemente Zhao y cols en su metaanálisis de 20 años encontraron que los programas de recuperación acelerada en cirugía hepática tanto abierta como laparoscópica disminuyen la estancia hospitalaria, las complicaciones a 30 días y los costos, recomendando esta estrategia de manejo como segura y eficaz.11
Por otro lado, la cirugía pancreática mayor a pesar de los avances tecnológicos sigue teniendo una alta morbilidad, cercana al 40%; inclusive en centros de alto volumen.12 Esto principalmente por fistula pancreática, sangrado y retardo del vaciamiento gástrico. La mortalidad que antes era del 30% ha logrado disminuir hasta valores menores al 9% con la implementación de protocolos de recuperación temprana y optimización en el manejo de variables perioperatorias.13,14 La implementación de estos protocolos ha logrado reducir la estancia hospitalaria, la incidencia de retraso en el vaciamiento gástrico y los costos sin llegar a afectar la tasa de reingresos como lo demuestra Xiong y cols en su metaanálisis de 2719 pacientes de cirugía pancreática.15
Las guías ERAS están fundamentadas en reducir el stress asociado al acto quirúrgico; y así, conseguir una recuperación optima en menor tiempo y con mayor calidad. Este cambio en los paradigmas debe involucrar la creación de equipos multidisciplinarios y sobretodo la auditoria continua en los procesos para asegurar una adecuada adherencia a las guías de manejo. Alrededor de 24 recomendaciones que van desde el preoperatorio hasta el alta del paciente han sido diseñadas para varias especialidades y procedimientos.
Las indicaciones para el preoperatorio incluyen valoración nutricional y soporte con ecoinmunonutrición, optimización de enfermedades crónicas, asesoramiento y educación lo cual reduce la ansiedad y mejora la adherencia del paciente a los protocolos, ayuno de 8 horas para sólidos y 2 horas para líquidos claros con carga de carbohidratos, no preparación intestinal, profilaxis antitrombótica, profilaxis antibiótica y profilaxis contra nausea y vomito. Para el intraoperatorio recomiendan técnicas mínimamente invasivas, evitar opioides de larga acción, manejo hídrico dirigido por metas para evitar hipo o hipervolemia, analgesia epidural para cirugía abierta, normotermia y disminución en el uso de drenajes o sondas nasogástricas. En el postoperatorio enfatizan la movilización temprana, inicio temprano de vía oral, retiro temprano de sondas, catéteres, drenes y analgesia multimodal libre de opioides.2,16,17
Las primeras guías publicadas fueron para el manejo perioperatorio de cirugía colorectal, posteriormente se han publicado recomendaciones para cirugía abdominal mayor (resección rectal, cistectomía, resección gástrica, cirugía ginecológica mayor, cirugía bariátrica, cirugía para cabeza y cuello, reconstrucción mamaria) entre las cuales se incluyen guías para pancreatoduodenectomías en el 2012 y guías para resección hepática en el 2016.2,16,17
Las guías ERAS por medio de estrategias multimodales han logrado reducir el tiempo de hospitalización, morbilidad y mejorar la capacidad funcional del paciente tempranamente.18 Estas estrategias desde el punto de vista anestésico están encaminadas a un mejor control del dolor lo cual conlleva a una movilización precoz; mejor control hídrico, lo cual inicia desde el preoperatorio con tiempos de ayuno menor para líquidos y disminución en los balances positivos.19 Es así como el paciente incluido en programas de recuperación temprana tiene altas hospitalarias en menor tiempo, menor número de complicaciones médicas comparados con los grupos de tratamiento perioperatorio estándar y menores costos hospitalarios.20,21
Uno de los papeles fundamentales del anestesiólogo es la terapia hídrica, la cual debe estar guiada por metas encaminadas a objetivos fisiológicos, sabiendo que estados de híper o hipovolemia aumentan el riesgo de complicaciones perioperatorias.22-24 Específicamente el tipo de fluido escogido para la cirugía debe ser administrado cuando el paciente se encuentre fuera de rango en las metas para alcanzar una adecuada perfusión tisular y cuando el paciente sea respondedor a volumen según las variables dinámicas elegidas como protocolo institucional.25-27 Navarro y cols recomiendan el uso de protocolos y terapia dirigidas por metas basados en la medición de variables dinámicas (variación de volumen sistólico: VVS, variación de presión de pulso: VPP) en cirugías mayores.28,29
Nuestro protocolo de manejo hídrico perioperatorio es similar al propuesto por Cannesson y cols en el cual se incluye una infusión basal de soluciones balanceadas y la medición periódica de variables dinámicas; asociado a un flujograma en el cual se tiene en cuenta el índice cardiaco y la presión arterial media para la decisión de administrar fluidoterapia, vasopresores o inotrópicos según respuesta.27
Nuestro estudio presenta las limitaciones propias de un estudio observacional retrospectivo en el cual las variables pueden tener sesgos de información ya que son tomadas de datos de la historia clínica. Así mismo, algunas variables que mostraban desenlaces clínicos no fueron analizadas ya que los datos no se encontraban en la historia clínica. Sin embargo, la necesidad de un estudio que analice las variables costo-beneficio en nuestro hospital resultarían de vital importancia para el personal financiero y administrativo; facilitando así la inversión económica en estos programas.
Conclusiones
La implementación de guías de recuperación acelerada mostró disminución en la cantidad de sangrado, cantidad de líquidos intravenosos administrados, estancia hospitalaria y mortalidad de los pacientes de cirugía HPB.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
REFERENCIAS
1. Foster JH. History of liver surgery. Arch Surg 1960-1991;126:381-387. [ Links ]
2. Lassen K, Coolsen MME, Slim K, et al. Guidelines for perioperative care for pancreaticoduodenectomy: Enhanced Recovery After Surgery (ERAS) Society recommendations. World J Surg 2013; 37:240-258. [ Links ]
3. De Pietri L, Montalti R, Begliomini B. Anaesthetic perioperative management of patients with pancreatic cancer. World J Gastroenterol 2014;20:2304-2320. [ Links ]
4. Snowden C, Prentis J. Anesthesia for hepatobiliary surgery. Anesthesiol Clin 2015;33:125-141. [ Links ]
5. Jones C, Kelliher L, Thomas R, et al. Perioperative management of liver resection surgery. J Perioper Pract 2011;21:198-202. [ Links ]
6. Edwin B, Nordin A, Kazaryan AM. Laparoscopic liver surgery: new frontiers. Scand J Surg 2011;100:54-65. [ Links ]
7. Dokmak S, Ftériche FS, Borscheid R, et al. 2012 Liver resections in the 21st century: we are far from zero mortality. HPB 2013;15:908-915. [ Links ]
8. Song W, Wang K, Zhang R-J, et al. The enhanced recovery after surgery (ERAS) program in liver surgery: a meta-analysis of randomized controlled trials. SpringerPlus 2016;5:207. [ Links ]
9. Wang C, Zheng G, Zhang W, et al. Enhanced recovery after surgery programs for liver resection: a meta-analysis. J Gastrointest Surg 2017;21:472-486. [ Links ]
10. Hughes MJ, McNally S, Wigmore SJ. Enhanced recovery following liver surgery: a systematic review and meta-analysis. HPB 2014;16:699-706. [ Links ]
11. Zhao Y, Qin H, Wu Y, et al. Enhanced recovery after surgery program reduces length of hospital stay and complications in liver resection: a PRISMA-compliant systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore) 2017;96:e7628. [ Links ]
12. Are C, Dhir M, Ravipati L. History of pancreaticoduodenectomy: early misconceptions, initial milestones and the pioneers. HPB 2011;13:377-384. [ Links ]
13. Kagedan DJ, Ahmed M, Devitt KS, et al. Enhanced recovery after pancreatic surgery: a systematic review of the evidence. HPB 2015;17:11-16. [ Links ]
14. Kobayashi S, Ooshima R, Koizumi S, et al. Perioperative care with fast-track management in patients undergoing pancreaticoduodenectomy. World J Surg 2014;38:2430-2437. [ Links ]
15. Xiong J, Szatmary P, Huang W, et al. Enhanced recovery after surgery program in patients undergoing pancreaticoduodenectomy: a PRISMA-compliant systematic review and meta-analysis. Medicine (Baltimore) 2016;95:e3497. [ Links ]
16. Ljungqvist O, Scott M, Fearon KC. Enhanced recovery after surgery: a review. JAMA Surg 2017;152:292-298. [ Links ]
17. Melloul E, Hübner M, Scott M, et al. Guidelines for perioperative care for liver surgery: enhanced recovery after surgery (ERAS) society recommendations. World J Surg 2016;40:2425-2440. [ Links ]
18. Visioni A, Shah R, Gabriel E, et al. Enhanced recovery after surgery for noncolorectal surgery?: A systematic review and metaanalysis of major abdominal surgery. Ann Surg 2018;267:57-65. [ Links ]
19. Scott MJ, Miller TE. Pathophysiology of major surgery and the role of enhanced recovery pathways and the anesthesiologist to improve outcomes. Anesthesiol Clin 2015;33:79-91. [ Links ]
20. Jones C, Kelliher L, Dickinson M, et al. Randomized clinical trial on enhanced recovery versus standard care following open liver resection. Br J Surg 2013;100:1015-1024. [ Links ]
21. Joliat G-R, Labgaa I, Hübner M, et al. Cost-benefit analysis of the implementation of an enhanced recovery program in liver surgery. World J Surg 2016;40:2441-2450. [ Links ]
22. Brandstrup B, T0nnesen H, Beier-Holgersen R, et al. Effects of intravenous fluid restriction on postoperative complications: comparison of two perioperative fluid regimens: a randomized assessor-blinded multicenter trial. Ann Surg 2003;238:641-648. [ Links ]
23. Gan TJ, Soppitt A, Maroof M, et al. Goal-directed intraoperative fluid administration reduces length of hospital stay after major surgery. Anesthesiology 2002;97:820-826. [ Links ]
24. Kulemann B, Fritz M, Glatz T, et al. Complications after pancreaticoduodenectomy are associated with higher amounts of intra- and postoperative fluid therapy: a single center retrospective cohort study. Ann Med Surg 2012-2017;16:23-29. [ Links ]
25. Voldby AW, Brandstrup B. Fluid therapy in the perioperative setting-a clinical review. J Intensive Care 2016;4:27. [ Links ]
26. Mythen MG, Swart M, Acheson N, et al. Perioperative fluid management: consensus statement from the enhanced recovery partnership. Perioper Med 2012;1:2. [ Links ]
27. Cannesson M, Ramsingh D, Rinehart J, et al. Perioperative goal-directed therapy and postoperative outcomes in patients undergoing high-risk abdominal surgery: a historical-prospective, comparative effectiveness study. Crit Care 2015;19:261. [ Links ]
28. Navarro LHC, Bloomstone JA, Auler JOC, et al. Perioperative fluid therapy: a statement from the international Fluid Optimization Group. Perioper Med 2015;4:3. [ Links ]
29. Benes J, Giglio M, Brienza N, et al. The effects of goal-directed fluid therapy based on dynamic parameters on post-surgical outcome: a meta-analysis of randomized controlled trials. Crit Care 2014; 18:584. [ Links ]











 text in
text in