Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.46 no.4 Bogotá Oct./Dec. 2018
https://doi.org/10.1097/cj9.0000000000000053
Reporte de casos
Granulocitopenia por dipirona: reporte de caso
a Grupo de Investigación en Farmacoepidemiología y Farmacovigilancia, Universidad Tecnológica de Pereira
b Audifarma S.A. Pereira, Colombia.
Introducción: La dipirona se ha posicionado en varios países como una de las primeras opciones de venta libre al público para el manejo del dolor. Sus posibles efectos adversos son conocidos a nivel mundial; entre ellos, la agranulocitosis es la más letal con una mortalidad aproximada del 10% y un riesgo asociado de 1 por cada 1.000.000 pacientes.
Hallazgos clínicos, intervención y resultados: Se presenta un caso de una paciente que luego de recibir 23 días seguidos dipirona para el manejo del dolor presentó disminución progresiva de los leucocitos documentados en el hemograma. Se descartaron otras posibles causas de dicho evento. Luego de suspender la administración de la dipirona los leucocitos volvieron a sus valores normales.
Conclusión: Se estableció la sospecha de diagnóstico probable de granulocitopenia como reacción adversa medicamentosa por dipirona. La granulocitopenia por dipirona aunque poco frecuente, se puede presentar en pacientes que la reciben por largos periodos de tiempo.
Palabras clave: Dipirona; Agranulocitosis; Farmacovigilancia; Efectos Adversos; Reporte de caso
Introduction:
Dipyrone has been positioned in several countries as one of the first over-the-counter options for pain management. Its possible adverse effects are known worldwide; among them, agranulocytosis is the most lethal, with a mortality of approximately 10% and an associated risk of 1 per 1,000,000 patients.
Clinical findings, interventions, and outcomes:
A case of a patient who, after 23 days of using dipyrone for pain management, developed a progressive drop in leukocyte count. Other potential causes of the event were ruled out. After dipyrone discontinuation, leukocyte counts returned to their normal values.
Conclusion:
The probable diagnosis of granulocytopenia as a dipyrone-related adverse drug reaction was established. Although rare, dipyrone-related granulocytopenia, may occur in patients who use this medication for long periods.
Keywords: Dipyrone; Agranulocytosis; Pharmacovigilance; Adverse effects; Case Report
Introducción
La dipirona (metamizol) es un fármaco con efectos analgésicos, usado para tratamiento de dolor agudo postoperatorio, dolor oncológico, cólico y migraña.1-3 Empleado ampliamente antes de 1970, donde se empezó a relacionar su uso con reacciones adversas graves como agranulocitosis,4,5 definida como la disminución de granulocitos en sangre menor a 0.5 x 109/L, que aunque poco frecuentes presentaban una mortalidad asociada del 10%, debido a la predisposición de presentar neumonía, sepsis, necrólisis epidérmica tóxica y fascitis necrotizante,6-9 lo que llevó a la Agencia Federal de Alimentos y Medicamentos (FDA) a prohibirla en Estados Unidos en el año de 197710; desde ese momento y hasta la actualidad, son más de 30 países que han prohibido su uso de manera general.
Se han propuesto diversos factores que podrían contribuir a la aparición de agranulocitosis, pero a ninguno de estos se le ha podido establecer una relación directa; entre los más destacados se encuentran: uso extendido (mayor 14 días), sexo femenino, edad (mayor de 60 años), uso concomitante de metotrexate, susceptibilidad inmunológica y metabólica.11 Se presenta a continuación la descripción de un caso donde se puede evidenciar dicho efecto.
Información del paciente
Mujer de 59 años de edad, con antecedentes patológicos de hipertensión arterial, trastorno depresivo no especificado, antecedentes quirúrgicos corrección de cistocele en 2010 y farmacológicos: hidroclorotiazida, losartan, verapamilo, ácido acetil salicílico y fluoxetina.
Hallazgos clínicos
Fue llevada al servicio de urgencias el día 17/10/16 tras presentar accidente de tránsito en motocicleta en calidad de pasajero, al ingreso al centro médico con evidencia de fractura expuesta de tibia, equimosis periorbitaria bilateral sugiriendo fractura base de cráneo, hipotensión, amnesia del episodio. Se inicia manejo médico con dipirona 2 gramos endovenosos cada 6 horas, cefazolina 1 gramo endovenoso cada 6 horas, y gentamicina 160 mg endovenosos cada 24 horas.
El mismo día es valorada por cirugía general que realiza toracostomía cerrada por neumotórax izquierdo, y por ortopedia que le realizan reducción abierta de fractura de tibia en el mismo momento quinirgico. En el posoperatorio continua con dipirona 1 gramo endovenoso cada 6 horas sumado a tramadol 100 mg cada 8 horas sólo si presenta dolor intenso, ranitidina 50mg endovenosos cada 12 horas, enoxaparina 40mg subcutáneos al día y el mismo manejo antibiótico. El hemograma inicial de la paciente era únicamente notorio por anemia severa (hemoglobina 6.6mg/dl) posterior a éste resultado se indica transfundir 2 unidades de glóbulos rojos.
El día 19/10/16 se aumenta dosis de dipirona a 2 gramos endovenosos cada 6 horas, mientras que los medicamentos previamente descritos no sufrieron cambios. El día 21/ 10/2016 se realizó osteosíntesis de tibia y peroné izquierdos. El hemograma de control evidenciaba leve mejoría de la anemia (hemoglobina 7 mg/dl). El día 21/10/16 se realizó el retiro de toracostomía con adecuada evolución clínica, y continuó igual manejo. Los hemogramas seriados de control se mantuvieron dentro de la normalidad. El 26/ 10/16 fue valorada por cirugía maxilo-facial quien realizó reconstrucción del piso de la órbita, y recibió transfusión de una unidad de concentrado globular durante el procedimiento. A causa de un reporte de derrame pleural izquierdo por tomografía axial computarizada de tórax y un ultrasonido de tórax que lo cuantificaba en 471 cc, se programó para toracentesis, sin embargo, por sospecha de celulitis en hemitórax izquierdo se postergó el drenaje, pero resultó ser solo irritación cutánea por la cinta adhesiva. Por una adecuada evolución posquirúrgica fue dada de alta por ortopedia y cirugía maxilo-facial. La paciente continuó su evolución a la espera de realización de toracentesis, se realizó nuevo ultrasonido de tórax el 07/11/16 que mostraba persistencia de derrame pleural izquierdo por lo cual se solicitaron paraclínicos de control para realizar dicho procedimiento, entre ellos, un hemograma del 08/11/17 que reportó leucopenia, neutropenia y linfopenia (ver Tabla 1), creatinina y nitrógeno uréico dentro de parámetros normales.
Intervención terapéutica
Se realizó toracentesis el día 09/11/16 obteniendo 180 cc de material seroso que se envió a estudio el cual resultó ser un exudado líquido, sin signos de infección; pero debido a los hallazgos en el hemograma el médico internista decide suspender la dipirona luego de 23 días de estarla recibiendo y se ordena hemograma de control que muestra empeoramiento de conteo de células blancas.
Seguimiento y resultados
Continua vigilancia estricta con hemogramas de control que muestran mejoría de los parámetros previos (ver Tabla 1).
Evaluación del diagnóstico
Después de aplicación del algoritmo de Naranjo y colaboradores se emite el concepto de leucopenia probable asociada a uso de dipirona. Se indica egreso con hemograma de control en un mes; además, tiene una evolución radiológica del derrame pleural satisfactoria por lo que cirugía general decide dar de alta con control por consulta externa.
Línea de tiempo
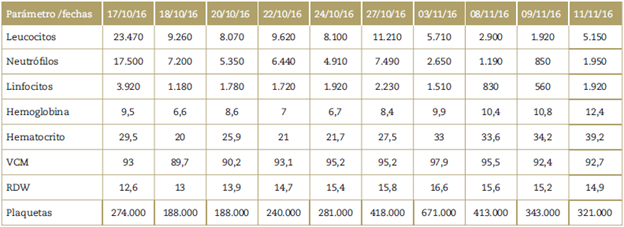
En la Tabla 1 se observan los resultados de todos los hemogramas tomados durante la hospitalización de la paciente.
Discusión
La dipirona es una pirazolona con efectos analgésicos, antipiréticos y anti espasmódicos, pero con poco efecto antinflamatorio.1,7 Es utilizada en el manejo del dolor postoperatorio, dolor tipo cólico, dolor por cáncer y migraña; aunque su uso es muy controvertido en muchos países debido al riesgo de agranulocitosis, en otros se sigue comercializando aun sin receta médica.12
Se considera que su efecto antipirético se debe a la reducción de los niveles de prostaglandina E2 sanguíneos, con posterior efecto antipirético en el receptor EP3 ubicado en las neuronas termorreguladoras del hipotálamo anterior.
Entre sus efectos adversos asociados se incluyen: náuseas, emésis,1 hipotensión, shock cardiogénico,13,14 exantemas, urticaria,5 nefritis intersticial, insuficiencia renal aguda,15 anafilaxia16 y síndrome de Stevens-Johnson17 pancitonenia, y agranulocitosis1,6,18; estas últimas son las que han limitado su uso generalizado. Con respecto a la agranulocitosis, se han planteado diversas teorías sobre su explicación, una de ellas sugiere un efecto tóxico en sangre periférica causado por la aminopirina en donde se desarrollan anticuerpos anti neutrófilos fármaco dependientes que luego inducen a la formación de complejos inmunes con el medicamento, conduciendo a la lisis celular de neutrófilos.19 Sin embargo, la lisis de estos leucocitos también puede ocurrir en médula ósea debido a que uno de los metabolitos de la dipirona puede interactuar con las cadenas de lisina de las células y causar una respuesta inmune. También existe una teoría donde los neutrófilos producen especies reactivas de oxígeno capaces de oxidar algunos fármacos en productos reactivos, los cuales actúan como haptenos induciendo la formación de anticuerpos.7,20 Otro mecanismo inmunológico, sugiere una disminución en el crecimiento in vitro de progenitores mieloides, progenitores primitivos multipotenciales y progenitores eritroides causados por dipirona en un cultivo in vitro de medula ósea con células CD34+.21
Por otra parte, se han propuesto diversos factores que podrían contribuir con la aparición de la agranulocitosis como lo son la exposición a dosis altas, tratamiento prolongado (más de 14 días), sexo femenino, edad mayor de 65 años, interacciones farmacológicas y predisposición genética.1,11 Sin embargo, en ninguna se ha establecido una relación directa de agranulocitosis inducida por dipirona.11,22
Se presenta el caso de una mujer de 59 años de edad en contexto de politraumatismo, que recibió manejo con dipirona durante 23 días, y que desarrolló una granulocitopenia sin otra causa aparente, los otros fármacos que estuvo recibiendo no se pudieron asociar temporalmente con este mismo tipo de evento adverso y al suspender el fármaco el hemograma de control evidenció un aumento de los leucocitos. La paciente no tenía un proceso infeccioso subyacente a la leucopenia, y fue dada de alta sin presentar ninguna otra complicación. Siguiendo los protocolos y recomendaciones que se deben realizar ante este tipo de eventos se aplicó el algoritmo de Naranjo y colaboradores23 para tratar de establecer la asociación de causalidad, que arrojó un puntaje de 7, lo que la califica como una reacción adversa medicamentosa probable.
Pese a que es una reacción poco frecuente en nuestro medio, los médicos y el personal tratante de pacientes que sufren dolor por periodos prolongados de tiempo deberían tener presente el riesgo que confiere el uso de dipirona por más de 14 días y su asociación con reducción del conteo de células blancas y por lo tanto la inmunosupresión y la probabilidad incrementada de infecciones que ello significa.
Perspectiva de la paciente
La paciente solamente expresó agradecimiento por la atención recibida y por poder volver a caminar.
Responsabilidades éticas
Protección de personas y animales. El reporte de caso se hizo bajo consentimiento informado de la familia, según la resolución No. 8430 de 1993 del Ministerio de Salud de Colombia, garantizando la confidencialidad de los datos de la paciente de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de la paciente y dos testigos. Este documento obra en poder del autor de correspondencia.
REFERENCIAS
1. Buitrago-González TP, Calderón-Ospina CA, Vallejos-Narváez Á. Dipyrone: Benefits underestimated or oversized risks? Review of the literature. Rev Colomb Cienc Quím Farm 2014;43:173-195. [ Links ]
2. Derry S, Faura C, Edwards J, et al. Single dose dipyrone for acute postoperative pain. Cochrane Database Syst Rev 2010;9:CD003227. [ Links ]
3. Koster HT, Avis HJ, Stevens MF, et al. Metamizole in postoperative pain management. Ned Tijdschr Geneeskd 2012;156:A4323. [ Links ]
4. Montoya GA, Vaca C, Parra MF. Adverse events associated with tramadol and dipirona administration in a level III hospital. Biomédica 2009;29:369-381. [ Links ]
5. Salgado P, Suarez-de-la-Rica A, Maseda E, et al. Severe Mucor necrotizing fasciitis associated to dipyrone-induced agranulocytosis. Rev Esp Quimioter 2015;28:58-60. [ Links ]
6. Basak GW, Drozd-Sokolowska J, Wiktor-Jedrzejczak W. Update on the incidence of metamizole sodium-induced blood dyscrasias in Poland. J Int Med Res 2010;38:1374-1380. [ Links ]
7. Arbeláez-Quintero I, Jiménez-Cardozo N. Agranulocytosis risk during use of Dipyrone: a systematic literature review. Salutem Scientia Spiritus 2015;1:19-24. [ Links ]
8. Hamerschlak N, Cavalcanti AB. Neutropenia, agranulocytosis and dipyrone. Sao Paulo Med J 2005;123:247-249. [ Links ]
9. Iskra MP, Membrilla E, Isbert F, et al. Severe sepsis due to cervical abscess after agranulocytosis associated with metamizole. Cir Esp 2015;93:e83-e85. [ Links ]
10. Dorr VJ, Cook J. Agranulocytosis and near fatal sepsis due to ‘Mexican aspirin’ (dipyrone). South Med J 1996;89:612-614. [ Links ]
11. Blaser LS, Tramonti A, Egger P, et al. Hematological safety of metamizole: retrospective analysis of WHO and Swiss spontaneous safety reports. Eur J Clin Pharmacol 2015;71:209-217. [ Links ]
12. AronsonJK. Metamizole (dipyrone) A2 - Meyler’s Side Effects of Drugs. 16th ed. Oxford: Elsevier; 2016; 859-862. [ Links ]
13. Kose N, Akin. PP-216 a case of inferior acute myocardial infarction due to intravenous metamizole use. Int J Cardiol 2013;163 (3 suppl 1):S166. [ Links ]
14. Garcipérez de Vargas FJ, Mendoza J, Sánchez-Calderón P, et al. Cardiogenic shock secondary to metamizole-induced type II Kounis syndrome. Rev Esp Cardiol 2012;65:1138-1139. [ Links ]
15. Redondo-Pachon MD, Enriquez R, Sirvent AE, et al. Acute renal failure and severe thrombocytopenia associated with metamizole. Saudi J Kidney Dis Transpl 2014;25:121-125. [ Links ]
16. Machado-Alba JE, Urbano-Garzón SF, Gallo-Gómez YN, Zuluaica S, Henao Y, Parrado-Fajardo IY. Reacción de anafilaxia grave por dipirona sin antecedente de hipersensibilidad. Informe de caso. Rev Colomb Anestesiol 2017;45:8-11. [ Links ]
17. Stamer UM, Soehle M, Park T-W, et al. Anaphylactic reaction after intravenous dipyrone. Acute Pain 2007;9:221-227. [ Links ]
18. Hedenmalm K, Spigset O. Agranulocytosis and other blood dyscrasias associated with dipyrone (metamizole). Eur J Clin Pharmacol 2002;58:265-274. [ Links ]
19. Ip J, Uetrecht JP. In vitro and animal models of drug-induced blood dyscrasias. Environ Toxicol Pharmacol 2006;21:135-140. [ Links ]
20. Uetrecht JP, Ma HM, MacKnight E, et al. Oxidation of aminopyrine by hypochlorite to a reactive dication: possible implications for aminopyrine-induced agranulocytosis. Chem Res Toxicol 1995;8:226-233. [ Links ]
21. Hargis JB, La Russa VF, Redmond J, et al. Agranulocytosis associated with “Mexican aspirin” (dipyrone): evidence for an autoimmune mechanism affecting multipotential hematopoietic progenitors. Am J Hematol 1989;31:213-215. [ Links ]
22. Ibáñez L, Vidal X, Ballarín E, et al. Agranulocytosis associated with dipyrone (metamizol). Eur J Clin Pharmacol 2005;60:821-829. [ Links ]
23. Busto U, Naranjo CA, Sellers EM. Comparison of two recently published algorithms for assessing the probability of adverse drug reactions. Br J Clin Pharmacol 1982;13:223-227. [ Links ]











 text in
text in