Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347
Rev. colomb. anestesiol. vol.48 no.1 Bogotá Jan./Mar. 2020 Epub Feb 28, 2020
https://doi.org/10.1097/cj9.0000000000000142
Investigaciones clínicas o de laboratorios
Incidencia acumulada y factores de riesgo para náuseas y vómitos posoperatorios en pacientes adultos sometidos a colecistectomía bajo anestesia general balanceada: estudio prospectivo de cohorte
a Servicio de Centro Quirúrgico y Anestesiología, Hospital EsSalud Talara. Piura, Perú.
b Servicio de Enfermería, Hospital EsSalud Talara. Piura, Perú.
c División Médico Legal I Catacaos. Piura, Peni.
Introducción:
Las náuseas y vómitos posoperatorios (NVPO) son problemas comunes que aparecen luego de la anestesia general, para los que se han descrito varios factores independientes de riesgo.
Objetivo:
Determinar la incidencia acumulada de NVPO durante las primeras 24 horas del periodo posoperatorio.
Métodos:
Se realizó un estudio observacional prospectivo de cohorte que incluyó a todos los adultos sometidos a colecistectomía bajo anestesia general balanceada en el Hospital EsSalud Talara desde octubre de 2014 hasta diciembre de 2016. Se evaluó la presencia de NVPO durante las primeras 24 horas posoperatorias y se ejecutaron análisis univariado, bivariado y de regresión logística.
Resultados:
Se incluyeron 244 pacientes, la mayoría con dos factores de riesgo en la escala de Apfel, que presentaron una incidencia acumulada de NVPO de 0.51 (IC 95% 0.45-0.57) en el periodo de observación, a pesar de que el 85.25% recibió profilaxis antiemética. El análisis de regresión logística identificó la presencia de sexo femenino (OR 3.30, IC 95% 1.66-6.55, p = 0.0007) y la historia de NVPO previos o cinetosis (OR 2.67, IC 95% 1.25-5.68, p = 0.011) como factores de riesgo independientes para NVPO. Se halló independencia entre la presencia de profilaxis antiemética y la presencia de NVPO (p=0.92).
Conclusiones:
La alta incidencia acumulada de NVPO pudiera ser ocasionada por el tipo de cirugía, uso de anestésicos volátiles y falencias en la profilaxis farmacológica antiemética.
Palabras clave: Náusea y vómito posoperatorio; Incidencia; Anestesia balanceada; Colecistectomía; Factores de riesgo
Introduction:
Postoperative nausea and vomiting (PONV) are common issues arising after general anesthesia, for which several independent risk factors (RF) have been described.
Objective:
To determine the accumulated incidence of PONV during the first 24hours of the postoperative period.
Methods:
A cohort observational, prospective study was conducted that included all the adults undergoing cholecystectomy under balanced general anesthesia at the EsSalud Talara Hospital from October 2014 until December 2016. The presence of PONV during the first 24hours after surgery was assessed, and univariate, bivariate, and logistic regression analyses were conducted.
Results:
A total of 244 patients were included, most of them with 2 RFs in the Apfel scale, that represented an accumulated incidence of PONV of 0.51 (95% confidence interval [CI] 0.45-0.57) during the observation period, notwithstanding the fact that 85.25% received antiemetic prophylaxis. The logistic regression analysis identified that being a female (odds ratio [OR] 3.30,95% CI 1.66-6.55, P = 0.0007) and previous PONV or motion sickness (OR 2.67, 95% CI 1.25-5.68, P = 0.011) were independent RFs for PONV. The administration of antiemetic prophylaxis and the presence of PONV (P = 0.92) were found to be independent.
Conclusion:
The high cumulative incidence of PONV could be the result of the type of surgery, the use of volatile anesthetic agents, and errors in the antiemetic pharmacological prophylaxis.
Keywords: Postoperative nausea and vomiting; Incidence; Balanced anesthesia; Cholecystectomy; Risk factors
Introducción
Las náuseas y vómitos posoperatorios (NVPO) son problemas comunes que se presentan después de la anestesia general en la unidad de recuperación posanestésica (URPA).1,2 Las investigaciones han permitido reconocer varios factores independientes de riesgo (FR) para NVPO relacionados con el paciente, la anestesia y cirugía.3-5
Las NVPO severos, junto con el despertar intraoperatorio y el dolor posoperatorio, tuvieron una fuerte relación con la insatisfacción de los pacientes después de la anestesia;6 asimismo, los vómitos posoperatorios fueron los resultados menos deseables del periodo posoperatorio, junto con el dolor incisional y las arcadas producidas por el tubo endotraqueal.7
Las NVPO pueden incrementar el costo sanitario, porque prolongan la estancia en URPA y aumentan el reingreso de pacientes posoperados luego del alta en cirugía ambulatoria.8,9 Además, cuando son severas pueden provocar efectos adversos como deshidratación, alteraciones electrolíticas, apertura de incisiones quirúrgicas, sangrado debajo de colgajos de piel, aspiración de contenido gástrico, enfisema mediastínico, enfisema subcutáneo, neumomediastino y neumotórax.10-13
Entre 1936 y 1990 se reportaron incidencias de NVPO en el rango entre el 9% y el 43% en distintas series de casos y revisiones en Europa, Norteamérica y Australia (desde neonatos hasta adultos, tanto hospitalizados como ambulatorios), con el uso de anestesia general inhalatoria (con anestésicos inhalatorios clásicos y modernos), general balanceada, combinada (general y regional), espinal y local.14,15 Sin embargo, otro estudio multicéntrico reportó un rango entre el 39% y el 73% en adultos (la mayoría operados bajo anestesia general y otros con técnicas regionales).16
Los reportes de NVPO en pacientes operados bajo anestesia general son escasos en Latinoamérica, donde se comunicaron incidencias del 10.9%17 y el 15.4%18 en hospitales de Colombia y Cuba, respectivamente. En Brasil, otra investigación informó que el 18.5% de pacientes fueron afectados con náuseas y el 8.5% con vómitos en el periodo posoperatorio.19 En Perú, los estudios descriptivos respecto a NVPO bajo anestesia general son casi inexistentes;20 asimismo, en nuestra institución la mayoría de los pacientes programados para colecistectomía electiva se someten a anestesia general balanceada. Por estos motivos, se desarrolló la presente investigación con el objetivo principal de determinar la incidencia acumulada de NVPO durante las primeras 24 horas del periodo posoperatorio. Los objetivos secundarios fueron determinar los FR implicados, las características de las NVPO, el número de FR de la escala simplificada de Apfel21 presentes en los pacientes y la calidad de la profilaxis antiemética posoperatoria.
Métodos
Población de estudio
Se seleccionaron todos los pacientes adultos desde los 18 años programados para someterse a colecistectomía electiva (convencional y laparoscópica) bajo anestesia general balanceada en el Hospital EsSalud Talara. Para el cálculo de la muestra se ejecutó un estudio piloto (de octubre a diciembre de 2014) que halló una incidencia acumulada de NVPO de 0.3. Así, se obtuvo un tamaño muestral mínimo de 225 pacientes, necesario para obtener la incidencia acumulada de NVPO con una amplitud de intervalo del 12% y con un nivel de confianza del 95%. Además, se consideró un porcentaje de pérdidas del 8%.
Se procedió a seleccionar consecutivamente los pacientes que cumplían con todos los criterios de inclusión y dieron su consentimiento para participar desde enero de 2015 hasta diciembre de 2016. Fueron excluidos todos los pacientes con índice de masa corporal (IMC) mayor de 40kg/m2 (la escala simplificada de Apfel no incluyó pacientes con IMC ≥ 40), con tratamiento antiemético previo, los que solicitaron alta antes de las 24 horas posoperatorias, aquellos con dificultad para responder al interrogatorio por diversas causas y los programados para cirugías electivas distintas de colecistectomía bajo anestesia general.
Fármacos usados en la anestesia
Todos los fármacos usados formaron parte del esquema anestésico habitual del servicio de centro quirúrgico. No se suministró premedicación y se realizó una inducción endovenosa con propofol o midazolam, fentanilo y rocuronio. Se aseguró la vía aérea mediante intubación endotraqueal. El mantenimiento se hizo con sevoflurano o isoflurano. Se realizó reversión del bloqueo neuromuscular con neostigmina (< 2.5 mg) en los pacientes que lo requirieron. Se inició analgesia en el intraoperatorio con metamizol y/o ketoprofeno. La pauta de profilaxis posoperatoria antiemética y analgésica fue elegida y prescrita por el cirujano tratante e iniciada en URPA.
Recolección de datos
Al momento del ingreso a centro quirúrgico se registró mediante anamnesis y revisión de la historia clínica la información concerniente a las siguientes variables: edad, sexo, peso, talla, IMC, cirugía programada, FR de la escala simplificada de Apfel para adultos, puntuación de estado físico de la American Society of Anesthesiology22 e índice de riesgo cardiológico de Goldman. Asimismo, se solicitó el consentimiento de los pacientes. La hora de ingreso a URPA marcó el inicio del periodo de observación de 24 horas. Se registraron la duración de la anestesia y pauta de profilaxis farmacológica antiemética prescrita en la historia clínica.
Evaluación de NVPO
Se realizó al finalizar el periodo de observación. La presencia de los distintos eventos de NVPO [náuseas sin vómito (N), náuseas acompañadas de vómito (NV) y episodios de vómito no precedido de náuseas (VSN)] se evaluó mediante el interrogatorio de los pacientes, usando un lenguaje sencillo y explicativo para tratar de disminuir la presencia de sesgo de memoria.
Las náuseas fueron definidas como el deseo de vomitar sin la presencia de movimientos musculares expulsivos,15 y el vómito como la expulsión oral enérgica de contenido gastrointestinal.15 El episodio donde no se expulsó contenido gástrico se denominó arcada15 y fue considerado vómito en este estudio. Asimismo, arcadas y vómitos fueron agrupados bajo el término de episodios eméticos (EE).23
Para la evaluación de náuseas (pacientes con N y NV) se utilizó una escala visual análoga (EVA) de 10 centímetros, donde 0 representó su ausencia y 10 la peor sensación de náuseas experimentada.24 Así, los pacientes expresaron una puntuación global de las náuseas experimentadas durante el periodo de observación. En el caso de los vómitos, se cuantificó el número de episodios21 (pacientes con NV y VSN).
La evaluación de la calidad en profilaxis antiemética se evaluó mediante las variables de presencia de profilaxis antiemética y presencia de terapia profiláctica ajustada, según los FR de la escala de Apfel presentes en el paciente. Para evaluar este ajuste se usó un esquema descrito por Apfel en el que los antieméticos se prescribían según el número de FR presentes en los pacientes hospitalizados, incluyendo asociaciones farmacológicas y la posibilidad o no de suministrar terapia total endovenosa.3
Métodos estadísticos
Los análisis estadísticos fueron realizados con los programas StatCrunch y StatsDirect3. En caso de tener más del 5% de datos faltantes, se planeó utilizar un método de imputación múltiple. Se ejecutaron los correspondientes análisis univariante y bivariante, incluyendo un análisis de normalidad de las variables numéricas (edad, peso, talla, IMC, duración de la anestesia) mediante la prueba de Kolmogorov-Smirnov con corrección de Lilliefors, con la finalidad de seleccionarlas correspondientes pruebas paramétricas y no paramétricas. Las pruebas estadísticas en el análisis bivariante incluyeron el cálculo de los coeficientes de correlación de Spearman, pruebas de Chi cuadrado, pruebas de Mann-Whitney y pruebas T de Student. Finalmente, se procedió a realizar una regresión logística binaria para la construcción de un modelo de asociación según la identificación de variables con significancia estadística y clínica. Luego, para la obtención del modelo ajustado, se procedió a eliminar las variables no relevantes, buscar la presencia de factores de confusión, comprobar la bondad de ajuste y realizar un análisis de residuos.
Aspectos éticos
El estudio se rigió por los principios éticos de la Declaración de Helsinki, por lo que los pacientes expresaron su consentimiento para la participación en la investigación, y la guía STROBE para el reporte de investigaciones observacionales. La base de datos clínicos fue confidencial, no pudiendo divulgarse ninguna información de los participantes, salvo autorización expresa. Asimismo, el protocolo del estudio fue aprobado por la dirección del hospital.
Resultados
Se incluyeron 248 pacientes, sin llegar a evaluar a 4 (1.6%), por lo que el número total de pacientes evaluados para la presencia de NVPO ascendió a 244 (su inclusión y exclusión se detallan en la Figura 1). El 77.9% fueron mujeres, tuvieron una mediana de 44 años y una media de IMC de 27.2 kg/m2 (ver características basales en la Tabla 1).
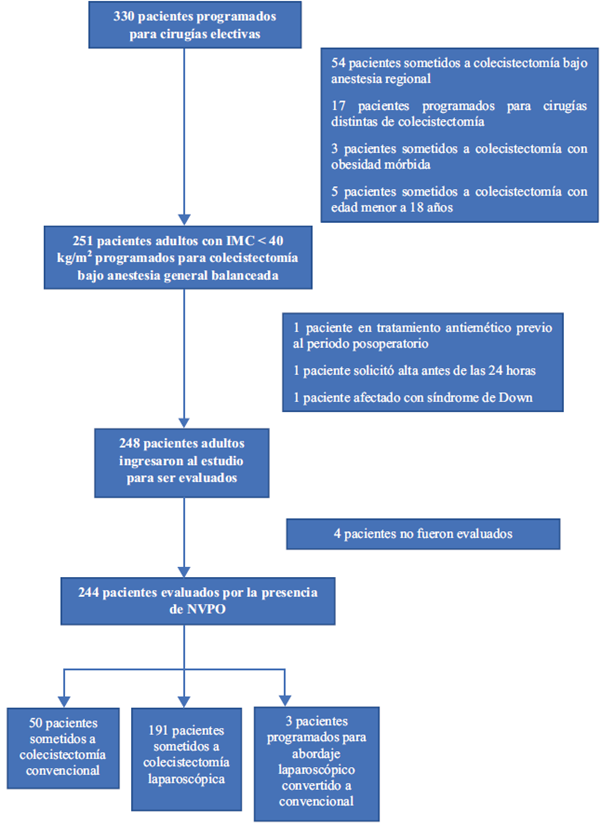
Fuente: Autores.
Figura 1 Diagrama de flujo de inclusión y exclusión de los pacientes de la investigación. IMC= Índice de Masa Corporal, NVPO= Náuseas y vómitos posoperatorios
Tabla 1 Características de referencia de los pacientes.
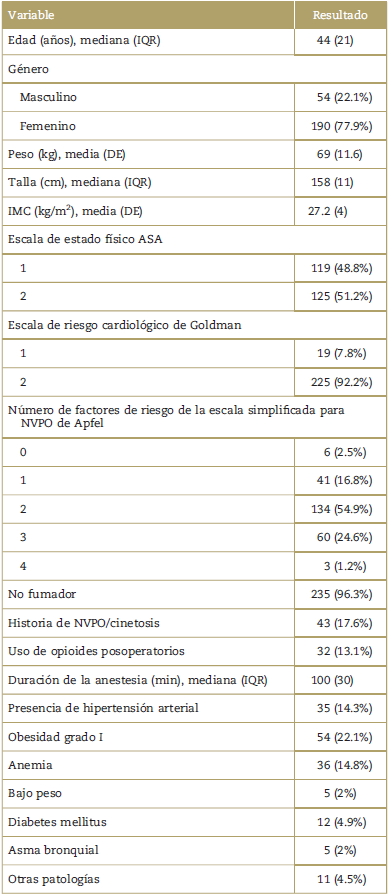
Todos los números expresan número de pacientes y porcentajes (%) a menos que se especifique lo contrario. ASA=American Society of Anesthesiologists, DE =Desviación estándar, IQR=Rango intercuartílico, NVPO = Náuseas y vómitos posoperatorios. Otras patologías: hipotiroidismo, migraña, dislipidemia, enfermedad coronaria crónica y artritis reumatoide.
Fuente: Autores.
Análisis descriptivo y univariado
Durante el periodo de observación, 124 pacientes presentaron NVPO, lo cual representó una incidencia acumulada de 0.51 [IC 95% 0.45-0.57] en 24 horas. Los diferentes tipos de NVPO se encuentran detallados en la Figura 2.
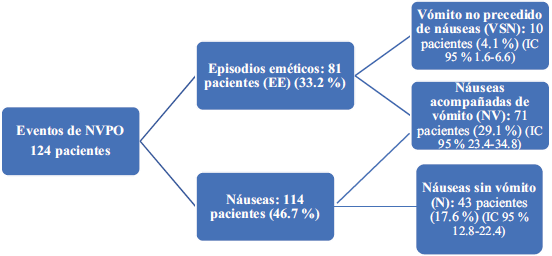
Fuente: Autores.
Figura 2 Tipos de evento de NVPO. Nota: Los porcentajes se expresan respecto a la totalidad de la población de estudio (244 pacientes).
Respecto al número de EE presentados, se halló que 63 pacientes (25.82%) sufrieron entre uno y cuatro EE, 15 (6.15%) entre cinco y ocho EE y 3 (1.23%) más de ocho EE. Asimismo, respecto a la intensidad de las náuseas (pacientes afectados con N y NV), 41 (16.8%) expresaron una puntuación entre 1 y 4, el mismo numero una puntuación de 5 a 7 y 32 (13.11%) de 8 a 10 puntos en la EVA.
Con respecto a la profilaxis farmacológica antiemética (Tabla 2), se encontró que la mayoría de los pacientes la recibieron durante el periodo posoperatorio (85.25%), pero solo 42 (17.21%) recibieron una profilaxis ajustada a los FR presentes en el paciente.3 Se utilizó metoclopramida en 203 (83.2%) y dimenhidrinato en 5 (2.05%) (un paciente recibió ambos antieméticos). Respecto a los pacientes afectados con NVPO (124), se evidenció que el 85.5% recibieron profilaxis antiemética, pero solamente el 12.1% recibieron terapia de rescate (que no estuvo prescrita en las indicaciones posoperatorias en ningun caso). Asimismo, se apreció que 135 pacientes (55.33%) presentaban dos FR en la escala simplificada para NVPO de Apfel. Además, se muestra el porcentaje de casos incidentales de NVPO para los pacientes que tuvieron 0, 1, 2, 3 y 4 FR (16.67%, 24.39%, 51.11%, 71.19% y 66.67%, respectivamente).
Tabla 2 Pacientes afectados con NVPO segun el numero de factores de riesgo de la escala simplificada de Apfel y presencia de profilaxis farmacológica antiemética.
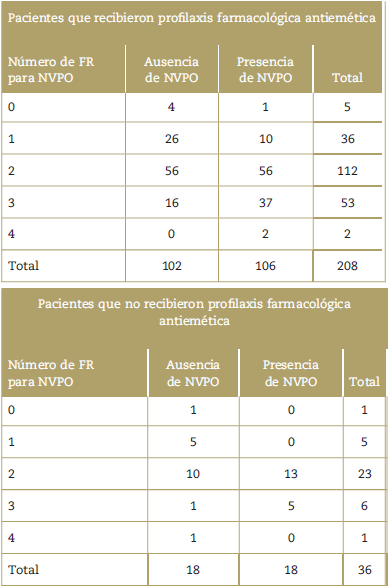
FR=Factores de riesgo, NVPO=Náuseas y vómitos posoperatorios.
Fuente: Autores.
También se realizó un análisis de normalidad de las variables cuantitativas que permitió identificar que las variables peso e IMC siguieron una distribución normal.
Análisis bivariado
Los valores de los coeficientes de Spearman entre las variables de duración de la anestesia e intensidad de náuseas y numero de EE mostraron valores muy débiles de correlación. Asimismo, la prueba de homogeneidad de la incidencia acumulada de NVPO en los pacientes sometidos a colecistectomía convencional, respecto a la de los pacientes sometidos a laparoscópica, no fue significativa (p = 0.065, OR 1.78 IC 95% 0.96-3.31).
Las variables que presentaron asociación con la presencia de NVPO (cualquier tipo de evento) fueron género femenino, historia de NVPO o cinetosis y presencia de terapia profiláctica ajustada segun los FR de la escala de Apfel presentes en el paciente (Tabla 3). Las variables que presentaron asociación con la presencia de náuseas (pacientes afectados con N y NV) fueron sexo femenino (p <0.001, OR 4.63 IC 95% 2.25-9.52), historia de NVPO o cinetosis (p < 0.001, OR 4.22 IC 95% 2.01-8.85) y presencia de terapia profiláctica ajustada (p=0.0003, OR 0.25 IC 95% 0.11-0.55). Para el caso de presencia de EE (pacientes afectados con NV y VSN), hubo significación estadística con sexo femenino (p < 0.001, OR 8.52 IC 95% 2.95-24.56), ausencia de tabaquismo (p=0.03), historia de NVPO o cinetosis (p < 0.001, OR 4.06 IC 95% 2.05-8.06) y presencia de terapia profiláctica ajustada (p=0.0003, OR 0.17 IC 95% 0.06-0.50).
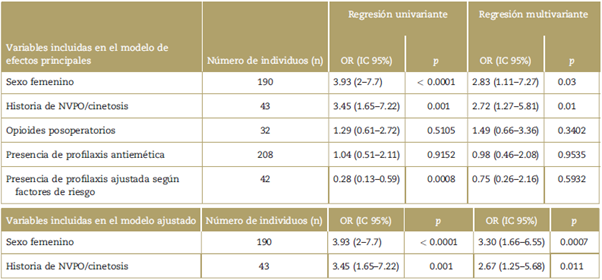
Tabla 3 Variables independientes y su asociación con la variable dependiente presencia de NVPO.
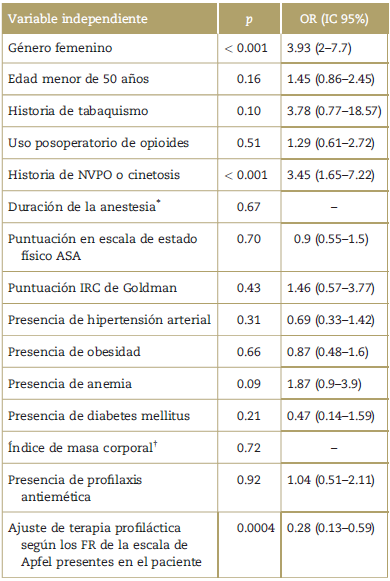
Todas las pruebas de significación estadística se realizaron con la prueba de Chi cuadrado a menos que se especifique lo contrario.
* Prueba U de Mann-Whitney.
† Prueba t de Student. ASA=American Society of Anesthesiologists, IC = Intervalo de confianza, IRC = Índice de riesgo cardiaco, NVPO=Náuseas y vómitos posoperatorios, OR=Odds ratio.
Fuente: Autores.
La variable presencia de NVPO no tuvo asociación con presencia de profilaxis antiemética, pero sí con la variable presencia de terapia profiláctica ajustada (Tabla 3).
Análisis multivariado
Se realizó un análisis de regresión logística binaria (Tabla 4), construyéndose un modelo de efectos principales con las variables con significación estadística en el análisis bivariante (sexo femenino, historia de NVPO/cinetosis y presencia de profilaxis ajustada según FR) y aquellas con alta importancia clínica (uso de opioides posoperatorios y presencia de profilaxis antiemética) para la presencia de NVPO. A partir de este modelo de mayor complejidad, se eliminaron las variables no relevantes por no estar asociadas con el desenlace ni ser factores de confusión para obtener un modelo más más ajustado al principio de parsimonia o principio de economía. Luego se calculó la prueba de bondad de ajuste de Hosmer-Lemeshow, que tuvo un valor p no significativo (0.6155) y mostró falta de disparidad entre las casillas de resultados observados y esperados. Finalmente, se hizo un análisis de residuos (Pearson, Pearson estandarizado, Deviance) que no mostró datos atípicos.
Discusión
En la presente investigación se encontró una alta incidencia acumulada de NVPO en las primeras 24 horas del periodo posoperatorio, hecho que puede tener varias causas. En primer lugar, debido al uso de anestésicos volátiles para la anestesia general suministrada.5 En segundo lugar, por el tipo de cirugía realizada, que fue colecistectomía (laparoscópica en el 78.28% de pacientes y convencional en el 21.72%). En investigaciones previas en pacientes sometidos a estas cirugías se reportaron también incidencias significativas. Así, una revisión sistemática reportó una OR combinada ajustada de 1.9 (1.36-2.68) proveniente de cuatro investigaciones en pacientes sometidos a colecistectomía; la misma también halló una OR combinada de 1.37 (1.071.77) en ocho investigaciones de pacientes sometidos a cirugía laparoscópica.4 Otras dos investigaciones en pacientes que recibieron colecistectomía laparoscópica Reportaron una incidencia del 69% con una OR ajustada de 3.23 (1.55-6.74) en la primera,25 y una OR de 2.85 (1.4-5.81) en la segunda.26 Por los hallazgos descritos, aunque la mayoría de los tipos de cirugía no mostraron ser predictores independientes para NVPO, se consideró una excepción para las colecistectomías laparoscópicas y también los procedimientos ginecológicos.3
Existen investigaciones previas que reportaron incidencias mucho menores de NVPO en el mismo periodo de observación (en pacientes hospitalizados y ambulatorios que recibieron anestesia general), lo que probablemente se debió a que recibieron distintos tipos de cirugías (no exclusivamente cirugía laparoscópica o colecistectomía).18,27,28 Asimismo, investigaciones anteriores que incluyeron tipos de anestesia distintos de anestesia general también informaron incidencias acumuladas menores,17,19,29 con una excepción en la cual no se permitió el suministro de profilaxis farmacológica a los pacientes.30 Por otra parte, un estudio peruano reportó incidencias acumuladas de NVPO de 0.24 y 0.14 en colecistectomía laparoscópica y convencional, respectivamente; sin embargo, fue de tipo retrospectivo, lo cual pudo haber causado un subregistro de NVPO.20
Otra causa para la alta incidencia hallada serían las deficiencias en la profilaxis antiemética, pues si se analiza la totalidad de pacientes que la recibieron, se puede apreciar que 113, 53 y 2 pacientes tenían 2, 3 y 4 FR para NVPO en la escala de Apfel, respectivamente. A pesar de lo anterior, casi la totalidad recibió profilaxis con un único fármaco, lo cual dista del abordaje multimodal adaptado al riesgo (de acuerdo con la cantidad de FR presentes en el paciente) con el uso de combinaciones de fármacos y la disponibilidad de anestesia total intravenosa.3 Asimismo, la evaluación preoperatoria del riesgo de NVPO y la creación de una guía de tratamiento adaptada al contexto local han sido recomendados de forma reciente.31
La mayoría de los pacientes recibieron profilácticamente 10 mg de metoclopramida, dosis que fue efectiva en cesáreas bajo anestesia neuroaxial;32 pero otra revisión no la consideró efectiva para reducir la incidencia de NVPO.33 Además, los pacientes que recibieron profilaxis antiemética con dimenhidrinato no recibieron la dosis recomendada (1mg/kg IV).33
El sexo femenino y la presencia de NVPO en cirugía previa o cinetosis constituyeron FR para NVPO en los pacientes de nuestra institución. Una limitación del estudio es que la ausencia de tabaquismo no pudo ser evaluada como FR, porque solo 9 pacientes (3.7%) eran fumadores, lo cual dificultó considerarlo dentro del análisis de regresión logística, pues un bajo número de eventos por variable puede causar problemas en el modelo logístico.34 La pequeña cantidad de fumadores pudiera ser producto del bajo consumo de cigarrillos35 y la tendencia decreciente de la prevalencia de tabaquismo en las últimas décadas en Peru.36 Lo anterior implicaría, para futuras investigaciones, considerar una mayor población de estudio o una con mayor prevalencia de tabaquismo.
El uso de opioides posoperatorios no fue FR en nuestra institución, donde se suministraron dosis bajas de tramadol a 32 pacientes (13.11%). El 65.63% de los mencionados recibieron el fármaco BID (dos veces al día, del latino bis in dei), el 18.75% en única ocasión y el 15.63% TID (tres veces al día, del latino ter in dei); y en ningún caso se alcanzó ni superó la dosis máxima recomendada para adultos y adolescentes (400mg/día).37 En el mismo sentido, el estudio de validaciones cruzadas en dos hospitales de la escala de Apfel comunicó que este FR pudiera ser cuestionable, ya que fue significativo solamente en un centro, en el cual se usaron dosis más altas (20 mg de oxicodona vs. 100mg de tramadol), y en la mayor parte de los pacientes (80% vs. 10%) en comparación con la otra institución.21
En términos de validez interna los pacientes del estudio que constituyeron la muestra fueron enrolados de forma continua e ininterrumpida. Sin embargo, a pesar de las medidas usadas en la anamnesis, pudiera haber existido un sesgo de memoria debido a que ciertos pacientes ya habían sufrido NVPO en cirugías previas, los cuales habrían reportado con mayor precisión las características del evento adverso, a diferencia de aquellos pacientes que no lo padecieron. Finalmente, en relación con su validez externa, los resultados del estudio pudieran ser generalizables a pacientes adultos sometidos a colecistectomía realizada con anestesia general balanceada en otras instituciones sanitarias. Sin embargo, no pueden ser extrapolados hacia pacientes que reciban anestesia distinta de anestesia general, pacientes pediátricos ni adolescentes.
Como recomendaciones se resaltan: 1) implementar la valoración mediante una escala del riesgo de NVPO en la consulta anestésica preoperatoria; 2) creación de una guía local hospitalaria para asignar esquemas farmacológicos profilácticos y de rescate según el riesgo para presentar NVPO, y 3) consignación de estos esquemas en las indicaciones posoperatorias inmediatas.
Conclusiones
En este estudio se halló una alta incidencia acumulada de NVPO en pacientes adultos sometidos a colecistectomía bajo anestesia general balanceada, la mayoría de los cuales tenían dos FR de la escala de Apfel. Los eventos adversos tipo NVPO más frecuentes fueron los vómitos acompañados de náuseas. Los FR para NVPO fueron el sexo femenino y la historia de NVPO previos o cinetosis. La profilaxis farmacológica antiemética presentó falencias respecto a las dosis y su ajuste respecto al riesgo; asimismo, solo un escaso número de pacientes afectados recibieron terapia antiemética de rescate, pues no fue prescrita dentro de las indicaciones posoperatorias.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Agradecimientos
Asistencia para el estudio. Los autores desean agradecer a la Licenciada Lourdes Alvinez Fernández, que colaboró en la recolección de datos, y a la Sra. Dora Villar Chunga, encargada del archivo de historias clínicas del Hospital EsSalud Talara.
REFERENCIAS
1. Dolin SJ, Cashman JN. Tolerability of acute postoperative pain management: nausea, vomiting, sedation, pruritis, and urinary retention. Evidence from published data. Br J Anaesth 2005;95:584-591. [ Links ]
2. Hines R, Barash PG, Watrous G, et al. Complications occurring in the postanesthesia care unit: a survey. Anesth Analg 1992;74:503-509. [ Links ]
3. Apfel CC. Miller RD, Cohen NH, Eriksson LI, et al. Postoperative nausea and vomiting. Miller’s anesthesia 8th ed.Canada: Elsevier-Saunders; 2015. [ Links ]
4. Apfel CC, Heidrich FM, Jukar-Rao S, et al. Evidence-based analysis of risk factors for postoperative nausea and vomiting. Br J Anaesth 2012;109:742-753. [ Links ]
5. Veiga-Gil L, Pueyo J, López-Olaondo L. Postoperative nausea and vomiting: physiopathology, risk factors, prophylaxis and treat-ment. Rev Esp Anestesiol Reanim 2017;64:223-232. [ Links ]
6. Myles PS, Williams DL, Hendrata M, et al. Patient satisfaction after anaesthesia and surgery: results of a prospective survey of 10,811 patients. Br J Anaesth 2000;84:6-10. [ Links ]
7. Macario A, Weinger M, Carney S, et al. Which clinical anesthesia outcomes are important to avoid? The perspective of patients. Anesth Analg 1999;89:652-658. [ Links ]
8. Fortier J, Chung F, Su J. Unanticipated admission after ambulatory surgery-a prospective study. Can J Anaesth 1998;45:612-619. [ Links ]
9. Gold BS, Kitz DS, Lecky JH, et al. Unanticipated admission to the hospital following ambulatory surgery. JAMA 1989;262:3008-3010. [ Links ]
10. Palazzo MG, Strunin L. Anaesthesia and emesis. I: Etiology. Can Anaesth Soc J 1984;31:178-187. [ Links ]
11. Forrest JB, Cahalan MK, Rehder K, et al. Multicenter study of general anesthesia. II. Results. Anesthesiology 1990;72:262-268. [ Links ]
12. Schumann R, Polaner D. Massive subcutaneous emphysema and sudden airway compromise after postoperative vomiting. Anesth Analg 1999;89:796-797. [ Links ]
13. Bremner WG, Kumar CM. Delayed surgical emphysema, pneumomediastinum and bilateral pneumothoraces after postoperative vomiting. Br J Anaesth 1993;71:296-297. [ Links ]
14. Waters RW. Present status of cyclopropane. Br Med J 1936;2:1013-1017. [ Links ]
15. Watcha MF, White PF. Postoperative nausea and vomiting. Its etiology, treatment, and prevention. Anesthesiology 1992;77:162-184. [ Links ]
16. Cohen MM, Duncan PG, DeBoer DP, et al. The postoperative interview: assessing risk factors for nausea and vomiting. Anesth Analg 1994;78:7-16. [ Links ]
17. Gempeler Rueda FE, Miranda Pineda N, Garrido Hartmann A, et al. Incidence of Postoperative Nausea and Vomiting and Associated Factors in Hospital Universitario San Ignacio. Universitas Médica 2016;57:11-21. [ Links ]
18. Pérez CD, Nieto MCG. Náuseas y vómitos postoperatorios en anestesia general para intervención quirurgica electiva. Acta Med Cent 2017;11:39-48. [ Links ]
19. Patti CA, Vieira JE, Benseñor FE. Incidence and prophylaxis of nausea and vomiting in post-anesthetic recovery in a tertiary teaching hospital. Rev Bras Anestesiol 2008;58:466-469. 462-466. [ Links ]
20. Egoavil Santana JC, Ruiz Portilla S. Náuseas y vómitos postoperatorios en pacientes sometidos a colecistectomía laparoscópica vs. colecistectomía abierta en el Hospital Nacional Ramiro Prialé Prialé durante el año 2011”. Thesis Huancayo: Repositorio de la Universidad Nacional del Centro del Peru; 2012. [ Links ]
21. Apfel CC, Láárá E, Koivuranta M, et al. A simplified risk score for predicting postoperative nausea and vomiting: conclusions from cross-validations between two centers. Anesthesiology 1999;91:693-700. [ Links ]
22. Wijeysundera DN, Sweitzer BJ. Miller RD, Cohen NH, Eriksson LI, et al. Preoperative evaluation. Miller’s anesthesia 8th ed.Canada: Elsevier-Saunders; 2015. [ Links ]
23. Apfel CC, Roewer N, Korttila K. How to study postoperative nausea and vomiting. Acta Anaesthesiol Scand 2002;46:921-928. [ Links ]
24. Boogaerts JG, Vanacker E, Seidel L, et al. Assessment of postoperative nausea using a visual analogue scale. Acta Anaesthesiol Scand 2000;44:470-474. [ Links ]
25. Apfel CC, Kranke P, Eberhart LH. Comparison of surgical site and patient’s history with a simplified risk score for the prediction of postoperative nausea and vomiting. Anaesthesia 2004;59:1078-1082. [ Links ]
26. Apfel CC, Kranke P, Eberhart HJ, et al. Comparison of predictive models for postoperative nausea and vomiting. Br J Anaesth 2002;88:234-240. [ Links ]
27. Habib AS, Chen YT, Taguchi A, et al. Postoperative nausea and vomiting following inpatient surgeries in a teaching hospital: a retrospective database analysis. Curr Med Res Opin 2006;22:1093-1099. [ Links ]
28. Doubravska L, Dostalova K, Fritscherova S, et al. Incidence of postoperative nausea and vomiting in patients at a university hospital. Where are we today? Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2010;154:69-76. [ Links ]
29. Moreno C, Veiga D, Pereira H, et al. Postoperative nausea and vomiting: incidence, characteristics and risk factors-a prospective cohort study. Rev Esp Anestesiol Reanim 2013;60:249-256. [ Links ]
30. Morino R, Ozaki M, Nagata O, et al. Incidence of and risk factors for postoperative nausea and vomiting at a Japanese Cancer Center: first large-scale study in Japan. J Anesth 2013;27:18-24. [ Links ]
31. De Hert S, Staender S, Fritsch G, et al. Pre-operative evaluation of adults undergoing elective noncardiac surgery. EurJ Anaesthesiol 2018;35:407-465. [ Links ]
32. Cao X, White PF, Ma H. An update on the management of postoperative nausea and vomiting. J Anesth 2017;31:617-626. [ Links ]
33. Gan TJ, Diemunsch P, Habib AS, et al. Consensus guidelines for the management of postoperative nausea and vomiting. Anesth Analg 2014;118:85-113. [ Links ]
34. Peduzzi P, Concato J, Kemper E, et al. A simulation study of the number of events per variable in logistic regression analysis. J Clin Epidemiol 1996;49:1373-1379. [ Links ]
35. Morgan BW, Leifheit KM, Romero KM, et al. Low cigarette smoking prevalence in peri-urban Peru: results from a population-based study of tobacco use by self-report and urine cotinine. Tob Induc Dis 2017;15:32. [ Links ]
36. Comisión Nacional para el Desarrollo y Vida sin Droga- DEVIDA Estrategia Nacional de Lucha contra las Drogas 2017-2021. Lima: Editorial Super Gráfica. 2017. [Cited 2018 Nov 16]. Disponible at: http://www.devida.gob.pe/documents/20182/314196/Estrategia_FINAL_castellano2.pdf. [ Links ]
37. Scott LJ, Perry CM. Tramadol: a review of its use in perioperative pain. Drugs 2000;60:139-176. [ Links ]
Cómo citar este artículo: Shiraishi-Zapata CJ, Arellano-Adrianzén SJ, Rodríguez-Velarde GJ. Cumulative incidence and risks factors for postoperative nausea and vomiting in adult patients undergoing Cholecystectomy under balanced general anesthesia: a prospective cohort study. Colombian Journal of Anesthesiology. 2020;48:3-11.
Copyright © 2019 Sociedad Colombiana de Anestesiología y Reanimación (S.C.A.R.E.). Published by Wolters Kluwer. This is an open access article under the CC BY-NC-ND license (https://creativecommons.org/licenses/by-nc-nd/4.0/).











 text in
text in