Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Colombian Journal of Anestesiology
versión impresa ISSN 0120-3347versión On-line ISSN 2256-2087
Rev. colomb. anestesiol. vol.50 no.4 Bogotá oct./dic. 2022 Epub 04-Nov-2022
https://doi.org/10.5554/22562087.e1031
REVISIÓN NARRATIVA
Lactancia materna y anestesia
a Departamento de Anestesiología, Universidad de Valparaíso. Valparaíso, Chile.
b Departamento de Anestesiología, Pontificia Universidad Católica de Chile. Santiago, Chile.
La lactancia materna tiene evidentes beneficios para el binomio maternofetal. El anestesiólogo debe ser un agente en la promoción de la lactancia, estar dispuesto a resolver dudas en el preoperatorio y elaborar un plan que no interfiera con su seguridad. Hay preocupación referente a la transferencia de los medicamentos (endovenosos y/o neuroaxiales) hacia la leche, que puede conducir a un consejo inconsistente de muchos profesionales de la salud, lo cual contribuye a la suspensión temprana de la lactancia materna. Sin embargo, existe evidencia de que la mayoría de los medicamentos que se utilizan en la anestesia (general y neuroaxial) son compatibles con la lactancia materna. Se debe iniciar la lactancia materna después de la anestesia tan pronto como la madre esté alerta y se sienta bien, sin necesidad de extraerla y eliminarla. Esta revisión entrega información farmacocinética sobre los medicamentos y técnicas anestésicas comúnmente utilizadas para que los profesionales realicen un balance riesgo-beneficio con la madre, enfatizando que la anestesia no debe interferir con los beneficios de la lactancia. Se presentan cuatro escenarios clínicos prácticos: embarazada preocupada por el efecto de la analgesia peridural en su lactancia posterior, anestesia raquídea para cesárea y efecto en lactancia, pacientes que requieren anestesia general para cesárea y, por último, paciente puérpera que requiere anestesia para cirugía. Las técnicas neuroaxiales permiten un mejor control del dolor y contacto piel con piel precoz en el parto vaginal o cesárea, lo que facilita que la madre inicie la lactancia más rápido. Si el escenario lo permite, se prefieren técnicas regionales, técnicas ahorradoras de opioides y cirugía ambulatoria, teniendo precaución con ciertos opioides y benzodiacepinas de acción larga especialmente ante dosis repetidas.
Palabras clave: Lactancia materna; Cirugía; Anestesia; Evaluación preoperatoria; Leche materna; Anestesia obstétrica; Anestesiología
The importance of breastfeeding with its positive impact on the wellbeing of the mother-infant pair is well established. Anesthesiologists should encourage the promotion of lactation by being willing to give reassurance during the preoperative period and preparing a plan that does not interfere with safe breastfeeding. There is concern regarding the transfer of drugs into breast milk, which may lead to inconsistent advice from many health professionals and to early discontinuation. However, evidence shows that most anesthetic drugs are safe in terms of transfer into breast milk, and hence, compatible with breastfeeding, which should be resumed after anesthesia as soon as the mother is alert and feels well enough to hold her infant, without the need to "pump and dump". This review provides pharmacokinetic information on commonly used anesthesia drugs and their passage into breast milk, to help practitioners discuss risks and benefits with the mother, emphasizing that anesthesia should not interfere with the benefits of breastfeeding. Four practical clinical scenarios are presented: pregnant women concerned about the effect of epidural analgesia on subsequent breastfeeding, spinal anesthesia for c-section and lactation, patients who will receive general anesthesia during cesarean section, and finally women who are breastfeeding and require anesthesia for elective or urgent surgery. Neuraxial anesthesia allows for better pain control and immediate skin-to-skin contact at the time of childbirth. Also, it interferes the least with the woman's ability to care for her infant. Regional techniques, opioid-sparing techniques and outpatient surgery are preferred. Drugs such as opioids and longer-acting benzodiazepines should be administered cautiously, particularly in repeat doses.
Key words: Breastfeeding; Anesthesia; Preoperative assessment; Surgery; Breastmilk; General anesthesia; Obstetric anesthesia; Anesthesiology
INTRODUCCIÓN
La Semana Mundial de la Lactancia Materna, que se celebra en agosto de cada año, tuvo como lema para 2021 proteger la lactancia materna, reforzando que es una tarea de todos. Esta celebración se originó en la conmemoración de la firma de la Declaración de Innocenti realizada en 1990, la cual declara la protección, fomento y apoyo de la lactancia materna en los distintos países del mundo 1.
La Organización Mundial de la Salud (OMS) y el Fondo de las Naciones Unidas para la Infancia (UNICEF) recomiendan que la lactancia materna comience idealmente dentro de la primera hora de vida, se mantenga en forma exclusiva hasta los 6 meses y luego se complemente con alimentos hasta los 2 años de vida 2,3. Sin embargo, mientras que cerca del 96 % de las madres comienza lactando, solo un 39 % y 15 % continúa con lactancia materna exclusiva (LME) a los 3 y 5 meses, respectivamente. La mayoría de ellas la suspende en las primeras 6 semanas, destacando entre las principales razones: disminución producción de leche o "lactante insatisfecho" (27,2 %), problemas de pezón o succión (14,7 %) y reinicio de actividades laborales/estudiantiles de la madre (10,4 %) 4,5.
A escala global, la prevalencia de LME al sexto mes bordea el 40 % 3. En Latinoamérica, fluctúa entre un 24-68 %, destacando Perú y Bolivia con cifras superiores al 60 %, siguiendo con Chile (43 %), Colombia (36 %), Brasil (35 %) y Paraguay (24 %) 5 . La OMS plantea como meta mundial para 2025 que al menos el 50 % de los niños reciban lactancia materna exclusiva hasta los 6 meses 3.
La leche materna entrega todos los requerimientos nutricionales e inmunitarios del neonato, lo protege contra las infecciones, favorece el vínculo afectivo con la madre y reduce el riesgo de muerte súbita, obesidad y diabetes. Para la madre, la lactancia materna tiene un papel preventivo en el cáncer de mama y probablemente de ovario 6. Desde el punto de vista económico, constituye el alimento más completo y costo-efectivo, que favorece la prevención de posibles causas de morbimortalidad infantil en todos los estratos socioeconómicos 7,8. El riesgo de mortalidad es 14 veces mayor en lactantes que no recibieron LME 9. Según el metaanálisis de Victora et al. la escalada de lactancia materna a un nivel más amplio puede prevenir cerca de 823.000 muertes al año en niños menores de 5 años y 20.000 muertes al año por cáncer de mama 6.
Viendo estas cifras estadísticas, es importante poder dar un consejo acertado sobre la seguridad de muchos fármacos, para promover una lactancia exitosa y sin interrupciones. El contacto con la atención médica puede ser un factor de riesgo para el destete temprano, ya que actualmente el consejo que recibe la madre es variable e inconsistente, resultando en la postergación del inicio de la lactancia por 24-48 horas, extracción y eliminación de la leche materna debido a los posibles efectos adversos de las drogas que se transfieren por ella 10. Por lo anterior, resulta de extrema importancia que los funcionarios de salud se alineen todos en pos de promover una LME exitosa.
El objetivo de este trabajo es realizar una revisión no sistemática en relación con la lactancia materna y los medicamentos utilizados en la anestesia, tanto en el intra/postoperatorio como en el parto/posparto, con el fin elaborar una serie de recomendaciones y asegurar que los anestesiólogos tengan los conocimientos necesarios para ayudar a las mujeres que van a amamantar, y evitar las interrupciones de esta.
REVISIÓN DE LA EVIDENCIA
Se hizo una búsqueda de reportes en las bases de datos PubMed (Medline), Google scholar, SciELO, Embase y Cochrane Library utilizando los términos: "breastfeeding", "anesthesia", "epidural anesthesia", "breastmilk", "preoperative assment" y "surgery". El idioma de la búsqueda se restringió a inglés y español. De manera concomitante, se incluyeron fuentes de lactancia específicas como UK Drugs in Lactation Advisory Service (UKDILAS) 11, Drugs and Lactation Database (LactMed) 12 , E-lactancia 13, referencias de artículos seleccionados y literatura gris. Mediante esta búsqueda estructurada se obtuvo un resultado de 293 artículos. Luego de su análisis por ambos autores, se excluyeron aquellos que no ofrecían información relevante, artículos duplicados, texto completo no disponible y artículos publicados hace más de 20 años. Finalmente, se identificaron 51 artículos con información relevante para el desarrollo de esta revisión.
DESARROLLO
Rol del anestesiólogo como promotor de la lactancia materna
El anestesiólogo forma parte activa del equipo quirúrgico. Sus funciones en el ámbito de promoción de la lactancia son:
• Establecer una comunicación anticipada con la madre, resolver dudas preoperatorias referentes a la analgesia en el trabajo de parto o la anestesia en la cesárea y explicarle las ventajas de la lactancia materna. Así como generalmente muchos anestesió-logos aprovechan la evaluación preanestésica como consejería antitabaco, se podría incentivar que las madres tengan contacto piel con piel, particularmente en la cesárea, donde muchas veces se difiere, lo que afecta la satisfacción materna y eventualmente la lactancia 14.
• Consignar en la evaluación preanestésica el antecedente de lactancia materna en toda paciente femenina con hijos menores de 2 años. Este antecedente rara vez se considera y se menciona antes de una cirugía.
• Realizar un plan anestésico para una paciente puérpera que permita otorgar condiciones quirúrgicas adecuadas y, al mismo tiempo, permita la continuación de la lactancia, privilegiando el tipo de anestesia que menos interfiera. En este sentido, se prefieren técnicas neuroaxiales en comparación con la anestesia general.
• Otorgar una adecuada analgesia postoperatoria y prevenir las náuseas y vómitos postoperatorios (NVPO). Madres con mal manejo de dolor postoperatorio y vómitos, tendrán más dificultades en proveer lactancia materna 15,16.
• Identificar y tratar precozmente la hipotensión arterial posterior a la raquídea y cefalea pospunción, las cuales pueden interferir con una lactancia materna efectiva 17.
• Fomentar el contacto piel con piel inmediato en cesárea.
• Discutir un plan revisado por expertos en almacenamiento de leche materna en el caso de que la cirugía se prolongue o si el lactante no puede permanecer con la paciente.
Las madres deben conocer el riesgo de no lactar, que incluyen obstrucción de ductos mamarios (mastitis), exposición a fórmula artificial en un niño alérgico, inhabilidad del lactante de alimentarse por biberón y riesgo de enterocolitis necrotizante en lactantes prematuros, si el pecho materno se reemplaza temporalmente por fórmula 18. Todos estos factores deben ser contrarrestados junto con cualquier duda que la madre tenga de los efectos adversos y la transferencia de medicamentos por la leche.
¿Qué afecta la concentración de un fármaco en la leche materna?
La transferencia de fármacos hacia la leche materna ocurre principalmente por difusión pasiva, proporcional a la concentración plasmática del medicamento. Las otras características del fármaco que influyen en este paso son la unión a proteínas, liposolubilidad, peso molecular y el pKa (logaritmo negativo de la constante disociación ácido-base o el pH en el cual se alcanza el equilibrio entre la forma ionizada y no ionizada del fármaco). En general, los medicamentos altamente liposolubles, con un bajo peso molecular, poca unión a proteínas o con pKa alto se asocian a mayor penetración en la leche materna. No obstante, el que un medicamento se excrete por la leche no supone necesariamente toxicidad para el recién nacido.
Las células epiteliales secretoras mamarias forman la barrera hematoláctea con uniones estrechas intercelulares (tight junctions) poco permeables para evitar la fuga de componentes de la leche. Una pérdida de la integridad de estas uniones se ha relacionado con reducción de la secreción mamaria y aumento del transporte paracelular de componentes plasmáticos hacia la leche, y viceversa. Esta barrera es bastante permeable antes del parto, lo que permite transferencia de moléculas grandes como anticuerpos, factores inmunes y células sanguíneas al calostro. El incremento de la prolactina y los glucocorticoides en el parto favorecen el cierre de estas uniones, volviéndolas casi impermeables a un mayor intercambio entre los componentes sanguíneo y lácteo. Así, la formación e integridad de esta barrera al comienzo de la lactancia es fundamental para asegurar el inicio de una abundante producción de leche 19.
Existen plataformas de búsqueda en internet, como LactMed, de la US National Library of Medicine, donde se busca el nombre del medicamento en inglés y se obtienen los datos más relevantes, el resumen de su uso y las referencias bibliográficas 12. La Asociación para la Promoción e Investigación científica y cultural de la Lactancia Materna (APILAM) mantiene E-lactancia, un riguroso sitio web de consulta sobre la compatibilidad de fármacos con la lactancia materna. Actualmente, la herramienta goza del aval internacional de la organización mundial The Academy of Breastfe-eding Medicine y del Comité de Lactancia Materna de la Asociación Española de Pediatría. Se trata de una página en español (con versión en inglés también), didáctica y completa, que incluye recomendaciones de LactMed y de la Administración de Alimentos y Drogas de Estados Unidos (FDA). Por otra parte, la plataforma es más intuitiva y cercana al paciente, clasifica los medicamentos según su riesgo con la lactancia en muy bajo, bajo, alto y muy alto. Esta clasificación se expone en la Tabla 1 13.
Tabla 1 Clasificación de riesgo de los medicamentos según E-lactancia.
| Riesgo | Definición | Ejemplos |
|---|---|---|
| Riesgo muy bajo | Medicamentos seguros, compatibles. Mínimo riesgo para la lactancia y el lactante. Literatura científica amplia con falta de toxicidad demostrada y uso frecuente en neonatos y lactantes. | Propofol, tiopental, etomidato, cefazolina, anestésicos locales, bloqueadores musculares, atropina, fentanilo, metadona, tramadol, midazolam, halogenados, acetaminofén. Adrenalina, noradrenalina, labetalol. |
| Riesgo bajo | Medicamentos bastante seguros, probablemente compatibles. Riesgo leve o poco probable. Sus características farmacocinéticas hacen muy poco probable la aparición de efectos adversos. | Petidina, pregabalina, efedrina, morfina, ácido acetilsalicílico, ketamina, tapentadol, óxido nitroso, fenilefrina, efedrina. |
| Riesgo alto | Medicamentos pocos seguros. Podrían provocar efectos adversos moderados o graves en el lactante. Usar alternativa más segura o interrumpir lactancia hasta que el fármaco se elimine de la madre (5 a 7 T/i)1. Existen pocos datos publicados y sus características farmacocinéticas hacen probable la aparición de efectos adversos. | Diazepam, oxicodona, codeína, metamizol, atenolol, clonidina, tabaco, alcohol. |
| Riesgo muy alto | Medicamentos muy inseguros, contraindicados. Uso de una alternativa o cese de la lactancia. Hay datos publicados que indican que puede ser tóxica para el lactante. | Ciclofosfamida, retinoides, antineoplásicos, fentermina, marihuana. |
1 T½: semivida de eliminación del fármaco.
Fuente. Autores, a partir de 13.
Sin embargo, hay algunos casos que presentan recomendaciones algo inconsistentes. Tal es el caso del tramadol que se metaboliza a 0 desmetiltramadol (M1) y ambos se excretan por la leche materna. E-lactancia lo clasifica como compatible (riesgo muy bajo) señalando que no se han observado problemas en madres que consumían este medicamento, a pesar de dedicarle algunas frases como "hay metabolizadores ultra-rápidos de tramadol que pueden acumular mayor concentración de M1" o "conviene emplear dosis mínima suficiente y vigilar en el lactante signos de sedación o dificultades de alimentación" 13. Por otra parte, LactMed en este aspecto es menos permisivo, concuerda más con FDA no recomendando su administración con la lactancia y en caso de uso por la madre, se debe observar cuidadosamente si el lactante presenta somnolencia excesiva, dificultad para amamantar y/o depresión respiratoria 12.
¿Qué factores influencian el riesgo de efectos adversos en el lactante20?
Momento de la dosis: amamantar antes de tomar el medicamento favorece que el lactante reciba una menor concentración. Algunas excepciones a este principio son las drogas con vida media más larga, como el diazepam, donde temporizar la lactancia no hace mayor diferencia.
Edad del lactante: la mayoría de los efectos adversos ocurre en neonatos y lactantes menores de 2 meses. Son rarísimos en mayores de 6 meses. Especial precaución se debería tener con los lactantes menores a 6 semanas de edad gestacional corregida. En el caso de los opioides, el orden de sensibilidad de efectos adversos debido a inmadurez de la función hepática y renal es prematuros>neonatos>lactantes. La capacidad de metabolización y excreción de un recién nacido es solo una tercera parte de la de un lactante de 8-9 meses.
Factores farmacocinéticos: las características que debe tener un fármaco para ser compatible con la lactancia materna se resumen en la Tabla 2.
Tabla 2 Resumen de las características farmacocinéticas que debe tener un fármaco para ser compatible con la lactancia materna
| Dosis relativa <10 % |
| Relación leche/plasma <1 |
| Unión proteínas plasmáticas >90 % |
| Peso molecular >200 Da |
| Pobre biodisponibilidad oral |
| Vida media corta del fármaco y de sus metabolitos activos |
| Medicamento certificado para su uso pediátrico |
Da: Dalton.
Fuente. Autores, tomado de 20.
Los principales parámetros farmacocinéticos son:
• Biodisponibilidad oral: es el porcentaje del medicamento absorbido cuando ya ha pasado por el intestino, hígado y pulmones. Un ejemplo es la gentamicina, que se administra por vía intravenosa a la madre. Como es pobremente absorbida oralmente por el bebé, las concentraciones de ella no se reflejarán en el plasma del lactante.
• Metabolismo de primer paso: este reduce la biodisponibilidad. Se prefieren medicamentos en la lactancia que son inactivados por este metabolismo.
• Unión a proteínas plasmáticas: solo la parte libre de la droga es capaz de atravesar las membranas biológicas. A mayor unión a proteínas plasmáticas, menor traspaso.
• Relación leche/plasma (L/P): refleja la concentración de las fracciones libres de proteína en la leche y en el plasma. Cualquier valor >1 implica que el medicamento no es adecuado para una mujer en lactancia materna.
• Peso molecular: mientras mayor es el peso, más difícil será su paso por la leche.
• Vida media: se define como el tiempo transcurrido hasta que la concentración plasmática del fármaco se reduce a la mitad. Está determinada por la absorción, metabolismo y excreción. A mayor vida media del fármaco, mayor es el riesgo de acumulación en la madre y el lactante. Deben transcurrir 5 vidas medias para alcanzar el estado de equilibrio, por lo que después de este tiempo sincronizar las alimentaciones para evitar los niveles máximos tiene un efecto mínimo. Del mismo modo, luego de 5 vidas medias y sin recibir más fármaco, casi un 98 % del fármaco ha sido eliminado del organismo. Sin embargo, los neonatos no metabolizan tan rápido como los adultos.
• Porcentaje de ionización: los medicamentos cruzan las membranas en su forma no ionizada. La leche es ligeramente más ácida (pH 7,2) que el plasma materno (pH 7,4) por lo que atrae bases débiles como oxicodona y codeína. Estas drogas se ionizan y sufren un atrapamiento iónico en la leche.
• Volumen ingerido de leche materna: a mayor volumen ingerido, mayor dosis del fármaco ingerida por el lactante. Así, los medicamentos utilizados en los primeros tres días posparto generalmente producen niveles subclínicos y seguros en el lactante, debido al volumen limitado del calostro.
• Dosis relativa: esta se ha reconocido como uno de los parámetros más importantes para establecer la seguridad de un medicamento en la paciente que está amamantando. Se prefieren drogas con proporción menor a 10 %. Se calcula dividiendo la dosis encontrada en el lactante por la dosis recibida por la madre.
Factores farmacogenómicos maternos: esto se ejemplifica con la codeína, apareciendo sedación excesiva en la madre y/o lactante en caso de ser metabolizadores rápidos o ultrarrápidos por exceso genético de la enzima citocromo P450 isoenzima 2D6 (CYP2D6). Esto puede ocurrir en el 3 % de afroamericanos, 10 % de caucásicos o 30 % de norteafricanos 12.
Medicamentos perioperatorios y transferencia hacia leche materna
La mayor parte de los medicamentos son compatibles con la lactancia materna (Figura 1). Los datos farmacocinéticos y su riesgo según e-lactancia se exponen en la Tabla 3.

√ Compatibles con la lactancia materna. √ * Mayoría compatibles con la lactancia. Ver detalles en el presente texto. √× Fármacos no compatibles o compatibles, pero con ciertas restricciones de uso. Se recomienda monitorizar al lactante. Ver detalles en el artículo. 1Fentanilo en dosis única (100 microgramos (µg) intravenoso) es seguro. Morfina y metadona son probablemente compatibles, pero se recomienda monitorizar. Meperidina y oxicodona, tienen alto riesgo, evitar. Fuente. Autores, tomado de 20.
Figura 1 Principios generales de anestesia/lactancia y compatibilidad de fármacos con la lactancia materna.
Tabla 3 Parámetros farmacocinéticos de los principales medicamentos anestésicos perioperatorios y su clasificación de riesgo según e-lactancia.
| Familia | Nombre | Unión de proteínas Biodisponibilidad Relación L/P plasmáticas oral (ideal <1)* | Vida Media (hrs) | Dosis relativa Riesgo (ideal <10 %) E-lactancia** | |||
|---|---|---|---|---|---|---|---|
| Inductores/ Sedantes | Propofol | 97 % | 3-12 | 0,007-0,5 | Muy bajo | ||
| Midazolam | 98 % | 44 % | 0,15 | 2-3 | 0,1-1,4 | Muy bajo | |
| Diazepam | 99 % | 100 % | 0,9 | 43-120 | 0,5-20 | Alto | |
| Etomidato | 77 % | 1,2 | 1,25 | 0,8-3,9 | Muy bajo | ||
| Ketamina | 47 % | 16 % | 3 | Bajo** | |||
| Tiopental | 60 % | 0,4 | 12 | 2-6 | Muy bajo | ||
| Analgésicos Opioides | Morfina | 35 % | 39 % | 1,6-5 | 1,5-2 | 7-15 | Bajo** |
| Metadona | 60-90 % | 90 % | 0,7-1,2 | 20-45 | 1,2-7 | Muy bajo** | |
| Fentanilo | 80-85 % | 65 % | 2,1 | 2-3 | 1,2-4 | Muy bajo** | |
| Remifentanilo | 70% | 2-4% | 0,3 | Bajo | |||
| Codeína | 7-25 % | 65-100 % | 1,3-2,5 | 3-4 | 0,6-7 | Alto | |
| Tramadol | 20 % | 60-75 % | 2,4-3 | 6-7 | 2,6 | Muy Bajo** | |
| Petidina | 60-80 % | 50-60 | 1,1-1,6 | 3-5 | 0,6-3,5 | Bajo** | |
| Oxicodona | 45 % | 60-87 % | 3,4 | 3,5-6 | 2,6-7,6 | Alto | |
| Analgésicos No opioides | Metamizol | 60 % | 85 % | 1,5 | 10-11 | 3,1-6,2 | Alto |
| Paracetamol | 10-25 % | 75-85 % | 0,9-1,4 | 1-3 | 2,3-5,2 | Muy bajo | |
| Naproxeno | 99,7 % | 95 % | 0,01 | 12-15 | 4,8 | Bajo | |
| Celecoxib | 97 % | 99 % | 0,3 | 11 | 0,3 | Muy Bajo | |
| Ketorolaco | 99 % | 81 % | 0,02-0,04 | 4-6 | 0,18 | Muy bajo | |
| Ketoprofeno | 99 % | 90 % | 1,5-4 | 0,3 | Muy bajo | ||
| Clonidina | 20-40 % | 65-99 | 2-4 | 6-24 | 13,3 | Alto | |
| Anestésicos locales | Lidocaína | 66-70 % | 35 | 0,4 | 1,8 | 0,8-4 | Muy bajo |
| Bupivacaína | 95 % | 0-1 | 2-4,6 | 0,2-6 | Muy bajo | ||
| Antieméticos | Dexametasona | 77 % | 70-78 % | 3,3-6 | Bajo | ||
| Domperidona | 91-93 % | 15-20 | 0,25 | 7-9 | 0,01-0,1 | Muy bajo | |
| Ondansetron | 75 % | 60 | 3 | Muy bajo | |||
| Droperidol | 85-90 % | 2,2 | Bajo | ||||
| Bloqueadores Musculares | Succinilcolina | 0-1 | 0,013 | Muy bajo | |||
| Rocuronio | 30 % | 0-1 | 1,2-1,4 | Muy bajo | |||
| Atracurio | 82 % | 0-1 | 0,3 | Muy bajo | |||
| Reversores | Neostigmina | 15-25 % | 1-2 | 0 | 0,9-1,2 | Muy bajo | |
| Sugammadex | 0 | 0 | 2 | Muy bajo | |||
| Antibióticos | Cefazolina | 89 % | 0-1 | 0,02 | 1-2 | 1,6 | Muy bajo |
| Ceftriaxona | 95 % | 0 | 0,04 | 6-9 | 0,15-0,6 | Muy bajo | |
| Clindamicina | 94 % | 90 | 0,5 | 2,4 | 0,6-5 | Muy bajo | |
| Cardiovasculares | Atropina | 14 % | 90 % | 4,3 | Muy bajo | ||
| Efedrina | 85 | 3-5 | Bajo | ||||
| Fenilefrina | 95 % | 38 | 2-3,4 | Bajo | |||
| Noradrenalina | 0 | 1 | Muy bajo | ||||
| Labetalol | 50 % | 25-40 | 1-2,6 | 6-8 | 0,05-0,45 | Muy bajo | |
| Otros | Pregabalina | 0 | 90 | 0,4-0,8 | 5-7 | 6 | Bajo |
| Ácido tranexámico | 3 % | 30-50 | 0,01 | 2 | Muy bajo | ||
| Omeprazol | 95-97 % | 40-60 | 1-2 | 0,9 | Muy bajo | ||
| Sulfato de magnesio | 25-40 % | 4-15 | 2 | 3-4 | 0,2 | Muy bajo | |
| Heparina no fraccionada | 95 % | 0 | 0 | 1-2 | Muy bajo | ||
| Enoxaparina | 0 | 0,02-0,1 | 4-5 | 1,3 | Muy bajo | ||
| Dalteparina | 0 | 0,02-0,2 | 3-5 | 1,3 | Muy bajo | ||
*Algunos medicamentos están con datos incompletos, porque a la fecha de la última actualización no se encuentra información publicada sobre su excreción en leche materna.
"Considerar que esta clasificación no se condice con algunas recomendaciones en este texto, basados en la plataforma LactMed y otros estudios. Para más detalles, véase el texto de este artículo.
Fuente. Autores, tomado de (13,18).
Se categorizarán de acuerdo con su riesgo según e-lactancia, LactMed y se tratarán brevemente según familia:
• Inductores/sedantes: La mayoría de los inductores son compatibles con la lactancia materna, dada su baja biodisponibilidad oral y vida media corta. La madre puede comenzar la lactancia una vez que esté despierta, no es necesario un período de espera. Sin embargo, se recomienda para la noche no compartir cama con el infante por riesgo de asfixia. La Figura 2 presenta un resumen de los inductores y sedantes.
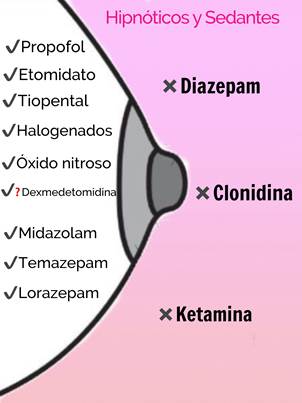
√ Compatibles con la lactancia materna. x No compatible con la lactancia materna. Evitar. √? No hay recomendaciones, pero se cree compatible. Fuente. Autores.
Figura 2 Resumen de la compatibilidad de fármacos hipnóticos y sedantes con la lactancia materna.
Los principales agentes hipnóticos y sedantes son:
- Propofol: pequeñas cantidades (0,0025 %) son transferidas a la leche materna.
- Tiopental: sus características farmacocinéticas predisponen a que sus cantidades en la leche sean muy bajas.
- Etomidato: cantidades de etomidato son pequeñas en la leche y disminuyen rápidamente, no se encuentran en la leche después de 3 horas.
- Ketamina: es el único de los inductores que no tiene mayores datos de transferencia en leche humana materna. Sumado a eso, puede provocar estados alucina-torios en la madre durante las primeras 24 horas, por lo que no cumpliría con el principio del inicio de la lactancia materna una vez que esté despierta y estable. Sin embargo, su corta vida media, rápida redistribución del plasma a los tejidos (4 minutos) y su mala biodisponibilidad oral le hacen probablemente segura en la lactancia. Por ello, e-lactancia lo clasifica como de bajo riesgo 13. Por otra parte, la recomendación de LactMed parece ser más conservadora señalando que se debe evitar y que si se requiere usar, se debe monitorizar al lactante por signos de mareo, sedación e inapetencia 11,12.
- Agentes inhalatorios (halogenados y óxido nitroso): debido a su corta vida media y alto aclaramiento, el uso en la anestesia no tendrá mayores consecuencias en la lactancia subsecuente.
- Benzodiacepinas: se usan generalmente para sedación consciente para procedimientos y ocasionalmente para premedicación. El lorazepam y el midazolam son de acción más corta que el diazepam. Midazolam es la benzodiacepina de uso más extendido. Por su sustancial efecto de primer paso hepático, su biodisponibilidad es baja, por lo que los niveles plasmáticos en el lactante son bajos. Una dosis única es segura en la lactancia, de modo que se puede iniciar la lactancia una vez que la madre esté despierta. Se recomienda optar por los de acción corta y utilizar una dosis mínima eficaz, evitando su uso repetido y crónico en madres de neonatos y prematuros, ya que se puede acumular. En ese sentido, se debe evitar el diazepam porque tiene un metabolito activo: desmetildiazepam (riesgo alto), que tiene una vida media larga, por lo que se transfiere a la leche en niveles significativos 12.
- Dexmedetomidina: existen reportes aislados y escasos donde no se prevé riesgo en lactantes y neonatos. El medicamento está totalmente ausente en la leche luego de 24 horas de terminada la infusión.
- Clonidina: sus usos son múltiples, anti-hipertensivo, sedación, ansiolisis, y analgesia. Puede aumentar la secreción de prolactina, produciendo ginecomastia y galactorrea. Debido a este impacto negativo en la lactancia, sumado a casos de efectos adversos en el lactante y a altas concentraciones plasmáticas, se sugiere evitar. No obstante, no ha sido estudiada una dosis única neuroaxial para reducir requerimientos.
• Analgésicos: La analgesia debe ser individualizada. Si se requieren opioides, se recomienda usar la mínima dosis efectiva por el menor tiempo posible. Los analgésicos no opioides/opioides y su compatibilidad con la lactancia se ejemplifican en la Figura 3.

√ Compatibles con la lactancia materna. x No compatible con la lactancia materna. Evitar. *Monitorizar ante dosis repetidas. ** En dosis analgésicas. Las dosis bajas son seguras(dosis antiplaquetarias). Fuente. Autores.
Figura 3 Resumen de compatibilidad de fármacos analgésicos no opioides y opioids.
Los principales fármacos analgésicos son:
- Acetaminofén (paracetamol): a pesar de unos parámetros farmacocinéticos poco favorables (Tabla 3), se excreta en ínfimas cantidades en la leche, siendo incluso mucho menor que la que recibiría con una dosis pediátrica normal por vía oral. Debido a la inmadurez hepática en neonatos y en lactantes pequeños (con LME), los bajos niveles de enzimas del citocromo P-450 dificultan la conversión del acetominofeno hacia sus metabolitos más tóxicos, por lo que la hepatotoxicidad es muy rara.
Antiinflamatorios no esteroidales:
- Ibuprofeno, ketorolaco, ketoprofeno, celecoxiby diclofenaco son compatibles con la lactancia, por lo que generalmente son la primera opción por ejemplo, en el postoperatorio de una cesárea, especialmente por vía endovenosa.
- Naproxeno: debido a su vida media más larga y reportes de casos de sedación en lactantes cuyas madres lo tomaban, no debería ser la primera opción.
- Parecoxiby meloxicam: no existen mayores datos y reportes por lo que se recomienda utilizar alternativas más seguras en lactancia.
- Ácido acetilsalicílico: su uso en dosis profilácticas antiplaquetarias (75-325 mg) es de bajo riesgo, no se detectan niveles de ácido salicílico en la leche. De hecho, se utiliza en embarazos de riesgo para prevención de preeclampsia 21. A mayores dosis por tiempo prolongado (analgésicas y antiinflamatorias) se considera de alto riesgo por posibilidad de acidosis metabólica por el ácido salicílico, sumado a esto existen dos reportes de casos antiguos de eventos adversos graves en lactantes. El síndrome de Reye está asociado con su consumo por niños con infecciones virales, pero se desconoce el riesgo de este síndrome por el salicilato en la leche materna.
- Metamizol: e-lactancia lo cataloga de alto riesgo para la lactancia, por lo que recomienda usar una alternativa más segura o iniciar la lactancia tras 48 horas de la última dosis 20. Sus metabolitos aparecen en la leche en cantidades considerables, y se ha publicado un caso de cianosis y depresión respiratoria que se atribuyó a su consumo. Se ha informado mayor riesgo de leucemia linfocítica aguda en infantes cuyas madres lo tomaban en el embarazo y la lactancia 13. Así, la FDA y la Agencia Europea de Medicamentos (EMA) han limitado la dosis y el uso principalmente por sus reacciones adversas y riesgo de agranulocitosis en lactantes/ niños y durante la lactancia 22. No obstante, hay retractores, principalmente en Israel y Latinoamérica donde es ampliamente usado, sugiriendo que el riesgo particular de agranulocitosis está relacionado con un alelo HLA específico, y es de alto riesgo entre descendientes de poblaciones celtobretonas, pero nulo o inexistente en otras 23.
- Opioides: es el grupo donde se encuentran los fármacos de mayor riesgo en la mujer en lactancia materna, por lo que conviene hacer una distinción de cada opioide. De esta manera, una dosis única endovenosa de fentanilo, comúnmente usado en la anestesia general, es compatible y seguro con la lactancia materna. Por otra parte, el empleo de opioides por vía neuroaxial no reviste mayor riesgo.
- Morfina: es excretada en la leche en cantidades insignificantes. Se ha señalado históricamente como uno de los opioides de elección en la mujer puérpera cuando se necesita una analgesia endovenosa potente. Sin embargo, también existe compatibilidad de otros opioides en lactancia como fentanilo, metadona y remifentanilo. Además, cuando se usa en dosis repetidas endovenosas, como puede ser en el postoperatorio, se recomienda monitorizar al lactante ante signos de sedación, inapetencia y depresión respiratoria.
- Metadona: se excreta en cantidades clínicamente no significativas y no se han reportado problemas en lactantes. Se recomienda monitorizar ante dosis repetidas. Riesgo muy bajo, al presentar menor índice de relación leche/plasma (L/P) y dosis relativa que otros opioides.
- Fentanilo: aproximadamente 100 veces más potente que la morfina, altamente lipofílico y con posibilidad de que se almacene en el tejido mamario. Un estudio que evaluó 5 mujeres a quienes se les administraron 100 µg de fentanilo endovenoso en la inducción anestésica, evidenció que menos del 0,1 % se encontró en la leche materna 24. Sus características farmacológicas (baja biodisponibilidad y baja duración de acción) lo hacen un fármaco seguro y de muy bajo riesgo en la lactancia, por lo que se recomienda comenzar la lactancia en el periodo postoperatorio inmediato, si la madre está alerta y se utilizó una dosis única y razonable de fentanilo (2 µg/kg). Lo mismo se extrapola para el alfentanilo.
- Remifentanilo: a pesar de que no existen muchos estudios del remifentanilo en lactancia, su baja biodisponibilidad oral, vida media sensible a contexto independiente de la duración de la infusión, metabolización por esterasas plasmáticas y alta unión a proteínas plasmáticas hacen de este el opioide ideal para mujeres en lactancia materna, especialmente si se espera que el dolor postoperatorio sea mínimo 25. En forma concomitante, se podría extrapolar su uso endovenoso en analgesia del trabajo de parto en los casos de contraindicación de técnicas neuroaxiales, donde se han evidenciado amplias ventajas en comparación con el resto de los opioides y mínimos efectos neonatales 18.
- Codeína: es uno de los fármacos que se deben evitar en madres amamantando. Debido a que la isoenzima encargada de su metabolización tiene un considerable polimorfismo genético, las mujeres me-tabolizadoras "ultrarrápidas" producen altas concentraciones de morfina en la leche materna, que pueden determinar en casos extremos una depresión neonatal 26. Su alta liposolubilidad y poca unión a proteínas plasmáticas, permiten que sea secretado en la leche materna con el consiguiente efecto en el infante. Si la madre ya tomó codeína, se le debe aconsejar suspender o desechar leche por 15 horas. Luego de ese intervalo la transferencia es insignificante 27.
- Tramadol: la advertencia de la FDA y el reporte de algunos casos de depresión respiratoria neonatal parecieron sentenciar el tramadol en la paciente puérpera 27) . No obstante, hay detractores, que aluden diferencias sustanciales con la codeína: el M1 (metabolito del tramadol) tiene un débil efecto opioide y además, la metabolización a M1 está disminuida en lactantes pequeños, excretándose en cantidades muy pequeñas en la leche 28) . Aun así, no es el fármaco ideal por sus propiedades (Tabla 3) e incidencia de mareos, náuseas y vómitos en la madre, por lo que si se decide usar, se debe monitorizar al lactante ante aparición de somnolencia, inapetencia, depresión respiratoria y sedación.
- Oxicodona: otro de los opioides que se deben evitar, pues los lactantes pueden recibir >10 % de la dosis terapéutica, tiene un metabolismo farmacogenómico similar a la codeína y además, existen reportes de casos de sedación/ depresión respiratoria en infantes expuestos por leche materna. El riesgo es mayor si la madre recibe dosis superiores a 30 mg/día 29.
- Hidromorfona: es casi 7 veces más potente que la morfina, y tiene un 62 % de biodisponibilidad oral 12. No hay mayores estudios de compatibilidad, en e-lactancia lo señalan como de bajo riesgo, pero sin mayor información 13. No obstante, se ha calculado que un infante con LME recibiría 0,15 µg/kg diarios de una única dosis materna de 2 mg de hidromorfona intranasal 12. Además, existe un reporte de depresión respiratoria en un lactante de 6 días asociado a su uso, que fue revertida con naloxona 30. Debido a esto, no se recomienda su uso, respaldando lo señalado en LactMed 12.
- Petidina o meperidina (demerol): debido a su metabolito de vida media larga (norpetidina), es aconsejable preferir otros fármacos, especialmente en prematuros. Su uso analgésico continuo en el trabajo de parto puede retrasar el inicio de la lactancia 31.
• Anestésicos locales: Sus propiedades fisicoquímicas son ideales debido a que son moléculas largas, polarizadas, que no cruzan fácilmente por los ductos mamarios maternos. Se han demostrado concentraciones insignificantes en la leche materna de anestésicos locales como bupivacaína y lidocaína. Se midieron concentraciones de su metabolito (pipecolylxylidide) en la leche materna y sangre materna, y se concluyó que la transferencia del anestésico y su metabolito fue mínima, por lo que se puede utilizar con seguridad 16. Además, se ha documentado que un buen control del dolor posparto facilita una lactancia más precoz, así la inyección de anestésicos locales peridurales luego del pinzamiento del cordón umbilical o adicionar levobupivacaína a la infiltración de la herida en la cesárea mejora el éxito de la lactancia materna.
• Bloqueadores neuromusculares: Se presume que no cruzan la barrera hematoláctea por sus propiedades: complejos de amonio cuaternario polarizados con pobre liposolubilidad, pobre biodisponibilidad oral y de gran peso molecular. La succinilcolina, debido a su alta ionización a pH fisiológico, pobre absorción oral y rápida eliminación del plasma materno, también es compatible con la lactancia materna, pudiendo amamantar cuando se haya despertado de la anestesia general 18.
• Reversores de relajación neuromuscular: La neostigmina y el sugammadex son compatibles con la lactancia materna. Con neostigmina se han descrito algunos casos de cólicos abdominales en el lactante, sin mayor trascendencia 12. Debido a que el sugammadex podría retener en su estructura a los progestágenos, se recomienda que las pacientes puérperas que toman anticonceptivos utilicen algún método de barrera por los primeros 7 días luego de su administración 32.
• Antieméticos: Aunque no hay mayores estudios de transferencia de los setrones (granisetron y ondansetrón), son de elección en la mujer puérpera; su alto volumen de distribución y corta vida media hacen improbable su excreción en leche en cantidad significativa. La dexametasona, usada ampliamente en la anestesia general para profilaxis de náuseas y vómitos, ha demostrado disminución de la prolactina tras su administración, pero su uso puntual y no prolongado es compatible con la lactancia. Además, una paciente con emesis postoperatoria difícilmente podrá amamantar, por lo que la profilaxis representa más beneficios que riesgos. Metoclopramida y domperidona, además de antieméticos, se usan como galactogogos, por lo que podrían aumentar la producción de leche. Droperidol, también usado como tratamiento de náuseas y vómitos postoperatorios, tiene parámetros farmacocinéticos favorables (alto porcentaje de fijación de proteínas y vida media corta), por lo que su uso es compatible en lactancia.
• Drogas cardiovasculares
- Atropina: en dosis sistémicas aisladas, como las que se usan en conjunto con neostigmina, es compatible con la lactancia. En dosis más repetidas puede disminuir la producción de leche al alterar la secreción de prolactina y de oxitocina y podría haber efectos anticolinérgicos muscarínicos en el lactante, por lo que es necesaria su vigilancia.
- Efedrina: riesgo bajo; dado su amplio volumen de distribución, es poco probable que provoque efectos en el lactante.
- Fenilefrina: es uno de los vasoactivos de elección tras la anestesia espinal en cesárea, siendo también compatible con la lactancia, dada su pobre biodisponibilidad oral (38 %) y alta unión a proteínas plasmáticas.
- Etilefrina: aunque no hay muchos datos publicados sobre su excreción en la leche materna, debido a su corta vida media y baja biodisponibilidad oral probablemente sea compatible con la lactancia materna 13.
- Noradrenalina y adrenalina: riesgo muy bajo. Compatibles con la lactancia materna.
- Betabloqueadores: labetalol, metoprolol y propanolol (riesgo muy bajo). Atenolol sería la excepción (riesgo alto), ya que presenta excreción por la leche materna clínicamente significativa, pudiendo afectar al lactante 13.
• Antibióticos: Solo se comentarán los que se usan en antibioticoprofilaxis.
- Cefazolina, ceftriaxona, ampicilina-sulbactam: riesgo muy bajo, seguros en la lactancia. Es normal esperar negatividad de cultivos en lactantes febriles y gastroenteritis en el lactante por alteración de la flora intestinal 33.
- Clindamicina y metronidazol: una dosis única probablemente sea compatible con la lactancia, pero puede alterar en mayor cantidad la flora intestinal, provocando diarrea, candidiasis o más raramente colitis pseudomembranosa en el caso de clindamicina.
• Otros medicamentos postoperatorios:
Omeprazol, pregabalina, ranitidina, ácido tranexámico, heparina no fraccionada y de bajo peso molecular son compatibles con la lactancia. Para mayor detalle, consultar las plataformas mencionadas previamente.
Lactancia y "drogas" sociales
Si bien no son fármacos anestésicos, es frecuente su consumo en la población, enfatizando en la responsabilidad del anestesiólogo en la promoción de salud. Así, el tabaco, tetrahidrocanabinol (THC o marihuana) y alcohol se deben evitar y considerar igualmente como fármacos que atraviesan la barrera hematoláctea. El tabaquismo, inclusive el pasivo, está asociado a muerte súbita del lactante. Un seguimiento de un año de lactantes de madres que usaron marihuana encontró deterioro en el desarrollo motor 34.
Escenarios
Para exponer de forma más práctica la compatibilidad de la anestesia con la lactancia se ejemplificará con los cuatro escenarios posibles más frecuentes.
Embarazada en trabajo de parto, preocupada por el efecto que puede tener la anestesia epidural en la lactancia
La analgesia neuroaxial es la técnica más efectiva para disminuir el dolor del trabajo de parto. Los medicamentos que habitualmente se usan son una combinación de anestésico local y opioide, como el fentanilo, por sus efectos sinérgicos.
La baja biodisponibilidad oral y propiedades fisicoquímicas de los anestésicos locales, permiten que sean seguros y compatibles con la lactancia.
La adición de fentanilo en la técnica combinada o epidural tradicional permite una menor concentración y menor masa de droga del anestésico local, lo que facilita una reducción del bloqueo motor materno y con esto se previene algún impacto negativo en el riesgo que tenga la epidural en la tasa de parto instrumentalizado. Sin embargo, dosis mayores de 150 µg epidurales podrían influir en la lactancia, reportándose un 19 % de dificultad de lactancia en las primeras 6 semanas versus un 2 y 6 % en el grupo que recibió menos dosis o no recibió fentanilo epidural, respectivamente 35,36. Si bien fue estadísticamente significativo (p = 0,002), probablemente sea marginal en términos clínicos. Sumado a esto, reportes posteriores, como el de Lee et al., han señalado que soluciones epidurales que contienen concentraciones de fentanilo tan altas como 2 µg/mL no influyen en las tasas de lactancia materna a las 6 semanas posparto 37. Por último, las madres que recibieron epidural versus las que no recibieron, tuvieron la misma efectividad de lactancia, sin diferencias en el estado neuroconductual del infante 38.
Respuesta escenario 1
La analgesia neuroaxial para el trabajo de parto es compatible con la lactancia materna.
Paciente programada para cesárea electiva preocupada por el efecto de la anestesia raquídea en la lactancia posterior
Existen factores que pueden alterar la iniciación y duración de la lactancia asociados a la cesárea: mayor dolor, náuseas y vómitos, mayor cantidad de fármacos administrados, posibilidad de reoperación y complicaciones como sufrimiento fetal y hemorragia posparto 39,40. El fentanilo intratecal es indetectable (<0,1 µg/L) en el calostro luego de 1 hora de su dosis, por lo que no tiene impacto en la tasa de lactancia ni en el puntaje de APGAR neonatal 41.
Por otra parte, la morfina intratecal tiene una biodisponibilidad oral de 30 % y su metabolito -morfina-6-glucurónido- es farmacológicamente activo y más potente, por lo que tiene una biodisponibilidad menor. Distintos informes han señalado sedación en el 50 % de los lactantes con concentraciones plasmáticas de morfina sobre 125 µg/mL. Feilberg et al. reportaron un pico de morfina de 82 µg/mL en leche materna 30 minutos después de un bolo de 4 mg de morfina epidural 16,42.
Así, la morfina intratecal en dosis habituales de 50-100 µg puede ser usada en forma segura (si no existe contraindicación ni factores de riesgo para depresión respiratoria materna) para analgesia intra y postoperatoria en pacientes operadas de cesárea que deseen amamantar en forma inmediata. De hecho, es el estándar de recomendación para el tratamiento del dolor postoperatorio en la cesárea, según las últimas guías 43.
El dolor postoperatorio es uno de los factores por los cuales las madres operadas de cesárea relatan alguna dificultad en cargar a su hijo y llevarlo al pecho 43. El anestesiólogo debe establecer una estrategia para evitar el dolor postoperatorio, ya que como vimos muchos opioides endovenosos (los más usados en el dolor postoperatorio inmediato), pueden interferir con una lactancia eficaz, especialmente en dosis repetidas, por lo que se deberían privilegiar técnicas regionales (morfina neuroaxial o bloqueo de pared abdominal). Se ha descrito que cuando se maneja adecuadamente el dolor después de la cesárea, hay mayor ganancia ponderal del recién nacido 15.
Otro de los factores que podría incidir en la suspensión precoz de la lactancia son las náuseas y vómitos, que aumentan al administrar morfina neuroaxial. El uso de dexametasona y/o ondansetrón podrían disminuir dichos síntomas después de la cesárea, si se administra morfina neuroaxial 44,45.
Por último, mantener a las madres con sus hijos juntos es una práctica segura y saludable. La evidencia señala que el contacto piel con piel ininterrumpido durante y posterior a la cesárea para todas las madres, promueve desenlaces óptimos maternos y fetales 46,47.
Respuesta escenario 2
La anestesia espinal para cesárea es compatible con la lactancia materna. Se debe preconizar una adecuada analgesia postoperatoria idealmente utilizando morfina intratecal para que la madre pueda iniciar precozmente la lactancia materna. Técnicas de contacto piel con piel intraoperatorios permiten mayor satisfacción materna y podrían incidir en una LME más exitosa.
Paciente que va a recibir anestesia general en su cesárea
Un 0,5-1 % de las cesáreas se realizan con anestesia general. Las guías internacionales recomiendan el uso de anestesia neuroaxial en cesárea sobre la anestesia general, principalmente por el riesgo de intubación traqueal difícil, aspiración de contenido gástrico, mejor control del dolor postoperatorio y para facilitar el contacto piel con piel inmediato. Además, porque promueve la movilidad y regreso rápido a las actividades diarias, con mejores índices de calidad de vida 48.
Madres que recibieron anestesia general en su cesárea no inician la lactancia en la primera hora de vida, lo cual se asocia con una menor frecuencia de LME a las 6 semanas y a los 6 meses al compararla con la anestesia neuroaxial 12,49.
Si va a recibir anestesia general, se deben privilegiar los medicamentos ya descritos que sean compatibles con la lactancia y seguir los 6 principios (Figura 1), optando por algún método regional (por ejemplo, bloqueo del plano del transverso abdominal o TAP-block) para control del dolor postoperatorio. Si la madre está alerta y estable, es recomendable iniciar la lactancia materna cuanto antes, monitorizando al neonato por la aparición eventual de sedación o depresión respiratoria. En lactantes prematuros, hipotónicos -y si la madre recibió dosis repetidas y mayores de opioi-des- se aconseja una interrupción breve de lactancia (6-12 h). Por último, se desaconseja compartir cama con el lactante, si recibió anestesia general.
Respuesta escenario 3
La lactancia es menos eficaz en cesáreas con anestesia general. Se debe manejar en forma óptima el dolor y las náuseas/vómitos, para que la madre pueda comenzar la lactancia al despertar, monitorizando al neonato ante aparición de síntomas.
Paciente puérpera con lactancia materna exclusiva que requiere cirugía electiva o de urgencia
La evaluación preanestésica es crucial para resolver dudas y establecer un plan intra y postoperatorio que sea lo más compatible con la lactancia materna. Las madres deben ser informadas de que extraer y eliminar su leche luego de la anestesia (pumping and dumping) no es necesario. Si se anticipa una cirugía prolongada y el niño no puede quedarse con su madre, se debe discutir la necesidad de extraer leche previamente y almacenarla. Esto debe llevarse a cabo con la participación de un experto en lactancia.
Aquí se deberían seguir los 6 principios de la Figura 1. Las técnicas regionales son de elección tanto en el intraoperatorio como en el postoperatorio, para reducir la necesidad de analgésicos sistémicos. Si se opta por anestesia general, las técnicas ahorradoras de opioides (dosis única inicial) o libres de opioides pueden ser una alternativa eficaz.
Se debe usar profilaxis antiemética, para facilitar que en el postoperatorio la madre pueda llevar a su hijo al pecho.
Si se administra anestesia general, es más probable el uso de opioides. El efecto puede variar por diferencias farmacocinéticas (mayor o menor metabolismo) y farmacodinámicas (diferente sensibilidad ante un mismo nivel plasmático) 18.
Es aconsejable evaluar signos de uso excesivo de opiáceos en la madre como un indicador de potenciales efectos en el lactante, evitar su uso especialmente en madres con lactantes menores a 6 semanas de edad, por representar el grupo de mayor riesgo por inmadurez hepática y renal. Si es necesario utilizar opioides, el fentanilo y la morfina, en dosis única, son los más indicados.
Habrá menos dolor postoperatorio si se utilizan técnicas analgésicas regionales en conjunto con la anestesia general (neuroaxial o bloqueo de nervio periférico). En forma concomitante, se debe indicar una analgesia multimodal con analgésicos no opioides, como el paracetamol y AINE, ambos compatibles con la lactancia materna. Si aun así, requiere opioides endovenosos postoperatorios, se debe tratar de usar la menor dosis efectiva por el menor periodo.
La cirugía ambulatoria debe ser la primera opción en una mujer que está amamantando. Se recomienda que posteriormente, en el domicilio, un adulto responsable esté con la paciente las primeras 24 h. Se les debe ofrecer asesoría y soporte en el caso de que la madre requiera uno o más días hospitalizada, por complicación o cualquier otro motivo 18.
Por último y dado el contexto pandémico actual, es recomendable mantener la lactancia si la madre resulta infectada con Covid-19. Los beneficios de la lactancia materna superan con creces el riesgo potencial de transmisión viral, mientras se mantengan las medidas de higiene y prevención 50.
Respuesta escenario 4
Se debe indagar en la evaluación preanestésica si la madre está amamantando. La mayoría de los fármacos anestésicos son compatibles con la lactancia, y se deben privilegiar las técnicas neuroaxiales, para permitir que la madre amamante una vez que esté despierta y estable 51. Se debe tener precaución con algunos opioides endovenosos, especialmente si recibieron dosis repetidas.
CONCLUSIONES
La lactancia materna es segura después de la anestesia, pues la mayoría de los medicamentos son compatibles. Las recomendaciones de esta revisión se resumen en la Tabla 4.
Tabla 4 Recomendaciones referentes a la lactancia materna y anestesia.
| 1. | Se debe incentivar a las pacientes puérperas a iniciar la lactancia materna después de la cirugía. |
| 2. | La anestesia no debe interferir con la seguridad de la lactancia materna. |
| 3. | Las técnicas neuroaxiales son las más efectivas para el dolor del trabajo de parto, y permiten un inicio precoz de la lactancia materna. |
| 4. | La anestesia espinal en cesárea permite que la madre tenga contacto piel con piel inmediato y un manejo del dolor adecuado en comparación con la anestesia general. |
| 5. | A toda mujer con hijos menores de 2 años se le debe preguntar rutinariamente en la evaluación preanestésica si está amantando. |
| 6. | No es necesario extraer y eliminar la leche de las pacientes puérperas postoperadas (pump and dump). Si se anticipa una cirugía prolongada, uso repetido de opioides endovenosos postoperatorios o el lactante no puede quedarse con su madre se debe discutir previamente la necesidad de extraer y almacenar con un experto en lactancia. |
| 7. | Los medicamentos anestésicos y analgésicos no opioides son compatibles con la leche materna, pues se transfieren en cantidades muy pequeñas, y no causan efectos en el neonato. |
| 8. | La codeína no se debe usar con la lactancia materna, debido a algunos reportes de sedación profunda en lactantes, relacionados con diferencias en su metabolismo. |
| 9. | Los fármacos como los opioides y benzodiacepinas de acción larga se deben usar con precaución en madres con niños de hasta 6 semanas de vida, especialmente tras múltiples dosis. El lactante se debe observar si presenta signos de somnolencia y depresión respiratoria, más aún si la madre experimenta signos de sedación. |
| 10. | Las técnicas ahorradoras de opioides o anestesia general libre de opioides son preferibles en la paciente puérpera. La anestesia regional sin sedación tiene amplios beneficios en este sentido, pues interfiere lo menos posible con la habilidad de la madre para cuidar a su hijo. |
| 11. | La cirugía ambulatoria, si es posible, debe ser de elección para evitar interrumpir rutinas normales. |
| 12. | Debe estar accesible la asesoría postoperatoria y el apoyo de lactancia para la paciente puérpera. Asimismo, se debe suministrar información actualizada (folletos, redes sociales informativas) sobre la compatibilidad de los distintos medicamentos anestésicos con la leche materna y de las guías enfatizadas en promover la lactancia en el período perioperatorio. |
Fuente. Autores, a partir de varias referencias 12,13,18,51.
El anestesiólogo debe ser un agente en la promoción y mantenimiento de la lactancia materna, estar dispuesto a resolver dudas en el preoperatorio y elaborar un plan anestésico que no interfiera con la seguridad de la lactancia materna. Se prefieren técnicas regionales, técnicas ahorradoras de opioides y cirugía ambulatoria. El apoyo multidisciplinario en el período perioperatorio y el asesoramiento preciso garantizarán una interrupción mínima de esta parte importante del cuidado infantil.
Agradecimientos
A todas las embarazadas y puérperas lactantes que con sus dudas constantes motivaron la redacción de esta revisión.
REFERENCIAS
1. OMS. Estrategia mundial para la alimentación del lactante y el niño pequeño (Internet). Ginebra: OMS; 2003 (cited 2020 Nov 24). Available at: Available at: https://www.who.int/nutrition/publications/gs infant feeding text spa.pdf [ Links ]
2. Sankar MJ, Sinha B, Chowdhury R, Bhandari N, Taneja S, Martines J, et al. Optimal breastfeeding practices and infant and child mortality: a systematic review and meta-analysis. Acta Paediatr. 2015;104(467)3-13. doi: https://doi.org/10.1111/apa.13147 [ Links ]
3. World Health Organization (WHO). Guide-line: protecting, promoting and supporting breastfeeding in facilities providing maternity and newborn services. Geneva: 2017 (cited 2020 Sep 23). Available at: Available at: https://apps.who.int/iris/bitstream/handle/10665/259386/9789241550086-eng.pdf?sequence=1 [ Links ]
4. Brown CR, Dodds L, Legge A, Bryanton J, Semenic S. Factors influencing the reasons why mothers stop breastfeeding. Can J Public Health. 2014;105(3):e179-85. doi: https://doi.org/10.17269/cjph.105.4244 [ Links ]
5. Ministerio de Salud. Informe técnico encuesta nacional de lactancia materna en la atención primaria (ENALMA), en colaboración con Comité Nacional de lactancia materna (CONALMA). Chile 2013 (cited 2020 Nov 4). Available at: Available at: https://www.minsal.cl/sites/default/files/INFORME_FINAL_ENALMA_2013.pdf [ Links ]
6. Victora CG, Bahl R, Barros AJ, França GV, Horton S, Krasevec J, et al. Breastfeeding in the 21st century: epidemiology, mechanisms, and life-long effect. The Lancet. 2016;387(10017):475-90. doi: https://doi.org/10.1016/S0140-6736(15)01024-7 [ Links ]
7. Aedo C. Economic Evaluation of prolonging the Postnatal Period. Rev Chil Pediatr. 2007;78(1):10-50. doi: http://dx.doi.org/10.4067/S0370-41062007000600003 [ Links ]
8. Bartick M, Reinhold A. The burden of suboptimal breastfeeding in the United States: a pediatric cost analysis. Pediatrics. 2010;125:e1048-56. doi: https://doi.org/10.1542/peds.2009-1616 [ Links ]
9. Sankar MJ, Sinha B, Chowdhury R, et al. Optimal breastfeeding practices and infant and child mortality: a systematic review and meta-analysis. Acta Paediatr . 2015;104(467)3-13. doi: https://doi.org/10.1111/apa.13147 [ Links ]
10. Dalal PC, Bosak J, Berlin C. Safety of the breast-feeding infant after maternal anesthesia. Paediatr Anaesth. 2014;24:359-71. doi: https://doi.org/10.1111/pan.12331 [ Links ]
11. UK Drugs in Lactation Advisory Service (UKDILAS). UK Medicines Information Specialist Pharmacy Service, 2018 (cited 2021 Mar 4). Available at: Available at: https://www.sps.nhs.uk/articles/ukdilas_acceso_20_noviembre_2020 . [ Links ]
12. Drugs and lactation database (LactMed) (internet). 2019 (cited 2020 Sep 20). Available at: Available at: https://www.ncbi.nlm.nih.gov/books/NBK501922/ [ Links ]
13. e-lactancia.org. APILAM: Asociación para la promoción e investigación científica y cultural de la lactancia materna; 2002 (cited 2020 Nov 20). Available at: Available at: http://e-lactancia.org [ Links ]
14. Chestnut DH. Labor epidural analgesia and breastfeeding. Anesthesiology. 2017(4);127:593-5. doi: https://doi.org/10.1097/ALN.0000000000001794 [ Links ]
15. Lim G, Facco FL, Nathan N, Waters JH, Wong CA, Eltzschig HK. A review of the impact of obstetric anesthesia on maternal and neonatal outcomes. Anesthesiology. 2018;129(1):192-215. doi: https://doi.org/10.1097/ALN.0000000000002182 [ Links ]
16. Cobb B, Liu R, Valentine E, Onuoha O. Breastfeeding after anesthesia: A review for anesthesia providers regarding the transfer of medications into breast milk. Transl Perioper Pain Med. 2015;1(2):1-7. doi: https://doi.org/10.31480/2330-4871/023 [ Links ]
17. Gyanesh P Radhika K, Sinha M, Haldar R. Postdural puncture headache after caesarean section: are preventive strategies worse than the cure? Rev Bras Anestesiol. 2015;65(1):82-83. doi: https://doi.org/10.1016/j.bjane.2014.04.002. [ Links ]
18. Mitchell J, Jones W, Winkley E, Kinsella SM. Cuideline on anaesthesia and sedation in breastfeeding women 2020. Anaesthesia. 2020;75:1482-93. doi: https://doi.org/10.1111/anae.15179 [ Links ]
19. Stelwagen K, Singh K. The role of tight junctions in mammary gland function. J Mammary Gland Biol Neoplasia. 2014;19(1):131-8. doi: https://doi.org/10.1007/s10911-013-9309-1 [ Links ]
20. Hotham N, Hotham E. Drugs in breastfeeding. Aust Prescr. 2015;38(5):156-9. doi: https://doi.org/10.18773/austprescr.2015.056 [ Links ]
21. Askie LM, Duley L, Henderson-Smart DJ, Stewart LA; PARIS Collaborative Croup. Anti-platelet agents for prevention of pre-eclampsia: a meta-analysis of individual patient data. Lancet. 2007;369(9575):1791-8. doi: https://doi.org/10.1016/S0140-6736(07)60712-0 [ Links ]
22. EMA. Committee for Medicinal Products for Human Use (CHMP). Referral under Article 31 of Directive 2001/83/EC metamizolecontaining medicinal products (internet). 2018 (cited 2020 dic. 2). Available at: Available at: https://www.ema.europa.eu/en/documents/referral/metamizole-article-31-referral-chmp-assessment-report en.pdf [ Links ]
23. Shah RR. Metamizole (dipyrone)-induced agranulocytosis: Does the risk vary according to ethnicity? J Clin Pharm Ther. 2019;44(1):129-33. doi: https://doi.org/10.1111/jcpt.12768 [ Links ]
24. Nitsun M, Szokol JW, Saleh HJ, Murphy GS, Vender JS, Luong L, et al Pharmacokinetics of midazolam, propofol, and fentanyl transfer to human breast milk. Clin Pharmacol Ther. 2006;79:549-57. doi: https://doi.org/10.1016/j.clpt.2006.02.010 [ Links ]
25. Stuttmann R, Schàfer C, Hilbert P Meyer MR, Maurer HH. The breast feeding mother and xenon anaesthesia: four case reports. Breast feeding and xenon anaesthesia. BMC Anesthesiol. 2010;10:1. doi: https://doi.org/10.1186/1471-2253-10-1 [ Links ]
26. Koren G, Cairns J, Chitayat D, Gaedigk A, Lee-der SJ. Pharmacogenetics of morphine poisoning in a breastfed neonate of a codeine-prescribed mother. Lancet. 2006;368:704. doi: https://doi.org/10.1016/S0140-6736(06)69255-6 [ Links ]
27. U.S. Food and Drug Administration. FDA restricts use of prescription codeine pain and cough medicines and tramadol pain medicines in children; recommendations against use in breastfeeding women (internet). 2017 (cited 2020 Nov 5). Available at: Available at: https://www.fda.gov/drugs/fda-drug-safety-podcasts/fda-drug-safety-pod-cast-fda-restricts-use-prescription-codei-ne-pain-and-cough-medicines-and-tramadol [ Links ]
28. Palmer GM, Anderson BJ, Linscott DK, Paech MJ, Allegaert K. Tramadol, breast feeding and safety in the newborn. Arch Dis Child. 2018;103:2017. doi: https://doi.org/10.1136/archdischild-2017-313786 [ Links ]
29. Lam J, Kelly L, Ciszkowski C, et al. Central nervous system depression of neonates breastfed by mothers receiving oxycodone for postparzwtum analgesia. J Pediatr. 2012;160:33-7; e2. doi: https://doi.org/10.1016/j.jpeds.2011.06.050 [ Links ]
30. Edwards JE, Rudy AC, Wermeling DP Desai N, McNamara PJ. Hydromorphone transfer into breast milk after intranasal administration. Pharmacotherapy. 2003;23(2):153-8. doi: https://doi.org/10.1592/phco.23.2.153.32081 [ Links ]
31. Martin E, Vickers B, Landau R, Reece-Stremtan S, the Academy of Breastfeeding Medicine. ABM Clinical Protocol #28, Peripartum analgesia and anesthesia for the breastfeeding mother. Breastfeed Med. 2018;13:164-71 doi: https://doi.org/10.1089/bfm.2018.29087.ejm [ Links ]
32. Corda DM, Robards CB. Sugammadex and oral contraceptives: Is it time for a revision of the anesthesia informed consent? Anesth Analg. 2018;126(2):730-1. doi: https://doi.org/10.1213/ANE.0000000000002677 [ Links ]
33. Bar-Oz B, Bulkowstein M, Benyamini L, Greenberg R, Soriano I, Zimmerman D, et al. Use of antibiotic and analgesic drugs during lactation. Drug Saf. 2003;26(13):925-35. doi: https://doi.org/10.2165/00002018-200326130-00002 [ Links ]
34. Moretti ME, Lee A, Ito S. Which drugs are contraindicated during breastfeeding? Practice guidelines. Can Fam Physician. 2000;46:1753-7. [ Links ]
35. Beilin Y, Bodian CA, Weiser J, Hossain, S, Arnold I, Feierman DE, et al. Effect of labor epidural analgesia with and without fentanyl on infant breast-feeding: a prospective, randomized, double-blind study. Anesthesiology. 2005;103:1211-7. doi: https://doi.org/10.1097/00000542-200512000-00016 [ Links ]
36. Halpern SH, Ioscovich A. Epidural analgesia and breast-feeding. Anesthesiology. 2005;103:1. doi: https://doi.org/10.1097/00000542-200512000-00002 [ Links ]
37. Lee A, McCarthy R, Toledo P, Jones MJ, White N, Wong C. Epidural labor analgesia- fentanyl dose and breastfeeding success: a randomized clinical trial. Anesthesiology. 2017;127:614-24. doi: https://doi.org/10.1097/ALN.0000000000001793 [ Links ]
38. Chang ZM, Heaman MI. Epidural analgesia during labor and delivery: Effects on the initiation and continuation of effective breastfeeding. J Hum Lact. 2005;21(3):305-26. doi: https://doi.org/10.1177/0890334405277604 [ Links ]
39. Hobbs AJ, Mannion CA, McDonald SW, Brockway M, Tough SC. The impact of caesarean section on breastfeeding initiation, duration and difficulties in the first four months postpartum. BMC Pregnancy Child-birth. 2016;16:90. doi: https://doi.org/10.1186/s12884-016-0876-1 [ Links ]
40. Brown A, Jordan S. Impact of birth complications on breastfeeding duration: an internet survey. J Adv Nurs. 2013;69(4):828-39. doi: https://doi.org/10.1111/j.1365-2648.2012.06067.x [ Links ]
41. Yousefshahi F, Davari-Tanha F, Najafi A, Kaveh M, Rezaei-Hemami M, Khashayar P et al. Effects of Intrathecal opioids in cesarean section on breastfeeding and Newborns' weight Caining. J Fam Reprod Health. 2016;10(4):176-83. [ Links ]
42. Oliveira MR, Santos MG, Aude DA, Lima RM, Módolo NS, Navarro LH. Should maternal anesthesia delay breastfeeding? A systematic review of the literature. Braz. J. Anesthesiol. 2019;69(2):184-96. doi: https://doi.org/10.1016/j.bjane.2018.12.006 [ Links ]
43. Roofthooft E, Joshi GP, Rawal N, Van de Velde M, & PROSPECT Working Croup of the European Society of Regional Anaesthesia and Pain Therapy and supported by the Obstetric Anaesthetists' Association. PROSPECT guide-line for elective caesarean section: updated systematic review and procedure-specific postoperative pain management recommendations. Anaesthesia . 2021;76(5):665-80. doi: https://doi.org/10.1111/anae.15339 [ Links ]
44. Abdel-Aleem M, Osman A, Morsy K. Effect of coadministration of dexamethasone with intrathecal morphine on postoperative out-comes after cesarean delivery. Int J Gynaecol Obstet. 2012;116(2):158-61. doi: https://doi.org/10.1016/j.ijgo.2011.10.002 [ Links ]
45. Imeh A, Olaniyi O, Simeon O, Omotola O. Dexamethasone versus a combination of dexamethasone and ondansetron as prophylactic antiemetic in patients receiving intrathecal morphine for caesarean section. Afr Health Sci. 2014;14(2):453-9. doi: https://doi.org/10.4314/ahs.v14i2.23 [ Links ]
46. Crenshaw JT. Healthy Birth Practice #6 Keep mother and baby together- It's best for mother, baby and breastfeeding J Perinat Educ. 2014;23(4):211-7. doi: https://doi.org/10.1891/1058-1243.23.4.211 [ Links ]
47. Guala A, Boscardini L, Visentin R, Angello-tti P, Crugni L, Barbaglia M, et al. Skin-toskin contact in cesarean birth and duration of breastfeeding: a cohort study. Scient World J. 2017;2017:1940756. doi: https://doi.org/10.1155/2017/1940756 [ Links ]
48. Ghaffari S, Dehghanpisheh L, Tavakkoli F, Mahmoudi H. The effect of spinal versus general anesthesia on quality of life in women undergoing cesarean delivery on maternal request. Cureus. 2018;10(12):e3715. doi: https://doi.org/10.7759/cureus.3715 [ Links ]
49. Karasu D, Yilmaz C, Ozgunay SE, Cansabuncu S, Korfali G. A comparison of the effects of general anaesthesia and spinal anaesthesia on breastfeeding. C R Acad Bulg Sci. 2018;71:993-1000. doi: https://doi.org/10.7546/CRABS.2018.07.17 [ Links ]
50. United Nations International Children's Emergency Fund (UNICEF). Breastfeeding during the COVID-19 pandemic. Tips on keeping your baby healthy and safe (internet). 2021 (cited 2021 Mar 25). Available at: Available at: https://www.unicef.org/eap/breastfeeding-during-covid-19 [ Links ]
51. Wanderer JP, Rathmell JP. Anesthesia & breastfeeding: more often than not, they are compatible. Anesthesiology. 2017;127(4):A15-A15. doi: https://doi.org/10.1097/ALN.0000000000001867 [ Links ]
Recibido: 13 de Julio de 2021; Aprobado: 12 de Enero de 2022; : 15 de Marzo de 2022











 texto en
texto en 


