Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347On-line version ISSN 2256-2087
Rev. colomb. anestesiol. vol.51 no.3 Bogotá July/Sept. 2023 Epub Sep 01, 2023
https://doi.org/10.5554/22562087.e1077
Artículo original
Modelo de predicción pronostica para NVPO en parto por cesárea
a Grupo Académico de Epidemiología Clínica (GRAEPIC), Universidad de Antioquia. Medellín, Colombia.
b Servicio de Anestesiología, Escuela de Medicina de la Universidad de Antioquia. Medellín, Colombia.
c Instituto de Investigaciones Médicas, Escuela de Medicina, Universidad de Antioquia. Medellín, Colombia.
d Escuela de Medicina, Universidad Pontificia Bolivariana. Medellín, Colombia.
e Clínica del Prado. Medellín, Colombia.
f Clínica Universitaria Pontificia Bolivariana. Medellín, Colombia.
Introducción:
La escala de riesgo simplificada de Apfel para náuseas y vómito posoperatorio (NVPO) ha mostrado utilidad en anestesia; sin embargo, al no haber sido calibrada en anestesia regional o en pacientes embarazadas, su utilidad en cesárea es limitado.
Objetivo:
Desarrollar un modelo de predicción pronóstica para náuseas y vómito posoperatorios en pacientes embarazadas, llevadas a cesárea bajo anestesia espinal.
Métodos:
En una cohorte de 703 pacientes con embarazo a término programadas para cesárea, se evaluaron 15 variables de forma prospectiva para construir un modelo de predicción pronóstica para el desarrollo de náuseas y vómito posoperatorio. Se utilizó el análisis de regresión logística para la construcción del modelo y se calculó su calibración y discriminación con la prueba de Hosmer-Lemeshow, las curvas de calibración y el estadístico C. Además, se realizó la calibración interna con el método de remuestreo Bootstrap.
Resultados:
Las náuseas y vómito posoperatorio se presentaron en el 27% de las pacientes durante las primeras seis horas después de la cirugía. El modelo incluyó como variables pro-nósticas el desarrollo de náuseas y vómito en el intraoperatorio, edad menor de 28 años, antecedentes de NVPO, índice de masa corporal (IMC) de la madre y el peso del recién nacido. El modelo mostró una adecuada calibración (x2: 4,65 p: 0,5888), aunque una baja discriminación (Estadístico C = 0,68).
Conclusiones:
Se construyó un modelo de predicción pronóstica para el desarrollo de NVPO en cirugía cesárea, y con este se construyó una escala pronóstica que permite clasificar a las pacientes por grupos de riesgo.
Palabras clave: Náusea y vómito posoperatorios; Cesárea; Anestesia espinal; Pronóstico; Modelo de predicción; Anestesiología
Introduction:
Apfel simplified risk score for postoperative nausea and vomiting (PONV) has shown to be useful in anesthesia; however, since it has not been calibrated in regional anesthesia or in pregnant patients, its use in cesarean section is limited.
Objective:
To develop a prognostic predictive model for postoperative nausea and vomiting in pregnant patients undergoing cesarean section under spinal anesthesia.
Methods:
In a cohort of 703 term pregnant patients scheduled of cesarean section, 15 variables were prospectively assessed, to design a prognostic predictive model for the development of postoperative nausea and vomiting. A logistic regression analysis was used to construct the model and its calibration and discrimination were based on the Hosmer-Lemeshow test, the calibration curves, and C statistic. Additionally, the internal calibration was performed with the Bootstrap resampling method.
Results:
Postoperative nausea and vomiting were experienced by 27% of the patients during the first six hours after surgery. The model included as prognostic variables the development of intraoperative nausea and vomiting, age under 28 years, a history of PONV, the mother's BMI and the weight of the newborn baby. The model showed an adequate calibration (x2: 4.65 p: 0.5888), though a low discrimination (Statistic C = 0.68).
Conclusions:
A prognostic predictive model was created for the development of PONV in cesarean section. This model was used to build a prognostic scale for the classification of patients into risk groups.
Keywords: Postoperative nausea and vomiting; Cesarean section; Spinal anesthesia; Prognosis; Predictive model; Anesthesiology
INTRODUCCIÓN
Las náuseas y vómito posoperatorio (NVPO) son el evento adverso más estudiado en anestesia por su alta frecuencia, relación directa con la satisfacción del paciente y posibles complicaciones subsecuentes 1.
En cesárea se presentan condiciones que facilitan el desarrollo de NVPO, hipotensión, gasto cardiaco reducido por la compresión aortocava, exteriorización uterina, aplicación de uterotónicos y morfina espinal 2,3. Se estima una incidencia de 23-79%, lo que incrementa la incomodidad de las pacientes o los efectos secundarios, como aspiración del contenido gástrico, aumento del dolor y del sangrado posoperatorio 2-4.
Para la población no obstétrica y pediátrica se han desarrollado modelos de predicción pronóstica que permiten individualizar a los pacientes, mediante la identificación de factores de riesgo y la clasificación en grupos de riesgo, implementando algoritmos de tratamientos profilácticos. Estos algoritmos han permitido un uso racional de medicamentos, que disminuyen los efectos secundarios asociados, los tiempos de estancia en la unidad de cuidados posanestésicos (UCPA) y los costos en los sistemas de atención en salud 1.
La puntuación de riesgo simplificada de Apfel es el método más utilizado por su conveniencia y sencillez. Sin embargo, los pacientes bajo anestesia regional y las gestantes fueron excluidas al momento del desarrollo del modelo 3,5, por lo que su extrapolación a la población obstétrica no es posible.
En la actualidad, no se cuenta con una escala pronóstica de NVPO adaptada o desarrollada para cesárea. Por lo tanto, el objetivo de este estudio fue desarrollar y validar una escala de predicción pronóstica basada en un modelo estadístico para NVPO en cesárea bajo anestesia espinal.
MÉTODOS
Estudio de cohorte prospectivo con 703 pacientes embarazadas de dos centros obstétricos de tercer nivel 6, entre el 1 de agosto de 2017 y el 31 de enero de 2019 en Medellín, Colombia. Este estudio recibió la aprobación ética según el acta N.° 019 de diciembre 1 de 2016, del Comité de Bioética del Instituto de Investigaciones Médicas de la Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
Se incluyeron pacientes con edad ≥16 años, edad gestacional ≥37 semanas, clasificación ASA I-III, programadas para parto por cesárea, electiva o urgente, bajo anestesia espinal, quienes aceptaron participar y firmaron el consentimiento informado.
Se excluyeron pacientes con náuseas o vómito en las 24 horas previas al procedimiento quirúrgico, bloqueo espinal inadecuado que requirió cambio a anestesia general, malformaciones congénitas del feto, embarazo múltiple o trastornos psicológicos y de conducta de la madre que dificultaran la obtención de datos.
La anestesia espinal se realizó con aguja punta de lápiz 27G, se administró una combinación de 10 mg de bupivacaína hiperbárica 0,5%, 100 μg de morfina y 25 μg de fentanilo. Como parte de los protocolos de atención institucional, todas las pacientes recibieron dexametasona de 8 mg para profilaxis NVPO, infusión de fenilefrina como profilaxis vasopresora y se evitó la exteriorización uterina, según la Declaración de Consenso y Recomendaciones de la Sociedad de Anestesia Obstétrica y Perinatología 7.
El desenlace de interés fue el desarrollo de náuseas, vómito, o su combinación, después del procedimiento quirúrgico. La evaluación clínica se realizó a las seis horas del posoperatorio, lo que corresponde al tiempo de estancia en la unidad de cuidados posanestésicos (UCPA).
Se consideró que las pacientes tuvieron náuseas posoperatorias si respondían afirmativamente a la pregunta ¿Siente o ha sentido náuseas durante su estancia en la unidad de cuidados posanestésicos? y se consideró que tuvieron vómito si respondía afirmativamente a la pregunta ¿Ha tenido arcadas o ha vomitado durante su estancia en la unidad de cuidados posanestésicos? Las pacientes que desarrollaron náuseas o vómito se consideraron positivas para NVPO. La variable NVPO se consideró como desenlace binario para ser aplicado al análisis de regresión logística.
Quince variables se consideraron candidatas para el modelo: la edad, el índice de masa corporal (IMC), el tiempo de ayuno (TA), el volumen de líquidos intravenosos administrados (LIVA), el tiempo quirúrgico (TQ) y el peso del recién nacido (PRN) se manejaron como variables continuas. Los antecedentes de cinetosis (AC), migraña (AM) y náuseas y vómito en un procedimiento quirúrgico previo (ANVPO), la aplicación de opioides en la analgesia del parto (OAP) mediante catéter epidural, la aplicación de metoclopramida como profilaxis NVPO (MPNV), el desarrollo intraoperatorio de náuseas o vómito (NVIO), la realización de tubectomía en la cesárea (TC) y el género del recién nacido (GRN) se manejaron como variables dicotómicas. El antecedente de tabaquismo (AT) se manejó como una variable politómica: ausencia de tabaquismo, tabaquismo antes del embarazo, tabaquismo durante el embarazo con suspensión mayor a 4 meses antes de la cirugía y suspensión menor a 4 meses antes de la cirugía 8.
Todas las variables fueron seleccionadas tras una revisión de la literatura, se incluyeron aquellas claramente asociadas, las que han generado conflictos y las claramente rechazadas o con relevancia clínica limitada para NVPO 1,9-12.
Para facilitar el diligenciamiento del cuestionario, este se completó en dos etapas. La primera etapa fue en el área de preparación, para identificar antecedentes y variables preoperatorias; la segunda etapa fue en la UCPA, para identificar variables intraoperatorias y el desenlace.
Por tratarse de un estudio prospectivo en pacientes hospitalizadas, no se esperó una pérdida importante de datos, por lo que, al presentarse, su manejo fue la exclusión del paciente del estudio sin realizar imputación de datos. La pérdida de seguimiento a las pacientes se definió como aquellos escenarios en los que no se pudo evaluar el desenlace principal, traslado a otra institución o necesidad de intubación orotraqueal.
Se siguieron los lineamientos de la Declaración TRIPOD 13 y Peduzzi et al.14, que establecen el requerimiento de al menos 10 desenlaces por variable que se estudia. La incidencia más baja encontrada en la literatura, 21 %-23%2,4,15, se utilizó para maximizar el número de pacientes. El cálculo del tamaño de muestra fue de 700 pacientes.
Para el análisis estadístico se realizó la prueba Shapiro-Wilk con el fin de comprobar la distribución normal de las variables continuas, por lo que los resultados se publicaron de acuerdo con esta. Las variables categóricas se presentaron de acuerdo con su frecuencia absoluta y relativa.
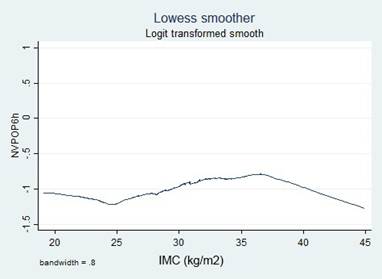
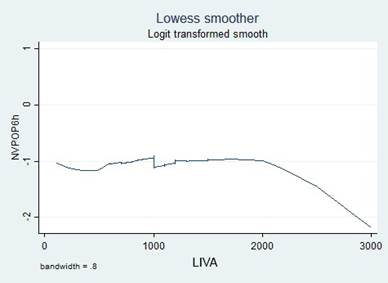
Para la selección de la variable candidata se utilizó un modelo de regresión logística simple, donde el valor de p < 0,25 fue el criterio de inclusión, de acuerdo con las recomendaciones de la literatura 16,17. Las variables continuas se introdujeron inicialmente en su forma natural y la suposición de monotonía se verificó utilizando la herramienta Locally Weighted Scatterplot Smoothing (LOWESS); cuando el supuesto no se cumplió, se desarrollaron transformaciones (cuadráticas, logarítmicas naturales y en base 10) para encontrar una mejor relación lineal con la variable independiente o se identificaron puntos de corte, basados en datos de la literatura o según los puntos de inflexión en los gráficos, para categorizar las variables.
Se realizó un proceso de selección de las variables, incluyendo y excluyendo una a una en un proceso de selección hacia adelante y hacia atrás, de acuerdo con su nivel de significancia en el estadístico de Wald a un nivel de 0,05 18,19.
Posteriormente, se agregaron aquellas variables con una significancia < 0,25, identificando en cada modelo nuevo la razón de verosimilitud parcial, la calibración y la discriminación, con el objetivo de identificar el aporte de la nueva variable al modelo. Finalmente, se exploraron aquellas variables con significancias > 0,25 para evaluar si de alguna forma, estas podrían mejorar el desempeño predictivo de los modelos evaluados. La calibración de los modelos se estimó mediante la prueba de bondad de ajustes de Hosmer-Lemeshow 16,20 y con las curvas de calibración 13. La discriminación se estimó a través del estadístico C, calculado por el área bajo la curva ROC (AUC-ROC) 17,20.
La colinealidad se evaluó mediante el factor de inflación de la varianza (VIF) y de los coeficientes de correlación de Pearson o Spearman o los coeficientes tetracóricos y policóricos, según la naturaleza de las variables. Un coeficiente > 0,8 o un VIF > 10 se asumió como colinealidad 21. Las interacciones se evaluaron mediante el cambio en los coeficientes de las variables del modelo, al incluir o excluir una nueva variable, así como con la significancia en el estadístico de Wald, al introducir los productos entre las variables predictoras del modelo.
Una vez obtenido el modelo final, se realizó la validación interna estimando las posibles desviaciones de los coeficientes (sesgo) con el método de remuestreo Bootstrap. Se construyeron 1.000 muestras aleatorias con reposición con las 703 pacientes, calculando la probabilidad del desenlace y comparando las curvas de calibración y AUC-ROC entre los grupos.
Con los coeficientes de regresión obtenidos, se calculó la probabilidad del desenlace y las pacientes se dividieron en grupos de riesgo (riesgo bajo, intermedio y alto) utilizando como punto de corte los percentiles 25 y 75 de la distribución de probabilidad del desenlace 22. Posteriormente, se construyó una escala pronóstica para facilitar el uso e interpretación del modelo desarrollado. Para esto, se construyeron dos formatos diferentes de presentación: Tabla gráfica de puntuación y Nomograma.
Para la tabla gráfica de puntuación se calculó la probabilidad de desenlace entre las variables independientes, en todas las diferentes combinaciones posibles, y se asignó un código de colores para cada grupo de riesgo. Para el desarrollo del Nomograma, se utilizó la herramienta "nomolog" del software Stata®, en el que, de forma visual, se puede asignar un puntaje a cada variable independiente y su sumatoria se correlaciona con la probabilidad de desenlace.
Todos los análisis se realizaron con el software estadístico Stata 15.1 (Statacorp LLC, 2019) y RStudio 2022.02.0 (RStudio Inc., 2022).
RESULTADOS
Se evaluaron 719 pacientes durante el período de recolección, de las cuales se descartaron 16 (2,22%) debido a pérdida de datos, que no se pudieron obtener por dificultades para contactarse con las pacientes o al revisar los registros médicos. La muestra final fue de 703 pacientes entre las dos instituciones participantes: 352 pacientes en la institución 1 y 351 pacientes en la institución 2.
El desenlace se presentó en 190 pacientes (27,03%), que corresponden a 91 casos (25,85%) en la institución 1 y 99 casos (28,21 %) en la institución 2.
Se realizó un análisis univariado con las 15 variables de estudio, de las cuales cinco alcanzaron una significancia ≤ 0,25 lo que les permitió ser consideradas como predictores candidatos para la construcción del modelo: Edad, ANVPO, IMC, NVIO y PRN (Tabla 1).
Table 1 Distribution of the predictive variables according to the outcome.
| Preoperatorio | NVPO (+) 190 (%) | NVPO (-) 513 (%) | P | OR | IC 95 % |
|---|---|---|---|---|---|
| Institución 1 n (%) 2 n (%) |
91 (47.89) 99 (52.11) |
261 (50.88) 252 (49.12) |
0.483 |
1.126 |
0.807 a 1.572 |
| Edad (años) Rango Mediana (Q1 a Q3) |
14 a 44 27 (24 a 31) |
15 a 43 29 (24 a 33) |
0.016 |
0.966 |
0.939 a 0.993 |
| Antecedente de NVPO n(%) | 39 (20.53) | 58 (11.31) | 0.002 | 2.026 | 1.298 a 3.164 |
| Antecedente de cinetosis n(%) | 20 (10.53) | 55 (10.72) | 0.941 | 0.980 | 0.570 a 1.683 |
| Antecedente de migraña n(% ) | 46 (24.21) | 112 (21.83) | 0.502 | 1.144 | 0.772 a 1.694 |
| Tabaquismo
|
182 (95.79) 7 (3.68) 1 (0.53) 0 (0.00) |
482 (93.96) 16 (3.12) 9 (1.75) 6 (1.17) |
- 0.750 0.247 - |
1 1.159 0.294 1 |
- 0.469 a 2.862 0.037 a 2.339 |
| IMC (kg/m2) Rango Mediana (Q1 a Q3) |
20.27 a 44.00 29.39 (27.29 a 33.29) |
19.13 a 44.92 29.21 (26.22 a 32.11) |
0.146 |
1.028 |
0.990 a 1.067 |
| Ayuno (horas) Rango Mediana (Q1 a Q3) |
0 a 31 11 (8 a 15) |
0 a 60 11 (8 a 14) |
0.596 |
0.993 |
0.967 a 1.019 |
| Uso de opioides n (%) | 14 (7.37) | 38 (7.41) | 0.986 | 0.994 | 0.526 a 1.880 |
| Uso de metoclopramida n (%) | 145 (76.32) | 407 (79.34) | 0.387 | 0.839 | 0.564 a 1.248 |
| Intraoperative | |||||
| NVIO n (%) | 65 (34.21) | 75 (14.62) | 0.000 | 3.037 | 2.062 a 4.472 |
| LIVA (litros) Rango Mediana (Q1 a Q3) |
0.2 a 2.2 1.0 (1.0 a 1.2) |
0.11 to 3.0 1.0 (1.0 a 1.2) |
0.797 |
0.999 |
0.999 a 1.000 |
| Tubectomía n (%) | 57 (30.00) | 140 (27.29) | 0.478 | 1.142 | 0.792 a 1.647 |
| Tiempo quirúrgico (minutos) Rango Mediana (Q1 a Q3) |
25 a 138 60 (50 a 65) |
20 a 180 60 (50 a 65) |
0.980 |
0.999 |
0.989 a 1.010 |
| Género del recién nacido Femenino n (%) Masculino n (%) |
85 (44.74) 105 (55.26) |
245 (47.76) 268 (52.24) |
0.476 |
1.129 |
0.808 a 1.578 |
| Peso del recién nacido (g) Rango Mediana (Q1 a Q3) |
1.360 a 4.240 3.130 (2.740 a 3.490) |
1.635 a 4.700 3.070 (2.720 a 3.440) |
0.193 |
1.000 |
0.999 a 1.000 |
IC: Intervalo de confianza; IMC: Índice de masa corporal; LIVA: Líquidos intravenosos administrados; NVIO: Náuseas y vómito intraoperatorio; NVPO: Náuseas y vómito posoperatorio.
Fuente: Autores.
El antecedente de tabaquismo (AT) no alcanzó significancia estadística dada la baja frecuencia de este, alrededor del 95% de las pacientes reportaron no ser fumadoras. Por esta razón, la variable fue recodificada simplificándola en dos estados y en dos posibles escenarios: nunca ha fumado o ha fumado en algún momento; No ha fumado recientemente o ha fumado recientemente (Tabla 2). Se realizaron transformaciones y categorizaciones con las variables continuas, de acuerdo con los puntos de inflexión en los gráficos LOWESS. Solo la variable Edad mantuvo su significancia estadística en su forma continua y al categorizarla (Tabla 2). Ninguna transformación mejoró la monotonía.
Table 2 Categorization of the continuous and polytomous variables.
| NVPO (+) 190 (%) | NVPO (-) 513 (%) | P | OR | 95 % IC | Gráficas LOWESS | ||
|---|---|---|---|---|---|---|---|
| Edad | ≤ 25 años > 25 años |
75 (39.47) 115 (60.53) |
158 (30.80) 355 (69.20) |
0.03 | 1.465 | 1.037 a 2.071 |
|
| ≤ 28 años > 28 años |
113 (59.47) 77 (40.53) |
248 (48.34) 265 (51.66) |
0.09 | 1.568 | 1.119 a 2.198 | ||
| ≤ 30 años > 30 años |
135 (71.05) 55 (28.95) |
324 (63.16) 189 (36.84) |
0.051 | 1.432 | 0.998 a 2.055 | ||
| ≤ 24 años 25 to 35 años ≥ 36 años |
65 (34.21) 105 (55.26) 20 (10.53) |
132 (25.73) 299 (58.28) 82 (15.98) |
- 0.074 0.016 |
1 0.713 0.495 |
- 0.492 a 1.033 0.280 a 0.878 |
||
| IMC (kg/m2) | ≤ 24.99 25.00 a 34.99 ≥ 35.00 |
24 (12.63) 138 (72.63) 28 (14.74) |
74 (14.42) 378 (73.68) 61 (11.89) |
- 0.643 0.289 |
1 1.126 1.415 |
- 0.683 a 1.856 0.744 a 2.689 |
|
| ≤ 24.99 25.00 a 29.99 30.00 a 34.99 ≥ 35.00 |
24 (12.63) 77 (40.53) 61 (32.11) 28 (14.74) |
74 (14.42) 209 (40.74) 169 (32.94) 61 (11.89) |
- 0.637 0.701 0.289l.k |
1 1.136 1.113 1.415 |
- 0.669 a 1.929 0.645 a 1.920 0.745 a 2.689 |
||
| LIVA | < 0.5 L ≥ 0.5 L |
3 (1.58) 187 (98.42) |
11 (2.14) 502 (97.86) |
0.635 | 0.732 | 0.202 a 2.653 |
|
| < 1 L ≥ 1 L |
44 (23.16) 146 (76.84) |
115 (22.42) 398 (77.58) |
0.835 | 1.043 | 0.702 a 1.549 | ||
| < 2 L ≥ 2 L |
178 (93.68) 12 (6.32) |
479 (93.37) 34 (6.63) |
0.882 | 1.053 | 0.533 a 2.079 | ||
| PRN | < 2.500 g 2.500 a 3.500g >3.500 g |
20 (10.53) 124 (65.26) 46 (24.21) |
75 (14.62) 337 (65.69) 101 (19.69) |
- 0.238 0.082 |
1 1.380 1.708 |
- 0.809 a 2.355 0.934 a 3.125 |
|
| < 2.000 g 2.000 a 4.000g > 4.000 g |
6 (3.16) 178 (93.68) 6 (3.16) |
18 (3.51) 481 (93.76) 14 (2.73) |
- 0.827 0.711 |
1 1.110 1.286 |
- 0.434 a 2.841 0.340 a 4.860 |
||
| Tiemnpo quirúrgico | ≤ 60 min > 60 min |
132 (69.47) 58 (30.53) |
355 (69.20) 158 (30.80) |
0.944 | 0.987 | 0.688 a 1.417 |
|
| ≤ 100 min > 100 min |
187 (98.42) 3 (1.58) |
506 (98.64) 7 (1.36) |
0.831 | 1.160 | 0.297 a 4.531 | ||
| ≤ 60 min 61 to 99 min ≥ 100 min |
132 (69.47) 54 (28.42) 4 (2.11) |
355 (69.20) 150 (29.24) 8 (1.56) |
- 0.864 0.633 |
- 0.968 1.345 |
- 0.669 a 1.401 0.398 a 4.540 |
||
| Tabaquismo | Sí No |
8 (4.21) 182 (95.79) |
31 (6.04) 482 (93.96) |
0.349 | 1.463 | 0.660 a 3.242 | |
| Reciente No reciente |
1 (0.53) 189(99.47) |
15 (2.92) 498 (97.08) |
0.290 | 5.692 | 0.747 a 43.395 |
IC: Intervalo de confianza; IMC: Índice de masa corporal; LIVA: Líquidos intravenosos administrados; NVIO: Náuseas y vómito intraoperatorio NVPO: Náuseas y vómito posoperatorio; PRN: Peso del recién nacido.
Fuente: Autores.
La colinealidad entre las variables se evaluó mediante la construcción de una matriz de correlación, incluyendo sus formas tanto continuas como recategorizadas. En la evaluación ningún coeficiente resultó ser > a 0,8 y no se pudieron evidenciar interacciones entre las variables.
Inicialmente se construyeron tres modelos con las variables con significancias ≤0,05 (NVIO, Edad de forma continua en 2 y 3 categorías y ANVPOP) y en estos modelos se fueron agregando y eliminando las variables con significancias ≤ 0,25 (PRN en 3 categorías e IMC de forma continua y en 3 categorías).
Se construyeron múltiples modelos agregando o eliminando variables una a una, evaluando el estadístico de Wald, la razón de verosimilitud y la contribución al modelo en calibración y discriminación (Figura 1). Se seleccionó el modelo dos, que corresponde a NVIO, Edad en 2 categorías y ANVPOP, dada su mayor discriminación, y al subgrupo F, que corresponde a la inclusión de las variables IMC en 3 categorías y PRN en 3 categorías, ya que mejoraron la calibración y discriminación del modelo, AUC-ROC 0,68 (95% IC: 0,64 a 0,73) (Figura 2).

A, C, E, G, I y K: Curvas de discriminación, B, D, F, H, J y L: Curvas de calibración. Modelo 1A: NVIO + Edad (años) + ANVPO. Modelo 1B: NVIO + Edad (años) + ANVPO + IMC (kg/m2). Modelo 1C: NVIO + Edad (años) + ANVPO + PRN3Cat. Modelo 1D: NVIO + Edad (años) + ANVPO + IMC (kg/m2) + PRN3Cat. Modelo 1E: NVIO + Edad (años) + ANVPO + IMC3Cat. Modelo 1F: NVIO + Edad (años) + ANVPO + IMC3Cat + PRN3Cat. Modelo 2A: NVIO + Edad2Cat + ANVPO. Modelo 2B: NVIO + Edad2Cat + ANVPO + IMC (kg/m2). Modelo 2C: NVIO + Edad2Cat + ANVPO + PRN3Cat. Modelo 2D: NVIO + Edad2Cat + ANVPO + IMC (kg/m2) + PRN3Cat. Modelo 2E: NVIO + Edad2Cat + ANVPO + IMC3Cat. Modelo 2F: NVIO + Edad2Cat + ANVPO + IMC3Cat + PRN3Cat. Modelo 3A: NVIO + Edad3Cat + ANVPO. Modelo 3B: NVIO + Edad3Cat + ANVPO + IMC (kg/m2). Modelo 3C: NVIO + Edad3Cat + ANVPO + PRN3Cat. Modelo 3D: NVIO + Edad3Cat + ANVPO + IMC (kg/m2) + PRN3Cat. Modelo 3E: NVIO + Edad3Cat + ANVPO + IMC3Cat. Modelo 3F: NVIO + Edad3Cat + ANVPO + IMC3Cat + PRN3Cat. ANVPO: Antecedente de náuseas y vómito posoperatorio; AUC: Área bajo la curva; Cat: Categorías; IMC: Índice de masa corporal; Mod: Modelo; NVIO: Náuseas y vómito intraoperatorio; PRN: Peso del recién nacido. Fuente: Autores
Figura 1 Curvas de calibración y discriminación de los modelos explorados.

A y B: Curvas de discriminación y calibración del modelo seleccionado 2F, C: Análisis de regresión logística del modelo seleccionado 2F, D y E: Curvas de discriminación y calibración de las muestras Bootstrap, F: Distribución de las AUC ROC de las muestras Bootstrap, G: Fórmula de la regresión del modelo seleccionado 2F. Modelo 2F: NVIO + Edad2Cat + ANVPO + IMC3Cat + PRN3Cat. AUC: Área bajo la curva; ANVPO: Antecedente de náuseas y vómito posoperatorio; Cat: Categorías; CI: Intervalos de confianza; IMC: Índice de masa corporal; Mod: Modelo; NVIO: Náuseas y vómito intraoperatorio; PRN: Peso del recién nacido. Fuente: Autores.
Figura 2 Modelo final seleccionado.
Se exploró la aplicación de metoclopramida como variable predictora (OR: 0,8729 IC 95%: 0,5744 a 1,3265) de acuerdo con las recomendaciones de la declaración TRIPOD para variables con un posible impacto significativo en el resultado 13. Asimismo, se incluyó la variable "Institución" para explorar el impacto de la atención institucional en el resultado (OR: 1,2938 IC 95%: 0,9101 a 1,8393). Ninguna de las variables anteriores mejoró la calibración, la discriminación o la predicción del desenlace en el modelo final.
En cuanto a las demás variables que no lograron ingresar al modelo, se llevó a cabo su exploración ingresándolas al modelo final propuesto una a una, tanto en sus formas naturales como recategorizadas, para evaluar mejoras en calibración y discriminación, sin encontrar mayor contribución de alguna de estas variables.
Se realizó la validación interna para evaluar cualquier optimismo en el modelo predictivo. Se utilizó el método de remuestreo Bootstrap y se observó una distribución similar en las curvas de calibración y discriminación en los nuevos modelos remuestreados y el modelo original propuesto. Se trazaron las curvas AUC de los modelos Bootstrap, se calculó el intervalo de confianza al 95% y se compararon con el modelo original propuesto (0,6437 a 0,7259) (Figura 2).
La probabilidad del desenlace de cada paciente se calculó con los coeficientes ajustados del modelo 2 (Figura 2), y se utilizaron los percentiles 25 y 75 de las probabilidades (16,20% y 33,02%) para clasificar a los pacientes en grupos de riesgo (bajo, intermedio y alto). Se observaron diferentes proporciones del evento según los grupos de riesgo (12,15%, 26,74% y 42,70%, respectivamente) y se encontraron diferentes distribuciones de las variables predictoras entre los grupos (Tabla 3).
Table 3 Distribution of the predictive variables in accordance with the outcome.
| Bajo riesgo | Riesgo intermedio | Riesgo alto | ||||
|---|---|---|---|---|---|---|
| PONV (+) | PONV (-) | PONV (+) | PONV (-) | PONV (+) | PONV (-) | |
| 22 casos | 159 casos | 92 casos | 252 casos | 76 casos | 102 casos | |
| NVIO n ( %) | 0 (0.0) | 0 (0.0) | 3 (3.26) | 3 (1.19) | 62 (81.58) | 72 (70.59) |
| Edad (años) Rango Mediana (Q1 a Q3) |
24 a 41 33 (31 a 36)1 |
18 a 43 33 (30 a 36) |
18 a 41 26 (24 a 29) |
16 a 42 26 (22 a 30) |
14 a 44 27 (22 a 31) |
15 a 43 27 (23 a 30) |
| Antecedente de NVPO n ( %) | 0 (0.0) | 0 (0.0) | 12 (13.04) | 22 (8.73) | 27 (35.53) | 36 (35.29) |
| IMC (kg/m2) Rango Mediana (Q1 a Q3) |
20.45 a 33.78 29.45 (24.97 a 31.43) |
19.61 a 35.38 28.60 (26.22 a 31.14) |
22.32 a 43.00 29.46 (27.51 a 33.40) |
19.13 a 43.96 29.55 (26.59 a 32.82) |
20.27 a 44.00 29.33 (27.02 a 33.61) |
19.47 a 44.92 29.41 (25.81 a 33.25) |
| PRN (gramos) Rango Mediana (Q1 to Q3) |
1.600 a 3.440 2.935 (2.525 a 3.190) |
1.700 a 3.500 2.930 (2.600 a 3.180) |
1.360 a 4.210 3.115 (2.665 a 3.555) |
1.635 a 4.185 3.150 (2.820 a 3.550) |
1.740 a 4.240 3.215 (2.955 a 3.525) |
2.100 a 4.700 3.130 (2.770 a 3.550) |
IMC: Índice de masa corporal; NVIO: Náuseas y vómito intraoperatorio; NVPO: Náuseas y vómito posoperatorio; PRN: Peso del recién nacido.
Fuente: Autores.
Con los datos obtenidos se construyó una escala pronóstica para facilitar su uso e interpretación, y se desarrollaron diferentes formatos de presentación (Tabla de puntuación gráfica y nomograma), según las sugerencias propuestas por Bonnett et al. 23 (Figura 3).
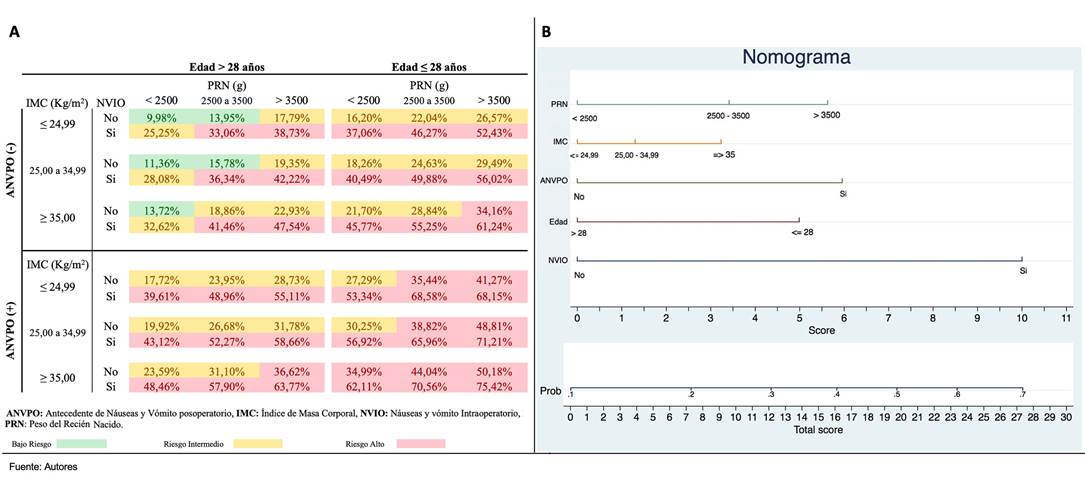
A: Tabla gráfica de puntuación para NVPO, B: Nomograma para NVPO. Fuente: Autores.
Figura 3 Formatos de presentación del modelo de predicción desarrollado
Para el uso de las tablas se incluye un caso a modo de ejemplo. Mujer de 26 años de edad, con 37 semanas de gestación, IMC de 24,44 kg/m2, con ANVPO, quien desarrolla NVIO y con peso del RN de 2.870 g.
Tendrá una probabilidad de desarrollar el desenlace del 68,58% según la tabla de puntuación gráfica y de acuerdo con el nomograma, tendrá un puntaje de 24,5 al que le corresponde una probabilidad del desenlace de 63 %, aproximadamente.
DISCUSIÓN
Se realizó un estudio prospectivo para desarrollar y validar un modelo de predicción pronóstica para NVPO en cesárea bajo anestesia espinal. El modelo incluyó como predictores el desarrollo de náuseas y vómito intraoperatorios, edad menor de 28 años, antecedentes de náuseas y vómito en un procedimiento quirúrgico previo, el índice de masa corporal de la madre y el peso del recién nacido. El modelo mostró una calibración adecuada, pero una baja discriminación 24.
La incidencia de NVPO fue del 27%, en estudios previos se han identificado incidencias entre 30% y 50% para anestesia general (AG), con valores menores para anestesia regional (7% a 18%) 1,5,11,25-27).
Sin embargo, debido a condiciones inherentes al embarazo y al uso rutinario de morfina espinal, se ha reportado que la incidencia de NVPO en cesárea es más alta, aunque aún no hay disponible un porcentaje generalizable 2,3,28. Los informes lo ubican entre 23% y 79% dependiendo de los diferentes regímenes de analgesia y profilaxis de NVPO utilizados 2.
El momento y el número de mediciones del desenlace difieren entre los estudios, con un periodo de observación que por lo general no excede las 24 horas 2,10,27. En el presente estudio, el desenlace se midió a las seis horas posoperatorias para desarrollar un modelo de predicción durante la estancia de las pacientes en la UCPA.
Se identificaron tres predictores importantes: NVIO, edad < 28 años y ANVPO. Dos variables más se incluyeron en el modelo, IMC y PRN, ya que mejoraron levemente la discriminación y de forma importante la calibración. El resto de las variables no demostraron ser predictores independientes para NVPO en el parto por cesárea bajo anestesia espinal, a pesar de haberse demostrado una fuerte asociación con el desenlace en otras poblaciones 1,10.
Se construyeron dos formatos diferentes de escalas pronósticas con el objetivo de permitir al lector la selección de aquella que presente la mayor facilidad de uso e interpretación, según sus necesidades y preferencias.
Se han estudiado pocas variables como factores de riesgo para NVPO en el parto por cesárea. Chao et al. 29 encontraron que el uso de medicamentos antieméticos durante y después de la cirugía y su uso en la terapia multimodal frente a la terapia única estaban asociadas a una disminución en la incidencia y la severidad de las NVPO (p: <0,001 y p: 0,018, respectivamente), mientras que Balla et al. 30 identificaron tres factores de riesgo para NVPO en una unidad obstétrica: no fumador, infusión de oxitocina en el quirófano y morfina espinal. En el presente estudio no se midió el efecto de la oxitocina y todas las pacientes recibieron morfina espinal. No obstante, ser no fumador y el uso de metoclopramida no fueron factores de riesgo ni predictores en la población de estudio.
En la población pediátrica y no obstétrica bajo AG, la edad y ANVPO han demostrado ser predictores y factores de riesgo para NVPO 1,10. Aunque su comportamiento en la población obstétrica era desconocida, en el presente estudio demostraron ser claros factores tanto de riesgo como de predicción para NVPO. Además, hasta donde se sabe, este estudio es el primero que explora las NVIO, el IMC y el PRN como nuevos factores de riesgo en la población obstétrica 3,29,30.
El tabaquismo es un factor protector importante para el desarrollo de NVPO 1,10, pero en la población obstétrica ha sido poco estudiado y su asociación no ha sido claramente establecida 30. En este estudio, el 5,55% de los pacientes manifestó haber fumado alguna vez y solo el 2,27% haber fumado durante el embarazo. Creemos que existe un subreporte debido a la desaprobación social del cigarrillo durante el embarazo, lo que podría haber afectado el modelo pronóstico final al no incluir un predictor importante.
Se ha demostrado que el AC, TQ y LIVA han demostrado tener un impacto en el desarrollo de NVPO en la población no obstétrica bajo AG 1,10. Sin embargo, en el presente estudio ninguno de ellos demostró ser un predictor o factor de riesgo de NVPO en el parto por cesárea.
En general, la eficacia antiemética de la metoclopramida es incierta, pero puede ser efectiva para la prevención de NVPO bajo AG, especialmente en dosis altas 1,27. A pesar de esto, Domínguez et al. 31 encontraron que no parece ser eficaz para la profilaxis de NVPO en pacientes embarazadas que recibieron morfina espinal, lo cual es compatible con lo encontrado en este estudio.
El AM, TA y la aplicación preoperatoria o intraoperatoria de opioides, no han demostrado ser factores de riesgo de NVPO en la población no obstétrica bajo AG 1,10,11. Iguales resultado se obtuvieron para el parto por cesárea.
En la validación interna no se observó sobreajuste, evidenciado en las similitudes en las gráficas de calibración, discriminación e intervalos de confianza de los modelos Bootstrap con el modelo desarrollado, posiblemente debido a la gran cantidad de pacientes que se incluyeron para el desarrollo del modelo; por otro lado, los autores del estudio consideran que la baja discriminación obtenida se debe al subregistro del tabaquismo o la ausencia de otras variables que no se tuvieron en cuenta, como la indicación de la cesárea, el número de embarazos, el uso de oxitocina y otras características sociodemográficas.
En el estudio se logran identificar cuatro limitaciones importantes, la tubectomía concomitante con la cesárea solo se realizó de forma rutinaria en una de las instituciones incluidas en el presente estudio. Teniendo en cuenta que es un factor de riesgo y predictor importante para NVPO, debido a su conocido efecto de estimulación visceral, no permitió una evaluación adecuada de esta variable ya que solo la mitad de la población habría estado disponible para el análisis.
El uso de poblaciones de entornos de centros de atención obstétrica de tercer nivel podría limitar la extrapolación a pacientes de atención primaria.
El bajo puntaje de discriminación del modelo final. La calibración y la discriminación son propiedades estadísticas que caracterizan el desempeño de un modelo de predicción, pero ninguno de estos captura las consecuencias clínicas de a un nivel particular 13. Por lo tanto, los autores de este estudio creen que no influye de forma importante en la utilidad del modelo desarrollado. Aun así, estos datos son importantes, ya que permitirán en el futuro la comparación con nuevos modelos que complementen o sustituyan el aquí desarrollado.
La inclusión de solo pacientes que recibieron morfina espinal y dexametasona para profilaxis de NVPO es inicialmente una desventaja, porque no todos los anestesiólogos utilizan los mismos medicamentos descritos en este artículo. Sin embargo, dado que este régimen está acorde con lineamientos y recomendaciones internacionales, en el futuro esto podría convertirse en una fortaleza al permitir una mayor extrapolación de los datos.
También se logran identificar varias fortalezas importantes en el estudio, su naturaleza prospectiva y la posibilidad de desarrollar un modelo con un tamaño de muestra suficiente, donde se obtuvieron 12,66 desenlaces por variable estudiada.
La escala pronóstica desarrollada puede ser útil en la práctica clínica porque no requiere pruebas de laboratorio, las preguntas son fáciles de responder y es fácil de aplicar, ya que no se requieren cálculos dispendiosos.
Las recomendaciones para el manejo de las NVPO en la población no obstétrica están dirigidas a la identificación y clasificación de pacientes de riesgo intermedio y alto para implementar terapias guiadas por objetivos que permitan mayor satisfacción y reducción de complicaciones y costos 1.
El presente estudio es el primer paso para introducir estas recomendaciones en el parto por cesárea; por lo tanto, es necesario continuar la investigación al respecto para confirmar el papel de los factores identificados en este estudio, validar de forma externa el modelo desarrollado y, de ser necesario, ajustarlo y someterlo a evaluación, para así lograr un modelo de predicción que permita una identificación temprana de pacientes que son susceptibles de recibir un manejo que reduzca la incidencia de NVPO en parto por cesárea.
RESPONSABILIDADES ÉTICAS
Aval de comité de ética
Este estudio recibió la aprobación ética, acta N.° 019 de diciembre 1 de 2016, del Comité de Bioética del Instituto de Investigaciones Médicas de la Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
Protección de personas y animales
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
RECONOCIMIENTOS
Contribución de los autores
MDLP y OLG: Participó en el diseño, análisis e interpretación, así como en la redacción y revisión del manuscrito.
DCA: Participó en el análisis e interpretación, así como en la revisión del manuscrito.
ADLP: Participó en el diseño y ejecución del proyecto, así como en la redacción y revisión del manuscrito.
JJA y RM: Participó en la ejecución del proyecto, así como en la revisión del manuscrito.
Agradecimientos
A la Sociedad Colombiana de Anestesiología y Reanimación (S.C.A.R.E.) por su acompañamiento, apoyo logístico y económico durante la concepción y desarrollo del proyecto; también, a la Clínica del Prado y la Clínica Universitaria Pontificia Bolivariana, por permitirnos desarrollar este proyecto en sus instalaciones, además de todo el apoyo brindado en la identificación y recolección de los datos de las pacientes.
REFERENCIAS
1. Gan TJ, Belani KG, Bergese S, Chung F, Die-munsch P, Habib AS, et al. Fourth consensus guidelines for the management of postoperative nausea and vomiting. Anesth Analg. 2020;131(2):411-48. doi: https://doi.org/10.1213/ANE.0000000000004833 [ Links ]
2. Griffiths JD, Gyte GM, Paranjothy S, Brown HC, Broughton HK, Thomas J. Interventions for preventing nausea and vomiting in wo-men undergoing regional anaesthesia for caesarean section. Cochrane Database of Systematic Reviews. 2012(9). doi: http://dx.doi.org/10.1002/14651858.CD007579.pub2 [ Links ]
3. Jelting Y, Klein C, Harlander T, Eberhart L, Roewer N, Kranke P. Preventing nausea and vomiting in women undergoing regional anesthesia for cesarean section: challenges and solutions. Local Reg Anesth. 2017;10:83-90. doi: https://doi.org/10.2147/LRA.S111459 [ Links ]
4. Allen TK, Jones C, Habib AS. Dexamethasone for the prophylaxis of postoperative nausea and vomiting associated with neuraxial morphine administration: A systematic review and meta-analysis. Anesth Analg . 2012;114(4):813-22. doi: https://doi.org/10.1213/ANE.0b013e318247f628 [ Links ]
5. Apfel CC, Láàrà E, Koivuranta M, Greim CA, Roewer N. A simplified risk score for predicting postoperative nausea and vomiting: conclusions from cross-validations between two centers. Anesthesiology. 1999;91(3):693-700. doi: https://doi.org/10.1097/00000542-199909000-00022 [ Links ]
6. Kilpatrick SJ, Menard MK, Zahn CM, Callaghan WM. Obstetric Care Consensus #9: Levels of Maternal Care: (Replaces Obstetric Care Consensus Number 2, February 2015). Am J Obstet Gynecol. 2019 Dec 1;221(6):B19-30. doi: https://doi.org/10.1016/i.ajog.2019.05.046 [ Links ]
7. Bollag L, Lim G, Sultan P Habib AS, Landau R, Zakowski M, et al. Society for Obstetric Anesthesia and Perinatology: Consensus Statement and Recommendations for Enhanced Recovery After Cesarean. Anesth Analg . 2021;132(5):1362-77. doi: https://doi.org/10.1213/ANE.0000000000005257 [ Links ]
8. Gadsby R, Barnie-Adshead AM, Jagger C. Pregnancy nausea related to women's obstetric and personal histories. Gynecol Obstet Invest. 1997;43(2):108-11. doi: https://doi.org/10.1159/000291833 [ Links ]
9. Pierre S, Whelan R. Nausea and vomiting after surgery. Continuing Education in Anaesthesia, Critical Care & Pain. 2013;13(1):28-32. doi: https://doi.org/10.1093/biaceaccp/mks046 [ Links ]
10. Apfel CC, Heidrich FM, Jukar-Rao S, Jalota L, Hornuss C, Whelan RP, et al. Evidence-based analysis of risk factors for postoperative nausea and vomiting. Br J Anaesth. 2012;109(5):742-53. doi: https://doi.org/10.1093/bja/aes276 [ Links ]
11. Apfel CC, Kranke P Eberhart LH, Roos A, Roewer N. Comparison of predictive models for postoperative nausea and vomiting. Br J Anaesth . 2002;88(2):234-40. doi: https://doi.org/10.1093/bja/88.2.234 [ Links ]
12. Maharaj CH, Kallam SR, Malik A, Hassett P Grady D, Laffey JG. Preoperative intravenous fluid therapy decreases postoperative nausea and pain in high risk patients. Anesth Analg . 2005;100(3):675-82. doi: https://doi.org/10.1213/01.ANE.0000148684.64286.36 [ Links ]
13. Moons KG, Altman DG, Reitsma JB, Ioannidis JP, Macaskill P, Steyerberg EW, et al. Transparent reporting of a multivariable prediction model for individual prognosis or diagnosis (TRIPOD): explanation and elaboration. AnnlnternMed. 2015;162(1):W1-73. doi: https://doi.org/10.7326/M14-0698 [ Links ]
14. Peduzzi P Concato J, Kemper E, Holford TR, Feinstem AR. A simulation study of the number of events per variable in logistic regression analysis. J Clin Epidemiol. 1996;49(12):1373-9. doi: https://doi.org/10.1016/S0895-4356(96)00236-3 [ Links ]
15. Gehling M, Tryba M. Risks and side-effects of intrathecal morphine combined with spinal anaesthesia: A meta-analysis. Anaesthesia. 2009;64(6):643-51. doi: https://doi.org/10.1111/j.1365-2044.2008.05817.X [ Links ]
16. Paul P Pennell ML, Lemeshow S. Standardizing the power of the Hosmer-Lemeshow goodness of fit test in large data sets. Statist Med. 2013;32(1):67-80. doi: https://doi.org/10.1002/sim.5525 [ Links ]
17. Núñez E, Steyerberg EW, Núñez J. Regression modeling strategies. Rev Esp Cardiol. 2011;64(6):501-7. doi: https://doi.org/10.1016/j.recesp.2011.01.019 [ Links ]
18. Hosmer DW, Lemeshow S, Sturdivant RX. Model-building strategies and methods for logistic regression. Applied logistic regression. Third Edit. John Wiley & Sons, Inc.; 2013. pp. 89-152. doi: https://doi.org/10.1002/9781118548387 [ Links ]
19. Sauerbrei W, Royston P Binder H. Selection of important variables and determination of functional form for continuous predictors in multivariable model building. Statist Med . 2007;26:5512-28. doi: https://doi.org/10.1002/sim.3148 [ Links ]
20. Royston P, Moons KGM, Altman DG, Vergouwe Y. Prognosis and prognostic research: Developing a prognostic model. BMJ. 2009;338:b604. doi: https://doi.org/10.1136/bmj.b604 [ Links ]
21. Steyerberg EW. Selection of main effects. En: Clinical Prediction Models: A Practical approach to development, validation, and updating. New York, NY: Springer New York; 2009. pp. 191-211. doi: https://doi.org/10.1007/978-0-387-77244-8_11 [ Links ]
22. Steyerberg EW. Study design for prediction models. En: Clinical prediction models: A practical approach to development, validation, and updating [Internet]. New York, NY: Springer New York ; 2009. pp. 33-52. doi: https://doi.org/10.1007/978-0-387-77244-8_3 [ Links ]
23. Bonnett LJ, Snell KIE, Collins GS, Riley RD. Guide to presenting clinical prediction models for use in clinical settings. BMJ. 2019;365:1737. doi: https://doi.org/10.1136/bmj.l737 [ Links ]
24. Hosmer DW, Lemeshow S, Sturdivant RX. Assessing the Fit of the Model. In: Applied logistic regression. John Wiley & Sons, Inc.; 2013. pp. 153-225. doi: https://doi.org/10.1002/9781118548387.ch5 [ Links ]
25. Apfel CC. Postoperative nausea and vomiting. In: Miller Anestesia. 8th ed. Elsevier; 2015. pp. 2947-73. [ Links ]
26. Koivuranta M, Láãrà E, Snãre L, Alahuhta S. A survey of postoperative nausea and vomiting. Anaesthesia. 1997;52(5):443-9. doi: https://doi.org/10.1111/j.1365-2044.1997.117-az0113.x [ Links ]
27. Weibel S, Rücker G, Eberhart LHJ, Pace NL, Hartl HM, Jordan OL, et al. Drugs for preventing postoperative nausea and vomiting in adults after general anaesthesia: a network meta-analysis. Cochrane Database of Systematic Reviews . 2020;2020(11). doi: https://doi.org/10.1002/14651858.CD012859.pub2 [ Links ]
28. Marrón-Peña M. Náusea y vómito perioperatorio en anestesia obstétrica y ginecológica. Revista Mexicana de Anestesiología. 2013;36(2):348-55. [ Links ]
29. Chao Y, Evangelista LS, Rietzel KL, Artinian S, Mullen K. Examining the predictors of postoperative nausea and vomiting in women following cesarean delivery. J Obstet, Gynecol Neonatal Nurs. 2013;42:S84. doi: https://doi.org/10.1111/1552-6909.12174 [ Links ]
30. Balla S, Baraz R. Audit of postoperative nausea and vomiting in obstetrics. Anaesthesia. 2014;69(Supplement 3):25. [ Links ]
31. Domínguez JE, Habib AS. Prophylaxis and treatment of the side-effects of neuraxial morphine analgesia following cesarean delivery. Curr Opin Anaesthesiol. 2013;26(3):288-95. doi: https://doi.org/10.1097/ACO.0b013e32836 [ Links ]
Apoyo financiero y patrocinio Sociedad Colombiana de Anestesiología y Reanimación (S.C.A.R.E.). Recursos propios.
Recibido: 19 de Septiembre de 2022; Aprobado: 21 de Marzo de 2023; : 23 de Mayo de 2023











 text in
text in