Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad Nacional de Salud Pública
Print version ISSN 0120-386X
Rev. Fac. Nac. Salud Pública vol.30 supl.1 Medellín Sep./Dec. 2012
INVESTIGACIONES
Impacto de la vacunación contra hepatitis B en el Amazonas colombiano 18 años después de su introducción
Impact of hepatitis bvaccination in the colombian Amazon 18 years after its implementation
Alexandra Porras R.1; Fernando De la Hoz R.2
1 Universidad Nacional de Colombia. Facultad de Medicina. Doctorado en Salud Pública. Bogotá, Colombia. Correo electrónico: aporraslu@yahoo.es
2 Doctor en epidemiología de enfermedades infecciosas. University of London
Porras A,Impacto de la vacunación contra hepatitis B en el Amazonas colombiano 18 años después de su introducción, 2009. Rev. Fac. Nac. Salud Pública 2012; 30 (supl 1): 32-35
Introducción
La hepatitis B es un problema endémico de salud pública en muchos países alrededor del mundo. Se estima que 350 millones de personas son portadoras del virus de hepatitis B (vhb). Una vacuna altamente efectiva ha estado disponible desde principios de los años ochenta y muchos países la están utilizando para controlar la infección. Sin embargo, todavía hay muchas áreas donde la vacuna no está en uso [1].
América Latina es considerada un área de baja endemicidad para la infección por hepatitis B, pero hay áreas de alta endemicidad donde la infección por el vhb se produce a una edad temprana. Una de las áreas más conocidas como endémica es la cuenca amazónica compartida por Brasil, Colombia, Venezuela y Perú [2].
En un estudio de Thêmis R. Silveira, et al [3], en el que se determinó la seroprevalencia de hepatitis B en seis países de América Latina: Argentina (las ciudades de Buenos Aires y Córdoba); Brasil (Río de Janeiro y Porto Alegre, en el sureste; Manaos, en la cuenca del Amazonas; y Fortaleza, en el noreste ); Chile (al norte de Santiago de Chile); República Dominicana (en Santo Domingo); México (en las ciudades en el norte, centro y regiones del sur del país); y Venezuela (Caracas), se encontró que la seroprevalencia general más alta fue en República Dominicana (21,4%), seguido por Brasil (7,9%), Venezuela (3,2%) y Argentina (2,1%).
Los niveles más bajos se encontraron en México (1,4%) y Chile (0,6%). En las diferentes regiones de Brasil se encontró una amplia gama de seroprevalencia, con una alta proporción en Manaos (21%), seguido de Porto Alegre (7,5%), Río de Janeiro (5,5%) y Fortaleza (1,2%). La única diferencia significativa en la seroprevalencia entre hombres y mujeres fue en Brasil, con una seroprevalencia más alta para los varones (OR=1,32, IC 95%: 1,01-1,65, p=0,02), y en República Dominicana, con una mayor tasa de las mujeres (OR=2.19, IC 95%: 1,05-3,07, p=0,01) [3].
La mayoría de los países de América Latina han introducido la vacuna contra hepatitis B dentro del programa ampliado de inmunizaciones (pai) pero pocas evaluaciones se han realizado sobre la eficacia de esta medida.
Colombia comenzó la vacunación contra la hepatitis B en 1992, para niños de 0 a 5 años que viven en zonas endémicas. En los primeros diez años del programa se utilizó una vacuna monovalente contra la hepatitis B recombinante en un esquema de tres dosis (2, 4, 6 meses). La presente propuesta tiene como objetivo contribuir en mayor medida a la evaluación de la política de control de la infección por hepatitis B, así como arrojar luz sobre la epidemiología de otros agentes de la hepatitis viral en áreas endémicas.
Aunque muchos estudios sobre la prevalencia de la hepatitis B se han llevado a cabo en Colombia en diferentes zonas del país, hay algunos aspectos de la epidemiología de esta enfermedad que siguen siendo desconocidos. Uno de los más importantes es el papel de la transmisión perinatal y la prevalencia de portadores de hepatitis B. Se desconoce cuál es la prevalencia de hbag en mujeres en edad fértil. Las políticas de vacunación contra la hepatitis B en Colombia no han tenido en cuenta este aspecto de la epidemiología del virus.
En las zonas endémicas, que se supone los niños son vacunados poco después del parto, se desconoce si esto se hace de forma sistemática. Hacer caso omiso de este factor podría llevar a un déficit importante en los objetivos de la vacunación, especialmente si las mujeres tienen una alta prevalencia de hbeag. En Lombok (Indonesia), los niños vacunados más de 7 días después del nacimiento tuvieron una prevalencia de 3% de HBSAG en comparación con el 1,4% en los niños vacunados en los primeros 7 días del nacimiento (p <0,001) [4].
El cumplimiento de los calendarios de vacunación es importante dada la relación de efectividad de la vacuna con el número de dosis aplicadas. Por esto es necesario identificar los factores que conducen a la dificultad de acceso a los servicios de salud locales y las posibles soluciones que garanticen un adecuado programa de vacunación a los niños en poblaciones endémicas.
Además de la barrera geográfica, es posible que las características sociales, culturales y económicas de las poblaciones objetivo impacten en las bajas coberturas de vacunación o en el cumplimiento de los calendarios de vacunación. Un estudio realizado en China ha encontrado diferencia en los títulos de anticuerpos entre las personas de diferentes grupos étnicos [5]. Colombia tiene una gran diversidad de grupos étnicos y algunos de ellos han sido afectados por el vhb. Es importante evaluar si la respuesta a la vacuna varía entre ellos. Si lo hace, entonces algunas poblaciones pueden necesitar diferentes números de dosis.
Dado lo anteriormente mencionado, se requiere ahondar en el conocimiento de cuál es la prevalencia de la infección por hepatitis B en una zona de alta endemicidad posterior a la introducción de la vacunación contra este virus y evaluar la prevalencia de portadores crónicos de vhb en la zona que estén relacionados no solo con la presencia del marcador serológico de antígeno de superficie positivo sino además con la posible relación existente con mutantes del virus por deleción del cromosoma S en el virus.
Dado que la efectividad de la vacunación está relacionada con el número de dosis de vacuna recibidas, se debe revisar el cumplimiento de los esquemas teniendo en cuenta la edad y la formulación de la vacuna. Antes del año 2002 se utilizaba vacuna monovalente y después de este año vacuna pentavalente.
Además, teniendo en cuenta que la vacunación depende de la accesibilidad a servicios de salud, es importante establecer cuáles pueden ser los factores asociados al incumplimiento de la vacunación que estén relacionados con los servicios de salud.
Todos estos aspectos permitirán responder la pregunta relacionada: ¿Cuál es el impacto epidemiológico de la vacunación contra hepatitis B en una zona de alta endemicidad por vhb (Amazonas), después de 20 años de la introducción de la vacuna?
Entre 1998 y 2000 se llevó a cabo en la Amazonia colombiana un estudio de evaluación del impacto del programa de vacunación. Se encontró una reducción del 70% de los portadores de vhb en comparación con los niveles históricos a pesar de la adherencia con los esquemas de vacunación normados por el PAI [6-8].
A partir de 2001, una vacuna pentavalente de hepatitis B combinada con dpt y hib, se ha utilizado con una dosis adicional de vacuna monovalente destinada al momento de nacer. La introducción de la vacuna pentavalente ha tenido un impacto significativo en la cobertura de vacunación promedio nacional contra este virus, pues aumentó de 70% a 85%. Es importante saber si el nuevo sistema ha mejorado el control de la infección.
Objetivos
Los objetivos planteados en este proyecto son:
- 1) Estimar la seroprevalencia de hepatitis B en la Amazonia colombiana con el fin de evaluar el impacto de la vacuna.
- 2) Estimar la prevalencia de la infección por hepatitis B y de portadores sanos en niños de 1 a 10 años en la Amazonia colombiana, de una zona endémica antigua de Colombia.
- 3) Evaluar el impacto de los cambios en los horarios de vacunación contra la hepatitis B y la formulación de la vacuna en Colombia.
- 4) Estimar la cobertura de la vacuna contra la hepatitis B, monovalente y pentavalente, en tres áreas de alta endemicidad de Colombia.
- 5) Identificar los factores individuales relacionados con la falta de cumplimiento de calendario de vacunas para la hepatitis B.
- 6) Identificar los mutantes del virus de la hepatitis B y su impacto potencial sobre la eficacia de la vacunación.
- 7) Estimar la mortalidad por enfermedades hepáticas y hepatitis viral en Colombia desde 1990 a 2008.
Metodología
Se realizará un estudio de corte transversal de base poblacional con pruebas serológicas. Se llevará a cabo en tres áreas del departamento de Amazonas. Todos estos lugares se conocen como zonas endémicas de alta para la infección por hepatitis B y los datos históricos están disponibles antes de la introducción de la vacunación contra el virus.
El estudio se realizará en Leticia, Puerto Nariño y Araracuara que forman parte de la región amazónica de Colombia. La mayor parte de la población está compuesta por los sobrevivientes de los aborígenes de América.
Su población es de alrededor 25.000 habitantes. El clima es tropical, con lluvias frecuentes, y salvajes bosques húmedos tropicales cubren más del 90% de estas áreas.
La gente vive de la pesca, la caza y los cultivos. Antes de la introducción de vacunas, la prevalencia de la infección por hepatitis B y de portadores sanos fue muy alta en las zonas rurales, más del 60% de infección y de 8 a 12% de portadores. La hepatitis B se introdujo probablemente en 1900, cuando la explotación del caucho trajo decenas de extranjeros a la selva amazónica [9].
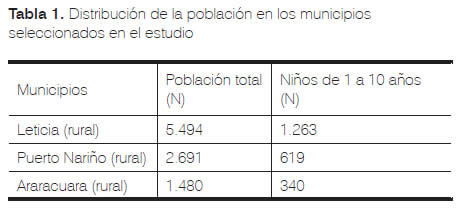
La población de estudio la conforman los niños entre 1 a 10 años de edad que viven en zonas rurales y urbanas de los municipios seleccionados (tabla 1).
La muestra tendrá en cuenta que en estas poblaciones hay niños vacunados de dos regímenes: 1) Niños menores de 7 años deberían haber recibido una dosis de vacuna monovalente al nacer, seguida por tres dosis de la pentavalente a los 2, 4 y 6 meses; 2) Los niños mayores de 7 años se supone que han recibido al menos tres dosis de vacuna contra la hepatitis B monovalente a los 0, 2 y 6 meses.
De la Hoz et al en el año 2008 encontraron que la prevalencia de portadores entre los niños de 1 a 5 años de edad fue de 0,7%, una disminución de 70% en comparación con la prevalencia antes de que la vacuna fuera introducida [7].
Un tamaño de muestra de 2.000 niños, 1.000 de cada grupo de edad, será suficiente para probar la hipótesis de que el nuevo régimen con la pentavalente tiene una eficacia similar a la monovalente, ya que sería capaz de detectar incluso las diferencias relativas del 3% en la prevalencia (cálculo realizado en StatCalc de epiinfo v 3.5.1 2008).
Ese número será suficiente para estimar la prevalencia de la hepatitis A, E o C con una precisión de 3%, si suponemos que la frecuencia de estos agentes se encuentra entre 1 y 6% (n=1.800).
La muestra de 2.000 niños será seleccionada de todas las áreas de la Amazonia. La muestra estará conformada por todos los niños que viven en Araracuara, porque es el área con mayor prevalencia, y los restantes serán seleccionados de una muestra aleatoria por conglomerado en el área urbana y rural de Leticia y Puerto Nariño.
Los criterios de inclusión de los participantes del estudio son: vivir en el área de estudio durante al menos 6 meses; consentimiento de los padres para participar en el estudio; edad entre 1 y 10 años.
Los criterios de exclusión son: los padres o tutor legal no aceptan participar en el estudio; la imposibilidad de obtener muestras de sangre en el brazo.
Se aplicará un cuestionario para recoger las variables relacionadas con las características demográficas de los participantes, los factores de riesgo para la hepatitis viral y antecedentes clínicos. Las fechas de vacunación para la hepatitis B se registrarán en un formulario separado.
Las definiciones de caso a utilizar serán: 1) Infección por hepatitis B: infectados con el vhb, se define como cualquier persona con un marcador de antiHBC positivo. 2) Portador sano de hepatitis B: un portador de la hepatitis B se define como alguien positivo para ambos marcadores, antiHBC y HBSAG.
Se realizarán pruebas de laboratorio para la detección del genoma del vhb, se llevarán a cabo en muestras de suero correspondientes a los pacientes que presentan dos marcadores serológicos positivos para la infección por el vhb por elisa (anti-HBC, HBSAG).
Para tal efecto, el genoma viral se aislará con el reactivo Trizol. Cebadores específicos para el vhb gen s se utilizan para detectar el vhb por pcr anidada hemi (s1r, ys1, ys2). Este análisis se desarrollará con el programa y la herramienta BioEdit ClustalX para determinar la presencia de mutaciones y variantes de escape.
La exposición principal en este estudio es el estado de vacunación contra la hepatitis B. Los niños se clasifican como esquema completo para la edad si han recibido al menos tres dosis de la vacuna contra la hepatitis B, ya sea mono o pentavalente.
Los menores de 7 años serán clasificados como esquema completo para la edad si reciben una dosis de hepatitis B al nacimiento y luego tres dosis adicionales antes de llegar a los 6 meses de edad.
Los niños mayores de 7 años se clasifican como oportunamente vacunados si han recibido tres dosis de la vacuna antes de cumplir 6 meses de edad.
El tiempo desde el nacimiento hasta la primera dosis debe tomarse en cuenta para el análisis de la eficacia. La principal hipótesis del estudio es que la prevalencia de portadores de antígeno de superficie de hepatitis B es inferior al 1% por efecto de la vacunación masiva contra hepatitis B.
Varios análisis se llevarán a cabo en este estudio. El principal es evaluar la relación entre las características de vacunación contra la hepatitis B y la hepatitis B y el estado de portador sano. Para ello, la prevalencia de infección por el virus y los portadores se medirá y se tendrán en cuenta las características de vacunación (tiempo entre el nacimiento y la primera dosis, pentavalente o monovalente), y el tiempo entre la primera dosis y la tercera (solo para pentavalente en niños menores de 7 años de edad y monovalente en los niños mayores de 6 años).
Las diferencias de la condición de infección entre las diferentes categorías de vacunación se evaluará mediante razones de prevalencia (RP) y sus intervalos de confianza (IC95%). Esas diferencias se ajustarán por edad, sexo, zona geográfica, características sociales y las características demográficas de las familias de los niños mediante el análisis multivariado y la regresión logística binomial.
Se calcularán los intervalos de confianza del 95% para las medidas descriptivas y medidas del efecto teniendo en cuenta los conglomerados. Una variable ecológica se creará para reflejar la prevalencia general de infección por la comunidad y el control de la influencia de las características individuales por la magnitud de la infección en la comunidad. Los modelos jerárquicos se utilizarán para evaluar la prevalencia en la comunidad de la infección, con relación a los factores sociales y contextos ambientales que podrían afectar los resultados.
Un segundo análisis se centrará en la identificación de factores relacionados con la cobertura de vacunación contra la hepatitis B. Los niños con esquema de vacunación completo y oportuno serán comparados contra los niños con vacunación incompleta o extemporánea con relación a las variables socioeconómicas y demográficas tales como edad, sexo, origen étnico, educación de la madre, estado de salud de seguridad social (estar afiliado o no a la seguridad de la salud), distancia del centro de salud, y los indicadores de pobreza.
Medidas de efecto descriptivo y epidemiológico se calcularán teniendo en cuenta la agrupación de datos. El análisis multivariante se llevará a cabo en caso de apropiación.
Un tercer análisis se realizará para identificar la prevalencia de otros virus de hepatitis, así como los factores sociales y demográficos relacionados con la infección por ellos. La prevalencia de la infección con hepatitis C, D, E y A se calculará en general y estratificada por categorías de edad, sexo, origen étnico, zonas geográficas, características sociales, económicas y demográficas de los niños y sus familias.
Un modelo catalizador se construirá con base en la prevalencia de la hepatitis A por grupos de edad, para estimar la fuerza de la infección de hepatitis A en niños de zonas urbanas y rurales de 1 a 10 años de edad.
Resultados esperados
Prevalencia de la infección por hepatitis B y de portadores sanos en niños de 1 a 10 años en la Amazonia de una zona endémica de Colombia.
Impacto de los cambios en los horarios de vacunación contra la hepatitis B y la formulación de la vacuna en Colombia.
Estimación de la cobertura de la vacuna contra la hepatitis B, monovalente y pentavalente, en la Amazonia colombiana.
Identificación de los factores individuales relacionados con la falta de cumplimiento de calendario de vacunas para la hepatitis B. Identificación de los mutantes del virus de la hepatitis B y su impacto potencial sobre la efectividad de la vacunación.
Estimación de la mortalidad por enfermedades hepáticas y hepatitis viral en Colombia desde 1990 a 2008.
Referencias
1 Mc Mahon J. Natural History of Chronic Hepatitis B - Clinical Implications. Medscape J Med. 2008;10(4):91. [ Links ]
2 Dehesa Violante M, Nunez Natera R. Epidemiology of hepatitis B and C. Archives of Medical Research 2007;38:606-11. [ Links ]
3 Silveira Thêmis R, Fonseca José Carlos da, Rivera Luis, Fay Oscar H, Tapia Roberto, Santos José I, et al. Hepatitis B seroprevalence in Latin America. Rev Panam Salud Pública (serial on the Internet). 1999 Dec (cited 2011 Oct 12);6(6):378-383. [ Links ]
4 Ruff T, Gertig D, Otto B, et al. Lombok Hepatitis B model immunization project: Toward universal infant hepatitis B immunization in Indonesia. Journal of Infectious Diseases. 1995;171:290-6. [ Links ]
5 Hsu HM, Chen DS, Chuang CH, Lu JC, Jwo DM, Lee CC, Lu HC, Cheng SH, Wang YF, Wang CY, et al. Efficacy of a mass hepatitis B vaccination program in Taiwan. Studies on 3464 infants of hepatitis B surface antigen-carrier mothers. JAMA. 1988;260(15):2231-2235. [ Links ]
6 Martínez M, De la Hoz F, Jaramillo LS, et al. Seroepidemiología de la infección por el virus de la hepatitis B en niños de la Amazonia Colombiana. Biomédica 1991;11:20-24. [ Links ]
7 De la Hoz F, Perez L, De Neira M and Hall A. Eight years of hepatitis B vaccination in Colombia with a recombinant vaccine. Factors influencing hepatitis B infection and effectiveness. International Journal of Infectious Diseases 2008;12(2):183-189. [ Links ]
8 De la Hoz F, Perez L, Wheeler J.G, De Neira M, and Hall AJ. Vaccine coverage with hepatitis B and other vaccines in the Colombian Amazon: do health worker knowledge and perception influence coverage? Tropical Medicine and International Health 2005;10(4):322-329. [ Links ]
9 Pineda R. Holocausto en el Amazonas. Bogotá: Editorial Espasa Fórum, Editorial Planeta Colombiana; 2000. [ Links ]
Recibido: 27 de Febrero de 2012. Aprobado: 28 de Junio de 2012.