Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Biomédica
versão impressa ISSN 0120-4157versão On-line ISSN 2590-7379
Biomédica v.27 n.2 Bogotá abr./jun. 2007
Caracterización de dos brotes de fiebre tifoidea en Apartadó, Antioquia, 2005
Nora María Cardona-Castro 1, Miryan Margot Sánchez-Jiménez 1, Luz Yaned Usuga-Silva 1, Margarita Arboleda-Naranjo 1, Eliana Garzón 2, Aminta Vélez 3, Magdalena Wiesner 4, Nélida Muñoz 4, Clara Inés Agudelo 4
1 Instituto Colombiano de Medicina Tropical-CES, Sabaneta-Apartadó, Colombia
2
Facultad de Medicina, Instituto de Ciencias de la Salud-CES, Medellín, Colombia3
Hospital Regional Antonio Roldán Betancur, Apartadó, Colombia4
Grupo de Microbiología, Instituto Nacional de Salud, Bogotá, D. C., ColombiaRecibido: 12/09/06; aceptado: 27/03/07
Introducción.
La caracterización de los brotes de fiebre tifoidea es importante epidemiológicamente, debido a que esto permite la búsqueda de la fuente y el desarrollo de medidas de control.Objetivo. Describir un brote de fiebre tifoidea en el municipio de Apartadó y caracterizar fenotípica y genotípicamente los aislamientos de Salmonella Typhi relacionados con él.
Materiales y métodos. Se estudiaron 44 pacientes, a 15 de ellos se les tomaron muestras para hemocultivos y a 7, muestras para coprocultivos. Los aislamientos bacterianos se estudiaron con pruebas bioquímicas y serotipificación y se determinó el perfil de susceptibilidad a antibióticos. Los aislamientos se evaluaron genotípicamente por reacción en cadena de la polimerasa para los genes hilA, invA e IS-200, y por electroforesis en campo pulsado con XbaI. Se estudiaron ocho muestras de agua asociadas al brote por reacción en cadena de la polimerasa y cultivo para la búsqueda de Salmonella.
Resultados. A 15/44 pacientes se les confirmó el diagnóstico clínico de fiebre tifoidea, a 13 por hemocultivos y a 2 por coprocultivos positivos para S. Typhi. Todos los aislamientos de S. Typhi fueron sensibles a los antibióticos probados.
La reacción en cadena de la polimerasa confirmó la presencia de los genes hilA y invA e IS-200 en todos los aislamientos estudiados. La electroforesis en campo pulsado agrupó 10 aislamientos en el patrón COINJPP.X01.0035, tres en el patrón COINJPPX01.0002, uno COINJPP.X01.0012 y uno COINJPPX01.0037.
El estudio de aguas fue negativo para Salmonella spp.
Conclusiones. La electroforesis en campo pulsado estableció la presencia de dos brotes, que inicialmente, por epidemiología y pruebas fenotípicas del patógeno, habían sido descritos como uno solo. Además, permitió diferenciar dos aislamientos de origen clonal diferente, que indicaron casos aislados. No se pudo corroborar la fuente de infección en el agua.
Palabras clave: brotes de enfermedades, fiebre tifoidea/epidemiología, Salmonella Typhi, infecciones por Salmonella, técnica de tipificación bacteriana, serotipificación.
Characterization of two typhoid fever outbreaks in Apartadó, Antioquia, 2005
Introduction. The characterization of typhoid fever outbreaks is important because it is necessary to find the source of the infection and development control measures.
Objective. A typhoid fever outbreak is described from Apartadó and the Salmonella Typhi isolates characterized by phenotypic and genotypic methods.
Materials and methods. From 44 patients, 15 blood cultures and 7 stools cultures were recovered. Phenotypic identification of isolates was done by biochemical and serological tests, and antibiotic susceptibility was tested. Genes hilA, invA and the IS200 marker were evaluated by polymerase chain reaction; pulsed field gel electrophoresis was used for the XbaI gene. Eight water samples were examined by polymerase chain reaction and culture methods in order to isolate Salmonella spp.
Results. Fifteen patients were confirmed for typhoid fever, 13 by blood cultures and two by stools cultures. All S. Typhi isolates were susceptible to the antimicrobials tested. The presence of hilA, invA and IS200 were confirmed by polymerase chain reaction in all isolates. The pulsed field gel electrophoresis method grouped 10 isolates in COINJPP.X01.0035 pattern, three in COINJPPX01.0002, one in COINJPP.X01.0012 and one in COINJPPX01.0037. Water isolates were negatives for Salmonella spp.
Conclusions. Pulsed field gel electrophoresis discriminated the isolates in two outbreaks. Initially the cases were described as only one outbreak, by epidemiological criteria and phenotypic test. Additionally two isolates with different clonal origin were discriminated, indicating that they were unrelated to the other cases. It was not possible to confirm the infection source from water samples.
Key words: Disease outbreaks, typhoid fever/epidemiology, Salmonella Typhi, Salmonella infections, bacterial typing techniques, serotyping.
Salmonella enterica es un patógeno transmitido por alimentos y animales; su diseminación se puede presentar también a partir de humanos reservorios, quienes luego de haber tenido la enfermedad pueden permanecer por más de un año excretando la bacteria por la materia fecal, pues Salmonella tiene la capacidad de resistir la acción de la bilis y permanecer en la vesícula biliar. Estos reservorios mantienen constante la circulación del microorganismo en una zona geográfica y contribuyen a la presentación de casos esporádicos y brotes (1).
Debido a estas características de transmisión, la salmonelosis se presenta como un problema de salud pública en países en desarrollo donde las condiciones de salubridad, de disposición de excretas, acueducto y alcantarillado son precarias. En Latinoamérica, Asia y África se encuentran rangos de prevalencia de 200 a 500 casos por 100.000 habitantes (1,2).
Entre las salmonelosis descritas en países en desarrollo se encuentran la fiebre tifoidea y la fiebre paratifoidea producida por S. enterica sero-variedades Typhi y Paratyphi, respectivamente; estas infecciones son graves y pueden producir complicaciones y muerte, y en forma exclusiva afectan al humano, el único reservorio y fuente de contaminación (2).
De acuerdo con el Boletín de la Organización Mundial de la Salud (OMS) de mayo de 2004 (1), se puede estimar que anualmente ocurren más de 21 millones de casos de fiebre tifoidea con más de 200.000 muertes por año y más de 5 millones de casos de fiebre paratifoidea. Latinoamérica está catalogada como una región de incidencia media de fiebre tifoidea (10-100/100.000 casos anuales) (1,3). En Colombia, de los 2.330 casos reportados al Sistema de Vigilancia en Salud Pública (SIVIGILA) entre 2002 y 2004, sólo 3,7% fueron confirmados por el laboratorio (4,5).
En Colombia, la prevalencia de fiebre tifoidea y paratifoidea no está definida; hay ausencia de datos reales debido al subregistro. El Programa de Vigilancia por el laboratorio de los serotipos y de la susceptibilidad a antibióticos de enteropatógenos y la vigilancia centinela de S. Typhi del Instituto Nacional de Salud (INS) en red con los laboratorios de salud pública departamen-tales, confirma los aislamientos clínicos enviados de las diferentes zonas. Sin embargo, estos aislamientos no corresponden al número real de casos de salmonelosis y fiebre tifoidea que ocurren en Colombia. La clasificación de Colombia como país de endemicidad media para fiebre tifoidea que hace la OMS, se basa en datos aportados por estudios realizados en otros países y que han sido extrapolados a nuestro medio (1,6).
Una de las herramientas que utiliza la vigilancia epidemiológica y el control de brotes, es la identificación de los agentes infecciosos responsables, los métodos bacteriológicos de cultivo en el caso de la salmonelosis son los utilizados para obtener el agente causal de las muestras clínicas de pacientes. Para el estudio de brotes, estos aislamientos bacteriológicos se analizan utilizando métodos de tipificación tradicionales, tales como las pruebas bioquímicas, antibiograma, serotipificación y tipificación por fagos, los cuales son útiles para describir la epidemiología de estas enfermedades. Sin embargo, estos métodos no son lo suficientemente sensibles para diferenciar los aislamientos del mismo serotipo, además, son dispendiosos y consumen mucho tiempo (7).
En respuesta a estas limitaciones, se han aplicado varias técnicas de biología molecular en estudios de infecciones por bacterias y otros microorganismos. Los métodos de tipificación más ampliamente usados son los métodos basados en el ADN, como el perfil plasmídico, la reacción en cadena de la polimerasa (PCR) y el análisis con enzimas de restricción y perfiles de ADN genómico utilizando electroforesis en gel de campo pulsado (PFGE) (7).
En Salmonella, el método de PCR se ha aplicado para la detección de genes involucrados en virulencia como invA y hilA y las secuencias de inserción IS200, específicos de este género (8,9). Dentro de los ensayos realizados por PCR para lograr una rápida identificación de los aislamientos de Salmonella spp. recuperados de muestras clínicas, de alimentos o ambientales, se ha empleado la amplificación del gen invA y del gen hilA, los cuales están involucrados en el proceso de invasión de células epiteliales y son característicos del género (9-15).
IS200 es un elemento genético móvil que se encuentra en géneros de eubacterias como Salmonella, Escherichia y Shigella, entre otras. El interés en IS200 como un marcador molecular del género Salmonella se basa en dos características: su baja tasa de transposición y su amplia distribución (8,16).
La técnica de PFGE para determinar el perfil genómico es considerada en el estudio de Salmonella como la prueba de oro para estudios epidemiológicos. Este procedimiento ha sido estandarizado por los Centers for Disease Control and Prevention (CDC) de Atlanta para los patógenos transmitidos por alimentos; es una herramienta valiosa para la subtipificación de patógenos bacterianos debido a que permite agrupar en una forma segura aislamientos epidemiológicamente no relacionados al generar patrones electroforéticos indistinguibles, así como también hace discriminación entre los aisla-mientos posiblemente relacionados. El poder discriminatorio y la reproducibilidad son atributos importantes de esta metodología (17).
En el presente trabajo, se describe la caracterización fenotípica y genotípica de dos brotes causados por Salmonella Typhi en el municipio de Apartadó, Antioquia, ambos ocurridos en un mismo período epidemiológico.
Materiales y métodos
Pacientes
En la primera y tercera semanas del mes de mayo de 2005, 44 personas habitantes de la vereda El Reposo, perteneciente al municipio de Apartadó, Antioquia, presentaron un cuadro febril acompañado de síntomas sistémicos.
Estudios clínicos y paraclínicos
Examen clínico: los pacientes consultaron al servicio de urgencias y al de consulta externa del Hospital Regional Antonio Roldán Betancur, Apartadó, Antioquia, fueron atendidos por el médico de turno, el cual les realizó un examen físico completo.
Gota gruesa: por ser una zona tropical en la cual se presentó el brote y ante la sintomatología febril que presentaron los pacientes, se realizó búsqueda de paludismo con la prueba de la gota gruesa.
Cultivos: de 36 de los 44 (81,8%) pacientes que consultaron, se tomaron muestras de sangre para tres hemocultivos seriados en caldo tripticasa soya, los cuales se incubaron a 37 °C y se subcultivaron en agar sangre y agar MacConkey (Becton Dickinson, Cockeysville, Madison, Estados Unidos). También se tomó muestra de materia fecal a 13 de los 44 (29,5%) pacientes; a estas muestras se les hizo coprológico y el coprocultivo en caldo selenito y agar xilosa, lisina, desoxicolato (XLD) (BD, Becton Dickinson, Cockeysville, Madison, Estados Unidos).
Estudios fenotípicos y moleculares de los aislamientos de Salmonella spp.
Identificación bioquímica: las colonias aisladas negativas para lactosa se identificaron bioquímicamente con el sistema API®20E (Biomerieux, Durham, USA) y se determinó el perfil numérico para cada aislamiento, el cual se confirmó con el programa correspondiente.
Serotipificación: los aislamientos identificados como S. enterica se clasificaron serológicamente con base en el antígeno somático O y los antígenos flagelares H, utilizando el esquema de Kauffmman y White, con antisueros monovalentes y polivalentes (Bio-Rad, Hercules, California, USA, Instituto Pasteur, París, Francia y Difco) (18).
Antibiotipo: la determinación del antibiotipo se realizó según el método de difusión Kirby-Bauer en agar Mueller Hinton (BD), de acuerdo con el protocolo del Instituto de Estándares Clínicos y de Laboratorio (CLSI) (19). Los 10 antibióticos se seleccionaron teniendo en cuenta el uso frecuente en el tratamiento de los diferentes cuadros clínicos producidos por Salmonella Enteritidis, Typhimurium y Typhi: enteritis, infección sistémica y fiebre tifoidea. Los antibióticos empleados y sus concentraciones fueron: ácido nalidíxico, 30 µg; ampicilina, 10 µg; cefotaxima, 30 µg; ciprofloxacina, 5 µg; cloranfenicol, 30 µg; estreptomicina, 10 µg; gentamicina, 10 µg; kanamicina, 30 µg; trimetoprim-sulfametoxazol, 25 µg, y tetraciclina, 30 µg (Oxoid Limited, Basingstoke, Hampshire, England). La interpretación se realizó según los criterios del CLSI (19).
Identificación molecular: para confirmar los aislamientos obtenidos por cultivo como pertenecientes al género Salmonella, se realizó por PCR la búsqueda de los genes invA y hilA, específicos de género (15,20).
Tipificación genotípica: los aislamientos fueron evaluados para detectar la presencia de la secuencia de inserción IS-200 (PCR) (8) y se realizó la PFGE con XbaI, utilizando la metodología descrita (17).
Extracción de ADN: a partir de un cultivo puro de S. Typhi se tomaron dos colonias y se inocularon en 200 µl de agua destilada estéril, se agitó y se realizó la extracción por el método de ebullición (21). Este proceso se realizó por duplicado.
Amplificación de ADN: para la realización de las pruebas de PCR se utilizaron los siguientes reactivos y cantidades: 1,25 µl de los iniciadores 5-3 en una concentración de 10 µM, 1,25 µl del iniciador 3-5 en una concentración 10 µM, 0,5 ml de la mezcla de los desoxinucleótidos 10 mM, 2,5 µl de tampón 10X, 0,5 µl de Taq polimerasa (Invitrogen) en una concentración de 5 U/µl, 18 µl de agua destilada estéril y 1µl de ADN, para un volumen final de reacción de 25 µl. El procedimiento se realizó siguiendo las recomenda-ciones previamente descritas en el protocolo (15).
Las secuencias de los iniciadores empleados en este estudio fueron reportadas previamente (8,15,20). Para todas las PCR realizadas se utilizó como control positivo la cepa de Salmonella Typhimurium ATCC 14028; como control negativo se utilizó agua destilada estéril. No se utilizó control de amplificación interno.
PFGE: el perfil genómico se estableció mediante la técnica de PFGE con la enzima XbaI, aplicando el protocolo estandarizado por los CDC de Atlanta, para los laboratorios que realizan la vigilancia de los patógenos transmitidos por alimentos (17). Los patrones electroforéticos generados por la PFGE se analizaron con el programa Fingerprinting II version 3.0 (Bio-Rad) utilizando el coeficiente de Dice y el árbol filogenético fue obtenido con la matriz de agrupamiento UPGMA (unweighted pair group method). En el dendrograma los aisla-mientos que presentaron una similitud de 100% se consideraron genéticamente iguales y se compararon con la base de datos de los patrones de PFGE que se encuentran en el Grupo de Microbiología del INS.
Análisis de aguas
Se estudiaron ocho muestras de agua; se recolectaron una muestra superficial y otra profunda de cada una de las siguientes fuentes: agua del canal de aguas negras, de aguas servidas provenientes de lavaderos de la zona, de aguas del tubo de distribución y de aguas del pozo en tierra. Todas se cultivaron en el medio Readycult® Coliforms 100 (Merck Darmstadt, Germany) para determinación de coliformes totales y fecales; se les realizó también la prueba de PCR para la detección del gen hilA (15).
Resultados
Descripción del brote
Después del desbordamiento de un canal de distribución de aguas negras que contaminó un pozo del cual tomaban el agua para consumo diario, 44 pacientes consultaron por un cuadro febril acompañado de síntomas sistémicos.
Datos demográficos de los pacientes
El rango de edad de los pacientes osciló entre 0 y 58 años, con un promedio de 17,8 años. Por género, 27 (61%) pertenecían al sexo masculino y 17 (39%) al sexo femenino.
Diagnóstico clínico
El tiempo de evolución varió entre 1 y 20 días, con una media de 12,8 días. Diez y siete (38,6%) de los 44 pacientes estuvieron hospitalizados, fueron dados de alta después de un promedio de siete días de hospitalización y sólo uno presentó una complicación por hemorragia gastrointestinal franca. Los pacientes hospitalizados fueron tratados con ciprofloxacina intravenosa y los restantes recibieron tratamiento ambulatorio con ciprofloxacina oral. En los 44 pacientes el diagnóstico inicial fue clínico, 15 fueron confirmados por laboratorio y los otros 29 por asociación epidemiológica. Los signos y síntomas de los pacientes se encuentran descritos en el cuadro 1.
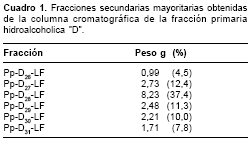
Diagnóstico por laboratorio
Gota gruesa: dos pacientes presentaron infección con Plasmodium vivax. El resto de pacientes fueron negativos en la gota gruesa.
Cultivos: por hemocultivo se obtuvo crecimiento bacteriano en 13/36 (36%) muestras de pacientes y el coprocultivo fue positivo en 2/13 (15%) muestras.
Estudios fenotípicos y moleculares de los aislamientos de Salmonella spp.
Identificación fenotípica: se obtuvieron 15 aislamientos de Salmonella Typhi, los cuales se confirmaron por pruebas bioquímicas y serotipificación.
Antibiotipo: según el antibiograma los 15 aislamientos fueron sensibles a los 10 antibióticos probados.
Identificación genotípica: todos los aislamientos de S. Typhi estudiados por PCR amplificaron un fragmento de 854 pb y de 450 pb correspondientes a los genes hilA e invA de la isla de patogenicidad 1 de Salmonella.
IS-200: en todos los aislamientos estudiados se detectó una secuencia de inserción de 700 pb.
PFGE: la subtipificación molecular con XbaI mostró que, de los 15 aislamientos, 10 presentaron el patrón electroforético COINJPPX01.0035, tres aislamientos, el patrón COINJPPX01.002, un aislamiento, el patrón COINJPPX01.0012 y uno, el patrón COINJPPX01.0037. El dendrograma del total de aislamientos de S. Typhi determinó una similitud genética de 83% entre ellos (figura 1).

Análisis de aguas
En el análisis de aguas se detectó por Readycult la presencia de coliformes totales y fecales en el agua del canal y de coliformes totales pero no fecales en el agua de lavaderos; no se obtuvo crecimiento de S. enterica. La prueba de PCR para detectar la presencia de S. enterica en aguas fue negativa.
Discusión
El reconocimiento de las propiedades fenotípicas a través de la serotipificación, las pruebas bioquímicas y las pruebas de susceptibilidad a antibióticos son la base para la identificación y el rastreo de una determinada bacteria en investigaciones epidemiológicas. Estos métodos permiten un acercamiento inicial a la relación entre los aislamientos, pero carecen de discriminación, pues no permiten la diferenciación clonal entre ellos (22-24).
Los 15 aislamientos de Salmonella Typhi caracterizados en este trabajo, fueron sensibles a los 10 antibióticos probados, lo cual coincide con lo reportado por el INS (4) y confirma que los aislamientos colombianos de S. Typhi son sensibles a los antibióticos de uso clínico, en contraste con los reportes hechos en Asia, África y Estados Unidos (25-27).
En todos los aislamientos estudiados se amplificaron por PCR los genes hilA e invA de la isla de patogenicidad 1 de Salmonella, los cuales están involucrados en el proceso de invasión a la mucosa intestinal (20,22). Estos resultados confirman la alta sensibilidad de esta técnica con estos genes para la detección rápida y el diagnóstico de Salmonella, como lo han reportado diversos autores (10-15,28). La utilización de esta técnica sería un apoyo a los laboratorios de salud pública, para la detección del agente etiológico. En cuanto a la detección de la presencia de la secuencia de inserción IS200 en los 15 aislamientos clínicos, se encontró una banda de 700 pb, similar a lo reportado por Beuzón y colaboradores (16). Otros estudios han demostrado ausencia de esta banda de 700 pb o presencia de una banda de 1.000 pb (8,16). La subtipificación molecular por PFGE discriminó los aislamientos y demostró la presencia de dos brotes simultáneos de fiebre tifoidea y no de uno solo, como aparentemente lo mostraban los hallazgos epidemiológicos, el serotipo y el antibiograma; además, identificó dos casos aislados. Este hallazgo confirma la importancia de la subtipificación molecular como PFGE, lo cual también se ha demostrado en estudios previos (29,30).
La PFGE mostró gran sensibilidad al diferenciar dos aislamientos provenientes de casos que no estaban relacionados con los brotes, pues no provenían del mismo sitio donde se presentaron los primeros casos clínicos, e indicó que existen varias cepas de S. Typhi y se encuentran circulando en el municipio de Apartadó, lo cual evidencia diferentes fuentes de infección.
La determinación de los clones de las bacterias involucradas en un brote es importante desde el punto de vista epidemiológico, pues permite la detección de la fuente de infección, establecer la relación entre casos clínicos y con estos resultados tomar medidas que eviten la dispersión de los patógenos y, de esta manera, controlar nuevos brotes (30).
En este estudio no fue posible confirmar la fuente de infección, ya que no se logró detectar S. enterica en las muestras de aguas analizadas por cultivo y por PCR; además, no se incluyó la búsqueda de los contactos de los casos índices.
El estudio de características moleculares de aislamientos de Salmonella spp. obtenidos a partir de brotes, es reciente en nuestro país (29,31), lo cual demuestra la importancia de las pruebas moleculares para determinar la relación clonal entre aislamientos involucrados en un brote, ya que brindan información más detallada sobre las características de la bacteria.
La detección de un brote epidémico en una región requiere de infraestructura y recurso humano capacitado para detectar la presencia de casos índice y la colaboración de laboratorios y entidades de salud en red, que permitan identificar el agente causal del brote. El fortalecimiento del nivel local del sistema de salud es necesario para garantizar dicha detección y controlar la aparición y diseminación de brotes como el descrito. Los brotes del presente estudio fueron detectados gracias a que esta zona cuenta con apoyo diagnóstico clínico y de laboratorio y al uso adecuado del sistema de vigilancia en red.
Agradecimientos
Al personal del Laboratorio Departamental de Salud Pública de Antioquia por su valiosa colaboración en el estudio de estos brotes epidémicos.
Conflictos de intereses
Los autores declaran que no tienen ningún conflicto de intereses con la publicación de estos datos.
Financiación
Instituto Colombiano de Medicina Tropical-Instituto de Ciencias de la Salud CES e Instituto Nacional de Salud.
Correspondencia:
Nora María Cardona Castro, Instituto Colombiano de Medicina Tropical, Cra 43ª # 52 sur-99, Sabaneta, Antioquia, Colombia.
Teléfono:(4) 301 4300; fax: (4) 301 4258
Referencias
1. Crump JA, Luby SP, Mintz ED. The global burden of typhoid fever. Bull World Health Organ. 2004;82: 346-53. [ Links ]
2. Lesser CF, Miller SI. Salmonellosis. En: Braunwald E, Fauci AS, Kasper DL, Hauser SL, Longo DL, Jamenson JL, editors. Harrisons Principles of Internal Medicine. 15th ed. New York: McGraw-Hill; 2001. p.970-3. [ Links ]
3. Andrews WH, Hammack TS, Amaguana RM. Salmonella. In: Merker RL, editor. Food and Drug Administration. Bacteriological Analytical Manual. 8th ed. Gaithersburg: AOAC International; 1998. [ Links ]
4. Grupo de Microbiología, Instituto Nacional de Salud. Proyecto vigilancia por el laboratorio: molecular y fenotípica de Salmonella spp., uno de los principales agentes implicados en la enfermedad diarreica aguda. Consultado: agosto de 2006. Disponible en: http://www.ins.gov.co/pdf_investiga/Microbiologia_salm_05.pdf [ Links ]
5. Boletín Epidemiológico Semanal. Situación de las enfermedades transmisibles objeto de vigilancia intensificada en salud Pública Colombia 2002. Consultado: agosto de 2006. http://www.col.ops-Oms.org/sivigila/2002/BOLE52_02.htm [ Links ]
6. Muñoz N, Agudelo CI, Realpe ME, Ovalle M, Laboratorios de Salud Pública. Vigilancia en red de la susceptibilidad antimicrobiana y de los serotipos de Salmonella spp, Shigella sp y Vibrio cholerae: informe de 2000-2001. Inf Quinc Epidemiol Nac. 2002;7:177-92. [ Links ]
7. Olive DM, Bean P. Principles and applications of methods for ADN-based typing of microbial organisms. J Clin Microbiol. 1999;37:1661-9. [ Links ]
8. Threlfall EJ, Torre W, Ward LR, Dávalos-Pérez A, Rowe B, Gilbert I. Insertion sequence IS200 fingerprinting of Salmonella typhi: an assessment of epidemiological applicability. Epidemiol Infect 1994; 112:253-61. [ Links ]
9. Marcus SI, Brumell JH, Pfeifer CG, Finlay BB. Salmonella pathogenicity islands: big virulence in small packages. Microbes Infect. 2000;2:145-56. [ Links ]
10. Wolffs P, Glencross K, Thibaudeau R, Griffiths M. Direct quantitation and detection of Salmonellae in biological samples without enrichment, using two-step filtration and real-time PCR. Appl Environ Microbiol. 2006;72:3896-900. [ Links ]
11. Chiu CH, Ou JT. Rapid identification of Salmonella serovars in feces by specific detection of virulence genes, invA and spvC, by an enrichment broth culture-multiplex PCR combination assay. J Clin Microbiol. 1996;34:2619-22. [ Links ]
12. Cortez AL, Carvalho AC, Ikuno AA, Bürger KP, Vidal-Martins AM. Identification of Salmonella spp. isolates from chicken abattoirs by multiplex-PCR. Res Vet Sci. 2006;81:340-4. [ Links ]
13. Kumar S, Balakrishna K, Batra H. Detection of Salmonella enterica serovar Typhi (S. Typhi) by selective amplification of invA, viaB, fliC-d and prt genes by polymerase chain reaction in mutiplex format. Lett Appl Microbiol. 2006;42:149-54. [ Links ]
14. Malorny B, Hoorfar J, Bunge C, Helmuth R. Multicenter validation of the analytical accuracy of Salmonella PCR: towards an International standard. Appl Environ Microbiol. 2003;69:290-6. [ Links ]
15. Sánchez-Jiménez MM, Cardona-Castro N. Validation of a PCR for diagnosis of typhoid fever and salmonellosis by amplification of the hilA gene in clinical samples from Colombian patients. J Med Microbiol. 2004;53:875-8. [ Links ]
16. Beuzon CR, Chessa D, Casadesus J. IS200: an old and still bacterial transposon. Int Microbiol. 2004;7:3-12. [ Links ]
17. Ribot EM, Fair MA, Gautom R, Cameron DN, Hunter SB, Swaminathan B, et al. Standardization of pulse-field gel electrophoresis protocols for the subtyping of Escherichia coli O157:H7, Salmonella, and Shigella for PulseNet. Foodborne Pathog Dis. 2006;3:59-67. [ Links ]
18. Popoff MY, Le Minor L. Antigenic formulas of the Salmonella serovars. 8th Ed. Paris: WHO Collaborating Center for Reference and Research on Salmonella, Institut Pasteur; 2001. [ Links ]
19. Clinical and Laboratory Standards Institute/NCCLS. Performance standards for antimicrobial susceptibility testing fifteenth informational supplement, M100-S15. Wayne, PA: Clinical and Laboratory Standards Institute; 2005. [ Links ]
20. Galan J, Curtiss R. Distribution of the invA, -B, -C, and -D genes of Salmonella typhimurium among other Salmonella serovars: invA mutants of Salmonella typhi are deficient for entry into mammalian cells. Infect Immun. 1991;59:2901-8. [ Links ]
21. McClelland M, Sanderson KE, Spieth J, Clifton SW, Latreille P, Courtney L et al. Complete genome sequence of Salmonella enterica serovar Typhimurium LT2. Nature. 2001;413:852-6. [ Links ]
22. Fantasia M, Paglietti B, Filetici E, Anastasio MP, Rubino S. Conventional and molecular approaches to isolates of Salmonella hadar from sporadic and epidemic cases. J Appl Microbiol. 1997;82:494-8. [ Links ]
23. Labarca J. Utilización del antibiotipo como marcador epidemiológico en infecciones intrahospitalarias: comparación con la epidemiología molecular. Rev Chilen Infect. 2002;19(Suppl.2):S157-60. [ Links ]
24. Salve A, Pichel M, Wiesner M, Hidalgo M, Terragano R, Alvarez A, et al. Molecular subtyping of Salmonella enterica serovar Typhi isolates from Colombia and Argentina. Foodborne Pathog Dis. 2006;3:142-52. [ Links ]
25. Chu YW, Cheung TK, Ng TK, Tsang D, To WK, Kam KM, et al. Quinolone resistance determinant qnrA3 in clinical isolates of Salmonella in 2000-2005 in Hong Kong. J Antimicrob Chemother. 2006;58:904-5. [ Links ]
26. Kariuki S, Gilks C, Revathi G, Hart CA. Genotypic analysis of multidrug-resistant Salmonella enterica serovar Typhi, Kenya. Emerg Infect Dis. 2000; 6:649-51. [ Links ]
27. Shakespeare WA, Davie D, Tonnerre C, Rubin MA, Strong M, Petti CA. Nalidixic acid-resistant Salmonella enterica serotype Typhi presenting as a primary psoas abscess: case report and review of the literature. J Clin Microbiol. 2005;43:996-8. [ Links ]
28. Cardona-Castro N, Sánchez-Jiménez M. Desarrollo y evaluación de una prueba de reacción en cadena de la polimerasa (PCR), utilizando la secuencia del gen hilA para diagnóstico de fiebre entérica por Salmonella spp. Biomédica. 2004;24:194-9. [ Links ]
29. Hidalgo M, Gracia M, Ovalle MV, Wiesner M, Chávez J, Realpe ME, et al. Caracterización de los aislamientos de Salmonella typhimurium, asociado con un brote de intoxicación alimentaria en una localidad de Pasto, Nariño. Inf Quinc Epidemiol Nac. 2004;9:81-96. [ Links ]
30. Ridley AM, Threlfall EJ, Rowe B. Genotypic characterization of Salmonella enteritidis phage types by plasmid analysis, ribotyping, and pulsed-field gel electrophoresis. J Clin Microbiol. 1998;36:2314-21. [ Links ]
31. Realpe ME, Gracia M, Ovalle MV, Wiesner M, Hidalgo M, Agudelo CI, et al. Brote de enfermedad transmitido por alimento causada por Salmonella Enteritidis, en Riosucio, Caldas. Caracterización fenotípica y molecular. Inf Quinc Epidemiol Nac. 2005;10:321-6. [ Links ]














