Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Biomédica
versão impressa ISSN 0120-4157versão On-line ISSN 2590-7379
Biomédica v.32 supl.1 Bogotá mar. 2012
ARTÍCULO ORIGINAL
1Instituto Colombiano de Medicinal Tropical, Universidad CES, Apartadó, Colombia
2Colegio Mayor de Antioquia, Medellín, Colombia
3Grupo Malaria, Universidad de Antioquia, Medellín, Colombia
Institución donde se realizó el trabajo:
Instituto Colombiano de Medicina Tropical, Universidad CES, sede Apartadó, Antioquia
Contribución de los autores:
Margarita Arboleda: diseño del estudio, análisis, edición y revisión del manuscrito.
María Fernanda Pérez y Luz Yaned Usuga: búsqueda y revisión de historias clínicas.
Diana Fernández: análisis de información, revisión bibliográfica y edición.
Miler Meza: procesamiento de información, análisis, gráfico y tablas.
Recibido: 08/06/11; aceptado:10/11/11
Introducción. La malaria representa un problema de salud pública en la región de Urabá, donde se registran tasas superiores a las del departamento de Antioquia; la carga de malaria por Plasmodium vivax es de 78,7 % y poco se ha explorado su perfil en la región.
Objetivos. Con el presente estudio se pretende conocer las características clínicas y de laboratorio de los pacientes hospitalizados por malaria por P. vivax en Apartadó.
Materiales y métodos. Se revisaron las historias clínicas de pacientes con malaria por P. vivax que requirieron manejo hospitalario en el Hospital “Antonio Roldán Betancur”, Empresa Social del Estado, durante los años 2004-2007.
Resultados. Se hospitalizaron 359 pacientes con malaria por P. vivax, de los cuales, el 23,1 % (83/359 casos) se complicó por anemia grave (51,8 %, 43/83), por trombocitopenia grave (15,6 %, 13/83) y por hiperbilirrubinemia (7,2 %, 6/83); algunos pacientes satisfacían varios criterios simultáneamente, incluyendo un caso de síndrome de dificultad respiratoria aguda. Los datos de laboratorio más significativos mostraron disminución de los niveles de hemoglobina, hematocrito y plaquetas, con aumento en los niveles de transaminasas y bilirrubinas. Sólo el 4,82 % (4/83) de los pacientes con malaria complicada, recibió tratamiento con quinina intravenosa, ninguno falleció.
Conclusiones. Se destaca en este trabajo la frecuencia importante de malaria complicada por P. vivax, particularmente en los menores de cinco años, en la región de Urabá, y la necesidad de fortalecer el conocimiento de la guía para la atención clínica integral del paciente con malaria, entre el personal de salud, para hacer un diagnóstico clínico correcto y ofrecer el tratamiento apropiado.
Palabras clave: malaria, Plasmodium vivax, anemia, trombocitopenia, Colombia
Clinical and laboratory profile of Plasmodium vivax malaria patients hospitalized in Apartadó, Colombia
Introduction. Malaria is a public health problem in the Urabá region recording rates of infection above those of the Antioquia department. The burden of vivax malaria is 78.7% and the profile of vivax malaria in this region has scarcely been studied.
Objectives. To analyze the clinical and laboratory characteristics of patients hospitalized for vivax malaria in Apartadó.
Materials and methods. We reviewed the medical records of patients with vivax malaria hospitalized in the Antonio Roldán Betancur hospital from 2004-2007.
Results. Of 359 patients with vivax malaria who requiried hospitalization, 23.1% (83/359 patients) had the following complications: severe anemia, 51.8% (43/83); severe thrombocytopenia, 15.6% (13/83); hyperbilirubinemia, 7.2 % (6/83). Some patients met several criteria for complicated malaria simultaneously, including one case of acute respiratory distress syndrome. The most significant laboratory changes were decreases in the hemoglobin, hematocrit and platelet levels, with increased levels of transaminases and bilirubin. Only 4.82% (4/83) of patients with complicated malaria were treated with intravenous quinine, no one died.
Conclusions. The elevated frequency of complicated vivax malaria found in the Uraba region in this study is noteworthy, particularly in children under 5 years. The results highlight the need to strengthen, amongst the health staff, the knowledge of the guidelines for the clinical care of malaria patients, in order to make a correct clinical diagnosis and provide appropriate treatment.
Key words: malaria, Plasmodium vivax, anemia, thrombocytopenia, Colombia.
El paludismo, o malaria, es una enfermedad infecciosa, producida por un parásito del género Plasmodium, del cual cinco especies infectan naturalmente al hombre: P. falciparum, P. vivax, P. malariae, P. ovale y P. knowlesi. Esta enfermedad constituye uno de los principales problemas de salud pública a nivel mundial. Aproximadamente, 1,2 billones de personas viven en áreas de alto riesgo y 2,1 billones en áreas de bajo riesgo, y al año, se producen cerca de 247 millones de casos y 1 millón de muertes (1).
La malaria por P. vivax está ampliamente distribuida alrededor del mundo; en las regiones del sur y sureste de Asia, representa 50 % de los casos de paludismo que se presentan (2, 3, Tjitra E, Warikar N, Ebsworth EP, Kenangalem E, Sugiarto P, Okoseray MJ, et al. Major burden of P.vivax infection in Papua, Indonesia; A region with high levels of chloroquine resistance; 16th IFTM Medicine in the Tropics; Marseille, France. 2005). No obstante, la carga de este tipo de malaria es mayor en Centroamérica y Suramérica, donde produce hasta 71 a 81 % de los casos (4).
En América Latina, el 7,3 % de la población está en riesgo de contraer la enfermedad y, para el año 2008, se reportaron 877.335 casos de malaria en esta región (5). En Colombia, el 85 % del territorio es apto para la transmisión de Plasmodium sp. y, para el año 2010, se reportaron 116.914 casos de paludismo, de los cuales, 82.193 (70,3 %) fueron por P. vivax. En el departamento de Antioquia, en este mismo año se registraron 47.021 casos con una distribución similar por especie (6); esta relación de malaria por P. vivax y por P. falciparum se ha mantenido en el departamento de Antioquia desde años precedentes (6).
Esta enfermedad representa un problema de salud pública en la región de Urabá (Antioquia), donde se registró un índice parasitario anual (IPA) de 8,96 casos por 1.000 habitantes en el año 2009, superior al del departamento, que fue de 5,34 por 1.000 habitantes; en Urabá se concentró el 15,8 % de los casos registrados en el departamento (5.068/32.029), convirtiéndose en la tercera región de mayor endemia para paludismo, después del Bajo Cauca y el nordeste antioqueño. El 90,3 % de los casos de malaria en Urabá fueron por P. vivax, el 9,5 %, por P. falciparum, y el 0,2 % restante, fue malaria mixta (7). En el año 2008 se registraron 25 casos de malaria complicada en el departamento de Antioquia, 44% (11/25) de los cuales procedían de la región de Urabá; infortunadamente no fue posible determinar el número de casos complicados por especie (Sivigila, 2010).
La malaria grave o complicada se ha definido según uno o más de los criterios clínicos o de laboratorio establecidos por la Organización Mundial de la Salud (OMS) (8), teniendo en cuenta que inicialmente fueron elaborados para los casos complicados por P. falciparum. Actualmente, dichos criterios se utilizan para los casos complicados con formas asexuadas de cualquier especie de Plasmodium en sangre y sin otra causa etiológica para sus síntomas (9)y son los siguientes:
• Malaria cerebral
• Anemia grave: hematocrito menor de 15 % o hemoglobina menor de 5 g/dl; los niveles adaptados para Colombia son menos de 20 % y menos de 7 g/dl, respectivamente (9).
• Insuficiencia renal con creatinina mayor de 3 mg/dl; en Colombia, mayor de 1,5 mg/dl (9).
• Hipoglucemia: glucemia menor de 40 mg/dl; en Colombia, menor de 60 mg/dl (9).
• Trastornos hidroelectrolíticos y del equilibrio ácido-base.
• Edema pulmonar y síndrome de dificultad respiratoria del adulto.
• Colapso circulatorio y estado de choque
• Hemorragias espontáneas o coagulación intravascular diseminada.
• Hiperpirexia: temperatura por encima de 40,5 °C, siempre y cuando persista a pesar del tratamiento.
• Hiperparasitemia mayor de 100.000 parásitos/mm3; en Colombia, mayor de 50.000 parásitos/mm3; es posible ver esquizontes (9), aclarando que este criterio es exclusivo para malaria por P. falciparum, dada la afinidad de P. vivax por los reticulocitos.
• Hemoglobinuria palúdica
• Complicaciones hepáticas e ictericia: bilirrubina total mayor de 3,0 mg/dl, si se evidencia compromiso de otro órgano; transaminasas ALT por encima de 120 UI/L; en Colombia, por encima de 60 UI/L (9).
• Insuficiencia respiratoria
• Trombocitopenia grave: plaquetas por debajo de 20.000/mm3*
* No es criterio de la OMS, pero sí fue utilizado por Tobón, et al. (10), según el criterio de Horstmann, et al. (1981), mencionado en la guía de la OMS.
Con el presente estudio se pretende establecer el perfil clínico y de laboratorio de los casos de malaria por P. vivax, hospitalizados en el municipio de Apartadó durante los años 2004 a 2007, para contribuir al conocimiento del comportamiento o de la expresión clínica de esta enfermedad en la región, y orientar mejor el tratamiento y la atención médica de los mismos.
Materiales y métodos
Se llevó a cabo un estudio descriptivo y retrospectivo, sobre los casos hospitalarios de paludismo por P. vivax en el Hospital “Antonio Roldán Betancur”, Empresa Social del Estado (E.S.E.), durante los años 2004-2007. Este hospital es de segundo nivel de atención y de referencia para los pacientes remitidos de los municipios de la región de Urabá.
Se consideraron “casos hospitalizados” aquellos que según criterio médico superaron 24 horas de observación hospitalaria. Se revisaron las historias clínicas y se extrajo la información, teniendo en cuenta variables de identificación personal, antecedentes, enfermedad actual, características clínicas, resultados parasitológicos y de laboratorio, y evolución del paciente.
Se tuvieron en cuenta para el presente trabajo los criterios de malaria grave establecidos por la OMS (8) y sólo algunos de los adaptados para Colombia de acuerdo con experiencias en investigación, descritos en la guía del Ministerio de la Protección Social (9): hemoglobina menor de 7,0 g/dl, creatinina mayor de 1,5 mg/dl y glucemia menor de 60 mg/dl, lo que garantiza que los resultados pueden compararse con los de otros trabajos con los mismos criterios.
Una de las limitaciones de este estudio es que el diagnóstico parasitológico por la gota gruesa, no se confirmó mediante métodos moleculares, ni se pudo hacer una segunda lectura del mismo, dado el carácter retrospectivo del estudio. Asimismo, vale mencionar que durante el período de estudio no se había estandarizado para Colombia el recuento parasitario de P. vivax, tal como se hace actualmente.
La información recolectada se sistematizó en Excel® y se analizó mediante Epi-Info 6.0, utilizando las medidas generales estandarizadas para los estudios descriptivos.
Desde el punto de vista ético, este trabajo se consideró de riesgo mínimo y como tal fue avalado por el Comité de Ética de la Universidad CES.
Resultados
Se identificaron 359 casos hospitalizados de paludismo por P. vivax, 53,2 % (191/359) de sexo femenino, con edad promedio de 23 años, con un rango entre un mes y 77 años (DE=17 años). Se registraron 42 episodios de malaria en 37 mujeres gestantes (42/359; 11,7 %), una con tres episodios durante el embarazo y tres con dos episodios.
En la figura 1 se presenta la distribución de malaria por grupos etarios, destacándose que el grupo de edad de 15 a 49 años fue el más afectado (56,8 %), seguido por el de 5 a 14 años (18,4 %).
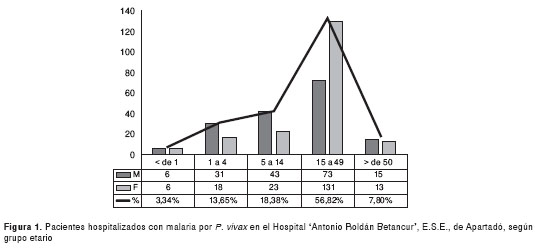
El promedio de días de evolución de los síntomas fue de 5,6 (1 y 60 días; DE=5,8). Los síntomas más frecuentes fueron fiebre, cefalea y escalofrío, y los hallazgos clínicos más frecuentes, dolor a la palpación abdominal, ictericia, hepatomegalia y esplenomegalia.
En el cuadro 1 se presentan los casos de paludismo según el tiempo de evolución de la enfermedad, y los signos y síntomas asociados en los pacientes con malaria complicada en comparación con la no complicada.
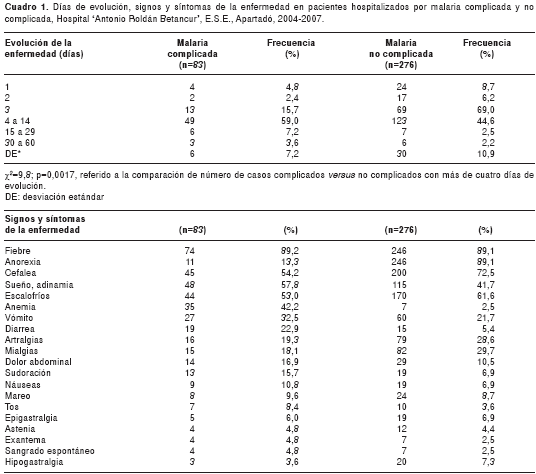
En el presente trabajo, hubo una mayor frecuencia de complicaciones en los pacientes que tenían más de cuatro días de evolución de la enfermedad, en comparación con los que tenían menos días (77,1 % versus 55,3%, respectivamente), siendo esta diferencia estadísticamente significativa (c2=9,8; p=0,0017). En el cuadro 1 se presentan los signos y síntomas más frecuentes, entre los cuales se destacan la fiebre, la anorexia y la cefalea, con frecuencias superiores a 50 % en los pacientes con malaria complicada y no complicada. Por su parte, síntomas como la infección pulmonar y la rinorrea se presentaron con una frecuencia muy baja, cada uno entre 3 y 4 %, tanto en los pacientes con malaria complicada como no complicada; sólo dos (0,7 %) pacientes con malaria no complicada presentaron odinofagia o dolor faríngeo. Estos datos no se consignaron en el cuadro.
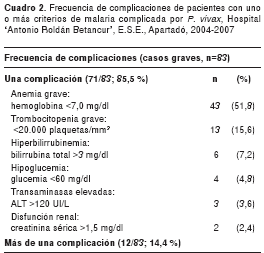
Se encontraron 83 casos de malaria complicada, lo que corresponde a 23,1 % de los casos hospitali-zados. En el cuadro 2 se presenta la frecuencia de los diferentes criterios de complicación, destacándose que algunos pacientes (12/83, 14,4 %) reunieron más de un criterio; los más importantes fueron la anemia grave asociada a hiperbilirrubinemia (4/12, 33,3 %), la trombocitopenia asociada a diversas complicaciones como síndrome de dificultad respiratoria del adulto, hiperbilirrubinemia, hipo-glucemia, anemia grave, disfunción renal y aumento de transaminasas (7/12, 58,3 %). Sólo en cuatro de los 83 pacientes que presentaron paludismo grave se instauró tratamiento intravenoso con quinina, lo mismo que en dos con malaria no complicada.
Según los grupos de edad, los 83 casos de malaria complicada se distribuyeron así: 8 (9,6 %), menores de 1 año; 24 (28,9 %), niños entre 1 y 4 años; 15 (18,1 %), grupo de 5 y 14 años; 33 (39,8 %), de 15 a 49 años, y 3 (3,6 %), mayores de 50 años. La frecuencia de malaria complicada fue mayor en los menores de cinco años (52,5 %: 32/61); al compararla con la frecuencia en los demás grupos etarios (17,1%: 51/298), la diferencia fue estadísticamente significativa (c2=35,5; p<0,00000; IC95% 2,8-10,0).
De los 83 casos de malaria complicada, 13 (15,7 %) correspondieron a mujeres gestantes y, uno (1,2 %), a mayores de 60 años. No hubo diferencia estadísticamente significativa entre la frecuencia de malaria complicada entre mujeres gestantes y no gestantes en edad fértil.
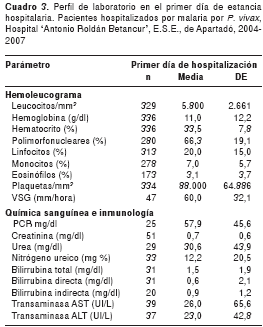
En el cuadro 3 se presentan los principales hallazgos de laboratorio; se encontró que la hemoglobina, el hematocrito y el recuento de plaquetas fueron los exámenes más alterados, con tendencia a la disminución al segundo día de hospitalización. Por otra parte, el examen citoquímico de orina evidenció que, a pesar de las alteraciones encontradas el primer día de hospitalización, tales como hematuria y proteinuria, no se hizo seguimiento de la evolución de los pacientes al segundo día de hospitalización, por lo cual no se pueden comparar los resultados de ambos días.
Finalmente, se encontró que 28 (7,8 %) de los 359 pacientes hospitalizados presentaban enfermedades concomitantes: 12 (3,3 %), dengue diagnosticado por las pruebas estandarizadas a través de la red de laboratorios de salud pública; 7 (1,9 %), infecciones urinarias comprobadas por urocultivo; 4 (1,1%), leptospirosis demostrada por pruebas estandarizadas a través de la red de laboratorios de salud pública; 2 (0,6%), otitis; 2 (0,6%), infecciones de las vías respiratorias superiores, y 1 (0,3 %), bronconeumonía.
Discusión
En este trabajo se reporta una serie de 359 casos de malaria por P. vivax hospitalizados en el Hospital “Antonio Roldán Betancur”, E.S.E., de Apartadó, durante el cuatrienio 2004-2007. Estos casos corresponden en su mayoría a adultos del sexo femenino, con un porcentaje importante de participación de los menores de 15 años (35,4 %), lo cual difiere con los hallazgos de Echeverri, et al., en su estudio sobre malaria por P. vivax en el municipio de Turbo, donde encontraron una mayor frecuencia de hombres adultos con paludismo (11). Esta diferencia podría explicarse porque en el estudio de Turbo se incluyeron pacientes ambulatorios, razón por la cual los niños con paludismo podían remitirse más fácilmente al servicio de urgencias.
El 11,7 % de los episodios de malaria se presentó en 37 mujeres gestantes, una de ellas registró tres episodios durante el embarazo y, tres mujeres gestantes, dos episodios. Piñeros encontró que, de las 173 mujeres gestantes infectadas por P. vivax, 46 (26,6 %) tuvieron recurrencia de la parasitemia durante el seguimiento, 40 presentaron una sola recurrencia, 4 presentaron dos recurrencias y 2 gestantes presentaron tres recurrencias durante el seguimiento (12). Todas las recurrencias ocurrieron después del día 28 de haber iniciado el tratamiento y, en promedio, se presentaron a las 12,4 semanas. Estas recurrencias por P. vivax podrían explicarse, en parte, por la falta de primaquina, que está contraindicada durante la gestación.
Tal como se describe en la literatura científica, el mayor tiempo de evolución de los síntomas se asocia con mayor riesgo de complicaciones (13). En el presente trabajo la frecuencia de complicaciones en pacientes que presentaron más de cuatro días de evolución de los síntomas, fue mayor que en los que consultaron con menos de cuatro días (77,1 % versus 55,3 %, respectivamente); esta diferencia fue estadísticamente significativa. Está demostrado que cuando el inicio del tratamiento es tardío, la carga de parásitos continúa aumentando y puede desencadenarse un paludismo complicado (14).
Un aporte importante de este estudio lo representa el hallazgo de 83 pacientes (23,1 %) con malaria complicada por P. vivax. Generalmente, se ha asumido que P. falciparum es el responsable de los casos de malaria grave o complicada; sin embargo, recientemente se ha informado un mayor número de casos de malaria complicada producida por P. vivax (15-23).
Es importante tener en cuenta que este diagnóstico de monoinfección por P. vivax no fue confirmado por métodos moleculares, debido a que éstos no se utilizan en la práctica médica, y el presente estudio se limita a describir retrospectivamente las características clínicas y de laboratorio de los pacientes hospitalizados con diagnóstico de malaria por P. vivax. Por lo tanto, se podría pensar que en algunos casos complicados pudo haberse dejado de diagnosticar P. falciparum, teniendo en cuenta que la gota gruesa, método utilizado comúnmente en la práctica clínica y considerado como prueba de referencia para el diagnóstico de la malaria, en algunos casos puede presentar dificultades relacionadas con bajas parasitemias (recuentos menores de 100 parásitos/µl), secuestro de parásitos o muestras mal coloreadas o insuficientes, lo cual podría ser el reflejo de un sesgo diagnóstico.
Asimismo, en la práctica médica, no se dispone de otros métodos diagnósticos que tengan la capacidad de complementar la gota gruesa, como las pruebas de diagnóstico rápido o métodos moleculares como la reacción en cadena de la polimerasa, que detecta el ADN de cada especie de Plasmodium con un límite de detección de 50 parásitos/ul de sangre. De todos modos, es importante destacar el peso que viene ganando P. vivax como responsable de presentaciones clínicas graves en diferentes partes del mundo, así como en la región de Urabá (15-24).
Aunque no se conocen los mecanismos fisiológicos que explican las diversas presentaciones clínicas graves en los pacientes con malaria por P. vivax, Andrade, et al., describieron en un estudio publicado en 2010, que estas se encuentran estrechamente asociadas con la respuesta inmunitaria del huésped, mediada por la activación de la respuesta proinflamatoria y el desequilibrio en la producción de citocinas (20).
La complicación más frecuente en este estudio fue la anemia grave (49/83, 59 %), que fue la única en 43 casos y que se asoció con otras en 6; esto es similar a lo encontrado por Herrera, et al., quienes reportaron 69,4 % de episodios de anemia grave en Apartadó, usando el mismo criterio de gravedad de este estudio: hemoglobina menor de 7 g/dl (24).
De igual modo, Kochar, et al. reportaron la anemia grave como el hallazgo más frecuente en 150 niños con malaria grave en India, en 63,1 % por P. vivax y en 42,7 % por P. falciparum (25). La anemia se ha asociado frecuentemente con paludismo y es producida por múltiples mecanismos, que incluyen la destrucción de eritrocitos parasitados y no parasitados, la eritrofagocitosis y la inhibición de la eritropoyesis (26).
El 24,1 % de los casos complicados presentaron trombocitopenia con recuento menor de 20.000 plaquetas/mm3 de sangre, incluyendo 15 pacientes con este único criterio y 5 con trombocitopenia asociada a otros. La trombocitopenia es un hallazgo frecuente en los pacientes palúdicos. Se ha propuesto que se debe a la destrucción mediada por complejos inmunitarios circulantes formados por antígenos de Plasmodium spp. e inmunoglobulinas séricas, principalmente anti-cuerpos antiplaquetarios de tipo IgG e IgM (27-29). En un estudio sobre plaquetas y anticuerpos antiplaquetarios en la misma zona, se informó que 77 % de los pacientes con P. vivaxy 63 % de aquellos con P. falciparum, residentes en el municipio de Turbo, tenían recuento plaquetario inferior a 150.000/mm3, con un promedio de 115.115/mm3 en los casos de P. vivax(27).
En el presente estudio se encontró un promedio de 88.000 plaquetas/mm3 el primer día de hospitalización, con tendencia al descenso en el segundo día (60.000/mm3). Es importante mencionar que los pacientes del estudio de Turbo eran ambulatorios, mientras que los de Apartadó eran hospitalarios, por lo cual podría esperarse un nivel más bajo de plaquetas por el posible deterioro clínico; de igual modo, merece destacarse que aun en pacientes no muy enfermos se presenta una leve disminución de plaquetas.
Un paciente de este estudio presentó síndrome de dificultad respiratoria del adulto; las complicaciones pulmonares suelen presentarse entre el segundo y tercer día de tratamiento, y pueden manifestarse como dicho síndrome o como edema pulmonar agudo (30). Varios autores describen la complicación pulmonar como uno de los hallazgos más frecuente-mente asociados con malaria grave por P. vivax, aunque los mecanismos fisiopatológicos en estos casos no se han esclarecido. Se sugiere que en ellos hay un mecanismo inflamatorio de base. La obstrucción de las vías aéreas pequeñas, la alteración de la ventilación pulmonar, la disminución del intercambio gaseoso y el aumento de la actividad fagocitaria pulmonar, son los mecanismos que explican la alteración de la función pulmonar (31). Según el grado de compromiso, ésta puede producir desde un cuadro respiratorio simple hasta uno grave de edema pulmonar agudo o síndrome de dificultad respiratoria del adulto. El grado de lesión pulmonar es reflejo del juego entre el sistema inmunitario del huésped y los antígenos del parásito, que condiciona la variabilidad de la alteración inflamatoria que puede producirse en unas infecciones y en otras no (32). El edema pulmonar no cardiogénico suele desarrollarse rápidamente después de iniciado el tratamiento antipalúdico (33).
Se sabe que la oportunidad en el diagnóstico y tratamiento es fundamental para disminuir la progresión de la enfermedad hasta estados complicados de difícil manejo, lo cual se evidencia con los resultados de este trabajo y que ya ha sido documentado previamente en la literatura científica (34). Aunque en algunos pacientes no se cumplieron los criterios extremos de gravedad establecidos por la OMS, requirieron manejo hospitalario porque tenían un deterioro importante de su estado de salud y presentaban alteraciones importantes en los exámenes de laboratorio; el inicio del tratamiento antipalúdico oportuno y las medidas de soporte, evitaron complicaciones mayores o muertes.
Vale la pena mencionar que no se registraron muertes por malaria por P. vivax en los cuatro años del estudio; sin embargo, habiendo criterios de gravedad palúdica en 83 pacientes, sólo en 4 (4,8 %) se administró quinina, lo cual permite suponer que estos pacientes respondieron bien al esquema con cloroquina y a las medidas de soporte que hacen parte del manejo integral del paludismo. Sin embargo, es un hecho que los casos de malaria complicada no están recibiendo un manejo adecuado, de acuerdo con la guía para la atención clínica integral del paciente con malaria del Ministerio de la Protección Social. Esto puede explicarse, en parte, por el desconocimiento de los funcionarios de salud, reflejado también en el manejo inadecuado de los casos de malaria no complicada. Otra causa podría ser la deficiente gestión del Programa de Control de la Malaria para la consecución de insumos.
Con respecto a la edad, se destaca la alta frecuencia de presentaciones graves en el grupo de menores de cinco años (38,5 %) y menores de un año (9,6 %). Varios autores reportan malaria grave en este grupo de riesgo. Al-Mekhlafi, et al. (35), y Kochar, et al. (25), encontraron asociación entre malaria grave y menores de cinco años en una serie de 78 casos en Yemen, y en una de 150 en India. Piñeros-Jiménez, et al., reportaron cinco casos de malaria neonatal grave por P. vivax en la región de Urabá, por lo cual concluyeron que los niños a esta edad tienen un alto riesgo de complicaciones y sugieren ser más acuciosos en el diagnóstico y tratamiento adecuados y oportunos de estos pacientes, partiendo de una vigilancia constante del paludismo durante la gestación y de un seguimiento sistemático a los neonatos en riesgo (15).
En términos generales, los pacientes presentan recuento constante de leucocitos, con diferencial dentro de límites normales, anemia moderada y trombocitopenia moderada. Sin embargo, hacia el segundo día de estancia hospitalaria y segundo día de tratamiento antipalúdico, hay una tendencia acentuada a la disminución de la hemoglobina, en promedio 1,2 g/dl, el recuento total de leucocitos permanece estable, aunque se insinúa un leve descenso de los neutrófilos y un ascenso ligero de los linfocitos; igualmente, al segundo día se intensifica la trombocitopenia (no se presentan los datos).
Sólo cinco pacientes presentaron disfunción renal, según el criterio de complicación definido para el presente trabajo, dos como criterio único y los otros asociados a otros criterios (anemia grave, trombocitopenia grave e hiperbilirrubinemia). La falla renal aguda en la malaria resulta del desequilibrio hemodinámico e inmunológico causado por la infección (32), y se puede manifestar como necrosis tubular aguda, nefritis intersticial o glomerulonefritis; sin embargo, en la mayoría de los casos la lesión renal era de origen isquémico y la necrosis tubular aguda fue la lesión más común (36).
Andrade, et al., en el estudio realizado en la Amazonia de Brasil en 2007, encontraron una frecuencia de malaria complicada por P. vivax confirmada por PCR, en 8,68 % de 219 pacientes. Entre los hallazgos más importantes estaba la alteración de los siguientes parámetros de laboratorio clínico (promedio): hemoglobina (6,4 g/dl), creatinina (1,7 mg/dl), aspartato aminotransferasa (385,5 U/L), alanino aminotransferasa (238,4 g/dl), bilirrubina total (2,1 mg/dl), bilirrubina directa (1,1 mg/dl) y bilirrubina indirecta (1,1 mg/dl), que evidencian el compromiso de diferentes órganos en la malaria producida por esta especie de Plasmodium. Las manifestaciones más frecuentes fueron dificultad respiratoria, anemia grave, ictericia y, con menor frecuencia, disfunción renal (20).
En otro estudio, Alexandre, et al., publicaron la caracterización clínica de 17 pacientes hospitalizados en la Amazonia brasilera, en los cuales se encontró con mayor frecuencia ictericia, seguida de anemia grave, disfunción renal y síndrome de dificultad respiratoria (19). Los resultados de ambos estudios son similares a los reportados en el presente trabajo, en el cual los criterios más frecuentes fueron anemia grave, trombocitopenia grave, ictericia y, con menor frecuencia, hipoglucemia, disfunción hepática y renal, y sólo un caso de síndrome de dificultad respiratoria del adulto.
Urabá es una región endémica para diversas enfermedades infecciosas que, inicialmente, producen un síndrome febril acompañado de otras manifestaciones generales y pueden confundirse fácilmente con malaria, dengue, leptospirosis, infecciones de las vías respiratorias superiores y fiebre tifoidea, entre otras. Conociendo la historia natural, y las manifestaciones clínicas y de laboratorio de cada una de estas enfermedades, es recomendable descartar una infección concomitante cuando los pacientes no mejoran a pesar del tratamiento específico adecuadamente instaurado. En el presente estudio se encontró que 7,8 % (28/359) de los pacientes presentaron infecciones asociadas, demostradas por pruebas de laboratorio, las cuales correspondieron a dengue, infección del sistema urinario, leptospirosis, infección del sistema respiratorio, otitis y bronconeumonía. En algunos de los reportes en la literatura científica se documentan estas enfermedades concomitantes con malaria (37-39); se resalta que en el municipio de Apartadó, 17 % de los casos hospitalizados por dengue en el 2000 presentaron simultáneamente malaria (37).
Como conclusión, se destaca la frecuencia significativa de malaria complicada por P. vivax, particularmente en los menores de cinco años, en la región de Urabá, y la necesidad de fortalecer el conocimiento de la guía para la atención clínica integral del paciente con malaria, entre el personal de salud, para hacer un diagnóstico clínico correcto, ofrecer un tratamiento apropiado a los pacientes complicados y evaluar la respuesta terapéutica utilizando parámetros clínicos y parasitológicos estandarizados actualmente para esta enfermedad en Colombia.
Los autores del presente trabajo quieren agradecer al personal administrativo y del archivo clínico del Hospital “Antonio Roldán Betancur”, E.S.E., de Apartadó, que facilitó el acceso a las historias clínicas de los casos, lo mismo que a los auxiliares de investigación del ICMT-CES.
No existe conflicto de intereses entre los autores, las instituciones financiadoras y el contenido del presente trabajo.
El presente trabajo fue financiado por el Instituto Colombiano de Medicina Tropical-Universidad CES (ICMT-CES),por el Colegio Mayor de Antioquia y por el Grupo Malaria de la Universidad Antioquia: proyecto Colciencias código 1115-493-26137; RC 488-2009.
Correspondencia: Margarita Arboleda Naranjo, Instituto Colombiano de Medicina Tropical-CES, Carrera 98 Nº 106-176, Barrio Chinita, interior, E.S.E. Antonio Roldán Betancur, Apartadó, Antioquia. Telefax: 828 1708 marboleda@ces.edu.co
1. World Health Organization. World Health Organization Global Malaria Programme. World Malaria Report 2008. Geneve: WHO; 2008. Fecha de consulta: 25 de marzo de 2010. Disponible en: http://www.who.int/malaria/publications/atoz/9789241563697/en/index.html [ Links ]
2. Luxemburger C, Thwai KL, White NJ, Webster HK, Kyle DE. Maelankirri L, et al. The epidemiology of malaria in a Karen population on the western border of Thailand. Trans R Soc Trop Med Hyg. 1996;90:105-11. [ Links ]
3. Zhou G, Sirichaisinthop J, Sattabongkot J, Jones J, Bjornstad ON, Yan G, et al. Spatio-temporal distribution of Plasmodium falciparum and P. vivax malaria in Thailand. Am J Trop Med Hyg. 2005;72:256-62. [ Links ]
4. Duarte EC, Gyorkos TW, Pang L, Abrahamowicz M. Epidemiology of malaria in a hypoendemic Brazilian Amazon migrant population: A cohort study. Am J Trop Med Hyg. 2004;70:229-37. [ Links ]
5. Vargas J. Prevención y control de la malaria y otras enfermedades transmitidas por vectores en el Perú. Rev Peruana Epidemiol. 2003;11:1-18. [ Links ]
6. Instituto Nacional de Salud. Estadísticas de vigilancia en salud pública, año 2008. Fecha de consulta: 24 de mayo de 2011. Disponible en: http//www.ins.gov.co/?idcategoria=1730. [ Links ]
7. Dirección Seccional de Salud y Protección Social de Antioquia. Eventos de interés en salud pública por municipio 2007-2009. Fecha de consulta: 24 de mayo de 2011. Disponible en: http://www.dssa.gov.co/index.php/estadisticas/eventos-de-salud-publica. [ Links ]
8. World Health Organization. Severe falciparum malaria. World Health Organization, Communicable Diseases Cluster. Trans R Soc Trop Med Hyg. 2000;94:S1-90. [ Links ]
9. Ministerio de la Protección Social. Guía para la atención clínica integral del paciente con malaria. Bogotá, D.C.: Ministerio de la Protección Social; 2010; 1-129. [ Links ]
10. Tobón C, Giraldo C, Piñeros J, Arboleda M, Blair S, Carmona-Fonseca J. Epidemiología de la malaria falciparum complicada: estudio de casos y controles en Tumaco y Turbo, Colombia, 2003. Rev Bras Epidemiol. 2006;9:283-96. [ Links ]
11. Echeverri M, Tobón A, Álvarez G, Carmona J, Blair S. Clinical and laboratory findings of Plasmodium vivax malaria in Colombia. Rev Inst Med Trop São Paulo. 2003;45:29-34. [ Links ]
12. Piñeros JG. Epidemiología de malaria durante el embarazo en Urabá, Colombia, 2005-2009: una construcción biosocial. Trabajo de grado (Doctor en Salud Pública) Bogotá, D.C.: Universidad Nacional de Colombia; 2011. p. 184. [ Links ]
13. World Health Organization. Management of severe malaria: A practical handbook. Second edition. Geneva: WHO; 2000. [ Links ]
14. World Health Organization. Guidelines for the treatment of malaria. Switzerland. 2006. Fecha de consulta: 29 de agosto de 2011. Disponible en: http://ec.europa.eu/echo/files/policies/sectoral/health_2006_malaria_treatment_guidelines_who.pdf. [ Links ]
15. Piñeros-Jiménez JG, Arboleda M, Jaramillo JC, Blair S. Reporte de cinco casos de malaria neonatal grave por Plasmodium vivax en Urabá, Colombia. Biomédica. 2008;28:471-9. [ Links ]
16. Lomar A, Vidal J, Lomar F, Valente BC, Janot de Matos G, Boulos M. Acute respiratory distress syndrome due to vivax malaria: Case report and literature review. Braz J Infect Dis. 2005;9:425-30. [ Links ]
17. Rifakis P, Hernández O, Fernández C, Rodríguez-Morales A, Von A, Franco-Paredes C. Atypical Plasmodium vivax malaria in a traveler: Bilateral hydronephrosis, severe thrombocytopenia, and hypotension. J Travel Med. 2008;15:119-21. [ Links ]
18. González L, Guzmán M, Carmona-Fonseca J, Lopera T, Blair S. Características clínico epidemiológicas de 291 pacientes hospitalizados por malaria en Medellín. Acta Med Colomb. 2000;25:163-70. [ Links ]
19. Alexandre M, Ferreira C, Siqueira A, Magalhães B, Mourão M, Lacerda M, et al. Severe Plasmodium vivax malaria, Brazilian Amazon. Emerg Infect Dis. 2010;16:1611-4. [ Links ]
20. Andrade B, Reis-Filho A, Souza-Neto S, Clarêncio J, Camargo L, Barral A, et. al. Severe Plasmodium vivax malaria exhibits marked inflammatory imbalance. Malar J. 2010. Fecha de consulta: 24 de mayo de 2011. Disponible en: http://www.malariajournal.com/content/9/1/13. [ Links ]
21. Genton B, D´Acremont V, Rare L, Baea K, Reeder J, Alpers M, et al. Plasmodium vivax and mixed infections are associated with severe malaria in children: A prospective cohort study from Papua New Guinea. Fecha de consulta: 27 de mayo de 2011. Disponible en: http://www.plosmedicine.org/article/info:doi/10.1371/journal.pmed.0050136. [ Links ]
22. Kakar A, Bhoi S, Prakash V, Kakar S. Profound thrombocytopenia in Plasmodium vivax malaria. Diag Microbiol Infect Dis. 1999;35:243-4. [ Links ]
23. Sarkar S, Saha K, Sekhar Das C. Three cases of ARDS: An emerging complication of Plasmodium vivax malaria. Lung India 2010;27:154-7. [ Links ]
24. Herrera A, Montoya L, Arboleda M, Ortiz L. Asociación de la malaria severa con tipo de grupo sanguíneo ABO en una zona endémica de Colombia. Rev CES Med. 2009;23:9-16. [ Links ]
25. Kochar DK, Tanwar GS, Khatri PC, Kochar SK, Sengar GS, Gupta A, et al. Clinical features of children hospitalized with malaria -A study from Bikaner, Northwest India. Am J Trop Med Hyg. 2010;83:981-9. [ Links ]
26. Llanos C, Flórez M, Arévalo-Herrera M, Herrera S. Mecanismos de generación de anemia en malaria. Colombia Médica. 2004;35:205-14. [ Links ]
27. Ríos-Orrego A, Álvarez-Castillo T, Carmona-Fonseca J, Blair-Trujillo S. Evolución temporal de las plaquetas y los anticuerpos antiplaquetarios en pacientes de área endémica con malaria no complicada. An Med Interna (Madrid). 2005;22:561-8. [ Links ]
28. Touze J, Mercier P, Rogier C, Hovette P, Schmoor P, Dabanian C. Platelet activity in malaria thrombocytopenia. Phatol Biol. 1990;38:678-81. [ Links ]
29. Kelton G, Keystone J, Moore J, Denomme G, Tozman E, Glynn M. Inmune-mediated thrombocytopenia of malaria. J Clin Inv. 1983;71:832-6. [ Links ]
30. Illamperuma C, Allen B. Pulmonary edema due to Plasmodium vivax malaria in an American missionary. Infection. 2007;35:374-6. [ Links ]
31. Anstey N, Jacups S, Cain T, Pearson T, Ziesing P, Fisher DA, et al. Pulmonary manifestations of uncomplicated falciparum and vivax malaria: Cough small airways obstruction, impaired gas transfer, and increased pulmonary phagocytic activity. J Infect Dis. 2002;185:1326-34. [ Links ]
32. Giraldo C, Blair S, Tobón A. Complicaciones pulmonares en malaria. Infectio. 2004;8:279-91. [ Links ]
33. Tagle R, Cabanban A. Severe and complicated malaria at San Lazaro Hospital. Fecha de consulta: 24 de mayo de 2011; Disponible en: http://www.psmid.org.ph/vol21/vol21num1topic2.pdf. [ Links ]
34. Luxemburger C, Ricci F, Nosten F, Raimond D, Bathet S, WhiteN. The epidemiology of severe malaria in an area of low transmission in Thailand. Trans R Soc Trop Med Hyg. 1997;9:256-62. [ Links ]
35. Al-Mekhlafi A, Mahdy M, Azazy A, Fong M. Clinical situation of endemic malaria in Yemen. Trop Biomed. 2010;27:551-8. [ Links ]
36. Prakash J, Singh A, Gujrati S, Maheshwari A. Acute renal failure in malaria: Changing trends. Indian Journal Nephrology. 2002;12:153-7. [ Links ]
37. Arboleda M, Campuzano M, Restrepo B, Cartagena G. Caracterización clínica de los casos de dengue hospitalizados en la E.S.E. Hospital "Antonio Roldán Betancur", Apartadó, Antioquia, Colombia. Biomédica. 2000;26:286-94. [ Links ]
38. Srinivas R, Agarwal R, Gupta D. Severe sepsis due to severe falciparum malaria and leptospirosis co-infection treated with activated protein C. Malar J. 2007;6:42. [ Links ]
39. Charrel R, Brouqui P, Foucault C, de Lamballerie X. Concurrent dengue and malaria. Emerg Infect Dis. 2005;11:1153-4. [ Links ]














