Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biomédica
Print version ISSN 0120-4157
Biomédica vol.33 no.3 Bogotá july/Sept. 2013
https://doi.org/10.7705/biomedica.v33i3.1441
ARTÍCULO ORIGINAL
doi: http://dx.doi.org/10.7705/biomedica.v33i3.1441
1 Departamento de Microbiología, Pontificia Universidad Javeriana, Bogotá, D.C., Colombia
2 Departamento de Patología, Fundación Santa Fe de Bogotá, Bogotá, D.C., Colombia
3 Laboratorio de Genética Humana, Departamento de Ciencias Biológicas, Universidad de los Andes, Bogotá, D.C., Colombia
4 Laboratoire de Pathologie, Université Paris Diderot, Paris, Francia
5 Facultad de Medicina, Departamento de Pediatría/Oncohematología Pediátrica, Universidad Nacional de Colombia, Bogotá, D.C., Colombia
6 Servicio de Onco-Hematología Pediátrica, Fundación Hospital de La Misericordia, Bogotá, D.C., Colombia
Instituciones donde se llevó a cabo el trabajo: Fundación Santa Fe de Bogotá, Fundación Hospital de la Misericordia y Pontificia Universidad Javeriana.
Contribución de los autores:
Sandra Milena Quijano, Carlos Eugenio Saavedra, María Mercedes Torres, Rafael Enrique Andrade: concepción del estudio.
Adriana Linares, Silverio Castaño, Isabel Cristina Sarmiento, Edgar Cabrera, Gloria Inés Uribe: selección de pacientes, obtención de muestras de médula ósea y obtención de consentimientos informados.
Gina Elizabeth Cuéllar y Edna Liliana Martín: procesamiento y marcación inmunofenotípica por citometría de flujo de las muestras de médula ósea.
Sandra Milena Quijano, Carlos Eugenio Saavedra, Martha Liliana Romero: análisis e interpretación del inmunofenotipo de las muestras de médula ósea.
Sandra Milena Quijano y Gina Elizabeth Cuéllar: procesamiento y marcación de muestras de médula ósea para estudios de ciclo celular por citometría de flujo.
Sandra Milena Quijano y Carlos Eugenio Saavedra: análisis e interpretación de estudios de ciclo celular de las muestras de médula ósea por citometría de flujo.
María Mercedes Torres, Liliana Edith Vásquez y Rafael Enrique Andrade: detección de traslocaciones cromosómicas por RT-PCR.
Sandra Milena Quijano y Liliana Edith Vásquez: elaboración de bases de datos.
Sandra Milena Quijano: análisis estadístico de los resultados y elaboración de tablas y figuras.
Todos los autores participaron en la escritura del artículo.
Recibido: 26/10/12; aceptado:23/05/13
Introducción. Del 60 al 80 % de los pacientes con leucemia linfoblástica aguda de precursores B presentan alteraciones genéticas que influyen en el pronóstico de la enfermedad y en la biología del tumor.
Objetivo. Analizar distintas alteraciones genéticas en leucemia linfoblástica aguda de precursores B en niños, y su relación con el inmunofenotipo y con la tasa de proliferación, en comparación con precursores B normales.
Materiales y métodos. En 44 pacientes se evaluó, por citometría de flujo, el inmunofenotipo, el contenido de ADN y la proliferación, y por RT-PCR, las traslocaciones t(9;22), t(12;21), t(4;11) y t(1;19). Mediante un análisis jerarquizado de conglomerados se identificaron los patrones inmunofenotípicos de expresión asociados a las traslocaciones, tomando como referencia precursores B normales.
Resultados. La cuantificación del ADN mostró que el 21 % de los casos de leucemia linfoblástica aguda de precursores B eran hiperdiploides de índice alto y, el 47,7 %, hiperdiploides de índice bajo. La presencia de hiperdiploidía se asoció con mayor proliferación tumoral y con inmunofenotipos aberrantes, que incluyeron expresión anormal de CD10, TdT, CD38 y CD45 y un mayor tamaño de los linfoblastos. La presencia de t(9;22) y t(12;21) discrimina células normales de células tumorales con aberraciones en la expresión de CD19, CD20, CD13, CD33, CD38, CD34 y CD45.
Conclusiones. El perfil de aberraciones fenotípicas detectado en conjunto con anormalidades en la proliferación tumoral, se asocia de forma significativa con hiperdiploidiía de ADN y discrimina de forma clara linfoblastos con t(9;22) y t(12;21) de los precursores B normales. La identificación de estos parámetros será de gran utilidad como herramienta para la clasificación y seguimiento de los pacientes.
Palabras clave: leucemia linfoblástica, citometría de flujo; médula ósea.
doi: http://dx.doi.org/10.7705/biomedica.v33i3.1441
Correlation of the t(9;22), t(12;21), and DNA hyperdiploid content with immunophenotype and proliferative rate of leukemic B-cells of pediatric patients with B-cell acute lymphoblastic leukemia
Introduction: Between 60 and 80% of patients with B-cell acute lymphoblastic leukemia show genetic abnormalities which influence the prognosis of the disease and the biology of the tumor.
Objective: To analyze different genetic abnormalities in acute B lymphoblastic leukemia in children, its relationship with the immunophenotype and the proliferative rate compared with normal B cell precursors.
Materials and methods: We assessed immunophenotype, DNA content and proliferative rate in 44 samples by flow cytometry, and translocations t(9;22), t(12;21), t(4;11), and t(1;19) by RT-PCR. Using a hierarchical cluster analysis, we identified some immunophenotypic patterns associated to genetic abnormalities when compared with normal B cell precursors.
Results: DNA quantification showed that 21% of the cases had high hyperdiploidy and 47.7% has low hyperdiploidy. The presence of hyperdiploidy was associated with increased tumor proliferation and aberrant immunophenotypes, including abnormal expression of CD10, TdT, CD38, and CD45 and an increased size of the lymphoblasts. The presence of t(9;22) and t(12;21) discriminates normal cells from tumor cells with aberrant immunophenotype in the expression of CD19, CD22, CD13, CD33, CD38, CD34, and CD45.
Conclusions: The aberrant immunophenotype profile detected in neoplastic cells along with abnormalities in the proliferative rate were significantly associated with DNA hyperdiploidy and clearly distinguished lymphoblasts with t(9;22) and t(12;21) from normal B cell precursors. The identification of these parameters is useful as a tool for classification and monitoring of these patients.
Key words: Leukemia, lymphoblastic, flow cytometry, bone marrow.
doi: http://dx.doi.org/10.7705/biomedica.v33i3.1441
La leucemia linfoblástica aguda de precursores B es una neoplasia de origen hematopoyético con características clínicas y biológicas heterogéneas. Esta leucemia representa el 25 % de todos los tumores diagnosticados en menores de 15 años (1-4) y, en Colombia, la incidencia anual reportada es de 5,6 a 6 casos por 100.000 niños (5).
En el desarrollo, comportamiento clínico y progresión de la enfermedad, se ha descrito que el 60 a 80 % de los niños con leucemia linfoblástica aguda presentan alteraciones genéticas en el número de cromosomas o cambios estructurales con un impacto significativo sobre el pronóstico. Se ha reportado que estas alteraciones afectan los genes reguladores de la diferenciación celular, el ciclo celular, las vías de señalización y la apoptosis, tales como las traslocaciones cromosómicas t(12;21) (p13;q22) con TEL-AML1, t(9;22) (q34;q11) con BCR-ABL, t(4;11) (q21;q23) con MLL-4F4 y t(1;19) (q23;p13) con E2A-PBX1, entre otras (1,2,3,6). Asimismo, se han descrito diferentes patrones inmunofenotípicos aberrantes en la leucemia linfoblástica aguda como consecuencia de las anomalías genéticas presentes en las células tumorales.
En el presente trabajo se analizó la correlación entre las traslocaciones cromosómicas t(9;22) (q34;q11) con BCR-ABL y t(12;21) (p13;q22) con TEL-AML1 y de la aneuploidía de ADN, con el perfil inmunofenotípico y la tasa de proliferación de células B neoplásicas de la leucemia linfoblástica aguda de precursores B de fenotipo común y de leucemia linfoblástica aguda pre-B. Además, se describieron las aberraciones fenotípicas asociadas al tumor en comparación con el control normal de cada tipo de leucemia, empleando un panel básico de anticuerpos de fácil aplicabilidad clínica y que contrasta con las tendencias actuales de paneles de anticuerpos más amplios (7,8).
Se encontró que, en comparación con los precursores B normales de la médula ósea, las células tumorales de la leucemia linfoblástica aguda tienen gran heterogeneidad en la expresión antigénica con una frecuencia variable (28-100 %) de aberraciones fenotípicas que incluyen asincronismos en la maduración (presencia de CD20 en células CD34+) e infidelidad de línea (expresión de marcadores asociados al linaje T y mieloide: CD7, CD15, CD13 y CD33), entre otras.
Se encontró gran frecuencia de hiperdiploidía de ADN (>60 %) en los linfoblastos leucémicos detectada por citometría de flujo, que se asoció a un incremento significativo en la tasa de proliferación tumoral (superior al 5 %), y en el inmunofenotipo con sobreexpresión de los marcadores CD10 y TdT en conjunto con mayor tamaño de los linfoblastos y menor expresión de CD38 y CD45.
Por otro lado, la presencia de linfoblastos t(9;22) y t(12;21) discrimina de forma clara las células tumorales con aberraciones fenotípicas (sobreexpresión o infraexpresión) de los marcadores CD19, CD20, CD38, CD34 y CD45 y expresión aberrante fuerte de CD13 y CD33.
La identificación de estas aberraciones fenotípicas y genéticas en los linfoblastos leucémicos puede ser de gran utilidad como herramienta para la evaluación y el seguimiento de la enfermedad mínima residual después de la quimioterapia.
Materiales y métodos
Definición de sujetos y muestras de estudio
En el presente estudio se evaluaron 44 muestras de médula ósea, obtenidas en EDTA, de niños (23 niñas y 21 niños) con diagnóstico de leucemia linfoblástica aguda de precursores B (7±5 años; rango, 1 a 17 años) procedentes de la Fundación Hospital de La Misericordia de Bogotá.
La distribución de los casos según el diagnóstico fue: leucemia linfoblástica aguda de precursores B pro-B (n=2), leucemia linfoblástica aguda de precursores B de fenotipo común (n=35) y leucemia linfoblástica aguda de precursores B pre-B (n=7).
El porcentaje de infiltración tumoral en la médula ósea detectado por citometría de flujo fue de 82±20 % (rango, 12 a 98,7 %). Como controles se emplearon siete muestras de médula ósea de niños (3±4 años; rango, 1 a 10 años) con diagnóstico de púrpura trombocitopénica inmunitaria (2 niñas y 5 niños), sin anormalidades hematológicas en la médula ósea.
Todas las muestras se recolectaron una vez los los padres o representantes de los pacientes hubieran firmado el consentimiento informado aprobado por el Comité de Ética de la Fundación Santa Fe de Bogotá, la Universidad de los Andes y de la Fundación Hospital de La Misericordia.
Análisis inmunofenotípico mediante citometría de flujo
Para hacer el análisis inmunofenotípico de las diferentes fases de maduración de células B de médula ósea, normales en los controles y neoplásicas en los 44 pacientes, se empleó un panel básico de anticuerpos monoclonales y policlonales combinados en tres a seis fluorescencias distintas, incluyendo marcadores reportados en la literatura científica que permiten la identificación y caracterización fenotípica de leucemias agudas de linaje B (9,10) (fluorocromos: FITC/PE/PERCPCY5.5/PECy7/APC/APCCy7): cyTdT/cyCD79a/CD19, CD20/CD10/CD19/CD38/CD34/CD45, CD15/7.1/CD19/CD13, cyIgM/CD33/CD19, y HLA-DR/CD7/CD19.
Para la marcación inmunofenotípica se siguió un protocolo estandarizado que permite la detección de antígenos celulares localizados en la membrana, en el citoplasma o en ambos (9,11,12). Para la marcación de los antígenos de membrana, se incubaron 50 µl de muestra de médula ósea con los anticuerpos conjugados con fluorocromos durante 15 minutos a temperatura ambiente y en la oscuridad. Una vez transcurrido este tiempo, se adicionó 1 ml de solución de lisis (BD FACS Lysing Solution) durante 10 minutos y se hicieron dos lavados con 2 ml de solución salina tampón ( Phosphate Buffered Saline, PBS), seguidos de centrifugación durante cinco minutos a 2.000 rpm.
Para la detección simultánea de antígenos celulares localizados en membrana y en citoplasma, se empleó el kit de fijación y permeabilización (InstraStain-Dako ), en el cual se hizo en un primer paso la marcación de los antígenos de membrana, seguida de incubación con 100 µl de solución fijadora (reactivo A) y 100 µl de solución de permeabilización (reactivo B), en conjunto con el anticuerpo dirigido contra el antígeno intracelular (marcadores: TdT, CD79a e IgM).
Las incubaciones en cada paso se hicieron durante 15 minutos (para los marcadores de membrana) y durante 30 minutos (para los marcadores intracelulares) a temperatura ambiente y en la oscuridad, seguidas de lavados con PBS. Como control de autofluorescencia (control negativo), se procesaron dos tubos adicionales sometidos a los mismos tratamientos descritos para las diferentes marcaciones, excepto que a estos no se les adicionó anticuerpo conjugado (12).
Una vez hecha la marcación, las muestras se adquirieron' en el citómetro de flujo (BD FACSCAnto II flow cytometer), empleando el programa informático FACSDiva (BDB) y almacenando la información de, aproximadamente, 50.000 eventos totales. El análisis de los datos se hizo con el programa INFINICYT TM (Cytognos SL, Salamanca, España), evaluando el porcentaje de expresión e intensidad media de fluorescencia para cada uno de los antígenos en estas células.
Las poblaciones celulares se clasificaron como positivas para cada marcador si la expresión del mismo (porcentaje e intensidad media de fluorescencia) era superior a la observada en el control negativo (autofluorescencia basal de las células sin anticuerpos) y, para establecer si el marcador analizado se encontraba negativo, con infraexpresión o sobreexpresión, se comparó la intensidad media de fluorescencia de cada marcador en las leucemias con la expresión del mismo marcador en las poblaciones B de médula ósea normal (no leucémica) (13-15).
Para llevar a cabo la compensación del equipo, se emplearon las esferas BD CompBeads , ajustando las señales de fluorescencia y voltajes de cada detector (FL-1-FL-6), con el fin de asegurar la discriminación adecuada entre las señales positivas y negativas. Para la calibración diaria del equipo se utilizaron microesferas fluorescentes (BD Cytometer Setup & Tracking Beads), siguiendo las recomendaciones del fabricante.
Análisis del contenido de ADN y del ciclo celular mediante citometría de flujo
El análisis del índice de ADN y de la distribución de las poblaciones de células B en médula ósea normal y de los casos de leucemia linfoblástica aguda de precursores B en las distintas fases del ciclo celular, se hizo mediante la marcación combinada de antígenos de membrana para identificar células B (CD10/CD19/CD20/CD22) y el colorante de ADN yoduro de propidio, siguiendo las instrucciones del estuche comercial Cycloscope B-ALL (Cytognos SL, Salamanca, España), y siguiendo la metodología técnica y de análisis descrita en estudios previos (13,14).
Las muestras de médula ósea (50 µl) se incubaron durante 15 minutos con la mezcla de anticuerpos monoclonales primarios anti-CD10/CD19/CD20/CD22 (40 µl) y, posteriormente, se adicionó el anticuerpo secundario anti-IgG de ratón (obtenido en cabra) conjugado con 20 µl de fluoresceína (FITC). A continuación, se añadieron 2 ml de solución de lisis de eritrocitos (solución hipotónica de cloruro de amonio libre de fijador) durante 10 minutos y las muestras se centrifugaron durante cinco minutos a 2.000 rpm. El botón celular obtenido fue resuspendido con 500 µl de la solución de marcación de ADN que contenía yoduro de propidio y ribonucleasa (RNasa), durante 10 minutos. Todas las incubaciones se hicieron a temperatura ambiente y en la oscuridad, seguidas de lavados con PBS.
Una vez hechas las adquisiciones en el citómetro de flujo BD FACSCAnto II y el análisis de datos con el programa INFINICYT TM (Cytognos SL, Salamanca, España), se evaluó el índice de ADN de las células tumorales (cociente entre el canal medio de fluorescencia de los linfoblastos en la fase G0/G1 y de las células B normales residuales presentes en la misma muestra del paciente en fase G0/G1 del ciclo celular), el porcentaje de células en la fase G0/G1, el coeficiente de variación del pico G0/G1 y el porcentaje de células en fase S+G2/M (tasa de proliferación) (13,14). La población de linfoblastos se catalogó como diploide, si el índice de ADN era igual a 1, como hiperdiploide de índice alto, si era de 1,16 o más, y como hiperdiploide de índice bajo o intermedio, si era de 1,01 a 1,15 (13,14,16,17).
Detección de traslocaciones cromosómicas mediante RT-PCR
Para la detección de las traslocaciones asociadas al pronóstico en leucemia linfoblástica aguda de precursores B [t(9;22) (q34;q11) con BCR-ABL; t(4;11) (q21;q23) con MLL-4F4; t(1;19) (q23;p13) con E2A-PBX1, y t(12;21) (p13;q22) con TELAML1 (4)], se extrajo ARN total a partir de 300 µl de muestra de médula ósea remanente de los estudios de inmunofenotipo, en las cuales el procesamiento no excedió un periodo mayor de 12 horas desde el momento de la toma de la muestra. Cada alícuota se homogenizó con Trizol LS Reagent (Invitrogen) en un volumen 1:3 y se almacenó a -70 °C, por un tiempo máximo de 30 días, para continuarse con el proceso de extracción del ARN total según el protocolo estándar.
El ARN se precipitó con isopropanol, se lavó con etanol en agua (70 %) y se almacenó a -70 °C hasta su uso. La integridad del ARN se determinó mediante electroforesis en gel de agarosa al 1 % y su concentración se estableció por espectrofotometría a una longitud de onda de 260 nm. La síntesis de ADNc se hizo a partir de 1µl de ARN total con 262 U de la enzima M-MLVRT (Invitrogen), hexámeros al azar (RandomPrimers de Invitrogen), dNTPs 25 mM, a 37 °C durante dos horas.
Cada uno de los fragmentos de interés se amplificó a partir de 1.000 ng del ADNc con iniciadores específicos para el transcrito de cada traslocación, los cuales se seleccionaron según el consenso europeo de estudio de las leucemias agudas BIOMED-1 (18). El proceso de amplificación enzimática se llevó a cabo mediante el kit comercial AmpliTaq Gold 360 Master Mix (Invitrogen), con un perfil térmico de desnaturalización a 95 °C por 30 segundos, anillaje a 65°C por 30 segundos y amplificación a 72 °C por un minuto, por un total de 35 ciclos. La identificación de los fragmentos se llevó a cabo por electroforesis en gel de agarosa al 1,8 % en 1X de solución TBE (Tris-Borate-EDTA ) con tinción de SYBR Safe, y se visualizaron con una lámpara de luz ultravioleta. Como control interno del proceso, se amplificó el gen de la ß -actina y se incluyeron controles positivos para cada una de las traslocaciones.
Análisis de conglomerado
Con el fin de identificar patrones de expresión inmunofenotípicos asociados a las alteraciones genéticas evaluadas, se hizo un análisis jerarquizado de conglomerado ( cluster ), utilizando los programas informáticos Cluster y Treeview. En este análisis los valores de intensidad media de fluorescencia calculados para cada antígeno en los linfoblastos, en cada paciente, se normalizaron utilizando como control los resultados medios correspondientes a las subpoblaciones B de médula ósea normal. Los datos se representaron en un dendrograma, en el cual se pueden discriminar las variables analizadas en grupos o conglomerados de acuerdo con el grado de similitud de los casos (14).
Análisis estadístico
Para el análisis estadístico de los datos, se hizo un análisis descriptivo, determinando para las variables cuantitativas: media, mediana y desviación estándar, y para las variables cualitativas, las frecuencias relativas, mediante el paquete estadístico SPSS , versión 17, y GraphPad Prism 5.0 ., y se aplicó el test de Mann-Whitney. Se consideró una diferencia significativa cuando p era menor de 0,005.
Resultados
Inmunofenotipo de poblaciones B normales de médula ósea
En el análisis inmunofenotípico de las subpoblaciones B de médula ósea normal, se encontró que la maduración del linaje B se caracteriza por cambios secuenciales en la expresión de diferentes antígenos desde las células más inmaduras (pre-pre-B) hasta las células más diferenciadas (pre-B y B maduras). Mediante la selección inicial de estas poblaciones, empleando el marcador CD19 (marcador pan-B) versus granularidad ( Side-Scattered Light , SSC) y analizando posteriormente cada uno de los antígenos del panel, se observó que las células pre-pre-B se caracterizan por la expresión fuerte de los marcadores de inmadurez CD34, TdT y CD10 (figura 1), en conjunto con expresión débil de CD19, CD45, CD79a y HLA-DR (figura 1), en comparación con las células pre-B y los linfocitos B maduros (p<0,05). En el estadio pre-B, de manera característica, los marcadores IgM (presente en el citoplasma) y CD20 se van adquiriendo de forma gradual hasta expresarse con mayor intensidad en los linfocitos B maduros (p<0,05). En relación con el marcador CD38, las células en estadio pre-B corresponden a la subpoblación celular con mayor expresión de esta molécula.
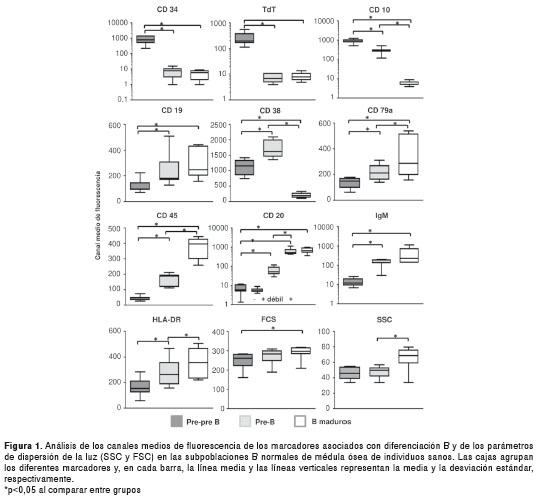
En general, las tres subpoblaciones de médula ósea analizadas fueron negativas para 7.1 (marcador asociado a alteraciones en el gen MLL ) (9,20), para los marcadores de linaje mieloide CD15, CD13, y CD33, y para el marcador de linaje linfoide T CD7. Los linfocitos B maduros mostraron valores superiores en complejidad (SSC) y tamaño ( Forward-Scattered Light , FSC), en comparación con las células pre-pre-B y pre-B (figura 1) (p<0,05).
Análisis comparativo del inmunofenotipo de células leucémicas y no leucémicas
La estrategia de análisis de los linfoblastos de niños con leucemia linfoblástica aguda de precursores B, fue la misma descrita para las poblaciones B normales, mediante una selección dual por medio de CD19 versus granularidad (SSC), seguida del análisis de los demás marcadores incluidos en el panel B. A diferencia de lo encontrado en las poblaciones B de los controles sanos, los linfoblastos leucémicos mostraron un patrón heterogéneo de expresión para los distintos marcadores, encontrándose que dentro de la misma población tumoral había células negativas, positivas débiles y positivas para cada marcador analizado (9,15) (figuras 2 y 3). En general, en esta leucemia se observaron patrones de expresión aberrantes en los 15 marcadores fenotípicos analizados y en los parámetros de dispersión de luz (SSC y FSC).
Respecto a las células normales pre-pre-B, las de la leucemia linfoblástica aguda de precursores B de fenotipo común (figura 2) se caracterizan por la infraexpresión (pérdida de expresión o expresión débil) de CD34, TdT, CD10, CD38, y CD45 (p<0,05), en conjunto con una expresión significativamente más elevada de CD19, y CD79a, y expresan de forma aberrante los marcadores CD20, CD15, CD7, CD13 y CD33, con mayor tamaño y complejidad interna (p<0,05). Se observó heterogeneidad en los niveles de expresión del marcador HLA-DR, en algunos casos había pérdida de expresión o expresión débil y, en otros, sobreexpresión.
Por otra parte, las leucemias linfoblásticas agudas pre-B (figura 3), al ser comparadas con los precursores pre-B normales, mostraron infraexpresión de CD19, CD20, CD38, CD45 e IgM y sobreexpresión de CD10. Entre los marcadores aberrantes presentes en estos linfoblastos se encontraron CD34, TdT, CD13, CD33, CD15 y CD7, y mayor tamaño y complejidad interna (p<0,05).
En las leucemias de precursores B comunes y las pre-B, se observó una frecuencia superior al 40 % de expresión aberrante de los marcadores mieloides CD13 y CD33 y, de forma característica en las pre-B fueron CD20+ (100 %) (marcador asociado con asincronismo en la maduración), CD34+ (86 %) (marcador presente normalmente en células pre-pre-B) y CD7+ (28 %) (marcador asociado a infidelidad de línea).
Detección de traslocaciones cromosómicas en la leucemia linfoblástica aguda de precursores B
Los análisis de RT-PCR revelaron la presencia de alguno de los reordenamientos cromosómicos de impacto pronóstico en 9/44 casos (20,4 %). Se detectaron los transcritos de fusión t(12;21) (p13;q22) con TEL/AML1 y t(9;22)(q34;q11) con BCR/ABL, en 6 casos (13,6 %) y 3 casos (6,8 %), respectivamente, de muestras de pacientes con leucemia linfoblástica aguda de precursores B de fenotipo común. Estos hallazgos están relacionados con estudios previos en los que se ha descrito que la t(12;21) (p13;q22) "asociada a mejor pronóstico", es más frecuente en niños con leucemia linfoblástica aguda de precursores B, en comparación con la t(9;22) (q34;q11) "asociada a peor pronóstico y de mayor frecuencia en adultos" (2,19). En nuestra serie no se encontró t(4;11) en casos de leucemia pro-B (n=2), ni t(1;19) en casos de leucemia pre-B (n=7). La ausencia de estas dos traslocaciones puede estar relacionada con el bajo número de casos incluidos con estos dos subtipos de leucemia linfoblástica aguda (19).
Cuantificación del contenido de ADN y distribución de linfoblastos leucémicos en el ciclo celular
La cuantificación del ADN de los linfoblastos mediante citometría de flujo, mostró que 13/44 (30 %) casos tenían ADN diploide, 9/44 (21 %), hiperdiploide de índice alto, 21/44 (47,7%), hiperdiploide de índice bajo, y 1 (1,3%), hipodiploide.
En la leucemia linfoblástica aguda de precursores B común, la frecuencia de ADN hiperdiploide de índice alto fue de 20 % (7/35 casos) (índice de ADN: 1,45; rango: 1,2-1,9) y, en las pre-B, de 28,6 % (2/7 casos) (índice de ADN: 1,25; rango: 1,2-1,3); por otra parte, la frecuencia de ADN hiperdiploide de índice bajo en la común fue de 48,6 % (17/35 casos) (índice de ADN: 1,05; rango: 1,01-1,15) y, en las pre-B, de 42,9 % (3/7 casos) (índice de ADN: 1,06; rango: 1,04-1,1) (figura 4).
Además, se encontraron 2 (4,5 %) casos de la leucemia de precursores B común con dos poblaciones de linfoblastos con diferente contenido de ADN; el primero mostró una población diploide (61 % de los linfoblastos con índice de ADN=1) y una hiperdiploide de índice alto (39 % de los linfoblastos con índice de ADN=1,3), y el segundo, dos poblaciones de linfoblastos hiperdiploides con contenido de ADN cercano a la tetraplodia (90 % y 10 % de los linfoblastos con índice de ADN de1,9 y 1,7, respectivamente) (20). Este último caso fue, además, positivo para t(12;21) (p13;q22). Las células tumorales con dos poblaciones distintas de linfoblastos con diferente contenido de ADN, pueden considerarse como biclonales, lo que contribuye a la heterogeneidad biológica de estos tumores (21).
En relación con el tipo de traslocación detectada en los linfoblastos, se observó que en 1/6 (17 %) y 3/6 (50 %) casos con t(12;21) (p13;q22) eran hiperdiploides de índice alto y bajo, respectivamente, y en 2/3 (67 %) casos con t(9;22) (q34;q11) eran hiperdiploides, uno con índice alto y dos con bajo.
El análisis de la tasa de proliferación de los linfoblastos mostró que, de manera global, la leucemia de precursores B tenía un mayor porcentaje de células en las fases S+G2/M del ciclo celular (mediana: 5,5 %; rango: 0,5 a 14 %), respecto a las células B normales residuales de la médula ósea del paciente (mediana: 0 %; rango: 0 a 5 %) y respecto a las células B de médula ósea de controles sanos (mediana: 0,6 %; rango: 0 a 1,1 %) (p<0,05) (figura 5 panel A). De manera similar, con respecto a las células B normales, los casos de leucemia linfoblástica aguda de precursores B por subgrupos diagnósticos tenían valores superiores en la tasa de proliferación de los linfoblastos: pro-B, 5,1 % con rango de 1,2 a 9 %; de precursores B común, 5,5 % con rango de 0,5 a 14 %, y pre-B, 2,8 % con rango de 0,9 a 9 % (p<0,05) (figura 5 panel B).
Por otra parte, en el resultado global de las leucemias de precursores B, al comparar los casos con contenido de ADN diploide con aquellos de ADN hiperdiploide (incluyendo los de índice alto y los de bajo), se observó que los primeros mostraron una menor tasa de proliferación (3,3 % con rango de 0,5 a 14 %) que los segundos (7 % con rango de 0,9 a 13%) (p= 0,04) (figura 5 panel C). Sin embargo, al analizar las leucemias de precursores B por subgrupos diagnósticos, no se encontraron diferencias significativas (figura 5 panel D).
Asociación de las las alteraciones genéticas con el inmunofenotipo de la leucemia linfoblástica aguda de precursores B
Al investigar las posibles asociaciones existentes entre el inmunofenotipo de los linfoblastos y las distintas alteraciones genéticas evaluadas en los casos diploides de leucemia de precursores B de fenotipo común, se observó que aquellos con hiperdiploidía se caracterizaron por una mayor expresión de CD10 (p=0,034), un mayor tamaño de los linfoblastos (p=0,031) y tendencia a una menor expresión de CD45 (figura 6 panel A). Por otro lado, los casos con hiperdiploidía de índice bajo mostraron menor expresión de CD38 con incremento de CD10 (p<0,05) y, los de índice alto, tendencia a expresar mayor cantidad de TdT dentro de la célula (p=0,07) (figura 6 paneles B y C). Asimismo, las casos hiperdiploides altos fueron de mayor tamaño que los hiperdiploides bajos (p<0,05) (figura 6 panel D). Finalmente, los casos de leucemia linfoblástica aguda de precursores B de fenotipo común con una tasa de proliferación mayor de 5 %, se caracterizaron por una expresión más baja de CD19 (p<0,05) y una mayor reacción para TdT (p=0,07) (figura 7).
Entre las aberraciones fenotípicas encontradas en los linfoblastos con t(9;22) (q34;q11) con BCR-ABL y t(12;21) (p13;q22) con TEL-AML1, en conjunto, se encontró sobreexpresión de los marcadores mieloides CD13 y CD33, con mayor complejidad y tamaño, e infraexpresión de CD38 (figuras 8 y 9). En comparación con las células pre-pre-B normales, los casos con t(12;21) (p13;q22) con TEL-AML1 mostraron mayor expresión de CD20 y menor expresión de CD34, TdT y CD45 (p<0,05) (figura 8), mientras que los casos con t(9;22) (q34;q11) con BCR-ABL se caracterizaron por mayor expresión de CD19 y CD79a (figura 9). Por otra parte, de los tres casos con t(9;22), uno fue CD7 positivo (33 %).
En el análisis de conglomerados se encontró que al considerar las características inmunofenotípicas de cada población de linfoblastos (leucemia linfoblástica aguda de precursores B común) con alteración genética en comparación con su control normal (células pre-pre-B), se discriminan de forma clara las células B normales de las tumorales, encontrándose dos grupos inmunofenotípicos distintos de los que se resalta que los linfoblastos positivos para t(9;22) (q34;q11) con BCR-ABL y t(12;21) (p13;q22) con TEL-AML1, muestran sobreexpresión de los marcadores CD19, CD20, CD13 y CD33, con infraexpresión de CD38, CD45 y TdT. Además, los parámetros de complejidad (SSC) y tamaño (FSC), también fueron anormales en los linfoblastos de leucemia linfoblástica aguda de precursores B (figura 10).

Discusión
Desde el punto de vista biológico, se ha avanzado en la identificación y la caracterización de las alteraciones genéticas más frecuentes en la leucemia linfoblástica aguda de precursores B (1,4), informándose en la literatura científica una frecuencia entre 60 y 80 % de alteraciones numéricas o estructurales. La detección de estas alteraciones genéticas es de gran utilidad como factor pronóstico independiente de otras variables clínicas y biológicas descritas en el desarrollo y evolución de la enfermedad (1,4). En la actualidad, los criterios establecidos por la Organización Mundial de la Salud (OMS) (22,23) para la clasificación diagnóstica de los pacientes con leucemia linfoblástica aguda de precursores B, se fundamentan en la evaluación morfológica, el inmunofenotipo (línea y fase de maduración) y las alteraciones genéticas recurrentes presentes en las células neoplásicas en la médula ósea y en otros tejidos infiltrados por el tumor (4,9,22,23).
Así, según las alteraciones genéticas, la clasificación de la OMS de este tipo de leucemia incluye principalmente tres grupos de pacientes con distinto pronóstico (4,22,23). Se consideran alteraciones genéticas asociadas a buen pronóstico, la presencia de cariotipos hiperdiploides entre 51 y 65 cromosomas y la t(12;21) (p13;q22) con TEL-AML1. Por el contrario, la hipodiploidía de menos de 30 cromosomas y las traslocaciones t(9;22) (q34;q11) con BCR-ABL, t(1;19) (q23;p13) con E2A-PBX y t(4;11) (q21;q23) con (MLL-4F4), junto con otros reordenamientos en 11q23, se asocian a leucemia linfoblástica aguda de precursores B de alto riesgo (4,23).
En la leucemia de precursores B se reconoce que dichas anomalías genéticas, además de estar implicadas en el proceso de transformación maligna, tienen un efecto directo sobre la activación aberrante de vías mitógenas reguladas por proteínas cinasas, proto-oncogenes y factores de transcripción que inducen desequilibrios entre la tasa de proliferación y la supervivencia de las células tumorales, y como consecuencia, la inhibición del proceso de apoptosis y de resistencia a la quimioterapia (24,25).
En el presente estudio se analizó la asociación entre las traslocaciones cromosómicas t(9;22) (q34;q11) con BCR-ABL y t(12;21) (p13;q22) con TEL-AML1 y de la aneuploidia de ADN con el perfil inmunofenotípico y la tasa de proliferación de células B neoplásicas de leucemia linfoblástica aguda de precursores B. Además, como contribución importante, se describe por primera vez en nuestro país el perfil de las aberraciones fenotípicas asociadas al tumor, en comparación con el control normal de cada tipo de leucemia, y las anormalidades del ciclo celular. Es importante recordar que en Colombia estas metodologías no se practican en la rutina diagnóstica de todos los pacientes con leucemia linfoblástica aguda, por lo que este tipo de estudios resalta la necesidad de implementar estas estrategias, tal como se llevan a cabo en países desarrollados y según las recomendaciones de la OMS.
En general, los estudios en que se evalúan las diferencias fenotípicas entre células tumorales y células B normales, son escasos (11,13,14,26). Sin embargo, de forma similar a lo reportado en la literatura científica, el análisis comparativo del inmunofenotipo de nuestros casos de leucemia linfoblástica aguda de precursores B con sus controles normales, muestra una gran heterogeneidad en la expresión de los diferentes marcadores analizados, lo que sustenta la existencia de fenotipos asociados a leucemia ( Leukaemia Associated Phenotypes , LAP) (8). En la leucemia linfoblástica aguda de precursores B de fenotipo común, estos fenotipos incluyen la infraexpresión de CD34, TdT, CD10, CD38 y CD45con sobreexpresión de CD19 y CD79a; por otra parte, en las pre-B tienen infraexpresión de CD19, CD20, CD38, CD45 e IgM y sobreexpresión de CD10. En general, estos subtipos de leucemia linfoblástica aguda de precursores B expresan de forma aberrante los marcadores CD20, CD15, CD7, CD13 y CD33.
Asimismo, el análisis del inmunofenotipo en relación con la alteración genética, muestra que la presencia de t(12,21) (p13;q22) con TEL-AML1 y t(9;22) (q34;q11) con BCR-ABL en las células tumorales de niños con este tipo de leucemia, se asocia de manera significativa con fenotipos aberrantes que incluyen asincronismos en la maduración, infidelidad de linaje, y sobreexpresión e infraexpresión antigénica (9,10,27) con alteración de los patrones de tamaño (FSC) y granularidad (SSC). En este sentido, las células tumorales con t(12;21) (p13;q22) muestran sobreexpresión de CD20, CD13, y CD33, junto a infraexpresión de CD34, CD38, CD45 y TdT. De forma similar, en los casos con t(9;22) (q34;q11) hay sobreexpresión de CD19, cyCD79a, CD13 y CD33, con disminución significativa del marcador CD38.
Es importante resaltar que en este estudio se encontró que el 100 % de las leucemias pre-B fueron positivas para CD20+ (marcador asociado a asincronismo en la maduración), el 86 %, para CD34+ (marcador presente en células pre-pre-B normales), y el 28 %, para CD7+ (marcador T asociado a infidelidad de línea); estas frecuencias son superiores a la descritas en trabajos previos reportados en la literatura científica (15,27).
Los casos con hiperdiploidía de ADN se caracterizan por una expresión más elevada de CD10 y TdT, junto con un mayor tamaño de los linfoblastos (FSC), y por la tendencia a una menor expresión de CD45 y CD38. La identificación de los fenotipos asociados a leucemia por citometría de flujo en el momento del diagnóstico de la enfermedad, representa una herramienta de gran sensibilidad y especificidad para incluir la evaluación de estos fenotipos en los estudios de enfermedad mínima residual posterior a la quimioterapia (que deben aplicarse en el 100 % de los casos), ya que representa uno de los factores pronósticos más importantes en niños con leucemia linfoblástica aguda para predecir el resultado del tratamiento y el riesgo de recaída, y para las evaluaciones previas y posteriores al trasplante para los pacientes con leucemia de alto riesgo que lo requieran (28,29).
Otras variables de importancia para el pronóstico son la evaluación del contenido de ADN y el análisis de la distribución a lo largo del ciclo celular de las células tumorales (13,14) (21,30). En general, en tumores hematopoyéticos se ha establecido que la tasa de proliferación tumoral (células en fase S+G2/M) se asocia de manera significativa con el grado histopatológico del tumor, el resultado del tratamiento, la evolución y la supervivencia. El papel pronóstico de la presencia de aneuploidía de ADN en estos tumores es controversial debido a que, por ejemplo, en pacientes con mieloma múltiple se ha reportado que la hiperdiploidía de ADN detectada por citometría se asocia con mayor supervivencia (21,30) y en la leucemia linfoblástica aguda se asocia con mayor sensibilidad de las células tumorales a distintos fármacos citotóxicos, como metotrexato, mercaptopurina, tioguanina, citarabina y L-asparaginasa (31,32), y con la presencia de ganancias en los cromosomas 4, 6, 10 y 21 (16,27,33-35). Se ha reportado un pronóstico adverso en la leucemia linfoide crónica B, debido a su asociación con anormalidades genéticas de mal pronóstico (trisomía 12) y elevada tasa de proliferación tumoral (13,14), y con mayor frecuencia de linfomas B agresivos (13).
Los resultados del presente trabajo muestran una frecuencia de 21 % de casos con hiperdiploidía de índice alto y de 47,7% con hiperdiploidía de índice bajo. En relación con reportes previos (16,31,32,36), la frecuencia de casos con hiperdiploidía de índice alto es similar a la descrita en otros trabajos (22-35 %), pero la frecuencia de hiperdiploidía de índice bajo es superior. Las diferencias en la frecuencia pueden deberse al tipo de población estudiada, los subtipos incluidos de leucemia linfoblástica aguda, el procesamiento técnico de la muestra; en el caso de los estudios de citometría de flujo, también puede variar según el tipo de colorante de ADN empleado, como bromuro de etidio, DRAQ5, yoduro de propidio, o la detección con yoduro de propidio en combinación con anticuerpos monoclonales, el uso de software multiparamétricos para análisis (Paint A gate BDB, Infinicyt Cytognos) o el porcentaje de células tumorales; incluso, para calcular la frecuencia, en algunos reportes excluyen los casos con índices de ADN superiores a 1,3 (32) o excluyen los casos con índices inferiores a 1,14 (37). En esta serie no se excluye ningún caso con contenido de ADN diferente a 1,0. Los casos de hiperdiploidía de índice bajo se han asociado con menor supervivencia y menor probabilidad de lograr una remisión completa (16).
Merece la pena resaltar que la mayoría de los reportes sobre la frecuencia de hiperdiploidía de ADN en la leucemia linfoblástica aguda, se fundamentan en resultados de cariotipo convencional, con las desventajas de tener una sensibilidad que oscila entre 5 y 10 % según la cantidad de metafases obtenidas, de analizar pocas células y de requerir células en división (2,38,39). La baja sensibilidad descrita en estudios de cariotipo, contrasta con lo reportado previamente mediante citometría de flujo (37).
Además, encontramos 4/6 casos (67 %) con t(12;21), tres con hiperdiploidía de índice bajo y uno con hiperdiploidía de índice alto. Clínicamente, en la leucemia linfoblástica aguda de precursores B se ha descrito una asociación entre t(12;21) (p13;q22) con TEL-AML1 con hiperdiploidía alta (cercana a la tetraploidia) y un pronóstico favorable reflejado en remisión completa con el tratamiento y mayor supervivencia (20). Por otra parte, 2/3 (67 %) casos con t(9;22) (q34;q11) con BCR-ABL mostraron hiperdiploidía, uno de índice bajo y otro de índice alto. En los estudios en los que se ha asociado la hiperdiploidía con un buen pronóstico, no se reportan casos BCR/ABL+ (20). En la leucemia linfoblástica aguda de precursores B de adultos se han descrito aberraciones cromosómicas secundarias asociadas a BCRABL como parte de la evolución clonal de la enfermedad, en 41 a 86 % de los casos. Entre estas aberraciones cromosómicas se encuentran +der(22) t(9;22), reordenamientos en 9p, +21, +8, HIA (>50 cromosomas) y -7. En la evolución clínica de estos pacientes se describe mayor probabilidad de recaída y un resultado variable con el imatinib (40). En este sentido, se puede deducir que el impacto de la hiperdiploidía en el pronóstico de las leucemias linfoblásticas agudas puede ser variable según el tipo de traslocación cromosómica presente en las células tumorales.
En relación con la tasa de proliferación, la leucemia de precursores B muestra un mayor porcentaje de células en las fases S+G2/M del ciclo celular, en comparación con las células B normales residuales presentes en la médula ósea del mismo individuo y con respecto a las células B de médula ósea de controles sanos. En las células B normales residuales presentes en el microambiente tumoral, la tasa de proliferación es mayor que en las de médula ósea de controles sanos; esto podría estar asociado con la presencia de factores solubles o moléculas expresadas en las células tumorales o por el nicho medular, que podrían contribuir a la activación de estas células y reflejarse en un incremento de la proliferación(13,41-43).
Al comparar la tasa de proliferación celular de los casos con hiperdiploidía de índice bajo o alto, con la de los casos con contenido de ADN diploide, se encontraron valores significativamente superiores. Estos hallazgos sugieren que la elevación anormal de dicha tasa en las células B neoplásicas, podría estar asociada con el bloqueo en la diferenciación celular, con las alteraciones genéticas presentes en estas células, tal como lo observamos en los casos de hiperdiploidía, y con el efecto de la interacción tumoral con el microambiente en la médula ósea (13,14). El incremento de células en fase S del ciclo celular, podría relacionarse con una mayor sensibilidad a los fármacos antineoplásicos descrita para casos con hiperdiploidía de ADN en estudios previos (1,31,32).
En resumen, los resultados de este estudio muestran una gran heterogeneidad en los perfiles inmunofenotípicos de las células neoplásicas de niños con leucemia linfoblástica aguda de precursores B, con una frecuencia importante de perfiles aberrantes asociados a leucemia, en comparación con subpoblaciones B normales de médula ósea, y relacionados con el tipo de alteración genética en el tumor. De manera importante, se encontró que los casos con hiperdiploidía de índice alto o bajo muestran un incremento significativo en la tasa de proliferación tumoral y anormalidades inmunofenotípicas. La identificación de estas aberraciones fenotípicas y genéticas en los linfoblastos leucémicos será de gran utilidad como herramienta para la evaluación y el seguimiento de la enfermedad mínima residual posterior a la quimioterapia en nuestros pacientes.
Estos resultados requieren ser analizados en un estudio de seguimiento a cinco años, con el fin de buscar correlación con las variables clínicas y biológicas asociadas con el pronóstico y la evolución de nuestros pacientes pediátricos con leucemia linfoblástica aguda de precursores B. La gran frecuencia de hiperdiploidía de índice bajo observada en nuestros pacientes, amerita la evaluación de su significado clínico, en comparación con la hiperdiploidía de índice alto y la diploidia.
Al Centro de Estudios e Investigación en Salud (CEIS) por la financiación del trabajo. A los familiares y pacientes pediátricos con leucemia linfoblástica aguda de precursores B de la Fundación Hospital de La Misericordia.
Los autores declaran no tener conflictos de intereses.
Este estudio fue financiado por el Centro de Estudios e Investigación en Salud (CEIS), la Fundación Santa Fe de Bogotá y la Fundación Hospital de La Misericordia.
Correspondencia:
Carlos Eugenio Saavedra, Grupo de Patología, Fundación Santa Fe de Bogotá, Calle 119 N° 7-75, segundo piso, Bogotá, D.C., Colombia Teléfono: (571) 603 0303, extensiones 5177 a 5892; fax: (517) 657 5714 celamsaa54@yahoo.es
1. Pui CH, Robison LL, Look AT. Acute lymphoblastic leukaemia. Lancet. 2008;22;371:1030-43. http://dx.doi.org/10.1016/S0140-6736(08)60457-2 [ Links ]
2. Onciu M. Acute lymphoblastic leukemia. Hematol Oncol Clin North Am. 2009;23:655-74. http://dx.doi.org/10.1016/j.hoc.2009.04.009 [ Links ]
3. Faderl S, O'Brien S, Pui CH, Stock W, Wetzler M, Hoelzer D, et al . Adult acute lymphoblastic leukemia: concepts and strategies. Cancer. 2010;116:1165-76. http://dx.doi.org/10.1002/cncr.24862 [ Links ]
4. Pui CH. Recent research advances in childhood acute lymphoblastic leukemia. J Formos Med Assoc. 2010;109:777-87. http://dx.doi.org/10.1016/S0929-6646(10)60123-4 [ Links ]
5. Piñeros M, Pardo C, Otero J, Suárez A, Vizcaíno M, Álvarez VH, et al . Protocolo de vigilancia en salud pública de las leucemias agudas pediátricas. Rev Colomb Cancerol. 2007;11:219-27. [ Links ]
6. Craig FE, Foon KA. Flow cytometric immunophenotyping for hematologic neoplasms. Blood. 2008;111:3941-67. http://dx.doi.org/10.1182/blood-2007-11-120535. [ Links ]
7. Coustan-Smith E, Song G, Clark C, Key L, Liu P, Mehrpooya M, et al . New markers for minimal residual disease detection in acute lymphoblastic leukemia. Blood. 2011;117:6267-76. http://dx.doi.org/10.1182/blood-2010-12-324004. [ Links ]
8. van Dongen JJM, Lhermitte L, Böttcher S, Almeida J, van der Velden VH, Flores-Montero J, et al . EuroFlow antibody panels for standardized n-dimensional flow cytometric immunophenotyping of normal, reactive and malignant leukocytes. Leukemia. 2012;26:1908-75. http://dx.doi.org/10.1038/leu.2012.120 [ Links ]
9. Orfao A, Ortuño F, de Santiago M, López A, San Miguel J. Immunophenotyping of acute leukemias and myelodysplastic syndromes. Cytometry A. 2004 ;58:62-71. http://dx.doi.org/10.1002/cyto.a.10104 [ Links ]
10. Saavedra C, Quijano SM, Romero M, Jaramillo R, Orduz R, Echeverri C, et al . Reporte del Primer Consenso Colombiano de Citometría de Flujo para el estudio de trastornos hematológicos. Biomédica. 2010;30(Suppl.1):11-21. [ Links ]
11. van Lochem EG, van der Velden VHJ, Wind HK, Malvelde JG, Westerdaal NAC, van Dongen JJM. Immunophenotypic differentiation patterns of normal hematopoiesis in human bone marrow: Reference patterns for age-related changes and disease-induced shifts. Cytometry B Clin Cytom. 2004;60:1-13. http://dx.doi.org/10.1002/cyto.b.20008 [ Links ]
12. Roa-Higuera DC, Fiorentino S, Rodríguez V, Campos AM, Infante EA, Cardozo C, et al . Análisis inmunofenotípico de muestras normales de médula ósea: aplicaciones en el control de calidad en los laboratorios de citometría. Universitas Scientiarum. 2010;15:206-23. [ Links ]
13. Quijano S, López A, Rasillo A, Barrena S, Luz Sánchez M, Flores J, et al . Association between the proliferative rate of neoplastic B cells, their maturation stage, and underlying cytogenetic abnormalities in B-cell chronic lymphoproliferative disorders: Analysis of a series of 432 patients. Blood. 2008;111:5130-41. http://dx.doi.org/10.1182/blood-2007-10-119289 [ Links ]
14. Quijano S, López A, Rasillo A, Sayagués JM, Barrena S, Sánchez ML, et al . Impact of trisomy 12, del(13q), del(17p), and del(11q) on the immunophenotype, DNA ploidy status, and proliferative rate of leukemic B-cells in chronic lymphocytic leukemia. Cytometry B Clin Cytom. 2008;74:139-49. http://dx.doi.org/10.1002/cyto.b.20390 [ Links ]
15. Seegmiller AC, Kroft SH, Karandikar NJ, McKenna RW. Characterization of immunophenotypic aberrancies in 200 cases of B acute lymphoblastic leukemia. Am J Clin Pathol. 2009;132:940-9. http://dx.doi.org 10.1309/AJCP8G5RMTWUEMUU. [ Links ]
16. Look AT, Roberson PK, Williams DL, Rivera G, Bowman WP, Pui CH, et al . Prognostic importance of blast cell DNA content in childhood acute lymphoblastic leukemia. Blood. 1985;65:1079-86. [ Links ]
17. San Miguel JF, Gutiérrez NC, Mateo G, Orfao A. Conventional diagnostics in multiple myeloma. Eur J Cancer. 2006;42:1510-9. http://dx.doi.org/10.1016/j.ejca.2005.11.039 [ Links ]
18. van Dongen JJ, Macintyre EA, Gabert JA, Delabesse E, Rossi V, Saglio G, et al . Standardized RT-PCR analysis of fusion gene transcripts from chromosome aberrations in acute leukemia for detection of minimal residual disease. Report of the BIOMED-1 Concerted Action: Investigation of minimal residual disease in acute leukemia. Leukemia. 1999;13:1901-28. [ Links ]
19. King RL, Naghashpour M, Watt CD, Morrissette JJD, Bagg A. A comparative analysis of molecular genetic and conventional cytogenetic detection of diagnostically important translocations in more than 400 cases of acute leukemia, highlighting the frequency of false-negative conventional cytogenetics. Am J Clin Pathol. 2011;135:921-8. http://dx.doi.org/10.1309/AJCPJCW6BY0CNIHD. [ Links ]
20. Lemez P, Attarbaschi A, Béné MC, Bertrand Y, Castoldi G, Forestier E, et al . Childhood near-tetraploid acute lymphoblastic leukemia: An EGIL study on 36 cases. Eur J Haematol. 2010;85:300-8. http://dx.doi.org/10.1111/j.1600-0609.2010.01493.x [ Links ]
21. Mateo G, Castellanos M, Rasillo A, Gutiérrez NC, Montalbán MA, Martín ML, et al . Genetic abnormalities and patterns of antigenic expression in multiple myeloma. Clin Cancer Res. 2005;11:3661-7. http://dx.doi.org/10.1158/1078-0432.CCR-04-1489 [ Links ]
22. Swerdllow SH, Campo E, Harris NL. WHO classification of tumours of haematopoietic and lymphoid tissues. 4 th edition. Lyon, France: IARC Press; 2008. p.167-75. [ Links ]
23. McGregor S, McNeer J, Gurbuxani S. Beyond the 2008 World Health Organization classification: The role of the hematopathology laboratory in the diagnosis and management of acute lymphoblastic leukemia. Semin Diagn Pathol. 2012;29:2-11. http://dx.doi.org/10.1053/j.semdp.2011.07.004 [ Links ]
24. Hazlehurst LA, Bewry NN, Nair RR, Pinilla-Ibarz J. Signaling networks associated with BCR-ABL-dependent transformation. Cancer Control. 2009;16:100-7. [ Links ]
25. Pérez-Vera P, Reyes-León A, Fuentes-Pananá EM. Signaling proteins and transcription factors in normal and malignant early B cell development. Bone Marrow Res. 2011;201:502751. http://dx.doi.org/10.1155/2011/502751 [ Links ]
26. Pérez-Andrés M, Paiva B, Nieto WG, Caraux A, Schmitz A, Almeida J, et al . Human peripheral blood B-cell compartments: A crossroad in B-cell traffic. Cytometry B Clin Cytom. 2010;78(Suppl.1):S47-60. http://dx.doi.org/10.1002/cyto.b.20547 [ Links ]
27. Porwit-MacDonald A, Björklund E, Lucio P, van Lochem EG, Mazur J, Parreira A, et al. BIOMED-1 concerted action report: Flow cytometric characterization of CD7+ cell subsets in normal bone marrow as a basis for the diagnosis and follow-up of T cell acute lymphoblastic leukemia (T-ALL). Leukemia. 2000;14:816-25. [ Links ]
28. Campana D. Minimal residual disease in acute lymphoblastic leukemia. Semin Hematol. 2009;46:100-6. [ Links ]
29. Øbro NF, Ryder LP, Madsen HO, Andersen MK, Lausen B, Hasle H, et al . Identification of residual leukemic cells by flow cytometry in childhood B-cell precursor acute lymphoblastic leukemia: Verification of leukemic state by flow-sorting and molecular/cytogenetic methods. Haematologica. 2012;97:137-41. http://dx.doi.org/10.3324/haematol.2011.051383 [ Links ]
30. Paiva B, Vidriales M-B, Pérez JJ, Mateo G, Montalbán MA, Mateos MV, et al. Multiparameter flow cytometry quantification of bone marrow plasma cells at diagnosis provides more prognostic information than morphological assessment in myeloma patients. Haematologica. 2009;94:1599-602. http://dx.doi.org/10.3324/haematol.2009.009100. [ Links ]
31. Whitehead VM, Vuchich MJ, Lauer SJ, Mahoney D, Carroll AJ, Shuster JJ, et al . Accumulation of high levels of methotrexate polyglutamates in lymphoblasts from children with hyperdiploid (greater than 50 chromosomes) B-lineage acute lymphoblastic leukemia: A Pediatric Oncology Group study. Blood. 1992;80:1316-23. [ Links ]
32. Kaspers GJ, Smets LA, Pieters R, van Zantwijk CH, van Wering ER, Veerman AJ. Favorable prognosis of hyperdiploid common acute lymphoblastic leukemia may be explained by sensitivity to antimetabolites and other drugs: Results of an in vitro study. Blood. 1995;85:751-6. [ Links ]
33. Smets LA, Slater RM, Behrendt H, Van't Veer MB, Homan-Blok J. Phenotypic and karyotypic properties of hyperdiploid acute lymphoblastic leukaemia of childhood. Br J Haematol. 1985;61:113-23. [ Links ]
34. Harris MB, Shuster JJ, Carroll A, Look AT, Borowitz MJ, Crist WM, et al . Trisomy of leukemic cell chromosomes 4 and 10 identifies children with B-progenitor cell acute lymphoblastic leukemia with a very low risk of treatment failure: A Pediatric Oncology Group study. Blood. 1992;79:3316-24. [ Links ]
35. Raimondi SC, Zhou Y, Shurtleff SA, Rubnitz JE, Pui C-H, Behm FG. Near-triploidy and near-tetraploidy in childhood acute lymphoblastic leukemia: Association with B-lineage blast cells carrying the ETV6-RUNX1 fusion, T-lineage immunophenotype, and favorable outcome. Cancer Genet Cytogenet. 2006;169:50-7. http://dx.doi.org/10.1016/j.cancergencyto.2006.04.006 [ Links ]
36. Shankey TV, Rabinovitch PS, Bagwell B, Bauer KD, Duque RE, Hedley DW, et al . Guidelines for implementation of clinical DNA cytometry. International Society for Analytical Cytology. Cytometry. 1993;14:472-7. [ Links ]
37. Torres J, Londoño M, Saavedra C. Determinación del índice de DNA en leucemias linfoides agudas en niños y adultos en el Instituto Nacional de Cancerología (tesis). Bogotá, D.C: Pontificia Universidad Javeriana; 2002. [ Links ]
38. Acevedo S. Seguimiento citogenético e hibridación in situ (FISH) en la enfermedad mínima residual. Medicina (Buenos Aires). 2000;60(Supl.II):87-90. [ Links ]
39. Gallego MS. Rol de la citogenética en pediatría. Arch Argent Pediatr. 2011;109:339-46. [ Links ]
40. Wetzler M, Dodge RK, Mrózek K, Stewart CC, Carroll AJ, Tantravahi R, et al . Additional cytogenetic abnormalities in adults with Philadelphia chromosome-positive acute lymphoblastic leukaemia: A study of the Cancer and Leukaemia Group B. Br J Haematol. 2004;124:275-88. [ Links ]
41. Yokota A, Kimura S, Tanaka R, Takeuchi M, Yao H, Sakai K, et al . Osteoclasts are involved in the maintenance of dormant leukemic cells. Leuk Res. 2010;34:793-9. http://dx.doi.org/10.1016/j.leukres.2009.08.034 [ Links ]
42. Lanasa MC. Novel insights into the biology of CLL. Hematology Am Soc Hematol Educ Program. 2010;70-6. http://dx.doi.org/10.1182/asheducation-2010.1.70. [ Links ]
43. Cocco C, Airoldi I. Cytokines and microRNA in pediatric B-acute lymphoblastic leukemia. Cytokine Growth Factor Rev. 2011;22:149-56. http://dx.doi.org/10.1016/j.cytogfr.2011.05.003 [ Links ]













