Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Biomédica
versão impressa ISSN 0120-4157
Biomédica vol.35 no.1 Bogotá jan./mar. 2015
CARTAS AL EDITOR Santiago de Cali, 19 de febrero de 2015 Señores Comité Editorial Revista Biomédica Estimados señores: Agradecemos los comentarios de los doctores José Julián López, Jorge E. Machado Alba, Diego A. Medina Morales y Mauricio Montoya Cañón, a los cuales nos permitimos responder con las aclaraciones que aparecen a continuación. Con respecto a los comentarios relativos a la sección de materiales y métodos, aclaramos lo siguiente. El cálculo del tamaño de la muestra del presente estudio se realizó con base en los siguientes elementos: - Se usaron los datos de los cinco años ante riores al estudio relacionados con la mortalidad atribuible a infección hospitalaria registrada en la institución. - Se estableció el uso de antibióticos como la varia ble de exposición para determinar el muestreo. Dicha variable fue dicotómica (uso adecuado o inadecuado), y se definió con base en la administración de un tratamiento antibiótico ajustado a las guías institucionales del hospital sobre manejo de infecciones. Esas guías se elaboraron con la in formación epidemiológica relativa a los estudios microbiológicos de las infecciones hospitalarias prevalentes en la institución y hacen parte de un programa de uso regulado de antibióticos que funciona en el hospital desde el 2009 cuyos resultados están publicados (1). Escogimos esta variable dependiente porque ha demostrado ser un factor importante de la mortalidad por infecciones hospitalarias, dado que se ha incrementado entre 9 % y 20 % (2,6). Además, de todas las variables escogidas para el análisis, esta era la que aportaba un mayor tamaño de muestra, por lo que decidimos usarla para el cálculo, con el objetivo de no comprometer el poder de la muestra en el análisis del resto de variables planteadas. - El nivel de confianza establecido para el cálculo fue de 95 %. - La potencia se estableció en 80 %. - Se agregó un 10 % a la muestra para compensar pérdidas en la información. - La razón de expuestos sobre no expuestos fue de 0,25. Su cálculo se basó en el dato histórico de la observancia de las guías de manejo antibiótico empírico por parte del cuerpo médico del hospital; dicha razón ha sido, en promedio, de 80 %. - La fórmula empleada para el cálculo del tamaño de la muestra en estudios de cohorte se estableció mediante el programa EPIDAT, versión 3.1, usando la siguiente ruta: métodos/muestreo/cálculo de tamaño de muestra/estudios de cohorte. Esta se basa en el riesgo en expuestos (proporción de mortalidad esperada en pacientes con infección hospitalaria y tratamiento antibiótico inadecuado) y en el riesgo en no expuestos (proporción de mortalidad esperada en pacientes con infección hospitalaria y tratamiento antibiótico adecuado). Es importante diferenciar direccionalidad de temporalidad en los estudios de cohortes y de casos y controles. La direccionalidad se define como el análisis de la información partiendo desde la exposición hacia el evento o viceversa. Desde esta perspectiva, los estudios de cohortes, que van desde la exposición hasta el evento definido, ofrecen medidas de incidencia (eventos nuevos en el tiempo) y hacen posible el cálculo de probabilidades de riesgo (riesgo relativo, RR) con fines epidemiológicos, en tanto que un estudio de casos y controles, en el que la direccionalidad se establece a partir del evento, permite calcular oportunidades ( odds ratio, OR), o razones de productos cruzados, debido a que no es posible establecer medidas de incidencia. La temporalidad, por su parte, puede ser retrospectiva o prospectiva, y se define como la captura de los datos una vez el evento ha ocurrido (retrospectiva), o desde que se inicia la exposición hasta que el evento ocurre (prospectiva). La temporalidad no define el tipo de estudio, pero la direccionalidad, sí. Es por esta razón que en la literatura científica se habla de cohortes retrospectivas o históricas, en las cuales, aunque el evento ya ha ocurrido, se reconstruye la información de los factores de exposición de los pacientes antes del evento. En el estudio en mención los pacientes se reclutaron cuando se les diagnosticó la infección hospitalaria con base en los criterios estandarizados internacionalmente (CDC), y hasta el momento de su muerte (evento definido) o egreso de la institución. En este caso, la direccionalidad va desde la exposición hasta el evento, como está establecido para los estudios de cohortes. Los pacientes se captaron mediante el sistema de vigilancia activa prospectiva a cargo del comité institucional de infecciones. Este sistema de vigilancia, integrado por personal profesional y técnico del comité de infecciones (enfermeras y auxiliares de enfermería), recopila diariamente la información de los pacientes con infecciones hospitalarias y les hace seguimiento durante toda su hospitalización hasta el egreso o la muerte. Los factores de riesgo se identificaban en el momento en que los pacientes los presentaban durante su seguimiento en la cohorte, y el evento (muerte) se reportaba cuando ocurría. Este estudio no es un estudio de casos y controles porque la información de los pacientes participantes se analizó a partir de la inclusión de los pacientes en la cohorte y hasta su muerte o su egreso del hospital, es decir, siguiendo una direccionalidad desde la exposición hasta el evento. La temporalidad también fue prospectiva. Gracias a esto se pudieron establecer los riesgos relativos (incidencias en expuestos e incidencias en no expuestos) para el análisis bivariado, el análisis de supervivencia en función del tiempo y el análisis multivariado mediante un modelo de riesgos proporcionales de Cox, el cual establece el peligro inmediato de que ocurra determinado evento (en el caso de nuestro estudio, la muerte), si el paciente está expuesto a determinado factor (en este caso, las variables incluidas en el estudio). El cuadro 1 resume la descripción de las variables sociodemográficas, clínicas, microbiológicas y de tratamiento, no es un cuadro comparativo de varia bles por exposición. Con respecto a la variable ´exposición´, con la que se calculó directamente el tamaño de la muestra (tratamiento antibiótico adecuado o inadecuado), no se encontraron diferencias estadísticamente significativas entre los grupos (cuadro 1), razón por la cual son comparables. Esta información hace parte de los análisis exploratorios de los datos y se determinó realizando pruebas estadísticas de comparación de los grupos categorizados según uso adecuado o inadecuado de antibióticos, pero no se incluyó en el manuscrito publicado. Para brindar al lector una mejor descripción de la población, consideramos de mayor importancia suministrar la descripción de la población de estudio sin categorizarla según uso adecuado o inadecuado de antibióticos.
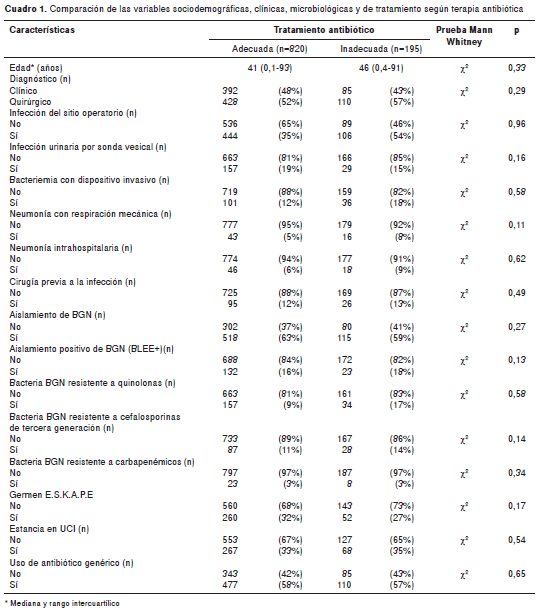
La definición de precisión de una variable hace alusión a la forma de captación y su medida (categórica o numérica), no a su comportamiento como dependiente o independiente en un estudio.
La inclusión de los pacientes, la forma de reco pilación de la información, su seguimiento y su análisis permiten clasificar el estudio como un estudio de cohortes. Los estudios de cohortes se definen como observacionales porque los investigadores no hacen ninguna intervención y como analíticos porque permiten establecer medidas de asociación en el tiempo. En el caso de nuestro estudio, se establecieron medidas de riesgo en los análisis bivariado y multivariado (RR y HR, respectivamente). Es importante hacer énfasis en la direccionalidad de este estudio (que parte de la exposición hacia el evento).
Con respecto a los aspectos metodológicos que pudieron influir en los resultados, aclaramos lo siguiente.
Las variables mencionadas en la sección de materiales y métodos que resultaron estadísticamente significativas en el análisis multivariado fueron el eje central de la discusión (neumonía hospitalaria, uso adecuado de antibióticos, hospitalización en unidad de cuidados intensivos y uso de antibióticos genéricos). Las guías de manejo empírico de la infección, basadas en la epidemiología local y su impacto en la mortalidad, se enuncian en los párrafos 3 y 4 de la discusión, explicando cómo su articulación con la estrategia de uso adecuado de antibióticos reduce la incidencia de infección por microorganismos multirresistentes (MDR) y los costos hospitalarios. Citamos textualmente del artículo: "[...] la caracterización de la infección con base en la ecología bacteriana, los patrones de resistencia y las infecciones más prevalentes (estos son los elementos provenientes de las guías institucionales), permite crear estrategias específicas de control epidemiológico que garanticen una reducción del uso inapropiado de antibióticos y la resistencia bacteriana [...]". Además, se cita la referencia bibliográfica de los datos que tenemos disponibles, publicada por el programa de uso regulado de antibióticos de la institución en la cual se realizó el estudio, el cual funciona desde el 2009, y cuya estrategia central es orientar el tratamiento antibiótico mediante guías institucionales basadas en la epidemiología local (Pallares CJ, Martínez E. Implementación de un programa de uso regulado de antibióticos en dos unidades de cuidado intensivo médico-quirúrgico en un hospital universitario de tercer nivel en Colombia. Infectio. 2012;16:192-8).
Con respecto a la definición de genérico es im portante mencionar que una vez caducan los derechos de propiedad intelectual es posible la competencia en el mercado farmacéutico, y aunque en Estados Unidos y Europa las normas de propiedad intelectual en el ámbito farmacéutico se aplican desde hace más de 50 años (7), su aplicación en América Latina comenzó apenas en 1995, después de la creación de la Organización Mundial del Comercio ( OMC ) y la adopción del Acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (ADPIC) (8).
Dado que en América Latina los mercados de medicamentos se consolidaron antes de los acuerdos y la aprobación de las normas de propiedad intelectual vigentes, la adopción de una definición clásica o estandarizada de medicamento genérico es difícil, lo cual ha sido reconocido inclusive en trabajos internacionales como el que se llevó a cabo en 14 países de América Latina y el Caribe (9), en el cual se recurrió a definiciones propias debido a las muchas y diferentes mencionadas en los documentos regulatorios de varios países (Brasil, México, Panamá, Costa Rica, Colombia, Perú, Bolivia, Ecuador), además de los publicados por la Organización Mundial de la Salud.
Entre las definiciones incluidas en dichos documentos podemos mencionar las siguientes: medicamento similar, equivalente, intercambiable o semejante a un producto de referencia o innovador; producto farmacéutico ´multiorigen´ (sic.), o medicamento con denominación común internacional (DCI), no identificado con un nombre de marca, o aquel cuya patente de invención haya expirado. Así, las definiciones de medicamento genérico varían según la forma de socialización, la exigencia de los países de hacer pruebas de equivalencia terapéutica y el momento de comercialización. Dada la heterogeneidad de definiciones de antibiótico genérico, consideramos que la definición planteada no va en contra de las alternativas empleadas a nivel nacional e internacional. Por último, es importante mencionar que algunos países de Latinoamérica (Barbados, Paraguay, Guatemala, Nicaragua y Venezuela) no cuentan con información disponible sobre definiciones estandarizadas (9).
Con relación a la afirmación sobre el objetivo del estudio, este no era evaluar la asociación de mortalidad entre antibióticos innovadores y genéricos, para lo cual la metodología sería diferente, sino determinar los factores asociados a la mortalidad en pacientes con diagnóstico de infección hospitalaria, siendo el uso de antibióticos genéricos uno de ellos. No se pretendía evaluar todos los antibióticos genéricos, sino el impacto de su uso en nuestra institución, teniendo en cuenta que durante el período del estudio solo se dispuso de una referencia comercial por principio activo.
En cuanto a las observaciones de los autores de las dos cartas al editor, relativas a los artículos consultados sobre medicamentos genéricos, contrariamente a lo expresado en estas, en las referencias citamos al menos siete trabajos (referencias 33 a 39 en la publicación) en los que los autores evaluaron antibióticos tanto innovadores como genéricos con diferentes metodologías y parámetros.
Los aspectos relacionados con el término genérico se discutieron en el inicio del presente documento.
En cuanto al programa "Demuestra la calidad" del Invima, se trata de un programa nacional para la verificación de la calidad de una muestra de medicamentos de gran consumo y relevancia clínica, los cuales se someten a análisis de control de calidad y a revisión de rótulos y condiciones de almacenamiento. Este programa no ejerce vigilancia en todos los antibióticos disponibles en el país y, desde el punto de vista metodológico, no constituye un programa de seguimiento clínico de la eficacia terapéutica de los antibióticos mediante vigilancia activa prospectiva.
El Decreto 677 de 1995 define como eficacia la capacidad de un medicamento, determinada por métodos científicos, para producir los efectos propuestos. El método científico que mejor deter mina la eficacia clínica de un medicamento es un ensayo clínico controlado, ya que garantiza la similitud entre los grupos, controlando por medio de intervenciones todas las variables que pueden influir en los resultados, pero en el artículo 22 del decreto en mención (denominado "De la documentación para la evaluación farmacéutica"), no se solicitan este tipo de estudios para la obtención del registro sanitario del Invima. En la literatura científica no se registra ningún antibiótico genérico de los que se usan en nuestro país que haya sido probado mediante ensayos clínicos controlados para esta blecer su eficacia clínica y su seguridad y, sin embargo, se ha asumido que son las mismas del producto innovador.
En cuanto a la guía de uso racional de medicamen tos, es importante aclarar que esta se elaboró con base en el perfil microbiológico de la resistencia bacteriana en la institución, el cual se obtuvo mediante el análisis de cada microorganismo, así como de la sensibilidad y el tipo de muestra asociado a la infección, datos estos provenientes de los archivos digitales del Laboratorio de Bacteriología del hospital (MicroScan, WHONET ). Esta guía se fundamenta en el manejo empírico de las enfermedades infecciosas según la especialidad, y ofrece un manejo inicial con alternativas en caso de falla terapéutica, pero no es específica para el manejo de pacientes que permanecen en la unidad de cuidados intensivos. Este punto se aclaró ex presamente en el artículo "Implementación de un programa de uso regulado de antibióticos en dos unidades de cuidado intensivo médico-quirúrgico en un hospital universitario de tercer nivel en Colombia", el cual evalúa el impacto del programa de uso racional de antibióticos en las unidades de cuidados intensivos de la institución (1).
Con respecto a los análisis de supervivencia, estos se hicieron teniendo en cuenta el tiempo de seguimiento desde el ingreso de los pacientes del estudio hasta su egreso hospitalario o su muerte. El promedio de estancia hospitalaria fue de 103 días (DE ± 86 días), con un rango de 3 a 406 días, razón por la cual los análisis de supervivencia cubren este lapso.
La institución en la que se llevó a cabo el estudio es un hospital público de tercer nivel de atención, que es centro de referencia para el suroccidente colombiano y donde son frecuentes las hospitalizaciones prolongadas.
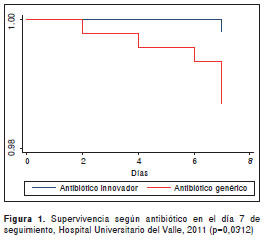
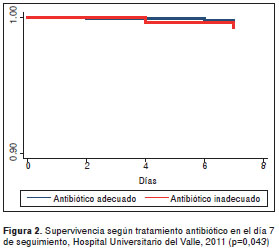
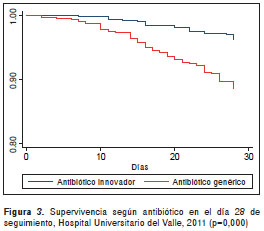
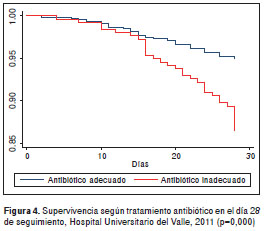
Es importante aclarar que los análisis de super vivencia son una representación de la probabilidad de supervivencia acumulada en el tiempo, que resumen los datos de forma visual, pero no establecen medidas de asociación con respecto al evento (muerte, en este caso). Para las variables más relevantes del estudio (uso adecuado o inadecuado del antibiótico y tratamiento antibiótico con productos genéricos), las diferencias en la mortalidad fueron estadísticamente significativas no solo durante el seguimiento, sino también en el día 7 y en el 28, respectivamente (figura 1 figura 2 figura 3 figura 4).
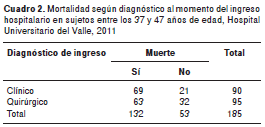
En cuanto a la mortalidad asociada con trauma por grupos de edad (específicamente en el de 37 a 47 años), es importante aclarar que en el presente estudio los pacientes se clasificaron según el diagnóstico al ingresar en el hospital (clínico o quirúrgico) y, aunque más del 60 % de los pacientes con requerimiento de cirugía presentaban trauma (explicable porque nuestra institución es un centro de referencia nacional para trauma), en el grupo de pacientes entre 37 y 47 años de edad no se presentaron diferencias estadísticamente significativas con respecto a la mortalidad según enfermedad (p=0,120/prueba de ji al cuadrado) (cuadro 2). La supervivencia según el diagnóstico de ingreso y el grupo de edad, no mostró diferencias significativas en el día 7 ni en el día 28 de seguimiento, y la diferencia fue significativa solo para los sujetos con diagnóstico de ingreso hospitalario menor de un año y enfermedad quirúrgica (figura 5 y figura 6).
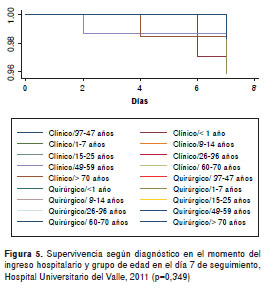
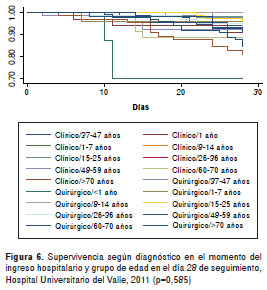
En relación con los análisis de supervivencia y el diagnóstico de neumonía hospitalaria, los hallazgos específicos de esta condición se hicieron en sujetos hospitalizados en salas diferentes a la unidad de cuidados intensivos. Los estudios que se mencionan en una de las cartas al editor (referencias 3 y 4, carta de los doctores Jorge E. Machado-Alba, Diego A. Medina-Morales y Mauricio Montoya-Cañón), no constituyen una evidencia comparable con los re sultados de nuestro estudio. Dichos estudios tenían como objetivo describir los factores pronóstico de mortalidad en pacientes ancianos (edad mayor o igual a 70 años), hospitalizados en unidades de cuidados intensivos (Santana-Cabrera L, et al. ), y el papel del choque y la acidosis metabólica como factores predictores de mortalidad en los primeros cuatro días de hospitalización en la unidad de cuidados intensivos (Aristizábal, RE, et al. ) hace referencia a fenómenos asociados con el uso de respiración mecánica en la unidad de cuidados intensivos. Solo 16 % de los sujetos de nuestro estudio tenían más de 70 años y 6 % (n=59) fueron diagnosticados con neumonía y asistidos con respiración mecánica.
En lo concerniente a las comparaciones entre antibióticos genéricos e innovadores, es importante aclarar que existen diferencias en los registros sanitarios de antibióticos genéricos publicados por el Invima http://web.sivicos.gov.co:8080/consultas/consultas/consreg_encabcum.jsp) en cuanto a su vida útil, la vía de administración y las indicaciones. Los dos últimos aspectos son fundamentales en el manejo terapéutico de pacientes con sospecha o diagnóstico de infección. Algunos ejemplos incluyen la piperacilina y el tazobactam para la infección abdominal en niños, la cual aparece como una de las indicaciones del antibiótico innovador, pero no en la mayoría de los genéricos; el cefepime para infecciones del sistema nervioso central en niños y recién nacidos, las cuales son parte de las indicaciones del antibiótico innovador, que en muchos genéricos, en cambio , aparecen como contraindicaciones por no atravesar la barrera hematoencefálica, y, por último, la claritromicina, que en su versión como medicamento inno vador enumera contraindicaciones tales como las alteraciones que se presentan cuando hay uso simultáneo de hipoglucemiantes y anticoagulantes orales, warfarina e inhibidores de la HMG-COA reductasa, las cuales no aparecen en el registro de la mayoría de los genéricos.
Debe tenerse en cuenta que las diferencias con cernientes a equivalencia química, potencia y biodisponibilidad, y a fallas terapéuticas de los antibióticos genéricos, así como las discrepancias en las indicaciones clínicas de los registros del Invima entre antibióticos innovadores y antibióticos genéricos, hacen que su uso requiera un segui miento especial y pueda considerárselo arriesgado.
Esperamos haber dado respuesta a las inquietudes de los remitentes y quedamos atentos ante cualquier inquietud al respecto.
Cordialmente,
Christian José Pallares, MD, MSc
Especialista asesor en Epidemiología Hospitalaria
Hospital Universitario del Valle
Ernesto Martínez, MD
Profesor titular
Universidad del Valle
Referencias
1. Pallares CJ, Martínez E. Implementación de un programa de uso regulado de antibióticos en dos unidades de cuidado intensivo médico-quirúrgico en un hospital universitario de tercer nivel en Colombia. Infectio. 2012;16:192-8. [ Links ]
2. Álvarez-Lerma F. Modification of empiric antibiotic treatment in patients with pneumonia acquired in the intensive care unit. ICU-Acquired Pneumonia Study Group. Intensive Care Med. 1996;22:387-94. [ Links ]
3. Luna CM, Vujacich P, Niederman MS. Impact of BAL data on the therapy and outcome of ventilator-associated pneumonia. Chest. 1997;111:676-85. [ Links ]
4. Rello J, Gallego M, Mariscal D, Sonora R, Vallès J. The value of routine microbial investigation in ventilator-associated pneumonia. AmJ Respir Crit Care Med. 1997; 156:196-200. [ Links ]
5. Kollef MH, Ward S. The influence of mini-BAL cultures on patient outcomes: Implications for the antibiotic man- agement of ventilator-associated pneumonia. Chest. 1998;113:412-420. [ Links ]
6. Alba-Pérez M, Álvarez-Peña MA, Iparraguirre-Góngora O, Arena-Rodríguez M. Influencia del tratamiento antibiótico empírico inadecuado en la sepsis grave. Revista Cubana de Medicina Intensiva y Emergencias 2010;9:1602-16. [ Links ]
7. Correa CM. Patentes, industria farmacéutica y biotecnología. Revista del Derecho Industrial. 1990;12:335-43. [ Links ]
8. Organización Mundial del Comercio. Acuerdo sobre los aspectos de los derechos de propiedad intelectual relacionados con el comercio. Ginebra: OMC; 1995. Fecha de consulta: 14 de noviembre de 2014. Disponible en: http://www.oepm.es/es/propiedad_industrial/Normativa/normas_comunes/Internacionales/Anexo_1. [ Links ]
9. Vacca-González CP, Fiztgerald JF, Bermúdez JAZ. Definición de medicamento genérico ¿Un fin o un medio? Análisis de la regulación en 14 países de las Américas. Rev Panam Salud Pública. 2006;20:314-23 . [ Links ]













