Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Biomédica
versão impressa ISSN 0120-4157
Biomédica vol.36 supl.1 Bogotá dez. 2016
https://doi.org/10.7705/biomedica.v36i2.2875
ARTÍCULO ORIGINAL
doi: http://dx.doi.org/10.7705/biomedica.v36i2.2875
1 Grupo de Microbiología Ambiental, Escuela de Microbiología, Universidad de Antioquia, Medellín, Colombia
2 Programa de Estudio y Control de Enfermedades Tropicales, Universidad de Antioquia, Medellín, Colombia
Contribución de los autores:
Todas las autoras participaron en el diseño del estudio, las actividades llevadas a cabo en la planta de Frigocolanta (Santa Rosa de Osos, Antioquia), la utilización de la técnica modificada de Dennis, el diagnóstico de los huevos, el análisis e interpretación de los datos, y la escritura del manuscrito.
Recibido: 23/06/15; aceptado: 24/10/15
Introducción. La fasciolosis bovina genera cuantiosas pérdidas económicas, que en Colombia se estiman en COP$12.483 millones anuales, y tiene una prevalencia de 25 % en vacunos lecheros. La enfermedad se diagnostica mediante pruebas parasitológicas. En el país se utiliza la técnica de Dennis modificada en el 2002, pero su sensibilidad, especificidad y validez se desconocen.
Objetivo. Evaluar la validez y el desempeño de la técnica modificada de Dennis para el diagnóstico de fasciolosis bovina, usando como prueba de referencia la observación de parásitos en el hígado.
Materiales y métodos. Se hizo un estudio de evaluación diagnóstica. Se seleccionaron por conveniencia bóvidos de descarte sacrificados entre marzo y junio de 2013 en Frigocolanta; de cada ejemplar se recolectaron 25 g de heces y se examinaron los conductos biliares y el hígado en busca de Fasciola hepatica . Se estimaron los valores de sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo e índice de validez, con intervalos de confianza de 95 %. Como prueba de referencia se usó la evaluación post mortem .
Resultados. Se analizaron 180 bóvidos. La sensibilidad y la especificidad de la técnica modificada de Dennis fueron de 73,2 % (IC 95% 58,4-87,9) y 84,2 % (IC 95% 77,7-90,6), respectivamente. El valor predictivo positivo fue de 57,7 % (IC 95 % 43,3-72,1) y el negativo fue de 91,4 % (IC 95% 86,2-96,6). La prevalencia de fasciolosis bovina fue de 22,8 % (IC 95% 16,4-29,2).
Conclusión. La validez y el desempeño de la técnica modificada de Dennis fueron superiores a los de la técnica tradicional, por lo que constituye una buena heramienta de tamización para el diagnóstico de la fasciolosis en estudios poblacionales y de prevalencia, así como en jornadas de salud animal.
Palabras clave: Fasciola hepatica , fascioliosis/diagnóstico, estudios de validación, enfermedades de los bóvidos, Colombia.
doi: http://dx.doi.org/10.7705/biomedica.v36i2.2875
Evaluation of modified Dennis parasitological technique for diagnosis of bovine fascioliasis
Introduction: Bovine fascioliasis causes important economic losses, estimated at COP$ 12,483 billion per year; its prevalence is 25% in dairy cattle. Parasitological techniques are required for it diagnosis. The Dennis technique, modified in 2002, is the one used in Colombia, but its sensitivity, specificity and validity are not known.
Objective: To evaluate the validity and performance of the modified Dennis technique for diagnosis of bovine fascioliasis using as reference test the observation of parasites in the liver.
Materials and methods: We conducted a diagnostic evaluation study. We selected a convenience sample of discarded bovines sacrificed between March and June, 2013, in Frigocolanta for the study. We collected 25 g of feces from each animal and their liver and bile ducts were examined for Fasciola hepatica . The sensitivity, specificity, predictive positive value, predictive negative value, and validity index were calculated with 95% confidence intervals. The post-mortem evaluation was used as the gold standard.
Results: We analyzed 180 bovines. The sensitivity and specificity of the modified Dennis technique were 73.2% (95% CI=58.4% - 87.9%) and 84.2% (95% CI= 77.7% - 90.6%), respectively. The positive predictive value was 57.7% (95% CI= 43.3% - 72.1%) and the negative one 91.4% (95% CI= 86.2% - 96.6%). The prevalence of bovine fascioliasis was 22.8% (95% CI= 16.4% - 29.2%).
Conclusion: The validity and the performance of the modified Dennis technique were higher than those of the traditional one, which makes it a good screening test for diagnosing fascioliasis for population and prevalence studies and during animal health campaigns.
Key words: Fasciola hepatica , fascioliasis/diagnosis, validity studies, cattle diseases, Colombia.
doi: http://dx.doi.org/10.7705/biomedica.v36i2.2875
El agente causal de la fasciolosis, Fasciola hepatica (Trematoda: Digenea), tiene una amplia distribución mundial en regiones tropicales y subtropicales, y afecta la salud de animales bovinos, ovinos y caprinos, y de seres humanos, sus huéspedes definitivos (1,2).
En Colombia, los bóvidos dedicados a la producción lechera son los más afectados por la fasciolosis, con una prevalencia de 25 % (3). En ese renglón de la economía nacional, las pérdidas ocasionadas por este digeneo se estiman en COP$ 12.483 millones (4), y se deben a la disminución en la producción de leche y en la tasa de fertilidad de las vacas (5-8). Además, en las plantas de sacrificio el hallazgo del parásito en el hígado de los bóvidos implica el decomiso de la víscera de acuerdo con la norma del Artículo 88 del Decreto 632 de 1920; el diagnóstico post mortem es obligatorio a partir de 2007 (3,9).
Las cifras demuestran la gran magnitud del pro-blema generado por la fasciolosis en el renglón ganadero colombiano. Sin embargo, las acciones para el manejo de esta parasitosis no se han desarrollado, posiblemente debido a la dificultad para hacer el diagnóstico clínico, ya que los signos y síntomas de la enfermedad son inespecíficos (10), por lo que es necesario hacer una prueba diagnóstica de laboratorio.
La prueba de referencia para el diagnóstico de fasciolosis bovina es la observación directa de los parásitos adultos en el hígado, los conductos biliares y la vesícula biliar (1,11). Sin embargo, las pruebas más confiables son, por un lado, las inmunológicas, como la ELISA directa, que detecta coproantígenos, y la ELISA indirecta, que detecta anticuerpos anti- F. hepatica en suero y leche (12,13), y por el otro, las moleculares, las cuales detectan el genoma del parásito (RAPD-PCR). Todas estas pruebas son costosas y poco comercializadas en nuestro país (14).
Los métodos coproparasitológicos utilizados en el diagnóstico de F. hepatica son más diversos pero menos confiables, y consisten en la concentración de huevos del digeneo a partir de las heces del huésped definitivo (15). Entre dichos métodos se cuentan las técnicas de flotación (McMaster clásica, McMaster INTA), de sedimentación (Dennis, técnica de sedimentación espontánea en tubo TSET, Kato Katz, técnica de sedimentación rápida-TSR) y de filtración (técnica de cuatro tamices, técnica de Boray y Pearson) (16-22), las cuales son las más empleadas por su bajo costo y accesibilidad.
En el 2002, la Unidad de Malacología Médica y Tremátodos del Programa de Estudio y Control de Enfermedades Tropicales de la Universidad de Antioquia, modificó la técnica de Dennis para utilizarla en zonas rurales en donde se desarrollan estudios sobre la fasciolosis bovina. Entre las modi-ficaciones implementadas, se eliminó el uso de colorantes, de detergente y de la centrífuga, y se aumentó a 25 g el peso de la muestra analizada. En la presente investigación se propuso evaluar el desempeño y la validez de la técnica modificada de Dennis para el diagnóstico de la fasciolosis bovina.
Materiales y métodos
Se llevó a cabo un estudio transversal de evaluación diagnóstica. Se incluyeron bóvidos de descarte sacrificados entre marzo y junio de 2013 en la planta de Frigocolanta, ubicada en Santa Rosa de Osos, Antioquia, Colombia. Los bóvidos se seleccionaron a conveniencia. Se excluyeron aquellos de los cuales no se pudieron obtener los 25 g de materia fecal necesarios para aplicar la técnica modificada de Dennis.
El veterinario de la planta de sacrificio recolectó las heces del recto de los bóvidos usando guantes de látex y aceite mineral; la muestra fecal se depositó en un recipiente plástico con tapa de rosca, se marcó con el código asignado al bóvido y se mantuvo en una nevera con aislante térmico hasta el traslado al laboratorio de la Unidad de Malacología Médica y Tremátodos. Un inspector de la planta de sacrificio examinó los conductos biliares y el hígado en busca de adultos de F. hepatica .
Las muestras de materia fecal se procesaron en el laboratorio para el diagnóstico parasitológico de F. hepatica mediante la técnica modificada de Dennis. Se diluyeron 25 g de heces en 200 ml de agua corriente, luego se filtraron a través de un embudo recubierto de una gasa doblada en cuatro en un vaso de precipitados plástico de 500 ml al que se añadieron 300 ml de agua; la mezcla se dejó en reposo durante 20 minutos, luego se descartó el sobrenadante y se reemplazó por agua limpia. Esta mezcla se dejó en reposo por 15 minutos, al cabo de los cuales se descartó nuevamente el sobrenadante remplazándolo por agua limpia y se la dejó en reposo durante otros 10 minutos; este paso se repitió hasta que se observó que el sobrenadante se aclaraba. Posteriormente, el sedimento obtenido se depositó en un recipiente plástico con tapa de rosca marcado con el código de la muestra y se agregaron 0,5 ml de formalina al 5 %.
La mezcla de 0,5 ml del sedimento con 2 ml de agua del grifo en una caja de Petri, se observó bajo el estereomicroscopio con un aumento de 3,5 en busca de huevos amarillos, ovalados y operculados correspondientes a F. hepatica . Este procedimiento estuvo a cargo de dos investigadores para cumplir con las condiciones de doble ciego y se repitió hasta agotar el sedimento (4,23,24). Se observaron huevos grises brillantes, ovalados y operculados correspondientes a los de los paramfistómidos (25-27). Se incluyó el diagnóstico de paramfistomosis bovina debido a que en varios estudios en Antioquia se ha registrado la infección simultánea con F. hepatica y paramfistómidos (5,25,28,29).
La detección de, al menos, un huevo en el sedimento se consideró como un resultado positivo y la ausencia de huevos se registró como resultado negativo. Las personas que hicieron el diagnóstico parasitológico desconocían el diagnóstico post mortem obtenido en la planta de sacrificio para garantizar el cegamiento del estudio.
Para evaluar la validez y el desempeño de la técnica modificada de Dennis, se calcularon los siguientes indicadores estadísticos con un intervalo de confianza de 95 %: sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo e índice de validez. Como prueba de referencia se usó la evaluación post mortem . La prevalencia de fasciolosis se determinó con base en el resultado de la evaluación post mortem de los hígados. Los resultados obtenidos en las pruebas diagnósticas se registraron en Microsoft Excel 2010 y los análisis estadísticos se hicieron con el programa Epidat 3.1.
Aspectos éticos
Esta investigación contó con el aval del Comité de Ética para la Experimentación con Animales de la Universidad de Antioquia, como consta en el acta N° 72.
Resultados
Se obtuvieron heces de 194 bóvidos que cumplían con los criterios de inclusión, pero se excluyeron 14 por no tener el peso necesario, es decir, la muestra analizada fue de 180 bovinos.
En 52 de las 180 muestras de materia fecal analizadas, se observaron huevos de F. hepatica , lo que corresponde a una frecuencia de 28,9 %. Sin embargo, solo en 41 de los 180 hígados se hallaron adultos de digeneo, lo que corresponde a una prevalencia de fasciolosis bovina de 22,8 % (IC 95% 16,4-29,2).
En esta evaluación se clasificó correctamente a 81,7 % de los bóvidos (índice de validez=81,7 %; IC 95% 75,7- 87,6). Sin embargo, con la técnica modificada de Dennis se clasificaron como positi-vos 22 bóvidos, en los cuales no se encontraron adultos de F. hepatica en el hígado (falsos positivos=15,8 %), y como negativos, a 11 bóvidos en los que sí se observaron parásitos durante la evaluación post mortem (falsos negativos=26,8 %) (cuadro 1).
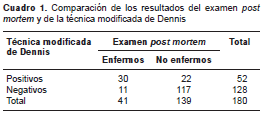
La técnica modificada de Dennis tuvo una sensibili-dad de 73,2 % (IC 95% 58,4-87,9) y una especificidad de 84,2 % (IC 95% 77,7-90,6). El valor predictivo positivo fue de 57,7 % (IC 95% 43,3-72,1) y el valor predictivo negativo de 91,4 % (IC 95% 86,2- 96,6).
En 37 de las 180 muestras analizadas se observaron huevos de paramfistómidos, lo que corresponde a una frecuencia de paramfistomosis bovina de 20,6 %, y una frecuencia de infección concomitante con F. hepatica de 13,3 % (24/180) (cuadro 1).
Discusión
La prevalencia de fasciolosis bovina determinada en este estudio fue alta (22,8 %) y similar a la prevalencia media registrada en Antioquia (21,6 %) (8), lo que evidencia la falta de medidas de prevención y de manejo ecoepidemiológico de la enfermedad en el departamento.
La frecuencia obtenida con la técnica modificada de Dennis (28,9 %) está dentro del intervalo de confianza de la prevalencia observada post mortem , lo que sugiere que resulta adecuada para estimar la prevalencia de la fasciolosis bovina; esto ratifica los hallazgos de estudios previos en los que se hizo el diagnóstico mediante dicha prueba (5).
Los falsos positivos observados con la técnica modificada (15,8 %) pudieron deberse a una inspección deficiente de los hígados debido a la premura con que se hace este procedimiento en la planta de sacrificio, en tanto que los falsos negativos (26,8 %) obedecerían a la poca cantidad de huevos en la muestra de materia fecal o a la inmadurez sexual de los parásitos hallados en el hígado de los bóvidos.
En este estudio se comprobó que la técnica modificada de Dennis tiene una alta probabilidad de detectar los bóvidos que no tienen fasciolosis (valor predictivo negativo=91,4 %; especificidad =84,2 %), por lo tanto, recomendamos su uso como prueba de tamización en los estudios de prevalencia, los estudios poblacionales y las jornadas de salud animal.
Se evidenció que la técnica modificada tiene mayor exactitud diagnóstica que la técnica tradicional descrita en el 2009 por Álvarez, et al. (11), según lo demuestran el valor del área bajo la curva ROC (técnica modificada de Dennis=0,79; tradicional=0,64), y el índice de validez de cada técnica (técnica modificada de Dennis=81,7 %; tradicional=59,7).
Al comparar la sensibilidad de 73,2% de la técnica modificada en este estudio con la de otras técnicas parasitológicas, como la de Kato-Katz, la de sedimentación espontánea en tubo y la de sedimentación rápida, cuya sensibilidad es de 45 %, 10 % y 75 %, respectivamente (30), se observó que dicha técnica es una de las mejores pruebas parasitológicas disponibles en Colombia para el diagnóstico de la fasciolosis. Ello se explicaría por el empleo de una mayor cantidad de muestra, lo cual aumenta la probabilidad de observar al menos un huevo de F. hepatica.
La técnica modificada de diagnóstico copro-parasitológico de Dennis es sencilla, económica y segura. Los materiales necesarios para su implementación son asequibles y de bajo costo; durante el procesamiento de la muestra no se requieren equipos de laboratorio, lo que facilita su empleo en campo, ni el uso de químicos que deterioren el huevo, el ambiente o la salud de las personas que hacen la prueba, por lo que puede usarse en zonas rurales con poca infraestructura y ayudar a reducir las pérdidas económicas causadas por la fasciolosis bovina, pues facilita el diagnóstico oportuno y el tratamiento adecuado de la enfermedad.
En estudios futuros podría validarse esta técnica para el diagnóstico de la fasciolosis bovina, y evaluar su desempeño y su validez tomando muestras seriadas de materia fecal, pues cabe la posibilidad de que bajo estas condiciones aumenten la sensibilidad y la especificidad del método, de manera que pueda emplearse como prueba confirmatoria.
Asimismo, se propone evaluar su desempeño como prueba diagnóstica de paramfistomosis bovina e, incluso, para su diagnóstico diferencial frente a F. hepatica.
En conclusión, los resultados del estudio permiten recomendar el uso de la técnica modificada de Dennis como instrumento de tamización para el diagnóstico de la fasciolosis bovina en Colombia.
A Mónica Uruburu, por sus aportes técnicos en campo y en el laboratorio, y a Iván Darío Vélez, director del PECET, por su apoyo a los estudios en trematodosis; a Frigocolanta, por colaborarnos en las diferentes actividades adelantadas en sus instalaciones.
Las autoras de este trabajo manifiestan que no existe conflicto de intereses.
El trabajo se hizo con recursos de la Unidad de Malacología Médica y Trematodos del Programa de Estudio y Control de Enfermedades Tropicales (PECET), y del Grupo de Microbiología Ambiental de la Escuela de Microbiología de la Universidad de Antioquia.
Correspondencia:
Luz Elena Velásquez, Sede de Investigación Universitaria, Universidad de Antioquia, Calle 62 N° 52-59, torre 2, laboratorio 730, Medellín, Colombia Teléfono: (574) 219 6514; fax: (574) 219 6511 luzelena333@yahoo.com
1. Andrews SJ, Graczyk TK, Fried B, Fairweather I, Threadgold LT, Torgerson P, et al. Fasciolosis. En: Dalton JP, editor. Fasciolosis. Wallingford: United Kingdom: CAB International; 1998. p. 113-49. [ Links ]
2. Mas-Coma MS, Esteban JG, Bargues MD. Epidemiology of human fascioliasis: A review and proposed new classification. Bull World Health Organ. 1999;77:340-46. [ Links ]
3. Estrada VE, Gómez M, Velásquez LE. La higiene del ganado y la fasciolosis bovina, Medellín y Rionegro, 1914-1970. Iatreia. 2006;19:393-407. [ Links ]
4. González C, Sánchez G, Castro C, Gómez C, Molina F, Velásquez LE. Control de Fasciola hepatica en el agua de consumo animal a través de filtración rápida y lenta. Revista EIA. 2013;10:133-41. [ Links ]
5. Quintero D, Valencia G, Zuluaga M, Velásquez LE, Valencia N, Gómez C. Vereda La Madera de El Carmen de Viboral - Antioquia: distribución de focos de fasciolosis bovina. Colanta Pecuaria. 2013;40:39-45. [ Links ]
6. Wilches C, Jaramillo G, Muñoz L, Robledo SM, Vélez D. Presencia de infestación por Fasciola hepatica en habitantes de San Nicolás, Oriente antioqueño. Infectio. 2009;13:92-9. [ Links ]
7. Pulido AD, Castañeda R, Arbeláez G. Fasciola hepatica : pedagogía de diagnóstico por laboratorio y su situación en Colombia. REDVET. 2010;12:1-11. [ Links ]
8. Valencia N, Malone JB, Gómez C, Velásquez LE. Climate-based risk models for Fasciola hepatica in Colombia. Geospat Health. 2012;6:67-85. http://dx.doi.org/10.4081/gh.2012.125 [ Links ]
9. Ministerio de la Protección Social. Decreto 1500 mayo 4 de 2007. Fecha de consulta: 1º de noviembre de 2013. Disponible en: https://www.invima.gov.co/images/stories/aliementos/Decreto1500_2007.pdf. [ Links ]
10. Gálvez AC, Duque F, Velásquez LE. La enfermedad es otra: itinerario terapéutico de la fasciolosis bovina en Rionegro (Antioquia). Ces Med Vet Zootec. 2012;7:74-87. [ Links ]
11. Álvarez A, Boyacá M. Comparación de la técnica de Dennis con los hallazgos hepáticos post mortem para el diagnóstico de la fasciolosis bovina. Cultura Científica. 2009;7:28-33. [ Links ]
12. Li O, Leguía G, Espino A, Duménigo B, Díaz A, Otero O. Detección de anticuerpos y antígenos para el diagnóstico de Fasciola hepatica en alpacas naturalmente infectadas. Rev Investig Vet Perú. 2005;16:143-53. [ Links ]
13. Uruburu M, Bedoya JC, Velásquez LE. ELISA indirecta para el diagnóstico de fasciolosis bovina en leche. Ces Med Vet Zootec. 2013;18:93-100. [ Links ]
14. Vargas D, Vega M, González CG. Aproximación a una caracterización molecular de Fasciola hepatica por la técnica RAPDs - PCR. Parasitol Latinoam. 2003;58:11-6. http://dx.doi.org/10.4067/S0717-77122003000100002 [ Links ]
15. Becerra WM. Consideraciones sobre estrategias sostenibles para el control de Fasciola hepatica en Latinoamérica. Rev Col Cienc Pec. 2001;14:30-5. [ Links ]
16. Winn WC, Allen D, Janda WM, Koneman EW, Procop GW, Schrenckenberger PC, et al . Koneman. Diagnóstico microbiológico. Sexta edición. Bogotá D.C: Editorial Médica Paramericana; 2008. p. 1199. [ Links ]
17. Pajuelo G, Luján D, Paredes B, Tello R. Aplicación de la técnica de sedimentación espontánea en tubo en el diagnóstico de parásitos intestinales. Rev Biomed. 2006;17:96-101. [ Links ]
18. Sandoval E, Morales G, Ybarra N, Barrios M, Borges J. Comparación entre dos modelos diferentes de cámaras de McMaster empleadas para el conteo coproscópico en el diagnóstico de infecciones por nematodos gastroentéricos en rumiantes. Zootecnia Trop. 2011;4:29. [ Links ]
19. Gabrie JA, Rueda MM, Canales M, Sánchez A. Utilidad del método Kato-Katz para diagnóstico de unciniariasis: experiencia en una zona rural. Rev Med Hondur. 2012; 80:96-101. [ Links ]
20. Aguirre DH, Viñabal AE, Gaido AB. Comparación de tres técnicas coproparasitológica para el diagnóstico de Fasciola hepatica en rumiantes. Vet. Arg. 1998;15:421-7. [ Links ]
21. Girao ES, Ueno H. Técnica de quatro tamises para o diagnóstico coprológico cuantitativo de fasciolose dos rumiantes. Pesq Agropec. 1985;20:905-12. [ Links ]
22. Dennis W, Stone W, Swanson L. A new laboratory and field diagnostic test for fluke ova in feces. Florida Agricultural Experiment Station Journal Series. 1954;172:47-50. [ Links ]
23. Valero AM, Pérez I, Periago MV, Khoubbane M, Mas-Coma S. Fluke egg characteristics for the diagnosis of human and animal fascioliasis by Fasciola hepatica and F. gigantica . Acta Trop. 2009;111:150-9. http://dx.doi.org/10.1016/j.actatropica.2009.04.005 [ Links ]
24. Castro N, Becerra M. Foco de fasciolisis ovina en una hacienda en la vereda Presidente, municipio de Chitagá, Norte de Santander, Colombia. Bistua. 2011;9:64-72. [ Links ]
25. López LP, Romero J, Velásquez LE. Aislamiento de Paramphistomidae en vacas de leche y en el hospedador intermediario ( Lymnaea truncatula y Lymnaea columella ) en una granja del trópico alto en el occidente de Colombia. Revista Colombiana de Ciencias Pecuarias. 2008;21:9-18. [ Links ]
26. Paucar S, Chávez A, Casas E, Suárez F. Prevalencia de fascioliasis y paramfistomiasis en el ganado lechero de Oxapampa, Pasco. Rev Investig Vet Perú. 2010;21:87-92. [ Links ]
27. Suárez H, Olaechea V, Rossanigo CE, Romero JR. Enfermedades parasitarias. Publ Tec. 2007;70:159-77. [ Links ]
28. Bedoya J, Hurtado Y, Pérez J, Solano S, Úsuga VM, Vanegas M, et al . Primer registro de focos de fasciolosis y paramfistomosis en bovinos doble propósito, Gómez Plata, Antioquia, Colombia. Hechos Microbiológicos. 2014;3:1-31. [ Links ]
29. López J, Velásquez LE. Cotylophoron panamensis (Digenea: Paramphistomidae) in cattle from Meta and Guaviare, Colombia. Acta Biol Colomb. 2012;17:421-30. [ Links ]
30. Uribe N, Sierra RF, Espinosa CT. Comparison of the technique Kato-Katz, TSET and TSR in diagnosis of the infection by Fasciola hepatica in humans. Salud UIS. 2012;44:7-12. [ Links ]














