Clostridium difficile es un bacilo Gram positivo anaerobio, formador de esporas, que usualmente se propaga por vía fecal-oral. Hace cuatro décadas se determinó su papel como un agente etiológico de diarrea asociada al uso de antibióticos y de colitis pseudomembranosa 1. La enfermedad asociada a C. difficile es la principal causa de diarrea de origen infeccioso en los hospitales y es la causa de hasta 30 % de la diarrea asociada a antibióticos 2.
La frecuencia y la gravedad de la infección por C. difficile han aumentado en los últimos años, con una incidencia reportada en Canadá de 22,5 casos por 1.000 hospitalizaciones 3 y una mortalidad atribuible en Norteamérica que va desde 1,5 hasta 25 % 3-6. Sumado al incremento en los costos directos e indirectos de atención de la enfermedad (alcanzan hasta USD$ 3,2 billones al año en Estados Unidos) 5, estas características han convertido la enfermedad en un problema de salud en los hospitales 6.
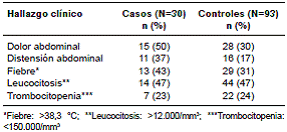
La enfermedad asociada a C. difficile se define como un cuadro de diarrea de inicio agudo y de causa no aparente en pacientes con presencia confirmada de C. difficile toxigénico o de su toxina 7. Los síntomas mas frecuentes son la diarrea, el dolor abdominal, la distensión abdominal y la fiebre. El espectro de la enfermedad es amplio y abarca desde los portadores asintomáticos hasta aquellos víctimas de episodios fulminantes asociados a colitis pseudomembranosa y megacolon tóxico.
Son múltiples los factores de riesgo, pero los más importantes son el uso previo de antibióticos 8,9 y la exposición al germen 7. Además, se han reconocido otros factores asociados, como la edad mayor de 65 años 8, el tiempo de hospitalización 10,11, la estancia previa en la unidad de cuidados intensivos 12, la gravedad de la condición de salud, la hipoalbuminemia (<2,5 g/dl) 11, el uso previo de quimioterapia, la manipulación del tubo digestivo (incluido el paso de sondas de nutrición) 13 y el uso de medicamentos que suprimen el ácido gástrico (bloqueadores de la histamina 2 o inhibidores de la bomba de protones) 12,14,15.
Entre las complicaciones de la infección por C. difficile están la alteración electrolítica, el megacolon tóxico, la perforación intestinal con peritonitis y el choque séptico, las cuales pueden llevar a la muerte 14.
Después del reconocimiento de la enfermedad y de determinar la presencia de complicaciones, el tratamiento de primera línea se basa en la administración de metronidazol o vancomicina, según la gravedad del cuadro clínico 16,17.
En el 2011, se llevó a cabo en Colombia un estudio sobre los factores de riesgo de la enfermedad, con 22 casos y 44 controles 12, en cuyo desarrollo se plantearon algunos inconvenientes en torno a la sensibilidad de la prueba diagnóstica utilizada. El Hospital Pablo Tobón Uribe cuenta desde febrero de 2010 con una prueba inmunológica de alto rendimiento para la detección de la toxina, con la cual se incrementa la exactitud del diagnóstico. En este contexto, el objetivo del presente estudio fue caracterizar clínicamente los casos de enfermedad asociada a C. difficile en ese hospital de referencia y determinar los principales factores de riesgo asociados con su aparición.
Materiales y métodos
Lugar del estudio
El Hospital Pablo Tobón Uribe es un hospital de tercer nivel, de 365 camas, ubicado en Medellín, Colombia. Tiene dos unidades mixtas de cuidados intensivos con 37 camas y una unidad de cuidados especiales con 20 camas.
Diseño del estudio
Se hizo un estudio de casos anidado en una cohorte establecida con base en la simultaneidad del momento de inicio de la infección y el periodo transcurrido hasta su desenlace. En dicha cohorte se estableció, mediante muestreo aleatorio, un subgrupo de pacientes que cumplían con los criterios establecidos para el caso y otro de control, representativo de todos los individuos que no presentaron el desenlace. Para una adecuada estimación del efecto de los factores potencialmente asociados con el desenlace, se complementaron los casos del estudio con aquellos que no quedaron incluidos en el subgrupo inicial. Aunque parezca que los casos están excesivamente representados con respecto a la cohorte original, si el tamaño del subgrupo es, al menos, de 15 % de dicha cohorte, no se considera necesaria una ponderación en el muestreo y las medidas de asociación estimadas no se ven afectadas por el sesgo debido a la selección completamente aleatoria de los controles 18.
Población de la cohorte
Se incluyeron pacientes con diarrea adquirida en el hospital a quienes se les había hecho la prueba para la toxina A-B de C. difficile entre febrero de 2010 y febrero de 2012. Solo se incluyó una prueba por paciente. Se excluyeron aquellos pacientes con muestras tomadas en consulta ambulatoria o que hubieran estado hospitalizados en otra institución.
Definición de caso
Se consideraron casos los pacientes con diarrea (al menos, tres deposiciones líquidas en un periodo de 24 horas) y resultado positivo en la prueba para la toxina (Enzyme Linked Fluorescent Assay, ELFA) realizada en un equipo miniVIDAS(r) Biomeriuex.
Definición de controles
Se consideraron controles los pacientes con diarrea (al menos, tres deposiciones líquidas en un periodo de 24 horas) y prueba negativa en el subgrupo (15 %), seleccionados al azar del total de individuos a quienes se les había ordenado la prueba. Los pacientes con resultado positivo en la prueba ELFA y sin diarrea no fueron incluidos en la cohorte.
Recolección de los datos
Dos investigadores revisaron las historias clínicas de forma independiente y recolectaron las variables en un formato diseñado previamente.
Variables
Se recolectó información sobre la edad, el sexo, el centro de salud en el que se había hecho el diagnóstico, el diagnóstico de ingreso a la institución, el índice de gravedad (APACHE II) 19, la exposición a antibióticos en los 90 días previos al diagnóstico (cefalosporinas, penicilinas, carbapenemas, aminoglucósidos, quinolonas, lincosaminas o macrólidos), la exposición y el tiempo de uso de bloqueadores de la histamina 2 hasta el momento del diagnóstico, la exposición y el tiempo de uso de los inhibidores de la bomba de protones hasta el momento del diagnóstico, el tiempo de hospitalización hasta el momento del diagnóstico, la quimioterapia para cáncer en los 90 días previos al diagnóstico, la cirugía gastrointestinal y el uso de sondas para nutrición durante la hospitalización, los valores de albúmina en sangre antes del diagnóstico, las manifestaciones clínicas (dolor abdominal, distensión abdominal), la temperatura, los valores de proteína C reactiva y del leucograma, el resultado del examen coprológico, el tipo de tratamiento (vancomicina oral, metronidazol intravenoso, metronidazol oral, combinado), las complicaciones (alteración en los niveles de sodio, potasio o magnesio que requirieran corrección por parte del médico tratante, megacolon tóxico definido con base en el diagnóstico del médico tratante, perforación intestinal, falla renal aguda), el tiempo de estancia en la unidad de cuidados intensivos, el tiempo de estancia en el hospital y el estado en el momento del egreso.
Análisis de los datos
Se emplearon métodos de estadística descriptiva básica según el tipo de variable: medias con desviación estándar (DE) y medianas con rangos intercuartílicos (RIC); análisis de asociación mediante regresión logística con variables candidatas, las cuales se seleccionaron según su relevancia de acuerdo con reportes previos en la literatura científica y la frecuencia en la población de estudio:
uso previo de antibióticos, de bloqueadores de histamina, de inhibidores de la bomba de protones, quimioterapia reciente, cirugía gastrointestinal o uso de sonda para nutrición durante la hospitalización.
No se hizo ninguna clase de ajuste o ponderación por la representación excesiva de los casos, se verificó el supuesto de ausencia de colinealidad mediante el factor de inflación de la varianza y no se consideraron términos de interacción en el modelo. Todos los análisis se hicieron con el programa Stata/IC 12.1 (Stata Co., College Station, TX, USA) y los resultados se presentan como riesgos relativos indirectos (odds ratio, OR) con su respectivo intervalo de confianza de 95 %.
Resultados
Durante el periodo de estudio se solicitaron 963 pruebas de toxina A-B para C. difficile, 147 para pacientes ambulatorios y 84 para pacientes de otras instituciones. De la cohorte restante (n=732) se seleccionó aleatoriamente un subgrupo de 110 pacientes (15 %), de los cuales 17 (15 %) fueron casos de infección confirmada con prueba positiva para la toxina. En la cohorte completa se encontraron 13 casos adicionales de infección por C. difficile confirmada por la prueba para la toxina, con lo cual la población final de estudio fue de 30 casos y 93 controles.
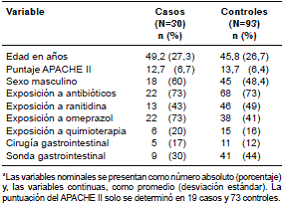
La edad media fue de 49 años (0 a 98 años) y 51 % (n=63) correspondió a pacientes de sexo masculino. El 73 % (n=90) de los pacientes había recibido antibióticos en los 90 días previos a la aparición de la diarrea, 48 % (n=59) recibió medidas de profilaxis para úlceras de estrés gástricas con ranitidina y, 49 % (n=60), con omeprazol. Veintiún pacientes (17 %) habían recibido quimioterapia en los tres meses anteriores al cuadro de diarrea, el 13 % (n=16) habían sido sometidos a cirugía gastrointestinal y en 41 % (n=50) se había empleado sonda nasogástrica antes del episodio infeccioso. El puntaje medio en el APACHE II fue de 13,5 (desviación estándar, DE=6,5), aunque en 31 pacientes (25 %) este no se pudo calcular debido a la ausencia de datos. En el cuadro 1 se muestran estas variables en los casos y los controles.
Cuadro 1 Caracterización de la población de estudio (casos y controles), Hospital Pablo Tobón Uribe, 2010-2012
Los síntomas predominantes en la población de estudio fue el dolor abdominal (n=43, 35 %), seguido de la distensión abdominal (n=27, 22 %). La fiebre, el dolor abdominal y la distensión abdominal fueron más frecuentes en los casos de enfermedad asociada a C. difficile (cuadro 2). En todos los pacientes estudiados el valor medio de leucocitos fue de 10.907 células/mm3 (DE=8,402), el de la proteína C reactiva fue de 10 mg/dl, con un rango de 0 a 42 (DE=10) y el de albúmina fue de 2,8 g/dl (SD=0,75). La mediana de estancia hospitalaria fue de 25 días (RIC=13-50), 34 pacientes (28 %) fueron atendidos en la unidad de cuidados intensivos y la mediana de estancia en dicho servicio fue de 20 días (RIC=12-26).
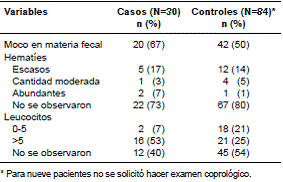
Los valores de estas variables en casos y controles se presentan en el cuadro 3 y, en el cuadro 4, los principales resultados del examen coprológico en la población de estudio. La presencia de moco fue más frecuente en los casos de enfermedad asociada a C. difficile. Aunque en el examen coprológico de pacientes con enfermedad asociada a C. difficile fue más frecuente la presencia de abundantes hematíes y leucocitos, dicho hallazgo no es indicativo de la enfermedad.
Cuadro 3 Resultados de los exámenes de laboratorio y evolución clínica de casos y controles, Hospital Pablo Tobón Uribe, 2010-2012
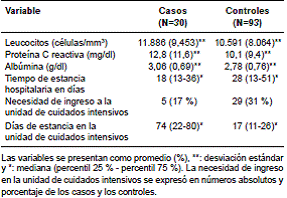
Cuadro 4 Resultados del examen coprológico en pacientes sometidos a la prueba de detección de la toxina para C. difficile, Hospital Pablo Tobón Uribe, 2010-2012
De los 30 casos con resultado positivo en la prueba de toxina para C. difficile, cinco tuvieron, además, resultados compatibles con colitis pseudomembranosa en la colonoscopia y tres en la histopatología de colon.
De los 30 casos confirmados, 12 (40 %) presentaron alguna alteración electrolítica, seis (20 %), falla renal aguda, ocho (27 %), sepsis grave, cuatro (13 %), choque séptico y cuatro pacientes (13 %) fallecieron en el hospital. Se presentó un caso de megacolon tóxico y no hubo casos de perforación intestinal. Entre los controles, la mortalidad hospitalaria fue de 11 % (n=10).
Los tratamientos administrados a los casos incluyeron metronidazol oral a 16 pacientes (53 %), vancomicina oral a cinco (17 %), vancomicina y metronidazol oral a cuatro (13 %), metronidazol intravenoso a tres (10 %), y vancomicina y metronidazol intravenosos a dos (7 %). En todos los pacientes (n=30) hubo remisión del cuadro clínico, definida esta como desaparición de la diarrea.
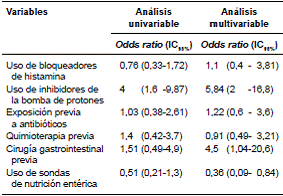
En el cuadro 5 se muestran los factores asociados con la infección por C. difficile.
Discusión
En este estudio la enfermedad asociada a C. difficile fue una causa frecuente de diarrea adquirida en el hospital (15 %) y afectó a diversos grupos de población, especialmente, adultos entre los 50 y los 70 años de edad, con un ligero predominio del sexo masculino. El uso previo de inhibidores de la bomba de protones, así como el antecedente de cirugía gastrointestinal, se asociaron con la aparición de la enfermedad.
El aporte primordial del trabajo de investigación fue la caracterización de un grupo de pacientes hospitalizados con diagnóstico de enfermedad asociada a C. difficile y la asociación en ellos de dos factores de riesgo (uso de inhibidores de la bomba de protones y cirugía gastrointestinal previa) y la aparición de la enfermedad. Dichos resultados pueden facilitar a los médicos algunos criterios adicionales para el diagnóstico de esta enfermedad, así como para iniciar oportunamente el tratamiento antibiótico y disminuir la aparición de algunas complicaciones.
La enfermedad asociada a C. difficile es la principal causa de diarrea adquirida en hospitales en el mundo entero y está asociada con altas tasas de morbilidad y mortalidad (5). Se encontró una prevalencia de la enfermedad de 15 %, muy similar a la encontrada por otros autores, la cual oscila entre 5 y 20 % 4,6,13,20.
La enfermedad asociada a C. difficile no ha sido claramente caracterizada a nivel local y, dadas las particularidades epidemiológicas, genéticas y microbiológicas de nuestro entorno, es válido considerar la posibilidad de un comportamiento biológico diferente al de otras latitudes.
En este orden de ideas, en una revisión bibliográfica hasta el 2009 de datos provenientes de Latinoamérica, Camacho-Ortiz, et al. 21, no encontraron datos procedentes de Colombia. No obstante, dos años después (2011), Becerra, et al., publicaron un estudio de casos y controles centrado en los factores de riesgo asociados a la infección por C. difficile (12) y encontraron una asociación significativa con la edad mayor de 65 años (OR=3,4; IC95% 1,1-10,1), la estancia en la unidad de cuidados intensivos (OR=4,0; IC95% 1,3-12,2) y el uso de inhibidores de la bomba de protones (OR=5,15; IC95% 1,6-15,9). A pesar de los datos encontrados por estos investigadores, la muestra solo incluía 22 casos y 44 controles, y se plantearon reparos sobre la sensibilidad de la prueba diagnóstica utilizada para la detección de la toxina.
Al igual que en esta investigación, diversos estudios 3,4,16,22,23 han documentado que esta enfermedad afecta a todos los grupos poblacionales sin distinción de edad ni de sexo, aunque parece presentarse con mayor frecuencia en los adultos mayores de 65 años, en quienes, además, es más agresiva 3,12,22,24.
El diagnóstico de la enfermedad se hace con base en la presencia de síntomas como diarrea, fiebre, dolor y distensión abdominal 1,25. Si bien la diarrea es el síntoma característico, hasta el 20 % de los pacientes puede presentar estreñimiento o deposiciones normales 17). En la institución donde se hizo la investigación, solo se solicita la prueba de detección de C. difficile para los pacientes que presentan diarrea, razón por la cual, el 100 % de los incluidos tenían este síntoma. El 57 % de ellos presentaron otros síntomas gastrointestinales, como distensión o dolor abdominal, la mitad tuvieron leucocitosis y solo el 34 % tuvo fiebre. En el trabajo realizado por Becerra, et al.12, la fiebre y la diarrea mucosa se relacionaron claramente con la enfermedad asociada a C. difficile, y el dolor abdominal mostró apenas una tendencia a la asociación.
En cuanto a la estancia hospitalaria, los pacientes con enfermedad asociada a C. difficile estuvieron el doble de tiempo en el hospital, en comparación con los pacientes sin la enfermedad (92 Vs. 45 días). Pese a esto, la estancia en la sala general fue menor en los pacientes con enfermedad asociada a C. difficile, y fue la estancia en la unidad de cuidados intensivos (cuatro veces más prolongada en los pacientes con enfermedad asociada a C. difficile), la que incidió en el aumento en los días de hospitalización. Este hallazgo no se pudo explicar. Infortunadamente, debido en parte a las características del estudio, no se consiguió establecer la relación entre el tiempo previo a la hospitalización y el desarrollo de la enfermedad asociada a C. difficile, un dato que hubiera podido dar luces sobre otro factor asociado con la presencia de esta enfermedad.
Se encontró una mortalidad similar en ambos grupos de pacientes (11 % Vs. 13 %; n=4). La mortalidad estuvo por encima del 4 % encontrado en Latinoamérica 21, pero por debajo de lo encontrado por Micek, et al., (25 %) en Estados Unidos en una muestra de pacientes con respiración mecánica asistida 26. Kyne, et al., registraron una mortalidad similar (12 %) en Irlanda 22, hallazgo que respondería a la gravedad de los pacientes en la cohorte, cuya puntuación media en el APACHE II fue de 12,7; 20 % de ellos tenía cáncer y 25% eran adultos mayores. Además, un alto porcentaje (73 %) de los pacientes había recibido antibióticos antes de la aparición de la diarrea. En una población de pacientes hospitalizados en la unidad de cuidados intensivos, Marcon, et al.27, encontraron una asociación entre el uso de antibióticos (principalmente ceftriaxona) y la aparición de la diarrea (OR=13; IC95% 1,95-552,38). Sin embargo, al igual que en este trabajo, algunos autores 9,12 no han hallado asociación entre el uso de antibióticos y el desarrollo de enfermedad asociada con C. difficile, lo cual probablemente se relacione con la definición de caso (paciente con diarrea) y la marcada asociación entre el uso de antibióticos y la diarrea de diversos orígenes adquirida en el hospital. Por otro lado, este dato, opuesto a lo reportado en otros estudios, puede ser el resultado del reducido número de pacientes.
Después del análisis ajustado, se determinaron como factores de riesgo para la infección los antecedentes de uso de inhibidores de la bomba de protones y la cirugía gastrointestinal previa. El uso de sondas para la nutrición entérica se comporta como un factor protector. El uso previo de antibióticos y el uso de bloqueadores de histamina no se asociaron con la infección por C. difficile.
El uso de inhibidores de la bomba de protones se ha descrito como un factor de riesgo para la infección por C. difficile9,12,15,28. Las posibles explicaciones se derivan de la supresión del ácido gástrico que actúa como neutralizador de la toxina y disminuye la carga de agentes patógenos que ingresan al tubo digestivo. A pesar de esto, la espora de C. difficile es relativamente estable frente al ácido gástrico, por lo que la explicación fisiopatológica para la asociación entre el uso de supresores de ácido y la infección por C. difficile no es del todo clara. Como factores que también pueden predisponer a esta infección, se han postulado la alteración de la flora intestinal, el efecto directo del germen sobre la actividad de los leucocitos 29,30, y la disminución en la expresión de genes con importantes funciones en la integridad del colonocito y en la sensibilidad a la toxina 31. En un metaanálisis en el cual se incluyeron 288.620 pacientes, Janarthanan, et al.15, encontraron una asociación entre el uso de inhibidores de la bomba de protones y la infección por C. difficile, con un riesgo relativo de 1,65 (IC95% 1,41-1,93). De la misma forma, Becerra, et al., en Colombia y Leonard en un metaanálisis 12,28) encontraron la misma asociación.
El otro factor de riesgo encontrado para la enfermedad asociada con C. difficile fue la cirugía gastrointestinal previa. En un análisis extenso para estimar el impacto de la enfermedad en pacientes sometidos a cirugía en Estados Unidos, Zerey, et al.32, encontraron que la incidencia de C. difficile fue 2,7 veces más alta en los pacientes que fueron operados de emergencia. Además, hallaron que la colectomía (OR=2,77; IC95% 2,65-2,89), la resección de intestino delgado (OR=2,40; IC95% 2,26-2,54) y la resección gástrica (OR=2,26; IC95% 2,03-2,52) representaban un mayor riesgo de adquirir la enfermedad. Los autores plantearon que, al ser el intestino un reservorio para muchos agentes patógenos que se adquieren en hospitales, su manipulación, sumada a la alteración de las defensas normales por otros factores, puede explicar la relación entre la cirugía gastrointestinal y la aparición de la enfermedad asociada con C. difficile. Pese a esta explicación, dicha relación no ha sido dilucidada del todo.
Contrario a lo hallado en la literatura científica 13,33, el uso de sondas de nutrición entérica se comportó como un factor protector en este estudio. Bliss, et al.13, encontraron que su uso, especialmente de sondas colocadas más allá del píloro, se relacionaba con un mayor riesgo de enfermedad asociada a C. difficile (20 % Vs. 8 %). Algunas explicaciones de estos hallazgos serían el uso limitado de fórmulas elementales, las cuales se han relacionado con la infección por este germen debido a la alteración de la flora intestinal del colon 34,35, y el poco uso de sondas en el yeyuno para nutrición entérica, las cuales se han relacionado más con la infección por este microorganismo 13. Infortunadamente, no se pudieron recopilar datos sobre el tipo de sonda utilizada para la nutrición de los pacientes.
Los 30 pacientes con diagnóstico de infección por C. difficile recibieron tratamiento antibiótico con metronidazol o vancomicina. En una muestra de pacientes con enfermedad asociada a C. difficile hospitalizados en la unidad de cuidados intensivos, Micek, et al.26, encontraron que el 94 % de ellos había sido tratado con metronidazol, el 48 %, con vancomicina oral y, cerca del 50 %, con una combinación de vancomicina y metronidazol. En el presente estudio, independientemente del tipo de tratamiento, hubo una mejoría del cuadro clínico definida como resolución del cuadro de diarrea. Infortunadamente, no se pudo establecer la tasa de recaídas de la enfermedad. La recomendación general, dada la similar reacción clínica a los dos tratamientos 36,37, es tratar las formas leves a moderadas de la enfermedad con metronidazol y dejar la vancomicina para las formas graves, pues ha habido un incremento en la proporción de pacientes que no mejoran con metronidazol y que tienen mayor porcentaje de recaídas 16,17. Vale la pena anotar que en Colombia, al igual que en gran parte de América Latina, la presentación más accesible de la vancomicina es la solución inyectable 21. En el presente estudio, los pacientes recibieron la solución inyectable de vancomicina por vía oral, con éxito en todos ellos y sin que se registraran reacciones adversas.
El estudio tuvo varias limitaciones que deben tenerse en cuenta. Primero, su ubicación en un solo centro de atención que, además, es un hospital universitario, no permite la generalización de los resultados. Segundo, a pesar de contar con una prueba inmunológica de alto rendimiento para la detección de la toxina, de sensibilidad cercana al 80 % 38, el método utilizado no es el más sensible, lo cual no permite descartar con certeza que algunos de los controles correspondieran realmente a casos. Pese a ello, los métodos diagnósticos empleados en el mundo (9) y en Latinoamérica 21 están restringidos, en general, a la detección de toxinas y son principalmente ensayos enzimáticos (toxinas A o AB); en pocas ocasiones se recurre a métodos de cultivo celular para determinar los cambios citopáticos 39,40 o a pruebas de reacción en cadena de la polimerasa. Tercero, el tamaño de la muestra no tuvo poder suficiente para detectar factores de riesgo con una menor magnitud de asociación con el resultado o con una aparición infrecuente en la población de estudio. Por último, es necesario tener en cuenta que la selección de los controles se hizo entre pacientes con diarrea de origen hospitalario y sospecha de infección por C. difficile, pero con resultado negativo en la prueba para la toxina. Estos controles podrían no representar realmente a toda la población en riesgo de adquirir la infección.
En conclusión, la infección por C. difficile está presente en una proporción significativa de pacientes adultos con cuadros de diarrea adquirida en el hospital. El uso de inhibidores de la bomba de protones y la cirugía gastrointestinal previa se relacionaron con la enfermedad asociada a C. difficile, en tanto que el uso de sondas para la nutrición entérica se comportó como un factor protector.