El trasplante es el tratamiento de elección en pacientes con enfermedad renal crónica avanzada, dado que se asocia con una mejor calidad de vida y una mayor supervivencia que la diálisis 1. La mortalidad global anual en la población de pacientes con trasplante es de 5 a 7 %; la primera causa de muerte es cardiovascular (30 %), seguida muy de cerca por las infecciones (21 %) 2. Aunque con los nuevos esquemas inmunosupresores se ha logrado disminuir la incidencia del rechazo, las infecciones siguen siendo uno de los principales factores de morbilidad. La inmunosupresión se asocia con un incremento en el riesgo de infección, por lo cual el cribado y el inicio de la profilaxis son fundamentales 3.
Los costos de las complicaciones infecciosas en trasplantes de órganos sólidos incluyen los de la estancia hospitalaria evitable y el tratamiento, además de la morbilidad y la mortalidad resultantes. En Canadá, la enfermedad por citomegalovirus (CMV) se ha asociado con un aumento de 2,5 veces en los costos del trasplante renal de los pacientes afectados, comparados con aquellos que no presentan la enfermedad 4. La infección viral por CMV es la más delicada después de un trasplante renal; ocurre frecuentemente entre el primero y el cuarto mes, y coincide con las dosis más elevadas del tratamiento inmunosupresor; sin embargo, pasados los seis primeros meses, puede aparecer una infección o una enfermedad tardía, por lo cual el riesgo sigue siendo alto a lo largo del primer año 5.
Entre los factores de riesgo plenamente establecidos para la presencia de alguna infección o enfermedad, el más importante depende de los niveles de IgG para CMV, tanto en el donante como en el receptor. Los casos con donante positivo (D+) y receptor negativo (R) se clasifican como de alto riesgo; cuando el donante y el receptor son positivos (D+/R+), o el donante es negativo y el receptor positivo (D/R+), se clasifican como de riesgo intermedio, y los casos de donante y receptor negativos (R/R), como de bajo riesgo 6. Otros factores de riesgo mencionados en algunos estudios son los receptores mayores de 60 años de edad, los antecedentes de episodios de rechazo agudo, la infección viral concomitante por polioma, el uso de medicamentos como la ciclosporina, los esquemas con tres medicamentos inmunosupresores comparados con los de dos 7, y, especialmente, la inducción con inmunoglobulina antitimoitos, que aumenta la probabilidad de infección de dos a cinco veces 6.
En Colombia, se han hecho tres estudios descriptivos: en el primero, realizado en Medellín entre 1988 y 1989, se evaluó la seroprevalencia de IgG para CMV en pacientes en lista de espera, donantes cadavéricos, donantes intrafamiliares y en la población general, y se encontraron valores de 92, 73, 87 y 74 %, respectivamente; se determinó, asimismo, el riesgo para infección por CMV en los pacientes con trasplante, 8 % de los cuales se clasificó como de riesgo alto, 90 % como de riesgo intermedio y 2 % como de riesgo bajo, con un porcentaje de casos de enfermedad por CMV de 9 % 8.
En el segundo estudio, realizado entre 1998 y 2010 tambien en Medellín, se registró 90 % de seroprevalencia en receptores y 90,2 % en donantes, con la siguiente distribución por estatus de riesgo: bajo, 0,8 %, intermedio, 91 %, y alto, 8 % 9.
En el último y más reciente estudio descriptivo y retrospectivo realizado entre 2010 y 2014, se evaluó todo el territorio nacional y se documentó una seroprevalencia para CMV de 86,2 % en donantes de trasplantes renales, y de 91 % en receptores, porcentajes similares a los de otros países en desarrollo. La distribución del riesgo en ese estudio fue de 7,3, 91,4 y 1,3 % para riesgo alto, intermedio y bajo, respectivamente 10.
La importancia del CMV no radica únicamente en su alta prevalencia e incidencia, sino en la asociación que ha tenido con diversos resultados adversos debidos a la aparición de la enfermedad, o a efectos indirectos asociados con la infección, como el aumento de la incidencia del rechazo del injerto, el factor de riesgo de fibrosis intersticial y la atrofia tubular en los tres meses posteriores al trasplante, la aparición de una glomerulopatía caracterizada por engrosamiento miointimal mediado por quimiocinas codificadas por el CMV 11, así como el aumento del riesgo de infecciones por Candida spp., Pneumocystis jirovecci, Aspergillus spp., virus de Epstein-Barr, herpes virus 6 y 8, y por último, un mayor riesgo cardiovascular y de estenosis de la arteria renal 12.
En ausencia de medidas preventivas, la frecuencia de la infección se ha registrado en 40 a 100 % de los receptores y, la de enfermedad, en cerca de 67 % 6,13. Para combatirlas se han diseñado estrategias de prevención como la profilaxis universal y el tratamiento anticipado 14.
La profilaxis universal implica la administración de medicamentos antivirales a partir de los diez días del trasplante y hasta tres a seis meses después; según los estudios, el ganciclovir y el valganciclovir tienen una efectividad similar 15, aunque se prefiere este último debido a su biodisponibilidad. La dosis recomendada en recientes estudios para pacientes con función renal mayor de 40 ml/minuto, es de 450 mg/día 16. Sin embargo, en años anteriores la dosis sugerida para pacientes con tasa de filtración glomerular mayor de 60 ml/minuto era de 450 mg cada 12 horas. En un metaanálisis reciente se comparó la dosis de 450 mg con la de 900 mg y no se encontraron mejores resultados con mayores dosis (odds ratio, OR=1,38: IC95%: 0,84-2,25; p=0,19), pero la presencia de leucopenia sí se aumentó tres veces (p=0,0002) 17.
El tratamiento anticipado es una estrategia para detectar la replicación en pacientes asintomáticos mediante la determinación semanal de la carga viral con reacción en cadena de la polimerasa (PCR) para CMV, durante los primeros tres meses (18). Para el diagnóstico se ha utilizado la prueba de anti- genemia pp65, pero esta no está estandarizada, por lo cual los últimos consensos recomiendan hacer el seguimiento de la carga viral mediante PCR dadas sus características operativas 18.
En algunos metaanálisis recientes de comparaciones directas ha quedado claro que no hay diferencia en cuanto a la presencia de rechazo, la pérdida del injerto, la enfermedad por CMV o la muerte, entre las dos estrategias 19. La profilaxis universal parece asociarse con menores grados de viremia después del trasplante, aunque con desventajas, como una mayor proporción de infecciones tardías y de toxicidad del medicamento (leucopenia, neutropenia y lesión renal) 19. El tratamiento anticipado involucra el gasto semanal de la verificación de la carga viral de CMV mediante PCR y la coordinación de la toma, aunque con la ventaja de que se evita la toxicidad farmacológica 20.
Con respecto al tiempo de duración del tratamiento, en el estudio IMPACT se comparó el tratamiento administrado durante 200 días con el de 100 días en pacientes con riesgo alto (D+/R) para CMV, y se documentó una disminución de la incidencia de la viremia, sin aumento de los efectos adversos, con el tratamiento de 200 días 21. En pacientes con riesgo intermedio para CMV, el tiempo promedio de tratamiento es de 100 días.
En publicaciones previas de comparaciones entre el ganciclovir intravenoso y el valganciclovir en pacientes con riesgo alto (D+/R), se evidenció una eficacia similar para prevenir infecciones; sin embargo, a los 12 meses, 36,8 % de los pacientes asignados al tratamiento de 100 días presentó enfermedad tardía comparado con 16,1 % de quienes tomaron el tratamiento durante 200 días. Este beneficio no se replicó en los pacientes con riesgo intermedio 22.
Siguiendo las recomendaciones de las guías y las revisiones previas, se empleó este modelo, con el enfoque de la mejor estrategia frente al riesgo de infección.
En cuanto al uso de timoglobulina, que es uno de los factores de riesgo para CMV, en los estudios consultados se registraron diferentes porcentajes de infección y enfermedad según el medicamento administrado para la inducción. En Grecia, se han reportado datos de infección de 12,8 % y de enfermedad de 3,9 % 13; en pacientes de riesgo intermedio en Estados Unidos, se ha determinado un porcentaje de infección de 5,7 % con la profilaxis universal y de 55,5 % con el tratamiento anticipado, y 6,3 % de casos de la enfermedad en el primer año 23).
En cuanto a la aparición de otras infecciones bacterianas, por hongos o por otros virus, no se han ncontrado diferencias significativas entre las dos estrategias (19)
Los pacientes de alto riesgo tienen mayor probabilidad de cursar con viremia y enfermedad, por lo tanto, hay consenso en torno a la necesidad de dar profilaxis universal; en los pacientes de bajo riesgo no se recomienda, pero no hay consenso de cuál estrategia utilizar en la población de riesgo intermedio. La frecuencia de infecciones en casos de riesgo intermedio varía en los diversos estudios entre 78 % con tratamiento anticipado y 38 % con profilaxis universal en un estudio 24, y 38,7 % con el tratamiento anticipado y 11 % con la profilaxis universal, en otro 15. El porcentaje de enfermedad fue más parecido y fluctuó entre 6 y 8 %. Los efectos secundarios del tratamiento incluyen la leucopenia, presente en algunas series hasta en 22,3 % 25 de los expuestos, la cual se ve potenciada por la interacción con otros fármacos, como el micofenolato de mofetilo, así como por el deterioro de la función renal, la edad avanzada, la hidratación inadecuada y el uso de otros medicamentos nefrotóxicos. La condición de los pacientes suele mejorar entre los tres y los siete días después de suspender el medicamento.
En el estudio sobre un modelo económico en Francia, se encontró que la profilaxis universal era menos costosa, ya que reducía los días de hospitalización y otros cuidados de la salud 4, en tanto que, en las guías colombianas, se aboga por un enfoque estratificado según el riesgo para ajustar el tratamiento 16. En un país como Colombia, con recursos limitados, y en donde los costos son diferentes a los europeos, es importante hacer un análisis de relación entre costos y resultados clinicos, para establecer una guía terapéutica ajustada a nuestras necesidades.
Materiales y métodos
Con el programa TreeAge Pro Healthcare®, versión 2008, se diseñó un árbol de decisiones bajo la perspectiva del tercer pagador (sistema de salud colombiano), considerando únicamente los costos médicos directos durante un año de atención de los pacientes (figura 1). La población incluyó pacientes on trasplante renal de riesgo intermedio para CMV (D+/R+, D/R+), y las intervenciones evaluadas fueron la profilaxis universal y el tratamiento anticipado. Además de comparar los costos de las dos alternativas, se compararon otros aspectos como las infecciones, la enfermedad y los eventos adversos evitados.
En el marco de este trabajo, el trasplante renal se consideró de riesgo intermedio para infección por CMV, según los valores serológicos de IgG, cuando el donante y el receptor eran positivos (D+/R+) o el donante era negativo y el receptor positivo (D/R+).
La profilaxis universal con valganciclovir era la dosis profiláctica administrada durante 90 días, iniciando el décimo día después del trasplante, dosificada según la tasa de filtración glomerular: si esta es mayor de 40 ml/minuto, se indican 450 mg diarios de valganciclovir, si es de 25 a 35 ml/ minuto, 450 mg día de por medio, y si es de 10 a 24 ml/minuto, 450 mg dos veces a la semana.
El tratamiento anticipado se hizo con un control semanal de CMV durante los primeros tres meses. Si se registran resultados positivos en la carga viral, se inicia la administración de una dosis de 450 mg de valganciclovir cada 12 horas.
Se diagnosticó infección por CMV cuando la PCR era positiva para CMV y el paciente permanecía asintomático 22.
Se diagnosticó enfermedad por CMV cuando la PCR era positiva para CMV y el paciente presentaba síndrome viral con fiebre, malestar, leucopenia o infección invasiva 22.
Se consideró complicación cuando el paciente padecía tanto la infección como la enfermedad por CMV.
Los eventos secundarios considerados fueron leucopenia (menos de 4.000 leucocitos por microlitro) y deterioro renal (aumento de más de 2,5 mg/dl de la creatinina sérica).
Las probabilidades de transición se extrajeron de los estudios clínicos reportados en revisiones de la literatura científica. Se usó el método Delphi modificado para validar las probabilidades, con la participación de expertos de diferentes partes del país (cuadro 1). La determinación y la medición de los recursos consumidos se hicieron mediante la construcción de un caso de base con datos tomados de los casos de infección y enfermedad por CMV atendidos en una institución especializada en trasplantes, con la información de la cohorte de pacientes del presente estudio y de la revisión de la literatura colombiana disponible.
Los costos se estimaron en pesos colombianos (COP) de 2014. Los costos de los medicamentos con precio regulado se tomaron de las circulares del Ministerio de Salud y, los de los demás, del sistema de información de medicamentos (Sismed), siguiendo las recomendaciones del Instituto de Evaluación de Tecnologías en Salud (IETS) 26. Los costos de los medicamentos se muestran en el cuadro 2.
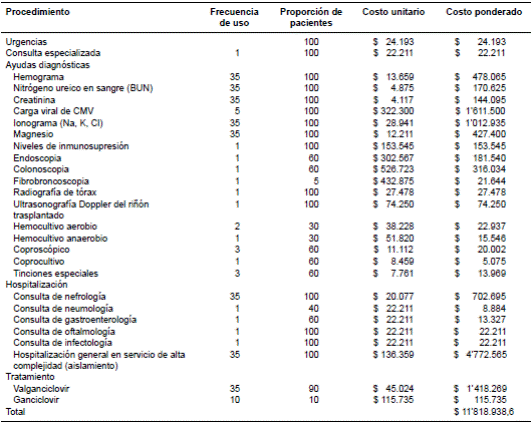
En cuanto a los costos de los procedimientos, se empleó el manual tarifario ISS 2001 con un incremento de 33 % basado en el índice de precios al consumidor (IPC) en salud del 2014. Los costos de los procedimientos incluidos se presentan en el cuadro 3.
Los estados de salud incorporados al modelo fueron los siguientes: sano, infección, enfermedad, presencia o ausencia de eventos secundarios. No se empleó la tasa de descuento dado el horizonte temporal.
Se hizo un análisis univariado de sensibilidad para cada una de las variables del modelo, empleando intervalos amplios, con el fin de determinar aquellas variables críticas que modificaran los resultados y la conclusión del modelo. Se hizo también un análisis probabilístico del tipo de Monte Carlo, repitiendo las simulaciones mil veces y aplicando distribuciones a cada una de las variables del modelo.
Resultados
Según nuestras estimaciones, el costo promedio del primer año de un paciente en tratamiento anticipado sería de COP$ 30’961.290; con profilaxis universal, ese costo sería de COP$ 29’967.834 (costo ‘incremental’ de COP$ 993.456). Con el tratamiento anticipado se presentarían 48 eventos adversos por cada mil pacientes, mientras que, con el tratamiento universal, se presentarían 124. Por otro lado, por cada mil pacientes con tratamiento anticipado, se presentarían 387 infecciones y, con la profilaxis universal, 110. El número de pacientes con enfermedad sería de 70 por cada mil con cualquiera de las dos alternativas. En total, el número de complicaciones por cada mil pacientes tratados sería de 457 con el tratamiento anticipado y de 180 con la profilaxis universal.
En el análisis univariado de sensibilidad, se encontró que los resultados del modelo en términos de costos se mantenían al modificar las variables de costos o las probabilidades de transición, con excepción de cuatro variables:
la dosis de valganciclovir, pues si se emplean 900 mg diarios en vez de 450, la profilaxis universal ya no permitiría ahorrar costos;
el costo de la verificación de la carga viral de CMV mediante PCR es crítico, y los resultados no favorecerían la profilaxis universal si se redujera el valor actual estimado para la prueba, que es de COP$ 322.300, a menos de COP$ 236.000 (una reducción de 27 %);
si la probabilidad de enfermedad con la profilaxis universal pasara de la estimación actual de 7 % a 13,4 %, o
si la probabilidad de infección con el tratamiento anticipado bajara de 38,7 % a apenas 2,9 %, pues la profilaxis universal ya no permitiría ahorrar costos (figura 2). En el análisis probabilístico con la simulación de Monte Carlo el costo de la profilaxis universal fue más bajo que el del tratamiento anticipado en 98,2 % de las simulaciones.
Discusión
La infección por CMV es frecuente en pacientes con trasplante renal. Los estudios en Colombia han demostrado un aumento en la mortalidad, con un OR de 4,51 (IC95%: 0,94-21,8) 27; además, está asociada con efectos indirectos, como el aumento de las tasas de rechazo y las bajas tasas de supervivencia del paciente y del injerto 11,12. Las tasas de infección y de enfermedad en pacientes de alto riesgo (D+/R) son muy altas, por lo que este grupo siempre debe recibir profilaxis universal. En los pacientes de bajo riesgo (D/R), las tasas son bajas, por lo que no se recomienda la profilaxis y, en el grupo de pacientes con riesgo intermedio, las tasas descritas en los estudios son variables (40 a 100 %, sin tratamiento), por lo que se proponen los dos tipos de estrategias: la profilaxis universal y el tratamiento anticipado 9. Las dos estrategias son igualmente efectivas en términos de infección y enfermedad 3, pero existen escasos estudios a nivel mundial, y en Colombia no hay ninguno, sobre cuál estrategia ofrece mayores ventajas en términos de costos.
En un metaanálisis de estudios en pacientes con trasplante de órganos sólidos y riesgo intermedio, se reportó que el tratamiento preventivo comparado con el placebo fue efectivo para prevenir la enfermedad por CMV (RR=0,29; IC95%: 0,11-0,80) y no se registraron diferencias al compararlo con la profilaxis universal (RR=0,42; IC95%: 0,07-2,65) 28. En el modelo utilizado en el presente estudio, los pacientes con tratamiento anticipado presentarían mayor número de infecciones comparado con aquellos con profilaxis universal, en tanto que no existirían diferencias en cuanto a los casos de enfermedad.
Si bien la capacidad para disminuir las tasas de infección y de enfermedad ha sido similar con las dos estrategias, preocupa que los eventos adversos, las tasas de resistencia a los antivirales y las infecciones tardías sean mayores con la profilaxis universal que con el tratamiento anticipado. En el metaanálisis citado, no se encontraron diferencias 28.
Al evaluar el tiempo de administración del tratamiento preventivo en el grupo de riesgo intermedio, no se encontró mejoría en la incidencia de la infección y la enfermedad entre una administración de 100 días y una de 200 días; aunque en el estudio IMPACT sí se encontró una diferencia a favor de los 200 días en el grupo de pacientes de alto riesgo 21. Al no existir diferencias aparentes en términos de efectividad, se decidió evaluar si había diferencias en los costos.
El análisis económico evidenció que la profilaxis universal no solo disminuía el riesgo de infecciones, sino que ahorraba costos en comparación con el tratamiento anticipado en pacientes con riesgo intermedio en Colombia. Este resultado se obtuvo en la profilaxis universal con dosis diarias de 450 mg de valganciclovir, y la recomendación es administrarla a pacientes con una tasa de filtración glomerular mayor de 40 ml/minuto, según el consenso colombiano y según el estudio de Kalil, et al. 16,17. Las dosis de 900 mg/día se han asociado con una mayor frecuencia de leucopenia. En el análisis de sensibilidad con una dosis de 900 mg, la profilaxis universal dejó de disminuir costos, aunque seguiría siendo costo-efectiva.
La efectividad del tratamiento anticipado se ha demostrado en condiciones ideales, en las cuales se verifica la carga viral mediante PCR cada semana durante los primeros tres meses y, en el momento en que la carga viral se hace positiva, se inicia la administración del fármaco antiviral. En Colombia resulta difícil llevar a cabo este tratamiento debido a las dificultades logísticas para determinar oportunamente la carga viral y las relacionadas con el suministro oportuno del medicamento al paciente, dado que se requiere autorización por no estar contemplado en el plan de beneficios de salud, lo cual hace que los pacientes permanezcan largos períodos sin profilaxis antiviral, con el consecuente aumento del riesgo de infección o de enfermedad y de los efectos en la morbilidad, la supervivencia del injerto, la supervivencia del paciente y los costos.
Dado que el tratamiento con valganciclovir es costoso, era necesario hacer un análisis de costo-efectividad para determinar cuál de las dos estrategias resultaría más conveniente para los pacientes y para el sistema de salud.
Este es el primer estudio en nuestro medio; se espera que contribuya a la práctica diaria de la atención de los pacientes con trasplante renal, aun que tiene las limitaciones propias de los modelos económicos, incluido el empleo de probabilidades de transición y de utilidades derivadas de estudios foráneos.
Si se aceptan sus supuestos y limitaciones, la recomendación sería utilizar la profilaxis universal con valganciclovir durante 100 días en pacientes con riesgo intermedio para CMV, ya que reduciría tanto los costos como los riesgos clínicos de infección y enfermedad por CMV en pacientes con trasplante renal en Colombia.