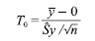En Colombia, la malaria es un problema de salud pública por las complicaciones que produce y las muertes que puede llegar a causar. El 85 % del territorio rural colombiano está situado por debajo de los 1.600 metros sobre el nivel del mar, condición que, sumada a factores climáticos, geográficos y epidemiológicos, favorece la transmisión de la enfermedad. Se estima que, aproximadamente, 25 millones de personas se encuentran en riesgo de enfermar por esta causa 1. Durante los años 2008 a 2010, el índice parasitario anual(IPA) pasó de 6,2 a 11,5 casos por 1.000 habitantes en riesgo 2. En el 2016, se registraron 83.356 casos de malaria no complicada en el Sistema Nacional de Vigilancia en Salud Pública (Sivigila), de los cuales, 47.497 (57 %) correspondieron a infecciones por Plasmodium falciparum, 33.055 (39,7 %) por Plasmodium vivax y 2.804 (3,3 %) por malaria mixta (P. vivax y P. falciparum)3, además de 1.494 casos de malaria complicada.
En el Plan Decenal de Salud Pública, 2012-2021, se proyectó la meta de reducir en 80 % la mortalidad por malaria en todo el país, meta que se ha trabajado de manera progresiva y sostenida, específicamente, fortaleciendo la calidad del diagnóstico de malaria 4, siguiendo las recomendaciones de la Organización Panamericana de la Salud (OPS), con el fin de establecer el ‘Programa de Aseguramiento de la Calidad del Diagnóstico de Malaria (PACDM). Entre las actividades del programa se encuentran: la capacitación, los programas de evaluación (directa e indirecta) del desempeño, la supervisión, la referencia y contrarreferencia, las asesorías y las visitas de asistencia técnica 2,5.
Recientemente, la Organización Mundial de la Salud (OMS) ha impulsado la transición de los programas de control hacia la eliminación, con el fin de lograr una tasa de láminas positivas inferior al 5 % que permite que la carga de la enfermedad se reduzca a un nivel que posibilite un seguimiento individual de cada paciente con malaria 6. En consecuencia, en el año 2012, la OPS, el Instituto Nacional de Salud, la Amazon Malaria Initiative (AMI) y la Red Amazónica de Vigilancia de la Resistencia a los Antimaláricos (RAVREDA) formularon seis líneas de trabajo para el periodo de 2012 a 2015. Una de ellas fue mejorar el acceso y la calidad del diagnóstico.
Con base en esta línea estratégica, se propuso unificar las metodologías de diagnóstico de malaria en la región, según las recomendaciones de la OMS, esto es: elaboración de gota gruesa y extendido en la misma lámina y uso de la coloración de Giemsa 7,8. Sin embargo, en Colombia se ha empleado la coloración modificada de Romanowsky con la metodología de dos gotas gruesas por lámina y un extendido en lámina por separado, obteniéndose históricamente una buena calidad de diagnóstico y resultados satisfactorios en los programas de evaluación del desempeño 4. Por esta razón, se planteó el presente estudio piloto con el objetivo de comparar la metodología propuesta por la OPS 9 y la utilizada en nuestro país para el diagnóstico microscópico del paludismo en Colombia.
El diagnóstico de la enfermedad por laboratorio se puede hacer mediante diferentes métodos, como microscopía, pruebas rápidas y diagnóstico molecular. Por su capacidad diagnóstica y sus ventajas económicas y operativas, el diagnóstico microscópico, es decir, la gota gruesa junto con el extendido, permite la identificación de las especies de Plasmodium spp. que parasitan al humano 10-12.
Empleando la microscopía, la malaria se puede diagnosticar a partir del examen de una muestra de sangre de la persona afectada. Existen dos metodologías para hacer el examen: 1) la gota gruesa, que consiste en depositar dos gotas de sangre (aproximadamente 10 µl por cada una) en una misma lámina y, de esta forma, concentrar varias capas de sangre, y 2) el extendido fino, que consiste en extender una pequeña cantidad de sangre sobre la lámina obteniendo una sola capa de sangre.
La gota gruesa es una muestra concentrada y sin hemoglobina, que permite revisar mayor cantidad de sangre en una pequeña área, lo que la hace más sensible que el extendido. Por su parte, el uso del extendido de sangre se recomienda para la confirmación de especies de Plasmodium ya que permite observar mejor la morfología parasitaria. Ambos tipos de muestra, la gota gruesa y el extendido, se pueden preparar en una misma lámina portaobjetos (gota gruesa combinada); esta es una de las metodologías recomendadas por la OMS, evaluada en el presente estudio: gota gruesa versus gota gruesa combinada. En Colombia, el método recomendado actualmente para el diagnóstico de malaria es el estudio de la gota gruesa y, como herramienta complementaria para confirmar la especie, el extendido 13.
En el diagnóstico de la malaria, la coloración permite identificar las estructuras parasitarias, principalmente el núcleo, el citoplasma y el pigmento malárico. Las coloraciones derivadas de la de Romanowsky son las utilizadas para visualizar este tipo de estructuras, entre las que se incluyen la coloración de Giemsa, la de Wright, la de Field y la modificada de Romanowsky 14. Esta última se utiliza actualmente en los puestos de microscopía de toda Colombia, según la norma nacional vigente, debido a que es una coloración estable y que no absorbe humedad del ambiente, dada su propiedad de solución acuosa que no presenta el problema de evaporación de los componentes alcohólicos, lo que la hace adecuada para los climas tropicales cálidos y húmedos existentes en el país. Por su parte, la OPS recomienda el uso de la coloración de Giemsa, procedimiento operativo estándar reconocido internacionalmente 7, la cual es una tinción de base alcohólica que requiere una serie de cuidados para evitar la evaporación y precipitación del colorante 9.
Materiales y métodos
Se llevó a cabo un estudio piloto de comparación de metodologías para el diagnóstico de malaria mediante examen por microscopía, con un ensayo controlado, en el cual intervienen variables como la metodología del diagnóstico, la coloración y el recuento parasitario.
Se evaluaron dos métodos distintos de diagnóstico, la gota gruesa y la gota gruesa combinada (una gota gruesa y un extendido por lámina); dos coloraciones, la modificada de Romanowsky y la de Giemsa, y cuatro recuentos parasitarios que, para facilitar el manejo de los datos, se tomaron como valores absolutos de 500 (rango de 300 a 662), 1.000 (rango de 888 a 1.136), 5.000 (rango de 3.815 a 7.636) y 10.000 (rango de 8.528 a 14.117) parásitos por µl de sangre. Los tratamientos de comparación fueron 16; para calcular el promedio y la desviación estándar de las medidas y que el diseño fuera sensible a la variabilidad, cada uno de estos 16 tratamientos se replicó tres veces, para un total de 48 muestras, por lo menos.
En tubos con EDTA, se recolectaron muestras venosas de siete pacientes con malaria por P. falciparum, P. vivax o infección mixta, del municipio de Tadó en el departamento del Chocó.
Se cumplió con lo establecido en el Artículo 11 del Capítulo 1 de la Resolución Nº 008430 de 1993, en la cual se establecen las normas académicas, técnicas y administrativas para la investigación en salud; además, se obtuvo el consentimiento informado de todos los participantes.
A partir de estas muestras, se prepararon 88 láminas en el Laboratorio del Hospital San José de Tadó, en condiciones de campo y teniendo en cuenta las condiciones ambientales de humedad y temperatura y su acción sobre los colorantes. Respecto al recuento parasitario y para efectos del estudio, fue necesario hacer diluciones con sangre del grupo sanguíneo O y con factor Rh positivo de un voluntario, a partir de las parasitemias iniciales de los pacientes y, así, obtener los niveles de recuento parasitario (parásitos/µl) propuestos para cada tratamiento. Las parasitemias iniciales de los siete pacientes incluidos oscilaban entre 1.073 y 26.093 parásitos/ul de sangre, de las especies de P. vivax, P. falciparum e infecciones mixtas. A partir de esas parasitemias iniciales, se hicieron las diluciones para obtener concentraciones parasitarias de 500, 1.000, 5.000 y 10.000 parásitos/ul de sangre, y se procedió a preparar las gotas gruesas y las gotas gruesas combinadas con las dos coloraciones empleadas.
Las láminas de gota gruesa se colorearon con la tinción modificada de Romanowsky, según las normas nacionales (sin hemoglobina y coloración) y, con la tinción de Giemsa, siguiendo las recomendaciones de la OPS (no se hizo una precoloración de la gota gruesa). Para las de metodología combinada, el extendido se fijó con metanol y las gotas gruesas se colorearon según las normas nacionales (sin hemoglobina y coloración). Se obtuvieron los siguientes tratamientos o arreglos factoriales: 28 láminas con 500 parásitos por µl de sangre, 28 con 1.000, 20 con 5.000 y 12 con 10.000; todas las láminas con metodología de gota gruesa y con metodología combinada, fueron coloreadas con la tinción de Giemsa y con la modificada de Romanowsky. El extendido fue revisado para confirmar la especie parasitaria. La distribución de muestras por tratamiento se muestra en el cuadro 1.
Cuadro 1 Distribución de láminas por tratamiento de investigación
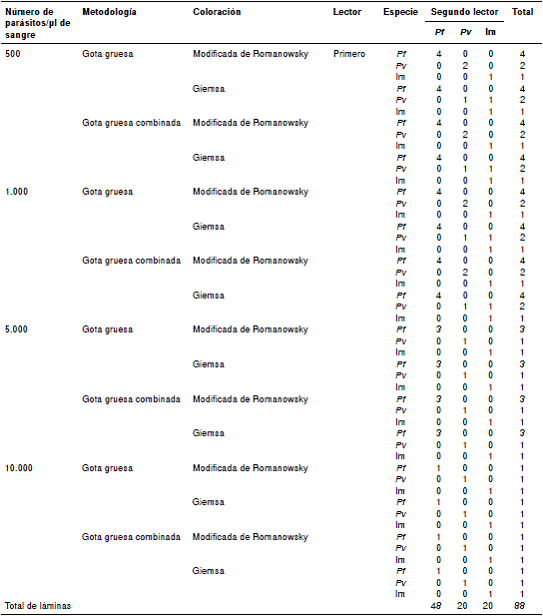
Pf: Plasmodium falciparum; Pv: Plasmodium vivax; Im: infección mixta
Las láminas se codificaron para su lectura a ciegas, con el fin de evitar sesgos en los resultados. La lectura la hicieron dos profesionales entrenados con experiencia en el diagnóstico de malaria, uno de ellos certificado como microscopista para el diagnóstico de malaria por la OPS y con experiencia en el desarrollo de evaluaciones del desempeño de malaria a nivel nacional. De manera ciega, se hizo la lectura microscópica para identificar la especie y hacer el conteo parasitario. Las láminas discordantes fueron revisadas por un tercer lector experto. Los resultados fueron consolidados en una base de datos, para hacer los análisis estadísticos.
Análisis estadístico
El análisis del estudio comprendió tres etapas: concordancia entre observadores, con el fin de establecer la concordancia de los dos observadores en el diagnóstico de la especie parasitaria; prueba de hipótesis de comparación de dos muestras, para establecer las diferencias en los recuentos parasitarios de los dos observadores, y análisis de varianzas (ANOVA) a dos factores, tomando como variable de respuesta el recuento parasitario.
1. Concordancia entre observadores. Se evaluó la precisión de dos microscopistas para identificar las especies parasitarias de cada una de las muestras. El grado de concordancia se midió con el índice kappa de Cohen, con un nivel de confianza del 95 % e intervalos de confianza definidos, el cual corresponde a la proporción de concordancias observadas sobre el total de observaciones, habiendo excluido las concordancias atribuibles al azar 15.
El coeficiente kappa (κ) toma valores entre 0 y 1; mientras más cercano a 1, mayor es el grado de concordancia entre observadores. Por el contrario, un valor deκ=0 refleja que la concordancia observada es precisamente la que se espera a causa, exclusivamente, del azar. La escala de interpretación usada para el índice kappa, según Landis y Koch, es la siguiente: concordancia pobre, 0,00; leve, entre 0,01 y 0,20; aceptable, entre 0,21 y 0,40; moderada, entre 0,41 y 0,60; considerable, entre 0,61 y 0,80, y casi perfecta, entre 0,81 y 1,00 16
Se calculó el índice kappa para valorar el acuerdo de los dos lectores, indistintamente de los tratamientos factoriales donde se presentara la valoración, con el fin de garantizar que los profesionales de laboratorio tenían las competencias para desarrollar el proceso posterior del experimento.
Se plantearon las siguientes hipótesis, bajo un nivel de significación del 5 %:
H0: no existe concordancia en la especie parasitaria entre los observadores.
H1: existe concordancia en la especie parasitaria entre los dos observadores.
2. Prueba de hipótesis de comparación de dos muestras. Su objetivo fue comprobar si los conteos de cada uno de los dos microscopistas eran significativamente diferentes, partiendo del hecho de que las condiciones de estudio eran dependientes, pues se estaba midiendo la misma muestra dos veces, lo que sugiere una prueba de hipótesis de diferencia de medias pareadas. Por tanto, se plantearon las siguientes hipótesis:
H0: no existe una diferencia significativa en el recuento de las dos muestras provenientes de las poblaciones de estudio.
H1: existe una diferencia significativa entre las dos muestras.
El valor estadístico de contraste fue:
Para los recuentos parasitarios no se cumplen los supuestos de normalidad ni de homocedasticidad. Además, se identificaron algunos valores atípicos (outliers) que afectan los cálculos estadísticos, por lo que se debieron usar pruebas no paramétricas de comparación de dos muestras por medio de la diferencia de medianas, la U de Mann-Whitney (prueba de suma de rangos de Wilcoxon) 17.
Por medio de esta prueba, se planteó el siguiente juego de hipótesis para evaluar si las medianas entre estas dos muestras eran iguales o diferentes:
H0: no existe una diferencia significativa entre las medianas de los recuentos parasitarios de los dos observadores.
H1: existe una diferencia significativa entre estas medianas.
3. Análisis de varianzas (ANOVA). Se desarrollaron pruebas de comparación múltiple en términos de los recuentos parasitarios. Existen dos factores asociados a este estudio: la metodología de elaboración (GG: gota gruesa; GG combinada: gota gruesa más extendido) y el método de coloración(F: modificado de Romanowsky; G: Giemsa), con una segmentación de los grupos de estudio de interés, que son los recuentos parasitarios (500, 1.000, 5.000 y 10.000 parásitos/µl). Se hizo la comparación para establecer si era más factible la visualización de los parásitos en casos de bajas parasitemias, teniendo una o dos gotas gruesas para examinar.
Con base en lo anterior, se llevó a cabo un análisis de varianza a dos vías para todas las posibles comparaciones de coloración con las dos metodologías usadas (gota gruesa y gota gruesa más extendido), según la coloración (modificada de Romanowsky y Giemsa).
Para el análisis multivariado ANOVA de dos factores, y tomando como variable de respuesta el recuento parasitario, se hicieron los respectivos cálculos para todas las posibles comparaciones de coloración con los dos métodos usados, según la coloración y la variable del resultado del conteo parasitario.
Resultados
Se analizaron 88 láminas así: 28 láminas con recuento de500 parásitos por µl de sangre, 28 con 1.000, 20 con 5.000, y 12 con 10.000.
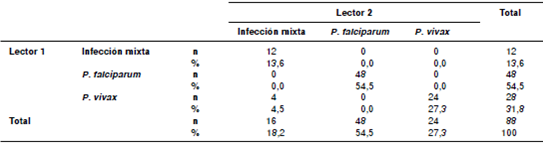
Con el coeficiente kappa de Cohen, la concordancia entre observadores fue de 0,923 (IC95% 0,768-1,000), la cual se interpreta como una concordancia casi perfecta para identificar la especie. Hubo concordancias entre el observador 1 y el observador 2 en, al menos, el 95 % de los casos, lo cual indica una buena concordancia entre evaluadores (cuadro 2). Se presentaron cuatro casos de discordancia en especie, en los cuales el lector 1 diagnosticó erróneamente P. vivax mientras el lector 2 diagnosticó infección mixta (cuadro 1).
Al analizar los casos discordantes por grupos de láminas según el conteo parasitario, se observó que los desacuerdos se presentaron en cuatro tratamientos distintos, cuyas principales características eran el uso del colorante de Giemsa y un conteo parasitario de 500 y 1.000 por µl, independientemente del tipo de metodología empleada, pues ocurrieron tanto en gota gruesa como gota gruesa combinada.
Se pudo establecer que los conteos no se distribuían en forma normal, por lo que se eligió la prueba no paramétrica de comparación de dos muestras por medio de la diferencia de medianas con la prueba U de Mann-Whitney.
No se encontraron diferencias estadísticamente significativas entre las medianas de las parasitemias (p=0,594).
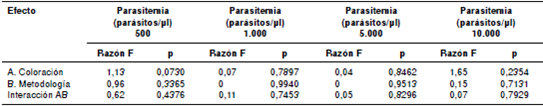
Para todos los conteos parasitarios se observó que, como ningún valor de p fue menor de 0,05, ninguno de los factores (A, coloración, o B, metodología) o sus interacciones (AB) tuvo un efecto estadísticamente significativo sobre las láminas, con un 95,0 % de nivel de confianza (cuadro 3).
Discusión
Al establecer el grado de concordancia entre observadores para identificar la especie parasitaria, se obtuvo un coeficiente kappa de 0,923 (IC95% 0,768-1,0) que permite confirmar que existe concordancia casi perfecta entre los dos observadores.
La variación del observador está relacionada con su entrenamiento, formación y capacidad. Esta variación puede ser del observador (respecto de sí mismo) respecto de un estándar (prueba estándar) o entre observadores, y se puede medir por medio de la concordancia alcanzada al examinar y clasificar una serie de elementos. Dicho valor estuvo influenciado por cuatro discordancias de especie entre los observadores, en las cuales el lector 1 diagnosticó erróneamente los cuatro casos como P. vivax, mientras el observador 2 los consideró positivos para infección mixta, siendo este último el diagnóstico real.
Llama la atención que estos casos se presentaron en el tratamiento de láminas coloreadas con Giemsa y con un conteo parasitario de 500 y 1.000 por µl (cuadro 1). Esta discordancia pudo deberse a la presencia de precipitado y acidez en las láminas coloreadas con Giemsa, evidenciada durante la lectura por parte por los microscopistas. Este aspecto, sumado a la baja parasitemia presente en la muestra, pudo ocasionar una mayor dificultad para observar los estadios asexuados de P. falciparum, lo cual dificulta el diagnóstico de infección mixta 18.
Respecto al factor de la coloración, es importante destacar los hallazgos de diversos estudios en los cuales se menciona la poca sensibilidad del diagnóstico microscópico empleando la coloración de Giemsa en casos de escasa parasitemia (100, 500 y 1.000 parásitos/µl) 19,20, lo que no sucedió en este estudio piloto. Sin embargo, es importante tener en cuenta que la coloración puede influir en forma negativa en la identificación parasitaria cuando la parasitemia es escasa, por lo cual se sugiere seguir empleando la metodología estandarizada y utilizada desde hace más de 15 años, y recomendada a nivel nacional, hasta que se hagan estudios más sólidos que justifiquen el cambio a la metodología recomendada por la OPS; debe aclararse que no existe falta de estandarización de la técnica de lectura entre observadores, lo que se evidencia en la experiencia de más de 10 años en la lectura de láminas de malaria y en los resultados de concordancia entre observadores de 0,923 (IC95% 0,768-1,0).
Los resultados de este estudio piloto permiten concluir, en términos de significancia estadística, que las dos coloraciones evaluadas son adecuadas para el diagnóstico de malaria. Sin embargo, el análisis permite concluir técnicamente que la coloración acuosa modificada de Romanowsky, usada de manera rutinaria en Colombia desde los años 90, demuestra un buen desempeño en la actividad diagnóstica de la enfermedad.
Al momento de establecer la coloración modificada de Romanowsky como recomendación nacional, se destacan los aspectos técnicos adecuados de coloración, como pH y ausencia de hemoglobina, así como ausencia de contaminación y precipitados de colorante. Por otra parte, algunos aspectos que se deben tener en cuenta para garantizar el buen funcionamiento y calidad de la coloración de Giemsa, son evitar la evaporación, la oxidación por humedad elevada y la agitación del colorante, ya que los precipitados asentados en el fondo del envase pueden desmejorar la calidad de la tinción y ocultar detalles importantes durante el examen microscópico 7.
Además, en la técnica de coloración de Giemsa sugerida por la OPS, no se utiliza el procedimiento de precoloración de Walker, lo que disminuye el contraste de colores de los parásitos y la homogeneidad del fondo de la gota gruesa 21, ya que el azul de metileno fosfatado, no solo contribuye a la lisis de los glóbulos rojos, sino que mejora el contraste de los colores y la uniformidad del fondo de lectura de la gota gruesa.
Por otro lado, como los sitios de diagnóstico de malaria se localizan principalmente en zonas rurales, de difícil acceso y bajo las condiciones óptimas de humedad relativa (60 %) y temperatura (20 a 30 °C) para la transmisión de la enfermedad 5,8, se dificulta garantizar las condiciones ideales para la coloración de Giemsa sugerida a nivel internacional. Además, en las zonas endémicas para la enfermedad, el diagnóstico lo hacen voluntarios, líderes comunitarios o personal técnico, y no profesionales, situación que supone mayores esfuerzos para mantenerlos capacitados y actualizados 5.
Otro aspecto es que la tinción modificada de Romanowsky requiere una fase previa con el método de Walker, el cual complementa la pérdida de la hemoglobina y proporciona un fondo blanco y claro que facilita la diferenciación de la especie de Plasmodium, pues permite observar los colores y formas características del parásito en muestras con un bajo conteo parasitario. Por ende, mejora la observación microscópica de las láminas coloreadas, en comparación con la técnica clásica de Giemsa 21. Las coloraciones acuosas, como la de Field y la modificada de Romanowsky, resultan más eficientes en lugares cálidos ya que no absorben la humedad del ambiente, como sí lo hacen la coloración de Giemsa y la de Wright (alcohólicas). Además, gracias a su sencillez y rapidez, la coloración modificada de Romanowsky es la elegida por los laboratorios de los hospitales tropicales que analizan gran número de muestras 22.
En este estudio, no se observaron diferencias estadísticamente significativas entre las metodologías evaluadas para preparar las láminas. Sin embargo, teniendo en cuenta los aspectos técnicos y operativos, se considera que la gota gruesa conformada por dos gotas de sangre en una lámina, en forma independiente del extendido, sigue siendo la metodología apropiada para las condiciones de los puestos de diagnóstico en Colombia, porque es sencilla, económica y rápida.
Bajo condiciones óptimas, la sensibilidad de la gota gruesa es superior al 95 %, con una detección de 10 a 30 parásitos por µl de sangre, lo que equivale, aproximadamente, a 0,001 % de los glóbulos rojos infectados 23,24. Además, en la gota gruesa se concentra aproximadamente 20 a 30 veces el número de capas de glóbulos rojos, y se considera, al menos, 15 veces más sensible que el extendido; esto es así en virtud de la mayor cantidad de sangre por área examinada y porque, estando los parásitos libres, es posible visualizar más parásitos por área que en la misma muestra examinada mediante extendido.
Por su lado, el extendido de sangre periférica se prepara con un volumen menor de sangre que la gota gruesa, y se utiliza principalmente para determinar la especie infectiva de Plasmodium o cuando hay dudas sobre las especies, lo cual hace del extendido delgado una prueba más específica 25.
La idea de unir ambas metodologías en una sola lámina, gota gruesa más extendido, podría disminuir la sensibilidad del diagnóstico pues solo se contaría con una gota concentrada de sangre y no permitiría observar los 500 campos microscópicos, lo cual es un criterio internacional de la OPS para considerar una lámina negativa para parásitos 18.
Por último, entre las limitaciones del presente estudio piloto está el número limitado de muestras. Por esta razón, se sugiere ampliar la investigación teniendo en cuenta otros aspectos, como el costo-efectividad, la logística de distribución, las condiciones ambientales y los aspectos técnicos, con el fin de reunir evidencia para que la OMS/OPS considere ampliar los criterios sobre las metodologías de preparación de láminas y el uso de diversas coloraciones derivadas de la de Romanowsky para gotas gruesas y extendidos, teniendo en cuenta los aquí sugeridos. Además, se quiso determinar si era factible visualizar los parásitos en casos de baja parasitemia, teniendo una o dos gotas gruesas para examinar.
Por lo anterior, y considerando que las bajas parasitemias son de gran interés debido a que cada vez son más frecuentes, sobre todo a medida que la incidencia de la enfermedad disminuye, se sugiere emplear parasitemias desde 16 parásitos por µl de sangre.