Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.12 no.1 Bogotá Jan./June 2007
PÉRDIDA DE TEXTURA post mortem DE LA CARNE DE PESCADO DURANTE EL ALMACENAMIENTO EN FRÍO
Post Mortem Lost of Texture of Fish Meat During Cold Storage
HÉCTOR SUÁREZ MAHECHA1, Ph. D.; ALICIA DE FRANCISCO2, Ph. D.; LUIZ HENRIQUE BEIRÃO2, Ph. D.; SANDRA PARDO CARRASCO3, Ph. D.; MISAEL CORTÉS RODRÍGUEZ1, Ph. D. 1Departamento de Ingeniería Agrícola y Alimentos. Facultad de Ciencias Agropecuarias, Universidad Nacional de Colombia, Sede Medellín. Calle 59A No.63020, bloque 14, oficina 400. Medellín, Antioquia, Colombia. hsuarezm@unal.edu.co 2Departamento de Ciencia e Tecnología de Alimentos. Centro de Ciencias Agrarias. Universidade Federal de Santa Catarina, Santa Catarina SC. Brasil. 3Departamento de Ciencias Acuícolas. Facultad de Medicina Veterinaria y Zootecnia, Universidad de Córdoba, Montería, Córdoba, Colombia.
Presentado 5 de octubre 2006, aceptado 29 de enero 2007, correcciones 26 de febrero de 2007.
RESUMEN
Este trabajo es una revisión sobre la conformación e importancia del tejido conectivo de la carne de los peces. El ablandamiento post mortem en los peces es un factor de calidad directamente influenciado por las características de los colágenos presentes en cada especie. La degradación del colágeno está relacionada con los fenómenos que acontecen durante el almacenamiento en frío o congelamiento. Varias investigaciones han demostrado a través de análisis bioquímicos y, principalmente, a través de microscopia electrónica de barrido y transmisión, que la pérdida de la textura en la carne de los peces es uno de los efectos ocasionados por la degradación del tejido conectivo pericelular y no por el tejido conectivo intersticial. En la actualidad son propuestas algunas prácticas postcosecha para disminuir este fenómeno.
Palabras clave: peces, post mortem, textura, colágeno.
ABSTRACT
This work is a review on the conformation and importance of connective tissue of fish meat. The post mortem softening of fish meat as a quality factor is influenced by the characteristics of the collagens present in each species. The degradation of collagen appears to be related to freezing. By biochemical analysis as well as electronic microscopy many researches have demonstrated that the loss of texture is related to pericelular connective tissue degradation. Currently some post crop practices are proposed to reduce this phenomenon.
Key words: fish, softening, storage, texture, collagen.
INTRODUCCIÓN
La firmeza es un factor muy importante para evaluar la calidad de la carne de pescado y fundamental al momento de comercializarla. Algunos estudios demuestran que, con cierta frecuencia, la carne de pescado ablanda después de 24 horas de almacenamiento en frío (Toyohara y Shimizu, 1988; Oka et al., 1990; Mochizuki y Sato, 1996). La mayor parte de estos trabajos han sido realizados principalmente en peces marinos para estudiar la causa del ablandamiento post mortem de su carne, pero poco ha sido realizado en especies de agua dulce, siendo algunos en carpa (Cyprinus carpio) y trucha (Oncorhynchus mykiss, Salmo irideus; Ma y Yamanaka, 1991; Ando et al., 1999). Algunos autores hacen referencia a la pérdida de textura ocasionada por la acción de proteasas sobre proteínas miofibrilares, en especial catepsinas, calpaínas y enzimas hidrolíticas como elastasas y colagenasas (DelbarreLadrat, 2006). Aunque ha sido reconocido que el efecto de las proteasas es posterior e independiente a la pérdida inicial de textura en algunos peces sometidos a refrigeración (Ladrat et al., 2003; Shigemura et al., 2003).
El colágeno es el mayor constituyente del tejido conectivo intramuscular de los peces ejerciendo una importante función en la textura de su carne (Sato et al., 1986; Hatae et al., 1986). Por otro lado, diferentes trabajos ultraestructurales han demostrado que el tejido conectivo pericelular es degradado más intensamente durante el almacenamiento en frío que el tejido conectivo intersticial (Bremner y Hallett, 1985, 1986; Hallett y Bremner 1988; Ando et al., 1991; Ando et al., 1995; Kubota et al., 1996). Además, estos estudios relacionan el ablandamiento de la carne con la presencia de algunos tipos de colágeno existentes en los peces, especialmente el colágeno tipo V, en cuanto otros relacionan este hecho con la presencia de colágenos que difieren genética y químicamente entre individuos de la misma especie (Bornstein y Sage, 1980). La firmeza del músculo es también un índice de frescura de la carne, de forma que el ablandamiento resulta en una disminución de la calidad. Es entonces importante entender los mecanismos que provocan este fenómeno para proponer y desarrollar métodos que, usados en la piscicultura, sean capaces de prevenir este proceso de pérdida de textura con la consecuente calidad de la carne. En este sentido, algunos trabajos se refieren a este fenómeno y vienen siendo realizados en especies cultivadas (Hatae et al., 1989; Tachibana et al., 1993; Ando et al., 1999). Con el propósito de tornar el tema sobre el ablandamiento de la carne de los peces más claro, se describirá inicialmente el tejido conectivo, su función con relevancia al colágeno, y finalmente se relatarán los resultados obtenidos en las principales investigaciones realizadas en esta área, así como algunas alternativas para la solución de este problema.
MORFOLOGÍA DEL TEJIDO MUSCULAR EN EL PESCADO
La carne de los peces teleósteos está formada por bloques musculares adyacentes, denominados miótomos y separados uno del otro por láminas de colágeno denominadas miocomata (Nurshall, 1956). Los miótomos de los dos lados del esqueleto axial forman una W y corren a lo largo del cuerpo formando series seguidas de W. Dentro de cada miótomo, las fibras musculares (miómeros) corren de forma paralela formando ángulos que favorecen los movimientos necesarios durante el nado. El miocomata está conectado internamente a la piel y al sistema esquelético, unido a la membrana que divide el pescado en región epiaxial e hipoaxial a través de un septum medio vertical, como se puede observar en la figura 1. La unión entre miómero y miocomata es realizada por el colágeno, el cual tiene su origen en el miocomata y envuelve cada fibra muscular (Love et al., 1969; Love et al., 1972).
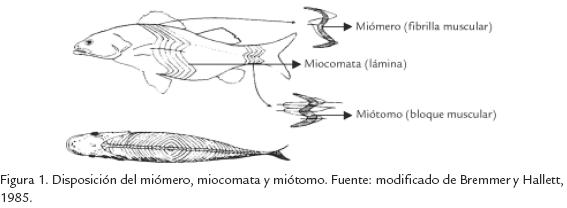
La microscopia ha sido ampliamente utilizada para el estudio del músculo de peces, especialmente la microscopia electrónica de transmisión (TEM) para determinar las fibras musculares (Jarenbäck y Liljemark, 1975). Sin embargo, a pesar de la importancia de la relación entre miómero/miocomata en el cuerpo de los peces in vivo y post mortem, pocos son los estudios en esta área. Una razón para esta situación podría ser la dificultad en la preparación de las muestras. Además, existen algunas diferencias entre la organización de las fibras musculares en peces y animales terrestres. En estos, los músculos terminan en tendones que unen al esqueleto, pero la microestructura puede ser similar. Por esta razón, diversos autores utilizan para peces, terminología aplicada a músculos de mamíferos, como por ejemplo, plasmalema (sarcolema) aplicada a la membrana celular de la fibra muscular de peces, lámina basal (membrana basal) que une las fibras de colágeno (reticular) al endomisio, protegido por el perimisio. En peces, la lámina basal es contigua al miocomata (Bremmer y Hallett, 1985).
EL TEJIDO CONECTIVO FIBROSO
El tejido conectivo mantiene y soporta los músculos a través de los tendones, epimisio y endomisio y es formado por varias fibras, diversos tipos de células y por una sustancia fundamental amorfa la cual es una mezcla que presenta estructura definida, formada por carbohidratos, proteínas y lípidos. Cierta cantidad de esta mezcla envuelve la célula formando parte del sarcolema. El sarcolema que envuelve la fibra muscular está ligado al tejido conjuntivo mediante una capa de sustancia intersticial constituida por glucosilaminoglicanos envuelto por finas fibras de colágeno. Este conjunto constituye el endomisio (Lindent y Lorient, 1996).
En el tejido conectivo existen diversos tipos de células: fibroblastos, células mesenquimatosas, macrófagos, células linfoides, células cebadas y células eosinófilas. Este tejido envuelve el músculo a través de una membrana que une el colágeno de los tendones que se insertan en el músculo (miocomatamiomero). Los constituyentes proteicos principales de los tendones son el colágeno y la elastina, siendo que la mayor parte del tejido conjuntivo está constituido por colágeno (70 a 80% materia seca) (Cheftel et al., 1989). Según Cheftel et al. (1989); Lindent y Lorient (1996) y Ando et al. (1999) estas son algunas características identificadas en el sistema muscular de los peces:
El contenido del tejido conectivo muscular es menor y las proteínas del estroma representan 310% de las proteínas totales. Las fibras musculares son cortas, con algunos centímetros de longitud y organizadas en láminas (miótomos).
La miosina, que representa 40% de las proteínas totales, es difícilmente separable de la actina (20%). Esta proteína es más sensible a la desnaturalización (calorseco) y a la proteólisis que la miosina de los mamíferos.
La rigidez cadavérica y la maduración son fenómenos relativamente rápidos en los peces. La disminución post mortem del pH es menor, de 7 a 6,56,2 dando al pescado una mayor inestabilidad microbiológica.
La temperatura de gelatinización del colágeno en el pescado es una decena de grados inferior a la de la carne. El diámetro de la fibra del colágeno es mayor en peces pelágicos y menor en demersales.
EL COLÁGENO
El colágeno es una proteína fibrosa, la fracción principal del tejido conectivo y contribuye con la firmeza y dureza de la carne. Es abundante en los tendones, miocomata, piel, huesos, sistema vascular y en las envolturas del tejido conectivo que rodean el músculo. La unidad estructural del colágeno es el tropocolágeno, una proteína en forma de varilla (15 Å de diámetro y 3.000 Å de longitud) formada por tres cadenas polipeptídicas llamadas cadenas α (alfa) súper envueltas en una triple hélice. Cada cadena α forma una hélice con giro a la izquierda con tres aminoácidos por vuelta. El entorchamiento de las tres cadenas forma triple hélice presentando giro a la derecha. Las cadenas polipeptídicas de las unidades del tropocolágeno están unidas por medio de enlaces cruzados covalentes, donde participan cadenas laterales de lisina e histidina. Los enlaces cruzados, son reducibles y durante la maduración del tejido conectivo van siendo gradualmente substituidos por enlaces no reducibles (Belitz y Gorsch, 1988). En animales más viejos, como por ejemplo los mamíferos, este tipo de enlaces cruzados no reducibles, son responsables de la dureza de la carne. Las cadenas α contienen 100 tipos de restos de aminoácidos, siendo su composición variada. Esta diversidad en la composición de los aminoácidos de las cadenas α es la causa de la existencia de los cinco tipos principales de colágeno (Tabla 1).
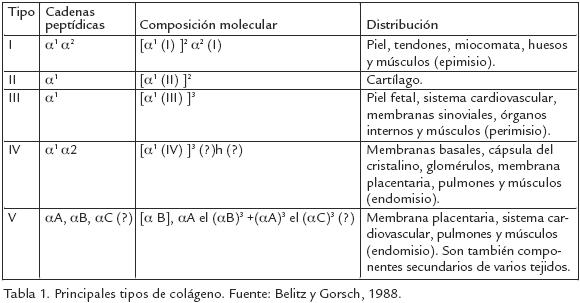
Tipos de colágeno. El colágeno existe en diversas formas polimorfas. El tipo más común es conocido como colágeno tipo I, el cual está formado por tres cadenas polipeptídicas; dos de ellas denominadas α1, idénticas y unidas entre sí por puentes de hidrógeno, la tercera cadena α2, posee una secuencia de aminoácidos diferente. Cada cadena tiene peso molecular de 100.000 daltons, dando un peso molecular total de 300.000 daltons para el colágeno (Lindent y Lorient, 1996). Otro tipo de colágeno encontrado en el músculo, que parece ejercer un papel importante en su dureza, es el tipo lll y está formado por tres cadenas α idénticas denominadas α1 (lll). Este tipo de colágeno posee enlaces disulfuro intramoleculares en el péptido en el helicoidal carboxiterminal. Otra clase de molécula de colágeno, conocida como tipo lV, es más compleja y parece encontrarse formada por cadenas polipeptídicas de tamaños diferentes. La composición del colágeno de tipo V aún no está muy clara y parece presentar más de un tipo de conformación molecular. Este tipo de colágeno se encuentra en peces. El colágeno es un grupo de moléculas similares, sin embargo sus componentes aún no han sido completamente identificados. En algunos casos, las cadenas de péptidos que constituyen el colágeno están unidas mediante enlaces covalentes cruzados. Cuando dos péptidos se unen de esta manera, se denomina componente, β y cuando los tres están unidos, el producto es conocido como componente γ. La solubilidad del colágeno disminuye a medida que aumentan los enlaces cruzados intermoleculares. Según Ando et al. (1999), el colágeno presente en el músculo de los peces está formado por los tipos I y V, y contiene fibras heterotípicas. La alta proporción en fibras del tipo V resulta en la formación de fibras delgadas, hecho mostrado a través del estudio del diámetro de la fibra de colágeno en peces pelágicos, siendo de 20,6 Å incluyendo mayor cantidad de fibras de colágeno del tipo V. Situación también presente en matrinxã (Brycon cephalus; Suárez Mahecha 2002) Este tipo de colágeno tiene tendencia a degradarse durante el almacenamiento, tornando la carne blanda en el período post mortem. Para peces demersales, el diámetro de la fibra de colágeno se encuentra en valores alrededor de 26 Å.
Composición de aminoácidos del colágeno. En general, los aminoácidos encontrados en el colágeno se caracterizan por la elevada riqueza en glicina (33%), prolina (12%) y alanina (11%) y por contener dos aminoácidos poco frecuentes en las demás proteínas, hidroxiprolina (12%) e hidroxilisina (1%). En las cadenas polipeptídicas del colágeno son producidas dos oxidaciones importantes: la conversión de prolina en hidroxiprolina y la conversión de lisina en hidroxilisina. Los sistemas enzimáticos utilizan oxígeno molecular, a cetoglutarato, ión ferroso y una sustancia reductora, como el ascorbato. Este último favorece la cicatrización de las heridas debido al papel en la síntesis del colágeno y en su deficiencia. En la deficiencia de ácido ascórbico, los mucopolisacáridos de la sustancia basal de la célula presentan un carácter anormal y existen cambios significativos en la naturaleza de las fibrillas de colágeno que son formadas. A nivel enzimático existe un indicio de que el ácido ascórbico está envuelto en la conversión de prolina a hidroxiprolina, funcionando como agente reductor (Coon, 1980).
En los mamíferos, con el pasar de los años, los enlaces cruzados de colágeno cambian de una forma reducible a otra no reducible, más estable. La naturaleza de este enlace cruzado no reducible es desconocida, aunque existen diversas hipótesis. Ese aumento de enlaces cruzados de colágeno que aumenta con la edad, puede explicar parcialmente por qué la carne de animales viejos (mamíferos) es más dura que la carne de animales jóvenes, aunque los músculos de los animales jóvenes generalmente contienen más colágeno. En peces esta situación es muy diferente. El colágeno de los miocomata de los peces más viejos es más débil y tiene menos enlaces cruzados que aquel de peces jóvenes. Por otro lado, peces más viejos tienen más colágeno (presencia de miocomata más espeso) que peces más jóvenes (Love, et al., 1972; Love, 1992). A medida que los enlaces cruzados de colágeno se van formando, la solubilidad, en diversos solventes, como soluciones salinas y ácidas, va disminuyendo, mientras la cantidad de colágeno insoluble aumenta en los mamíferos, con el pasar de la edad. En peces, como por ejemplo el bacalao, permanece casi inalterado. En tanto el colágeno soluble, aumenta claramente en peces. En este sentido, los peces sometidos a una subalimentación prolongada producen más colágeno con enlaces cruzados que peces bien alimentados (Fenema, 1993).
Con relación a la proteólisis enzimática, según Coon (1980) la mayoría de las enzimas proteolíticas tienen baja actividad en el colágeno nativo, además, degradan fácilmente el colágeno desnaturalizado. Se han identificado colagenasas en diversos tejidos animales, sin embargo, es difícil detectar su presencia debido al hecho de exhibir una escasa actividad, por los mecanismos de control que opera en los tejidos. La mayoría de las colagenasas animales hidrolizan un solo enlace en cada una de las tres cadenas de la molécula de colágeno. Diversos microorganismos, especialmente Clostridium, producen colagenasas. Estas enzimas difieren de las colagenasas animales porque degradan extensamente el colágeno. Las proteínasas no colagenasas pueden hidrolizar la molécula del colágeno en la región telopeptídica. Se desconoce la importancia de las colagenasas para la degradación del colágeno in situ, aunque estas pueden tener cierta importancia en el almacenamiento post mortem.
FACTORES QUE AFECTAN LA TEXTURA DEL PESCADO
PECES DE CULTIVO Y AMBIENTE NATURAL
Otro aspecto importante que debe ser tenido en cuenta es la procedencia de los peces, dado que pueden presentar diferencias en las propiedades físicas de la carne (Alasalvar et al., 2001; Alasalvar et al., 2002). Sobre la textura de la carne en peces marinos cultivados y de ambiente natural, Hatae et al. (1989) comparó la firmeza de la carne de la misma especie cultivada y de ambiente natural. Los valores para firmeza se encontraron de forma decreciente para yellowtai (Seriola quinqueradiata), red sea bream (Pagrus major) y finalmente flounder (Paralinchthys olivaceus). Cuando la carne fue cocida, pequeñas diferencias fueron encontradas para yellowtail y red sea bream, sin embargo, para flounder se encontraron diferencias significativas en favor de los peces de ambiente natural. Tachibana et al. (1993), a través del análisis de la microestructura y citoquímica del músculo del pescado red sea bream (Pagrus major) de ambiente natural y de cultivo, mostraron como la degeneración de la línea Z durante el primer día de almacenamiento en hielo es iniciada en los peces de cultivo. En los peces de ambiente natural, la línea Z presentó continuidad durante los tres días de almacenamiento. Por otra parte, Kumano y Seki (1993) estudiaron el α conectina, filamentos que unen el disco Z con los filamentos gruesos (miosina) en peces de cultivo como carpa (Cyprinus carpio), trucha arco iris (Oncorhynchus mykiss) y flatfish (Paralinchthys olivaceus) y de ambiente natural como stone flounder (Kareius bicoloratus), almacenados en hielo, congelados y descongelados. Estos autores sugieren que existen otros factores que causan un fuerte ablandamiento del músculo descongelado en adición a la desintegración del α conectina. Estos factores podrían ser responsables de la desintegración estructural del músculo, afectando en diferentes intensidades a cada especie. Resultados similares fueron encontrados por Kubota et al. (1996), aunque no se comprobó correlación entre el ablandamiento de la carne de peces de cultivo como carpa (Cyprinus carpio), tiger puffer (Fugu rubripes), trucha (Oncorhynchus mykiss) con peces de ambiente natural red sea bream (Pagrus major), flounder (Paralichthys olivaceus) y sardina (Sardinops melanostica), así como cambios en αconectina durante un día de refrigeración a 5 °C. Respecto a los cambios ocurridos en el tejido conectivo como efecto de períodos prolongados de inanición, Bugeon et al. (2004) sometieron a la trucha (Salmo trutta) a un período de dos meses de ayuno. En estos peces se encontró disminución del contenido de materia seca y aumento del pH post mortem a nivel muscular. La estructura muscular presentó disminución de la fibra muscular y mayor contenido de tejido conectivo en miocomata. Después de un mes de alimentación no fueron observadas diferencias. Las características del tejido conectivo fueron significativamente afectadas por el período de ayuno donde se determinó aumento del peso molecular del colágeno y de la temperatura de galatinización de la piel. Estas diferencias permanecieron constantes después del período de alimentación, sin embargo las pruebas reológicas no mostraron diferencia.
EFECTO DEL MÉTODO DE SACRIFICIO
Los métodos de sacrificio también han sido estudiados, porque existían dudas sobre la influencia en la textura de la carne. Azam et al. (1989) compararon los efectos de algunos métodos de sacrificio como descarga eléctrica, concentraciones elevadas de dióxido de carbono y golpe en la cabeza, sobre la calidad de la carne de la trucha (Salmo gairdneri) almacenada en hielo. Ningún efecto significativo sobre la firmeza de la carne, medido con texturómetro, fue encontrado. Resultados similares fueron reportados para channel catfish por Boggess et al. (1973). Oka et al. (1990), también obtuvieron resultados similares y no encontraron correlación con la firmeza de la carne, utilizando como métodos de sacrificio, el corte espinal, hielo en agua y asfixia. Sin embargo, Mochizuki et al. (1998) recomiendan utilizar la sangría como método efectivo con el fin de demorar el progreso del rigor mortis y su efecto sobre la textura de la carne.
EFECTO DE LA RESOLUCIÓN DEL Rigor Mortis
Otro evento también relacionado con el ablandamiento de la carne es la resolución del rigor mortis, el cual podría tener relación con la firmeza de la carne. Para determinar la posible relación entre el ablandamiento de la carne de pescado y la resolución del rigor mortis, Ando et al. (1991) utilizaron parámetros valorativos como el índice del rigor y la fuerza a la ruptura de la carne, medido por texturómetro, en los siguientes peces: plaice (Paralichthys olivaceus), parrot bass (Oplegnathus fasciatus), yellowtail (Seriola quinqueradiata), carpa (Cyprinus carpio), red seabream (Pagrus major), striped grunt (Parapristipoma trilineatum), tiger puffer (Fugu rubripes) y trucha arco iris (Oncorhynchus mykiss). Algunos peces consiguieron alcanzar el máximo rigor mortis 24 horas después de la muerte. En otros, la duración del rigor fue superior a 72 horas después de la muerte y no fue observada su resolución dentro de este período. La carpa solo alcanzó 60% del índice de rigor. Entretanto, la fuerza a la ruptura de los músculos de todos los peces evaluados, excepto tiger puffer, disminuyó rápidamente dentro de las 24 después de la muerte y luego decreció gradualmente. Los valores encontrados son diferentes para cada especie, demostrando que el ablandamiento del músculo de los peces es un proceso independiente del rigor mortis.
EFECTO DEL COCINADO
Algunos estudios presentan diferentes resultados con relación a la textura de la carne cruda y cocida para diferentes especies estudiadas. En un estudio sobre la importancia del tejido conectivo en las diferentes texturas de cinco especies de peces, Hatae et al. (1986) encontraron que los valores de firmeza para la carne cruda de los peces plaice (Limanda yokohamae), channel rock fish (Sebastolobues macrochir), flying fish (Exocoetide sp.), skipjack (Katsuwonus pelamis) y horse mackere (Trachurus japonicus), diminuyeron respectivamente, no obstante, para la carne cocida el orden fue respectivamente: skipjack, flying fish, horse mackere, plaice y channel rock fish. El resultado sobre la textura fue inverso entre la carne cruda y cocida, excepto para el channel rock fish. También fue relacionada la mayor cantidad de colágeno con la firmeza de la carne cruda, de forma que en la carne cocida la firmeza no dependía de la cantidad de proteínas del tejido conectivo, sino probablemente de otros factores asociados a las características de la fibra muscular. En la investigación realizada por Ayala et al. (2005) en sea bass, (Dicentrarchus labrax) el cocinado de la carne descongelada causo masiva coagulación de la proteína y desintegración de miofibrillas, cuando fue observada en microscopia electrónica de transmisión. El evento más significativo fue la presencia de cavidades (huecos) entre las fibras musculares, las cuales fueron ocupadas por líquido, material amorfo y agregado granular. Se determinó correlación entre los cambios estructurales, textura y características organolépticas, donde la pérdida de textura fue determinada y relacionada a la degradación del colágeno.
DEGRADACIÓN post mortem DEL TEJIDO CONECTIVO
Diversos estudios demuestran que los cambios ocurridos en relación con las propiedades físicas de la carne de los peces, conocidos generalmente como ablandamiento de la carne durante el almacenamiento, son más causados por cambios en las estructuras del tejido muscular que por cambios en los componentes de las proteínas (Hatae et al., 1985). En la década de los ochenta, trabajos específicos sobre el ablandamiento de la carne de los peces como efecto del almacenamiento en frío fueron realizados. Bremmer y Hallett (1986), estudiando la degradación del tejido conectivo y su unión en la fibra muscular del pescado spotted trevalla (Seriolella punctata), a través del uso de microscopía electrónica de barrido (SEM), demostraron un deterioro progresivo y visible en las fibras de colágeno del pez almacenado durante varios días en hielo. Esta degradación era un fenómeno común que resultaba en la baja cohesión de la carne de pescado almacenada en frío, conjuntamente con otros factores de degradación, como aumento del pH y efectos bacterianos. Otro estudio realizado por Hallett y Bremmer (1988), también con microscopía electrónica de barrido, sobre la estructura de la unión del miocomatafibra muscular en hoki (Macruronus novazelandiae) almacenado nueve días en hielo, observaron que esta estructura permanece igual durante el prerigor y rigor mortis y solamente es afectada durante el postrigor, ocurriendo un debilitamiento en la invaginación de las fibras de colágeno y la lámina basal, dando por resultado una desconexión de las fibras musculares del miocomata. Estos autores sugieren la refrigeración en estado de prerigor para preservar la textura de la carne de este pez.
DIFERENCIAS ENTRE EL COLÁGENO I Y IV
Diferentes estudios vienen demostrando la presencia de varios tipos de colágeno en peces, asociados con el ablandamiento de la carne. Sato et al. (1988a; Sato et al., 1987) comprobaron la presencia de colágeno tipo I y V en el músculo de varias especies de peces; mientras que Montero y Borderias (1990), Montero y Mackie (1992) detectaron solamente colágeno tipo I en el músculo de trucha (Salmo irideus). En este sentido Mizuta et al., (2005) investigando sobre fracciones de colágeno crudo y preparado por extracción alcalina de varias partes del cuerpo; músculo, hígado, piel, espinas, branquias y tracto digestivo en tiger puffer (Takifugu rubripes), por determinación bioquímica e inmunoquímica, encontraron colágeno tipo I y V, mostrando patrones muy similares. Los resultados sugieren que estos dos tipos de colágeno están principalmente distribuidos en los diferentes tejidos analizados. En lo que respecta a pruebas bioquímicas, Montero y Borderias (1990) estudiaron el colágeno relacionado con el ablandamiento de la carne en trucha (Salmo irideus) bajo refrigeración después de 24 horas post mortem sin observar relación entre enzimas proteolíticas durante el prerigor y el rigor mortis, además solo encontraron colágeno tipo I. Este ablandamiento fue asociado con la presencia de ácido láctico producido por la glicólisis anaeróbica como actividad de las proteasas, en un período de almacenamiento superior a 72 horas. Sato et al. (1991) estudiaron los cambios post mortem en los tipos de colágeno I y V en el músculo de trucha arco iris con relación al ablandamiento del músculo durante el almacenamiento a 5 °C, sin encontrar degradación en la región helicoidal del colágeno; además, la solubilidad del colágeno tipo V aumenta de forma significativa, mientras que el colágeno tipo I no cambia. Estos factores sugieren que la degradación de las regiones no helicoidales o intermoleculares sucede preferiblemente en colágenos tipo V. Para esta especie, el ablandamiento post mortem del músculo, causado por la desintegración de las fibras de colágeno pericelular, fue demostrado por Ando et al. (1992; Ando et al., 1997) utilizando microscopía electrónica de transmisión, donde observaron cambios en la microestructura del músculo durante el almacenamiento y relacionaron estos eventos con las lecturas obtenidas en el texturómetro. Fue concluido que la pérdida de firmeza de la carne es causada por la desintegración de las fibras de colágeno en el tejido conectivo pericelular. Ando et al. (1991) han sugerido que la integridad de la estructura matriz extracelular del colágeno es muy importante para la firmeza del músculo del pescado. A través de microscopía óptica de luz, observaron que ocurre una desintegración gradual de la estructura de la matriz extracelular, donde fueron observados pequeños cambios dentro del tejido conectivo después de una prueba de compresión. Estos autores concluyen que el ablandamiento post mortem del músculo de pescado está relacionado con la desintegración gradual de la matriz extracelular después de la muerte.
En investigaciones realizadas en los últimos años sobre el fenómeno del ablandamiento de la carne de pescado, se observa una tendencia a la utilización de microscopia electrónica. Donde es pertinente demostrar la degradación del tejido conectivo y su correlación con la firmeza de la carne a través de métodos cuantificables (Ando et al.,1991). En un estudio realizado con microscopía electrónica de barrido (SEM), Ando et al. (1995) demostraron los cambios tridimensionales en la red del tejido conectivo pericelular, correspondiente al ablandamiento post mortem en trucha arco iris, yellowtail y tiger puffer. La carne de la trucha arco iris y yellowtail fue afectada por el ablandamiento durante el almacenamiento, pero el músculo del tiger puffer no lo fue afectado, aún trascurridas 72 horas de almacenamiento. De acuerdo con las observaciones histológicas, las fibras del tejido conectivo pericelular en el músculo de trucha arco iris y yellowtail comienzan a disminuir después de 24 horas. Sin embargo, en el músculo de tiger buffer no se observaron cambios estructurales, lo que significa que los cambios en la red del colágeno fibrilar corresponde al ablandamiento post mortem. Estos estudios también confirman la presencia de algunos tipos específicos de colágeno en los peces, especialmente tipo I y V. Sato et al. (1988b); Montero y Borderias (1990); Sato et al. (1997); Nishimoto et al. (2004).
Sato et al. (1997) investigando sobre la responsabilidad del colágeno tipo V en el ablandamiento de la carne de sardina (Sardinops melanosticta) y tiger puffer (Fugu rubripes) encontraron los siguientes resultados. Para la sardina, durante un día de almacenamiento a 5 °C, detectaron que el colágeno tipo V comienza a solubilizarse simultáneamente con el ablandamiento del músculo. Evento causado por la debilidad del tejido conectivo pericelular y provocado por la desintegración de las fibras delgadas del colágeno. Aunque cambios en la estructura del tejido conectivo intersticial o en las propiedades bioquímicas del colágeno tipo I no fueron observadas. Para el tiger puffer no fueron detectados efectos del ablandamiento durante el almacenamiento. Estos factores sugieren que la desintegración del colágeno tipo V causa degradación de las fibras del colágeno en el tejido conectivo pericelular, debilitando el tejido conectivo y resultando en un ablandamiento post mortem. Resultados similares fueron encontrados para la degradación del colágeno en peces de cultivo pelágicos y demersales por Ando et al. (1999), además fue identificado el diámetro de la fibra de colágeno en 20,6 nm y 26,3 nm respectivamente. En este trabajo fue utilizado el microscopio electrónico de transmisión, y el diámetro encontrado fue mayor para los peces demersales como red sea bram (Pagrus major), rudder fish (Girella punctatae), flatfish (Paralichthys olivaceus), y menor para peces pelágicos striped Jack (Caranx delicatissimus), yellwtail (Seriola quinqueradiata) y horse mackerel (Trachurus japonicus). También se considera que el grosor de las fibras de colágeno difiere por la existencia genética de diferentes formas moleculares, tipo I y V (Sato et al., 1988a) y estos tipos de colágenos pueden tener fibras heterotípicas. La alta proporción del colágeno tipo V resulta en la formación de fibras delgadas (Adachi y Hayashi, 1986; Birk et al., 1990). Según estos estudios, las fibras de colágeno de los peces pelágicos son más delgadas y pueden contener más colágeno tipo V. Este tipo de colágeno tiene la tendencia a degradarse durante el almacenamiento, causando el ablandamiento post mortem. Sato et al. (1997) propone la realización de una sangría previa en los peces post captura para demorar el ablandamiento.
MECANISMOS IMPLICADOS EN EL ABLANDAMIENTO post mortem
Finalmente, para explicar el fenómeno del ablandamiento post mortem encontrado especialmente en especies sometidas a cultivo, serán planteadas algunas teorías. Hatae et al. (1989), Tachibana et al. (1993) proponen simplemente, que el ablandamiento sucede, más temprano en especies de cultivo que en individuos de la misma especie provenientes de ambiente natural. Entretanto, Ando et al. (1999) considera que peces de cultivo bien alimentados tienen una taza de rotación de proteína o turnover mucho más elevada que peces de ambiente natural, situación que podría originar una actividad de proteólisis elevada en el músculo de los peces de cultivo. Sin embargo, Bjornevik et al. (2004) en organismos diploides y triploides de salmo solar, considera que la variación intraespecies, en cuanto a textura de la carne y gaping está más relacionada a la estación y tamaño corporal que al promedio del tamaño de la fibra muscular. Por otra parte, el incremento de colágeno por situaciones de ayuno, confiere mayor peso molecular en la forma estructural y mayor temperatura de solubilización. Estas diferencias permanecen significativas después de la realimentación (Bugeon, et al., 2003; Bugeon, et al., 2004).
Kubota et al., (2003) considera que las metaloproteínasas podrían estar envueltas en procesos proteolíticos generando la degradación de colágeno tipo I y V. Estos autores utilizaron un recombinante (MMP9) celular que mostró actividad gelatinolítica en el análisis simográfico, pero no actividad proteolítica en la estructura elíptica de los colágenos I y V. El recombinante solubilizó el colágeno tipo I, indicando que podría estar envuelto en la degradación del tejido conectivo intramuscular. De otra parte, Suárez et al. (2005) estudiando el ablandamiento post mortem en sea brean (Sparus aurata) procedente de cultivo, proponen como responsable de este fenómeno a las colagenasas presentes al finalizar el rigor mortis, donde se determinó la solubilidad de colágeno, encontrándose una disminución en el colágeno ácidosoluble en las primeras horas post mortem. El colágeno pepsino soluble aumentó, mientras el colágeno insoluble disminuyó, coincidiendo con una pérdida de firmeza. Este ablandamiento puede explicarse como resultado específico de colagenasas que actúan en el fragmento insoluble del colágeno. Resultados similares fueron reportados por Espe et al. (2004) trabajando con salmón del Atlántico, donde el colágeno insoluble estuvo relacionado con filetes que presentaron gaping durante el almacenamiento en hielo. Aunque no exista evidencia clara sobre el catabolismo de las proteínas del tejido conectivo, existe un aumento marcado de la espesura del miocomata observado en el bacalao subalimentado (Lavety y Love, 1972; Love, 1992), probablemente debido la adición de fibras de colágeno en la capa del miocomata durante el período de la subalimentación (Love, 1992), incidiendo posiblemente en el efecto de la temperatura de almacenamiento sobre la textura de la carne, presentado en los referidos peces de ambiente natural y de cultivo.
AGRADECIMIENTOSA la Universidad Nacional de Colombia, Sede Medellín, la Universidade Federal de Santa Catariana y la Universidad de Córdoba por el apoyo a los autores de este trabajo.
BIBLIOGRAFÍA
ADACHI E, HAYASHI T. In vitro Formation of Hybrid Fibrils of Type V Collagen and Type I Collagen. Connective Tissue Res. 1986;14:257266.
[ Links ]ALASALVAR C, TAYLOR K, KSUÈ A, GARTHWAITE T, ALÉXIS M, GRIGORAKIS K. Freshness Assessment of Cultured Sea Bream (Sparus aurata) by Chemical, Physical and Sensory Methods. Food Chem. 2001;72:3340.
[ Links ]ALASALVAR C, ANTHONY KD, SHAHIDI F. Comparative Quality Assessment of Cultured and Wild Sea Bream (Sparus aurata) Stored in Ice. J Agri Food Chem. 2002;50:20392045.
[ Links ]ANDO M, TOYOHARA H, SHIMIZU Y, SAKAGUCHI M. Validity of a Puncture Test for Evaluating the Change in Muscle Firmness of Fish During Ice Storage. Nippon Suisan Gakkaishi. 1991;57:2341.
[ Links ]ANDO M, TOYOHARA H, SAKAGUCHI M. Post mortem Tenderization of Rainbow Trout Muscle Caused by the Disintegration of Collagen Fibers in the Pericellular Connective Tissue. Bull Japan Soc Sci Fish. 1992;58:567570.
[ Links ]ANDO M, YOSHIMOTO Y, INABU K, NAKAGAWA T, MAKIMODAN Y. Post mortem Change of ThreeDimensional Structure of Collagen Fibrillar Network in Fish Muscle Pericellular Connective Tissues Corresponding to Post mortem Tenderization. Fisheries Sci. 1995;61:327330.
[ Links ]ANDO M. Softening Mechanism of Fish Meat. Suisangaku Series. Kouseisha Kouseikaku. Tokyo. Japan. 1997;114:7382.
[ Links ]ANDO M, NISHIYABU A, TSUKAMASA Y, MAKINODAN Y. Post mortem Softening of Fish Muscle During Chilled Storage as Affected by Bleeding. J Food Sci. 1999;64(3):423428.
[ Links ]AYALA MD, LÓPEZ AO, BLANCO A, GARCÍA A, ABELLÁN E, RAMÍREZ ZG, GIL F. Structural and Ultrastructural Changes on Muscle Tissue of Sea Bass, Dicentrarchus labrax L., After Cooking and Freezing. Aquaculture. 2005;250(12):215231.
[ Links ]AZAM K, MACKIE M, SOUTH J. The Effect of Slaughter Method on the Quality of Rainbow Trout (Salmo gardneri) During Storage on Ice. Int J food Sci Technol. 1989;24:6979.
[ Links ]BELITZ HD, GORSCH W. Química de los alimentos. Ed. Acribia, S.A. Zaragoza, 1988.
[ Links ]BIRK D, FITCH M, BABIARZ P, LINSENMYER E. Fibrogenesis in vitro: Interaction of Type I and V Collagen Regulates Fibril Diameter. J Cell Sci. 1990;95:649657.
[ Links ]BJORNEVIK M, ESPE M, BEATTIE C, NORTVEDT R, KIESSLING A. Temporal Variation in Muscle Fibre Area, Gaping, Texture, Colour and Collagen in Triploid and Diploid Atlantic Salmon (Salmo salar L). J Sci Food Agri. 2004;84(6):530540.
[ Links ]BOGGESS T, HEATEN E, SHEWFELT A, PARVIN D. Techniques for Stunning Channel Catfish and their Effects on Product Quality. J Food Sci. 1973;38:11901193.
[ Links ]BORNSTEIN H, SAGE H. Structurally Distinct Collagen Types. Annu Rev Biochem. 1980;49:9571003.
[ Links ]BREMMER H, HALLETT L. Muscle FiberConnective Tissue Junctions in the Fish Blue Grenadier (Macruronus novaezelandiae). A Scanning Electron Microscope Study. J Food Sci. 1985;50:975980.
[ Links ]BREMMER H, HALLET C. Degradation Muscle FibreConnective Tissue Junctions in the Spotted Trevalla (Seriolella punctata) Examined by Scanning Electron Microscopi. J Sci Food Agri. 1986;37:10111018.
[ Links ]BUGEON J, LEFEVRE F, FAUCONNEAU B. Fillet Texture and Muscle Structure in Brown Trout (Salmo trutta) Subjected to LongTerm Exercise. Aquaculture Res. 2003;34(14):12871295.
[ Links ]BUGEON J, LEFÈVRE F, FAUCONNEAU B. Correlated Changes in Skeletal Muscle Connective Tissue and Flesh Texture During Starvation and ReFeeding in Brown Trout (Salmo trutta) Reared in Seawater. J Sci Food Agri. 2004;84(11):14331441.
[ Links ]CHEFTEL C, CUQ L, LORIENT D. Proteinas alimentarias. Zaragoza: Ed. Acribia, S.A.; 1989.
[ Links ]COON E, STUMPF. Introdução a Bioquímica. São Paulo: Ed. Edgard Blucher Ltda.; 1980.
[ Links ]DELBARRELADRAT C, CHERET R, TAYLOR R, VERREZBAGNIS V. Trends in Post mortem Aging in Fish: Understanding of Proteolysis and Disorganization of the Myofibrillar Structure. Crit Rev Food Sci Nutri. 2006;46(5)409421.
[ Links ]ESPE M, RUOHONEN K, BJORNEVIK M, FROYLAND L, NORTVEDT R, KIESSLING A. Interactions Between Ice Storage Time, Collagen Composition, Gaping and Textural Properties in Farmed Salmon Muscle Harvested at Different Times of the Year. Aquaculture. 2004;240(14)489504.
[ Links ]FENEMA R, Química de los alimentos. Zaragoza, España: Ed. Acribia S.A.; 1993.
[ Links ]HALLETT I, BREMMER H. Fine Structure of the Myocommata Muscle Fiber Junction in Hoki (Macruronus novaezelandie). J Sci Food Agri. 1988;44:245261.
[ Links ]HATAE K, TAMARI S, MIYANAGA K, MATSUMOTO J. Species Difference and Changes in the Physical Properties of Fish Muscle as Freshness Decreases. Bull Japanese Soc Sci Fish. 1985;51:11551161.
[ Links ]HATAE K, TOBIMATSU A, TAKEYAMA M, MATSUMOTO J. Contribution of Connective Tissues on the Texture Difference of Varies Fish Species. Bull Japan Soci Sci Fish. 1986;52:20012007.
[ Links ]HATAE K, LEE H, TSUCHIYA T, SHIMADA A. Textural Properties of Cultured and Wild Fish Meat. Bull Japan Soci Sci Fish. 1989;(55)363368.
[ Links ]JARENBÄCK L, LILJEMARK A. Ultratrustural Changes During Frozen Storage of Cod (Gadus morthua) 1. Structure of Myofibrils as Rivaled by Freeze Etching Preparation. J Food Technol. 1975;10:229236.
[ Links ]KUBOTA S, SATA K, OHSTSUKI K, KAWABATA M, Degradation de αConnectin in Raw Fish Muscle and Softening Evaluated by Breaking Strength Occur Independently During one Chilled Storage. Fisheries Sci. 1996;3:600602.
KUBOTA M, KINOSHITA M, TAKEUCHI K, KUBOTA S, TOYOHARA H, SAKAGUCHI M. Solubilization of Type I Collagen from Fish Muscle Connective Tissue by Matrix Metalloproteinase9 at Chilled Temperature. Fisheries Sci. 2003;69(5):10531059.
[ Links ]KUMANO Y, SEKI N. Change in α Connecting Content During Storage of Iced, Frozen and Thawed Fish Muscle. Nippon Suisan Gakkaishi. 1993;59:559564.
LADRAT C, VERREZBAGNIS V, NOËL J, FLEURENCE J. In vitro Proteolysis of Myofibrillar and Sarcoplasmic Proteins of White Muscle of Sea Bass (Dicentrarchus labrax L.): Effects of Cathepsins B, D and L. Food Chem. 2003;81:517525.
[ Links ]LAVETY J, LOVE M. The Strengthening of Cod Connective Tissue During Starvation. Comp Biochem Physiol. 1972;41A:3942.
[ Links ]LINDEN G, LORIENT D. Bioquímica agroindustrial. Zaragoza: Ed. Acribia S. A.;1996.
[ Links ]LOVE M, LAVETY J, STEEL J. The Connective Tissues of Fish ll. Gaping in Commercial Species of Frozen Fish in Relation to Rigor mortis. J Food Technol. 1969;4:3944.
[ Links ]LOVE M, HAQ M, SMITH l. The Connective Tissues of Fish V. Gaping in Cod of Different Sizes as Influenced by a Seasonal Variation in the Ultimate pH. J Food Techno. 1972;7:281290.
[ Links ]MA B, YAMANAKA H. Studies on ThawRigor in Red Sea Bream and Carpa Muscles. Nippon Suisan Gakkaishi. 1991;57:13651368.
[ Links ]MIZUTA S, FUJISAWA S, NISHIMOTO M, YOSHINAKA R. Biochemical and Immunochemical Detection of Types I and V Collagens in Tiger Puffer Takifugu rubripes. Food Chem. 2005;89(3):373377.
[ Links ]MOCHIZUKI S, SATO A. Effects of Various Killing Procedures on Post mortem Changes in the Muscle of Horse Mackerel. Bull Japan Soc Sci Fish. 1996;64:276279.
[ Links ]MOCHIZUKI S, NORITA Y, MAENO M. Effects of Bleeding on Post mortem Changes in the Muscle of Horse Mackerel. Bull Japan Soc Sci Fish. 1998;62:453457.
[ Links ]MONTERO P, BORDERIAS J. Effect of Rigor mortis and Ageing on Collagen in Trout (Salmo irideus) Muscle. J Sci Food Agri. 1990;52:141146.
[ Links ]MONTERO P, MACKIE M. Changes in Intramuscular Collagen of Cod (Gadus morhua) During Post mortem Storage in Ice. J Sci Food Agri. 1992;59:8996.
[ Links ]NISHIMOTO M, MIZUTA S, YOSHINAKA R. Characterization of Molecular Species of Collagen in Muscles of Japanese Amberjack, Seriola Quinqueradiata. Food Chem. 2004;84(1):127132.
[ Links ]NURSHALL R. The Lateral Musculature and the Swimming of Fish. Proc Zool Soc Lond. 1956;126127.
[ Links ]OKA H, OHNO K, NINOMUYA J. Changes in Texture During Cold Storage of Cultured Yellowtail Meat Prepared by Different Killing Methods. Bull Japan Soc Sci Fish. 1990;56:16731678.
[ Links ]SATO K, YOSHIMAKA R, SATO M, SHIMIZU Y. Collagen Content in the Muscle of Fishes in Association with their Swimming Movement and Meat Texture. Bull Japan Soc Sci Fish. 1986;52:15951600.
[ Links ]SATO K, YOSHINAKA R, SATO M, SHIMIZU Y. Collagen Content in the Muscle of Fishes in Association with their Swimming Movement and Meat Texture. Bull Japan Soc Sci Fish. 1987;52(9):15951600.
[ Links ]SATO K, YOSHINAKA R, ITOH Y, SATO M. Molecular Species of Collagen in the Intramuscular Connective Tissue of Fish. Comp Biochem Physiol. 1988a;92B(1):8791.
[ Links ]SATO K, YOSHINAKA R, SATO M, ITOH Y, SHIMIZU Y. Isolation of Types I and V Collagens from Carp Muscle. Comp Biochem Physiol. 1988b;90B(1):155158.
[ Links ]SATO K, OHASHI C, OHTSUKI K, KAWABATA M. Type V Collagen in Trout (Salmo gairdneri) Muscle and its Solubility Change Chilled Storage of Muscle. J Agri Food Chem. 1991;39:12221225.
[ Links ]SATO K, ANDO M, KUBOTA S, ORIGASA K, KAWASE H. Involvement of Type V Collagen in Softening of Fish Muscle During ShortTerm Chilled Storage. J Agri Food Chem. 1997;45:343348.
[ Links ]SHIGEMURA Y, ANDO M, TSUKAMASA Y, MAKINODAN Y, KAWAI T. Correlation of Type V Collagen Content with Post mortem Softening of Fish Meat During Chilled Storage. Fisheries Sci. 2003;69(4):842848.
[ Links ]SUÁREZ MD, ABAD M, RUIZCARA T, ESTRADA JD, GARCÍAGALLEGO M. Changes in Muscle Collagen Content During Post mortem Storage of Farmed Sea Bream (Sparus aurata): Influence on Textural Properties. Aquaculture Inter. 2005;13:315325.
[ Links ]SUAREZMAHECHA, H. Efeito do resfriamento sobre a textura post mortem da carne do matrinxã Brycon cephalus (pisces: characiforme). Dissertação (Mestrado)Florianópolis: Departamento de Ciencia e Tecnolgia de Alimentos, Centro de Ciencias Agrarias, Universidade Federal de Santa Catarina, Brasil. 2002.
[ Links ]TACHIBANA K, MISIMA T, TSUCHIMOTO M. Changes of Ultrastructure and Cytochemical Mg2+ATPase Activity in Ordinary Muscle of Cultured and Wild Red Sea Bream During Storage in Ice. Bull Japan Soc Sci Fish. 1993;59:721727.
[ Links ]TOYOHARA H, SHIMIZU Y. Relation of the Rigor mortis of Fish Body and the Texture of the Muscle. Bull Japan Soc Sci Fish. 1988;54:17951798.
[ Links ]











