Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.13 no.2 Bogotá May./Aug. 2008
MODELO TEÓRICO PARA EXPLICAR LA ACUMULACIÓN DE GOTAS LIPÍDICAS EN EMBRIONES BOVINOS MACHOS O HEMBRAS PRODUCIDOS in vitro
Theoretical Model For Explaining Accumulation Of Fat Drops In In Vitro Produced Bovine Embryos
OMAR CAMARGO1,2, MVZ, M.Sc.; TATIANA RUIZ2, MV, Ms, Ph. D.; MARTHA OLIVERA2*, DMV, Dr. Sci. Agr.
1 Grupo de Biotecnología Animal, Universidad Nacional de Colombia Sede Medellín, 2 Grupo Biogénesis, Facultad de Ciencias Agrarias, Universidad de Antioquia, Carrera 75 Nº 65-87, AA 1226. Tel: 574 - 425 91 49, Medellín, Colombia. *molivera@catios.udea.edu.co
Presentado 4 de septiembre de 2007, aceptado 23 de febrero de 2008, correcciones 11 de abril de 2008.
RESUMEN
La glucosa 6-fosfato deshidrogenasa (G6PD), codificada por un gen ubicado en el cromosoma X, es la enzima limitante de vía de las pentosas fosfato (PF). La entrada de la glucosa así como su flujo y el rendimiento metabólico de esta vía están determinados tanto por los mismos niveles glucosa así como por la actividad de la G6PD. Por esta vía, la glucosa regula la trascripción de varios genes lipogénicos. En algunos embriones hembra producidos in vitro, se registra un retardo en la normal inactivación de uno de sus cromosomas X, lo cual se traduce en una doble actividad de los genes allí ubicados, si se compara con los embriones macho producidos in vitro. Se postula entonces que, la sobre-regulación de la vía PF a consecuencia de la doble dosis de su enzima limitante (G6PD) y en presencia de elevados niveles de glucosa (mayores a 2,5 mM en el medio de cultivo), conllevaría a un dimorfismo sexual en relación con la transcripción de los genes Acetil CoA Carboxilasa Alfa (en adelante ACACA, símbolo oficial de la acetyl-Coenzyme A carboxylase alpha), y la Sintetasa de Ácidos Grasos (en edelante FASN, símbolo oficial de la fatty acid synthase) que corriente abajo codifican para las enzimas limitantes en la síntesis de lípidos. Este dimorfismo sexual para el fenotipo metabolismo de lípidos, derivaría en una mayor acumulación citoplasmática de gotas lipídicas en los embriones hembra en comparación con los embriones machos que, de ser así, tendría efectos expansivos sobre el metabolismo general, la actividad transcripcional de otros genes y sobre la resistencia a la criopreservación.
Palabras clave: compensación dosis cromosómica, genes lipogénicos, metabolismo glucosa.
ABSTRACT
The encoding gene for glucose 6-phosphate dehydrogenase (G6PD) is located on chromosome X. This enzyme regulates the entrance of glucose into the pentose phosphate pathway (PPP). Besides, throughout this route, glucose regulates the transcription of some lipogenic genes. Compared with in vitro produced male embryos, and due to a delaying in X-chromosome inactivation as a consequence of in vitro culture conditions, some early female embryos show two-fold increase in this enzyme (G6PD) and consequently in PPP. It is postulated therefore that this kind of failures in genetic dosage compensation, and in a dependent manner of glucose levels, would generates a sexual dimorphism in lipid metabolic phenotype, at the level of transcription of genes associated to rate limiting enzymes of the synthesis of lipids such as Acetyl-CoA Carboxylase-Alpha (ACACA) and Fatty Acid Synthase (FASN). This would lead to a higher cytoplasmic accumulation of lipid droplets in female embryos with effects on their general metabolism, transcriptional activity of some down stream genes and on their cryotolerance
Key words: Chromosome dose compensation, lipogenic genes, glucose metabolism.
INTRODUCCIÓN
Los medios estándar de cultivo de tejidos generalmente contienen una concentración de glucosa de 5,6 mM, correspondiente a la glicemia en humanos (Biggers, 1998). Este nivel de glucosa, sin embargo, parece ser inapropiado si se usa en los medios de cultivo para embriones mamíferos antes de la compactación en donde ejerce un efecto inhibidor del desarrollo (Revisado por Barnett y Bavister, 1996). Antes de la compactación en embriones bovinos, niveles de glucosa por encima de 2,5 mM en los medios de cultivo, no solo afecta negativamente el desarrollo embrionario sino que también afecta la normalmente esperada equitativa proporción de los sexos (Kimura et al., 2005). Después del estado de 8-16 células, el metabolismo embrionario cambia y la glucosa pasa a convertirse en el sustrato energético de preferencia para el desarrollo embrionario normal (Leese, 1995; Barnett y Bavister, 1996, Riley y Moley, 2006). El metabolismo de la glucosa incrementa significativamente durante el estado de 8-16 células, lo cual es acompañado de un incremento aun mayor en la toma de glucosa (Rieger et al., 1992). En las primeras fases del desarrollo embrionario in vitro, la poca glucosa consumida es metabolizada a través de la vía de las Pentosas Fosfato -PF, pero desde el estadío de 816 células en adelante, la glucosa es metabolizada principalmente a través de la vía glicolítica (Javed y Wright, 1991; Rieger et al. 1992; Thompson et al., 1996). De otro lado ha sido observado que en embriones bovinos producidos in vitro tanto la cantidad de lípidos acumulados en el citoplasma (Crosier et al. 2001) como la abundancia relativa de ARNm para genes lipogénicos aumentan a medida que se alcanza el estadio de blastocisto (Algriany et al., 2007). Se sostiene, por parte de algunos autores, que una excesiva acumulación de lípidos a manera de gotas intracitoplasmáticos hacen menos resistentes a los oocitos/embriones frente a los procesos de criopreservación (Diez et al., 2001; Leibo y Loskutoff, 1993; Moore y Quadros, 2006; Seidel, 2006; Tominaga et al.2000; Ushijima et al., 1999).
La baja sobrevivencia post-criopreservación de oocitos y embriones producidos in vitro constituye un cuello de botella importante que limita significativamente el desarrollo de esta industria y sus aplicaciones biotecnológicas (Seidel, 2006; Moore y Quadros, 2006; Hiemstra et al., 2005). En embriones bovinos producidos in vitro, al igual que lo reportado para células somáticas, es posible que exista un nexo entre el nivel de glucosa metabolizada a través de la vía PF y el nivel de expresión de ciertos genes lipo-génicos y en consecuencia con la acumulación de lípidos. Adicionalmente, en algunos embriones hembra producidos in vitro, se registra un retardo en la normal inactivación de uno de sus cromosomas X, lo cual se traduciría en una doble actividad de los genes allí ubicados, entre ellos el de la G6PD. En consecuencia, la sobre-regulación de la vía PF, a consecuencia de la doble dosis de su enzima limitante (G6PD) y en presencia de elevados niveles de glucosa, estaría conduciendo a una mayor acumulación de lípidos en los embriones hembra. Este nexo hipotético, sus detalles macro, sus particularidades según el sexo y algunas de sus potenciales consecuencias, se esbozan a continuación. Cada uno de los numerales que encabezan cada sección del presente documento se corresponden con los números asignados sobre la Figura. 1 (Modelo) a los diferentes pasos a describir sobre las vías metabólicas.
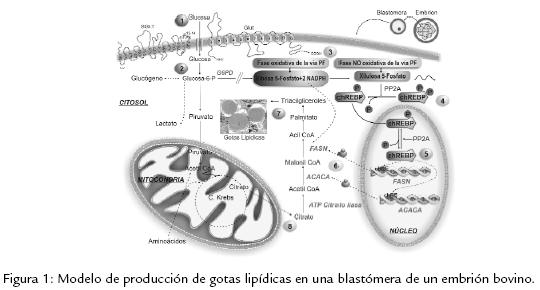
LA GLUCOSA
La glucosa es requerida por el embrión no solo como un sustrato energético (Leese y Barton, 1984), sino que participa en la síntesis de bio-moléculas importantes y sobretodo actúa como una molécula con actividad transduccional, con incidencia directa sobre el crecimiento y la diferenciación (Jansen et al., 2006). En resumen, aunque la glucosa no hace un mayor aporte de ATP a los requerimientos energéticos durante el desarrollo pre-implantación, si interviene en la regulación de la expresión de enzimas y proteínas, algunas de ellas con actividad transportadora ubicadas en membrana celular (Moley et al., 1998a, 1998b; Jansen et al., 2006). En estudios con células somáticas se ha demostrado que la glucosa induce la trascripción de varios genes glicolíticos y lipogénicos (Doiron et al., 1996; Hillgartner y Charron 1998; Massillon et al., 1998; Vaulont et al., 2000; Guillet-Deniau et al., 2003; Kabashima et al., 2003). Mientras algunos autores sugieren que la señal de la glucosa es generada a través del brazo no oxidativo de la vía PF (Doiron et al., 1996; Massillon et al., 1998; Stabilé, 1999), otros por su parte sostienen que la regulación metabólica aplicada sobre la vía PF repercute no solo sobre el metabolismo lipídico (Foretz et al., 1998; Stabilé 1999; Leese 2002; De La Torre-Sanchez et al., 2004; Park et al., 2005; De La Torre-Sanchez et al., 2006), sino también sobre la producción elevada de interferón tau (IFNτ registrada en embriones bovinos hembra producidos in vitro, sugiriendo de paso que ésta es causada por la sobre-expresión de la G6PD (Kimura et al., 2004).
EL MODELO
1. EL TRANSPORTE DE GLUCOSA
En eucariontes, la glucosa entra a la célula ya sea me-diante un proceso activo vía transportadores de glucosa acoplados al sodio (SGLT, abreviatura en inglés de sodium glucosa transporters) o por transporte facilitado mediado por proteínas conocidas como transportadores de glucosa (GLUT, abreviatura en inglés de glucosa transporters), en un proceso independiente de energía, favorecido por un gradiente de concentración. La información sobre la presencia de SGLT durante el desarrollo embrionario preimplantación es ambigua, por lo tanto se asume que la entrada de glucosa al embrión durante el periodo preimplantatorio se realiza mayormente por transporte facilitado, mediado por la GLUT (Riley y Moley, 2006).
2. VÍAS ALTERNATIVAS DE METABOLISMO DE LA GLUCOSA
Una vez la glucosa se encuentra dentro de la célula y mediante la condensación del acido fosfórico al grupo hidroxilo del carbono 6 de la glucosa, se forma un enlace éster fosfato y se convierte en glucosa 6-fosfato (Glucosa-6-P). La fosforilación, que activa los azúcares para su subsecuente transformación química, habilita la glucosa 6-fosfato para seguir por una de las siguientes vías metabólicas: síntesis de glucógeno, glicólisis (conversión en lactato o piruvato) o pentosas fosfato (Johnson et al., 2003). El modelo presentado aquí se centra en el papel regulador ejercido por la glucosa a través de la vía PF sobre la trascripción de genes lipogénicos, que sería la vía que se considera podría producir la acumulación de gotas lipídicas en el citoplasma del embrión. El metabolismo global de la glucosa se incrementa 30 veces desde el clivaje de dos células hasta el blastocisto expandido y de estos 15 veces es a través de la vía PF. El primer incremento se registra en el estadío de 8-16 células, momento de la activación del genoma embrionario, y el segundo, durante la expansión del blastocisto, presumiblemente debido al incremento en las demandas de energía de la ATPasa Na+/K+, necesaria para la formación y el mantenimiento del blastocele (Rieger et al., 1992; Thompson et al., 1996).
3. FASE OXIDATIVA Y FASE NO OXIDATIVA DE LA VÍA DE LAS PENTOSAS FOSFATO
La vía PF es una ruta alternativa de oxidación de glucosa cuyos productos primarios son NADPH: y ribosa 5-fosfato; el primero agente reductor en los procesos de biosíntesis y la se-gunda necesaria en síntesis de ribonucleótidos componentes de RNA, DNA, ATP, NADH, FAD y Coenzima A. Esta vía consta de dos fases, la primera fase oxidativa en la cual se registra la oxidación irreversible de glucosa-6-fosfato a ribulosa-5-fosfato y la producción de dos moléculas de NADPH (De La Torre-Sánchez et al., 2006, Dumollard et al., 2007), y la segunda fase, reversible y no oxidativa, en la cual se registra la interconversión de azúcares de 3, 4, 5, 6 y 7 carbonos y la síntesis de nucleótidos (ribosa-5-fosfato), así como de intermediarios de la glicólisis, entre ellos la xilulosa 5-fosfato (Xu-5P) (Doiron et al., 1996; Kabashima et al., 2003) La G6PD, es una enzima reconocida por ser la primera en actuar y por controlar el flujo de la vía PF, de ella depende el rendimiento de la misma. La mayor actividad de esta enzima, se asocia con un mayor rendimiento de la vía en general. Normalmente considerada una enzima de mantenimiento con expresión constitutiva, es inducida por agentes que causan estrés oxidativo, y otros agentes tales como la insulina, el fac-tor de crecimiento epidermal y las condiciones de la dieta (su actividad es estimulada por los carbohidratos e inhibida por las grasas poli-insaturadas) (Salati y Amir-Ahmady, 2001). Se sabe que en las células somáticas, la regulación de la trascripción de ciertos genes no es realizada por la glucosa directamente, pero si por algunos de sus metabolitos. Se han sugerido varias moléculas que regulan factores de trascripción sensibles (respondedores) a la glucosa, además de ésta, sus metabolitos, la glucosa 6-fosfato (Prip-Buus et al., 1995), uno o dos metabolitos del piruvato (3-fosfoglicerato y/o fosfoenolpiruvato) (Kang et al., 1996) y la Xu-5P (Doiron et al., 1996). La formación de una mezcla de varios intermediarios, hace difícil señalar inequívocamente el verdadero compuesto regulador, especialmente cuando el factor de trascripción respondedor a la glucosa es desconocido (Kabashima et al., 2003). El uso en los medios de cultivo de embriones de inhibidores de la G6PD, tales como Dehidroepiandrosterona –DHEA (Pérez-Crespo et al., 2005; Kimura et al., 2005) o de ácidos grasos poli-insaturados (Hochi et al., 1999; Pereira et al., 2007), no solo corrigen el desbalance entre la proporción de los sexos sino que además hace que una mayor proporción de embriones sobreviva un proceso de criopreservación.
4. ACTIVADOR DE LA TRASCRIPCIÓN EN RESPUESTA A LOS CARBOHIDRATOS
Un factor que reúne todas las características para la activación de la trascripción en respuesta a los carbo-hidratos, caracterizado inicialmente en células hepáticas (Yamashita et al., 2001), es el llamada proteína de unión al elemento respondedor a los carbohidratos (de aquí en edelante chREBP, abreviatura en inglés de carbohydrate responsive element binding protein), el cual se ha encontrado interviniendo en la regulación de la trascripción de genes como L-piruvato kinasa (LPK), al igual que en genes de enzimas lipogénicas como la ACACA y la FASN (Kabashima et al., 2003). De acuerdo con los hallazgos de Nishimura y Uyeda (1995), la activación de chREBP es llevada a cabo por una proteína fosfatasa 2A (PP2A) dependiente de Xu-5P. En resumen, la presencia de carbohidratos incrementaría la concentración de Xu-5P, a su vez ésta, activaría la PP2A, la cual actuaría sobre chREBP, quien finalmente induciría en el núcleo la expresión de genes que codifican para enzimas lipogénicas promoviendo, por lo tanto, la conversión de carbohidratos en grasa (lipogénesis).
5. LA PROTEÍNA DE UNIÓN AL ELEMENTO RESPONDEDOR A LOS CARBOHIDRATOS
La proteína de unión al elemento respondedor a los carbohidratos (chREBP) es un miembro de la familia de los factores de trascripción conocidos como cremallera de leucina hélice-bucle-hélice básicos (basic helix–loop–helix_leucine zipper - bHLH_ZIP-) con una Mr de 94.600. Contiene una señal de localización nuclear (nuclear localization signal -NLS), una extensión rica en prolina (proline-rich stretches -PRO), un bHLH_ZIP, y un dominio similar a ZIP (ZIP-like domain) (Yamashita et al., 2001; Kabashima et al., 2003). chREBP esta localizado inicialmente en el citosol de la célula, y en presencia de carbohidratos se activa (mediante el mecanismo arriba descrito) y se transloca al núcleo (Kawaguchi et al., 2001), en donde es activado por desfosforilación de su residuo treonina-166, situada dentro del dominio de los aminoácidos básicos de unión al ADN. En resumen, el exceso de glucosa estimula la actividad de chREBP mediante dos mecanismos: la desfosforilación y activación de la señal de localización nuclear (NLS) en el citosol y la unión al ADN en el núcleo. Una vez en el núcleo, actúa sobre el elemento respondedor de la glucosa presente en los genes lipogénicos, entre ellos los genes que codifican para la ACACA y la FASN (Kabashima et al., 2003).
6. SÍNTESIS DE ÁCIDOS GRASOS DE CADENA LARGA
La síntesis de ácidos grasos de cadena larga (lipogénesis de novo o síntesis de novo) se da en el citoplasma a partir de un intermediario activado de dos carbonos: el acetil-CoA. La síntesis de malonil-CoA a partir de acetil-CoA además de ser el primer paso en la síntesis de ácidos grasos, es una reacción irreversible catalizada por la ACACA, enzima en la cual se concentra el principal sitio de regulación de la síntesis de ácidos grasos y a través de la cual se controla el flujo de esta vía (lipogénesis de novo) (Barber et al., 2005). En bovinos existen dos isoformas: la ACACA (alfa) y la ACACB (beta) (Roy et al., 2005). La ACACA, una de las enzimas sobre las que se requiere investigación, se expresa princi-palmente en tejidos lipogénicos, y dentro de su regulación se incluyen interacciones alostéricas con metabolitos y fosforilaciones reversibles (Hardie, 1989; Kim et al., 1989), disparadas extracelularmente por varias hormonas (Iritani, 1992). El control a largo plazo es ejercido a nivel transcripcional (Kim, 1997). El malonil-CoA, producto de la actividad de la ACCA, es usado como eslabón para elongar la cadena de ácidos grasos. Los ácidos grasos de cadena larga, son ensamblados en una secuencia repetida de cuatro pasos. Un grupo acilo saturado, producido por este conjunto de reacciones, se convierte en sustrato por subsecuente condensación con un grupo malonil activado. En cada pasaje a través del ciclo, la cadena de ácidos grasos es extendida en dos carbonos, cuando alcanza una longitud de 16 car-bonos, el producto (palmitato 16:0) sale del ciclo (Barber et al., 2005). Todas las reacciones en el proceso sintético son catalizadas por FASN, un complejo multienzimático el cual cataliza la síntesis de ácidos grasos saturados usando acetil Co-A, malonil Co-A y NADPH; los niveles de FASN son controlados por la tasa de transcripción y la estabilidad de su ARNm (Hillgartner et al., 1995). Es de resaltar que además de estar controlando la expresión de enzimas lipogénicas, la misma vía PF aporta los cofactores reductores (NADPH) necesarios para la síntesis de lípidos. El palmitato, principal producto de la FASN, mediante la acción de un sistema de elongación de ácidos grasos presente en el retículo endoplásmico liso y la mitocondria (Smith, 1994) es el precursor de otros ácidos grasos de cadena larga en células animales; puede ser elongado para formar estearato (18:0) o mediante adiciones sucesivas de grupos acetilo, convertirlo en ácidos grasos saturados mas largos
7. DESTINO DE LOS ÁCIDOS GRASOS SINTETIZADOS
La mayoría de los ácidos grasos sinteti-zados o ingeridos por un organismo tienen dos destinos: su incorporación en triacilgliceroles para el almacenamiento de energía metabólica (previa conversión del acido graso en acil Co-A por acción de la acil CoA sintetasa), o la incorporación en los fosfolípidos componentes de la membrana. Un triacilglicerol (triglicérido o molécula grasa) esta compuesta por tres moléculas de ácidos grasos unidas mediante un enlace ester al glicerol. Los triacilgliceroles no tienen carga y son virtualmente insolubles en agua, y coalescen en gotas en el citosol (Crosier et al., 2001; Barcelo-Fimbres, 2007). La acumulación de gotas lipídicas en el citoplasma es uno de las alteraciones ultraestructurales observadas en embriones bovinos producidos in vitro lo cual tiene implicaciones sobre su metabolismo, su criotolerancia y en general sobre su viabilidad (Pollard y Leibo, 1994, Abe et al., 1999; Ushijima et al,. 1999; Abd El Razek et al., 2000; Abe et al., 2002, Rizos et al., 2003; Nedambale et al., 2004; De La Torre-Sánchez et al., 2006, Seidel 2006).
8. EL CITRATO, MATERIA PRIMA PARA LA PRODUCCIÓN DE ÁCIDOS GRASOS
El citrato, materia prima para la producción de ácidos grasos, proviene del catabolismo de moléculas orgánicas como el piruvato, los ácidos grasos y algunos aminoácidos (principalmente los cetogénicos) presentes en el medio de cultivo y en las reservas endógenas del em-brión, las cuales son oxidadas para producir fragmentos de dos carbonos a la forma de los grupos acetil del acetil CoA, y de esa manera ingresar al ciclo del acido cítrico (ciclo del ácido tricarboxilico o ciclo de Krebs) (Swain et al. 2002). Se conoce poco sobre el metabolismo embrionario de los ácidos grasos y de cuales son las cantidades relativas de sustratos endógenos mas allá de los primeros días de desarrollo; ni tampoco se han realizado muchos estudios de cómo se utilizan éstos sustratos (Johnson et al., 2003).
LA HIPÓTESIS
La hipótesis que se postula para resolver varios de los interrogantes que se formulan dice que: “En presencia de glucosa, la abundancia relativa de ARNm de los genes lipogénicos acetil-CoA carboxilasa –ACACA y sintetasa de ácidos grasos –FASN de los embriones bovinos producidos in vitro, es mayor en hembras que en machos, lo cual afecta su contenido de lípidos y su criotolerancia”. Los argumentos que sustentan esta tesis son los siguientes: El gen para la glucosa 6fosfato deshidrogenasa, la enzima que se halla a la entrada de la vía de las pentosas fosfato y que controla el flujo y el rendimiento a través de esta vía, se ubica en el cromosoma X. Los embriones hembra, por lo tanto, tienen el potencial para producir una cantidad doble de esta enzima (y de otras ubicadas en el mismo cromosoma), en comparación con los embriones macho, los cuales tienen solo un cromosoma X (Epstein et al., 1978, revisado por Gutierrez-Adan et al., 2006). En embriones hembras producidos in vitro, la actividad de la vía PF fue hallada cuadruplicada en relación con la actividad registrada por la misma vía en embriones macho (Figura. 1 , numeral 3) (Tiffin et al., 1991). Igualmente, los embriones hembra registran una mayor actividad transcripcional para la enzima G6PD (Fig. 1 , numeral 2) la cual fue hallada duplicada (Wrenzycki et al., 2002), sugiriendo esto que en los embriones hembra, ambos cromosomas X estarían activos (Gutierrez-Adan et al., 2000; Lonergan et al., 2000, Tian et al. 2007). Análisis de embriones hembras y machos en los estadios de mórula y blastocisto generados in vivo, no mostraron tal desbalance para la expresión de esta enzima, indicando que la no compensación de dosis para la expresión de esta enzima, ocurre solamente en embriones producidos in vitro. Al igual que en ratones (Lathman et al., 2000), en embriones bovinos producidos in vitro, la compensación de dosis parece estar retardada y se hace muy evidente en los estadíos de mórula y blastocisto (De La Fuente et al., 1999; Wrenzycki et al., 2002; Carrel, Willard 2005). De ahí que la inclusión de glucosa en los medios de cultivo, induzca importantes modificaciones en el metabolismo embrionario todas ellas asociadas con la trascripción genética diferencial entre machos y hembras para genes localizados en el cromosoma X (G6PD, HPRT, XIAP) (De La Fuente et al., 1999; Peippo et al., 2001; Donnay et al., 2001; Kimura et al., 2005). Ya se han reportado algunas diferencias de género, desencadenadas por las condiciones de cultivo in vitro o por los componentes de los medios, principalmente por la presencia de glucosa, los cuales afectan de manera significativa no solamente la proporción natural de los sexos (Gutierrez-Adan et al., 2001; Larson et al., 2001; Kimura et al., 2004; Gutierrez-Adán, 2005) sino también la resistencia al enfriamiento. Nedambale et al., (2004) hallaron que, en general, los embriones macho producidos in vitro resisten mejor un proceso de criopreservación en comparación con los hembra. En este sentido, se postula que la demora en la compensación de dosis en embriones bovinos hembra producidos in vitro generaría un dimorfismo sexual a nivel transcripcional, en relación con la expresión de algunos genes asociados con la síntesis de lípidos (ACACA, FASN). Esta descompensación derivaría, entre otros, en una mayor acumulación citoplasmática de gotas lipídicas en embriones bovinos hembra en comparación con los machos, lo cual las dejaría en desventaja para tolerar el enfriamiento y superar un proceso de criopreservación de manera exitosa.
BIBLIOGRAFÍA
ABD EL RAZEK IM, CHARPIGNY G, KODIA S, MARQUANT-LE GUIENNE B, MERMILLOD P, GUYADER-JOLY C, HUMBLOT P. Differences in lipid composition between in vivo- and in vitro-produced bovine embryos. Theriogenology. 2000;53:346.
[ Links ]ABE H, YAMASHITA S, ITOH T, SATOH T, HOSHI H. Ultrastructure of bovine embryos developed from in vitro-matured and -fertilized oocytes: comparative morphological evaluation of embryos cultured either in serum free or serum-supplemented medium. Mol Reprod Dev 1999;53:325-335.
[ Links ]ABE H, YAMASHITA S, SATOH T, HOSHI H. Accumulation of cytoplasmic lipid droplets in bovine embryos and cryotolerance of embryos developed in different culture systems using serum-free or serum-containing media. Mol Rep Dev 2002;61:57-66.
[ Links ]ALGRIANY O, VOS PLAM, SIRARD MA, DIELEMAN SJ. Switch in the expression of genes involved in lipid metabolism for in-vivo matured bovine oocytes and blastocysts. Reprod Fert and Devel. 2007;19:244-244.
[ Links ]BARBER MC, PRICE NT, TRAVERS MT. Structure and regulation of acetyl-CoA carboxylase genes of metazoan. BBA. 2005;1733:1-28.
[ Links ]BARNETT DK, BAVISTER BD. What is the relationship between the metabolism of preimplantation embryos and their developmental competence? Mol Reprod Dev. 1996;43:105-133.
[ Links ]BARCELÓ-FIMBRES M, SEIDEL GE. Effects of either glucose or fructose and metabolic regulators on bovine embryo development and lipid accumulation in vitro. Mol Reprod Dev 2007 Mar 6; DOI 10.1002/mrd [Epub ahead of print].
[ Links ]BIGGERS JD. Reflections on the culture of the preimplantation embryo. Int J Dev Biol 1998;42,879-884.
[ Links ]CARREL L, WILLARD HF. X-inactivation profile reveals extensive variability in X-linked gene expression in females. Nature, 2005; 434, 400-404.
[ Links ]CROSIER AE, FARIN PW, DYKSTRA MJ, ALEXANDER JE, FARIN CE. Ultrastructural morphometry of bovine blastocyst produced in vivo or in vitro. Biol. Reprod. 2001;64:1375-1385.
[ Links ]DE LA FUENTE R, HAHNEL A, BASRUR PK, KING WA. X inactive specific transcript (Xist) expression and X chromosome inactivation in preattachment bovine embryo. Biol Reprod. 1999;60:769-775.
[ Links ]DE LA TORRE-SANCHEZ J, GARDNER D, PREIS K, SEIDEL JRG. Regulation of glucose metabolism to decrease lipid content of in-vitro produced bovine embryos. Reprod Fertil Dev. 2004; 17:218.
[ Links ]DE LA TORRE-SANCHEZ JF, GARDNER DK, PREIS K, GIBBONS J, SEIDEL JrGE. Metabolic regulation of in-vitro-produced bovine embryos. II. Effects of phenazine ethosulfate, sodium azide and 2,4-dinitrophenol during post-compaction development on glucose metabolism and lipid accumulation. Reprod Fertil Dev. 2006; 18:597-607.
[ Links ]DIEZ C, HEYMAN Y, LE BOURHIS D, GUYADER-JOLY C, DEGROUARD J, RENARD JP. Delipidating in vitro-produced bovine zygotes: effect on further development and consequences for freezability. Theriogenology 2001; 55:923-936.
[ Links ]DOIRON B, CUIF MH, CHEN R, KAHN A. Transcriptional glucose signaling through the glucose response element is mediated by pentose phosphate pathway. J Biol Chem. 1996;271:5321-5324.
[ Links ]DONNAY I, FEUGANG JM, BERNARD S, MARCHANDISE J, PAMPFER S, MOENS A DESSY F. Impact of adding 5.5 mM glucose to SOF medium on the development, metabolism and quality of in vitro produced bovine embryos form the mórula to the blastocyst stage, Zygote 2001;10:189-199.
[ Links ]DUMOLLARD R, WARD Z, CARROLL J, DUCHEN MR. Regulation of redox metabolism in the mouse oocyte and embryo. Development 2007; 134:455-465.
[ Links ]EPSTEIN CJ, SMITH S, TRAVIS B, TUCKER G. Both X chromosomes function before visible X-chromosome inactivation in female mouse embryos. Nature 1978;274:500-502.
[ Links ]FORETZ M, CARLING D, GUICHARD C, FERRÉ P, FOUFELLE F. AMPactivated protein kinase inhibits the glucose-activated expression of fatty acid synthase gene in rat hepatocytes. J Biol Chem. 1998;273:14767-14771.
[ Links ]GUILLET-DENIAU I, PICHARD A-L, KONÉ A, ESNOUS C, NIERUCHALSKI M, GIRARD J, PROP-BUUS C. Glucose induces de novo lipogenesis in rat muscle satellite cells through a sterol-regulatory-element-binding-protein-1c-dependent pathway. J Cell Sci. 2003;117:1937-1944.
[ Links ]GUTIERREZ-ADAN A, OTER M, MARTINEZ-MADRID B, PINTADO B, DE LA FUENTE J. Differential expression of two genes located on the X chromosome between male and female in vitro-produced bovine embryos at the blastocyst stage. Mol Reprod Dev. 2000;55:146-151.
[ Links ]GUTIÉRREZ-ADAN A, LONERGAN P., RIZOS D, WARD FA, BOLAND MP FAIR, PINTADO B, DE LA FUENTE J. Effect of the in vitro culture system on the kinetics of blastocyst development and sex ratio of bovine embryos. Theriogenology. 2001;55:1117-1126.
[ Links ]GUTIERREZ-ADAN A. Developmental consequences of sexual dimorphism for gene transcription during preimplantation embryonic development. The Society for the Study of reproduction -SSR. 38th Annual Meeting: July 24-27, 2005. Quebec City. Quebec, Canada. MS8.
[ Links ]GUTIERREZ-ADAN A; PEREZ-CRESPO M, FERNANDEZ-GONZALEZ R, RAMIREZ RA, MOREIRA P, PINTADO B, et al. Developmental consequences of sexual dimorphism during pre-implantation embryonic development. Reprod Domest Anim. 2006;41(Suppl 2):54-62.
[ Links ]HARDIE DG. Regulation of fatty acid synthesis via phosphorylation of acetyl-CoA carboxylase. Prog Lipid Res. 1989;28:117-146.
[ Links ]HIEMSTRA SJ, VAN DER LENDE T, WOELDERS H. The potential of cryopreservation and reproductive technologies for animal genetic resources conservation strategies. The role of biotechnology. Villa Gualino, Turin, Italy -5-7 March, 2005.
[ Links ]HILLGARTNER FB, SALATI LM, GOODRIDGE AG. Physiological and molecular mechanism involved in nutritional regulation of fatty acid synthesis. Physiol Rev. 1995;75:47-76.
[ Links ]HILLGARTNER FB, CHARRON T. Glucose stimulates transcription of fatty acid synthase and malic enzyme in avian hepatocytes. Am J Physiol Endocrinol Metab. 1998; 274: E493-E501.
[ Links ]HOCHI S, KIMURA K., HANADA A. Effect of linoleic acid-albumin in the culture medium on freezing sensitivity of in vitro-produced bovine morulae. Theriogenology. 1999;52:497-504.
[ Links ]IRITANI N. Nutritional and hormonal regulation of lipogenic-enzyme expression in rat liver. Eur J Biochem. 1992;205:433-442.
[ Links ]JANSEN S, ESMAEILPOUR T, PANTALEON M, KAYE L. Glucose affects monocarboxylate cotransporter (MCT) 1 expression during mouse preimplantation development. Reproduction. 2006;131:469-479.
[ Links ]JAVED MHM, WRIGHT JrRW. Determination of pentose phosphate and Embden-Meyerhof pathway activities in bovine embryos. Therogenlogy. 1991;1029-1037.
[ Links ]JOHNSON MT, MAHMOOD S, PATEL MS. Intermediary Metabolism and Energetics during Murine Early Embryogenesis. J. Biol. Chem. 2003;278:31457-31460.
[ Links ]KABASHIMA T, KAWAGUCHI T, WADZINSKI BE, UYEDA K. Xylulose 5phosphate mediates glucose-induced lipogenesis by xylulose 5-phosphate-activated protein phosphatase in rat liver. Proc Natl Acad Sci USA. 2003;100:5107-5112.
[ Links ]KANG R, YAMADA K, TANAKA T, LU T, NOGUCHI T. Relationship between the concentrations of glycolytic intermediates and expression of the L-type pyruvate kinase gene in cultured hepatocytes. J Biochem (Tokyo). 1996;119:162-166.
[ Links ]KAWAGUCHI T, TAKENOSHITA M, KABASHIMA, T., UYEDA K. Glucose and cAMP regulate the L-type pyruvate kinase gene by phosphorylation/ dephosphorylation of the carbohydrate response element binding protein. Proc Natl Acad Sci USA. 2001;98:13710-13715.
[ Links ]KIM K-H, LOPEZ-CASILLAS F, BAI DH, LIO X, PAPE ME. Role of reversible phosphorylation of acetyl-CoA carboxylase in long chain fatty acid synthesis. FASEB J. 1989;3:2250-2256.
[ Links ]KIM K-H. Regulation of mammalian acetyl-coenzyme A carboxylase. Ann Rev Nutr. 1997;17:77-79.
[ Links ]KIMURA K, SPATE LD, GREEN MP, ROBERTS RM. Effects of oxidative stress and inhibitors of the pentose phosphate pathway on sexually dimorphic of IFN-� by bovine blastocysts. Mol Reprod Dev. 2004;68:88-95.
[ Links ]KIMURA K, SPATE LD, GREEN MP, ROBERTS RM. Effects of D-glucose concentration, D-fructose, and inhibitors of enzymes of the pentose phosphate pathway on the development and sex bovine blastocysts. Mol Reprod Dev. 2005;72:201-207.
[ Links ]LATHMAN KE, PATEL B, BAUTISTA DM, HAWES SM. Effects of X chromosome number and parental origin on X-linked gene expression in preimplantation mouse embryos. Biol Reprod. 2000;63:64-73.
[ Links ]LARSON M, KIMURA K, KUBISCH HM., ROBERTS RM. Sexual dimorphism among bovine embryos in their ability to make the transition to expanded blastocyst and the expression of the signaling molecule IFN-� . Proc Natl Acad Sci USA. 2001;98:9677-9682.
[ Links ]LEESE HJ. Metabolic control during preimplantation mammalian development. Hum Reprod Update. 1995;1:63-72.
[ Links ]LEESE HL. Quiet please, do no disturb: a hypothesis of embryo metabolism and viability. BioEssays. 2002;24:845-849.
[ Links ]LEESE HJ, BARTON AM. Pyruvate and glucose uptake by mouse ova and preimplantation embryos. J Reprod Fertil. 1984;72:9-13.
[ Links ]LEIBO SP, LOSKUTOFF NM. Cryobiology of in vitro-derived bovine embryos. Theriogenology. 1993:39:81-94.
[ Links ]LONERGAN P, GUTIERREZ-ADAN A, PINTADO B, FAIR T, WARD F, DE LA FUENTE J, BOLAND M. Relationship between time of first cleavage and the expression of IGF-I growth factor, its receptor, and two housekeeping genes in bovine two-cell embryos and blastocysts produced in vitro. Mol Reprod Dev. 2000;57:146-152.
[ Links ]MASSILLON D, CHEN W, BARZILAI N, PRUS-WERTHEIMER D, HAWKINS M, LIU R, TAUB R, ROSSETTI L. Carbon flux via the pentose phosphate pathway regulates the hepatic expression of the glucose-6-phosphatase and phosphoenolpyruvate carboxykinase genes in conscious rats. J Biol Chem. 1998;273:228-234.
[ Links ]MOLEY KH, CHI MM, KNUDSON CM, KORSMEYER SJ, MUECKLER MM. Hyperglycemia induces apoptosis in pre-implantation embryos through cell death effector pathways. Nat Med. 1998a;4:1421-1424.
[ Links ]MOLEY KH, CHI MM, MUECKLER MM. Maternal hyperglycemia alters glucose transport and utilization in mouse preimplantation embryos. Am J Physiol. 1998b;275:E38-47.
[ Links ]MOORE K, QUADROS BA. Cryopreservation of Mammalian Embryos: The State of the Art. ARBS Annual Review of Biomedical Sciences. 2006;8:19-32.
[ Links ]NEDAMBALE T, DINNYÉS A, YANG X, TIAN XC. Bovine blastocyst development in vitro: timing, sex, and viability following vitrification. Biol Reprod. 2004;71:1671-1676.
[ Links ]NISHIMURA M, UYEDA K. Purification and Characterization of a Novel Xylulose 5-Phosphate-activated Protein Phosphatase Catalyzing Dephosphorylation of Fructose-6-phosphate, 2-kinase:Fructose-2,6-bisphosphatase. J Biol Chem. 1995;270:26341-26346.
[ Links ]PARK J, RHO HK, KIM KH, CHOE SS, LEE YS, KIM JB. Overexpression of glucose-6-phosphate dehydrogenase is associated with lipid dysregulation and insulin resistance in obesity. Mol Cell Biol. 2005;25:5146-5157.
[ Links ]PEIPPO J, KURKILAHTI M, BREDBACKA P. Developmental kinetics of in vitro produced bovine embryos: the effect of sex, glucose and exposure to time-lapse environment. Zygote. 2001;9:105-1113.
[ Links ]PEREIRA RM, BAPTISTA MC, VASQUES MI, HORTA AEM, PORTUGAL PV, BESSA RJB, et al. Cryosurvival of bovine blastocysts is enhanced by culture with trans10 cis-12 conjugated linoleic acid (10t,12c CLA). Animal Reproduction Science. 2007;98:293-301.
[ Links ]PEREZ-CRESPO M, RAMIREZ MA, FERNANDEZ-GONZALEZ R, RIZOS D, LONERGAN P, PINTADO B, GUTIERREZ-ADAN A. Differential sensitivity of male and female mouse embryos to oxidative induced heat-stress is mediated by glucose-6-phosphate dehydrogenase gene expression. Mol Rep Dev. 2005;72:502-510.
[ Links ]POLLARD JW, LEIBO SP. Chilling sensitivity of mammalian embryos. Theriogenology. 1994;41:101-106.
[ Links ]PRIP-BUUS C, PERDEREAU D, FOUFELLE F, MAURY J, FERRE P, GIRARD J. Induction of fatty-acid-synthase gene expression by glucose in primary culture of rat hepatocytes. Dependency upon glucokinase activity. Eur J Biochem. 1995;230:309-315.
[ Links ]RIEGER D, LOSKUTOFF NM, BETTERIDGE KJ. Developmentally related changes in the uptake and metabolism of glucose, glutamine and pyruvate by cattle embryos produced in vitro. Reprod Fertil Dev. 1992;4:547-557.
[ Links ]RILEY J, MOLEY KH. Glucose utilization and the PI3-K pathway: mechanisms for cell survival in preimplantation embryos. Reproduction. 2006;131:823-835
[ Links ]RIZOS D, GUTIÉRREZ-ADÁN A, PÉREZ-GARNELO S, DE LA FUENTE J, BOLAND MP, LONERGAN P. Bovine embryo culture in the presence or absence of serum: implications for blastocyst development, cryotolerance, and messenger RNA expression. Biol Reprod. 2003;68:236-243.
[ Links ]ROY R, TAOURIT S, ZARAGOZA P, EGGEN A, RODELLAR C. Genomic structure and alternative transcript of bovine fatty acid synthase gene (FASN): comparative analysis of the FASNgene between monogastirc and ruminant species. Cytogenet Genome Res 2005; 111:65-73.
[ Links ]SALATI LM, AMIR-AHMADY B. Dietary regulation of expression of glucose -6- phosphate dehydrogenase. Annu Rev Nutr 2001; 21:121-140. [ Links ]
SEIDEL GE. Modifying oocytes and embryos to improve their cryopreservation. Theriogenology 2006; 65:228-235. [ Links ]
SMITH S. The animal fatty acid synthase: one gen, one polypeptide, seven enzymes. FASEB J 1994; 8:1248-1259. [ Links ]
STABILÉ LP. Regulation of glucose-6-phosphate dehydrogenase by polyunsaturated fatty acids in cultured rat hepatocytes (tesis de doctorado). Morgantown: Department of Biochemistry, School of Medicine, West Virginia University; 1999. [ Links ]
SWAIN JE, BORMANN CL, CLARK SG, WALTERS EM, WHEELER MB, KRISHER RL. Use of energy substrates by various stage preimplantation pig embryos produced in vivo and in vitro. Reproduction 2002; 123:253-60. [ Links ]
THOMPSON JG, PARTRIDGE J, HOUGHTON FD, COX CI, LEESE HJ Oxygen uptake and carbohydrate metabolism by in vitro derived bovine embryos. J Reprod Fertil 1996; 106:299-306. [ Links ]
TIAN XC, SMITH SL, ZHANG SQ, KUBOTA C, CURCHOE C, XUE F, et al. Nuclear reprogramming by somatic cell nuclear transfer the cattle story. Soc Reprod Fertil Suppl. 2007; 64:327-39. [ Links ]
TIFFIN GJ, RIEGER D, BETTERIDGE KJ, YADAV BR, KING WA. Glucose and glutamine metabolism in pre-attachment cattle embryos in relation to sex and stage of development. J Reprod Fertil 1991; 93:125-132. [ Links ]
TOMINAGA K, SHIMIZU M, OOYAMA S, IZAIKE Y. Effect of Lipid Polarization by Centrifugation at Different Developmental Stages on Post-Thaw Survival of Bovine in vitro Produced 16-Cell Embryos. Theriogenology 2000; 53:1669-1680. [ Links ]
USHIJIMA H, YAMAKAWA H, NAGASHIMA H. Cryopreservation of bovine pre-morula-stage in vitro matured/in vitro fertilized embryos after delipidation and before use in nucleus transfer. Biol Reprod 1999; 60:534-539. [ Links ]
VAULONT S, VASSEUR-COGNET M, KAHN A. Glucose regulation of gene transcription. J Biol Bioch 2000; 275:31555-31558. [ Links ]
YAMASHITA H, TAKENOSHITA M, SAKURAI M, BRUICK RK, HENZEL WJ, SHILLINGLAW W et al. A glucose-responsive transcription factor that regulates carbohydrate metabolism in the liver. Proc Natl Acad Sci USA 2001; 98:9116-9121. [ Links ]
WRENZYCKI C, LUCAS-HAHN A, HERRMANN D, LEMME E, KORSAWE K, NIEMANN H. in vitro Production and Nuclear Transfer Affect Dosage Compensation of the X-Linked Gene Transcripts G6PD, PGK, and Xist in Preimplantation Bovine Embryos Biol Repro 2002; 66:127-134. [ Links ]














