Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.15 no.1 Bogotá Jan./Apr. 2010
INDUCCIÓN DE FENILALANINA AMONIO LIASA Y VARIACIÓN EN EL CONTENIDO DE COMPUESTOS FENÓLICOS EN FRUTOS DE LULO (Solanum quitoense Lam) INFECTADOS CON Colletotrichum acutatum.
Induction of phenylalanine ammonia lyase and variation in phenolic compounds content in Lulo fruits (Solanum quitoense Lam) infected by Colletotrichum acutatum).
MAIRA ANDREA ARRIETA-GUEVARA1 Ms. Sc, BLANCA LIGIA HIGUERA-MANCIPE1 Dr. Sc. Ciencias-Química, SIXTA TULIA MARTÍNEZ-PERALTA1, Ms. Sc. 1 Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia-Sede, Carrera 30 No. 45-08. Bogotá, Colombia, Correspondencia: maarrietag@unal.edu.co , blhiguerad@unal.edu.co .
Presentado 7 de septiembre de 2009, aceptado 5 de noviembre de 2009, correcciones 14 de diciembre de 2009
RESUMEN
Se evaluó la dinámica de la actividad fenilalanina amonio liasa (PAL) en corteza de frutos de lulo (Solanum quitoense Lam) con el fin de determinar su participación en respuestas bioquímicas hacia Colletotrichum acutatum. Se establecieron como mejores condiciones para la extracción de la enzima, buffer ácido bórico-borato de sodio 0.1M pH 8.8, 1% SDS, 3% PVPP y para medir la actividad, sustrato L-fenilalanina 5 mM, pH 8,0, 20°C, 30 μL de extracto y 45 min. Se realizó un ensayo in vivo usando frutos en tres estados de madurez, los cuales fueron inoculados con el patógeno o tratados con agua estéril. A cinco tiempos (hpi = horas post-infección) se determinó la actividad PAL y el contenido total de fenoles, encontrándose que hay una respuesta diferencial de la enzima por efecto del patógeno y por el estado de madurez. Para frutos en el estado pintón se obtuvo el mayor aumento de PAL, el que perduró hasta 48 hpi, al compararlo con los controles y con los otros dos estados de madurez. Este aumento mostró relación con un marcado incremento en el contenido total de fenoles y con el desarrollo más tardío de síntomas característicos de antracnosis, observado para los frutos pintones. Estos resultados permiten postular, una posible relación positiva entre inducción de PAL, aumento de fenólicos y respuesta de tolerancia a C. acutatum. Para lulos en estado verde y maduro se observó aumento de PAL a 12 y 24 hpi que coincidió también con incremento en el contenido de fenoles totales, aunque para estos dos últimos estados dicho contenido disminuyó significativamente a tiempos mayores.
Palabras clave: Lulo, fenilalanina amonio liasa, antracnosis, enzimas de defensa vegetal.
ABSTRACT
Phenylalanine ammonia lyase (PAL) activity induction was evaluated in lulo fruits to determine the role of this enzyme in biochemical responses towards the pathogen Colletotrichum acutatum. We studied the experimental conditions to obtain the enzyme, using lulo peel, and found that the best conditions for extraction were buffer of boric acid-sodium borate 0.1M pH 8.8, 1% SDS, 3% PVPP and, for measuring the enzymatic activity: L- phenylalanine 5mM, pH 8.0, 20°C, 30 μL of extract and incubation during 45 min. Then, we performed an in vivo assay using lulo fruits in three maturity stages, which were inoculated either with the fungus or sterile water. Enzymatic induction was studied at five post-inoculation times, and it was found that there is a differential response as a consequence of the presence of the pathogen and the maturity stage. In semi-mature lulos, a bigger increase in PAL was obtained among 12-48 hpi which is related to a higher content of phenolic compounds and to the latest development in the characteristic symptoms of anthracnose. These results allow postulating, in a preliminary way, a possible positive relationship between inductions of PAL, phenolics and responses of tolerance to C. acutatum. For green and mature lulos we observed as well, an increase of PAL activity but only at 12 and 24 hpi which showed relation with an increase in the total phenolic content. However, for these stages the phenolics were significantly lower at higher times.
Key words: Lulo, phenylalanine ammonia lyase, anthracnose, vegetal defense enzymes.
INTRODUCCIÓN
Un importante número de frutas de origen andino tienen gran potencial de convertirse en productos de exportación con un alto beneficio económico para los agricultores. Entre estas frutas, el lulo ó naranjilla (Solanum quitoense Lam), originario de los bosques húmedos subtropicales de Colombia, Ecuador y Perú, ha sido seleccionado por el DANE (2004) como una de las diez frutas más promisorias en Colombia debido a su valor nutritivo, sabor agridulce, aroma particular y posibilidad de usos agroindustriales; correspondiendo su produción a 11.36% entre las diez. Sin embargo, esta especie tiene limitantes importantes que restringen su cultivo, como son la susceptibilidad a enfermedades ocasionadas por hongos y virus, problemas de deterioro post-cosecha, heterogeneidad en la calidad de la fruta, disponibilidad limitada del material libre de patógenos, entre otros. La antracnosis producida por el hongo Colletotrichum acutatum (Tamayo, 2001; Cerón, 2005) es una enfermedad que ocasiona pérdidas importantes en los cultivos de lulo con el correspondiente impacto socio-económico.
A pesar del potencial económico que representan los frutos para el país, no se dispone actualmente de un conocimiento científico básico que permita caracterizar, desde el punto de vista bioquímico, las principales enfermedades que los afectan, en especial aquellas que son de particular impacto económico. Dicho conocimiento es básico para implementar programas de manejo de estas enfermedades y para la obtención de variedades resistentes. En el país se han realizado estudios sobre el fruto de lulo pero enfocados principalmente a caracterizar procesos fisiológicos de poscosecha (Cortés, 2006; Rubio, 1999). Son escasos los reportes conocidos hasta el momento de estudios referentes a la caracterización de los eventos bioquímicos que median la interacción del fruto de lulo con el patógeno que causa la antracnosis y que aporten al conocimiento científico básico de la enfermedad, el cual es fundamental para poder buscar estrategias tendientes a disminuir la susceptibilidad del fruto frente al patógeno. Se conocen sólo los trabajos recientes (Caicedo e Higuera, 2007; Caicedo et ál., 2009) en este mismo modelo, en los que se reportó inducción de las enzimas polifenoloxidasa y peroxidasa como respuesta a este patógeno, inducción que presentó dependencia con el tiempo y con el estado de madurez. En estos estudios se postuló una posible relación positiva entre inducción enzimática más rápida y síntomas más tardíos de la enfermedad. El objetivo del presente estudio fue evaluar la actividad de la enzima fenilalanina amonio liasa en corteza de frutos de lulo en tres estados de madurez sometidos a la acción del patógeno C. acutatum, con el fin de determinar su posible participación en respuestas bioquímicas del hospedero y su relación con el contenido de compuestos fenólicos totales y con el desarrollo de la enfermedad antracnosis. Esta enzima es clave y la primera en la ruta fenilpropanoide, ruta metabólica involucrada con frecuencia en mecanismos de defensa vegetal.
MATERIALES Y MÉTODOS
MATERIAL BIOLÓGICO
Se utilizó una cepa del hongo Colletotrichum acutatum, adquirida en el cepario del departamento de Microbiología de la Universidad de los Andes, la cual fue cultivada en medio PDA (papa-dextrosa-agar) a 20 °C y sub-cultivada en medio líquido papa-dextrosa, manteniendo el cultivo en agitación constante por 10-12 días a 20 °C. A partir de este cultivo se preparó una suspensión (1x106 conidias/ mL) para la inoculación de los frutos. Los materiales vegetales usados fueron frutos de lulo (Solanum quitoense) var. quitoense, cosechados en tres estados de madurez (verde, pintón y maduro) provenientes de un mismo cultivo de Campohermoso (Boyacá) situado a 1.300 msnm y temperatura promedio de 23°C.
SELECCIÓN DE LAS CONDICIONES EXPERIMENTALES PARA LA EXTRACCIÓN DE LA ENZIMA FENILALANINA AMONIO LIASA (EC 4.3.1.5) A PARTIR DE LA CORTEZA DE LOS FRUTOS
Para la extracción se tomaron 500 mg de corteza de lulo y se maceraron en presencia de nitrógeno líquido, seguido de tres lavados consecutivos con 2 mL de acetona fría (4 ºC) cada uno. Las muestras fueron luego centrifugadas por 10 min a 10.000 x g. Sobre el péllet obtenido se evaluaron 9 sistemas de extracción, empleando como buffer de partida ácido bórico / borato de sodio 0.1 M, pH 8.8 , SDS (dodecil sulfato de sodio) al 1 %; se utilizó un diseño experimental del tipo cuadrado latino, se evaluaron 3 variables, la primera relacionada con la composición del buffer (adición de polivinilpolipirrolidona / PVPP 0%, 3%, 5%), la segunda referente a la relación buffer: material vegetal (1:2, 1:3, 1:4) y la tercera sobre el tiempo de extracción (30, 45 y 60 min). Se realizaron tres réplicas por sistema evaluado. Una vez obtenidos los extractos enzimáticos, se determinó la actividad PAL (Ardila, 2005) con el fin de establecer el buffer con el cual se logra la mayor actividad de esta enzima.
SELECCIÓN DE PARÁMETROS ADECUADOS PARA LA MEDIDA DE ACTIVIDAD ENZIMÁTICA PAL
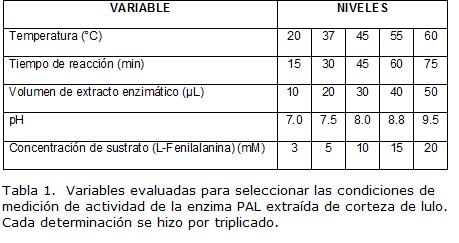
Se estudiaron diversas condiciones experimentales (Tabla 1) para poner a punto la medida de actividad PAL tomando como base, para la escogencia de estos intervalos, reportes previos (Ardila, 2005; Kovacik y Backor., 2007). La actividad enzimática se determinó espectrofotométricamente midiendo el cambio de absorbancia a 270 nm y se expresó como nmoles de ácido trans-cinámico/min*mg de proteína. La mezcla de reacción contenía el extracto enzimático, 400 μL de sustrato (L-fenilalanina) y buffer boratos 0.1 M, con pH según valor a evaluar. Los parámetros se estudiaron siguiendo un diseño experimental escalonado. Cada determinación se hizo por triplicado.
CUANTIFICACIÓN DE PROTEÍNA
El contenido de proteína se determinó en los diferentes extractos por el método de Lowry (Deutscher, 1990) usando BSA (albúmina de suero bovino) como estándar. Cada determinación se realizó por triplicado.
PROPIEDADES FISICOQUÍMICAS DE LOS FRUTOS DE LULO (Solanum quitoense L)
Con el fin de establecer el índice de madurez, y clasificar con éste los frutos usados en el estudio, y para evaluar si se presenta alguna relación entre propiedades fisicoquímicas y desarrollo de los síntomas de antracnosis, se realizó la determinación de los parámetros: pH (utilizando un potenciómetro SCHOOT Handylab pH/LF12®), dureza, acidez titulable y grados Brix. La acidez se determinó realizando una titulación ácido base con NaOH 0,1 N (Norma Técnica Colombiana, NTC 4623) y se expresó como % de ácido cítrico. Los grados Brix (sólidos solubles) se evaluaron según NTC 4624, colocando la pulpa sobre un refractómetro (ATAGO 8682®) a temperatura ambiente. Todas estas determinaciones se realizaron por triplicado.
EVALUACIÓN DE LA INDUCCIÓN DE PAL POR EFECTO DE LA INFECCIÓN DE LOS FRUTOS DE LULO CON C. acutatum
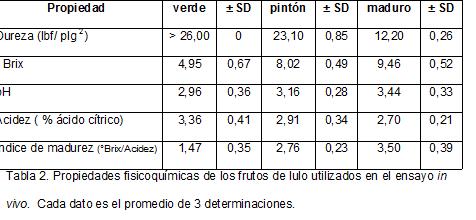
Los frutos para el ensayo in vivo fueron clasificados en verde, pintón y maduro haciendo uso del índice de madurez (°Brix/acidez titulable) (Tabla 2). Los frutos fueron previamente desinfectados por lavado con solución de hipoclorito de sodio al 5%, luego lavados exhaustivamente con agua estéril y una vez secos, se inocularon con 15 μL de una suspensión del patógeno (C. acutatum) de concentración aproximada 1x106 conidias/mL, sobre una herida superficial hecha con bisturí (1 cm de longitud) en dos sitios opuestos (simétricos) del fruto. Adicionalmente, se trataron de la misma forma frutos que se usaron como testigo, a los cuales se les colocó el mismo volumen de agua estéril en vez de la suspensión del patógeno, y también se usaron frutos sin ningún tratamiento (frutos control). Se almacenaron luego en frascos de vidrio (un fruto por frasco) provistos de una servilleta humedecida con agua (todo el sistema previamente esterilizado) con el fin de mantener una humedad relativa elevada. Se taparon con vinilpel y se mantuvieron todos los frutos bajo las mismas condiciones de temperatura y luz. Se realizaron muestreos a las cero, 12, 24, 48 y 72 horas post-inoculación (hpi), tomando en cada tiempo tres frutos por tratamiento y por estado de madurez, a los que se les retiró la corteza cercana al área de inoculación (en todos los casos se tomó un área de 1 cm2) y se registró la aparición de algún signo visible del desarrollo de la enfermedad como por ejemplo, aparición y profundidad de manchas necróticas alrededor del sitio de infección y aparición de micelio algodonoso. Sobre estas muestras se realizó la extracción y se evaluó la actividad PAL. Se conservaron muestras de lulo inoculadas, durante tiempos mayores, para ser usados como control positivo del desarrollo de la enfermedad.
DETERMINACIÓN DEL CONTENIDO DE FENOLES TOTALES
Para la determinación del contenido de compuestos fenólicos totales presentes en la corteza de los frutos inoculados con el patógeno y en los inoculados con agua estéril, se tomaron 500 mg de la muestra los cuales fueron macerados con nitrógeno líquido. Luego se realizó la extracción de los compuestos fenólicos para cada muestra agitándola por un periodo de 30 segundos con acetona fría en proporción 1:2. Posteriormente se centrifugó durante 10 minutos, a 4 °C, 7000 g y se retiró el sobrenadante (este procedimiento fue realizado tres veces). Los sobrenadantes fueron recolectados en frascos ámbar y refrigerados a -20 °C hasta su posterior análisis. La cuantificación de los compuestos fenólicos totales se realizó utilizando el método de Folin-Ciocalteu´s (Makkar et ál., 2000) determinando el cambio de absorbancia a 765 nm con ayuda de una curva de calibración realizada con ácido gálico como patrón (Sigma-Aldrich Chem. Co) en un intervalo de concentración entre 0 y 25 ppm. El contenido de fenoles totales fue expresado como ppm de ácido gálico por mg de material vegetal.
ANÁLISIS ESTADÍSTICO
Los resultados obtenidos se procesaron usando análisis de varianza (ANDEVA) y pruebas de rango múltiple (P=0,05), usando el programa Statgraphics Plus 5.1®. Se utilizó la prueba de Diferencias Mínimas Significativas (DMS).
RESULTADOS Y DISCUSIÓN
SELECCIÓN DE CONDICIONES ADECUADAS PARA LA EXTRACCIÓN DE LA ENZIMA PAL
Los resultados obtenidos al evaluar los nueve sistemas de extracción se muestran en la Figura 1. El análisis de estos resultados (ANDEVA) indicó que el sistema compuesto por buffer boratos 0.1M pH 8,0, 1 % de SDS, 3 % de PVPP, en proporción 1:2 (material vegetal: buffer) y agitación durante 45 minutos (2 en la Figura 1), permitió obtener los mayores valores de actividad PAL, con diferencias significativas (P= 0,05) respecto a los demás sistemas estudiados. Por tanto, se seleccionó éste como el más adecuado para la extracción de PAL a lo largo del estudio de inducción. Este resultado coincide con algunos reportes (Alunni et ál., 2003) en los cuales se indica que el uso de PVPP (polímero insoluble) ayuda a retirar los compuestos fenólicos remanentes después del tratamiento con acetona fría, los cuales pueden actuar como inhibidores de la enzima PAL.
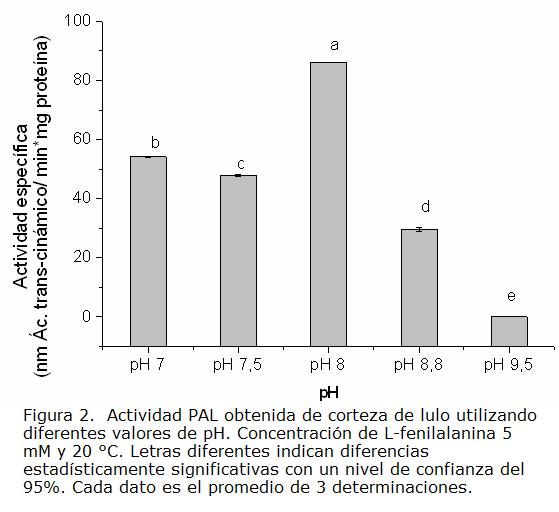
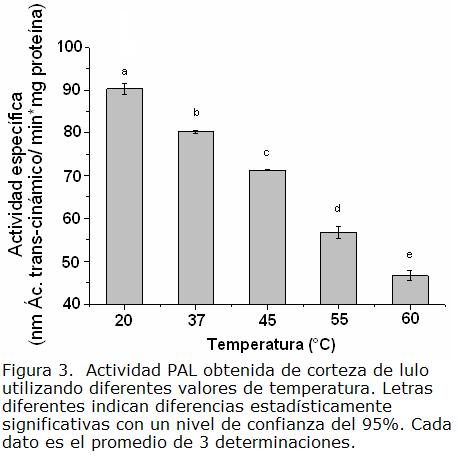
DETERMINACIÓN DE LAS CONDICIONES APROPIADAS PARA MEDIR ACTIVIDAD ENZIMÁTICA DE FENILALANINA AMONIO LIASA (PAL)
Para establecer las condiciones adecuadas de pH, temperatura, volumen de extracto enzimático y concentración de sustrato, para la medida de actividad PAL, se midió la actividad específica utilizando el sistema de extracción No. 2 (Figura 1) y el dato del contenido de proteína de cada extracto enzimático evaluado. En las Fig. 2 a Fig. 6, se presentan los valores obtenidos para cada parámetro experimental estudiado. Teniendo en cuenta estos resultados, se pudo establecer que los parámetros adecuados para la medida de actividad de la enzima PAL, extraída a partir de corteza de lulo, son: pH 8,0; sustrato L- fenilalanina 5 mM, 20 °C, 30 μL de extracto enzimático y 45 minutos de tiempo de incubación, dados los mayores valores de actividad obtenidos, con diferencias significativas respecto a las otras condiciones evaluadas. Al comparar con diversos reportes de literatura se encontró que el pH es similar al obtenido para PAL de tomate (Sudhamoy et ál., 2008), lechuga (Hyodo et ál., 1978), avena (Rybka et ál., 1998). Sin embargo, se encontraron diferencias con respecto a datos cinéticos de otras PAL´s estudiadas en diferentes fuentes vegetales, las cuales pueden ser atribuidas posiblemente a la existencia de diferentes isoformas de PAL presentes en las especies vegetales. Para el caso de la extraída del fruto de lulo se observa que a concentraciones de sustrato por encima de 20 mM la actividad disminuye significativamente, posiblemente por inhibición por efecto del producto de reacción. En cuanto al tiempo de reacción, en otros estudios se ha reportado 60 minutos como el tiempo óptimo (Zhang et ál., 2008; Kovacik y Backor, 2007; Morelló et ál., 2005). En el presente estudio, el tiempo de reacción encontrado fue de 45 minutos; la diferencia puede ser atribuida a la presencia de diferentes isoformas de PAL en las especies vegetales. Puede postularse que las isoformas de PAL presentes en corteza de lulo son más activas, en comparación con las encontradas por ejemplo en alfalfa, pimienta, pepino, entre otras, (Orr et ál., 1993; Garmendia et ál., 2006; Shaldea et ál., 2003).
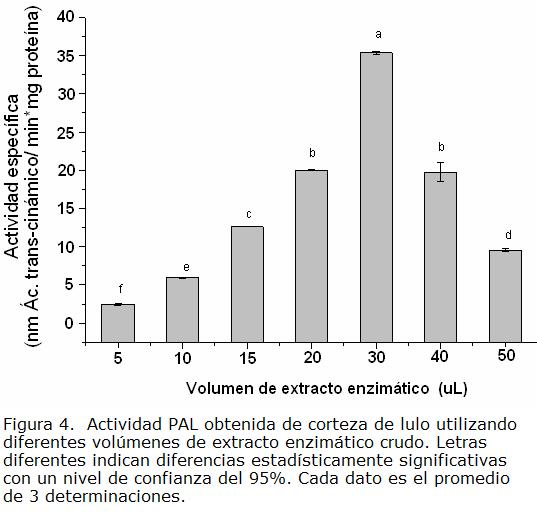
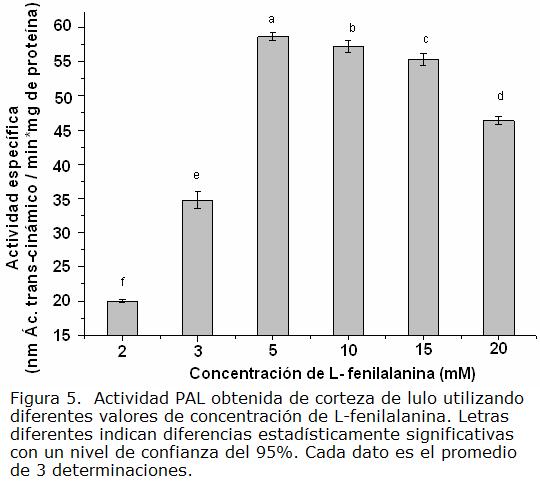
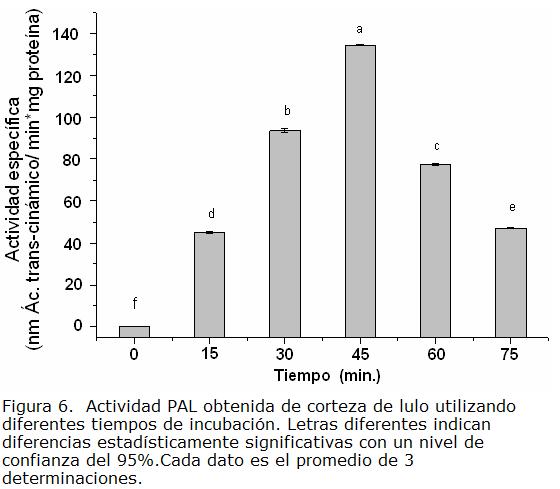
Es de resaltar que para lulo no se encuentran estudios de caracterización de enzimas en general, y menos aún de las involucradas en respuestas de defensa frente a patógenos, y tampoco se dispone de mayor información sobre la cinética de esta enzima en particular.
PROPIEDADES FISICOQUÍMICAS DE LOS FRUTOS DE LULO
En la Tabla 2 se indican los resultados obtenidos para algunos parámetros fisicoquímicos de los frutos usados en la investigación. Con base en la relación entre los grados Brix y la acidez, se clasificaron los frutos para conformar los grupos correspondientes a los estados verde, pintón y maduro. Cabe mencionar que estos valores están acordes con lo reportado en estudios previos (Casierra, et ál., 2004, Caicedo, 2005; Caicedo e Higuera, 2007), realizados usando lulos de la misma variedad que los que se emplearon en este estudio. Como se muestra en la Tabla 2, no se obtuvieron diferencias marcadas en la mayoría de las propiedades medidas, por tanto, no es posible inferir que alguna de éstas favorezca o no la invasión por parte del patógeno. En la propiedad que se observó mayor diferencia con el estado de madurez fue en la dureza, pero no se pudo establecer que existiera relación con la infección, pues los frutos con mayor dureza (verdes) fueron, en este estudio, los más susceptibles a desarrollar síntomas de infección. La poca diferencia en propiedades como pH y acidez entre los tres estados de madurez ya ha sido previamente documentada para el lulo y es por ello que estos parámetros no se utilizan por lo general para caracterizar el grado de madurez del fruto.
EVALUACIÓN DEL COMPORTAMIENTO DE LA ENZIMA FENILALANINA AMONIO LIASA (PAL) EN FRUTOS DE LULO (Solanum quitoense Lam) FRENTE AL ATAQUE DEL PATÓGENO Colletotrichum acutatum DURANTE LA INTERACCIÓN FRUTO- PATÓGENO
Evaluación de síntomas de antracnosis
Los resultados de la evaluación visual diaria de los frutos permitieron establecer que los síntomas característicos, tales como manchas necróticas y aparición de micelio algodonoso sobre la zona de inoculación, se presentaron en promedio a 72 hpi para los frutos en estado verde y maduro, siendo más afectados los frutos en estado verde, mientras que los frutos en estado pintón fueron los menos afectados. En estos últimos, la aparición de síntomas se observó solo a partir de 144 hpi. Ninguno de los frutos control o testigo presentó evidencias de antracnosis durante el tiempo que duró el experimento. Se comprobó, así mismo, que los frutos usados para el estudio estaban inicialmente libres del patógeno, mediante cultivo de muestras de corteza tomadas al azar en medio PDA durante 7 días. En ninguna caja se observó crecimiento alguno de microorganismos.
Evaluación de la inducción de la enzima fenilalanina amonio liasa (PAL) durante el ensayo In vivo
Los resultados de actividad PAL obtenidos a cada tiempo de muestreo se analizaron estadísticamente entre tratamientos, a un determinado tiempo, para establecer una posible inducción por efecto del patógeno.
a) Estado de madurez verde. En la Figura 7 se comparan los resultados de actividad PAL obtenidos a los diferentes tiempos para lulos en estado verde, durante el ensayo de inoculación. Entre 12 y 24 hpi la actividad PAL aumentó significativamente en los tres tratamientos, pero en los frutos inoculados con el hongo el aumento fue mayor. Dicha inducción de la enzima puede atribuirse a un cambio en el metabolismo del fruto que puede estar relacionado con respuestas a la presencia del patógeno, pues al realizar la comparación con el respectivo control y con el testigo se observa una diferencia significativa. Este comportamiento coincide con otros modelos reportados en la literatura como es el caso de avena - Stagonospora nodorum (Rybka et ál., 1998), pimienta- Verticillium dahliae (Garmendia et ál., 2006), alfalfa- Verticillium albo-atrum (Koike y Nanbu, 1997). Cabe anotar que a partir de 48 hpi las actividades PAL para frutos en estado verde en los tres tratamientos fueron notablemente menores a las que se determinaron para frutos en estado pintón y aún para los maduros y esta respuesta podría estar relacionada con el grado de severidad de la enfermedad, pues en frutos verdes los síntomas se presentaron más rápido, si se comparan con los otros dos estados de madurez.
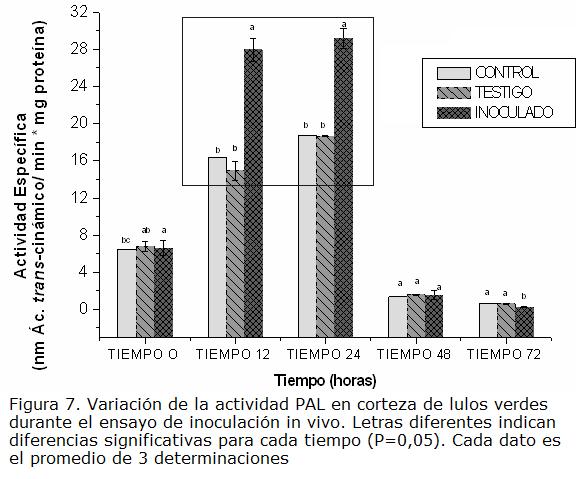
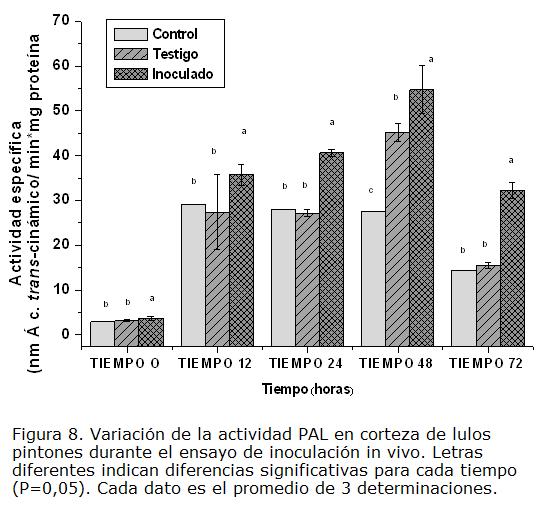
b) Estado de madurez pintón. En la Figura 8, se presentan los resultados obtenidos para el comportamiento de la enzima PAL obtenida de frutos en estado pintón durante el ensayo In vivo de respuesta a la inoculación. Puede apreciarse un aumento significativo, que perduró a todo lo largo de los tiempos evaluados, para el caso de los frutos sometidos a la inoculación con el patógeno. Dicho aumento puede atribuirse a una respuesta del fruto al hongo, dadas las diferencias con sus respectivos controles. Se descarta que este aumento pueda deberse sólo a respuesta al estrés de la herida pues la actividad obtenida es mucho más alta que la que se observó para los frutos testigos (también sometidos a inoculación pero con agua). Se encontró, además, que las actividades PAL para los frutos en este estado de madurez son, en general, significativamente más altas (casi el doble) si se comparan con las obtenidas en los estados verde y maduro (Fig. 7 y Fig. 9). Esta notable diferencia en la magnitud de actividad PAL, observada para los tres tratamientos, puede estar asociada con los metabolismos activos que tienen lugar en el fruto que está en proceso de maduración, además de la ya comentada y evidente inducción en los que estuvieron sometidos a la acción del hongo. Los resultados permiten entonces asociar una importante inducción de actividad de la enzima PAL con la respuesta de los frutos al patógeno C. acutatum. La literatura reporta modelos en los que PAL ha sido relacionada con estreses, ya sea bióticos ó abióticos, como es el caso de espárrago- Fusarium oxysporum f. sp asparagi (Chenyang et ál., 2001), caupí- Rhizoctonia solani (Chandra et ál., 2007), canola- Leptosphaeria maculans (Chakraborty et ál., 1993). Al analizar la observación de los síntomas de la enfermedad con relación a la actividad PAL, puede postularse una posible relación positiva entre inducción de esta enzima y retardo en la aparición de síntomas característicos de ésta, pues como se anotó anteriormente, en este estudio los frutos en estado pintón fueron los que tardaron más en presentarlos.
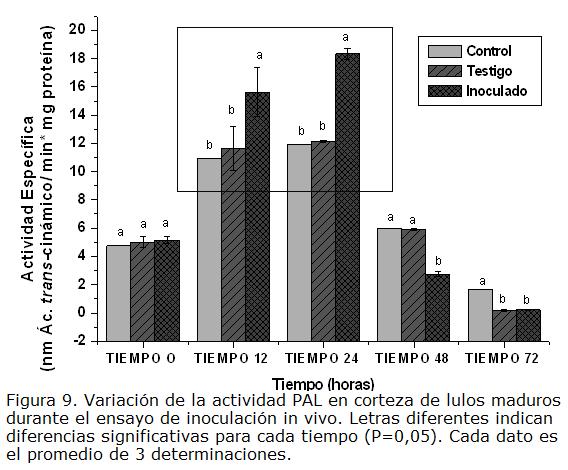
c) Estado maduro. En la Figura 9 se muestran los resultados obtenidos para actividad PAL de corteza de frutos en estado maduro. Como se observa, se presentó también aumento a tiempos 12 y 24 hpi, el cual fue significativamente mayor en los frutos inoculados con el patógeno. Puede entonces postularse que hay una inducción de PAL la cual se asocia con una respuesta del fruto frente al estrés ocasionado por la inoculación con el patógeno, dado que para los frutos testigo y control los valores fueron significativamente menores. A 48 y 72 hpi los valores de actividad PAL disminuyeron en forma importante para los tres tratamientos y no se observó diferencia en los inoculados con el hongo. Cabe resaltar que las magnitudes de la actividad PAL obtenidas para este estado de madurez fueron notablemente menores si se comparan con los estados pintón y verde. Aunque no existen reportes donde se correlacione la incidencia de la enfermedad con el estado de madurez en frutos como el lulo, es claro que durante los procesos de maduración se promueven cambios bioquímicos y/o histológicos que pueden tener incidencia durante la interacción hospedero-patógeno.
EVALUACIÓN DEL CONTENIDO DE FENOLES TOTALES
La determinación del contenido de fenoles totales se realizó con el fin de evaluar si se presenta un aumento en la concentración de estos compuestos, producto de los cambios metabólicos que se suceden en los frutos como consecuencia de la inoculación con el patógeno, y si este aumento tiene relación con la inducción observada de la enzima PAL.
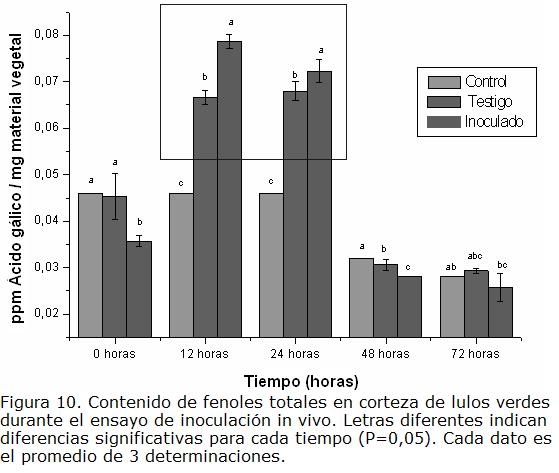
a) Frutos en estado verde. Los resultados obtenidos para este estado de madurez, los cuales se presentan en la Figura 10, muestran a tiempos 12 y 24 hpi un alto contenido de fenoles en los frutos testigo y los inoculados con el patógeno, aumento que puede estar relacionado con el estrés producido a causa de la herida ocasionada con el bisturí. Sin embargo, puede apreciarse que en los frutos inoculados con C. acutatum el contenido de fenoles es significativamente mayor. Este aumento coincide con el aumento de la actividad PAL observado a estos tiempos, y este comportamiento puede también ser atribuido a una respuesta del fruto frente al ataque del hongo. A partir de 48 hpi se aprecia una disminución notable en el contenido de fenoles para los tres tratamientos, hecho este que coincide con la aparición de los primeros síntomas de la enfermedad, como la aparición de manchas necróticas y la formación de micelio algodonoso en el sitio de la inoculación, indicando que la defensa pasiva del fruto ha sido vulnerable al ataque del patógeno. Cabe recordar que los frutos en estado verde fueron los que presentaron primero los síntomas de antracnosis.
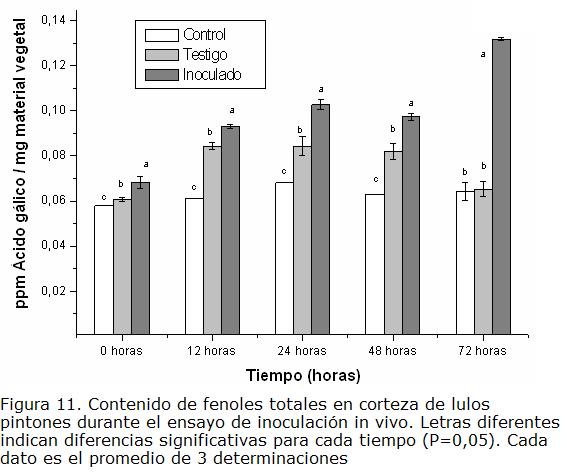
b) Frutos en estado pintón. La Figura 11 muestra los resultados obtenidos en la determinación del contenido de fenoles para los frutos en estado pintón durante el ensayo de inoculación. Como en el caso de los frutos verdes, se aprecia un incremento significativo en el contenido de fenoles para los frutos sometidos al estrés del corte. Sin embargo, para los inoculados con el hongo el aumento fue mayor en comparación con los controles y testigos. Es muy notable el aumento observado a 72 hpi para los sometidos a la acción del patógeno (más del doble respecto a los controles), hecho que no sucedió con los frutos en estado verde. Puede determinarse que dicho aumento se relaciona con una respuesta del hospedero al patógeno, pues las diferencias que hay entre los frutos testigo y los inoculados con el hongo son significativas. Esta acumulación de compuestos fenólicos presentó relación con la elevada actividad PAL obtenida durante el ensayo In vivo, a partir de 48 hpi para este estado de madurez, que como se anotó antes, fue en el que se demoró más la aparición de síntomas de la enfermedad. No se observó disminución a los tiempos mayores (48 y 72 hpi) como sucedió con los frutos verdes y maduros.
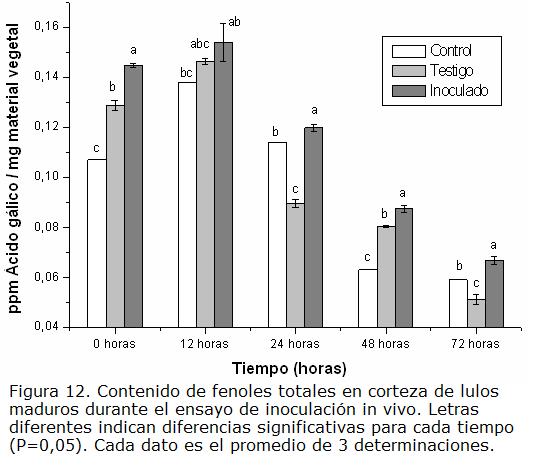
c) Frutos en estado maduro. Se observó que a tiempos tempranos (0 y 12 hpi) el contenido de fenólicos es mayor comparado con los otros dos estados evaluados, para los tres tratamientos (Figura 12). Sin embargo, dicho contenido presentó una disminución significativa a partir de 24 hpi, tal como sucedió en los frutos verdes, la que podría estar entonces relacionada con la más rápida aparición de los primeros síntomas de la enfermedad antracnosis. En promedio, se observó que el contenido constitutivo de fenoles totales es mayor en frutos de lulo en estado maduro para los tres tratamientos, si se compara con los otros dos estados de madurez, hecho éste que puede estar asociado con los cambios metabólicos normales que se presentan en el fruto como consecuencia del proceso de maduración. El hecho de presentar este estado de madurez los mayores contenidos de fenoles totales no se puede asociar a priori con posibilidad de menores síntomas, pues es sabido que con frecuencia el efecto en defensa se debe sólo a ciertos fenoles particulares más que al total de ellos. En caso de que se trate de compuestos específicos (se está analizando este aspecto en otro estudio aún no publicado) podría tenerse el caso de que en los frutos maduros éstos compuestos específicos no estén evidentemente aumentados por la infección, lo que explicaría el desarrollo de síntomas.
Los resultados observados en el modelo Lulo (Solanum quitoense Lam)- C. acutatum están de acuerdo con algunos reportes de la literatura en los cuales se ha encontrado que el metabolismo fenólico es uno de los que con frecuencia se induce durante la interacción planta-patógeno. Por ejemplo, estudios realizados en diferentes modelos muestran un aumento en la concentración de los compuestos fenólicos presentes, los cuales actúan principalmente como inhibidores del crecimiento de patógenos. En plantas de olivo (Olea europaea L.) infectadas se ha demostrado que las sustancias fenólicas aumentan su concentración y que pueden inhibir el crecimiento de bacterias, tales como Lactobacillus plantarum y Leuconostoc mesenteroides, entre otras, así como hongos pertenecientes al género Phytophthora, (Del Río et ál., 2003). Otros ensayos realizados usando cultivo de células de Hierba de San Juan (Hypericum perforatum L), elicitadas con el hongo Colletotrichum gloeosporioides, muestran aumento en la concentración de xantonas, compuestos con características apolares a los que le atribuyen propiedades antimicrobiales. Dicho aumento es considerado como una respuesta de defensa provocada por algunos componentes presentes en el hongo elicitor (glicoproteínas, oligosacáridos) (Conceição et ál., 2006). Teniendo en cuenta lo anterior, es posible sugerir que la acumulación de compuestos fenólicos totales, observada a partir de 12 hpi en los frutos de lulo en los tres estados de madurez inoculados con el patógeno, se trate de una respuesta a su presencia, acumulación que en el caso de los frutos pintones se mantiene durante todo el tiempo del experimento y se incrementa notablemente a las 72 hpi, lo que se puede asimilar, en principio, a una respuesta defensiva, dada la relación positiva encontrada entre este aumento y la demora en la aparición de los síntomas de la enfermedad.
CONCLUSION
Los resultados de esta investigación se constituyen en los primeros reportes de participación de la enzima PAL en respuestas del lulo al patógeno C. acutatum. Las evidencias acumuladas muestran que en frutos de lulo en estado pintón la actividad PAL fue mucho mayor que en estado verde y maduro y que en este estado de madurez la aparición de síntomas de la antracnosis fue más tardía. En general todos los frutos respondieron al patógeno (y a la herida) activando esta enzima hacia las 12 y 24 horas de estar en contacto con éste. La inducción de actividad PAL por efecto del hongo mostró relación positiva con el aumento en el contenido de fenólicos totales, al nivel de corteza de frutos de lulo,
comportamiento que también evidenció dependencia con el estado de madurez del fruto.
AGRADECIMIENTOS
Los autores expresan su agradecimiento al Departamento de Química y a la División de investigación de la Sede Bogotá de la Universidad Nacional de Colombia por el apoyo otorgado para este estudio.
BIBLIOGRAFÍA
ALUNNI S, CIPICIANI A, FIORINI G, OTTAVI L. Mechanisms of inhibition of phenylalanine ammonia lyase by phenol inhibitors and phenol / glycine synergistic inhibitors. Archives of Biochemistry and Biophysics. 2003; 412: 170-175.
[ Links ]ARDILA H. Evaluación de algunas respuestas bioquímicas y moleculares relacionadas con el metabolismo de los fenoles en el modelo Clavel (Dianthus caryophyllus L.)-Fusarium oxysporum f. sp.dianthi raza 2. [Tesis de Maestría]. Bogotá: Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 2005.
[ Links ]CASIERRA F, GARCÍA E, LUDDERS P. Determinación del punto óptimo de cosecha en el lulo Solanum quitoense Lam. var. quitoense y septentrionale. Agronomía Colombiana. 2004; 22(1):32-39.
[ Links ]CAICEDO O. Evaluación de la inducción de polifenoloxidasa y peroxidasa como respuesta a la interacción fruto de lulo (Solanum quitoense Lam)- Colletotrichum acutatum. (Tesis de Maestría). Bogotá: Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 2005.
[ Links ]CAICEDO O. Inducción de polifenoloxidasa en frutos de Lulo (Solanum quitoense) como respuesta a la infección con Colletotrichum acutatum. Acta biol. Colomb. 2007; 12 S: 41 - 54.
[ Links ]CAICEDO O, HIGUERA B, MARTÍNEZ S. Inducción de actividad peroxidasa y de fenoles totales como respuesta del fruto de lulo (Solanum quitoense Lam) al patógeno causal de la antracnosis. Rev. Colomb. Quím. 2009; 38 (1): 25-42.
[ Links ]CERÓN S. Detección de Colletotrichum (Penz) Sacc en estructuras vegetativas y reproductivas de lulo Solanum quitoense Lam [tesis de maestría en Fitopatología]. Bogotá DC: Facultad de Agronomía, Universidad Nacional de Colombia; 2005.
[ Links ]CHAKRABORTY U, CHAKRABORTY BN, KAPOOR M. Changes in the levels of peroxidase and phenylalanine ammonia-lyase in Brassica napus cultivars showing variable resistance to Leptosphaeria maculans. Folia Microbiol. 1993; 38 (6): 491- 496.
[ Links ]CHANDRA A, RAGHVENDRA S, DUBEY A, SAXENA P. Change in phenylalanine ammonia lyase activity and isozyme patterns of polyphenol oxidase and peroxidase by salicylic acid leading to enhance resistance in cowpea against Rhizoctonia solani. Acta Physiol Plant. 2007; 29: 361-367.
[ Links ]CHENYANG H, HSIANG T, WOLYN D. Activation of defense responses to Fusarium infection in Asparagus densiflorus. Eur J Plant Pathol. 2001; 107: 473-483.
[ Links ]CONCEIÇÃO LF, FERRERES F, TAVARES R, DIAS A. Induction of phenolic compounds in Hypericum perforatum L. cells by Colletotrichum gloeosporioides elicitation. Phytochemistry. 2006; 67: 149-155.
[ Links ]CORTÉS RA. Efecto de la refrigeración y el choque térmico sobre algunos indicadores de actividad antioxidante en lulo (Solanum quitoense Lam) [tesis de maestría]. Bogotá: Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 2006.
[ Links ]DANE. I Censo nacional de 10 frutas agroindistriales y promisorias. 2004 Oct. Disponible en: http://www.frutasyhortalizas.com.co/portal/includej/zip/CENSO21oct04.zip ? PHPSESSID=69af5c1e0b2671dd3d1066934a4a51a3
[ Links ]DEL RÍO JA, BAÍDEZ AG, BOTÍA JM, ORTUÑO A. Enhancement of phenolic compounds in olive plants (Olea europaea L.) and their influence on resistance against Phytophthora sp. Food Chem. 2003; 83:75-8.
[ Links ]DEUTSCHER M. Method Enzymol, Guide to Protein Purification. Vol 182. Academic Press. Inc. New York; 1990.
[ Links ]GARMENDIA I, AGUIRREOLEA J, GOICOCHEA N. Defence- related enzymes in pepper roots during interactions with arbuscular mycorrhizal fungi and / or Verticillium dahliae. Biocontrol. 2006; 51: 293-310.
[ Links ]HYODO H, KURODA H, FA YANG S. Induction of phenylalanine ammonia lyase and increase in phenolics in letucce leaves in relation to the development of ruseet spotting caused by ethylene. Plant Physiol. 1978; 62: 31-35.
[ Links ]KOIKE M, NANBU K. Phenylalanine ammonia-lyase activity in alfalfa suspension cultures treated with conidia and elicitors of Verticillium albo-atrum. Biol Plantarum. 1977; 39 (3): 349-353.
[ Links ]KOVACIK J, BACKOR M. Phenylalanine ammonia lyase and phenolics compounds in Chamonile tolerance to cadmium and cooper excess. Water Air Soil Poll. 2007; 185: 185-193.
[ Links ]MAKKAR H, BLUEMMEL M, BOROWY NK, BECKER K. Quantification of tannins in tree foliage. En: A laboratory manual for the FAO/IAEA Co-ordinated research Project on use of nuclear and related techniques to develop simple tannins assays for predicting and improving the safety and efficiency of feeding ruminants on tannins tree foliage¨. Viena. 2000.
[ Links ]MORELLÓ JM, ROMERO MP, RAMO T, MOTILVA MJ. Evaluation of L-phenylalanine ammonia-lyase activity and phenolic profile in olive drupe (Olea europaea L.) from fruit setting period to harvesting time. Plant Sci. 2005; 168:65-72.
[ Links ]ORR JD, EDWARDS R, DIXON R. Stress responses in alfalfa (Medicago sativa L.). Plant Physiol. 1993; 101: 847-856.
[ Links ]RUBIO E. Estudio del cambio de actividad de polifenoloxidasa, PFO, durante el proceso de maduración del lulo (Solanum quitoense L.) [Tesis de Maestría]. Bogotá: Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 1999.
[ Links ]RYBKA K, ARSENIUK E, WISNIEWSKA J, RACZYNSKA- BOJANOWSKA K. Comparative studies on the activities of chitinase, B-1,3-glucanase, peroxidase and phenylalanine ammonia lyase in the leaves of triticale and wheat infected with Stagonospora nodorum. Acta Physiol Plant. 1998; 20 (1): 59-66.
[ Links ]SHADLEA GL, WESLEYA S, KORTHA K, CHENA F, LAMBB C, DIXON R. Phenylpropanoid compounds and disease resistance in transgenic tobacco with altered expression of L-phenylalanine ammonia-lyase. Phytochemistry. 2003; 64: 153-161.
[ Links ]SUDHAMOY M, ADINPUNYA M, NIRUPAMA M. Time-course study on accumulation of cell wall-bound phenolics and activities of defense enzymes in tomato roots in relation to Fusarium wilt. World J. Microb Biot. 2008; 42: 135-139.
[ Links ]TAMAYO P. Principales enfermedades del tomate de árbol, la mora y el lulo en Colombia. Corpoica, Boletín técnico, Bogotá, 2001. [ Links ]
ZHANG S, ZHANG F, HANG F, HUA B. Enhancement of Phenylalanine ammonia lyase, polyphenoloxidase, and peroxidase in Cucumber Seedlings by Bemisia tabaci (Gennadius) (Hemiptera: Aleyrodidae) Infestation. Agricultural Sciences in China. 2008; 7(1): 82-87
[ Links ]













