Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Acta Biológica Colombiana
versión impresa ISSN 0120-548X
Acta biol.Colomb. v.16 n.2 Bogotá mayo/ago. 2011
DIFERENCIACIÓN DE ESPECIE MICOBACTERIANA POR FT-IR (ESPECTROSCOPIA INFRARROJA CON TRANSFORMADA DE FOURIER)
Differentiation of Mycobacterial Species by FT-IR (Fourier Transform Infrared Spectroscopy)
JORGE ANDRÉS CUÉLLAR GIL1, B.Sc; SANDRA MILENA CORONADO RÍOS1,2, Lc. M.Sc.; ROBERTO CARLOS ARRUBLA QCO3
1 Centro de Investigaciones Biomédicas, Programa de Biología, Universidad del Quindío. Colombia.
2 Maestría en Microbiología, Universidad de Cartagena. Colombia.
3 Laboratorio de Química Instrumental, Programa de Química, Universidad del Quindío, Carrera.15 Calle 12 Norte. Armenia, Quindío, Colombia. jacg136@gmail.com
Presentado 25 de noviembre de 2010, aceptado 18 de marzo de 2011, correcciones 1 de junio de 2011.
RESUMEN
Se trabajó con espectroscopía infrarroja transformada de Fourier (FT-IR) para diferenciar diez especies de micobacterias. Mycobacterium intracelullare y M. fortuitum (ATCC), M. flavensces, M. smegmatis, M. chelone, M. gordonae, M. triviale, M. vaccae, M. terrae y M. nonchromogenicum (IP). Como control de diferenciación de género se incluyó Staphylococcus aureus, Streptococcus viridans y Streptococcus pyogenes, Klebsiella pneumoniae y Escherichia coli, cada especie se corrió por triplicado en KBr y ATR. Los espectros se analizaron según el método de diferenciación de componentes principales, y se realizaron derivadas de primer orden (D1) en modalidad de transmisión usando la pastilla de KBr y la base ATR, además se diseñó una biblioteca espectral con la primera derivada de ATR. La sensibilidad de detección fue de 100% al trabajar con KBr y el nivel de diferenciación fue de 100% en tres de cuatro muestras problema.
Palabras clave: micobacterias, espectroscopia, infrarrojo, gram negativas y gram positivas.
ABSTRACT
Spectroscopy Fourier Transform infrared (FT-IR) was used to differentiate 10 species of mycobacteria. Mycobacterium intracelullare and M. fortuitum (ATCC). M. flavensces, M. smegmatis, M. chelone, M. gordonae, M. triviale, M. vaccae, M. terrae and M. nonchromogenicum (IP). For gender differentiation Staphylococcus aureus, Streptococcus viridans and Streptococcus pyogenes, Klebsiella pneumoniae y Escherichia coli were incluided as controls, each species was run for triplicate in KBr and ATR. The spectra were analyzed with the method of principal components to make the first derivatives of first order (D1) in the transmission mode using KBr pellet and ATR base, and a spectral library of the first derivative of ATR was kept. The detection sensitivity was 100% with KBr and the level of differentiation was 100% in three of the four samples problems.
Key words: mycobacteria, spectroscopy, infrared, gram negative and gram positive.
INTRODUCCIÓN
El género Mycobacterium comprende más de 100 especies y su diferenciación normalmente se basa en pruebas fenotípicas y bioquímicas post aislamiento pero estas son lentas, costosas y de bajo rendimiento. La prueba de amplificación del gen Hsp65 y su posterior restricción con endonucleasas (PRA) es rápida pero identifica sólo un rango limitado de especies; los métodos cromatográficos usados para diferenciar los componentes de la pared celular tienen baja reproducibilidad y no discriminan entre cepas (Tortoli, 2003). El desarrollo de técnicas rápidas y precisas de identificación es de gran importancia en términos de diagnóstico, tratamiento y control de las micobacteriosis (Cardoso, 2004). Recientemente se ha usado espectroscopía infrarroja con transformada de Fourier (FT-IR) para la identificación de microorganismos según los porcentajes de diferentes componentes celulares, demostrando alta reproducibilidad y fácil manejo de las muestras. El nivel de diferenciación de la técnica está basado en la expresión de la huella dactilar de componentes celulares, que generan espectralmente características moleculares propias de especie y cepa bacteriana; esto ofrece la posibilidad de detectar e identificar microorganismos en una microcolonia, por lo que se reduce significativa-mente tiempo y costo necesarios para la identificación (Nieto, 2004). La técnica FT-IR comprende dos método de análisis: el primero por KBr (bromuro de potasio), usando un soporte universal y el segundo por ZnSe (celenurio de zinc) en un soporte ATR (reflectancia total atenuada), que muestra más específicamente grupos funcionales de cada una de las muestras bacterianas por tener un contacto mayor con el infrarrojo (Parikh, 2008). En este trabajo se evalúo la capacidad de diferenciación de 10 especies micobacterianas por espectrometría FT-IR.
MATERIALES Y MÉTODOS
SELECCIÓN DE LA MUESTRA Y TIPO DE ESTUDIO
Se compararon los principales compuestos bioquímicos de diez especies de micobacterias potencialmente patógenas de crecimiento rápido o moderadamente rápido Mycobacterium intracelullare y M. fortuitum ATCC (American Type Culture Collection) 13.950 y 6.841 respectivamente, M. flavensces, M. smegmatis, M. chelonae, M gordonae, M. triviale, M. vaccae, M. terrae y M. nonchromogenicum, son especies de referencia del Institute Pasteur-Francia; como control de diferenciación de género se usaron: Staphylococcus aureus ATCC 25923, Streptococcus viridans ATCC 19952 y Streptococcus pyogenes ATCC 19615, Klebsiella pneumoniae y Escherichia coli, ATCC 13883 y 4157 respectivamente.
MEDIOS DE CULTIVO Y PRUEBAS DE VIABILIDAD
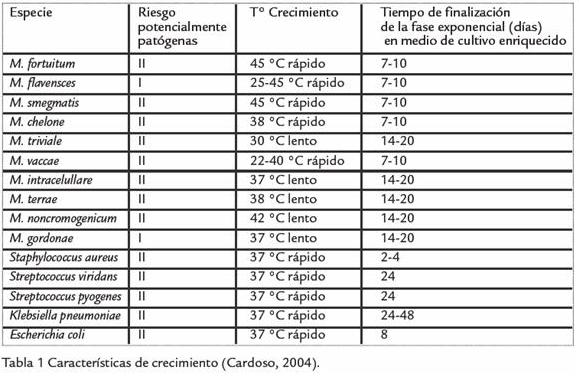
Las especies micobacterianas se recuperaroón de congelación (-85 °C), sembrando 50 µL de bacteria en medio líquido Dubos Broth Base (Becton Dickinson, Microbiology System) suplementado con ampicilina (Bayer), penicilina (Sandoz), cefalotina (Recipe) y anfotericina B (Abbott france) y se incubaron de acuerdo a los requerimientros de temperatura de cada especie hasta observar crecimiento por variación en la turbidez del medio. Se realizó coloración de Ziehl Neelsen para verificar que las muestras estivueran puras, posteriormente, para probar viabilidad en medio de cultivo sólido se tomaron 100 µL de cada especie y se sembraron por triplicado en Lowestein Jensen y Middlebrook 7H11 suplementados con OADC (ácido oleico y complejo albumina-dextrosa) sin antibiótico, hasta obtener un cultivo al final de la fase exponencial y comienzos de la fase estacionaria según la especie (Garzon, 2001). S. viridans, S. pyogenes y S. aureus se recuperaron de agar base sangre (Oxoid), K. pneumoniae y E. coli se recuperaron en medio Mac Conkey (Oxoid) también por triplicado hasta obtener un cultivo a finales de la fase exponencial (Tabla 1; Brown, 2001).
EQUIPOS Y ACCESORIOS
Se usó el espectrómetro FT-IR NICOLET 380 (Thermo Electron Corporation) y su software de funcionamiento EZ- OMNIC versión 7.2. Se usó el accesorio ATR Smart Multi Bounce Hartr modelo 0028-297 serie 509003 con un ángulo de soporte de 45º. En el caso de KBr se usó un detector DTGS y el accesorio de transmisión E.S.P., para hacer las pastillas se utilizó un mortero de ágata y la prensa estándar del equipo.
PREPARACIÓN DE LA MUESTRA Y OBTENCIÓN DE ESPECTROS
De cada replica de cultivo se tomó con microespátula una muestra colonial de aproximadamente 5 mg (5x106 UFC) del día 10 para las rápido crecedoras y del día 20 para las lento crecedoras, se almacenó en un tubo estéril y se preparó una pastilla mezclando la muestra con 100 mg de KBr. En cada caso se tomó el espectro FT-IR comprendida entre 400 y 4.000 cm-1(IR medio, MIR) a una resolución de 8 cm-1, acumulando n= 256 interferogramas por espectro, a una velocidad de 0,6329 y una apertura de 100, el espacio de los datos fue 3,857 cm-1. Todas las medidas fueron precedidas por la toma de “background” o espectro de referencia, para calibrar las can-tidades de CO 2 y vapor de agua.
Para las medidas en el ATR se colocaron 5 mg (5x106 UFC) de cada muestra sobre la base de ATR-ZnSe (reflectancia total atenuada) y las condiciones de medida mencionadas anteriormente. Se tomó en cuenta que cada muestra tuviera la misma profundidad de penetración, el ATR se calibró y normalizó previamente, para obtener el espectro de referencia (Rebuffo, 2007).
ANÁLISIS DE RESULTADOS
Los espectros obtenidos para cada especie, se analizaron según varias referencias espectrales (Rebuffo, 2007; Yu, 2005; Silverstein, 1999).
De acuerdo a las frecuencias obtenidas en las muestras analizadas, se usó el programa TQ. Analyst Ez Edition para calcular la primera derivada “Savistsky Golay” de los espectros procesados en KBr y ATR; esto se realizó para aumentar la resolución de las bandas. Por otro lado, se calcularon sensibilidad de detección y nivel de diferenciación del FT-IR (Oust, 2007).
RESULTADOS Y DISCUSIÓN
INTERPRETACIÓN ESPECTRAL
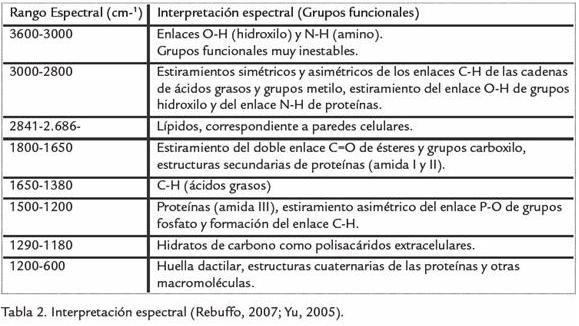
Los espectros de las bacterias muestran como regiones espectrales de interés: región lipídica correspondiente a pared celular (2.841-2.686 cm-1), de hidratos de carbono como polisacáridos extracelulares (1.290-1.180 cm-1), la denominada huella dactilar asociada a estructuras cuaternarias de proteínas y otras macromoléculas (1.200-600 cm-1) específicas para cada especie, observándose sus diferencias fenotípicas. Otra región de análisis es la de 3.000-2.800 cm-1, donde se aprecian estiramientos simétricos y asimétricos de los enlaces C-H de las cadenas de ácidos grasos y grupos metilo, estiramiento del enlace O-H de grupos hidroxilo, estiramiento del enlace N-H de proteínas. En la región de los 1.800-1.650 cm-1se aprecia estiramiento del doble enlace C-O de ésteres y grupos carboxilo, contribución de estructuras secundarias de proteínas (amidas I y II). Por último la región de 1 500-1 200 cm-1se interpreta como la contribución de proteínas (amidas III), estiramiento asimétrico del enlace P-O de grupos fosfato y de formación del enlace C-H. En la región comprendida entre los 3.600 a 3.000 cm-1, se observan absorbancias características a tensiones de enlace O-H (hidroxilo) y también N-H (amino) grupos funcionales que son muy variables en el momento del análisis espectral, debido a los compuestos del medio, a la cantidad de agua y a posibles enlaces y puentes de hidrógeno generados por resonancia, por lo que se descarta esta región para análisis.
Todas las regiones espectrales seleccionadas, 3.000-2.800 cm-1, 1.800-1.400 cm-1 y 1.200-500 cm-1 presentan en general un contenido de ácidos y grasas, remarcando la región de los 1.800-1.650 cm-1(C=O) y 1.650-1.380 cm-1 (C-H), porque son las regiones más representativas de ácidos grasos en las especies estudiadas (Tabla 2; Essendoubi, 2005. Erukhimovitch, 2004. Garip, 2009. Beekes, 2007).
En la prueba de KBr para E. coli y K. pneumoniae (Fig. 1), se aprecia una intensidad en la región de 2.800 a 3.000 cm-1 característica de enlaces C-H (alcanos). E. coli con mayor absorción en IR posee cadenas C-H más largas, las demás partes de los espectros poseen absorbancia similar y característica de la familia Enterobacteriaceae. E. coli también presenta mayor intensidad en la región 1.400 a 1.800 cm-1 o carbonilos, ésteres y aldehídos con respecto a K. pneumoniae; por otro lado la región de la huella dactilar se sitúa entre los 600 a 1.200 cm-1 donde se observa una pequeña diferencia entre los 1.100 y 1.200 cm-1, porque al parecer E. coli, presenta mayor cantidad de alcanos y en general de ésteres.
El perfil comparativo de ATR entre E. coli y K. pneumoniae (Fig. 2), muestra alta similaridad con KBr, aunque esta prueba es más selectiva en la resolución de los picos permitiendo inferir similitudes y diferencias entre las especies. E. coli sigue presentando mayor relación de alcanos y carbonilos en la región 1.650 a 1.380 cm>-1 y 1.650 a 1.800 cm-1 respectivamente; por otro lado la región de la huella dactilar muestra gran diferencia entre las dos especies, debido a que E. coli presenta con claridad un contenido más alto de grupos funcionales carbonilo. El mismo comportamiento se observa con la primera derivada de ATR. En la primera derivada “Savistsky Golay” bajo KBr la huella dactilar se constituye en la región 600 a 1.200 cm-1, mientras en K. pneumoniae la tendencia de la curva es casi lineal, las inflexiones observadas en E. coli diferencian bien las dos especies lo que mejora la interpretación.
El perfil comparativo de KBr para S. aureus, S. viridans y S. pyogenes (Fig. 3), manifiesta tensiones espectrales en 2.800 a 3.000 cm-1, de los 1.400 a 1.800 cm-1 se determinan los ácidos grasos en las tres especies, la composición de lípidos, ésteres, carbonilos, amidas I, II y proteínas son similares entre las especies S. aureus y S. viridans, mientras que en S. pyogenes se presentan en baja cantidad. En la región de 1.200 a 600 cm-1 quizás se registran cantidades iguales de enlaces C-H y C-O entre las tres especies, pero S. viridans presenta mayor absorción entre los 1.200-1.000 cm-1 de enlaces C-O o posibles ácidos.
En el análisis espectral por ATR (Fig. 4), se aprecia el mismo comportamiento que posiblemente se presenta en el análisis bajo KBr en las región de los 3.000 a 2.800 cm-1 y en la de 1.800 a 1.400 cm-1. En cuanto la región de flexión sigue presentando a S. viridans como la de mayor composición de carbohidratos y la de mayor relación C-O y C-N (amino), seguida por S. pyogenes. El análisis bajo la primera derivada de ATR es similar a excepción de la alta relación C-H en S. pyogenes en 3.000 a 2.800 cm-1. En cuanto a la primera derivada de KBr por el método “Savistsky Golay”, se observa presencia muy ajustada en los compuestos y grupos funcionales, observándose inflexiones iguales en las regiones de 3.000 a 2.800 cm-1 y 1.650 a 1.350 cm-1; por otra parte la región de flexión alrededor de 1.200 a 600 cm-1 se aprecia un comportamiento lineal en S. aureus que no se observa en S. pyogenes y S. viridans, lo cual parece ser la diferencia más representativa entre los dos géneros.
En cuanto a la diferenciación de micobacterias por KBr (Fig. 5), se muestra alta similitud de especies en la región de 3.000 a 2.800 cm-1 en la relación C-H y ácidos grasos como tal; esta región junto con la de 1.800 a 1.400 cm-1 son las regiones características del género Mycobacterium por presentar el mismo comportamiento espectral, aunqueM. terrae muestra el pico de género muy atenuado (1.800 a 1.700 cm-1), la relación de carbonilos, aldehídos, ésteres, anhídridos, lípidos, proteínas y carbohidratos son similares entre especies, al igual que la relación C-H, que se encuentra entre 1.400 a 1.500 cm-1.
La región de 1.200 a 500 cm-1 expresa picos característicos de especie. M. terrae presenta mayor intensidad en la zona de 1.200 a 1.100 cm-1 o carbohidratos, posiblemente porque esta especie se cultivó en medio Middlebrook 7H11, que es de alto valor energético por su suplementación con OADC, lo que permite a la bacteria la elaboración de polímeros carbonados de reserva y que explicaría la intensidad que se presenta en dicha región (Robledo, 2006).
El análisis con ATR, para micobacterias muestra que M. intracellulare, M. nonchromogenicum, M. chelonae y M. triviale (Fig. 6), cuentan con alto contenido de ácidos grasos y con una mayor relación de alcanos; en cambio M. smegmatis presenta una composición y relación totalmente diferente en la región de 3.000 a 2.800 cm-1. En cuanto a la región de análisis de 1.800 a 1.400 cm-1 M. terrae sigue presentando el pico de género atenuado. Otro comportamiento espectral característico en esta región es la disposición que tiene M. nochromogenicum (1.600 a 1.500 cm-1) que presenta doble banda o duplete de alta intensidad, esto se interpreta en un alto contenido de proteínas con amidas tipo III característico al parecer de esa especie, porque las demás especies solamente presentan una banda.
En la región de 1.200 a 600 cm-1, se observan diferencias grandes en los picos interpretándose como diferencias en la composición de carbohidratos, alcanos, ésteres y en general de carbonilos. En este análisis espectral bajo ATR, M. terrae presenta en la región de la huella dactilar mayor intensidad que la observada bajo KBr, esto posiblemente se deba al alto nivel de diferenciación y selectividad que proporciona la base de ZnSe. En cuanto a la primera derivada de ATR se obtienen inflexiones y picos más selectivos que ayudan a diferenciar más fácilmente las especies, lo que indica que es la prueba más apropiada para la elaboración de bibliotecas espectrales.
SENSIBILIDAD DE DETECCIÓN Y NIVEL DE DIFERENCIACIÓN
En la prueba general de KBr (Fig. 7) con M. smegmatis (1 mg, 5 mg, 10 mg y 15 mg) y KBr (100 mg, 200 mg y 300 mg) se observó el mismo comportamiento espectral, la mínima cantidad de KBr que se puede usar para formar la pastilla es 100 mg, lo cual con 1 mg de bacteria identifica correctamente la especie, por lo que puede reportarse una sensibilidad de detección del 100% al trabajar bajo KBr; estos datos permiten minimizar el tiempo de cultivo requerido al necesitarse menor cantidad de colonia, más aun si se usa un medio de cultivo enriquecido y la técnica de crecimiento de capa delgada (Mejía, 1999; Mejía, 2004).
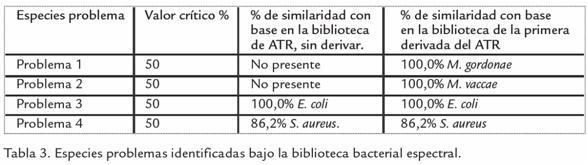
El nivel de diferenciación fue de 100%, en tres de las cuatro muestras problema que fueron correctamente identificadas por IR como M. gordonae, M. vaccae y E. coli. Para la última muestra problema S. aureus se obtuvo un porcentaje de identificación de 86,2% en ATR y 86,22% en la primera derivada de ATR, 0,2% más de selectividad, pero en ambos casos correctamente identificada (Tabla 3).
El perfil comparativo en la primera derivada de ATR entre los tres grupos de bacterias estudiados muestra claramente la similitud de géneros y diferencias entre especies, lo que indica que las pruebas de especie deben realizarse bajo ATR como sugiere Branan, 2007; en este estudio se recomienda sumar al procedimiento el análisis de la primera derivada. Lo más relevante para la diferenciación de las micobacterias (Fig. 8) es la presencia de picos específicos e intensos en infrarrojo concordantes a la composición de ácidos micólicos, los más abundantes y variables compuestos lipídicos situados en la envoltura de micobacteria. Otra diferencia observada es la banda en 1.745 cm-1 cuyos responsables son los grupos ésteres y carbonilos que se unen particularmente a arabinogalactano y ácidos micólicos atados a la capa de péptidoglicano que no está presente en otros grupos bacterianos como indica (Rebuffo, 2007).
AGRADECIMIENTOS
A las instituciones participantes: Universidad del Quindío y Universidad de Cartagena, Colombia.
BIBLIOGRAFÍA
BEEKES M, LASCH P, NAUMANN D. Analytical applications of Fourier transform-infrared (FT-IR) spectroscopy in microbiology and prior research. Vet Microbiol. 2007;4:305-319.
[ Links ]BRANAN N, WELLS TA. Microorganism characterization using ATR-FTIR on an ultrathin polystyrene layer. Vib Spectrosc. 2007;1:192-196.
[ Links ]BROWN A. Benson s Microbiological Application. Laboratory Manual in General Microbiology. The McGraw-Hill Companies; 2001.
[ Links ]ERUKHIMOVITCH V, PAVLOV V, TALYSHINSHY M, SOUPRUN Y, HULEIHEL M. FTIR microscopy as a method for identification of bacterial and fungal infections. J Pharmaceut Biomed. 2004;5:1105-1108.
[ Links ]ESSENDOUBI M, TOUBAS D, BOUZAGGOU M, PINON MJ, MANFAIT MI, SOCKALINGUM DG. Rapid identification of Candida species by FT-IR microspectroscopy. Biochim Biophys Acta. 2005;3:239-247.
[ Links ]GARIP S, CETIN GA, SEVERCAN F. Use of Fourier transform infrared spectroscopy for rapid comparative analysis of Bacillus and Micrococcus isolates. Food Chem. 2009;4:1301-1307.
[ Links ]GARZÓN CM, NARANJO NO, SIERRA RCL, LLERENA C, ORJUELA LD. Bacteriología de Mycobacterium tuberculosis y de micobacterias no tuberculosas, manual de procedimientos. Instituto Nacional de Salud, Subdirección de Epidemiología y Laboratorio Nacional de Referencia-Laboratorio de Micobacterias. Bogotá D.C.; 2001.
[ Links ]LEAO SC, MARTIN A, MEJÍA GI, PALOMINO CJ, ROBLEDO J, TELLES MADS SILVA, PORTAELS F. Practical Handbook For The Phenotypic And Genotypic Identification of Mycobacteria; 2004. p. 1-165.
[ Links ]MEJÍA GI, CASTRILLON L, TRUJILLO H, ROBLEDO JA. Microcolony detection in 7H11 thin layer culture is an alternative for rapid diagnosis of Mycobacterium tuberculosis infection Int J Tuberc Lung Dis 1999;3:138-142.
[ Links ]MEJÍA GI, GUZMÁN A, AGUDELO CA, TRUJILLO H, ROBLEDO JA. Cinco años de experiencia con el uso de agar de capa delgada para el diagnostico rápido de tuberculosis. Biomédica. 2004;24:52-9.
[ Links ]NIETO I, LAURA, DONOLO SA, BAVA JA, YANTORNO MO. Empleo de espectroscopia infrarroja con transformada de Fourier para diferenciar bacterias de importancia clínica. Microbiología. Acta Bioquim Clin L. 2004;38:289-295.
[ Links ]OUST JA, MORETRO T, BERTRAND D, KHOLER A. FT-IR Microspectroscopy: A Promising Method for the Rapid Identification of Listeria Species. FEMS Microbiol Lett. 2007;278:164-170.
[ Links ]PARIKH SANJAI J, CHOROVER J. ATR-FTIR Study of Lipopolysaccharides at Mineral Surfaces. Colloids Surfaces B. 2008;62:188-198g.
[ Links ]REBUFFO SC, KIRSCHNER C, STAEMMLER M, NAUMANN D. Rapid Species and Differentiation of Non-Tuberculous Mycobacteria by Fourier-Transform Infrared Microspectroscopy. J Microbiol Meth. 2007;68:282-290.
[ Links ]ROBLEDO JA, MEJÍA GI, MORCILLO N, CHACÓN L, CAMACHO M, LUNA J. et al. Evaluation of a Rapid Culture Method for Tuberculosis Diagnosis: A Latin American Multi-Center Study-Int J Tuberc Lung Dis. 2006;10:613-619.
[ Links ]SILVERSTEIN MR, WEBSTER XF. Spectrometric identification of Organic Compounds. 6a ed. New York, John Wiley & Sons, 1998.
[ Links ]TORTOLI E. Impact of Genotypic Studies on Mycobacterial Taxonomy: The New Mycobacteria of the 1990s. Clin Microbiol Rev. 2003;319-354.
[ Links ]YU C, IRUDAYARAJ J. Spectroscopic Characterización of Microorganisms by Fourier Transform Infrared Microspectroscopy. Biopolymers. 2005;77:368-377.
[ Links ]













