Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.20 no.1 Bogotá Jan./Apr. 2015
https://doi.org/10.15446/abc.v20n1.39109
http://dx.doi.org/10.15446/abc.v20n1.39109
DIMORFISMO, USO DE HÁBITAT Y DIETA DE Anolis maculiventris (LACERTILIA: DACTYLOIDAE), EN BOSQUE PLUVIAL TROPICAL DELCHOCÓ, COLOMBIA
Dimorphism, habitat use and diet for Anolis maculiventris (Lacertilia: Dactyloidae), in tropical rainforest in Chocó, Colombia
Efren PINILLA-RENTERIA1, Jhon Tailor RENGIFO-MOSQUERA1, Jovanny SALAS LONDOÑO1.
1 Universidad Tecnológica del Chocó, Ciudadela Universitaria- B/ Nicolás de Medrano, bloque 11, oficina 412. Quibdó, Colombia.
For correspondence. d-jhon.rengifo@utch.edu.co
Received 30th July 2013, Returned for revisión 31st October 2013, Accepted 5th May 2014.
Citation / Citar este artículo como: Pinilla-Renteria E, Rengifo-Mosquera JT, Salas Londoño J. Dimorfismo, uso de hábitat y dieta de Anolis maculiventris (Lacertilia: Dactyloidae), en bosque pluvial tropical del Chocó, Colombia. Acta biol. Colomb. 2015;20(1):89-100. doi: http://dx.doi.org/10.15446/abc.v20n1.39109
RESUMEN
Se estudiaron algunos aspectos de la biología poblacional de Anolis maculiventris, en zonas de bosque pluvial tropical de la región natural chocoana. Los machos y hembras presentaron una coloración café claro con un pequeño lunar en la parte posterior de la cabeza, las proporciones de sexo en los individuos capturados mostraron diferencias estadísticas significativas (X2: 4,81, gl: 1, p: 0,028). El grado de dimorfismo sexual (GDS) e índice de dimorfismo sexual fue de 1,08 mm y un de 8,5 mm respectivamente. Las hembras difieren significativamente de los machos en todas las regiones corporales medidas. Se disectaron 30 individuos a los cuales se les determino su estado reproductivo, en donde la talla mínima de madures en hembras (LHA) fue de 30,7 mm, con un máximo de 39,9 mm y una media de 36,5 mm. En machos la talla mínima de madurez fue de 30,4 mm, y máxima de 36,7 mm, con una media de 33,8 mm; lo cual indica que las hembras fueron más grandes que los machos. Se evaluó el uso de hábitat, mostrando diferencias estadísticas significativas entre los sustrato utilizados (X2=16,89, gl: 3, p: 0,001); y para las posiciones verticales mostraron el mismo comportamiento (X2=3,77, gl: 3, p: 0,207). Para el análisis dietario de la especie se disectaron 30 estómagos, de los cuales 15 pertenecieron a machos y 15 a hembras, se registróun total 46 presas gastrointestinales que componen su dieta mostrando a los órdenes Himenóptera (Formicidae) y Coleóptera como los de mayor importancia relativa en la dieta.
Palabras clave: biología, ecosistemas, reproducción, región Chocoana, Squamata.
ABSTRACT
We studied some aspects of the population biology of A. maculiventris, in areas of tropical rainforest in the natural region of Choco. The males and females brown coloration with a small mole on the back of the head, the proportions and gender in the captured individuals showed significant statistical differences (X2: 4,81, gl: 1, p: 0,028). The degree of sexual dimorphism (GDS) and sexual dimorphism index was 1.08, mm and 8.5 mm respectively. Females differ significantly from males in all the parts of the body measures. 30 Individuals have spread, which was determined to their reproductive status and failed to register a size minimum of maturity (LHA) in females is 30.7 mm, with a maximum of 39.9 mm and an average of 36.5 mm. In the male the minimum maturity sexual 30.4 mm, and a maximum of 36.7 mm, with an average of 33.8 mm; which indicates that females were more large than males. Assessed habitat use, showing significant statistical differences between the used substrate (X2=16,89, gl: 3, p: 0,001); and for vertical positions, showed the same behavior (X2=3,77, gl: 3, p: 0,207). For analyzing dietary species spread 30 stomach, of which 15 belonged to males and 15 females, will register a total 46 gastrointestinal dams that compose its diet showing the orders Coleoptera and Hymenoptera (Formicidae) as the of greater relative importance in the diet.
Keywords: biology, Chocoana region, ecosystems, reproduction, Squamata.
INTRODUCCIÓN
En la mayoría de las especies del género Anolis el macho es más grande que la hembra; esta diferencia entre los tamaños de machos y hembras es importante ya que puede reducir la competencia por alimento u otras necesidades entre las poblaciones (Rand, 1967). Por otro lado, las especies del género Anolis ocupan un lugar de gran importancia en las redes tróficas de los ecosistemas terrestres, puesto que consumen una cantidad considerable de artrópodos, fundamentalmente de insectos (Rodríguez y Martínez, 1996).
El género Anolis contiene cerca de 368 especies que representan entre el 5-10% de lagartos del mundo (Rougharden, 1995), ocupan una amplia variedad de microhábitats en todo el neotrópico, desde el arbóreo al terrestre, y aún en semiacuático. La mayoría de los Anolis utilizan variedad de sustrato como troncos, rocas y vegetación colgantes donde se perchan para cazar y huir fácilmente de los depredadores, son de hábitos diurnos y se alimentan durante el día de invertebrados que capturan en la hojarasca y arbustos (García et al., 2006; Rengifo, 2012). Por lo general los Anolis prefieren estar en la sombra para mantener una temperatura corporal baja entre 24,2 y 28,4°C (Bitt et al., 1995; Beuttell y Losos, 1999; Leal y Losos, 2000; Bitt et al., 2001), pocas especies de Anolis han sido estudiadas con detalles (biologia y ecologia poblacional) (Campbell, 1973; Hertz, 1975; Rand y Rand, 1976). Los Anolis presentan problemas de conservación debido a que en algunas zonas del país, los ecosistemas naturales vienen siendo severamente perturbados por las actividades antrópicas como la minería, la agricultura y la extracciones de madera, entre otras, lo cual ha generado fragmentación, alteración y modificación de sus hábitats provocando una potencial disminución en sus poblaciones. (Rengifo et al., 2014)
En la actualidad para Colombia se han registrado 71 especies del género Anolis, las cuales se encuentran distribuidas en las diferentes regiones colombianas, para el Chocó biogeográfico se reportan 31 especies, de las cuales, 27 se registran para el departamento del Chocó, que corresponden al 38% de las encontradas para el país y a un 87% para las reportadas para el Chocó Biogeográfico (Castaño et al., 2004; Rentería y Rengifo, 2006; Rentería, 2006). Acerca de la biología poblacional de A. maculiventris en Colombia no existe información detallada, debido al poco conocimiento de dicha especie, sumado a la trasformación de su hábitat por este motivo el presente estudio pretende conocer algunos aspectos biológicos de esta población en zonas de bosque pluvial tropical del departamento del Chocó, con el fin de contribuir al conocimiento de este grupo faunístico como estrategia de conservación.
MATERIALES Y MÉTODOS
Área de estudio
Este estudio se desarrolló en el corregimiento de Samurindo, perteneciente al municipio del Atrato, Chocó (Colombia), situado al occidente del municipio del Atrato, sobre la margen derecha del Río Atrato a los 5°35’ N y 76°39’ W, dista a 15 km de la cabecera municipal Yuto, posee una población de 921 habitantes en una área de 29,2 km2. Según la división político-administrativa del municipio, limita al norte con la comunidad de Vuelta Mansa, Puente del Real de Tanando, y al oriente con la vía carreteable hacia que conduce al municipio de Quibdó y al occidente con la comunidad de la Molana, al sur con el corregimiento de Doña Josefa y Yuto cabecera municipal. Presenta una humedad relativa de 90% y una altitud de 32 m s.n.m., una temperatura promedio de 28°C, con una precipitación anual de 8000 mm, presenta una zona de vida de bosques pluviales tropicales (bp- T) y bosque muy húmedo tropical (bmh-T) (Rangel-Ch, 2004).
Selección de zonas de estudio
Se establecieron sitios de muestreos dentro del área de estudio seleccionada, estos se caracterizaron por presentar diferentes coberturas vegetales pertenecientes a un Bosque Pluvial Tropical (bp-T) (bosques sin intervención, bosques intervenidos, zonas donde se aplican procesos productivos, etc.).
Capturas
Se realizaron manualmente con base a la metodología utilizada por Dunlap y Mena (2009), que consiste en inspeccionar en diferentes coberturas vegetales, los troncos de árboles, arbustos y demás formaciones vegetales, los recorridos y capturas se realizaronmediante el método de búsqueda por encuentros visuales sin restricción, la cual es una técnica de inventario y/o monitoreo para determinar la riqueza de especie en una área y estimar las abundancias relativas de poblaciones (Crump y Scott, 1994). En el momento de la captura de cada individuo se tomaron datos: merísticos, habitacionales y color, y se le praticó la eutanasia en el lugar de trabajo. Eutanasia: se tomó una muestra de 30 ejemplares, los cuales se sacrificaron mediante una cantidad letal de anestésico (Roxicaina o Junicaina) inoculado por punción cardiaca, la cantidad suministrada se realizó de acuerdo al tamaño del animal, evitando la sobre saturación de líquidos en el cuerpo de los individuos lo cual ocasiona la deformación de los mismos. Fijación: se realizó en una cámara húmeda de formalina en donde a los ejemplares se les inyectó una solución de formalina al 10% (por todo el cuerpo para evitar su descomposición), luego permanecieron por un periodo de 24 horas en la cámara de fijación; igualmente se le inyectó en la parte posterior de la cola para conocer el sexo del animal con base a la metodología de Jackson (1971), citado por Rengifo (2002).
Preservación: los ejemplares se depositaron en recipientes con agua durante dos horas, y luego se conservaron en alcohol al 7 %. El material determinado fue catalogado con los códigos del UTCH:COLZOOCH-H 160 hasta UTCH:COLZOOCH-H 200 y entregado a la Colección de Referencia de La Fauna Chocoana – Herpetología de la Universidad Tecnológica del Chocó "Diego Luis Córdoba" con registro único nacional de colecciones (197).
Uso de microhabitat de A. maculiventris
Para la caracterización de la distribución espacial, se contaron con algunos datos ecológicos sugeridos por Heyer et al., (1994), como son: 1). posición vertical (altura desde el suelo o agua) tomada de forma cualitativa así: suelo (0cm), baja (<49 cm.), media (50 – 149cm), alta (>150cm) y 2). tipo de sustrato en el que se encontró el individuo en el momento de captura (hojas, ramas, piedras, hojarascas, tallo, etc.).
Dimorfismo en A. maculiventris
Para conocer el grado de dimorfismo sexual de A. maculiventris, de cada ejemplar se tomaron medidas corporales siguiendo a Velasco y Herrel (2007) como: 1). longitud hocico cloaca (LRC); desde la escama mentoniana, hasta el borde anterior de la cloaca; 2). largo de la cabeza (LC), desde la escama rostral hasta el occipital; 3). altura de la cabeza (AC), va desde la parte gular hasta la occipital; 4). ancho de la cabeza (ANC), desde el borde supra ocular derecho al izquierdo; 5). longitud fémur derecho, (LFD); 6). longitud de la tibia derecha (LTD), desde la unión femoral hasta el cóndilo tarsal; 7). ancho de la boca (APB), que se mide de lado a lado en boca; 8). longitud del humero derecho (LHD), desde la unión clavicular hasta el cóndilo humeral; 9). largo de la cola (LCO), desde el borde posterior de la cloaca hasta su extremo apical; 10). (LCU). longitud del cuerpo, que va desde la parte superior del humero hasta el fémur; 11). (DPD), dedo posterior derecho; 12). (LRD), longitud del radio derecho. Las medidas de establecieron con calibrador digital caliper (150 mm), en el laboratorio de Zoología de la Universidad Tecnológica de Chocó "Diego Luis Córdoba"
Proporción de sexo
El sexo de los individuos se determinó por revisión de órganos genitales en los ejemplares capturados, y la presencia del abanico gular en machos.
Aspecto reproductivo
En el laboratorio se realizó una incisión medio-ventral a cada ejemplar preservado (diseminación), con el fin de determinar el estado reproductivo de la especie A. maculiventris. Consideramos machos adultos aquellos individuos que presentaron testículos agrandados (30,4 X 2,3 mm de acuerdo con nuestro registro de macho menor en LHA, sexual mente activo) y epidimos dilatados (Vitt y Zani, 2005).
Las hembras se clasificaron según las condiciones de madurez de acuerdo con Licht y Gorman (1970), en: privelogenica (sin folículos vitelogénicos, ni presencia de huevos en los oviductos), vitelogénica (con folículos vitelogénicos, diámetro mayor a 2 mm, de color amarillo) vitelogenica y ovigera (con folículos vitelogenico en un ovario y un huevo oviductal en el otro tracto simultáneamente), y ovigera (huevo en un oviducto con cascara completo y en el oviducto contrario empieza la formación de cascaras del segundo huevo)
Identificación de los contenidos estomacales
Para identificación de los contenidos estomacales, se realizó una incisión medio-ventral a 30 individuos repartidos equitativamente entre machos y hembras. Esta se realizó in situ, por medio de una disección a cada espécimen sobre la región ventral, luego se le retiro todo el tracto digestivo y se almaceno en frascos plásticos que contenían alcohol al 70% las muestras colectadas se trasladaron al laboratorio de zoología de la Universidad Tecnológicas del Chocó, para su respectiva identificación.
En laboratorio se trabajó con contenidos estomacales e intestinales ya que se ha demostrado que al revisar solo los contenidos estomacales se podría perder información y además se tendría una tendencia a encontrar presas grandes, ya que las presas pequeñas pasarían más rápidamente a la porción intestinal del tubo digestivo, (Schoener, 1989).
Para la identificación de los ítems alimenticios se utilizaron guías de campo y claves de Coronado y Márquez (1972), Mesa y Zuluaga (1995), Cabezas (1996) esta determinación se llevó hasta la mayor categoría posible, principalmente orden o familia, con la ayuda de un estereoscopio (Carl Zeiss México), después de haber sido realizado el análisis dietético de los ejemplares, se almacenaron y se preservaron los contenidos gastrointestinales y el alcohol 70%; los cuales fueron depositados en la Colección Científica de Referencias Zoológicas del Chocó – Herpetología.
Análisis de los datos
Dimorfismo sexual, estado reproductivo y proporción sexual
Dimorfismo Sexual
Para el grado de dimorfismo sexual (GDS) e índice de dimorfismo sexual (IDS), se consideró la metodología usada por Selander y Giller (1963), en donde se usa la diferencia de los promedios dividido por la suma de los promedios en donde: Xh = promedio de hembras y Xm = promedio de machos.
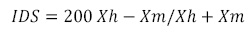
Ralls (1976) y Fitch (1981), plantean que cuando uno de los sexos es más grande que el otro, se debe utilizar el promedio simple de tamaño de hembras dividido por el tamaño de machos y esto podría ser considerado como el grado de dimorfismo sexual (GDS).
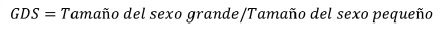
Aspecto reproductivo
Calculamos el volumen del testículo derecho de cada macho adulto basado en la formula esferoide propuesta por (Pianka, 1970).
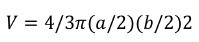
Donde V es el volumen, a corresponde al largo y b al ancho del testículo. Determinamos el tamaño mínimo de madures en cada sexo, basados en el registro de macho menor en longitud hocico ano del individuo más pequeño que presente gónadas con actividad reproductivas (Vitt y Zanig, 2005), y además se realizó una prueba de Chicuadrado para conocer las diferencias estadísticas en volumen de los testículos.
Las hembras adultas se clasificaron según la condición reproductiva de acuerdo con Licht y Gorman (1970) en: previtelogénica (sin folículos vitelogénicos, ni presencia de huevos en los oviductos), vitelogénica (con folículos vitelogénicos, diámetro mayor a 2 mm, de color amarillo), vitelogénica y ovigera (con un folículo vitelogénico en un ovario y un huevo oviductal en el otro tracto simultáneamente) y ovígeras con dos huevos oviductales (huevo en un oviducto con cáscara completo y en el oviducto contrario empieza la formación de la cáscara del segundo huevo). Calculamos el volumen del testículo derecho de cada macho adulto basándonos en la fórmula del esferoide prolapasado (Pianka, 1970).
Proporción de sexo
El sexo de los individuos se determinó por revisión de órganos genitales en los ejemplares capturados y la presencia del abanico gular (ya que es características únicamente de los machos).
Se tomaron 12 medidas corporales con el propósito de establecer diferencias entre los machos y hembras teniendo encuenta estos aspectos morfométricos, se realizo una prueba no paramétrica de Mann–Whitney U-test, con su respectivo valor de significancia y graficados con el program estadístico SPSS por Windows.
Uso de hábitat de A. maculiventris en zonas de bosque pluvial tropical
Para determinar la existencia o no de diferencias estadísticas significativas entre los sustratos y la posición vertical usados por la especie A. Maculiventris, se aplicó una prueba no paramétrica de Chi-cuadrado, se elaboraron tablas de contingencias y gráficos de barras en el programa Excel (2007). Se elaboraron tablas de contingencia para expresar la actividad de los individuos en el momento del encuentro visual con los investigadores.
Análisis dietario de A. maculiventris, en zonas de bosque pluvial tropical
Se calcularon las novedades tróficas acumuladas utilizándose para establecer la muestra mínima de ejemplares en este estudio, usando estimadores (Chao 1 e ICE) de riqueza para conocer la representatividad de los estómagos diseminados.
Se diseminaron 30 estómagos (15 machos y 15 hembras), determinándose las presas hasta el nivel de orden; cada presa se le midió su largo (L) y ancho (A) con el fin de calcular su volumen, con la fórmula de una esfera elipsoide (Dunham, 1983) la fórmula es:
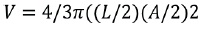
Para conocer la contribución de cada categoría de alimento en la dieta se calculó el Índice de Importancia Relativa (IRI) propuesto por Pinkas et al., (1971). La fórmula: IRI = (%N +% W )x % F donde N: es el porcentaje numérico agregado, W: es el volumen porcentual agregado y F: la frecuencia de ocurrencia. Este índice permite comparar la importancia relativa que cada ítem representa en la dieta total de la especie depredadora.
Para calcular la jerarquía de las presas en la dieta, se aplicó al valor de IRI el Índice de Jerarquización (DJ), que toma el valor más alto del IRI y calcula el porcentaje de todos los demás valores a partir de él. Si el porcentaje del ítem presa se encuentra incluido entre el 100% y 75% se lo considera fundamental; si se ubica entre el 75% y 50% se lo considera secundario, si esta entre 50% y 25% es accesorio, y si está por debajo del 25% se lo considera accidental (Martori, 1991).
Además, se calculó la diversidad trófica (H’) según el criterio de Hurtubia (1973) y amplitud de nicho trófico, utilizando la siguiente fórmula, propuestas por Levins (1968). Amplitud de nicho trófico (Simpson)
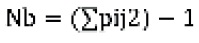
RESULTADOS
Dicromatismo sexual
La especie A. maculiventris presentó tanto en machos como en hembras una coloración café clarocon un pequeño lunar en la parte posterior de la cabeza, además, las hembras presentan una estrecha línea dorsal con una intercalación de colores entre café claro y oscuro que se extiende desde la cabeza hasta la cola, y su parte ventral de color blanco con moteaduras de color café, en machos el abanico gular es grande y de color anaranjado con puntos irregulares de color negro, en las hembras estas características no se notan puesto que no las presentan. Hay una gran variación de color y patrones de coloración, según estados de los individuos, tienden a tener cambios momentáneos de sus color y el patrón. Es posible que algunas hembras adultas tengan en la región medio dorsal una lista clara desde la cabeza hasta la cola, patrónmas relacionado a una forma de camuflaje generando un patrón disruptivo corporal.
Proporción macho y hembras
Fueron registrados 75 individuos de A. maculiventris (25 hembras y 50 machos), donde las proporciones y razón de sexo en los individuos capturados mostraron diferencias estadísticas significativas (X2: 4,81, gl: 1, p: 0,028) Grado (gds) e índice (ids) de dimorfismo sexual de A. maculiventris
El grado de dimorfismo sexual (GDS) e índice de dimorfismo sexual de A. maculiventris, fue de 1,08 mm, y un de 8,5 mm, respectivamente, lo cual indica que las hembras son ligeramente más grandes que los machos, presentando un promedio de diferencia respecto a la LHA de 33,5 a 36,54 mm. Al comparar las medias de las distintas regiones corporales de A. maculiventris en macho y hembras mostraron que difieren en todas las regiones corporales medidas, (tabla 1). Se realizó una correlación de las 12 medidas tomadas a hembras y machos se logra demostrar que las hembras difieren significativamente de los machos en todas las regiones corporales medidas; encontrándose diferencias estadísticas significativas entre machos y hembras adultos, en las siguientes variables: longitud rostro cloaca (Mann-Whitney U Test, Z = -2.90346; p = 0.003691), longitud cabeza (T-tests, t-value = -5.16098; p = 0.000018), ancho de la cabeza (T-tests, t-value = -2.50824; p = 0.018203), longitud cola (Mann-Whitney U Test, Z = -2.13612; p = 0.032670), (fig. 1), las hembras presentaron tamaños superiores a los machos en todas las regiones corporales medidas.
Evaluación de las características reproductivas
De los 30 individuos diseminados de A. maculiventris (15 hembras 15 machos), a los cuales se les determino su estado reproductivo y se pudo registrar un tamaño mínimo de madurez (LHA), se encontró que en hembras es de 30,7 mm, con un máximo de 39,9 mm y una media de 36,5 mm; para machos se registró una mínima de madurez sexual de 30,4 mm, con un máximo de 36,7 mm, con una media de 33,8 mm; lo cual indica que las hembras pueden alcanzar madurez sexual a tallas muchas más grandes en comparación con los machos. No se encontraron diferencias significativas en el volumen de los testículos de los machos adultos (x2 = 5,667, SI = 9. p = 0,773). El estado reproductivo mas común de las hembras adultas en los periodos de muestreo fue vitelogénico, todas las hembras fueron consideradas sexualmente activas, ya que fueron encontradas con folículos vitelogénicos mayor a 2,0 diámetros de color amarillo, por lo tanto se consideraron como adultas.
Uso de hábitats
La población de A. maculiventris reportada (n=75) en los sustratos evaluados, mostró una mayor abundancia
o frecuencia de ocurrencia en el sustratos troncos con (n: 31) individuo que representa el 23,25% de los reportados en el estudio, seguido por los sustratos rama (n: 23) con 17,25% de los estudiado, mostrando diferencias estadísticas significativas con relación a los demás sustrato utilizados. (X2=16,89, gl: 3 p: 0,001); el resto de sustratos estuvieron muy baja frecuencia de individuos.
Este estudio muestra que los individuos de la especie A. maculiventris, tuvieron una mayor frecuencia de ocurrencia en los extractos medios (baja y media) en las diferentes coberturas vegetales estudiadas, no encontrando una diferencia estadística significativa entre los mismos (X2=3,77, gl: 3, p: 0,207.) , los otros extracto de coberturas vegetales mostraron valores muy similares (tabla 2).
Dieta de A. maculiventris
Para el análisis dietario de la especie A. maculiventris se diseminaron 30 estómagos (fig. 2), de los cuales 15 pertenecieron a machos y 15 a hembras, se registró un total de 46 presas gastrointestinales. En los ejemplares de los machos se encontraron un total de 20 presas, de las cuales las hormigas fueron las de mayor proporción, mientras que en las hembras se registró un total de 26 presas, con las hormigas como las de mayor consumo, pero con un volumen más alto de presas ingeridas que los machos; los Coleópteros en segundo lugar (tabla 3), mostrando a los órdenes Himenóptera (Formicidae) y Coleóptera como los de mayor importancia relativa en la dieta de la población de A. maculiventris, se registraron en algunos individuos restos de organismos no identificados, los cuales no fueron tenidos en cuenta en el análisis de los datos.
Se realizó una curva de novedades tróficas la que determinó la representatividad trófica encontradas en los 30 estómagos diseminados, usando los estimadores ICE y Chao 1, los cuales indicaron que los items registrados no hacen parte de la dieta absoluta de la especies, ya que según ICE representa el 77% y Chao 1 63% de lo estimado de representatividad de las presas (fig. 2). Anolis maculiventris presentó una diversidad trófica de H`= 1,47 y una amplitud de nicho de Nb = 0,75.
DISCUSIÓN
Una característica importante de resaltar en los diferentes estadios de desarrollo entre hembras y machos de la especies A. maculiventris, es que pueden cambiar de color cuando son capturados, el color del cuerpo se torna pardo, pero luego de un tiempo de estar fuera de su ambiente natural vuelven a su color que es café claro con franjas en la parte dorsal que se extiende desde la cabeza hasta la cola, según Young (1977), el color de los Anolis pueden cambiar de color de acuerdo con el ambiente, en respuesta a la temperatura y otras variaciones ambientales; además este mismo autor indica que probablemente en estas lagartijas no existen nervios que vayan a los melanóforos, los cuales son controlados mediante hormonas producidas por el lóbulo posterior de la hipófisis y otras glándulas; como ocurre en los camaleones.
En la mayoría de los Anolis machos, el tamaño del abanico gular, es proporcional al longitud corporal y es más que el 35% con relación al tamaño del cuerpo. Los machos mediante despliegues del abanico gular, anuncian su presencia ante otros machos, antes que otros animales pequeños o grandes se acerquen a ellos, también ante las hembras para atraerlas e incitaras a copular Crews (1973).
Encontrando mayor número de machos (proporción 2:1), como caso muy atípico con relación a este grupo taxonómico, (ya que la razón de sexos en poblaciones de lagartijas durante los meses del año no es variable y siempre se mantiene cerca al 1:1), esto sugiere que probablemente debe existir un fuerte limitante como efecto negativo de depredación en la población.
Las 12 regiones corporales medidas mostraron que las hembras son más grandes que los machos; caso contrario de lo que reportaran (Savage y Villa, 1986; Leal et al., 2002), quienes afirman que en la mayoría de las especies de la familia Polychrotidae el macho es más grande que la hembra, coincidiendo con Gibbon y Lovich (1990), quien afirma que en los Anolis, los machos son más grandes que las hembras, por ventajas competitivas en los encuentros machos-machos en presencia de una hembra. Las diferencias en tamaños, entre machos y hembra reducen la competencia entre los sexos, por alimentos y otras necesidades (Price, 1984; Carothers, 1984; Selander, 1972). Lo anteriot contrasta con lo afirmado por Price (1984) y Carothers (1984), quienes indican que en algunos reptiles, las hembras son más grandes que los machos por el requerimiento de llevar los huevos y tener mejor éxito reproductivo.
Nuestros resultados mostraron que las hembras de A. maculiventris presentaron un tamaño corporal mayor que los machos, estos datos concuerdan con los resultados encontrados para la especie A. tolimensis, A. fuscauratus, A. trachyderma y A. antonii, donde los machos y las hembras presentaron diferencias morfométricas en la longitud rostro cloaca (Vitt et al., 2002; Vitt et al., 2003, Castañeda, 2001). Lo cual indica que las hembras fueron más grandes que los machos, caso contrario a lo que afirman Rodríguez-Schettino et al., (1999), donde sostienen que el género Anolis, en muchas especies los machos son de mayor tamaño que las hembras.
La no variación del tamaño testicular en machos adultos y la presencia de hembras adultas con actividad reproductiva, sugieren que la población presenta reproducción constante. Sin embargo, consideramos que sería importante progresar en conocimientos al respecto. Para el caso del tamaño testicular, nuestros resultados concuerdan con lo registrado por Vitt et al., (2002), en A. trachyderma, Licht y Gorman (1970) y Sherbrooke (1975), quienes resaltan la dependencia que puede existir entre el tamaño testicular y la actividad reproductiva.
Uso de hábitat
Se puede percibir que la especie A. maculiventris tiene un alto grado de preferencia por los troncos, ya que se le observó con un alto nivel de ocurrencias en este con un 41,3% de los individuos registrados. Además, tiene la capacidad de explorar otros sustratos, demostrando ser una especie bastante adaptable a cualquier tipo de hábitat comportamiento similar a la mayoría de las especies de este género (Velasco y Herrel, 2007).
Los individuos de A. maculiventris estudiados son principalmente arborícolas – arbustivos. Esta especie mostró más actividad en los estratos de mayor diámetro (troncos) con un 41,3% de los reportados, lo cual podría estar relacionado con estrategias de defensas de esta especie.
La mayoría de los individuos de A. maculiventris utilizaron variedad de sustratos como troncos, ramas, hojarascas, raíces (tabla 3), donde se perchan para cazar y huir fácilmente de sus depredadores, lo cual hace que se pueda estudiar mejor esta especie ya que no se tiene una información detallada de esta en la región, al igual que muchas otras especies de este grupo (Campbell, 1973; Hertz, 1975; Rand y Rand, 1976).
La selección de hábitat de los individuos de A. maculiventris es un proceso de elegir determinados recursos s entre los que se encuentran disponibles en el ambiente (Partridge, 1978; Garshelis, 2000), tal proceso depende de la estructura física del ambiente, la fisiología del animal, la disponibilidad de alimento y la protección contra depredadores (Reaney y Whiting, 2003).
Los individuos de A. maculiventris fueron registrados en todos las áreas muestreadas y en casi todos los sustratos evaluados, concordando con lo reportado por Páez et al., (2002) quienes afirman que los Anolis son un grupo de animales que se puede adaptar a una gran diversidad de biotopos, y con Duellman (1979) quien sostiene que los reptiles en las selvas tropicales exploran habitas arbóreos, terrestre, acuático o semiacuáticos. Se encuentran distribuidos desde los Estados Unidos hasta Brasil y desde los 0 hasta los 2000 m s.n.m. (Williams, 1976; Guyer y Savag, 1986; Frost y Etheridge, 1989).
Dieta de A. maculiventris
El hecho de que las hormigas hayan sido las presas más consumidas en este estudio, puede ser porque son un recurso fácilmente y disponible para predadores, ya que se encuentran en colonias y son lentas, (Parmelee, 1999), lo que les proporciona A. maculiventris un alimento contaste y abundante para la satisfacción de sus requerimientos tróficos.
Según Rodríguez-Schettino y Martínez-Reyes, 1992; Rodríguez-Schettino y Martínez-Reyes,1994; Rodríguez-Schettino y Martínez-Reyes, 1996) y Eaton et al., (2002), la ingesta alta de hormigas es común en las especies del género Anolis al ser estos, insectos sociales muy abundantes en todos los ecosistemas y proporcionar a los lagartos, (que son oportunistas en su dieta), de un alimento fácil de obtener, cuyo tamaño pequeño se compensa con el número alto de ítems.
Al analizar la curva de novedades tróficas se pudo determinar la representatividad trófica encontradas en los 30 estómagos diseminados, lo cual permitió establecer el porcentaje y representatividad de las presas, pero las pocas capturas no permitieron realizar inferencias sobre la verdadera conducta de A. maculiventris, que por ser un integrante del género Anolis se convierte en un eminente consumidor secundario, por lo que se alimentan de una gran cantidad de insectos (Ortóptera, Homóptera, Díptera), y otros artrópodos como Aracneida, Chilopoda y Crustacea, estos últimos no reportados en la dieta de esta especie que a la vez integra a su dieta pequeñas frutas (Castro, 2008).
De acuerdo al análisis de importancia relativa de las presas gastrointestinales de A. Maculiventris, se muestra que el orden Himenóptera (hormiga) ocupo el primer lugar de importancia con un IRI, 82,3 seguido por los Coleópteros (cucarrón), con un IRI 64,9 respectivamente, hecho relacionado con el tamaño de las presas. También hubo una contribución del orden Ortóptera, las otras categorías de presa consumidas, (Dípteros, Hemípteros y Homóptero), presentaron un volumen reducido o quizás porque se encontraron en un estado avanzado de digestión.
Con relación al tipo de sexo, a las hembras se les registro 26 tipos de presas, mientras que los machos se les registro 20 presas gastrointestinales, con los Himenópteros (hormigas) en mayor frecuencia y los Coleópteros, en segundo lugar, esto puede atribuirse a que las hembras tienen una mayor demanda energética durante la época de reproducción, caso contrario de lo que afirma (Rodríguez-Schettino et al., 1999), quienes mencionan que en el género Anolis, los machos son de mayor tamaño que las hembras, en casi todas las especies, y consumen mayor número de presas y de mayor tamaño.
Las apreciaciones anteriores ponen de manifiesto que las especies del género Anolis son eminentemente consumidores secundarios, por lo que se alimentan de una gran cantidad de insectos (Himenópteros, Coleópteros, Hemípteros, etc.) y en otras ocasiones de artrópodos como Arácnida, Chilopoda y crustacea, que para este estudio no fueron reportados y que a la vez son potencialmente nocivos para la agricultura, la salud humana y animal, así que de esta manera los Anolis contribuyen al mantenimiento del equilibrio ecológico en la naturaleza junto con el consumo de pequeñas frutas (Castro, 2008). A su vez estos animales al ser presas de otros, intervienen en importantes redes alimentarias que tienen lugar en la naturaleza.
CONCLUSIONES
La especie presenta un bajo grado de diferenciación en términos de coloración entre machos y hembras, siendo la única diferencia una línea más clara sobre la región dorsal de las hembras, la cual se extiende desde la cabeza hasta la cola. Las hembras de A. maculiventris mostraron ser más grandes que los machos en todas las regiones corporales medidas, expresando diferencia estadística significativa de acuerdo al GDS y IDS, indicando una difierenciación leve de las hembras con los machos.
La especie tiende a usar microhábitats en los estratos bajos y medios, generalmente en los troncos y ramas de los árboles, pero también fue encontrada usando las partes bajas donde su coloración critica les ayuda a la obtención de su alimentación y las partes altas para huir de sus predadores naturales y escapar de posibles intrusos. Según la curva de novedades tróficas, en los estómagos diseminados se pudo registrar un porcentaje significativo de la amplia variedad trófica que esta especie puede alimentarse en los bosques tropicales. El orden de insectos con mayor importancia relativa en la dieta de la especies fue el Himenóptero, seguido del orden Coleóptero, ya que su frecuencia y volumen así lo confirman.
AGRADECIMIENTOS
Los autores agradecen al grupo de investigación en Herpetologia de la Univerisdad Tecnológica del Chocó, Cumunidad de Samurindó – Municipio del Atrato, Jhon Jairo López, Jefferson Asprilla Perea y Dario Barahona por sus contribuciones al documento.
REFERENCIAS
Beuttell K, Lososs JB. Ecological morphology of Caribbean anoles. Herpetol Monogr. 1999;13:1- 28. [ Links ]
Bitt LJ, Zani PA, Durtsche RD. Ecology of the lizadrs Norop soxilophus Policrotydae in lowland forest of southeastern Nicaragua. Can J Zool. 1995;73:1918-19127. [ Links ]
Cabezas-Melara FA. Introducción a la entomología. Ed. Trillas. México. 1996. 142 p. [ Links ]
Campbell HW. Ecological observations on Anolis lionotus and Anolis poecilopus (Reptilia, Sauria) in Panamá. Am Mus Nat Hist Univ Florida. New York. 1973;2516:1-29. [ Links ]
Carothers JH. Sexual selection and sexual dimorphismin some herbivorous lizards. Am Natur. 1984;124(2):244-254. [ Links ]
Castañeda M. Caracterización y dinámica de poblaciones de Anolis antonii (Sauria: Polychrotidae) en bosques y coberturas secundarias de la zona norte del Quindío, Colombia. Departamento de Biología. Facultad de Ciencias. Universidad de los Andes, Trabajo de grado. 2001. p. 115. [ Links ]
Castaño O, Cárdenas G, Hernández E, Castro F. Reptiles en el Chocó biogeográfico. In: Rangel-Ch., editor. Colombia diversidad bioética tomo IV. Editorial Guadalupe Ltda. Bogotá; 2004. p. 277-324. [ Links ]
Castro F. Ecología de una comunidad de lagartos del bosque pluvial central de Costa Pacífica colombiana. Departamento de Biología. Facultad Ciencias Básicas. Universidad del Valle, Cali. Trabajo de Grado. 1988. p.113. [ Links ]
Coronado R, Márquez A. Introducción a la Entomología. Limusa-Wiley, S.A., Arcos de Belem. México. 1972. 282 p. [ Links ]
Crews D. Condition-induced inhibition of sexual receptivity in female lizards (Anolis carolinensis) Physiol Behav. 1973;11(4):463-468. [ Links ]
Crump M, SCott N. Visual encounter surveys. In: Heyer R, Donnelly M, McDiarmid R, Hayek L, M. Foster M, editors. Measuring and Monitoring Biological Diversity: standard methods for amphibians. Smithsonian Institution Press. Washington; 1994. p. 84-92. [ Links ]
Duellman WE. The Biology of an Equatorial Herpetofauna in Amazonian Ecuador. Publ Mus Nat Hist Univ. Kansas; 1978. 352 p. [ Links ]
Duellman WE. The herpetofauna of the Andes: Patterns of distribution, origin, differentiation and present cornmunities. In: Duellman WE, editor. The South American Herpetofauna: Its origin, Evolution and Dipersal. Museum of Natural History Monograph 7, the University of Kansas. 1979. p. 371-459. [ Links ]
Dunham AE. Realized niche overlap, resource abundance and intensity of interspecific competition. In: Huey RB, Pianka ER, Schoener TW, editors. Lizard Ecology. Harvard University Press, Cambridge, Massachusetts, U.S.A; 1983. p. 261-280. [ Links ]
Dunlap J, Mena C. Diversidad de Anolis (Lacertilia: Policrotydae) en áreas con diferentes grados de intervención, corregimiento de Corregimiento de Salero, Unión Panamericana, Chocó-Colombia. 2009; p. 86. [ Links ]
Eaton JM, Larimer SC, Howard GK, Powell R, Parmerlee JS. Population densities and ecological release of the solitary lizard Anolis gingivinusin Anguilla, West Indies. Car J Science. 2002;38:27-36. [ Links ]
Fitch HS. Sexual size difference in reptiles. Misc Pbl Mus Nat Hist Univ Kansas. 1981;70:1-72. [ Links ]
Frost DR, Etheridge RA. Phylogenetic Análisis and Taxonomy of Iguanian Lizards. (Reptilia: Squamata). Misc Pbl Mus Nat Hist Univ Kansas. 1989;81:1-65. [ Links ]
García U, Rengifo J, Moreno F, Jiménez M. Diversidad de lagartos (Squamata: Lacertilia) en el sotobosque de cuatro localidades asociadas a la cuenca del rio Cabí, Chocó, Colombia. Revista Institucional Universidad Tecnológica del Chocó "D. L. C.". 2006;25:47-55. [ Links ]
Gibbons JW, Lovich JE. Sexual dimorphism in turtles with emphasis on the slider turtle (Trachemys scripta). Herpet Monogra. 1990;4:1-29. Stable URL: http://www.jstor.org/stable/1466966. [ Links ]
Guyer C, Savage JM. Cladistic relation ships among Anoles (Sauria: Iguanidae). Syst Zool. 1986;35(4):509-531. [ Links ]
Hertz PE. Thermal passivity of tropical forest lizard Anolis polylepis. J Herp. 1975;8(4):23-327. [ Links ]
Heyer W, Donnelly M, Mediainmid R, Hayek L, Foster M. Measuring and Monitoring Biological Diversity. Standard Methodos for Amphibians. Smithsoni an Institution Press, Washington D.C. 1994;364 p. [ Links ]
Hurtubia J. Trophic diversity measurement in sympatric predatory species. Ecology. 1973;54(4):885-890. [ Links ]
Leal M, Knox AK, Losos JB. Lack convergence in aquatic Anolis lizards. Evolution. 2002;56(4):785-991. [ Links ]
Levins R. Evolution in Changing Environment. Princeton University Press, Princeton; 1968. 132 p. [ Links ]
Licht P, Gorman GC. Reproductive and fat cycles in Caribean Anolis lizards. University of California Publications in Zoology.1970;95:1-52. [ Links ]
Martori A. Alimentación de los adultos de Eoproctus asper (Dugés 1853) en la montaña media del Pirineo catalán. Rev Esp Herp. 1991;5:23-36. [ Links ]
Mesa N, Zuluaga J. Guía básica para identificación de familias de insectos. UNC. Departamento de Agricultura Sede Palmira, Valle, Colombia; 1995. p.55-56. [ Links ]
Páez PV, Bock CB, Estrada J, Ortega MA, Daza JM, Gutierrez PD. Guía de campo de algunas especies de anfibios y reptiles de Antioquia. Colciencias. Multimpresos Ltda. Medellin; 2002. 87 p. [ Links ]
Parmelee JR. Trophic ecology of a tropical anuran assemblage. Scientific Papers Natural History Museum The University of Kansas.1999;11:1-59. [ Links ]
Pianka ER. Comparative autecology of the lizard Cnemidophorus tigris in different parts of its geographic range. Ecologic.1970;51(4):703-720. Doi: http://dx.doi.org/10.2307/1934053. [ Links ]
Pianka ER. Species diversity. Chapter in Topics in the Study of Life: The Bio Source Book. Harper and Row, New York; 1971. p. 401-406. [ Links ]
Price TD. The evolution of sexual size dimorphism in Darwin´s finches. Am Natur. 1984;123(4):500-518. [ Links ]
Ralls K. Mammals in whi females are larger tan males. Q Rev Biol. 1976;51:245-276. [ Links ]
Rand AS. Ecology and social organization in the iguana lizard Anoles lineatopus. Proc US Nat Mus. 1967;(122):1-77. [ Links ]
Rand WM, Rand AS. Agonistic behavior in nesting iguanas: a stochastic analysis of dispute settlement dominated by the minimization of energy cost. Z Tierpsichologie. 1976;40(3):279-299. Doi: 10.1111/j.1439-0310.1976. tb00938.x [ Links ]
Rangel JO. Colombia Diversidad Biótica, IV, El Chocó Biogeográfico/Costa Pacífica. Instituto de Ciencias Naturales de la Universidad Nacional de Colombia, Conservación Internacional, Bogotá; 2004; 997 p. [ Links ]
Reaney LT, Whiting MJ. Picking a tree: habitat use by the tree agama, Acanthocercus atricollis atricollis, in South Africa. Afr Zool. 2003;38(2):273-278. [ Links ]
Rengifo JT, Asprilla J, Jiménez OA, Renjifo RJ, CAstro AA. Ecología y estructura de la comunidad de reptiles presente en el corregimiento de Pacurita municipio de Quibdó. Chocó - Colombia. Memoria del V Seminario de Medio Ambiente y Desarrollo Sostenible. Bucaramanga; 2002. 89 p. [ Links ]
Rengifo JT, Castro FC, Purryo FJ. Diversidad de una comunidad de Anolis (Iguana: Dactyloidae) en la selva pluvial central del Chocó, Colombia. Basic Appl Herpet. 2014. Doi: http://dx.doi.org/10.11160/bah.12004. [ Links ]
Rengifo JT. Estudio de la comunidad de reptiles en dos zonas del bosque pluvial tropical en el departamento del Chocó. Trabajo de grado. Universidad Tecnológico del Chocó "Diego Luis Córdoba". 2002. [ Links ]
Rentería E. Caracterización taxonómica de la comunidad de reptiles presentes en la estación ambiental Tutunendo (EAT) Quibdó-Chocó. Universidad Tecnológica del Chocó, Facultad de Ciencias Básicas. Programa de Biología con Énfasis en Recursos Naturales. Trabajo de grado. Quibdó, Colombia. 2006. [ Links ]
Rodríguez-Schettino L, Martínez-Reyes M. Algunos aspectos de la ecología trófica de Anolis argenteolus (Sauria: Polychridae) en una población de la costa suroriental de Cuba. Biotropica. 1996;28(2):252-257. [ Links ]
Rodríguez-Schettino L, Martínez-Reyes M. Características tróficas de una población de Anolis lucius (Iguania: Polychridae) en la costa septentrional de Cuba. Avicennia. 1994;1:67-77. [ Links ]
Rodríguez-Schettino L, Martínez-Reyes M. Hábitos alimentarios de Anolis bartschi en San Vicente, Pinar del Río, Cuba. Ciencias Biológicas. 1992;25:30-40. [ Links ]
Rodríguez-Schettino L. Systematic accounts of the species. In: The Iguanid Lizards of Cuba. Rodriguez L, editor. University Press of Florida, Gainesville, USA; 1999. p. 104- 380. [ Links ]
Rougharden J. Anolis lizards of the Caribbean: ecology, evolution, and plate tectonics. Oxford University Press, New York, U.S.A; 1995. 200 p. [ Links ]
Savage JM, Guyer C. Infrageneric classification and species composition of the Anole Genera, Anolis, Ctnonotus, Dactyloa, Norops and Semiurus (Sauria: Iguanidae). Amphibio Reptilia. 1989;10:105-116. [ Links ]
Savage JM, Villa J. Herpetofauna de costa Rica Society fort the study of amphibians and reptiles. New York. 1986. 207 p. [ Links ]
Schoener TW. The ecological niche. In: Ecological concepts: The contribution of ecology to an understanding of the natural world. University College, London, Oxford and Boston: Blackwell. 1989. p. 79-113. [ Links ]
Selander RK. Sexual selection and dimorphism in birds. In: Campbell B, editor. Sexual selection and the descent of man: 1871-1971. Aldine Publishing. Chicago; 1972. p. 180-230. [ Links ]
Sherbrooke WC. Reproductive cycle of a tropical teiid lizard, Neusticurus ecpleopus. Cope, In Perú. Biotropica. 1975;7:194-207. [ Links ]
Velasco JA, Herrel A. Ecomorphology of Anolis lizards of the Chocó Region in Colombia and comparisons with Greater Antillean ecomorphs. Biol J Linnean Soc. 2007;92(1):29-39. Doi: 10.1111/j.1095-8312.2007.00885.x [ Links ]
Vitt LJ, Avila-Pirest CS, Zani PA, Espósito MC. Life in shade: The ecology of Anolis trachyderma (Squamata: Polychrotidae) in Amazonian Ecuador and Brazil, with comparisons to Ecologically Similar Anoles. Copeia. 2002;2:275-286. [ Links ]
Vitt LJ, Avila-Pirestcs, Zanipa PA, Espósito MC, Sartorius SS. Sharing Amazonian rain-forest trees: Ecology of Anolis punctatus and A. transversalis (Squamata: Polychrotidae). J Herpetol. 2003;37(2):276-285. Doi: 10.1670/00221511(2003)037[0276:SARTEO&2. [ Links ]0.CO;2
Vitt LJ, Zani PA. Ecology and reproduction of Anolis capito Rain forest of Southeastern Nicaragua. J Herpetol. 2005;39(1):36-42. [ Links ]
Williams EE. South American Anoles: The species groups. Papeis Avulsos Zoo.1976;29:259-268. [ Links ]
Young JZ. La vida de los vertebrados Segunda Ed. Edición Omega. S.A. Barcelona, España; 1977. 660 p. [ Links ]













