Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.21 no.2 Bogotá May./Aug. 2016
https://doi.org/10.15446/abc.v21n2.49393
Doi: http://dx.doi.org/10.15446/abc.v21n2.49393
REPTILES DEL BOSQUE SECO ESTACIONAL EN EL CARIBE COLOMBIANO: DISTRIBUCIÓN DE LOS HÁBITATS Y DEL RECURSO ALIMENTARIO
Reptiles from the Seasonal Dry Forest the Caribbean Region: Distribution of Habitat and use of Food Resource
Luis Eduardo ROJAS MURCIA1, Juan E. CARVAJAL COGOLLO1, Javier Alejandro CABREJO BELLO1.
1 Grupo Biología de la Conservación, Laboratorio Museo de Historia Natural Luis Gonzalo Andrade. Universidad Pedagógica y Tecnológica de Colombia, Av. Central del Norte. Tunja, Colombia.
2 Grupo Biodiversidad y Conservación, Línea Reptiles, Instituto de Ciencias Naturales, Universidad Nacional de Colombia. Bogotá, D.C., Colombia.
For correspondence. leduardo.rojasm@gmail.com
Received: 4th March 2015, Returned for revision: 18th April 2015, Accepted: 30th November 2015. Associate Editor: Martha Ramírez Pinilla.
Citation / Citar este artículo como: Rojas Murcia LE, Carvajal Cogollo JE, Cabrejo Bello JA. Reptiles del bosque seco estacional en el Caribe Colombiano: distribución de los hábitats y del recurso alimentario. Acta biol. Colomb. 2016;21(2):365-377. doi: http://dx.doi.org/10.15446/abc.v21n2.49393
RESUMEN
Con el fin de caracterizar la distribución horizontal (repartición de los hábitats) y la utilización del recurso alimentario (tipo y tamaño de las presas) del ensamblaje de reptiles del bosque seco estacional al norte de la región Caribe de Colombia, en el departamento del Cesar, se realizaron cinco salidas de campo con una duración de doce días cada una. Los muestreos se realizaron en jornadas diurnas y nocturnas, en un diseño de transectos replicados a lo largo de diferentes hábitats que incluyeron: pastizales, bordes e interiores de bosque. Se realizaron análisis descriptivos de uso de hábitat en un perfil de vegetación por cada época climática y análisis de amplitud y sobreposición de nicho. Se registraron 38 especies de 14 familias del orden Squamata. Las especies se distribuyeron de manera homogénea entre zonas abiertas y boscosas. Se encontraron registros de 31 categorías de presa en 109 estómagos de seis especies de serpientes (61 estómagos) y siete de lagartos (48 estómagos) con un porcentaje de estómagos vacíos de 38 %. Las presas de mayor importancia para los lagartos fueron Coleoptera y Araneae, y para las serpientes fueron los anfibios. La mayoría de las especies presentaron un amplio espectro de dieta y entre especies similares, como entre Anolis auratus y A. gaigei, se presentó uso de recursos similares. En síntesis, el ensamblaje de reptiles presentó una distribución homogénea en los hábitats evaluados (áreas abiertas y boscosas) y el recurso alimentario fue variado entre las diferentes especies; la estacionalidad de la zona presenta un papel fundamental en la estructura del ensamblaje de reptiles, presentándose menos abundancia durante la época seca, tanto en las áreas abiertas como en las boscosas.
Palabras clave: competencia, distribución horizontal, dieta, nicho trófico, bosque seco estacional.
ABSTRACT
We assessed the horizontal distribution and use of the food resource of the reptile's assemblage of the seasonal tropical dry forest in the North of the Caribbean region of Colombia, department of Cesar. Five fieldtrips of 12 days each were performed, sampling was diurnal and nocturnal, following a transect design replicated along different habitats including grasslands, edge and interior of forest. We performed descriptive analyzes of habitat use, using a profile of vegetation by each climatic period; we also did an analysis of amplitude and niche overlap. We recorded 38 species of 14 families of the Squamata order. Species distributed evenly between open and forested areas. Record of 31 categories of prey in 109 stomachs of six species snakes (61 stomachs) and seven of lizards (48 stomachs) with a percentage of empty stomachs of 38 % was found. The preys of greater importance for the lizards were Coleoptera and Araneae and for snakes, amphibians. Most of the species presented a wide range of diet and between similar species, such as Anolis auratus and A.gaigei, found a similar use of resources. In summary, the assembly of reptiles presented a homogeneous distribution in the habitats evaluated (forested and open areas) and the food resource varied among the different species; the seasonality of the area plays a fundamental role on the structure of this reptile assembly with less abundance during the dry season in both, open and forested habitats.
Keywords: competition, diet, horizontal distribution, trophic niche, tropical dry forest.
INTRODUCCIÓN
Los reptiles ocupan una gran variedad de hábitats y de tipos de coberturas, desde áreas abiertas y bosques transformados, hasta bosques conservados (Duellman, 1979); este uso diferencial de los hábitats o de las coberturas originales da lugar a patrones de distribución horizontal y vertical diferente de los ensamblajes, con la consiguiente diferenciación en el uso de los recursos, entre estos el alimentario (Pianka, 1973; Duellman, 1979; Vitt y Pianka, 2005; Mesquita et al., 2006a). Esta estructuración de los ensamblajes (su riqueza y abundancia) son producto de múltiples procesos, entre los cuales están las características abióticas del ambiente local, las interacciones interespecíficas que promueven o limitan la coexistencia, eventos estocásticos de colonización y extinción local, y factores históricos, como son la especiación, las invasiones y extinciones regionales (Ricklefs y Schluter, 1993; Chase y Leibolt, 2003). En este sentido mediante dos enfoques fundamentales se ha tratado de dar explicación a los patrones de uso de recursos observados en un ensamblaje y/o comunidad determinada, el primero aborda los ensamblajes desde la estructuración por nicho ecológico, el cual considera la composición de especies de una comunidad como resultados de filtros impuestos por el ambiente y por interacciones interespecíficas (MacArthur y Levins, 1967), y el segundo es el de los ensamblajes por dispersión,el cual se fundamenta en la capacidad de los organismos de colonizar nuevos hábitats, bajo este enfoque los mecanismos biogeográficos y evolutivos tienen un papel fundamental en la explicación de los patrones observados, excluyéndose notablemente los mecanismos ecológicos asociados a las interacciones interespecíficas (Hubbel, 2001; Berazategui, 2012).
Bajo este contexto la importancia del uso y repartición de cada recurso, difiere en las relaciones intra e interespecificas y en particular en las especies simpátricas (Toft, 1985; Pianka, 1993). Este hecho ayuda a comprender los patrones de distribución, de abundancia y de diversidad de las especies. La repartición de los recursos se puede dar en tres categorías y/o dimensiones: el hábitat, el alimento y el tiempo. Estas dimensiones se pueden subdividir en macro y microhábitat, tipo y tamaño de alimento y tiempo de actividad, estacional y diaria (Pianka, 1969; Pianka, 1973; Pianka, 1993), las cuales están directamente relacionadas con los factores ecológicos, históricos e intraespecíficos que las definen.
En condiciones naturales el espectro de recurso disponible cambia constantemente ya sea por variaciones geográficas (distribución de las especies), o temporales (anual y estacional) (Teixeira-Filho et al., 2003; Manjarrez, 2005). Cuando ocurren cambios en el paisaje, por acción antropogénica como la fragmentación y pérdida de coberturas vegetales, se afecta la disponibilidad, abundancia y riqueza del recurso disponible (Carvajal y Urbina-Cardona, 2008). Esta situación repercute en la respuesta y amoldamiento de las especies a las nuevas condiciones de uso de los recursos que queden disponibles.
Los reptiles pueden habitar una amplia gama de coberturas vegetales, que para el caso del Caribe Colombiano, de manera general incluyen: zonas abiertas, bordes de vegetación, matorrales, fragmentos de bosque seco tropical, entre otros, en donde se abastecen de los recursos necesarios para su óptimo desarrollo en las tres dimensiones básicas del nicho (Carvajal-Cogollo, 2014).
Para los ensamblajes de reptiles, el análisis de la dieta es uno de los factores más importantes a tener en cuenta en su organización natural (Pianka y Huey, 1978), para la mayoría de las especies de este grupo, la descripción de la dieta y las implicaciones a nivel de interacciones ecológicas han sido poco evaluadas; algunos estudios se han enfocado en análisis de diversidades y en menor medida a evaluar amplitudes y solapamientos de nicho, la mayoría de éstos, abarcando una sola dimensión (Martins, 1991; Cobb, 2004; Bell y Donnelly, 2006; Mesquita et al., 2006; Brennan, 2010; Goodyear y Pianka, 2011; Jordán y Amaya, 2011). Partiendo de estas bases teóricas y las falencias en información para la formación de bosque seco estacional, en esta investigación se puso a prueba la hipótesis que la distribución de los hábitats y del recurso alimentario disponible y utilizado por las especies del ensamblaje de reptiles, varía entre las áreas abiertas y boscosas y de acuerdo con la estacionalidad natural que presenta el bosques tropical seco estacional.
MATERIALES Y MÉTODOS
Área de estudio
La investigación se llevó a cabo en la formación vegetal de bosque seco tropical estacional, en el sector norte de la región Caribe de Colombia, en la cuenca media y baja del río Cesar, departamento del Cesar. Los principales usos del suelo en el área de estudio son la ganadería intensiva y extensiva, la agricultura, las plantaciones forestales, principalmente de teca (Tectona grandis), eucalipto (Eucalyptus pellita) y acacia (Acacia mangium) y actualmente la bonanza de los cultivos extensivos de palma de aceite (Elaeis guineensis). Todos estos cambios en el uso del suelo, han ocasionado que el paisaje esté dominados principalmente por áreas abiertas, cultivos y plantaciones forestales, zonas muy intervenidas y pocas áreas de boques (secundarios principalmente).
El régimen de distribución de las lluvias es de tipo bimodal-tetraestacional, con montos de precipitación anual que van desde los 1500 hasta los 1900 mm, la temperatura media es de 27 °C (Rangel-Ch y Carvajal-Cogollo, 2012). En la cuenca media y alta del río Cesar (localidades de Valledupar y Agustín Codazzi), los bajos montos de precipitación y la cercanía a la península de La Guajira, condicionan una vegetación de bajo porte con bosques dominados por Bulnesia arborea y Copernicia tectorum y especies de fabáceas. En la cuenca baja (localidades de Chiriguaná) la humedad y la influencia de las zonas inundables del complejo cenagoso de Zapatosa aportan las condiciones para una vegetación con estrato arbóreo desarrollado y en su mayoría anfibia, con bosques dominados por Guazuma ulmifolia, Samanea saman, Spondias mombin y Attalea butyracea (Rangel-Ch y Carvajal-Cogollo, 2012).
Diseño del muestreo
Se escogieron seis fragmentos de bosque seco tropical estacional, de tamaño variable (tres considerados pequeños entre 41-69 ha; tres grandes entre 469-901 ha). Los fragmentos pequeños se ubicaron al norte de la cuenca del rio Cesar con distancia promedio entre ellos de 600 m y los grandes ubicados en la cuenta media y baja del rio Cesar con distancia promedio entre ellos de 1200 m. En cada fragmento se identificaron dos tipos de hábitat, las zonas abiertas y boscosas. En cada hábitat se dispusieron cinco transectos lineales paralelos al borde físico de los fragmentos de bosque. Los transectos estuvieron separados uno de otro a distancias preestablecidas de 35 m.
Muestreos
Se realizaron cinco salidas de campo entre marzo de 2011 y marzo de 2012 con una duración de 12 días cada una, con las que se cubrió las dos épocas climáticas del año. Para la recolección de datos se realizó búsqueda por encuentros visuales (Crump y Scott, 1994). Los muestreos se llevaron a cabo por seis investigadores entre las 9:00 y 12:45 h y las 18:00 a 21:45 h. El esfuerzo de muestreo de 1125 horas/hombre. Algunos ejemplares de las especies registradas fueron colectados con el debido permiso de la autoridad ambiental competente (convenio N° 19-7-001-0-2010), para extraer los contenidos estomacales. Los individuos se preservaron según los protocolos y procedimientos propuestos por Pissani (1973). Los individuos fijados fueron etiquetados, almacenados en frascos y depositados en la colección de reptiles del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia.
Análisis de datos
Composición de dieta
A las especies de las cuales se contaba con más de cuatro ejemplares recolectados se les realizó una disección por el lado lateral derecho, se les extrajo el estómago y posteriormente el contenido estomacal, el cual fue fijado en alcohol al 70 % (Pisani y Villa, 1974). Los contenidos fueron separados por categorías de presa y llevados al nivel taxonómico más bajo posible con ayuda de expertos en cada grupo.
Para determinar la importancia de cada tipo de presa en la dieta de las especies, se calculó el índice de importancia relativa IRI: (F% + N% + V%)/3 (Mesquita et al., 2006); donde la frecuencia F%, es el número de apariciones de la presa por estómago; el porcentaje numérico N%, es la relación de estómagos con presa i sobre el total de estómagos; el volumen V% de cada ítem se calculó con la ecuación del elipsoide V = 4/3π (l/2)(w/2)2 donde se midió el largo (l) y ancho (w) de la presa. Se excluyeron del análisis los elementos volumétricos de presas altamente digeridas, dado que con éstas no se puede estimar correctamente el volumen de las presas ingeridas. La información de la dieta se organizó en matrices, modificadas de las expuestas por Pianka (1971) y Vitt et al. (2007), donde se especificó el nombre de la especie y los ítems presa con su respectivo porcentaje volumétrico, porcentaje numérico y el porcentaje de frecuencia.
Amplitud y sobreposición de nicho
Para calcular la amplitud de nicho trófico (B) de cada especie, se utilizó el índice de diversidad de Levins B = 1/∑pi2 donde p es la proporción de cada ítem alimentario utilizado por cada especie y n es el número de ítems alimentarios o recurso disponible. Este índice es más robusto que su versión normalizada, cuando se desconoce la abundancia de las presas en el ambiente o cuando éstas no son igualmente abundantes (Feinsinger et al., 1981). El índice se calculó en el programa Havistat (Montenegro y Acosta, 2008).
El porcentaje de sobreposición de nicho se calculó con el índice de sobreposición de Pianka Ojk = ∑(Pij.Pjk)/(√∑ Pij.Pik) donde pi es la proporción de recurso, n número de categorías y j y k las especies a comparar (Pianka, 1973), ésta es una medida cuantitativa no influenciada por el número de categorías de presas consideradas (Cortés, 1997). Los valores del índice varían de 0 cuando no hay sobreposición a 1 cuando hay sobreposición completa. Para los cálculos se utilizó el paquete estadístico Ecosim Versión 7 (Gotelli y Entsminger, 2009).
Distribución horizontal y temporal
Se realizó un análisis descriptivo del uso de zonas abiertas y boscosas durante la época seca y de lluvias; se ubicaron las especies por su versatilidad ecológica en perfiles de vegetación del bosque seco tropical estacional Bs-T. Las especies se categorizaron basados en los resultados, como raras (< 5 ind), comunes (< 20 ind) y abundantes (> 20 ind). Se realizó un análisis no paramétrico de varianza de Kruskal Wallis para evaluar si existían diferencias significativas entre las riquezas de los hábitats y otra para evaluar estas diferencias entre las abundancias de las especies entre zonas abiertas y boscosas y entre las épocas climáticas. La prueba se realizó en el paquete estadístico SPSS V20 (IBM, 2011).
RESULTADOS
Aspectos taxonómicos
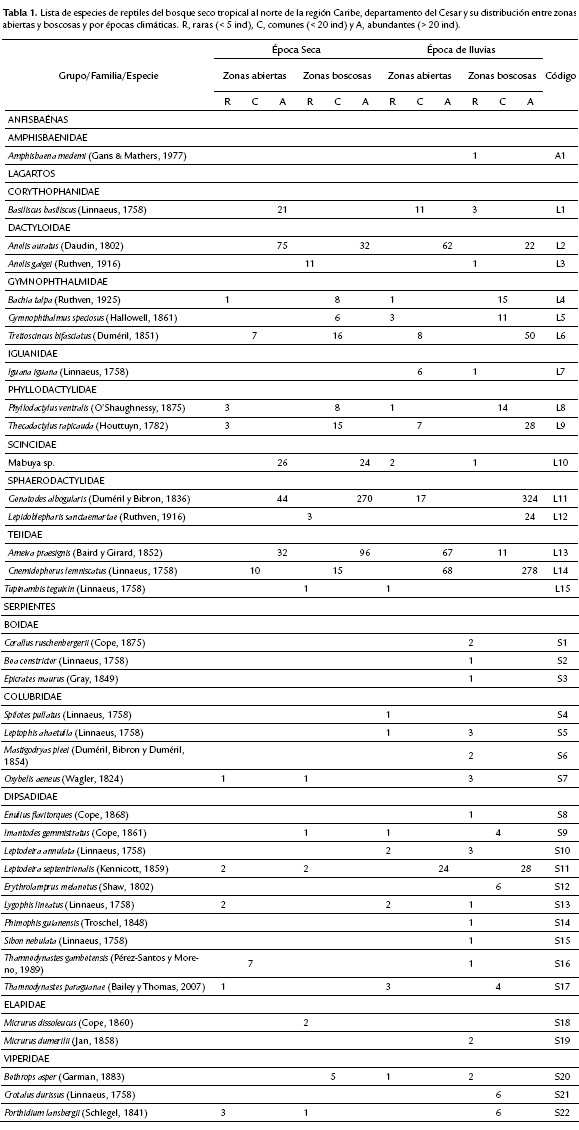
Se registraron 38 especies, distribuidas en 14 familias. Del total de taxones, 15 especies de ocho familias fueron de lagartos, 22 especies de cinco familias fueron de serpientes y una especie de anfisbaena (Tabla 1).
Composición de la dieta
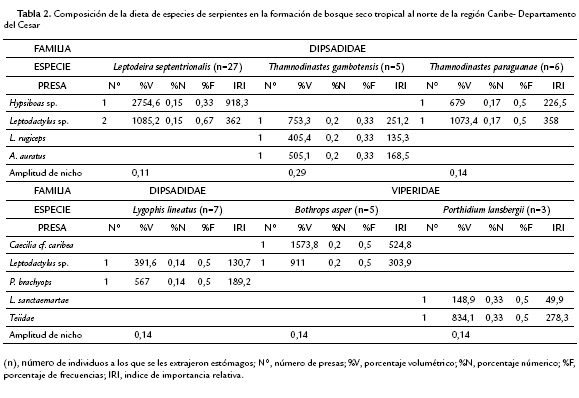
Se analizaron 109 estómagos, de seis especies serpientes (61 estómagos) y siete de lagartos (48 estómagos, Tabla 1 y 2), el 62 % de los estómagos tenían contenido, representado por 143 presas que se agruparon en 31 categorías o tipos de presa. El 38 % restante de los estómagos estaban vacíos.
Análisis de la dieta en serpientes
El 73 % de los estómagos se encontraron vacíos, de éstos el 15 % fueron de hembras grávidas. En el 27 % restante se registraron ocho tipos de presas; las categorías mejor representadas fueron las conformadas por especies de anfibios presentes en el 83 % de los estómagos, principalmente las especies halladas fueron Caecilia caribea, Pleurodema brachyops, Hypsiboas spp. y Leptodactylus spp., seguida de los lagartos, Anolis auratus, Lepidoblepharis sanctaemartae, Leposoma rugiceps y representantes de la familia Teiidae (Tabla 2). De manera particular la especie T. gambotensis consumió tanto anfibios como lagartos. El 90 % de las especies mostraron preferencia a ingerir las presas por la parte delantera o cefálica (Tabla 2).
Análisis de la dieta en lagartos
En este grupo se registraron 23 categorías de presa, los mejor representados fueron los órdenes, familias, subfamilias y géneros de artrópodos, principalmente los órdenes, Araneae, Blattodea, Coleoptera, Hemiptera, Hymenoptera, Isoptera, Ortoptera y Lepidoptera, las familias Chrysomelidae, Tenebrionidae, Formicidae (géneros Camponotus spp. y Solenopsis spp.) y las subfamilias Nassutermitinae y Termitinae, al igual que larvas de especies de los Órdenes Diptera (Calliphoridae, Culicidae, Chironomidae), Hemiptera, Hymenoptera y Lepidoptera. También se encontró material vegetal y otro material que no fue determinado. El Orden Coleoptera fue la categoría de presa más frecuente, seguida de Araneae y Lepidoptera. Se halló un porcentaje de estómagos vacíos del 42 %.
Las especies A. auratus y A. gaigei (Dactyloidae, Tabla 3) compartieron en su dieta taxones de los órdenes Hymenoptera y Araneae, de estos Hymenoptera fue la presa más importante para ambas especies. La especies Bachia talpa (Gymnophthalmidae), presentó diez categorías de presa (Tabla 3), las presas de mayor importancia fueron las larvas de Lepidoptera y de Diptera. En el lagarto Ameiva praesignis (Teiidae, Tabla 3), las presas de mayor importancia fueron los órdenes Isoptera y Ortoptera. En cuanto al número de presas, Lepidoptera fue la más abundante (40 individuos en estado larval). Dentro de los geckos de la familia Phyllodactylidae, Thecadactylus rapicauda presentó como presa más importante a ejemplares de los órdenes Ortoptera y Blattodea y Phyllodactylus ventralis a representantes de los órdenes Lepidoptera e Hymenoptera. Por último Lepidoblepharis sanctaemartae (Sphaerodactylidae) presentó como presas representativas a especies de Araneae y larva de Coleoptera. Los lagartos de las familias Phyllodactylidae y Sphaerodactylidae compartieron presas de los Órdenes Araneae y Coleoptera (Tabla 3).
Amplitud y sobreposición de nicho trófico
La amplitud de nicho trófico fue baja para todas las especies de reptiles. El valor más alto para las serpientes lo presentó T. gambotensis 0,29 y el más bajo fue para L. septentrionalis con 0,11 y para los lagartos el valor más alto fue 0,18 para B. talpa y el más bajo 0,07 para A. auratus.
La sobreposición de nicho en el ensamblaje, varió de 0.07 a 0.93. Se presentaron valores altos entre las serpientes; L. septentrionalis y T. paraguanae, con un valor de 0.93, seguido de T. gambotensis y T. paraguanae con 0.64. Para los lagartos el valor más alto se presentó entre las especies A. auratus y A. gaigei, con 0.83.
Distribución de los hábitats
En general se presentó una distribución homogénea del ensamblaje, desde las áreas abiertas hasta las boscosas y entre las épocas climáticas. En el bosque se registraron 37 especies de reptiles, de las cuales 19 fueron en la época seca y 35 en la época de lluvias. Mientras que en las áreas abiertas se registraron 23 especies de reptiles, 16 especies en época seca y 21 en época de lluvias (Fig. 1, Tabla 1).
De los lagartos, 11 especies se encontraron tanto en bosque como en las áreas abiertas en ambas épocas climáticas. La especie Iguana iguana se encontró en ambas zonas pero solo en época de lluvias, Tupinambis teguixin se observó en época seca en el bosque y en época de lluvias en las zonas abiertas y Lepidoblepharis sanctamartae y Anolis gaigei se encontraron restringidos al bosque en ambas épocas climáticas (Fig. 1, Tabla 1). De las serpientes, siete especies se hallaron tanto en las zonas abiertas como en las boscosas y en ambas épocas climáticas y nueve se registraron en las zonas boscosas solo en época de lluvias (Fig. 1, Tabla 1). La especie Leptodeira septentrionalis se encontró en las dos zonas y en ambas épocas climáticas, Leptophis ahaetulla y Leptodeira annulata se observaron en ambas zonas, en la época de lluvias, Micrurus dissoleucus se observó en zonas boscosas en época seca, mientras que Spilotes pullatus y Thamnodinastes paraguanae se registraron en las zonas abiertas en la época de lluvias (Fig. 1, Tabla 1).
DISCUSIÓN
Aspectos taxonómicos
La riqueza taxonómica encontrada representa el 21 % de las especies del Orden Squamata registradas en la región Caribe Colombiana, en sus diferentes formaciones vegetales desde bosque húmedo a áreas xerofíticas (Carvajal-Cogollo et al., 2012). En general la composición de reptiles es similar a otros estudios de bosque seco llevados a cabo en la llanura Caribe, por ejemplo Carvajal-Cogollo y Urbina-Cardona (2008) encontraron 35 especies, 20 de lagartos, 14 de serpientes y una Amphisbaena en el departamento de Córdoba. Medina-Rangel (2011), registró 40 especies en el complejo cenagoso de Zapatosa en el departamento de Cesar, 20 fueron de lagartos y 20 de serpientes. En estos trabajos se comparten las especies más comunes y ampliamente distribuidas como los lagartos A. gaigei (antes A. tropidogaster), A. auratus, B. basiliscus, A. ameiva (ahora A. praesignis), T. teguixin y C. lemniscatus, así como las serpientes B. constrictor, C. ruschembergerii, E. maurus, L. annulata y L. septentrionalis entre otras.
Composición de la dieta
En general los lagartos tienden a ser generalistas al incluir en sus dietas gran cantidad de artrópodos. Los artrópodos más frecuentes en la dieta fueron representantes de Aranea, Coleoptera, Hymenoptera y Lepidoptera, que son los grupos más abundantes y diversos a nivel del Neotrópico (Fernández y Sharkey, 2006).
La dieta de las serpientes incluyó varias especies de ranas. Los anuros son presas comunes en la dieta de serpientes el Bs-T del Caribe Colombiano (Pérez-Santos y Moreno, 1986), posiblemente por su abundancia y por la capacidad de ocupar diferentes hábitats (Cuentas et al., 2002). Para la planicie de la cuenca del río Cesar, Romero y Lynch (2012) registraron 38 especies de anfibios, de las cuales siete especies estuvieron incluidas en la dieta de las serpientes y corresponden a especies que se pueden distribuir tanto en zonas abiertas y boscosas de la planicie de la región Caribe (Romero y Lynch, 2012).
Los lagartos fueron un grupo poco representado en la dieta de las serpientes, sin embargo puede que estén presentes en la dieta de otras especies (Pérez-Santos y Moreno, 1986), por ejemplo B. asper, de la cual se ha registrado que pueden consumir tanto anfibios como reptiles al igual que la otra especie de viperido P. lansbergii. (Campbell y Lamar, 2004).
El porcentaje de estómagos vacíos, quizás se deba a factores como la variación estacional del recurso, la actividad reproductiva de cada especie, la defensa territorial, el cuidado parental y las condiciones climáticas como precipitación, temperatura, las cuales varían a lo largo del día (Whitfield y Donnelly, 2006), tal como se evidenció con la presencia de algunas hembras grávidas sin contenido estomacal. La suma de estos factores juega un papel importante en la reducción del tiempo que las especies ocupan para las actividades de forrajeo.
Distribución de los hábitats
En la distribución de los hábitats se observó un aumento de la riqueza de las especies entre las épocas climáticas (Tabla 1), que está influenciada por la estacionalidad del Bs-T, dado que con la época de lluvias el número y altura de las herbáceas tanto en el pastizal como en el bosque se incrementa lo que puede favorecer las condiciones para que se establezca un flujo de especies entre estos dos hábitats; además este fenómeno en las herbáceas permite que aumentan los recursos incluyendo las presas, las condiciones de sombra, la humedad entre otros.
La mayoría de las especies de lagartos no estuvieron restringidas espacialmente a una sola zona, lo que sugiere que la repartición de los recursos disponibles puede ser uniforme entre las zonas de pastizales y bosques, y la utilización de los recursos no implica competencia (Carvajal-Cogollo et al., 2008). Cabe aclarar que los resultados de riqueza de las áreas abiertas, se deban quizá a la ubicación espacial con respecto a los bosques y al diseño que estableció una zona de contacto entre ambas (Carvajal-Cogollo, 2014). Por otro lado la presencia de las especies L. sanctamartae y A. gaigei únicamente en las zonas boscosas, sugieren que las condiciones adecuadas para su establecimiento solo se presentan en los remanentes de bosque; sin embargo sería necesario investigar si en la época de lluvias y con el crecimiento de herbáceas estas especies exploran las áreas abiertas.
La mayoría de las serpientes se encontraron restringidas algún tipo de cobertura (boscosa o abierta), sin embargo estos resultados no son contundentes, ya que este grupo se caracteriza por ser críptico, lo que implica una baja detección, por lo cual no se puede aseverar la preferencia estricta por algún tipo de cobertura (Pough et al., 2001).
Relación de la dieta con la distribución horizontal y temporal
En el Bs-T del Caribe Colombiano, los lagartos y serpientes presentan características generalistas en el uso de los recursos (ej. hábitats, microhábitats, alimentario) (Carvajal-Cogollo et al., 2012), hecho que puede explicar el consumo una gran variedad de presas (ej. el observado en las serpientes como consumidoras de múltiples especies de anfibios). Estas presas se caracterizan por distribuirse vertical y horizontalmente en muchos hábitats, por lo cual la ubicación espacial de las especies de serpientes y lagartos podría estar dada por la presencia del recurso alimentario.
Las especies Anolis auratus y A. gaigei usan de forma similar el recurso alimentario, sin embargo las especie A. auratus presenta mayores abundancias con relación a las de A. gaigei, este hecho podría mostrar las dinámicas poblacionales entre ambas especies estructuradas por el uso de recursos. Durante la época seca, el hábitat de ambas especies se sobrelapan en las áreas boscosas, pero no se tienen evidencias de cómo interactúan y/o evitan la competencia ambas especies en los bosques, lo cual constituye un tópico importante para investigar, ya que en otras formaciones vegetales como el bosque húmedo tropical, se presenta una división clara de los hábitat, donde A. auratus se restringe a las zonas abiertas y A. gaigei en zonas boscosas, en los bordes de los bosques y rara vez en su interior (Carvajal et al., 2007).
La especie B. talpa parece ser generalista y oportunista en su dieta dada la cantidad de presas encontradas en sus estómagos, la alta amplitud de nicho, la presencia de presas como larvas de dípteros Calliphoridae asociados a cuerpos en descomposición, así como la presencia de presas subterráneas como las termitas (Isoptera) de las subfamilias Termitinae y Nassutermitinae. Además puede existir un cambio estacional de la dieta teniendo en cuenta la presencia de las larvas acuáticas de los dípteros de las familias Culicidae y Chironomidae las cuales se desarrollan en cuerpos de agua como charcos temporales (Wade et al., 2004). Sin embargo se sugiere un estudio de dieta de la especie que tenga en cuenta de una forma más detallada la estacionalidad del bosque. La preferencia de presas pequeñas, suaves y de movimientos lentos en la dieta de B. talpa podría deberse a su fácil captura y digestión; como se ha demostrado en otras especies de Gymnophthalmidos y amphisbaenas esto puede obedecer a un rasgo histórico que parece haber favorecido la evolución del grupo de excavadores (Barros et al., 2011).
El género Bachia está representado por lagartos altamente especializados en hábitos fosoriales (Colli et al., 1998; Rodrigues et al., 2007; Rodrigues et al., 2008) por lo que B. talpa puede explotar estas características al aprovechar el recurso disponible tanto de hábitos terrestres como subterráneos, reduciendo así la competencia con otras especies de hábitos similares de la misma familia como G. speciosus y T. bifasciatus y otros como L. sanctamartae y la culebra ciega Amphisbaena medemi una especie fosorial, todos estos presentes en el ensamblaje del Bs-T.
La especie Ameiva praesignis presentó como principal recurso a los artrópodos, su modo de forrajeo activo y su capacidad para estar tanto en las zonas boscosas como abiertas, le facilitan tener una amplia gama de recurso alimentario (Silva et al., 2003). La especie aprovecha tanto presas blandas como larvas de insectos, isópteros, arañas entre otros, así como presas duras como coleópteros y hormigas, lo que sugiere que el tipo de presas no determina la composición de la misma. Durante el trabajo de campo se observó escarbando en estiércol bovino, presumiblemente en búsqueda de escarabajos coprófagos de la familia Scarabidae o de sus larvas. El amplio espectro dietario para el género Ameiva viene de un linaje que se adecúa al recurso disponible, al usar a los artrópodos aprovechando su gran número y variedad, además también consumen pequeños vertebrados y poco material vegetal; lo que se evidencia en especies como A. ameiva, A. edracantha, A. septemlineata y otros Teiidae (Martins, 1991; Pough et al., 2001; Silva et al., 2003; Brennan, 2010; Jordán y Amaya, 2011).
Las dos especies de lagartos nocturnos P. ventralis y T. rapicauda, se encontraron compartiendo la misma ubicación espacial y la dieta de ambas especies se caracterizan por el consumo principalmente de artrópodos, especialmente coleópteros y arañas, así como lo documenta Ávila-Pires (1995), en otras especies de lagartos nocturnos del mismo linaje, sin embargo difieren en el tamaño del cuerpo, lo que hace una diferencia en el tamaño de las presas consumidas. Además presentan valores de amplitud de nicho trófico cercanos, aunque el valor de sobreposición es muy bajo. Quizá la cercanía filogenética entre estas especies, hace que el nicho trófico y temporal sea semejante, sin que exista competencia excluyente como sucede en otras especies de lagartos nocturnos del género Hemidactylus, que pueden desplazar poblaciones de T. rapicauda (Howard et al., 2001).
Las serpientes L. septentrionalis y T. paraguanae con actividad en horas nocturnas se observaron usando el recurso trófico de forma similar; los valores de sobreposición de nicho se pueden explicar en la manera como estas dos especies se reparten espacialmente en el hábitat, por un lado L. septentrionalis se observó principalmente forrajeando en el suelo, entre hierbas y hojarasca del bosque y de las zonas abiertas y por otro lado T. paraguanae se observó exclusivamente en zonas abiertas o en los bordes físicos de los bosques. Se sugiere realizar más estudios de dietas para estas especies para tener más certeza.
Según nuestras observaciones en campo sobre la distribución espacial de las especies Crotalus durissus y Bothrops asper, en las cuales la primera estaba restringida a las áreas secas en cercanías a los fragmentos evaluados y la segunda en las zonas inundables de dichos fragmentos, esto sugiere que las especies parecen preferir diferentes ambientes y evitar así el uso de recursos similares. Se sugiere realizar estudios detallados que abarquen preguntas sobre los usos y distribución de los recursos en las dos poblaciones para describir mejor sus preferencias y como evitan competir entre ellas.
CONCLUSIONES
En síntesis el bosque seco tropical estacional por su dinámica entre las épocas climáticas y su heterogeneidad de ambientes y de hábitats, hace que los recursos espaciales y tróficos varíen a lo largo del año, lo que causa efectos sobre las abundancias de estos tanto horizontal como verticalmente (Janzen, 1988), situación que moldea la estructura de los ensamblajes de reptiles, posiblemente su supervivencia y propicia el flujo de las especies entre las zonas abiertas y de bosques, así como entre los microhábitats. Se presentaron diferencias entre la dieta, el espacio y el tiempo de actividad de las especies, lo que podría indicar segregación de los diferentes nichos de estas dentro de la dinámica del bosque seco tropical. Sin embargo, es fundamental investigar la posible competencia por recursos de las poblaciones de aquellas especies similares. Por otro lado también sería importante abordar investigaciones enfocadas a determinar el efecto que los factores limitantes que se hacen evidentes durante la época seca (ej. disponibilidad de agua, hábitats, alimento, temperaturas, entre otras), tienen sobre los ensamblajes de reptiles.
AGRADECIMIENTOS
CORPOCESAR y la Universidad Nacional de Colombia financiaron el proyecto de investigación. J. Orlando Rangel facilitó la logística entre las entidades financiadoras y en la fase campo. Vladimir Bernal, Azarys Paternina, Rocio López, Johann Cárdenas, Nadia Torres, Alexander Mendoza y Alexander Trujillo, colaboraron en la fase muestreos; Irina Morales identificó los contenidos estomacales. Martha Calderón colaboró con el acceso a la colección de reptiles del ICN. Olga Castaño, Gladys Cárdenas, Guido Medina, Rafael Moreno colaboraron en la identificación de los ejemplares recolectados. Los especímenes fueron recolectados con la aprobación de la autoridad ambiental competente CORPOCESAR mediante convenio N° 19-7-001-0-2010.
REFERENCIAS
Ávila-Pires TCS. Lizards of Brazilian Amazonia (Reptilia: Squamata). Zoologische Verhandelingen. 1995;599:1-706. [ Links ]
Ayala S, Castro F. Lagartos de Colombia/ Lizards of Colombia. In press. 520 p. [ Links ]
Barros F, Herrel A, Tkohlsdorf T. Head shape evolution in Gymnophthalmidae: does habitat use constrain the evolution of cranial design in fossorial lizards?. J Evol Biol. 2011; 24(11):2423-2433. Doi:10.1111/j.1420-9101.2011.02372.x. [ Links ]
Bell K, Donnelly Ma. Influence of Forest Fragmentation on Community Structure of Frogs and Lizards in Northeastern Costa Rica. Conserv Biol. 2006; 20(6):1750-1760. Doi:10.1111/j.1523-1739.2006.00522.x. [ Links ]
Berazategui M. Evaluación de las teorías neutral y de Nichos en Comunidades Temporales (Tesis de Doctorado). Uruguay: Universidad de la República, Facultad de ciencia- PEDECIBA; 2012. p. 60. [ Links ]
Brennan R. Un Estudio Ecológico de las Lagartijas del Valle Seco de Buenavista y de los Valles Húmedos de La Josefina y Salango. ISP Collection. 2010. p 828. [ Links ]
Campbell J, W Lamar. The venomous reptiles of western hemisphere I. Londres: Cornell University Press; 2004. p 870. [ Links ]
Carvajal-Cogollo JE, Castaño-Mora OV, Cárdenas-Arévalo G, Urbina-Cardona JN. Reptiles de Áreas Asociadas a Humedales de la Planicie del Departamento de Córdoba, Colombia. Caldasia. 2007;29(2):427-438. [ Links ]
Carvajal-Cogollo JE, Urbina-Cardona JN. Patrones de Diversidad y Composición de Reptiles en Fragmentos de Bosque Seco Tropical en Córdoba, Colombia. Trop Conserv Sci. 2008;1(4):397-416. [ Links ]
Carvajal-Cogollo JE, Cárdenas-Arévalo G, Castaño Mora O. Reptiles de la región Caribe de Colombia. In: Rangel Ch JO, editor. Colombia Diversidad Biótica XII: La Región Caribe de Colombia, Universidad Nacional de Colombia-Corpocesar. Bogotá:Arfo Editores; 2012. p. 91-812. [ Links ]
Carvajal-Cogollo JE. Evaluación A Múltiples Escalas de los Efectos de la Transformación del Paisaje Sobre los Ensamblajes de Reptiles en Localidades de la Región Caribe Colombiana (Tesis doctorado). Bogotá: Departamento de Biología, Facultad de Ciencias, Universidad Nacional de Colombia. 2014. p. 136. [ Links ]
Chase JM, MA Leibold. Ecological Niches: Linking Classical and Contemporary Approache. Chicago: University of Chicago Press; 2003. p. 221. [ Links ]
Cobb V. Diet and prey size of the flathead snake, Tantilla gracilis. Copeia. 2004;2: 397-402. Doi: http://dx.doi.org/10.1643/CH-03-174R. [ Links ]
Colli G, Zatz M, Cunha H. Notes on the Ecology and Geographical Distribution of the Rare Gymnophthalmid lizard Bachia bresslaui. Herpetologica. 1998;54(2):169-174. [ Links ]
Cortés E. 1997. A Critical review of Methods of Studying Fish Feeding Based on Analysis of Stomach Contents: Application to Elasmobranch Fishes. Can J Fish Aquat Sci. 1997;54:726-738. [ Links ]
Crump ML, Scott NY. Relevantamientos por Encuentros Visuales. In: Heyer W, Donnelley MA, Mcdiarmid RA, Hayek LC, Cfoster M, editors. Medición y Monitoreo de la Diversidad Biológica: Métodos Estandarizados para Anfibios. USA: Smithsonian Institution; 2004. p 84-92. [ Links ]
Cuentas M, Borja A, Lynch J, Renjifo J. Anuros del departamento del Atlántico y Norte de Bolívar. Barranquilla: Cencys 21; 2002. p. 117. [ Links ]
De Queiroz A, De Queiroz K. Handling Behavior of Eumeces gilberti with Comments on Headfirst Ingestion in Squamates. J Herpetol. 1987;21(1):57-63. Doi:10.2307/1564377. [ Links ]
Duellman W. The South American Herpetofauna: its Origin, Evolution and Dispersal. Kansas: Museum of Natural History the University Kansas; 1979. p. 470. [ Links ]
Feinsinger P, Spears E, Poole RW. A simple measure of niche breadth. Ecology. 1981;62(1):27-32. Doi:10.2307/1936664. [ Links ]
Fernández F, Sharkey M. Introducción a los Hymenoptera de la Región Neotropical. Bogotá: Sociedad Colombiana de Entomología-Universidad Nacional de Colombia;2006. p. 893. [ Links ]
Glaudas X, Jezkovat, Rodríguez-Robles J. Feeding ecology on the Great Basin Rattlesnake (Crotalus lutosus, Viperidae). Can J Zool. 2008;86(7):723-7234. [ Links ]
Goodyear SE, Pianka ER. Spatial and Temporal Variation in Diets of Sympatric Lizards (genus Ctenotus) in the Great Victoria Desert, Western Australia. J Herpetol. 2011;45(3):265-271. Doi:10.1670/10-190.1. [ Links ]
Gotelli NJ, Entsminger GL. EcoSim: Null Models Software for Ecology. Version 7. Acquired Intelligence Inc. & Kesey-Bear. Jericho, VT 05465. 2009. Available at: http://garyentsminger.com/ecosim.htm. [ Links ]
Hammer Ø, Harper DA.T., Ryan PD. Past: Paleontological Statistics Software Package for Education and Data Analysis. Palaeontologia Electronica. 2001;4(1):9. [ Links ]
Howard K, Parmerlee J, Powell R. Natural History of the Geckos Hemidactylus mabouia, Thecadactylus rapicauda, and Sphaerodactylus sputatoron Anguilla. Caribbean J Sci. 2001;37(3):285-288. [ Links ]
Hubbell S P. The unified neutral theory of biodiversity and Biogeography. New Jersey, USA: Princeton University Press; 2001. 392 p. [ Links ]
IBM Corp. Released 2011. IBM SPSS Statistics for Windows, Version 20.0. Armonk, NY: IBM Corp. 2011. [ Links ]
Janzen D H. Management of habitat fragments in a tropical dry forest growth. Ann Missouri Bot Gard. 1988;75(1):105-116. [ Links ]
Jordán J, Amaya D. Note on the Diet of Ameiva edracantha (Squamata, Teiidae) in Cerros de Amotape National Park, Tumbes, Perú. Rev Peru Biol. 2011;18(2):253-255. [ Links ]
Krausman PR. Some Basic Principles of Habitat Use. Idaho: Grazing Behavior of Livestock and Wildlife; 1999. p. 70. [ Links ]
Losos J. Lizards in an evolutionary tree. Ecology and Adaptive Radiation of Anoles. University of California Press; 2009. 528 p. [ Links ]
Macarthur R H, Levins R. The limiting similarity convergence and divergence of convergence and divergence of coexisting species. Amer Nat. 1967;101:377-385. [ Links ]
Manjarrez J. Posible invasión de un nicho alimentario nuevo y microevolución en una especie mexicana de serpientes. Ciencia Ergo Sum. 2005;12(3):275-281. [ Links ]
Martins M. The Lizards of Balbina, Central Amazonia, Brazil: a qualitative analysis of resource utilization. Stud Neotrop Fauna E. 1991;26(3):179-190. [ Links ]
Medina-Rangel G. Diversidad alfa y beta de la comunidad de reptiles en el Complejo Cenagoso de Zapatosa, Colombia. Rev Biol Trop. 2011;59(2):935-968. [ Links ]
Mehta R. Prey-handling Behavior of Hatchling Elaphehelena (Colubridae). Herpetologica, 2003;59(4):469-474. [ Links ]
Mehta R. Early experience shapes the development of behavioral repertoires of hatchling snakes. J Ethol. 2008;27(1):143-151. Doi: 10.1007/s10164-008-0097-9. [ Links ]
Mesquita O, Corréa G, Colli G. Ecology of an Amazonian savanna lizard assemblage in Monte Alegre, Pará State, Brazil. South Am J Herpetol. 2006;1(1):61-71. [ Links ]
Mesquita D, Colli G, Franc F, Vitt L. Ecology of a Cerrado Lizard assemblage in the Jalapao Region of Brazil. Copeia. 2006;3:460-471. Doi: 10.1643/0045-8511(2006)2006%5B460:EOACLA%5D2.0.CO;2. [ Links ]
Montenegro J, Acosta A. Programa para inferir uso, preferencia de hábitat y amplitud de nicho. Unesis, Departamento de Biología, Pontificia Universidad Javeriana. 2008. Havi Stat© v 1.0. [ Links ]
Pérez-Santos C, Moreno A. Ofidios de Colombia. Monografía: Torino. 1988; 517 p. [ Links ]
Pianka ER. Sympatry of desert lizards (Ctenotus) in Western Australia. Ecology. 1969;50:1012-1030. Doi: 10.2307/1936893. [ Links ]
Pianka ER. Comparative ecology of two Lizards. Copeia. 1971;1:129-138. Doi: 10.2307/1441606. [ Links ]
Pianka ER. The Structure of Lizard Communities. Annu Rev Ecol Syst. 1973;4:53-74. Doi:10.1146/annurev.es.04.110173.000413. [ Links ]
Pianka ER. Ecological Phenomena in Evolutionary Perspective. In: Polunin N, editor. Ecosystem Theory and Application. Wiley and Sons; 1986. p. 325-336. [ Links ]
Pianka ER. The Many Dimensions of a Lizard's Ecological Niche. In: Valakos ED, Bohme W, Perez-Mellado V, Maragou P, editors. Lacertids of the Mediterranean Basin. University of Athens, Greece: Hellenic Zoological Society; 1993. p. 121-154. [ Links ]
Pianka ER, Huey RB. Comparative ecology, niche segregation, and resource utilization among gekkonid lizards in the Southern Kalahari. Copeia. 1978;4:691- 701. Doi:10.2307/1443698. [ Links ]
Pissani GR. A Guide to Preservation Techniques and Amphibians and Reptiles. Kansas: Published by the Society for the Study of Amphibians and Reptiles; 1973. p.1-22. [ Links ]
Pough FH, Andrews R, Clade J, Crump M, Savitzky A, Wells K. Herpetology. Prentice Hall. Second Edition. New York: Prentice Hall; 2001. 612 p. [ Links ]
Rangel-Ch JO, Carvajal-Cogollo JE. Clima de la Serranía del Perijá. In: Rangel-Ch JO, editor. Diversidad Biótica VIII. Media y baja montaña de la serranía de Perijá. Colombia Bogotá D.C: Universidad Nacional de Colombia-Instituto de Ciencias Naturales-Corpocesar; 2009. p. 3-49. [ Links ]
Ricklefs RE, Schluter D. Species Diversity: Regional and Historical Influences. In: Ricklefs RE, Schluter D, editors. Species Diversity in Ecological Communities: Historical and Geographical Perspectives. Chicago: University of Chicago Press; 1993. p. 350-263. [ Links ]
Rodríguez-Robles J, Leal M. Effects of prey type on the feeding behavior of Alsophis portoricensis (Serpentes: Colubridae). J Herpetol. 1993;27(2):163-168. Doi:10.2307/1564932. [ Links ]
Rodrigues MT, Pavan D, Curcio FF. Two new species of lizards of the genus Bachia (Squamata, Gymnophthalmidae) from Central Brazil. J Herpetol. 2007;41(4):545-553. Doi: 10.1670/06-103.1. [ Links ]
Rodrigues M, Camacho A, Sales P, Sousa R, Teixeira M, Valdujo P, Ghellere J, Mott T, Nogueira C. A New Species of the Lizard Genus Bachia (Squamata: Gymnophthalmidae) from the Cerrados of Central Brazil. Zootaxa. 2008;1875:39-50. [ Links ]
Romero-Martínez HJ, Lynch JD. Anfibios de la Región Caribe. In: Rangel-Ch. J.O. Colombia Diversidad Biótica XII. La Región Caribe de Colombia. Bogotá D.C.: Universidad Nacional de Colombia-Instituto de Ciencias Naturales; 2012. p. 677-701. [ Links ]
Schmidt De Aguiar L, Di-Bernardo M. Diet and feeding behavior of Helicops infrataeniatus (Serpentes: Colubridae: Xenodontinae) in Southern Brazil. Stud Neotrop Fauna E. 2004;39(1):7-14. [ Links ]
Silva B, Andrade B, Teixeira R, Giovanell M. Ecología de Ameiva ameiva (Sauria, Teiidae) na Restinga de Guriri, Sao Mateus, Espírito Santo, sudeste do Brasil. Bol Mus Biol Mello Leitão, 2003;15:5-15. [ Links ]
Teixeira-Filho, Rocha P, Ribas S. Relative feeding specialization may depress ontogenetic, seasonal, and sexual variations in diet: the endemic lizard Cnemidophorus littoralis (Teiidae). Braz J Biol. 2003;63(2):321-328. [ Links ]
Toft C. Resource partitioning in amphibians and reptiles. Copeia, 1985(1):1-21. [ Links ]
Toledo LF, Ribeiro RS, Haddad CFB. Anurans as prey: an exploratory analysis and size relationships between predators and their prey. J Zool. 2007;271:170-177. Doi:10.1111/j.1469-7998.2006.00195.x. [ Links ]
Vitt LJ, Avila-Pires TCS, Zani PA, Espósito MC. Life in Shade: The Ecology of Anolis trachyderma (Squamata: Polychrotidae) in Amazonian Ecuador and Brazil, with comparisons to ecologically similar anoles. Copeia. 2002;2:275-286. [ Links ]
Vitt LJ, Pianka E R, Cooper W, Schwenk K. History and the global ecology of Squamate reptiles. Amer Nat. 2003;162(1):44-60. [ Links ]
Vitt L J, Pianka ER. Deep history impacts present day ecology and biodiversity. Proc Natl Acad Sci USA. 2005;102(22):7877-7881. Doi:10.1073/pnas.0501104102. [ Links ]
Vitt LJ, Ávila-Pires TCS, Espósito MC, Sartorius SS, Zani PA. Ecology of Alopoglossus angulatusand and A. atrventris (Squamata, Gymnophthalmidae) in western Amazonia. Phyllomedusa. 2007;6(1):11-21.Doi: 10.11606/issn.2316-9079.v6i1p11-21. [ Links ]
Wade S, Corbin T, Mcdowell L-M. A guide to the Aquatic Invertebrates of South Australian Inland Waters. Environment Protect Authority; 2004. 186 p. [ Links ]
Whitfield SM, Donnelly MA. Ontogenetic and seasonal variation in the diets of a Costa Rican leaf-litter herpetofauna. J Trop Ecol. 2006;22(4): 409-417. Doi: 10.1017/S0266467406003245. [ Links ]
Winemiller K, Pianka ER. Organization in natural assemblages of desert lizards and tropical fishes. Ecol Monogr. 1990;60(1):27-55. Doi:10.2307/1943025. [ Links ]