INTRODUCCIÓN
El cáncer y sus condiciones asociadas impactan la salud pública mundial: causan muertes prematuras, incrementan el gasto por alto costo de las terapias y requieren tratamientos prolongados que aminoran la calidad de vida del paciente y sus familias (Miller et al., 2016)". Hoy día no hay cura para la mayoría de cánceres a pesar de intensa investigación en fármacos sintéticos de acción selectiva (Dunn y Kramer, 2016). El uso de medicamentos herbales sigue siendo alternativa para aliviar síntomas del cáncer, pueden actuar como coadyuvantes en tratamientos de quimioterapia y radioterapia (Harvey et al., 2015; Zheng et al., 2016; Shareef et al., 2016).
Los aceites esenciales (AEs) son líquidos hidrofóbicos de compuestos aromáticos que están presentes en varias partes de la planta, un sinnúmero de ellos se usan como saborizantes o potenciadores de aromas en cosméticos, perfumes y jabones (Pandey et al., 2017). Resultados de estudios indican que los AEs y componentes aislados poseen actividad in vitro anticancerígena y en ratones de laboratorio pueden reducir el tamaño de tumores inducidos (Bhalla et al., 2013; Lesgards et al., 2014; Sobral et al., 2014; Manion y Widder, 2017). Existe suficiente evidencia para concluir que los AEs pueden servir como puntos de partida para desarrollo de medicamentos herbales y descubrimiento de nuevos fármacos.
En Colombia, el número de plantas medicinales depositadas en colecciones botánicas es cerca de 2800 (Bernal et al., 2011; Gómez et al., 2016). Solo 144 especies tienen uso médico autorizado por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos, aunque ninguna como coadyuvante en tratamiento del cáncer (INVIMA, 2017). Este escaso aprovechamiento de las plantas se debe en buena parte a carencia de suficiente evidencia científica sobre sus propiedades anticancerígenas. Algunos trabajos se han realizado. De Croton lechleri Müll. Arg, conocida como sangre de drago, está documentado el uso popular para aliviar síntomas del cáncer y estudios in vitro e in vivo indican que el extracto posee potencial farmacológico para tratar cáncer de colon (Gupta, 2008; Bernal et al., 2011). Del AE de Ocotea caparrapi (Sandino Groot ex Nates) Dugand, palo de Caparrí, se registra su potencial como coadyuvante del tratamiento convencional de tumores cutáneos (Palomino et al. 1996; Bernal et al., 2011). Los extractos de Vismia baccifera Reichart, Passiflora edulis Sims y especies del género Piper presentaron actividad antiproliferativa en células de cáncer hepático (Osma et al., 2013; Lizcano et al., 2015).
La investigación en medicamentos herbales y fármacos de base natural para tratamiento del cáncer comienza con la selección de la planta apropiada. Esto ahorra tiempo y dinero y la probabilidad de encontrar un producto activo es mayor (Mazzio y Soliman, 2009; Harvey et al., 2015). El objetivo de este trabajo fue evaluar la actividad antiproliferativa de AEs de 11 especies cultivadas en Colombia en células de tres cánceres humanos. Se analizaron 15 muestras siguiendo un protocolo guiado para identificar los AEs más apropiados para investigación y desarrollo de medicamentos.
MATERIALES Y MÉTODOS
Plantas
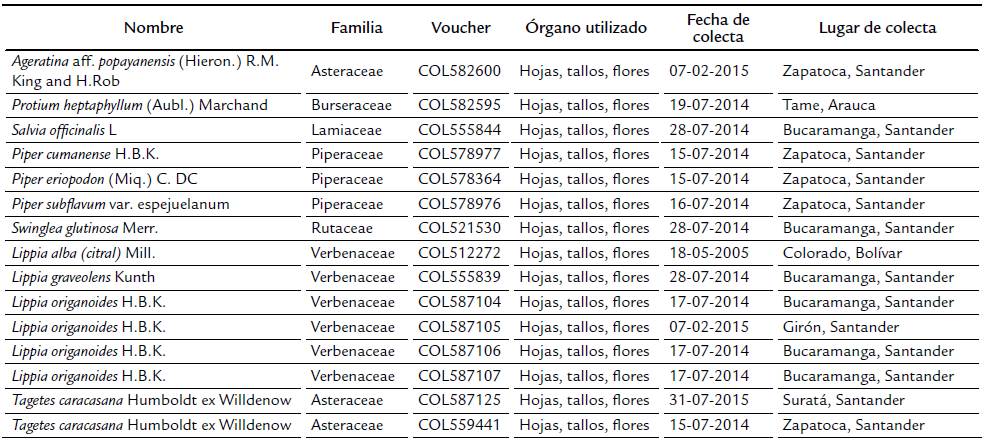
Se incluyeron 15 ejemplares de 11 especies. Las plantas se colectaron en áreas rurales y semiurbanas de los departamentos de Santander, Arauca y Bolívar. El Prof. Dr. José Luis Fernández, Universidad Nacional (Bogotá) y Real Jardín Botánico de Madrid (España), realizó la identificación taxonómica. Una muestra del espécimen se depositó en el Herbario Nacional Colombiano con el respectivo código de identificación como se presenta en la Tabla 1.
Aceites esenciales (AEs)
Las muestras se obtuvieron por hidrodestilación asistida por radiación de microondas, en un equipo de destilación tipo Clevenger adaptado a un sistema de calentamiento (Stashenko et al., 2013). Brevemente, el material vegetal (210 g), sumergido en agua (300 mL), se colocó en un balón conectado al equipo con un reservorio de destilación Dean-Stark y la mezcla se calentó 15 min x 3 veces en el microondas. El AE se secó usando sulfato de sodio anhidro y se almacenó en un frasco ámbar a 4 °C. Cada extracción se llevó a cabo por triplicado. De cada muestra se hizo una preparación concentrada (100 mg/mL) en dimetilsulfóxido y alícuotas se almacenaron a -20 °C. Para cada experimento se usó una alícuota de la misma preparación diluida en medio de cultivo.
Análisis químico de aceites esenciales
Las muestras que presentaron actividad antiproliferativa se analizaron por cromatografía de gases/ espectrometría de masas como se ha descrito (Stashenko et al., 2013). Se usó un equipo Agilent Technologies 6890N Series Network System (Palo Alto, California, EE.UU) acoplado a un detector selectivo de masas Agilent Technologies MSD 5975 Inert XL. Se utilizaron dos columnas capilares de 60 m x 0,25 mm (d.i.) x 0,25 μιτι (df): DB-5MS con fase estacionaria apolar de 5 % fenil-poli (dimetilsiloxano) y DB-WAX, con fase estacionaria polar de poli (etilenglicol). Helio (1 ml/min) se usó como gas de arrastre. La temperatura del horno se programó de 45 °C (5 min) hasta 150 °C (3 min) a 3 °C/ min; luego, hasta 220 °C (5 min) a 4°C/min. La temperatura del inyector se mantuvo a 250 °C; se usó la relación split 1:30. Los índices de retención lineales (IRL) se calcularon con base en la serie homóloga de n-alcanos C9-C25 (Sigma-Aldrich, Milwaukee, Wisconsin, EE.UU.). Los componentes se identificaron comparando sus espectros de masas e IRL con espectros de bases de datos (NIST14 y Wiley) y reportados por otros (Davies, 1990; Babushok et al., 2011). Se emplearon además compuestos de referencia (Sigma-Aldrich).
Células
La actividad antiproliferativa de los AEs se evaluó en líneas celulares de cáncer de mama (MCF-7, ATCC ® HTB-22™), cáncer cervical (HeLa, ATCC ® CCL-2™) y cáncer de hígado (HepG-2, ATCC® CRL-11997™). Para evaluar si los AEs presentaban más acción selectiva por las células cancerosas que otras, se incluyeron líneas celulares de riñón humano embrionario (HEK293-ATCC ® CRL-1573™), riñón de mono (Vero, ATCC ® CCL-81™) y piel de ratón (B16F10, ATCC ® CRL-6475™). Cada línea celular se cultivó en cajas de 25 cm2 en el medio de cultivo recomendado (MEM, DMEM-F12 o RPMI-1640, Gibco Co.) suplementado (810 %) con suero bovino fetal (Gibco Co.). Las cajas se incubaron por 3-4 días a 37 oC en atmosfera con 5 % de CO2. Se hicieron curvas de crecimiento para determinar el número de células apropiado para obtener monocapas confluentes viables por 72 h.
Ensayo del MTT [3-(4,5-dimetil-tiazol-2-il)-2,5-difeniltetrazolio]
El ensayo se usó para evaluar actividad antiproliferativa y selectividad de los AEs. Actividad antiproliferativa: las células cancerosas (10,000 por pozo) de interés (MCF-7, Hela y HepG-2) se sembraron en placas de 96 pozos en medio de cultivo (200 μL/pozo) que contenía concentración distinta (50, 100, 200, 300, 400 o 500 μg/mL) de AE y se incubaron 72 h a 37 oC. Células HEK293, Vero y B16F10 se trataron antes de proliferación como las cancerosas y en otros ensayos después de la proliferación en consideración a que el efecto sobre la viabilidad celular varia dependiendo del estado de la monocapa. Las células se dejaron proliferar sin tratamiento 24 h, posteriormente el medio se reemplazó por medio fresco con AE a las concentraciones mencionadas y la placa se incubó hasta 72 h a 37°C. Este segundo tratamiento se denominó después de proliferar. En cada placa se incluyeron células tratadas con dimetilsufóxido y no-tratadas con AE como controles. Para determinar la viabilidad se eliminó el medio de cultivo, se adicionaron 20 μ! de MTT (5 mg/mL) en cada pozo y la placa se incubó 4 h a 37°C. La intensidad del color de la reacción se determinó por espectrofotometría (Multiskan Go., Thermo Scientific) a longitud de onda de 580 nm. El valor de densidad óptica se consideró proporcional a la viabilidad celular y se estimó referente a 100 % de las células no tratadas.
Ensayo de condensación de cromatina
La condensación de cromatina se usó como indicador de actividad antiproliferativa. Brevemente, 8000 células en medio de cultivo que contenía AE (50 μg/mL) se depositaron en micropocillos de placas de vidrio. Las placas se incubaron 24 h a 37oC en atmosfera CO2 5 %; al término, las células se fijaron con p-formaldehído por 10 min y después de varios lavados con tampón fosfato salino se adicionó colorante Hoechst-33342 (Sigma-Aldrich, 5 μg/mL). Las placas se incubaron 15 min a 37 oC en oscuridad y enseguida se examinaron en un microscopio de inmunofluorescencia (Ex 450 - 490; cámara Nikon P6000). Células con cromatina condensada se contaron como porcentaje del número total de células teñidas con Hoechst-33342. En cada experimento se incluyeron células no tratadas y tratadas con ectoposide (Sigma-Aldrich: 250 μM)] como controles. Cada AE se analizó por duplicado en tres experimentos independientes.
Análisis de datos
Los datos de ensayos del MTT obtenidos en células cancerosas de interés (HeLa, MCF-7 y HepG-2) se expresaron como concentración inhibitoria 50 (CI ). Los datos con las otras células como concentración citotóxica 50 (CC ). El índice de selectividad (IS) fue la proporción entre CC50 en la célula normal (HEK293) y CI50 en la cancerosa. Los valores de CI50 y CC50 se calcularon por regresión lineal simple usando el programa R (R Development Core Team, 2013). La significancia de la diferencia entre datos del ensayo de condensación de cromatina se determinó por ANOVA y prueba de Tukey.
RESULTADOS
Los AEs variaron en su habilidad para afectar la viabilidad de células distintas a las cancerosas de interés, rangos de CC50 de 500-201 μg/mL, 200-100 μg/mL y 99-50 μg/mL indicaron citotoxicidad baja, media y alta, respectivamente, según lo sugerido por otros (Cos et al., 2006; Mazzio y Soliman, 2009). Como se presenta en Fig. 1, los cinco AEs menos citotóxicos fueron en el siguiente rango: S. officinalis < P. cumanense < L. origanoides (especímen COL587107) < A. popayanensis < P. eriopodon. Los cinco más citotóxicos fueron: T. caracasana (especimen COL587125) > L. graveolens > T. caracasana COL559.441 > S. glutinosa > L. alba.
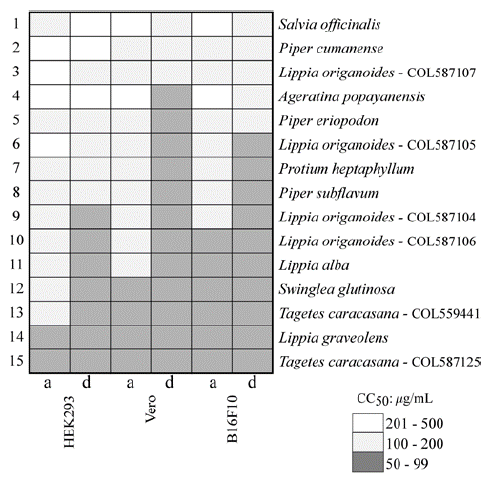
Figura 1 Perfiles de citotoxicidad de los AEs analizados. Células de riñón humano (HEK293), riñón de mono (Vero) y melanoma de ratón (B16F10) se trataron antes (a) y después (d) de proliferación. Los AEs aparecen organizados de menor a mayor citotoxicidad con base en valores de CC50 (Tabla 1 suplementaria). Citotoxicidad es menor cuanta menor intensidad de color.
No hay acuerdo sobre los valores de CI50 e IS indicando actividad antiproliferativa in vitro relevante. Se ha sugerido (Mazzio y Soliman, 2009; Ferraz et al. 2013) que valores de CI50 menores que 100 μg/mL e IS mayores que 3.0 se podrían usar para seleccionar muestras vegetales activas. Con base en este criterio, la actividad antiproliferativa en este estudio se categorizó como relevante (CI50=50 μg/mL; IS >4.0), moderada (CI50=50 μg/mL; IS=3.9-3.1) o irrelevante (CI50=50 μg/mL; IS <3.1). Valores CI50 >50 μg/mL indicaron inactividad. La Fig. 2 muestra resultados representativos del ensayo del MTT y la Tabla 2 presenta los valores de CI.
Tabla 2 Valores de CI50 de los aceites esenciales analizados.
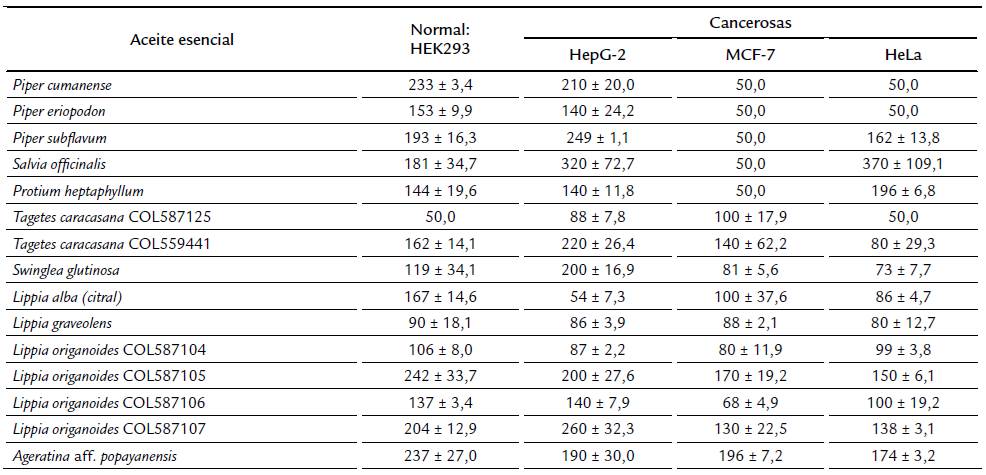
Datos (μg/mL) se presentan como promedio ± DS de tres ensayos independientes por duplicado. 50.0: concentración mínima que redujo más de 50% la viabilidad celular con respecto al control (no-tratado).
Los AEs variaron con respecto al grado de actividad en las células cancerosas (Fig. 3). AE de P. cumanense presentó actividad antiproliferativa relevante (CI50=50 μg/mL; IS=4.7) en células MCF-7 y HeLa; AEs de P. subflavum, S. officinalis y P. eriopodon actividad moderada (IS=3.9 y 3.6) en células MCF-7; y AEs de P. heptaphyllum y T. caracasana (especimen COL587125) actividad irrelevante (CI50=50 μg/mL; IS=2.9 y 1.0). El AE de L. alba fue el más activo en células HepG-2 con CI50 (54 ±7.3 μg/mL) e IS (3.1) cercanos al punto de corte. En un intento de corroborar actividad relevante y moderada, las células tratadas con los AEs de P. cumanense y S. officinalis se tiñeron con Hoechst para evidenciar condensación de cromatina (Fig. 4): con P. cumanense se observó mayor frecuencia de células con cromatina condensada respecto a las no-tratadas: 55 ± 3.7 % vs. 15 ± 3.7 % (p < 0.01) y con S. officinalis la diferencia no fue significante (19 ± 2.4 % vs. 15 ± 3.7 %; p > 0.05).
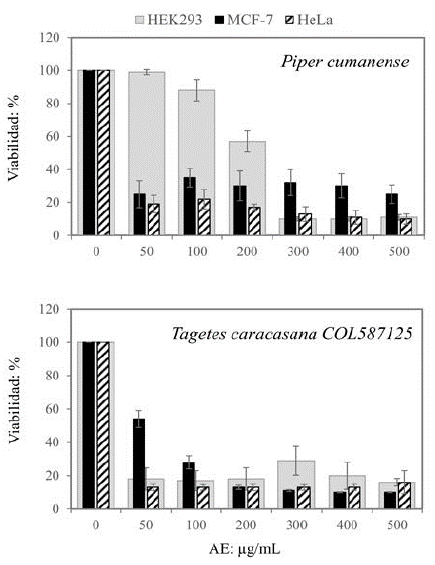
Figura 2 Efecto sobre la viabilidad celular de AEs analizados. Reducción de la viabilidad celular en ensayos del MTT dependiendo de la concentración de AE. P. cumanense presentó actividad antiproliferativa relevante: a concentración de 50 μg/mL redujo >50 % la viabilidad de las células cancerosas (MCF-7, HeLa) pero no la célula normal (HEK293). T. caracasana presentó actividad antiproliferativa irrelevante: a concentración de 50 μg/mL redujo >50 % la viabilidad de las células cancerosas y la normal.
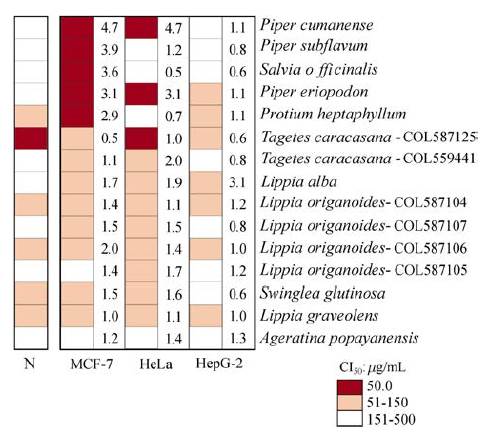
Figura 3 Perfiles de actividad antiproliferativa de los AEs analizados. Células cancerosas (MCF-7, HeLa, HepG-2) y células normales de riñón humano embrionario (N: HEK293). Números en los recuadros son índices de selectividad (IS=CC50 HEK293 /CI50 célula cancerosa; Tabla 2). Valores de CI50=50 μg/mL indicaron actividad relevante (IS >4.0), moderada (IS=3.1-4.0) o irrelevante (IS < 3.1). Valores de CI50 > 50 μg/mL indicaron inactividad.
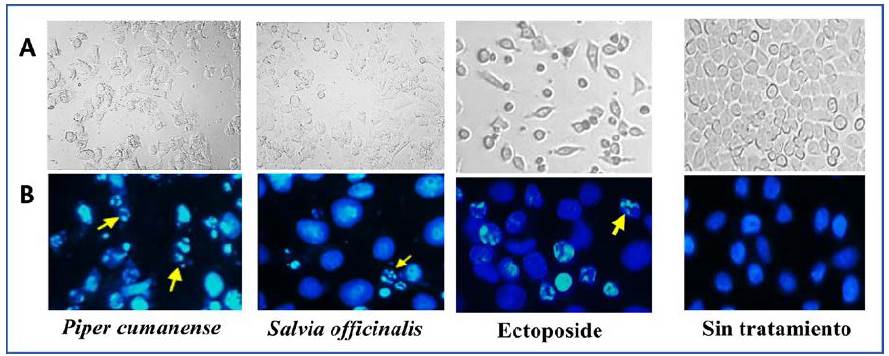
Figura 4 Condensación de cromatina en células MCF-7 tratadas con AE (50 pg/mL). Arriba: fotografías de cultivos celulares en fresco. Abajo: fotografías de células teñidas con Hoechst 33342 presentando condensación de cromatina (flecha).
De acuerdo a los perfiles de actividad antiproliferativa presentados en la Fig. 3, los AEs de cinco especies resultaron inactivos (CI50 >50 μg/mL). Con muestras diferentes de AEs pero de la misma especie se observaron diferencias: T. caracasana, un AE afectó en alto grado (CI50=50 μg/mL) la célula cancerosa y normal sugiriendo alta toxicidad pero el otro ejemplar mostró menor afectación tanto de células tumorales como de la normal (CI50=220-80 μg/mL); L. origanoides, el AE del especímen COL587104 (planta de Bucaramanga) fue el que más afectó la viabilidad de células cancerosas y normal (CI50=106-80 μg/mL) y al contrario el AE del especímen COL587105 (planta de Girón) (CI50=150-242 μg/mL). Los AEs de S. glutinosa (CI50=73-200 μg/mL) y L. graveolens (CI50=80-90 μg/mL) afectaron en igual grado células cancerosas y normal. El AE de Ageratina popayanensis fue el único que afectó en bajo grado (CI50=190-237 μg/mL) células cancerosas y las no cancerosas.
Composición química de los AEs
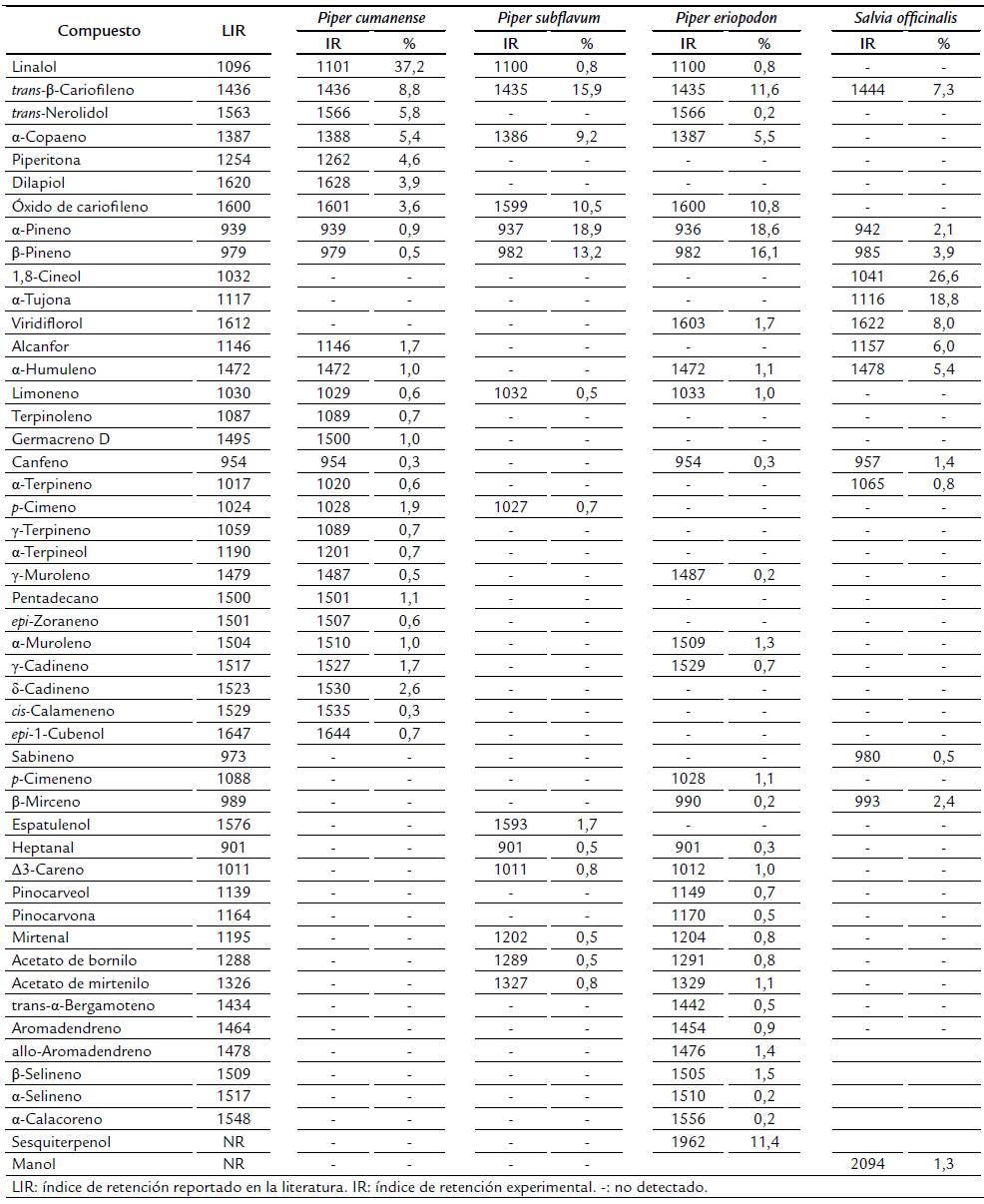
La Tabla 3 presenta la composición química de los AEs con actividad antiproliferativa relevante y moderada. La mayoría de compuestos fueron monoterpenos y sesquiterpenos. El 62 % del contenido del AE de P. cumanense está constituido de seis compuestos, linalol (37,2 %) y trans-P-cariofileno (8,8 %) son los mayoritarios; el 60 % de P. subflavum de cinco compuestos, α-pineno (18,9%), trans-P-cariofileno (15,9 %) y β-pineno (13,2 %) son los mayoritarios; el 63 % del AE de P. eripopodon corresponde a cinco compuestos, α-pineno (18,6 %), β-pineno (16,1 %) y trans β -cariofileno (11,6 %) son los mayoritarios; y el 71.4 % del contenido del AE de S. officinalis corresponde a seis compuestos, 1,8-cineol (26.6 %) y α -tujona (18.1 %) son los mayoritarios.
DISCUSIÓN
La selectividad es una propiedad tenida en cuenta al momento de seleccionar muestras vegetales para investigación en medicamentos para el cáncer (Ferraz et al. 2013; Harvey et al., 2015). Dado que el uso de ratones de laboratorio tiene limitaciones, los ensayos en células surgen como una alternativa para predecir selectividad (Xia et al., 2008). En este estudio se generaron perfiles de citotoxicidad en células cancerosas de interés, células humanas normales y células de órganos blanco (riñón y piel) de animales seleccionados para evaluación toxicológica. Con las primeras se pretendió evaluar actividad antiproliferativa y con las segundas selectividad. La estrategia sirvió para identificar los AEs de especies de Piper y Salvia officinalis como los más citotóxicos para células cancerosas y los menos para las no cancerosas. La estrategia podría robustecerse evaluando simultáneamente otros indicadores de viabilidad celular e incluyendo otras líneas celulares de órganos normales y blanco de análisis toxicológico como cerebro, hígado y piel.
El género Piper L. incluye cerca de 2000 especies y al menos 36 son nativas de América (Giovannini y Howes, 2017). En Colombia estas plantas se conocen con los nombres de cordoncillos o anises y 38 tienen reporte de uso medicinal (Bernal et al., 2011; Fonnegra y Villa, 2011). No se encontraron estudios evidenciando actividad antiproliferativa de muestras preparadas a partir de las plantas colombianas, pero sí de al menos 16 especies cultivadas en otros países (Kumar et al., 2015). Los AEs de especies de Piper incluidos en este estudio presentaron actividad antiproliferativa en células MCF-7 y HeLa sugiriendo potencial anticancerígeno. Es conocido que las diversas actividades biológicas de los AEs se explican por la acción de los compuestos que contienen (Pandey et al., 2017). El análisis por cromatografía identificó β-cariofileno, α-copaeno y pineno (α y β) como constituyentes mayoritarios de los AEs de Piper. Se ha demostrado que el β-cariofi leno y óxido de cariofileno tienen potente actividad anticancerígena (Fidyt et al., 2016); y el α-copaeno, β-pineno, a-pinene y otros monoterpenos inhiben la proliferación de una amplia variedad de células cancerígenas (Zhao et al., 2017; Scotti et al., 2017). El linalol se identificó como el componente mayoritario (37 %) del AE de P. cumanesey esto podría explicar su baja citotoxicidad observada en células humanas renales (HEK293) y hepáticas (HepG-2). En un estudio se demsotró que el linalol no causó hepatotoxicidad en ratones de laboratorio (Jana et al 2014). El potencial farmacológico de especies de Piper es bien reconocido, del extracto de P. nigrum Carlos L. se aisló piperina un alcaloide con potente actividad antitumoral (Wang et al., 2014; Zheng et al., 2016).
Del género Salvia al menos 66 especies tienen uso medicinal en Colombia, S. officinalis se conoce con el nombre de salvia (Bernal et al., 2011). No se encontraron estudios evidenciando actividad antiproliferativa de muestras de estas especies. En países alrededor del mundo varias especies se usan en la medicina tradicional (Baricevic y Bartol, 2000). Se ha reportado que el AE inhibe células leucémicas y de cánceres de colon, mama y pulmón (García et al., 2016) y el desarrollo de tumor en ratones de laboratorio (Bonesia et al., 2017). El AE de S. officinalis incluido en este estudio presentó actividad antiproliferativa en células MCF-7 sugiriendo potencial anticancerígeno. El 46 % de su contenido está constituido de 1,8-cineol, α -tujona y β-cariofileno. En una muestra extraída de una planta del Valle del Cauca se encontraron β-cariofileno y α -copaeno como los constituyentes mayoritarios (Saldarriaga et al., 2009) y los mismos terpenos se identificaron en AEs de plantas de otros países (Cvetkovikj et al., 2015). La actividad antiproliferativa del AE puede deberse a la presencia de estos terpenos, el 1-8-cineol mostró eficacia para inhibir el desarrollo de cáncer colorectal en ratones (Murata et al., 2013) y de los otros terpenos existe evidencia de la actividad anticancerígena como se mencionó.
CONCLUSIONES
En este estudio se pretendió identificar especies de plantas de la medicina popular colombiana apropiadas para investigar en medicamentos para cáncer de mama, cervical y hepatocelular. Se estudió la actividad antiproliferativa de sus AEs y se identificaron los componentes químicos de las muestras activas usando GC-MS. El estudio tiene limitaciones, la actividad observada en el ensayo del MTT no se confirmó con otro ensayo y no se investigaron los mecanismos moleculares de inhibición de la proliferación celular. No obstante, los resultados aportan conocimiento nuevo sobre el potencial farmacológico de la flora colombiana, específicamente, de AEs de P. cumanense, P. subflavum var. espejuelanum, P. eriopodom y S. officinalis. Las muestras de estas especies pueden servir como puntos de partida para desarrollo de medicamentos herbales y descubrimiento de fármacos para tratamiento paliativo y curativo del cáncer de mama y cáncer cervical.