INTRODUCCIÓN
La enfermedad infecciosa de la bursa (IBD) o enfermedad de Gumboro es una infección viral aguda y altamente contagiosa que afecta aves comerciales jóvenes, en las que el virus infecta los linfocitos B de la bursa de Fabricio y genera lesiones en los órganos linfoides. Pese a los esfuerzos para su control a través de la vacunación, los cuadros de inmunosupresión debido a las lesiones en estos órganos han sido reportados desde años atrás alrededor del mundo, cursando con infecciones secundarias, tratamientos antibióticos recurrentes, bajos rendimientos productivos y fallas en la respuesta inmune a vacunas (Cheville, 1967; Saif, 1991; Lukert y Saif, 1997).
El virus que ocasiona la IBD (IBDV) pertenece a la familia Birnaviridae, género Avibirnavirus y posee un genoma dsARN que presenta altas tasas de mutación (Dobos et al., 1979), reordenamiento y recombinación genética, lo cual altera la antigenicidad y por ende afecta la eficacia en la protección conferida por el uso de vacunas (Jackwood y Sommer-Wagner, 2011). Existen dos serotipos designados como I y II, de los cuales sólo al I se le han atribuido los cuadros clínicos de la enfermedad en pollos (Cosgrove, 1962; McNulty et al., 1979). El genoma tiene dos segmentos: A y B; el primero codifica la proteína no estructural VP5 y una poliproteína sobre la que actúa la proteasa viral VP4 para generar dos proteínas de la cápside (pVP2 y VP3) (Kibenge et al., 1988; Birghan et al., 2000). La pVP2 se escinde para generar la proteína de cápside madura VP2 con tres dominios (B-base, S-shell y P-proyección) (Coulibaly et al., 2005). El dominio P posee cuatro estructuras de bucle en la superficie del virión (PBC, PDE, PHI y PFG) y es el responsable de inducir la respuesta inmune protectora en las aves al permitir la unión con anticuerpos monoclonales (Schnitzler et al., 1993; Letzel et al., 2007). Asimismo, las mutaciones que generan cambios en la secuencia de aminoácidos en algunos de estos dominios de VP2 pueden modificar la antigenicidad del virus (Bayliss et al., 1990; Snyder et al., 1992; Jackwood et al., 2006); especificamente se ha reportado la alta variabilidad del dominio P (Jackwood y Sommer-Wagner, 2011; Jackwood, 2012), por lo que se le ha dado la denominación de región hipervariable (hvVP2). Estos cambios también han llevado a la clasificación de los aislamientos en dos grupos antigénicos: cepas clásicas (cv) y variantes que ocasionana cuadros subclínicos (sc); sin embargo, diversos estudios han demostrado que existen variaciones antigénicas al interior de los grupos (Lukert et al., 1975; Skeeles et al., 1979; Snyder et al., 1988; Sapats y Ignjatovic, 2000; Liu et al., 2002; Jackwood y Sommer-Wagner, 2011), a las cuales se les pueden atribuir la ineficacia en la protección conferida por las vacunas. De esta forma, la clasificación de los IBDV en los dos grupos antigénicos es insuficiente para evidenciar las diferencias antigénicas entre aislamientos de campo (Jackwood et al., 2018).
Las cepas del IBDV detectadas alrededor del mundo también se han clasificado con base en su patogenicidad o virulencia en muy virulentas (vv) (van den Berg et al., 2004). Aunque existen otros esquemas de nomenclatura y clasificación del IBDV como los basados en los nombres de los investigadores que los describieron por primera vez (Winterfield, Lukert, Baxendale), designaciones alfa numéricas (STC, D78, S706, 228E, GLS) y localizaciones geográficas (Del-A, Del-E, MD), es necesario desarrollar metodologías unificadas, rápidas y precisas para caracterizar las propiedades antigénicas de las cepas que circulan en campo y así orientar las estrategias de control de esta enfermedad (Banda et al., 2003).
Las técnicas moleculares (RT-PCR, RFLP y qRT-PCR) permiten la caracterización más precisa de los cambios en el genoma que se relacionan con modificaciones de la antigenicidad (Ikuta et al., 2001; Jackwood et al., 2001; Fellahi et al., 2016). Como resultado de lo anterior, recientemente Jackwood et al., (2018) propusieron un esquema de clasificación en genogrupos basado en el análisis de la región hvVP2 del IBDV, que intenta brindar más información de los cambios que se han presentado en este virus, buscando una mejor correlación con los cuadros clínicos observados en campo. La organización en genogrupos también parte de la necesidad de clasificar los aislamientos de campo que presentan linajes diferentes a los grupos cv, sc o vv (Jackwood y Sommer, 2005; Hon et al., 2006; Yamaguchi et al., 2007; Lupini et al., 2016).
En Colombia, la IBD se considera endémica con el reporte de 853 casos en el último boletín epidemiológico del Instituto Colombiano Agropecuario (ICA, 2015), siendo la segunda enfermedad de mayor presentación en aves comerciales; sin embargo, no es considerada de control oficial. A pesar de la frecuencia de las infecciones por este agente en el país y la importancia de realizar un monitoreo continuo de los cambios en las regiones hipervariables del virus para orientar las estrategias de control, son pocos los estudios en Colombia que caracterizan los cuadros clínicos e identifican los genogrupos circulantes. En consecuencia, el diagnóstico molecular se realiza en diversos laboratorios, en los que se utiliza principalmente la clasificación en los dos grupos antigénicos reportados (cepas clásicas y variantes), lo cual no permite realizar apropiadamente el monitoreo de los cambios de las cepas de campo. En cuanto a la información disponible en el país, la investigación más reciente fue en 2012, la cual demostró la existencia de aminoácidos típicos de cepas variantes o clásicas; sin embargo, en una muestra de Colombia del 2001 se evidenció una combinación de aminoácidos no identificada previamente en el mundo, hallazgo cuya importancia se desconoce (Jackwood, 2012). Con base en lo anterior, el objetivo de esta investigación fue identificar la frecuencia de lesiones en órganos del sistema inmune de aves con diagnóstico presuntivo de IBD y establecer la presencia de los genotipos circulando en el país. Los resultados obtenidos en este estudio representan un aporte al conocimiento del virus de la IBD y constituyen el primer reporte de los genogrupos del IBDV circulantes en aves comerciales de Colombia, permitiendo además evidenciar la variación que se ha presentado en años recientes.
MATERIALES Y MÉTODOS
Análisis de casos e identificación de lesiones histopatológicas
Se analizaron los resultados histopatológicos de 381 casos en las bases de datos del Laboratorio de Patología Aviar (LPA) de la Universidad Nacional de Colombia durante el periodo 2016-2018, para identificar la frecuencia de presentación de lesiones en órganos del sistema inmune (bursa de Fabricio, timo, bazo y médula ósea). Los tejidos evaluados fueron fijados en formol bufferado al 10 % y se les realizó un proceso de imbibición en parafina y tinción con hematoxilina-eosina. La escala de las lesiones de depleción y/o necrosis linfoide en bursa y timo se categorizaron de acuerdo con lo descrito por Sharma et al., 1989, con una escala de 0-4 para bursa y de 0-3 para timo. A las lesiones de depleción linfoide en bazo y medula ósea se les asignó una escala de gravedad de 0-3 que corresponde a: 0= ausencia de lesión, 1 = depleción leve, 2 = depleción moderada y 3 = depleción severa.
Extracción de ARN viral
Se analizaron 35 bursas de Fabricio de aves de estirpes comerciales (Pollo de engorde n = 32, Reproductoras n = 2 y Ponedora comercial n = 1) provenientes de tres departamentos de Colombia (Antioquia, Cundinamarca y Santander); también se empleó una muestra de una vacuna a base de virus vivo atenuado como control positivo. A partir de los tejidos y la vacuna se realizó la extracción de ARN con el kit comercial High Pure Viral Nucleic Acid kit® (Roche Molecular Systems), de acuerdo con las recomendaciones de la casa comercial en un volumen final de elución de 50 μL. La concentración y pureza del ARN fueron medidos con un espectrofotómetro de microvolumen (NanoDrop Technologies, Wilmington).
RT-PCR del gen VP2 del IBDV
Se obtuvo cADN a partir de 10 Lde ARN extraído (concentración aproximada de 100 ng/ L) con el kit comercial High Capacity cDNA Reverse Transcription Kit® (Applied Biosystems). El volumen final de reacción fue 20 μL con 10 μL de mezcla de reacción que contenía: 50 U de RT, 20 U de inhibidor de ARNasas, 4 mM de dNTP (100 nM) y 2,0 μL de random primers (10X). Las reacciones de RT se llevaron a cabo con las siguientes condiciones: 25 oC por 10 minutos y 37 oC por 120 minutos, seguidos por un calentamiento a 85 oC por 5 minutos. El cADN fue empleado para la PCR con los primers VP2 802 F - GTAACAATCACACTGTTCTCAG y VP2 1050 R - GATGTYARTGGCTGGGTTATC, específicos para amplificar un fragmento de 248 pb de la región hvVP2 del IBDV. La PCR se realizó en un volumen final de reacción de 25 μL con los siguientes reactivos: 0,04 U de Taq Polimerasa, 1,5 mM de MgCl2, 0,5 mM dNTPs y 0,32 μM de cada primer. Las temperaturas y tiempos de amplificación fueron: 94 oC por 5 minutos, 35 ciclos de 94 oC por 30 segundos, 54 oC por 35 segundos y 72 oC por 40 segundos, y una extensión final de 5 minutos a 72 oC. Los productos se visualizaron en geles de agarosa al 1,5 % con el colorante EZ-Vision® en un sistema digital de fotodocumentación (Gel Doc® Bio-Rad Laboratories Inc.).
Análisis de secuencia de nucleótidos
Los productos de 248 pb fueron purificados por medio de precipitación en alcohol y secuenciados en el Instituto de Genética de la Universidad Nacional de Colombia con el BigDye Terminator v3.1Cycle Sequencing kit (Applied Biosystems,California, EEUU) usando electroforesis de capilares y el secuenciador ABI3730XL (Applied Biosystems). El análisis de las secuencias y la construcción de los árboles filogenéticos se realizó con el software MEGA 6.0 (Molecular Evolutionary Genetics Analysis, The Pennsylvania State University) (Tamura et al., 2013). Las relaciones filogenéticas fueron inferidas usando el método de Neighbor-Joining (Saitou y Nei, 1987) con 1000 réplicas bootstrap. Las distancias evolutivas se calcularon con el método estadístico maximum-likelihood (Tamura et al., 2004) y se muestran en las unidades del número de sustituciones de bases por sitio. Los análisis incluyeron 97 secuencias de nucleótidos correspondientes a las 35 muestras de este estudio y 62 secuencias de referencia de la VP2 del IBDV reportadas en el GenBank. El análisis de los cambios en la secuencia de aminoácidos de la proteína VP2 se realizó con la herramienta BLAST® blastx del National Center for Biotechnology Information (NCBI).
RESULTADOS
Lesiones microscópicas
De 381 casos clínicos recibidos en el LPA para diagnóstico histopatológico en el período 2016 - 2018, en 97 (25 %) se evidenciaron lesiones microscópicas en los órganos inmunes relacionadas con procesos de inmunodepresión y en 30 (8 %) se encontraron lesiones compatibles con la enfermedad de Gumboro. De éstos, 20 corresponden a pollo de engorde con rangos de edad entre 30 y 90 días con el 90 % de presentación alrededor de los 45 días, nueve corresponden a ponedora comercial con rangos de edad de 2 - 10 semanas con mayor frecuencia de presentación entre la cuarta y sexta semana y una explotación de pollo criollo de seis semanas.
Las lesiones encontradas en la bursa fueron: depleción linfoide (100 %) con un escala promedio de 3,4 (63 % grado 4 y 37 % grado 3), atrofia (77 %), repliegue epitelial (70 %), presencia de quistes epiteliales (56 %), quistes foliculares (50 %), infiltración de células inflamatorias intra o interfolicular (73 %) distribuidos en macrófagos y linfoplasmocitaria (37 %), heterófilos (20 %) y mixta (17 %), edema (23 %), linfocitolisis (23 %), fibroplasia interfolicular (20 %), hiperplasia del epitelio folicular (17 %), presencia de granulomas foliculares (10 %) y hemorragia (7 %) (Fig. 1). En el 67 % de los casos se analizó bazo, en el 60 % timo y en el 26 % médula ósea con grados de depleción linfoide promedio de 2,6, 2,3 y 1,5 respectivamente. Las lesiones evidenciadas en timo fueron: depleción linfoide (100 %) medular y cortical (75 %), cortical (15 %), infiltración de células inflamatorias (100 %), linfocitolisis (30 %), edema (27 %) y congestión (22 %). Las lesiones en bazo fueron: depleción linfoide en áreas T y B (100 %), hiperplasia reticuloendotelial (16 %) y linfocitolisis (13 %). Por último en la médula ósea se observó hipoplasia o depleción de la línea mieloide en la totalidad de los casos.
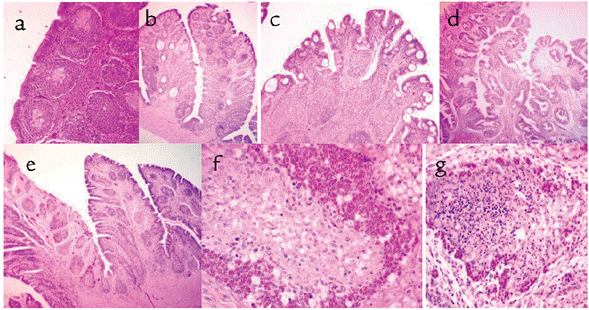
Figura 1 Lesiones histológicas en bursa de Fabricio compatibles con Enfermedad de Gumboro. HyE. a-d: diversos grados de depleción linfoide y atrofia; a: depleción linfoide centros germinales; b: quistes foliculares; c: quistes epiteliales; d: atrofia y repliegue epitelial; e: atrofia, inflamación y fibrosis interfolicular; f: detalle de infi ltración por heterófi los a nivel folicular; g: linfocitolisis y depleción linfoide marcada. b, d y e: 4x; a y c: 10x; f y g: 40x.
Se encontraron lesiones en otros órganos relacionadas con infecciones concominantes, manifestando los siguientes porcentajes de presentación: infecciones bacterianas en sistema músculo esquelético como tendinitis y osteomielitis (47 %), bronquitis y neumonía de origen bacteriano (30 %), enteritis por Coccidia spp (27 %), hepatitis y/o miocarditis de origen bacteriano (24 %), traqueítis no granulocíticas de origen viral con o sin encefalitis compatibles con infecciones por el virus de la bronquitis infecciosa y/o Enfermedad de Newcastle (23 %), dermatitis de origen bacteriano y viral (10 %) y presencia de Cryptosporidium spp en epitelio bursal (10 %).
Distribución de genogrupos
En este estudio se analizaron 35 secuencias obtenidas a partir de muestras de bursas provenientes de unidades productivas de pollos de engorde (32), reproductoras (2) y ponedoras comerciales (1). Las granjas de pollo de engorde estaban ubicadas en dos departamentos: Cundinamarca (número de detecciones = 19) y Santander (n = 8), con un rango de edad de las aves a partir de las cuales se obtuvo la muestra entre 19 y 30 días. La procedencia no fue reportada en cinco de las muestras analizadas. Las dos detecciones de reproductoras con edades de 3 y 5 semanas se realizaron en Cundinamarca y la única muestra de ponedora comercial de 5 semanas de edad se ubicó en Antioquia (Fig. 2 y 3).
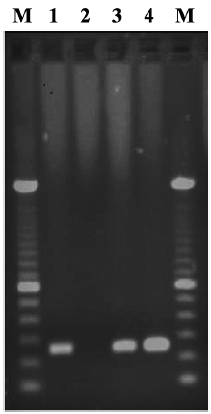
Figura 2 Imagen representativa del gel de electroforesis de RTPCR positivas al gen VP2 del Virus de la Enfermedad de Gumboro (IBDV). M: marcador de peso molecular 100 pb; 1: control positivo que corresponde a una vacuna viva contra IBDV; 2: control negativo de reacción; 3 y 4: muestras de bursas positivas al gen VP2 del IBDV (tamaño del producto 235 pb).
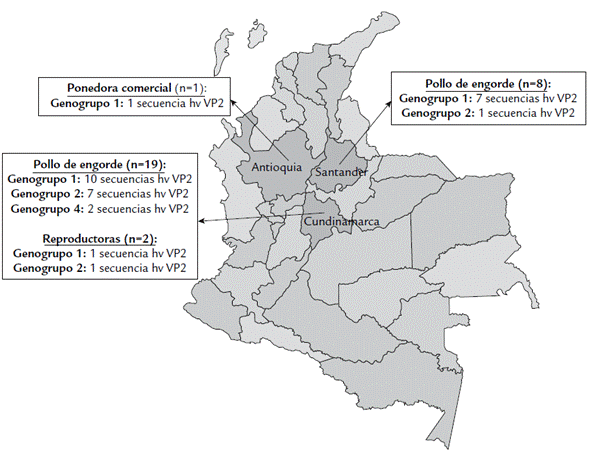
Figura 3 Distribución de genogrupos basados en el análisis de la hvVP2 del IBDV por tipo de unidad productiva (Pollo de engorde, Reproductora y Ponedora Comercial) y por Departamento. En cinco secuencias de pollos de engorde no se reportó la procedencia o la ubicación de las granjas.
Después de la secuenciación, el análisis de la alineación de la región hvVP2 y el establecimiento de las relaciones filogenéticas se encontró que las 35 secuencias de este estudio se ubicaron en tres de los siete genogrupos reportados a nivel mundial (Michel y Jackwood, 2017). En el genogrupo 1 se clasificaron 24 secuencias (69,4 %), nueve en el genogrupo 2 (25 %) y dos en el genogrupo 4 (5,6 %). De las secuencias detectadas en lotes de pollos de engorde (n = 32), 23 se ubicaron en el genogrupo 1 (72 %), siete en el genogrupo 2 (22 %) y dos en el genogrupo 4 (6 %).
Las dos secuencias obtenidas de muestras de reproductoras se ubicaron en los genogrupos 1 (secuencia identificada -ID como 1703) y 2 (ID 1601) y la muestra de ponedora comercial (ID 1810) en el genogrupo 1 (Fig. 4).
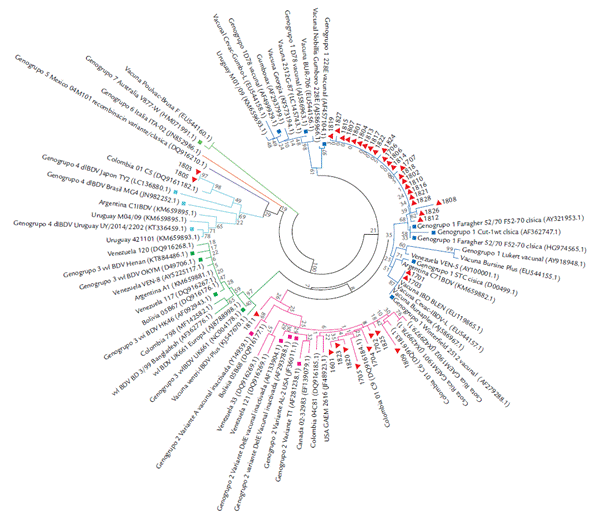
Figura 4 Distribución de las secuencias de la hvVP2 de 32 detecciones del IBDV en granjas de pollos de engorde de Colombia. Las relaciones filogenéticas se infirieron utilizando el método de Neighbor-Joining. Se muestra el árbol óptimo después del análisis de 1000 réplicas de bootstrap con la suma de la longitud de las ramas = 1,14404678. Las distancias evolutivas se calcularon utilizando el método estadístico Maximum Composite Likelihood y están dadas en las unidades del número de sustituciones de bases por sitio. Los análisis evolutivos se realizaron con el software MEGA 6.0. El color de las ramas representa el genogrupo (azul: genogrupo 1, rosa: 2, verde: 3, azul claro: 4, violeta: 5, naranja: 6 y verde claro: 7). Los cuadros de colores (•) corresponden a las cepas de referencia disponibles en GenBank de cada genogrupo y los triángulos rojos ( ) a las secuencias del estudio.
) a las secuencias del estudio.
Las secuencias que se ubicaron en el genogrupo 1 presentaron mayor similitud genética (98,7 %) con la cepa de referencia Faragher 52/70 (AY321953.1), seguida de la cepa Cu-1wt (AF362747.1) (97,5 %). El menor porcentaje de similitud fue con la cepa Lukert (AY918948.1) (93,3 %) y D78 (AF499929.1) (93,4 %) (Tabla 1). Dos secuencias (ID 1701 de pollo de engorde y 1703 de reproductoras) evidenciaron mayor similitud con cepas vacunales (Fig. 4). Asimismo, el porcentaje de identidad entre ellas fue 97,5 %.
Tabla 1 Porcentajes de identidad genética entre secuencias de la proteína viral VP2 y cepas de referencia de los genogrupos 1, 2 y 4 del virus de la enfermedad de Gumboro (IBDV).
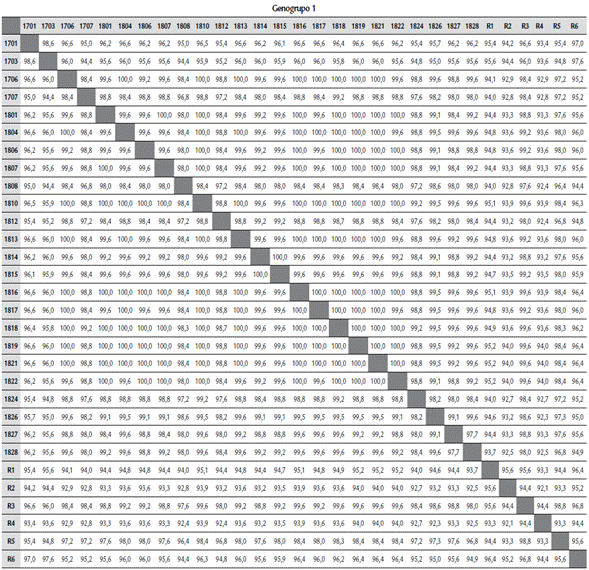
La primera fila y la primera columna corresponden a las muestras (identificadas con números) y a las cepas de referencia (identificadas con R). R1: 228E (AF457104.1); R2: D78 AF499929.1); R3: Faragher 52/70 (AY321953.1); R4: Lukert (AY918948.1); R5: Cu-1wt (AF362747.1) y R6: STC (D00499.1). Los porcentajes fueron calculados con el software Geneious Prime®.
Las nueve secuencias del genogrupo 2 presentaron alta similitud genética (99 - 100 %) con cepas detectadas previamente en el país (DQ916183.1 y DQ916184.1) (Fig. 4). Sin embargo, al comparar las secuencias de aminoácidos se evidenció un cambio en la posición 254 de asparagina a serina (N254S) en seis de las nueve muestras. El porcentaje de identidad entre las nueve secuencias del estudio y cuatro cepas variantes de referencia fue 96,4 % (Tabla 1).
Las dos muestras que se ubicaron en el genogrupo 4 tuvieron una alta similitud genética (99 %) con la cepa Colombia01_C5 (DQ916182) del mismo genogrupo. Las secuencias de aminoácidos tuvieron el perfil representativo del genogrupo (272T, 289P, 290I y 296F). En las dos secuencias de aminoácidos de este estudio se encontró un cambio en la posición 280 de histidina a asparagina (H280N) al compararlas con las cepas de referencia de este genogrupo. El porcentaje de identidad entre ellas y cepas de referencia fue 93,4 % (Tabla 1).
DISCUSIÓN
La IBD es una enfermedad inmunosupresora importante en las aves de producción, siendo considerada uno de los problemas más significativos para la industria avícola por las pérdidas económicas que ocasiona al tener impactos directos (mortalidad y bajos rendimientos productivos) e indirectos (infecciones secundarias y fallas en la vacunación) (van den Berg et al., 2004). Mediante el análisis de los hallazgos histopatológicos de esta investigación se logró establecer que corresponden en su mayoría a lesiones depléticas y atróficas que son difíciles de interpretar sin la ayuda de otras pruebas diagnósticas y de datos de anamnesis completos. La mayoría de los casos son de unidades avícolas comerciales que cuentan con diversos planes vacunales que incluyen una o hasta tres dosis de vacunas vivas atenuadas intermedias o intermedias plus que pueden ocasionar lesión en el tejido. De todos los casos analizados, únicamente el 20 % correspondían a aves sin vacunación o que utilizaban una vacuna recombinante, lo que permitiría inferir que probablemente las lesiones evidenciadas fueron ocasionadas por un virus de campo. De allí la importancia de un soporte de diagnóstico con otras pruebas que permitan esclarecer los IBDV circulantes. Asimismo, en el presente estudio fueron evidentes las lesiones ocasionadas por infecciones concomitantes, similar a lo reportado en presencia de cepas variantes (Lukert y Saif, 1997). Lo anterior sumado a la necesidad de evaluar y orientar las estrategias de prevención y control de la enfermedad, justifica la realización de investigaciones que busquen la caracterización de las cepas circulantes en campo, teniendo en cuenta la capacidad de cambios por mutación, recombinación y reordenamiento en los genes del IBDV que codifican dominios específicos de las proteínas inmunodominantes.
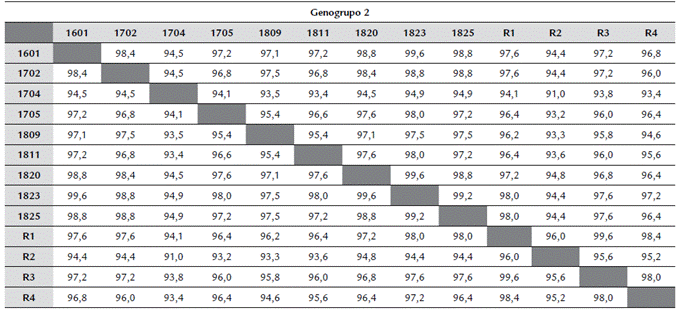
R1: Variante AL-2 USA (JF736011.1); R2: Variante A (Y14959.1); R3 Variante DelE (AF133904.1) y R4: Variante T1 (AF281238.1).
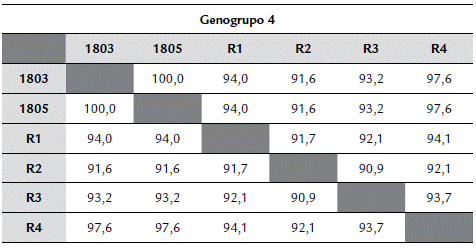
R1: Uruguay UY/2014/2202 (KT336459.1); R2: Brasil MG4 (JN982252.1); R3: Japon TY2 (LC136880.1) y R4: Colombia 01_C5 (DQ916182.1).
A través del análisis de la región hvVP2 realizado en este estudio, se lograron clasificar en genogrupos 35 detecciones moleculares provenientes de aves comerciales de granjas en Colombia. La contribución de esta proteína a las propiedades antigénicas del IBDV ha sido demostrada, debido a que es la única reconocida por anticuerpos neutralizantes y es la responsable de la unión a la célula huésped (Brandt et al., 2001; Letzel et al., 2007). La VP2 es una proteína de 441 aminoácidos que se ubica en la superficie del virus con tres dominios; el dominio P, comprendido entre los aminoácidos 206 a 350, es el que presenta la mayor variación debido a la presión de selección (Bayliss et al., 1990). Los primers empleados en esta investigación amplifican una secuencia que codifica parte de esta región (aa 225 a 307), en la que se han reportado variaciones e incluso se recomienda su análisis para el seguimiento de cambios característicos del virus de diferentes zonas geográficas (Michel y Jackwood, 2017). Sin embargo, la proteína VP2 no es la única responsable de los fenotipos como el vv (Boot et al., 2000).
Diversos estudios sugieren adicionalmente reordenamientos del segmento B (Hon et al., 2006; Le Nouen et al., 2006), por lo que se debería incluir el análisis de secuencias más grandes de los dos segmentos del virus para evidenciar la evolución en términos de mutaciones, recombinaciones o reordenamientos del material genético asociados con cambios antigénicos y por lo tanto, con la presentación de los cuadros clínicos en campo.
En este estudio se lograron clasificar las 35 detecciones en los genogrupos 1, 2 y 4, siendo la primera investigación en el país con este sistema propuesto por Michel yJackwood en el 2017. La clasificación en genogrupos permite una mayor discriminación entre secuencias similares, al generar grupos politéticos que comparten una serie de características, de las cuales ninguna es esencial para pertenecer al grupo (van Regenmortel et al., 1997). Otra de las ventajas de la clasificación en genogrupos es que permite la identificación precisa del fenotipo vv, debido a que con la nomenclatura convencional (c, sc y vv), algunas cepas clasificadas en el patotipo vvIBDV no presentan los aminoácidos típicos (A222, I242, I256, I294 y S299) y los cambios en el genoma corresponden a reordenamientos del segmento B que no lo tienen las verdaderas cepas muy virulentas (Escaffre et al., 2013).
El empleo de este sistema en la presente investigación permitió ubicar dos secuencias en el genogrupo 4, que por sus características genotípicas no se logran clasificar por el sistema convencional empleado en los laboratorios de diagnóstico. Los cambios en el genoma de las cepas del genogrupo 4 se atribuyen al drift antigénico, los cuales generan variaciones antigénicas (Tomás et al., 2019). Estas variaciones se podrían reflejar en la baja efectividad de las vacunas disponibles para el control de la enfermedad (Jackwood y Sommer-Wagner, 2011); sin embargo, lo anterior no ha sido demostrado. El perfil de aminoácidos de las dos secuencias identificadas en el genogrupo 4 de esta investigación es similar al reportado en Suramérica (Hernández et al., 2015), los cuales pertenecen a un linaje independiente de IBDV (dIBDV por distinto o distintivo) relacionado con cepas históricas de Europa y restringido a algunas áreas geográficas (Jackwood et al., 2018). Estos linajes independientes también han sido reportados con cepas italianas, las cuales se clasifican en el genogrupo 6 (Lupini et al., 2016). Adicionalmente, en las dos secuencias de este estudio se detectó el cambio H280N, el cual no ha sido reportado previamente en la literatura, por lo que se recomienda realizar el seguimiento para conocer las implicaciones que puede tener en la antigenicidad y la patogenicidad en campo, aún más considerando que fue el genogrupo con el menor porcentaje de identidad entre secuencias y cepas de referencia.
Las secuencias del genogrupo 1 evidenciaron los aminoácidos típicos de cepas clásicas en la región hvVP2, siendo el grupo con el mayor porcentaje de identidad genética entre las mismas secuencias y con cepas de referencia al compararlo con los porcentajes de los otros dos genogrupos identificados en este estudio. A diferencia del genogrupo 4, este grupo politético se encuentra distribuido alrededor del mundo y corresponde a cepas predominantemente clásicas (Jackwood et al., 2018).
Las secuencias del genogrupo 2 también evidenciaron el patrón de aminoácidos típicos de cepas variantes previamente reportado (Michel y Jackwood, 2017); sin embargo, el porcentaje de identidad entre secuencias y cepas de referencia fue menor al evidenciado en el genogrupo 1. Particularmente, en seis secuencias se detectó el cambio N254S con relación a cepas aisladas de Colombia y reportadas por Jackwood y Sommer-Wagner en el 2007. Este cambio adicional fue también evidenciado en cepas de Colombia y México en un estudio previo (Jackwood, 2012), por lo que se considera que hace parte del perfil de aminoácidos en el dominio PDE de algunas cepas variantes y posiblemente se genera por uno o más eventos de recombinación (Jackwood, 2012). Los eventos de recombinación en el segmento A del genoma han involucrado cepas de vacunas atenuadas de IBDV (Hon et al., 2008), variantes y vvIBDV (He et al., 2009). Nuevamente se reitera la necesidad de corroborar la importancia de estos cambios en la antigenicidad de los IBDV mediante estudios inmunológicos, incluyendo ensayos de vacunación/desafío, lo cual implica el desarrollo de protocolos con estándares internacionales (Jackwood, 2012).
A pesar de la necesidad de realizar pruebas in vivo para determinar la antigenicidad y la patogenicidad de las cepas de IBDV que circulan en campo, se debe considerar la complejidad que existe en el montaje y las diferencias que se pueden presentan en los resultados de estos ensayos en los distintos laboratorios (Jackwood et al., 2018). De esta forma, los análisis de secuencias de nucleótidos y la clasificación en genogrupos se proponen como una opción de diagnóstico y seguimiento de los cambios evolutivos del IBDV, al generar datos consistentes que pueden ser divulgados en documentos científicos y bases de datos internacionales, haciendo posible la comparación entre secuencias de este virus dentro del país y entre países. Asimismo, se debe buscar la estandarización de la secuencia a analizar, generando un sistema internacional de clasificación aceptado y comparable a nivel internacional (Jackwood et al., 2018).
CONCLUSIONES
Estos hallazgos demuestran las lesiones histopatológicas de órganos inmunes en aves comerciales, producto de la presencia de virus o factores inmunosupresores, lo cual aumenta la susceptibilidad a infecciones con patógenos oportunistas y afecta las respuestas a vacunas y tratamientos. A pesar de los esfuerzos en vacunación, por los cambios del virus se vuelve difícil su control. Los resultados de esta investigación demuestran la variación entre los genogrupos, justificando la necesidad de implementar modelos de clasificación específicos en los laboratorios de diagnóstico veterinario en el país. Esto generará una mejor comprensión de los cuadros clínicos en campo, que a su vez orientará el diseño y la implementación de estrategias de control de esta enfermedad en la industria avícola nacional e internacional.















