INTRODUCCIÓN
La infección por el virus de la Hepatitis C (VHC) constituye una importante causa de morbilidad y mortalidad en el mundo (World Health Organization, 2017). El cuadro clínico es variable e incluye infecciones agudas que pueden derivar en infecciones crónicas, cirrosis hepática que pueden requerir trasplante de hígado, carcinoma hepatocelular y muerte. La infección crónica se presenta en el 75 % al 85 % de las personas. La cirrosis se genera en el 10 % al 20 % de los pacientes con infecciones crónicas en un periodo de 20 a 30 años (Rustgi, 2007). En pacientes cirróticos, el riesgo de carcinoma hepatocelular está entre el 1 al 5 % (Westbrook and Dusheiko, 2014). En cuanto al trasplante, se ha documentado que la cirrosis secundaria a la infección por el VHC es la principal causa de trasplante de hígado en Estados Unidos (Dhingra et al., 2016).
Al tratarse de una infección crónica, el diagnóstico precoz es fundamental para evitar la progresión y el contagio a otras personas. Más aún si se tiene en cuenta que los agentes antivirales de acción directa son altamente eficaces para su control (Abad et al., 2017). En este sentido, se han realizado esfuerzos por documentar la prevalencia de infección e identificar grupos de riesgo. La OMS estima que la prevalencia mundial de infección es del 1 % lo que corresponde a 71 millones de personas infectadas. Tal prevalencia varía dependiendo de los países, así en los del mediterráneo oriental alcanza el 2,3 %, mientras que en el Sureste de Asia es del 0,5 %. En cuanto a la incidencia, se estima que cada año en el mundo ocurren 1,75 millones de infecciones nuevas (World Health Organization, 2017).
En Colombia no existe un programa de vigilancia epidemiológica activa, de manera que las cifras provienen de investigaciones en grupos poblacionales específicos que han permitido documentar que en pacientes en diálisis crónica la prevalencia es del 60,4 %, con trasplante de órganos del 49,5 %, en hemofílicos del 32,4 %, en pacientes con hepatopatías crónicas del 31 % (Botero et al., 1992) y en trabajadores del sector salud las cifras alcanzan el 1,6 % (Jaramillo et al., 1996).
Debido a que la frecuencia en grupos de riesgo no es buen indicador de la frecuencia en población general, en Colombia los estudios en donantes de sangre se han constituido en la mayor fuente de información para monitorear la prevalencia de VHC. En el año 1992 se hizo un estudio en Medellín en el que se halló una prevalencia de 0,97 % (Echavarría, 1992). En un estudio del mismo año en Cali se encontró una prevalencia de 0,45 % (Buelvas et al., 1992). En otra investigación del año 1996 en bancos de sangre de diez ciudades colombianas la prevalencia global fue del 0,39 %, con cifras más altas en Valledupar 0,77 % e inferiores en Manizales 0,50 % (Cortés y García, 1996). El estudio más reciente se realizó en Medellín e incluyó cifras desde el 2007 hasta el 2010, la prevalencia global hallada fue de 0,6 % (Patiño et al., 2012). Los estudios enunciados han aportado información relevante sobre la magnitud del evento; sin embargo, es necesario actualizarlos y ampliar el periodo de observación para dar cuenta de la evolución de la infección. Por ello, el objetivo de este estudio fue estimar la seroprevalencia del VHC en donantes de un banco de sangre de Colombia en el periodo 2005-2018 e identificar sus factores asociados.
MATERIALES Y MÉTODOS
Sujetos de estudio
La totalidad de donantes registrados en el banco de Sangre de la Escuela de Microbiología de la Universidad de Antioquia en Medellín-Colombia, desde el año 2005 hasta el primer semestre del año 2018, fue 166603. Se aplicaron los criterios de inclusión y autoexclusión de la guía nacional de donantes de sangre resolución nacional No 00901 de 1996 (República de Colombia. Ministerio de Salud Pública, 1996), además, de la fuente secundaria se excluyeron los donantes con información incompleta en los resultados de la infección por el VHC, la edad y el sexo.
Recolección de la información
Se utilizó una fuente de información secundaria consistente en los registros del banco de sangre consignados en el software "Hexabank" licencia 1.28.30.50, del cual se tomaron las variables de grupo etario (agrupado en 1840 y 41-65 años), sexo, lugar de captación (intramural o extramular), tipo de donación (altruista o de reposición), frecuencia de donación (primera vez, no repetitivo y repetitivo) y resultado de la infección por el VHC. El banco de sangre emplea la tecnología de Inmunoanálisis de micropartículas quimioluminiscentes (CMIA) para detección de anticuerpos virales, empleando el equipo Architect I2000 de la casa comercial Abbott, con sensibilidad del 99 % y especificidad de 96,4 % (Abbott laboratories, 2014).
Control de sesgos
Se realizó una exhaustiva aplicación de los criterios de selección de los donantes, control de calidad interno en las fases preanalítica, analítica y post-analítica del banco, el banco tiene controles de calidad internos y externos para todas las pruebas biológicas.
Análisis de la información
La descripción se realizó con frecuencias y para realizar las series de tiempo se determinó la seroprevalencia de infección en cada año de estudio con su intervalo de confianza del 95 %. En el análisis bivariado se estimó la seroprevalencia general del VHC y las frecuencias específicas según las variables independientes del estudio, además de razones de odds crudas y ajustadas (mediante regresión) para controlar efectos confusores en las asociaciones bivariadas. Finalmente, para determinar la fuerza de asociación de las variables independientes asociadas con la infección por el VHC, se realizó un modelo multivariado explicativo mediante regresión logística con el método intro, tomando como variables independientes únicamente las significativas en el modelo de ajuste (que representan relaciones reales, no confundidas). Los análisis se realizaron en SPSS 25.0® con significación del 0,05.
Aspectos éticos
Se aplicaron los principios de la Declaración de Helsinki, la Resolución 8430 del Ministerio de Salud de Colombia 1993 en la que clasifica como investigación sin riesgo, la Resolución 1995 de 1996 del Ministerio de salud sobre uso de datos de una historia clínica y se contó con aval del director del banco de sangre.
RESULTADOS
El 49,8 % (n = 82 902) fueron mujeres, el 72,0 % (n =119 929) personas con edad entre 18 - 40 años, 59,0 % (n = 98 272) captados de manera extramural (fuera de las instalaciones del banco de sangre), 65,4 % (n = 108 954) altruistas, 59,3 % (n = 98 837) de primera vez, 25,4 % (n = 42319) no repetitivos y 15,3 % (25 444) repetitivos.
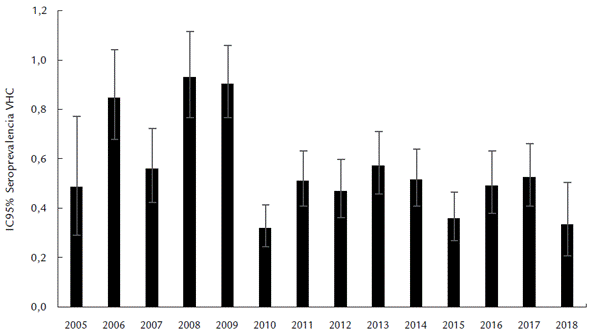
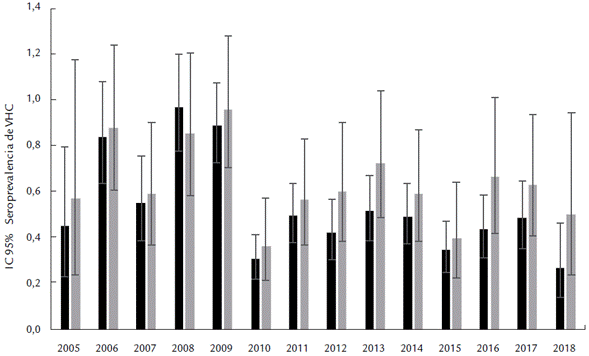
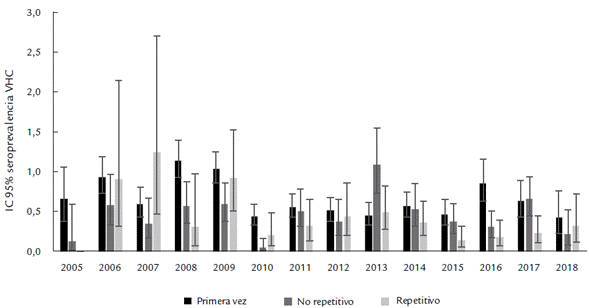
La seroprevalencia fue 0,567 % (IC 95 % = 0,531 - 0,604), siendo mayor en los años 2008 (0,938 %) y 2009 (0,912 %), y con una reducción para el periodo 2010-2018 en el cual las seroprevalencias oscilaron entre 0,32 % y 0,58 % (Figura 1). En las series de tiempo se halló una mayor ocurrencia de casos del VHC en los donantes mayores de 40 años (Figura 2) y en los de primera vez (Figura 3).
Al analizar toda la población, independiente del año de estudio, se presentaron diferencias estadísticas en la seroprevalencia del VHC según el grupo etario, el lugar de captación, el tipo de donación y la frecuencia de donación; luego de eliminar los efectos confusores solo fueron significativos el grupo etario y la frecuencia de donación.
Tabla 1 Seroprevalencias específicas del VHC según sexo, edad, captación, tipo y frecuencia de donación
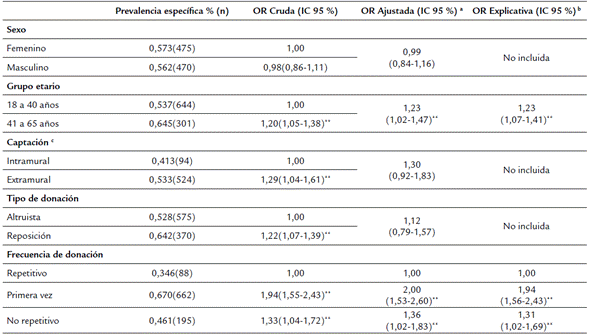
**p < 0,01. a Modelo de regresión logística de ajuste tomando como variables independientes el sexo, grupo etario, captación, tipo de donación y frecuencia de donación. b Modelo de regresión logística explicativa tomando como variables independientes al grupo etario y la frecuencia de donación. c El 27,3 % de los donantes no tienen la clasificación de la captación
La frecuencia de infección fue 23 % mayor en los donantes con edad mayor de 40 años (frente a las personas con edad entre 18 - 40), 31 % mayor en los no repetitivos y 94 % mayor en los de primera vez, en comparación con los repetitivos.
DISCUSIÓN
Este estudio puso de manifiesto que la seroprevalencia global de VHC en donantes de sangre fue 0,57 % (IC 95 %= 0,53 - 0,60), resultado similar a lo encontrado en un metaanálisis de donantes de sangre de Irán donde fue del 0,50 % (IC 95 % = 0,40 - 0,60 %) (Khodabandehloo et al., 2013) y superior a lo hallado en ciudades de Serbia con 0,19 % (IC 95 % = 0,14 - 0,24 %) (Mitrovic et al., 2015), Estados Unidos con 0,07 % (IC 95 % = 0,07 - 0,08) (Murphy et al., 2010), y fue menor a lo hallado en un estudio de México con 1,11% (IC 95% = 0,80-1,49) (Carreto-Vélez et al., 2003). La discrepancia entre los países puede atribuirse a la epidemiología de la infección en ellos, acceso al sistema de salud, el diagnóstico precoz y tratamiento oportuno de la infección, pero también a diferencias en los criterios de exclusión temporal de donantes que tienen los distintos bancos de sangre, criterios que pueden contribuir a aumentar o disminuir la probabilidad de encontrar un donante positivo (Goldman, 2013).
En el mismo sentido, es importante destacar que la seroprevalencia hallada en este estudio es inferior a la prevalencia estimada en el mundo 1,0 % (IC 95 % 0,80 - 1,10), pero estadísticamente igual a los datos estimados para la región de las Américas 0,7 % (IC 95 % 0,60 - 0,80) (World Health Organization, 2017). Los estudios de seroprevalencia en comparación con los de prevalencia tienen la desventaja de sobreestimar la frecuencia del evento al utilizar pruebas diagnósticas menos específicas que las confirmatorias; sin embargo, la prueba diagnóstica utilizada en esta investigación tiene una alta especificidad (96,4 %) lo que contribuye a explicar la similitud de los hallazgos con los estudios de prevalencia (Gupta et al., 2014). Además, el resultado pone de manifiesto que la frecuencia del evento en donantes de sangre es un buen indicador indirecto de la frecuencia del evento en población general.
Otro hallazgo relevante de la investigación fue la disminución de la seroprevalencia en el periodo 2010-2018. La disminución en la prevalencia del VHC es consistente con lo observado en otros estudios de donantes de sangre en los Estados Unidos y Canadá (Zou et al., 2004; O'Brien et al., 2008; Murphy et al., 2010). Una posible explicación a la seroprevalencia decreciente es que se está presentando un efecto de cohorte de nacimiento para la infección por VHC, es decir, los donantes nacidos desde finales de la década de 1940 hasta principios de la década de 1970 tuvieron mayor probabilidad de exposición a factores causales para la infección como transfusiones de sangre sin pruebas de tamización, uso de drogas inyectables con jeringas contaminadas y tatuajes con elementos no esterilizados; estos factores están progresivamente menos representados entre los donantes de sangre jóvenes. En adición a lo anterior, los datos que muestran una mayor ocurrencia de VHC en los donantes mayores de 40 años apoyan la hipótesis de un efecto de una cohorte de nacimiento. Otros autores que han sugerido una hipótesis de efecto de cohorte de nacimiento son Alter et al., (1999), Tanaka et al., (2004) y Murphy et al., (2010). La confirmación de un efecto de cohorte de nacimiento es importante, porque implica que la prevalencia del VHC en la ciudad probablemente continuará disminuyendo en las próximas décadas.
La mayor frecuencia de reactividad en donantes con edad superior a los 40 años supone que en ellos el diagnóstico se está realizando en etapas avanzadas de la infección. Desafortunadamente, el 75 - 80 % de los pacientes que contraen el virus de la hepatitis C son asintomáticos, lo que retrasa el diagnóstico y evita el tratamiento temprano. El tratamiento temprano es fundamental para evitar la progresión a cirrosis, trasplante hepático, carcinoma hepatocelular y muerte por lo que se sugiere implementar programas de tamización poblacionales. Estos programas podrían enfocarse inicialmente en la generación nacida a finales de la década de 1940 hasta principios de la década de 1970, porque en ella probablemente se manifestará el pico de incidencia de las consecuencias graves de la infección como cirrosis y carcinoma hepatocelular. Al respecto estudios previos han demostrado la costo-efectividad de este tipo de programas comparados con los costos y QALYS (Años de vida ajustados por calidad) asociados al diagnóstico tardío (McEwan et al., 2013).
En relación con la frecuencia de donación, esta investigación puso en evidencia que la seroprevalencia es mayor en los donantes de primera vez. Este hallazgo coincide con otros estudios en Estados Unidos (Glynn et al., 2000) y Cuba (Rivero, 2006). La mayor frecuencia de infecciones en los donantes de primera vez ha sido explicada porque los donantes repetitivos no solo deben negar las conductas de riesgo en la evaluación de pre-donación, sino que también deben haber dado negativo en las pruebas serológicas de su donación previa. Además, los donantes de primera vez generalmente son personas que acuden presionadas a efectuar la donación, con mayores factores de riesgo y en las que se detectan infecciones crónicas asintomáticas no diagnosticadas en sus chequeos médicos (Lieshout-Krikke et al., 2017). En este sentido, en algunos países se ha propuesto incentivar la donación voluntaria habitual y reducir de manera gradual los donantes de reposición o familiares (Rivero, 2006).
Entre las limitaciones de este estudio se encuentra que los análisis estadísticos realizados no presentan carácter confirmatorio sino de exploración de factores que podrían modificar la seroprevalencia, de la misma manera, esta seroprevalencia demuestra el nivel de exposición al virus, pero la prevalencia de infección activa puede ser menor, por lo que estudios posteriores deberían incluir la tamización de anti-core con el fin de mejorar la información epidemiológica de infecciones activas y pasadas, así como el mejoramiento de decisiones clínicas. Finalmente, la extrapolación de los resultados a población general debe tener en cuenta que los donantes de sangre son una población menos expuesta porque pasaron por un sistema de selección en el que se difieren las personas con ciertos factores de riesgo.
CONCLUSIONES
Se concluye que en Medellín-Colombia los niveles endémicos del VHC han sido estables y bajos en la última década, evidenciando la importancia de la vigilancia epidemiológica que realizan los bancos de sangre. La menor prevalencia en la última década hace suponer un efecto de cohorte de nacimiento que debe ser estudiada en investigaciones posteriores.