INTRODUCCIÓN
La malaria congénita es ocasionada por la transmisión transplacentaria de eritrocitos maternos parasitados con Plasmdiumfigura 1 o por contagio perinatal, cuando hay presencia del patógeno en cordón umbilical del neonato al momento del parto o en sangre periférica en los 30 días posteriores al mismo 1, 2. Los recién nacidos con esta condición en un 80 % pueden presentar fiebre, anemia y esplenomegalia. Otros signos y síntomas incluyen hepatomegalia, ictericia, irritabilidad, regurgitación, trastornos respiratorios, heces blandas y mala alimentación. Normalmente, los síntomas ocurren entre 10 y 30 días después del parto.
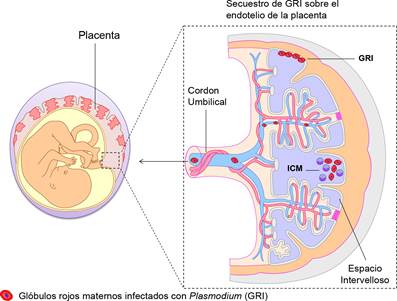
Fuente: propia de autores.
Figura 1 Mecanismo de la malaria congénita. La malaria congénita es ocasionada por la transmisión transplacentaria de formas asexuales del Plasmdium durante el embarazo. La infección de la placenta se acompaña de infiltrados intervellosos de células mononucleares (ICM), los cuales originan cambios patológicos en los trofoblastos, que facilitan la entrada transplacentaria de eritrocitos infectados al feto.
La transmisión congénita de especies de Plasmodium, principalmente de falciparum y vivax, se ha documentado por muchos años como un evento poco frecuente tanto en zonas endémicas como no endémicas. Hasta el momento se han publicado 300 casos esporádicos en la literatura 3, 4.
En este artículo se reporta el caso de un neonato con malaria congénita por P. vivax, teniendo como objetivo alertar al cuerpo médico sobre la importancia de establecer el diagnóstico oportuno en estos pacientes con el fin de ofrecer un manejo adecuado y eficaz tratamiento.
DESCRIPCIÓN DEL CASO CLÍNICO
Se presenta el caso clínico de una neonata de 25 días de nacida, sexo femenino y procedente de una zona de Bazurto, en Cartagena de indias (Colombia). Fue ingresada al Hospital por presentar cuadro febril 3 días de evolución. Además, se reportó ictericia desde el nacimiento, razón por la cual estuvo hospitalizada toda la primera semana de vida, dándose de alta por mejoría clínica. Pero la ictericia persiste, incluso presentó un incremento notario 3 días antes del reingreso. Antecedentes familiares: madre multigestante de 16 años, natural de Bosconia (municipio de Cesar-Colombia), trabajadora sexual, residente en el mercado de Bazurto de Cartagena de Indias (Colombia).
Al ingreso la recién nacida presentaba aspecto general muy regular. Activa, reactiva y de llanto fuerte. Con una T: 38.5 ºC, FC: 144 x min, FR: 68 x min y peso de 3.000 g. El examen físico reveló hepatoesplenomegalia figura 2. Los datos de laboratorio: anemia marcada, hiperbilirrubinemia y aumento de la PCR indicaron un proceso inflamatorio agudo tabla 1. Las impresiones diagnósticas iniciales se orientaron a una sepsis neonatal tardía y sospecha de infección por Torch, por lo cual se inició tratamiento con antibióticos, lactancia mater- na a libre demanda y líquidos endovenosos. Al segundo día, se decidió transfundir 30 cc de glóbulos rojos empacados.

Fuente: propia de autores.
Figura 2 Paciente con malaria congénita. Imagen del abdomen de la paciente mostrando hepatoesplenomegalia. Abdomen blando, depresible, hígado palpable 4 cm por debajo del reborde costal derecho y bazo palpable 2 cm por debajo de reborde costal izquierdo.
Tabla 1 Pruebas de Laboratorio de la neonata a los 25 días de nacida en el momento del ingreso hospitalario
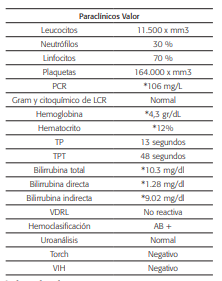
*valores alterados
PCR: proteína C reactiva. TP: Tiempo de protrombina. TPT: Tiempo parcial de tromboplastina parcial. Torch: IgG e IgM para toxoplasma, rubéola, citomegalovirus, herpes virus. VIH: Elisa para el virus de la inmunodeficiencia Humana.
Al cuarto día: paciente afebril, sin cambios en el examen físico. Resultados del extendido de sangre periférica mostraron la presencia de glóbulos rojos con hipocromía moderada, anisocitosis moderada, microcitosis. Glóbulos blancos y plaquetas normales en número y morfología. De forma incidental, se observaron trofozoítos de P. vivax. Se realizó gota gruesa encontrándose una parasitemia de 3500 parásitos/µl de sangre. La madre fue interrogada nuevamente refiriendo haber vivido los primeros 7 meses de su embarazo en Tierralta, Córdoba (Colombia), con antecedente de malaria al 4.º mes de embarazo. Con el diagnóstico: malaria congénita, se suspende la terapia antibiótica y se inicia tratamiento con cloroquina, la primera dosis 10 mg/kg; a las 8 horas 5 mg/kg; a las 24 horas 5 mg/kg; a las 40 horas 5 mg/kg. La prueba de gota gruesa resultó negativa al noveno día del ingreso.
Una semana después del tratamiento antimalárico, la recuperación fue completa: afebril, sin ictericia, cardiopulmonar normal, abdomen con hígado palpable 1 cm por debajo del reborde costal derecho y bazo no palpable.
DISCUSIÓN
La rareza de la transmisión congénita se atribuye a la efectividad de la placenta como una barrera a los glóbulos rojos maternos infectados 1, 5, a la transferencia pasiva de anticuerpos maternos y al efecto protector de la hemoglobina fetal (HbF) 1, 6, 7. Sin embargo, reportes recientes sugieren que la malaria congénita no es tan rara entre los recién nacidos como se pensaba anteriormente y que la enfermedad puede pasar sin diagnosticar durante un largo período en un bebé enfermo 1, 2, 8.
En Colombia, solo 12 casos se habían reportados antes de 1986. Existe un reporte entre 2002-2004 en el Urabá antioqueño, donde se encontraron cinco casos de malaria neonatal, todos por P. vivax9, 10. En otro estudio publicado en el 2011, se encontró una prevalencia de malaria congénita de 4,3 % entre los recién nacidos de madres con malaria gestacional en la región de Urabá (Colombia) 10, lo cual podría sugerir una tasa alta de frecuencia en los recién nacidos de madres que han tenido malaria durante el embarazo en regiones endémicas en Colombia. No obstante, otro estudio realizado en la misma zona en el 2013 arrojó una baja prevalencia para malaria congénita 11.
Los neonatos generalmente cursan con características clínicas inespecíficas como cuadros febriles, irritabilidad, anemia, etc., los cuales sugieren diagnósticos diferenciales con enfermedades febriles del recién nacido, en este con caso sepsis neonatal; aun así se debe tener en cuenta la presencia de hepatoesplenomegalia e ictericia, que son más indicativos de malaria 12-14.
Así mismo se hace necesario correlacionar la historia clínica y buena anamnesis de la madre, que para el presente reporte refirió haber vivido en zona endémica y presentar antecedentes de malaria en su cuarto mes de embarazo. Lo anterior, podría indicar que la paciente no fue tratada adecuadamente, por lo que persistieron formas latentes del parásito (hipnozoítos) que contagiaron al neonato 15-17.
Por otra parte, la gota gruesa y el frotis de sangre periférica continúan siendo las herramientas principales para el diagnóstico de malaria; sin embargo, requieren de una sospecha clínica de la enfermedad y de la experiencia del microscopista para un diagnóstico oportuno y acertado.
El tratamiento para la malaria congénita aun cuando no cuenta con evidencia suficiente para establecer un tratamiento ideal, el uso de un esquizonticida como cloroquina, en caso de infección por P. vivax, ha mostrado resultados satisfactorios. Por el contrario, se sugiere in- necesaria la aplicación de primaquina, puesto que en estos casos no se realiza ciclo hepático debido a la inmadurez fisiológica (hígado) del neonato 1, 18-20.














