INTRODUCCIÓN
Por muchos años, el hidróxido de calcio ha sido el material estándar utilizado en el mantenimiento de la vitalidad de la pulpa dental. La percepción de que la pulpa dental podía ser reparada como cualquier otro órgano del cuerpo mientras no estuviera sometida a condiciones irritantes llevó en 1930 a Hermann 1 a proponer el hidróxido de calcio como material para la protección directa de la pulpa. La estimulación en la formación de una dentina reparadora en contacto con el tejido pulpar vital avaló la utilización del hidróxido de calcio en los recubrimientos pulpares directo e indirecto. Sin embargo, los problemas de adhesión a la superficie dentinal, reabsorción del material y su inestabilidad mecánica fueron responsable de una microfiltración que parece ser responsable de la pérdida la vitalidad pulpar del diente 2,3.
En 1993, Torabinejad et al. 4 desarrollaron el agregado de trióxido mineral (MTA, en inglés), material empleado inicialmente en casos de perforaciones radiculares pero posteriormente utilizado en el recubrimiento pulpar directo, procesos de apexificación y como material de relleno temporal. Los resultados clínicos en la resolución de lesiones periapicales permitieron que este producto se posicionara como la primera opción de tratamiento en muchos procedimientos quirúrgicos y no quirúrgicos a nivel bucal. A pesar de la eficacia del MTA, este material tiene como desventaja el largo tiempo de fraguado, alto costo y difícil manipulación 5,6. Para superar los problemas del hidróxido de calcio y el MTA, desde 2010 se comercializa un nuevo biomaterial denominado biodentine 7.
La biodentine es un cemento biológicamente activo a base de silicato de calcio que se ha presentado como un sustituto de la dentina. Dadas sus características físico-químicas, biocompatibilidad y facilidad de manipulación, la biodentine tiene una amplia gama de aplicaciones que comprende los procedimientos clásicos de endodoncia, recubrimiento pulpar directo e indirecto y los casos clínicos restaurativos donde se desea 'reemplazar la dentina'.
Este artículo de revisión tiene como objetivo proporcionar un análisis detallado de las propiedades fisicoquímicas, biológicas y las principales aplicaciones clínicas de la biodentine.
MATERIALES Y MÉTODOS
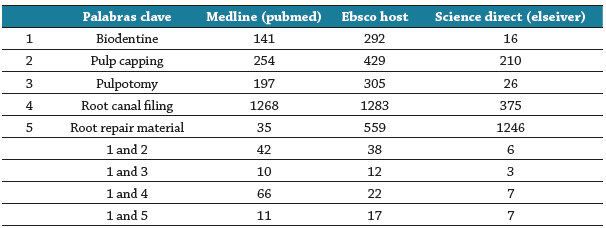
Se realizó una búsqueda electrónica de literatura en las bases de datos Medline (Pubmed), EBS-CO-Host y Science direct (Elsevier) desde 2012 hasta la última semana de julio de 2020, utilizando como palabras clave Biodentine, Pulp capping, Pulpotomy, Root canal filing y Root repair material. Se encontraron artículos evidenciables, con alto niveles de verificación que clasificaron con el tema de estudio. Para refinar la búsqueda se tuvieron en cuenta estudios in vivo / in vitro, textos completos, textos en PDF, artículos en inglés y los conectores booleanos "AND y OR". No se utilizó restricciones por edad ni sexo. Se excluyeron revisiones narrativas, cartas al director, tesis, periódicos, conferencias, noticias, comentarios y editoriales. Finalmente, se procedió a realizar un tamizaje con aplicación de criterios a los artículos hallados en las bases de datos y se seleccionaron 168, de los cuales 46 cumplieron con los requisitos de inclusión, y posteriormente fueron analizados y discutidos (tabla 1).
RESULTADOS Y DISCUSIÓN
Composición química de la biodentine
La biodentine (Septodont, Saint Maur des Fossés, France) se encuentra disponible en forma de cápsula que contiene la proporción ideal polvo-liquido. El componente en polvo consiste en silicato tricálcico (3CaO.SiO), silicato dicálcico (2CaO.SiO2), carbonato de calcio (CaCO2), dióxido de Zirconio (ZrO2) y óxido de hierro. El silicato tricálcico, principal componente del polvo, y el silicato dicálcico son los componentes responsables de regular la reacción de fraguado. El carbonato de calcio es un material de relleno, en tanto que el óxido de zirconio le confiere el carácter de radio-pacidad a la biodentine. El componente líquido contiene cloruro de calcio (CaCl2), que actúa como un acelerador, al tiempo que un polímero hidrosoluble disminuye la viscosidad del cemento y permite reducir la cantidad de agua requerida en la mezcla y contribuyendo así a su fácil manipulación 7. Durante la mezcla, las partículas de silicato de calcio de la biodentine reaccionan con el agua a pH alto en una solución que contiene Ca2+, OH- e iones de silicato. El cemento tiene un tiempo de fraguado inicial superior a 6 minutos y un tiempo de fraguado final de 10-12 minutos. En comparación con los ionómero de vidrio y el MTA, la biodentine muestra una mejoría en el tiempo de fraguado gracias al aumento de tamaño de la partícula, la adición de cloruro de calcio como vehículo de la reacción y la disminución del contenido liquido 7. Camilleri et al. 8 en una investigación sobre la hidratación y bioactividad de la biodentine y el MTA constataron que el cemento no deshidratado de la biodentine corresponde a un silicato tricálcico, mientras que el MTA presenta un silicato monocálcico. Según los autores, la diferencia de composición en el cemento no deshidratado junto al tamaño del área de supericie de las partículas de silicato tricálcico en la Biodentine (2.811 m2/g) y del MTA (1,0335 m2/g) son factores fisicoquímicos determinantes que permiten una actividad biológica más importante de la biodentine en los tejidos dentales. La tabla 2 resume los componentes y su concentración en la biodentine.
Porosidad e interface material-dentina
Dada la indicación de la biodentine en los procesos de reparación de perforaciones; y tratamientos de pulpa vitales, en los que es obligatorio un sellado hermético, el grado de porosidad de un material es un factor crítico que determina el nivel de filtración y, en consecuencia, el éxito del tratamiento realizado. De Souza et al. 9 compararon la biodentine con otros cementos de silicato cálcico de uso endodóntico. Los resultados indicaron que la biodentine presentó una porosidad mayor que el MTA (7.09 % versus 6.63 %). En consecuencia, los autores mencionaron que los resultados pueden ser consecuencia del bajo contenido de agua en la etapa de mezclado que presenta la biodentine.
Un estudio reportado por Camilleri et al. 8 evaluó también la porosidad de la biodentine en la interfase dentina-raíz en dientes humanos extraídos y sometidos 28 días a condiciones ambientales secas y húmeda. De acuerdo con los resultados, la biodentine exhibió un nivel bajo en su grado de porosidad, en ambas condiciones. Sin embargo, los cambios en la microestructura observadas en la dentina permitieron el paso de microesferas fluorescentes que potencialmente pudiesen permitir la entrada y transmisión de microorganismos. Mientras que Radwan et al. 10 estudiaron la influencia del uso de fluido corporal simulado como medio de curado y su impacto en las propiedades fisicomecánicas de biocementos de silicato tricálcico experimental y la biodentine. Los análisis por microscopia electrónica de barrido revelaron una adaptación confiable de ambos biocementos. Estos resultados, de acuerdo con los investigadores, son producto de la capacidad que poseen estos cementos de formar cristales de hidroxiapatita. Por su parte, Atmeh et al. 11 investigaron sobre las propiedades de la biodentine y el cemento de ionómero de vidrio sobre la dentina. Los resultados señalaron que la biodentine crea una zona de infiltración mineral donde el efecto cáustico alcalino de los productos de hidratación del cemento de silicato cálcico degrada el colágeno de la dentina. Esta degradación conduce a la formación de una estructura porosa que facilita la penetración de altas concentraciones de iones de Ca (2+), OH (-) y CO (3) (2-) y un aumento de la mineralización en esta zona.
Adaptación marginal y capacidad de sellado
La adhesión micromecánica de la biodentine le permite obtener una óptima adaptabilidad a la dentina subyacente 12. Son escasos los estudios que han expuesto la adaptación marginal y la capacidad de sellado de la biodentine, sin embargo, un estudio in vitro realizado por McMichael et al. 13 se comparó la resistencia microtensil de resinas cuando se emplea con cementos de silicato de calcio y cemento de ionómero de vidrio. Constataron que no hubo diferencia signiicativa entre el efecto del envejecimiento de enlaces sobre la resistencia microtensil de la biodentine y el MTA. Este resultado significa que la unión resina-biodentine no se deterioró con el tiempo, por lo menos durante el periodo del estudio (1 mes).
Resistencia mecánica
Según la información suministrada por el fabricante, la biodentine presenta una resistencia a la compresión que puede llegar a alcanzar un rango similar con la dentina. Su resistencia a la compresión comprende un rango de hasta 100 megapascal (MPa) la primera hora luego de su aplicación y hasta 200 MPa 24 horas después de su aplicación, pudiendo continuar su mejoría hasta alcanzar 300 MPa posterior a un mes, valor comparable a la resistencia a la comprensión de la dentina natural, que es de 297 MPa 7. En estudios realizados por Grech et al. 14 se evidencia que la biodentine presenta una resistencia a la compresión más alta cuando se le comparó con el Bioaggregate. Los autores señalan que la mayor resistencia de la biodentine se debe a la utilización del polímero hidrosoluble que permite reducir la relación agua/cemento utilizada en su preparación.
Al mismo tiempo, se ha reportado que la resistencia a la flexión de la biodentine, que permite disminuir el riesgo a la fractura de este material, es de 34 MPa dos horas después de haber sido aplicada 7.
Microdureza
La microdureza de la biodentine es de 51 VHN (Vickers Hardness Number) a las 2 horas y de 69 VHN después de un mes 7. Los valores de microdureza de referencia para la dentina natural se sitúan en el rango de 60-90 VHN. Estos valores son comparables a los reportados por Camilleri et al. 8, quienes en un estudio compararon las propiedades físicas de biodentine con un ionómero de vidrio convencional (Fuji IX) y un ionómero de vidrio modificado con resina (Vitrebond), reportando una microdureza superior de la biodentine. Por su parte, Grech et al. 14 también evidenciaron que la biodentine muestra un valor superior de microdureza en comparación con Bioaggregate y IRM©.
Radiopacidad
En la biodentine, el material que le confiere la propiedad de radiopacidad es el óxido de zirconio. Este material biocompatible, con propiedades mecánicas y de resistencia favorable a la corrosión, le confiere una radiopacidad de 3 mm de aluminio a la biodentine, según estudios realizados por Grech et al 14. Sin embargo, un trabajo realizado por Ochoa-Rodríguez et al. 15 evidenció valores importantes de radiopacidad en términos de absorbancia y de escala de grises respecto a otros materiales, pero sin alcanzar el mínimo de 3 mm recomendado.
Solubilidad
Escasos estudios exhiben los valores de solubilidad de la biodentine. Un estudio registró que la biodentine presenta la captación de fluidos más baja (p = 0.228, 0.188, 0.238, 0.153, 0.143 para 1, 7, 14, 21 y 28 días, respectivamente) en comparación con el cemento de silicato tricálcico (Mineral Research Processing, Meyzieu, Francia) reemplazado con 20 % de óxido de zirconio y el Bioaggregate (Verio Dental Co. Ltd., Vancouver, Canadá). Sin embargo, este estudio también reportó que la solubilidad de la biodentine fue similar a un material de restauración intermedio IRM© (Dentsply DeTrey, Konstanz, Alemania) utilizado como control. Estos resultados ponen en evidencia la estabilidad dimensional que presenta la biodentine 14.
Microfiltración
La liberación de iones de calcio y del silicato de calcio por parte de la biodentine estimula la mineralización al permitir la creación de una zona de infiltración mineral en la interfase cemento-dentina. Mousavi et al. 16 reportaron en una evaluación In vitro valores de microfiltración sellado muy similares entre el MTA, biodentine y OthoMTA. Por su parte, Samuel et al. 17 compararon la capacidad de sellado del MTA y biodentine en preparaciones de furcas en molares primarios por microscopia electrónica de barrido. Los resultados indicaron que la Biodentine presentó menos iltraciones en comparación con el MTA. Niranjan et al. 18 reportaron que la biodentine exhibe una adaptación y sellado marginal superiores a los encontrados en restauraciones tratadas con MTA. Contrariamente, Ozbay et al. (19) mediante el método de filtrado de fluidos observaron una menor microiltración cuando utilizaron el MTA frente a la utilización de la biodentine.
Fuerza de adhesión
Hashem et al. 20 en un estudio sobre las características físicas de los silicatos de calcio constataron que la biodentine exhibía baja resistencia durante las etapas iniciales de fraguado. En consecuencia, para lograr una fuerza de adherencia adecuada, la realización de la restauración final en resina compuesta es recomendada realizarse dos semanas después de utilizar la biodentine. Prasanthi et al. 21 evaluaron la fuerza de adherencia de la biodentine y el MTA frente a agentes quelantes. Los resultados mostraron que la biodentine tuvo una fuerza de unión de expulsión significativamente mayor que el MTA. Estos resultados coinciden con Ózyurek et al. 22, quienes compararon la resistencia de adhesión del MTA y la biodentine, confirmando una mejor fuerza de adhesión por parte de la biodentine.
Decoloración
En un estudio in vitro, Palma et al. 23 evaluaron la estabilidad del color de la biodentine y MTA, y concluyeron que después de 6 meses, la biodentine exhibía una estabilidad de color superior al MTA. Basados en esos resultados, los autores sugirieron que la biodentine podría servir como una alternativa para el uso de materiales y procedimientos de endodoncia regenerativa.
Actividad antibacteriana y antifúngica
La capacidad antibacteriana y antifúngica de la biodentine es atribuible a su alcalinidad; dado su alto pH, este material inhibe el crecimiento bacteriano y desinfecta la dentina. Bhavana et al. 24 evaluaron las características antibacterianas y antifúngicas de la biodentine, MTA y el cemento de ionómero de vidrio, y llegaron a la conclusión que la biodentine presenta una acción antimicrobiana superior al MTA y al ionómero de vidrio. Por su parte, Hiremath et al. 25 y Hiremath et al. 26 en dos experimentos independientes constataron que la biodentine muestra un efecto antimicrobiano significativo contra los Enterococcus faecalis, mientras que el MTA demostró ser un buen agente contra la Candida albicans.
Biocompatibilidad
Varios estudios han reportado la biocompatibilidad de la biodentine. Ghilotti et al. 27 compararon la biocompatibilidad de la biodentine versus el MTA y Bio-C Repair sobre células de la pulpa dental humana, y observaron que el grupo de la biodentine sin diluir mostró una mayor viabilidad en comparación con las células del grupo control. Por su parte, Abuarqoub et al. 28 investigaron la concentración optima de biodentine compatible con células madre derivadas del ligamento periodontal (hPDLSC), y determinaron que hubo un aumento signiicativo en la proliferación de hPDLSC a bajas concentraciones de biodentine (2 mg/mL). Esta misma concentración de biodentine registró un aumento signiicativo en la migración, adhesión y mineralización de las células en cultivo.
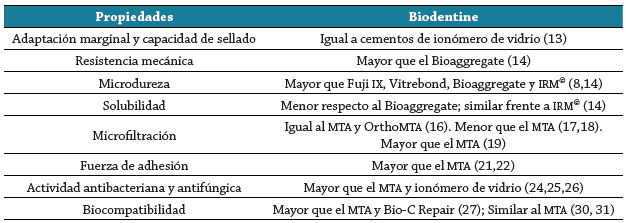
Otro estudio realizado por Jung et al. 29 investigó los efectos biológicos de la biodentine durante o después del fraguado en células madre de dientes deciduos humanos (SHED). El estudio demostró que la biodentine en el grupo celular 'durante el fraguado' indujo una diferenciación odontogénica importante en comparación con el grupo control. Todo indica que la biodentine es un biomaterial diferenciador de odontoblastos con potencial en la regeneración del tejido dental. Corral Núñez et al. 30 evaluaron también la viabilidad celular y la expresión de ARN mensajero de la interleucina IL-1 α e IL-6 en células de ibroblastos 3T3 cuando están en contacto directo con la biodentine y el MTA, y encontraron que estas células en contacto con ambos materiales odontológicos muestran un patrón similar de viabilidad, a excepción de las primeras horas de cultivo. La expresión del ARN mensajero de la IL-1α e IL-6 fue también muy similar entre la biodentine y el MTA en contacto con las células fibroblásticas. Por su parte, Scelza et al. 31 observaron la citocompatibilidad in vitro de los osteoblastos humanos en contacto con la biodentine y el MTA durante 42 días en cultivo celular. El análisis simultáneo de la actividad mitocondrial, integridad de la membrana y densidad celular permitió concluir que la biodentine es biocompatible con los osteoblastos humanos, lo cual valida su utilización en contacto directo con los tejidos óseos. La tabla 3 resume las propiedades de la biodentine en comparación con otros materiales dentales de acuerdo con la revisión bibliográica analizada en este trabajo.
Usos clínicos de biodentine
Recubrimiento pulpar
Una evaluación de la capacidad de la Biodentine en la inducción de la dentina reparativa fue realizada por Laurent et al. 32, y constataron que este material bioactivo induce la formación de focos de mineralización en forma de osteodentina gracias a una probable modulación de la secreción de TGF-β1 de las células pulpares. Diversos reportes bibliográficos muestran que la biodentine contribuye a preservar y mantener la vitalidad dental, y contribuye a una tasa de éxito importante en los tratamientos de recubrimientos pulpares directo e indirecto 33,34,35. En molares libres de caries programados para extracción por razones ortodonticas, Nowicka et al. 34 sometieron estos dientes a una exposición pulpar y luego fueron tratados con biodentine. El análisis histológico de la mayoría de los dientes presentaba una formación completa del puente dentinario y ausencia de respuesta inflamatoria pulpar. Así mismo, Brizuela et al. 35 a través de un ensayo clínico aleatorizado de 169 pacientes con dientes permanentes cariado y exposición pulpar pusieron en evidencia que la biodentine presenta una tasa de éxito superior respecto al hidróxido de calcio hasta un año después de ser utilizado en el recubrimiento pulpar directo. Estos autores mencionaron que la biodentine es un material adecuado para reemplazar el hidróxido de calcio; sin embargo, su éxito clínico no fue estadísticamente significativo al ser comparado con los dientes tratados con MTA. Por su parte, Katge et al. 36 en una comparación de la tasa de éxito del tratamiento con la biodentine y MTA en el recubrimiento pulpar directo de molares permanentes en niños de 7 a 9 años reportaron una tasa de éxito del 100 % cuando se utilizó la biodentine y el MTA hasta 12 meses después del tratamiento.
Jalan et al. 37) compararon la respuesta de la pulpa dental humana al hidróxido de calcio y biodentine en cuarenta premolares humanos permanentes. Los resultados indicaron que los puentes dentinarios hallados en los dientes en los que se utilizó la biodentine fueron significativamente más gruesos, continuos y se observaba un menor grado de inflamación pulpar en comparación con los dientes tratados con hidróxido de calcio. Los autores de este estudio sugieren que la biodentine puede ser usada en el recubrimiento pulpar directo en lugar del hidróxido de calcio. Garrocho-Rangel et al. 38 evaluaron los resultados clínicos y radiográficos de la biodentine y un revestimiento basado en hidróxido de calcio en el tratamiento indirecto de la pulpa de 80 niños con molares primarios vitales y lesiones cariosas profundas. Los resultados resaltaron que la biodentine presenta una tasa de éxito clínico y radiográfico de 98,3 % comparada con la tasa de éxito del hidróxido de calcio, que fue de 95 %. En consecuencia, este estudio recomienda que la biodentine puede ser utilizado en el tratamiento de dientes primarios profundamente cariados sin síntomas degenerativos. Así mismo, Hegde et al. 39 en una evaluación de la respuesta clínica del complejo pulpo-dentinal después de un recubrimiento pulpar directo en 24 molares permanentes con exposición cariosa y sin síntomas de pulpitis irreversible utilizando MTA y Biodentine, reportaron que la biodentine presenta una tasa de éxito de 83.3 % versus 91.7% del MTA. En efecto, aunque la biodentine mostró una tasa de éxito inferior al MTA, los autores maniiestan que es posible la utilización de la biodentine en casos de una pulpitis reversible.
Pulpotomía
En los casos de exposición pulpar profunda, en los que la pulpotomía fue el procedimiento más indicado, diversos estudios clínicos reportan haber utilizado la biodentine como opción de tratamiento. Sirohi et al. 40 compararon las tasas de éxito clínico y radiográfico de sulfato férrico (FS) y la biodentine en la pulpotomía de molares primarios durante 9 meses. Los resultados indicaron que el grupo de dientes tratados con la biodentine presentó una tasa de éxito clínico del 100 % y radiográfico del 92 %, mientras que el grupo tratado con FS obtuvo un 96 y 84 % de éxito clínico y radiográfico, respectivamente. Este estudio concluye diciendo que la biodentine puede ser utilizado como agente para los procedimientos de pulpotomía. En otro estudio, Bakhtiar et al. 41 investigaron la eficacia clínica de TheraCal en comparación con la biodentine y el MTA cuando son aplicados directamente sobre la pulpa dental durante pulpotomías parciales. Los resultados indicaron que los pacientes tratados con la biodentine y el MTA no presentaron sensibilidad al calor, frío o palpación, mientras que el grupo tratado con TheraCal manifestó un dolor significativo en una semana. Igualmente, se observó una formación completa de puente dentinario en todos los dientes tratados con la biodentine. En conclusión, el estudio sugiere la utilización de la biodentine y MTA en la pulpotomía parcial.
Juneja et al. 42 también demostraron que los dientes tratados la biodentine y MTA son clínica y radiográicamente exitosos después de 18 meses en comparación con los tratados con Formocre-sol en pulpotomía realizadas a 51 molares de dientes primarios en pacientes entre 5 y 9 años de edad. Por su parte, Villat et al. 43 describieron el manejo inmediato y seguimiento realizado en una lesión cariosa extensa de un segundo premolar mandibular derecho inmaduro tratado con la biodentine. Después de 6 meses del tratamiento se informó que el diente era vital y con respuestas normales a las pruebas térmicas. El examen radiográfico indicó la formación del puente denti-nario en la cámara pulpar y la formación continua de la raíz. En este caso clínico se demuestra la biocompatibilidad de la biodentine con la pulpa dental y la dentina de la raíz.
Apexificación
La biodentine también ha resultado exitosa en los tratamientos de apexificación. Elumalai et al. 44 describieron el tratamiento de los ápices abiertos de un paciente con sintomatología dolorosa y secreción de material purulento de 3 meses de evolución en los incisivos centrales superiores. El tratamiento consistió en la utilización de MTA y biodentine con el objetivo de formar una barrera apical. Los resultados indicaron que ambos materiales dentales bioactivos se pueden utilizar de forma exitosa en el cierre del extremo de la raíz de ápices abiertos. Sin embargo, los autores concluyen que la biodentine tiene un mejor efecto a largo plazo en comparación con el MTA. Recientemente, Sharma et al. 45 decribieron el tratamiento con biodentine y fibrina rica en plaquetas en tres pacientes no relacionados que presentaban ápices abiertos y lesiones periapicales/quísticas de manera concomitante. En los 3 casos, los resultados clínico-radiográicos fueron considerados altamente satisfactorio gracias a la formación del tapón apical y la cicatrización ósea periapical. Los autores indican que el éxito del tratamiento se debió a que la biodentine proporciona una buena adhesión y sellado con la dentina mediante la deposición de cristales de hidroxiapatita en la interfase material-dentina.
Otros usos clínicos de la biodentine
En la literatura se reporta que la biodentine ha sido utilizada igualmente en defectos de resorción, obturación del espacio pulpar, fractura vertical de la raíz, lesiones periapicales, restauraciones de clase II, lesiones de furca, necrosis pulpar, reimplante dental y endodoncia regenerativa 15, 46-50.
CONCLUSIÓN
La manipulación relativamente fácil, el bajo costo, su alta biocompatibilidad y la excelente bioactividad hace de la biodentine un material de gran utilidad a nivel odontológico. La biodentine parece poseer una resistencia a la compresión y flexión superior al MTA. De acuerdo con los estudios actuales sobre la biodentine, es difícil afirmar que este material sea un verdadero sustituto de la dentina; sin embargo, por los aspectos fisicoquímicos y biológicos descritos en este trabajo, la biodentine es hasta hoy un material altamente recomendado en la práctica odontológica.