Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.26 no.1 Bogotá Jan./Apr. 2006
Francisco J. Sánchez C.,1 Carlos Cesteros,2 e Issa A. Katime3
1 Dr. Sc. Profesor en el Departamento de Ingeniería Química, Universidad Nacional de Colombia, Bogotá, D.C. frasaca@hotmail.com
2 Departamento de Química Física, Grupo de Nuevos Materiales, Universidad del País Vasco, Bilbao.
3 Departamento de Química Física, Grupo de Nuevos Materiales, Universidad del País Vasco, Bilbao.
RESUMEN
Se empleó un reactor batch (por lotes), dotado de tres detectores: pH, Sonda IR y operación en continuo, de tal forma que puede operarse como un reactor CSTR. En la medida en que la esterificación procede, decrecen las bandas correspondientes al grupo –COOH del ácido carboxílico y la del grupo C-OH del alcohol, presentándose al mismo tiempo incremento en la banda del grupo –COOR del éster que se está formando. El progreso de la reacción se puede seguir por el registro continuo de los espectro IR. La banda correspondiente a H-O-H del agua no se puede seguir ya que se requiere de un ambiente absolutamente anhidro para hacerlo. De otro lado, por aparte pueden prepararse soluciones patrones para poder cuantificar la intensidad de los picos en el espectro IR, según la composición del componente en la mezcla. Sin embargo, cuando se presentan cambios de fase en la mezcla reactiva, este método no puede emplearse para seguir el curso de una reacción, ya que se presenta una variación muy aleatoria en la señal de intensidad de los picos.
Palabras clave: esterificación, ácidos grasos, sonda Infrarroja.
ABSTRACT
A batch reactor was employed having pH meter, IR probe and continuous operation detectors so that it could work as a CSTR reactor. As esterification advanced, then IR bands corresponding to the carboxyl acid COOH group and the alcohol C-OH group decreased whilst a parallel increase was presented in the ester –COOR group band which was forming. Reaction progress could be observed by continuous IR spectrum registration. The IR band for HOH (water) could not be studied because it needed a completely anhydrous medium for doing so. Standard solutions could be prepared for quantifying IR band peak intensity, according to a component’s composition in the mixture. However, when phase changes occurred in the reaction mixture, this method could not be employed for following the course of a particular reaction because random variation was detected in band intensity.
Keywords: esterification, fatty acids, IR probe.
Recibido: agosto 9 de 2005
Aceptado: diciembre 28 de 2005
Introducción
En la reacción de esterificación se produce agua. En un reactor batch, si el agua no se retira por decantación o destilación, quedará disuelta en la mezcla reactiva, permitiendo el avance de la reacción solamente hasta su punto de equilibrio (Groggins, 1958). La adición de un adsorbente para el agua al medio de reacción puede causar el desplazamiento de la reacción beneficiando la formación de éster. Este adsorbente puede ser tamiz molecular o un hidrogel. Para lograr un buen efecto sobre el proceso, la velocidad de adsorción de agua por parte del aditivo, ha de ser similar o superior a la velocidad de formación de agua en la reacción (Machado y López, 1993).
El mecanismo de la esterificación ya ha sido planteado (Sánchez y Rodríguez, 1996; Morrison y Boyd, 1987; Vogel’s Textbook of practical organic chemistry, 1999). Primero se protona el grupo carboxilo, por el catalizador ácido, y luego reacciona con el grupo hidroxilo del alcohol. En el caso de los hidrogeles, la capacidad de adsorción de agua no es buena a bajos pH (Katime, 1980), ya que la mayoría de ellos presentan excelentes propiedades de adsorción a pH neutros o alcalinos.
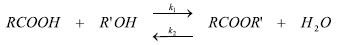
Si se quisiera seguir el curso de la reacción por el incremento de los picos IR del agua, resultaría muy dispendioso, ya que sería necesario usar sellos herméticos y procurar ausencia absoluta de humedad en la cámara de reacción, puesto que en el background del espectro aparecerían los picos de agua debidos a la humedad atmosférica. Es aconsejable seguir el decremento o incremento de picos de otras funciones o grupos que presenten picos IR diferentes a los de la región del agua. Existen diferentes opciones para poder hacer esto; por ejemplo en catálogos de espectros infrarrojos, se tiene (Charles, 1985):
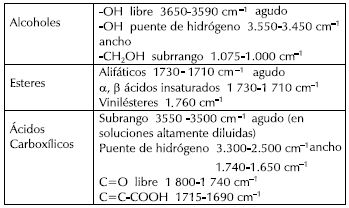
Sin embargo, es mejor hacer un análisis preliminar tomando por separado cada uno de los espectros de reactantes y productos que intervienen en la reacción y luego superponerlos (el software lo permite), de esta forma se puede visualizar una vez inicie la reacción qué picos empezarán a decrecer de los reactantes y cuáles de los productos a incrementar, y que no se vean interferidos por el background (normalmente del agua).
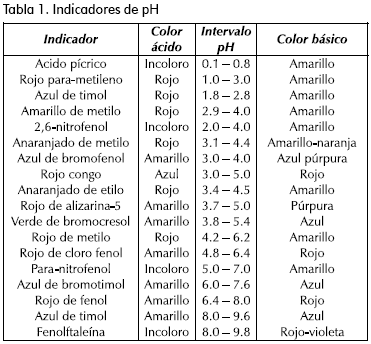
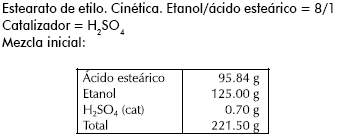
Para poder cuantificar el curso de una reacción puede hacerse una curva de calibración previa: la intensidad (I) (de un pico IR que crece o aumenta) vs. la concentración medida para la especie en cuestión, en una mezcla patrón, determinada por otro método (p. ej: titulación) (MaClaurin y Crabb, 1996). El avance de la reacción puede seguirse por la relación I/I0 (I0 = intensidad inicial del pico; I = intensidad del pico en un tiempo t). En el caso de usar la titulación como método de calibración, es importante emplear un indicador apropiado (Tabla 1).
Por ejemplo, para una reacción que emplea H2SO4 como catalizador, cuyo pKa2 es 1.92 y se está esterificando un ácido orgánico, por ejemplo ácido acético, cuyo pKa es 4.74, es necesario realizar dos titulaciones. En la primera se usará como indicador azul de timol que vira a pH= 3.0 (superior a 2.0 pero inferior a 4.5), esto asegura la titulación del ácido fuerte. En la segunda titulación se empleará como indicador fenolftaleína, que vira a pH= 8.0, esto asegura la titulación de toda la acidez de la mezcla. Para determinar el volumen empleado en la titulación solamente del ácido orgánico residual, se calcula:
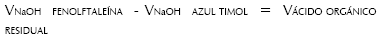
En el presente trabajo se empleó el método de titulación para la determinación de la conversión en el equilibrio en la esterificación del ácido acético con metanol y con etanol y su comparación con los resultados reportados en la literatura.También se utilizó el método de titulación para la esterificación de ácido esteárico con metanol para dos ensayos, uno con MgO como catalizador y el otro con H2SO4.
Para los demás ensayos se presenta la evolución de la reacción siguiendo en los espectros IR la disminución de unos picos y el incremento de otros. A continuación se muestra en la tabla 1 los pH de variación para algunos indicadores (Kolthoff y Sandell, 1952; Weast., 1988).
Procedimiento experimental
Ensayos con sonda IR
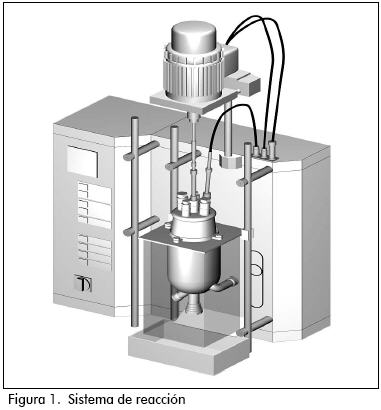
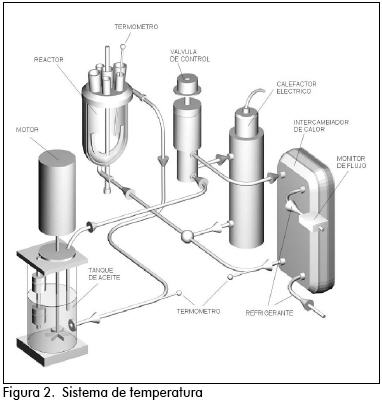
Se usó un reactor de vidrio de 1 litro Lab Max Mettler Toledo, dotado con condensador de reflujo, sonda IR y detector con N2 líquido; controles de temperatura, de velocidad de agitación, de pH, de velocidad de alimentación. Su manejo se ejecuta desde un computador. El esquema puede verse en las figuras 1 y 2. En este caso el sistema se operó como un batch. Se cerró el sistema, se puso a funcionar el condensador de reflujo, se introdujo la sonda IR, evitando su roce con el ancla del agitador. Se procedió a ajustar los parámetros IR, altura de pico superior a 10.000 y contraste superior a 140: logrado esto, se tomó el espectro IR de background.
Luego se procedió a colocar dentro del reactor el ácido orgánico, se puso la velocidad de agitación requerida y la temperatura de reacción, enseguida se adicionó el alcohol. Se tomó un segundo espectro IR cuando la mezcla presentó homogeneidad. Se programó el intervalo de tiempo para la toma secuencial de los espectros IR y el tiempo total de duración del evento. Se adicionó el catalizador y se dio inicio al programa de toma de espectros. Se ejecutaron los ensayos que a continuación se relacionan.
Reacciones de esterificación
Nota: En todos los casos, el programa inicia la toma de los espectros IR, inmediatamente, luego de adicionar el catalizador.











Ensayos con titulación
Para seguir la cinética por titulación, para diferentes tiempos, se tomaron dos muestras, cada una aproximadamente de 0.5 gr, y se le adicionaron 2 mL de metanol. Una muestra se tituló usando azul metileno y en la otra fenolftaleína. En ambos casos se usó NaOH 0.1N.

Luego de 2.5 hr de iniciada la reacción, no se presentó variación en la acidez de la mezcla.
Peso de muestra = 3.9 gr
Volumen de NaOH 0.49N (usando fenolftaleína) = 26.3 ml
Volumen de NaOH 0.49N (usando rojo de metilo) = 2.1 ml
Ácido acético residual en la muestra = (26.3 – 2.1)x10–3 L x 0.49 Eq/L = 1.18x10–2 Eq.
Ácido acético residual en el reactor = 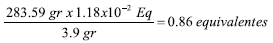
X (% de avance de la reacción): 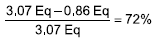
X (% avance teórico (Groggins , 1958)) = 69.56%

Después de 2.5 hr de iniciada la reacción:
Peso de muestra = 3.7 gr
Volumen de NaOH 0.49N (usando fenolftaleína) = 27.3 mL
Volumen de NaOH 0.49N (usando rojo de metilo) = 3.3 mL
Ácido acético residual en la muestra = (27.3 – 3.3)x10–3 L x 0.49 Eq/L = 1.18x10–2 Eq.
Ácido acético residual en el reactor = 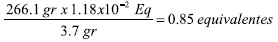
X (% de avance de la reacción): 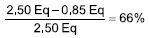
X (% avance teórico (Groggins , 1958)) = 66%.
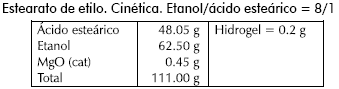
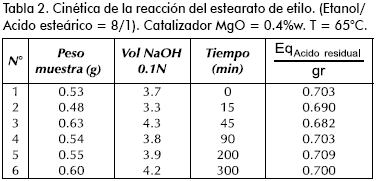
Los resultados se muestran en la Tabla 2.
Los resultados se muestran en la Tabla 3.
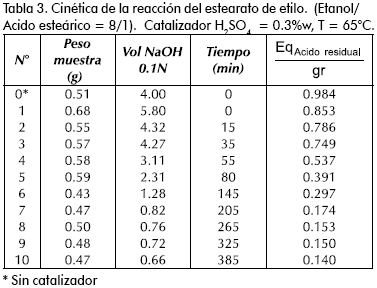
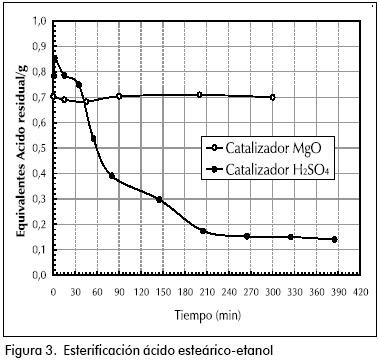
Los resultados de las Tablas 2 y 3 pueden apreciarse en la Figura 3. Puede observarse que a 65°C, el MgO no cataliza la reacción de esterificación del ácido esteárico y el etanol, mientras que el H2SO4, aunque está en concentración baja (0.3%) cataliza bien esta reacción.
Avance de la reacción con H2SO4:
Equivalentes de H2SO4 iniciales= 0.853 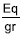 – 0.784
– 0.784 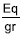 = 0.069
= 0.069 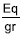 inicial.
inicial.
Eq H2SO4 iniciales = Eq H2SO4 finales.
Eq de ácido esteárico inicial = 0.784 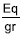
Eq de ácido esteárico final = (0.140 – 0.069) = 0.071 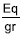 final.
final.
X (% ) = 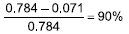 de conversión después de 6.4 horas.
de conversión después de 6.4 horas.
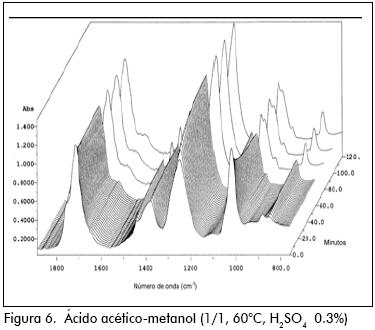
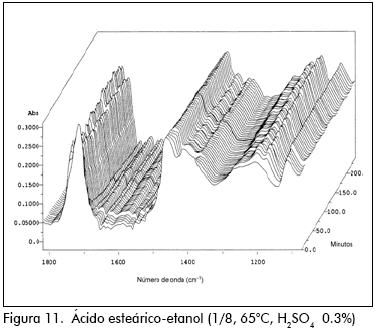
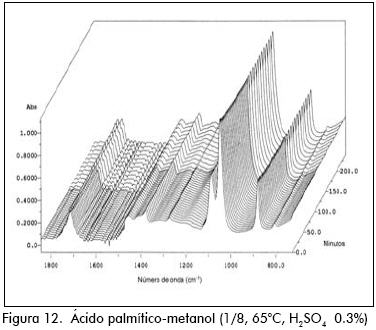
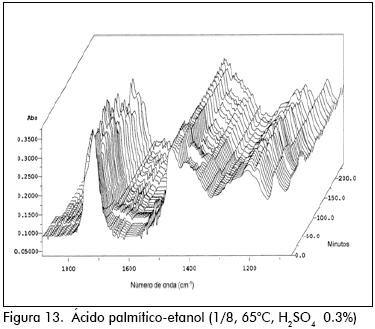
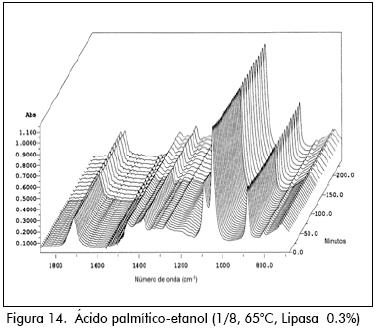
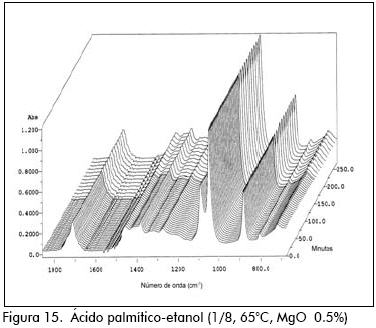
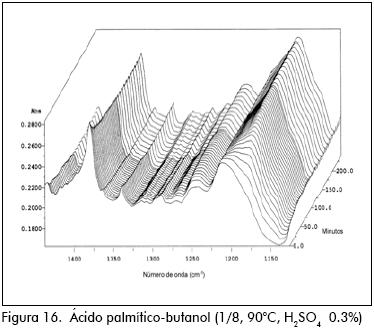
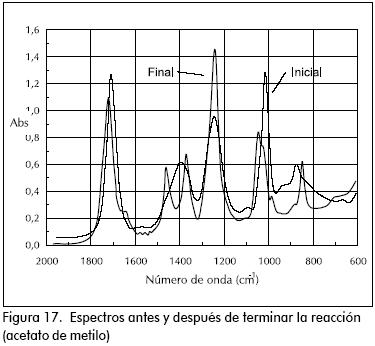
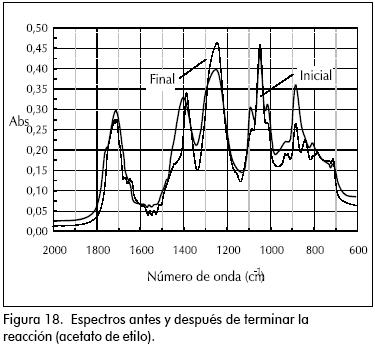
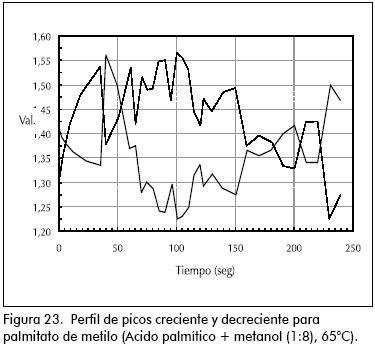
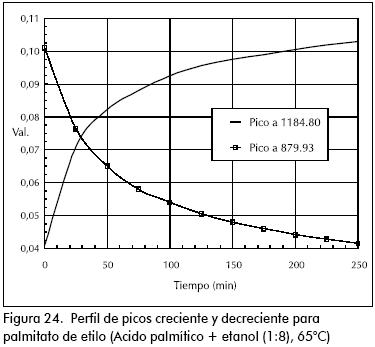
Los espectros IR para los ensayos pueden verse en las Figuras 4 a 24.
Discusión
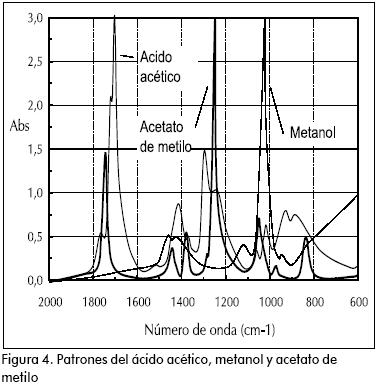
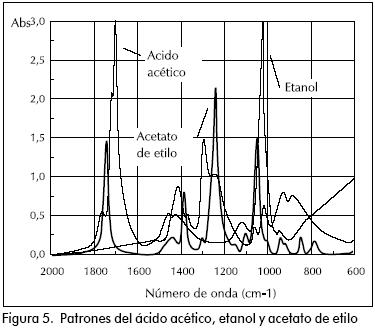
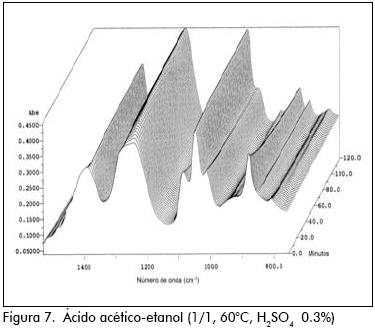
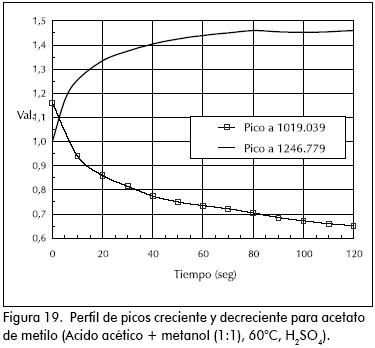
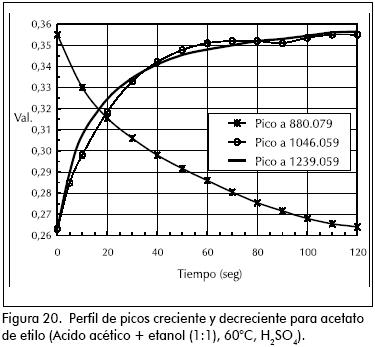
En las esterificaciones de ácido acético con metanol y etanol, puede verse el incremento en las bandas 850, 1.220 cm–1 propia del éster y la disminución de las bandas 890, 1.640 cm–1 y 1.020 cm–1 del grupo carboxilo y del alcohol, respectivamente. Al graficar la intensidad de incremento o decremento de estas bandas contra el tiempo, puede verse perfectamente el avance de la reacción. El incremento de unas bandas y decremento de otras, de antemano podía predecirse a partir de los espectros superpuestos para los componentes puros que intervienen en la reacción. (Figuras 4 y 5).
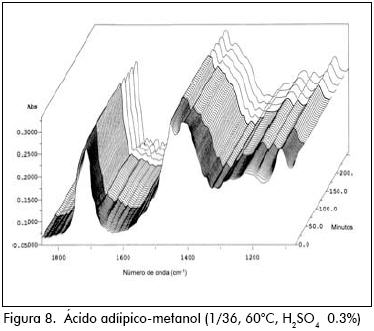
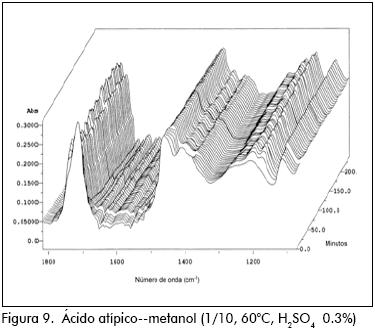
Cuando se obtuvo adipato de metilo (ácido adípico/metanol = 1/36), se nota el incremento en las bandas 1.177, 1.370 cm–1 y decremento en las bandas 1.020, 1.415 cm–1, pero debido a la fuerte presencia de metanol la variación de las bandas apenas si es perceptible en el IR. En cambio, para la misma reacción pero empleando relación molar ácido adípico/metanol = 1/10, la variación de las bandas es más apreciable, debido a que el espectro del metanol no es tan dominante en este caso.
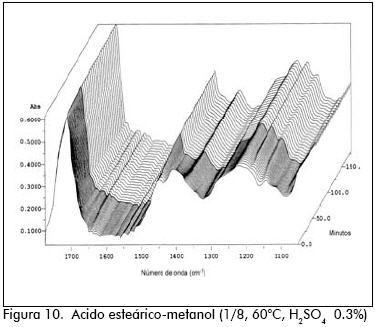
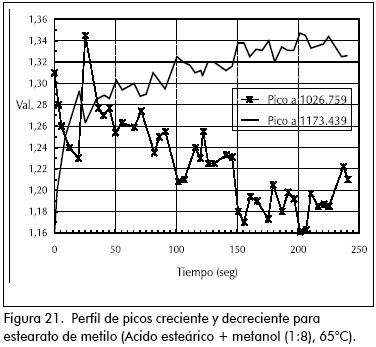
Durante la preparación del estearato de metilo, en los primeros 15 minutos de reacción, la variación de las bandas IR fue pareja y se observó una mezcla homogénea; pero luego la mezcla se enturbió y los espectros IR fueron disparejos, muy seguramente por la falta de solubilidad del estearato de metilo en el medio reaccionante que entró en suspensión. Aunque la reacción puede seguir avanzando, la heterogeneidad que se presenta en el sistema hace que el método IR falle para seguir el curso de la reacción.
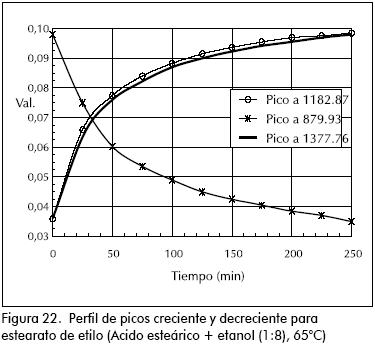
De otro lado, cuando se esterificó ácido esteárico con etanol, la mezcla permaneció homogénea, la variación de los espectros IR fue pareja, mostrando en este caso que la reacción puede seguirse perfectamente empleando esta técnica.
En la preparación de palmitato de metilo y de etilo, ocurrió algo similar al caso anterior. Cuando se usó metanol, después de 15 minutos de reacción el sistema se enturbió y la variación de los IR fueron disparejos. Para el etanol la mezcla reactiva permaneció homogénea y los IR variaron uniformemente.
Cuando se emplearon como catalizadores Lipasa y MgO a 60°C en la esterificación de palmítico y etanol, no se observa reacción alguna. En el caso de la Lipasa, bien si estaba desactivada o no, se aplicó un procedimiento adecuado para su activación. En el caso del MgO la temperatura fue muy baja, pues este es activo a T>110°C. Aunque en ambos casos la mezcla permaneció turbia–lechosa (fases inmiscibles) los espectros IR no fueron parejos.
En la preparación del palmitato de butilo se observó una fase inmiscible en el fondo del reactor (agua), pero esta no entró a emulsionarse en el seno de la mezcla reactiva y se pudo obtener la evolución uniforme de los espectros IR.
En las reacciones donde la secuencia de los espectros IR fue uniforme, graficando la intensidad de una banda (creciente o decreciente) contra el tiempo, puede seguirse el curso de la reacción. En el caso donde la variación de los IR no fue uniforme, es imposible aplicar esta técnica.
Conclusiones
Para las reacciones de esterificación, puede seguirse el curso de la reacción por el espectro IR tomado in situ siguiendo el incremento o decremento de la intensidad de una banda a cierta longitud de onda. Para poder cuantificar se requirió de un trabajo paralelo adicional, preparando soluciones de concentraciones conocidas y tomando los espectros IR, lo que permite preparar una curva de calibración, graficando intensidad de un pico vs. concentración en la muestra.
Si durante la reacción se forma una fase inmiscible que causa enturbamiento de la mezcla reactante, la técnica de seguir el curso de una reacción tomando espectros IR in situ no es aplicable.
De otro lado, si la fase que se forma, aunque sea inmiscible, se separa nítidamente de la mezcla reactante (por ejemplo: decanta) la técnica sí puede emplearse. Adicionalmente, si desde el inicio la mezcla es turbia debido a un sólido o a una fase emulsificada, y esta permanece estable, la técnica también se puede aplicar.
Los catalizadores Lipasa y MgO no mostraron actividad catalítica para la esterificación a las condiciones usadas.
Recomendaciones
Buscar un hidrogel que pueda adsorber agua a pH bajos.
Buscar catalizadores básicos para esterificación que trabajen a temperaturas menores de 90°C (para evitar daño al hidrogel).
Agradecimientos
Al grupo de Nuevos Materiales de la Universidad del País Vasco; a la Facultad de Ingeniería, Universidad Nacional de Colombia, Bogotá, y al CYTED.
Bibliografía
Charles, J., The Aldrich Library, FI–IR spectros, Poncelet, Aldrich Chemical Co., Vols. I, II, 1985. [ Links ]
Groggins, P. H., Unit processes in Organic Synthesis, 5a Ed., McGraw Hill, 1958, pp. 697. [ Links ]
Katime, A., Síntesis y usos de hidrogeles, CYTED, Universidad del País Vasco, 1980. [ Links ]
Kolthoff, M., and Sandell, E. B., Textbook of quantitative inorganic analysis, 3a Ed., Ed. McMillan, New York, 1952, pp. 427-453. [ Links ]
Machado, F., y López, C. M., Tamiz molecular, CYTED, Dic. 1993. [ Links ]
MaClaurin, P., and Crabb, N. C.., Quantitative in situ monitoring of an elevated temperature reaction using a water-cooled mid-infrared fiber-optic probe, Anal. Chem., 68, 1996, pp. 1116-1123. [ Links ]
Morrison, R. T., y Boyd, R. N., Química Orgánica. Ed. Addison Wesley Iberoamericana, México, 1987. [ Links ]
Sánchez, F., y Rodríguez, G., Esterificación, En Revista Ingeniería e Investigación, Facultad de Ingeniería, UN, Bogotá, 33, 1996, pp. 19. [ Links ]
Vogel’s Textbook of practical organic chemistry, 5a Ed., Editorial Longman, 1999. [ Links ]
Weast, R. C., CRC, Handbook of chemistry and physics, CRC Press, 1988, pp. D-101. [ Links ]














