Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.26 no.1 Bogotá Jan./Apr. 2006
Álvaro Orjuela Londoño1, Fernando Leiva Lenis2, Luis Alejandro Boyacá Mendivelso3, Gerardo Rodríguez Niño4, Luis María Carballo Suárez5
1 Ingeniero químico. M.Sc. Profesor, Universidad Nacional de Colombia, Bogotá. Departamento de Ingeniería Química. aorjuelal@unal.edu.co
2 Ingeniero químico. M.Sc. Andercol. feleiva@hotmail.com
3 Ingeniero químico. M.Sc. Profesor Universidad Nacional de Colombia, Bogotá. Departamento de Ingeniería Química. laboyacam@unal.edu.co
4 Ingeniero químico. M.Sc., Ph. D. Profesor Universidad Nacional de Colombia, Bogotá. Departamento de Ingeniería Química. grodriguezn@unal.edu.co
5 Ingeniero químico. M.Sc., Ph. D. Profesor Universidad Nacional de Colombia, Departamento de Ingeniería Química. lmcarballos@unal.edu.co
RESUMEN
Es este trabajo se realizó un estudio de la adsorción del sistema reactivo: ácido acético – n-butanol – acetato de butilo – agua, en fase líquida y presión de 0.76 Bar, sobre una resina de intercambio catiónico (Bayer® Lewatit K-2431). Se verificó la distribución de tamaño de partícula del sólido y se observó baja dispersión con un 86% de la masa entre mallas 20 y 30. El sólido seco presenta una distribución binodal con un 40% por encima de la malla 25 y un 45% entre las mallas 25 y 40. Se desarrollaron pruebas de hinchamiento de la resina en los componentes puros y en mezclas binarias no reactivas, y se observó un aumento en el volumen de la matriz entre 2,2 y 3,8 veces. Se notó una adsorción selectiva en el sistema reactivo en el orden: agua > n-butanol ≈ ácido > acetato. Se evaluaron dos modelos de tipo ideal y no-ideal para cuantificar la adsorción a través de una isoterma compuesta, demostrando la debilidad de los modelos teóricos para representar la adsorción en matrices poliméricas iónicas. Finalmente, se desarrollaron ensayos de caracterización calorimétrica del catalizador hinchado, y se reconoció a través del análisis del espectro IR un cambio en la estructura del sólido debido al tratamiento térmico.
Palabras clave: resinas de intercambio, esterificación, acetato de butilo, adsorción
ABSTRACT
Reactive system (acetic acid–n-butanol–butyl acetate–water, in liquid phase, 0.76 Bar pressure) adsorption on a cationic exchange resin (Bayer Lewatit K-2431) was studied in this work. Solid particle size distribution was verified and low dispersion was noticed with 86% of total mass between 20 and 30 mesh. The dried solid showed a bi-nodal distribution with 40% above 25 mesh and 45% between 25 and 45 mesh. Resin swelling assays were carried out on pure components and non-reactive binary mixtures and increased matrix volume was observed (2.2 to 3 times higher). Selective adsorption on the reactive system was observed in the sequence: water > n-butanol ≈ acid > acetate. Both ideal and non-ideal models were tested for calculating adsorption using a composite isotherm, demonstrating these models’ weakness in representing adsorption on ionic polymer matrices. Calorimetric characterisation assays were carried out on swelled catalyst and a change in solid structure caused by thermal treatment was recognised using infrared scanning.
Keywords: ion exchange resins, sterification, butyl acetate, adsorption
Recibido: enero 27 de 2005
Aceptado: septiembre 26 de 2005
Introducción
El acetato de butilo es uno de los solventes más utilizados en la industria química, y se espera que su consumo aumente en los próximos años debido a su bajo impacto ambiental en comparación con otros solventes orgánicos, además de las nuevas tecnologías desarrolladas para su producción (destilación reactiva: Gangadwala et al., 2004; Hanika et al., 1999, 2003; Steinigeweg 2002; Venimadhavan et al., 1999; Wang et al., 2003; Zhicai et al., 1998. preevaporación: Liu et al., 2001). En general, las reacciones de esterificación son aceleradas con catalizadores ácidos fuertes, y su conversión está limitada por el equilibrio químico (Dhanuka et al., 1977; Orjuela et al., 2003, 2004, 2005). Entre los catalizadores heterogéneos más utilizados (como reemplazo de los ácidos minerales), se encentran las resinas de intercambio catiónico, sólidos fuertemente ácidos, sintetizados a través de la copolimerización de monómeros aromáticos ramificados y/o acrílicos, y activados a través de procesos tales como la sulfonación (Bayer, A.G., 2001; Coutinho et al., 2004; Harmer, 2001; Matatov, 2002; Rhodes, 1999).
Durante el proceso catalítico heterogéneo se presenta la confluencia de varios fenómenos de transporte (Bayer, A.G., 2001; Corain et al., 2001; Kippling, 1965), y en el caso particular de las resinas ácidas, el carácter hidrofílico de los grupos sulfónicos, y el hidrofóbico de las cadenas aromáticas y alifáticas dentro de la estructura polimérica, da como resultado un medio complejo y heterogéneo que condiciona los procesos de transferencia de masa. Este hecho hace que el medio sea afectado por cambios en la polaridad y la temperatura del sistema, los cuales indudablemente se producen debido a la energía suministrada para alcanzar la activación de la reacción, las entalpías de adsorción y reacción, y la variación de concentración de los reactantes y productos de naturaleza físico-química diferente. Esta variación en el ambiente dentro de la resina provoca la expansión y la contracción de los poros, debido a la elasticidad propia del polímero y la rigidez generada por el entrecruzamiento (Bayer, A.G., 2001; Kippling, 1965).
Cuando un componente no polar entra en contacto con un grupo altamente polar de la resina como el ácido sulfónico, es repelido y la estructura porosa se contrae, dificultando la difusión de los componentes. Por otro lado, los solventes polares son adsorbidos fuertemente en los sitios activos generando un hinchamiento de la matriz, lo que aumenta la accesibilidad de los componentes a los sitios activos y por consiguiente la velocidad de difusión (Bayer, A.G., 2001; Kippling, 1965; Anasthas, 2001; Harmer, 2001). Este comportamiento refleja una de las características de las resinas de intercambio como catalizadores: la adsorción selectiva entre las diferentes sustancias presentes en las mezclas.
La adsorción selectiva evidenciada por el catalizador genera una relación de componentes de reacción a sitios activos muy diferente de la obtenida con catalizadores homogéneos. En el caso específico de la esterificación, la adsorción selectiva del agua y la exclusión del acetato afectan la velocidad, la conversión final y la selectividad de la reacción. Este hecho ha sido ampliamente reconocido por diferentes investigadores (Anasthas, 2001; Favre et al., 1986; Kanazawa et al., 2001; Patel, 1965; Sainio et al., 2004; Song et al., 1998).
En general, los modelos matemáticos que representan y permiten evaluar la cinética de la reacción catalítica (LHHW, Eley-Rideal, etc.), involucran términos asociadas con la adsorción de los reactantes y productos sobre el catalizador (Favre et al., 1996; Song et al., 1998; Mazzotti, et al., 1997). Con el propósito de realizar un análisis preliminar de los fenómenos adsortivos sobre el catalizador, en el presente trabajo se realizó un estudio de la adsorción del sistema reactivo: ácido acético – n-butanol – acetato de butilo – agua, en fase líquida y presión de 0.76 Bar, sobre una resina de intercambio catiónico (Bayer® Lewatit K-2431).
Inicialmente se desarrolló un análisis de distribución de tamaño de partícula para el catalizador húmedo y seco, y se realizaron ensayos de hinchamiento en cada uno de los componentes puros del sistema reactivo. Después de realizar un reconocimiento de los modelos teóricos y semiempíricos utilizados para la caracterización de la adsorción sobre matrices sólidas, se realizaron ensayos con mezclas binarias no reactivas ajustando los datos experimentales a modelos teóricos. Finalmente, se desarrollaron ensayos de caracterización calorimétrica del catalizador saturado en cada uno de los componentes puros y en la mezcla, y se reconoció, a través del análisis del espectro IR, un cambio en la estructura del sólido debido al tratamiento térmico.
Aspectos teóricos
La valoración de los efectos adsortivos sobre la superficie de los catalizadores históricamente se ha desarrollado a través de las isotermas de adsorción, como lo describe Kippling. Los acercamientos teóricos originalmente utilizan los conceptos aplicados en los gases para describir el fenómeno de la adsorción individual de cada componente, como función de su composición en la fase líquida. Langmuir desarrolló el primer modelo teórico de equilibrio reversible de adsorción y encontró una ecuación sencilla para describir el mismo, la cual se fundamentaba en algunas suposiciones básicas:
- La superficie tiene un número constante de lugares donde se puede efectuar la adsorción.
- Cada sitio puede albergar una sola molécula.
- No hay interacción entre las moléculas adsorbidas.
- El calor de adsorción es igual para todos los lugares y no dependen de la superficie cubierta.
Si Θ es la fracción de superficie cubierta y C la concentración del soluto, la expresión resultante es:

Donde b es el coeficiente de adsorción y refleja la relación entre las constantes de adsorción y desorción del componente sobre el sólido.

Esta ecuación ha sido ampliamente utilizada, principalmente en reacciones en fase vapor, aunque se reconocen algunos trabajos que hacen uso de este modelo en la fase líquida y con resinas de intercambio como catalizador (Harper, 2001; Kawase et al., 1996). Freundlich desarrolló un modelo seudoempírico que supone una disminución exponencial del calor de adsorción con el aumento del cubrimiento de la superficie libre del catalizador. El modelo corresponde a:

Donde x es el peso del adsorbato, m el peso de sólido y C es la concentración de la solución en equilibrio; α y n (< 1) son constantes asociadas al sistema en estudio. A través de este modelo, algunos autores (Kanazawa et al., 2001; Romero, 1996) describen la adsorción de líquidos sobre matrices sólidas.
Tempkin corrige el modelo de Langmuir, y supone una disminución lineal del calor de adsorción respecto del aumento de la cobertura de la superficie

Donde se toman en cuenta los efectos de la temperatura y la concentración de los adsorbatos, el factor de cubrimiento α, la entalpía de adsorción en condiciones de referencia ΔH0 y una constante específica del sistema b0.
El modelo de Brunauer, Love y Keenan cubre en un intervalo más amplio a las isotermas de Langmuir y Tempkin (las cuales son casos límite de este modelo), que corresponde a:
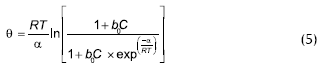
Debido a la dificultad de representar de forma adecuada el fenómeno de la adsorción competitiva en soluciones multicompuestas con los modelos anteriores, Kippling, con base en una extensa recopilación de modelos teóricos y empíricos, describió el fenómeno físico a través de la isoterma de adsorción compuesta. Dicha isoterma toma en cuenta el cambio de composición en la fase líquida, enfatizando, el hecho de que la adsorción ocurre desde una solución.
Cuando una masa m de sólido se pone en contacto con no moles de líquido, la fracción molar en el líquido disminuye como Δx con respecto al componente 1. Este cambio de concentración se debe a la entrada de n1s moles del componente 1 y n2s moles del componente 2 sobre la superficie de peso unitario. En el equilibrio, permanecen en el líquido n1 y n2 moles de los mismos componentes, dando una fracción molar x respecto del componente 1, la fracción molar inicial es x0. La obtención de la expresión que describe este comportamiento a través de la isoterma compuesta se describe a continuación:
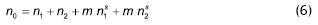



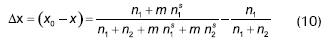


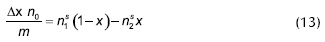

Esta deducción no está basada sobre suposiciones del mecanismo del proceso, excepto que cada componente de la mezcla líquida puede ser adsorbido en la interfase.
En la ecuación (14) las variables n1s y n2s son desconocidas y hay dos estrategias para determinar estos valores y caracterizar la adsorción de una mezcla binaria. La primera involucra medidas indirectas en el laboratorio; la segunda introduce consideraciones teóricas sobre la naturaleza de la capa adsorbida.
En el laboratorio se intenta medir el peso total de la mezcla adsorbida en la fase sólida (hinchamiento en matrices poliméricas), utilizando la ecuación 15

Donde se mide el peso total en la fase líquida adsorbida w (M1 y M2, pesos moleculares de los adsorbatos), y se determinan junto con la ecuación 14 las moles de los componentes en la matriz sólida. Los acercamientos teóricos utilizan los conceptos aplicados en los gases para describir el fenómeno de la adsorción individual de cada componente como función de su composición en la fase líquida por ejemplo, la ley de acción de masas. En este tipo de formulación se hacen consideraciones similares a las de Langmuir, pero se permite el análisis de equilibrio de adsorción para un sistema binario:
- La capa adsorbida está confinada en monocapa.
- Todos los sitios de adsorción son equivalentes.
- Los dos componentes de una mezcla binaria tienen la misma área molecular en la fase adsorbida.
- La fracción de sitios ocupados es constante para todos los pares binarios a todas las composiciones.
Para una mezcla binaria no ideal, el formalismo retoma las variables de la isoterma compuesta, si se considera el proceso de quimisorción como una reacción química de la siguiente forma:
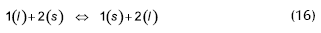
Además, si se asume que la fase líquida es no ideal y el sólido es ideal, la constante de equilibrio para la reacción está dada por:

k2,1 puede ser expresada como la relación entre dos constantes de adsorción de procesos independientes de la forma:
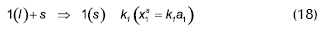
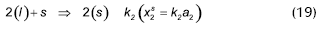
La ecuación (16) se obtiene por sustracción de las ecuaciones (18) y (19), de tal forma que la constante de equilibrio se puede expresar como:

Dado que la composición en la fase sólida del componente 2 es:

La expresión, tomando en cuenta el equilibrio de la reacción, queda:

Como el número de sitios ocupados es constante y todas las moléculas ocupan el mismo número de sitios (igual área molecular), la cantidad total de moles adsorbidas en la superficie es independiente de la concentración superficial, así que:

Donde ns representa el número total de moles sobre la superficie por unidad de masa. Representando la ecuación 12 respecto del número de moles (xs = n1s/ns)

Y finalmente, reemplazando en la isoterma compuesta (ecuación 14)
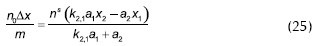
En este modelo hay dos parámetros por determinar ns y k2,1 , los cuales se encuentra por regresión no lineal de datos experimentales de adsorción de la mezcla binaria sobre el catalizador. En el sistema de esterificación estudiado hay cuatro pares binarios no reactivos susceptibles de ser analizados por esta metodología (agua-ácido acético, agua-butanol, butanol-butilacetato y ácido acético-butilacetato). Sólo tres de ellos son independientes (el cuarto podría ser utilizado para hacer un análisis de consistencia de los resultados), de tal forma que puede utilizarse un componente como referencia e introducir las constantes de adsorción en la expresión cinética respecto de este último. Song utilizó este formalismo para la determinación de las constantes de adsorción en la esterificación de metanol y ácido acético sobre Amberlyst 15, tomando como referencia la constante de adsorción del acetato que se determina a través de los ensayos cinéticos.
Otros modelos para la determinación de parámetros de adsorción, a nivel teórico o empírico, en general resultan de refinaciones sobre las suposiciones básicas de Langmuir, entre otros se reconocen el modelo BET, la formulación potencial, el modelo de Frumkin (Tamura et al., 1998), las isotermas BSA (Tao, et al., 1997), el método Chi (Condon, 2002), el método de Schay-Nagy (Zimehl, 1998), la teoría de Flory-Huggins (Favre et al., 1996; Mazzotti et al., 1997) y los semiempíricos. Dentro de este último grupo se reconoce el trabajo de Patel, quien presenta una expresión para la adsorción noiónica de ácidos carboxílicos en matrices poliméricas sulfonadas de E-DVB, dependiente de la naturaleza del ácido y del grado de entrecruzamiento.
Metodología
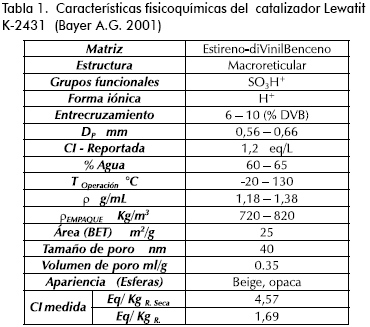
La pureza de los reactivos utilizados, ácido acético (Merck 99,9%), n-butanol (Merck 99,5%), acetato de n-butilo (Merck 99,6%), y agua desionizada, fue confirmada por cromatografía de gases. La resina ácida usada fue Bayer® Lewatit K-2431 (Tabla 1) Previo a la utilización del catalizador húmedo, este se lavó con etanol anhidro para retirar el agua presente, y posteriormente se secó a 80°C durante 24 h, luego al vacío a 100°C por 12 h, y se almacenó en un recipiente hermético, dentro de un desecador.

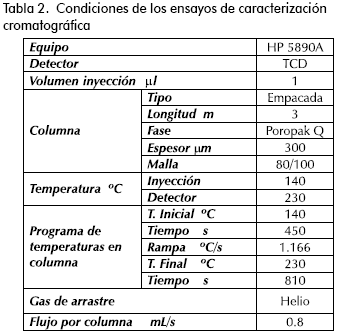
Durante los ensayos de adsorción se utilizó un sistema como el mostrado en la Figura 1: un reactor de vidrio de 500 mL con chaqueta (1), al que se adaptó un sistema de agitación con velocidad controlada (2), un condensador para operación a reflujo total (3), un termómetro y una toma de muestras. El control de temperatura se realizó con un baño de recirculación (4) con aceite térmico (Julabo 4®, Julabo Labortechnik GMBH), el cual mantenía el valor de temperatura constante en un intervalo de ± 0,1 °C. Para el seguimiento y caracterización de las muestras de reacción se utilizó un cromatógrafo de gases, en las condiciones descritas en la Tabla 2. Las muestras se diluyeron en etanol anhidro justo antes de su inyección para evitar la separación en dos fases inmiscibles. Por calibración del método analítico se obtuvieron los factores de respuesta individuales respecto del etanol (Orjuela, 2003).
La caracterización calorimétrica se realizó a través de análisis de calorimetría diferencial de barrido (DSC) con un equipo Universal V2.5H de TA Instruments. El barrido se efectuó entre -40 y 250°C, con una velocidad de calentamiento de 0.166°C/s y tiempo de estabilización isotérmica de 5 minutos. Los espectros IR se tomaron sobre los sólidos macerados y encapsulados en KBr, en un equipo NICOLET 150P con accesorio de refractancia difusa.
Resultados y discusión
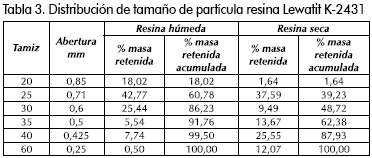
Para realizar los ensayos de adsorción con muestras representativas del catalizador se realizó un análisis de distribución de tamaño de partícula (Tabla 3). La resina muestra una baja dispersión en la presentación comercial, con un 86% de la masa con un tamaño entre 0,6 – 0,85 mm. El sólido seco presenta una distribución binodal marcada, con un 40% por encima de la malla 25 y un 45% entre las mallas 25 y 40. Sin embargo, la distribución de tamaño es bien uniforme en comparación con otro tipo de resinas (Bayer, A.G., 2001). En los ensayos de saturación (hinchamiento) y adsorción posteriores, se tomó la fracción de sólido seco superior a malla 40 (diámetro y volumen de partícula seca promedio de 0,63 mm y 0,13 mm3, respectivamente).
El estudio de saturación se realizó con cada una de las sustancias que componen el sistema reactivo. Para esto se colocó una muestra de resina seca de aproximadamente 1 g en 20mL de cada compuesto y se dejó por un tiempo de 72 horas, a temperatura ambiente, al cabo de las cuales se filtró, retirando el exceso superficial, y se tomó el peso final (ver Tabla 4). El porcentaje de hinchamiento corresponde al contenido de solvente en base húmeda dentro de la matriz polimérica, y la razón de hinchamiento es el cociente entre el peso de la resina saturada en solvente y el peso de la resina seca.
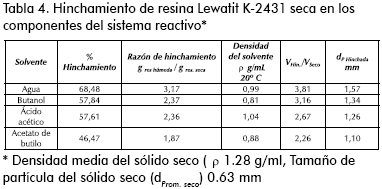
En la Tabla 4 se observa que el orden de afinidad de los compuestos por la resina es agua >> butanol ≈ ácido >> acetato. Este comportamiento ha sido ampliamente descrito antes (Kippling, 1965; Anasthas, 2001; Patel, 1965; Song, 1998; Mazzotti et al., 1997; Kawase et al., 1996), y refleja la elasticidad de la matriz polimérica y la alta polaridad de la misma. Si se supone un hinchamiento isotrópico (homogéneo en toda la matriz) respecto del volumen de una partícula seca Vseco, se puede calcular el aumento de volumen de la partícula saturada VHin (suponiendo aditividad entre el volumen de la partícula seca y el volumen de solvente absorbido), y un diámetro de partícula promedio en saturación dp Hin, respecto del catalizador seco:
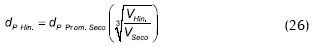
Los datos reportados indican un apreciable aumento del volumen del lecho empacado en presencia de los componentes del sistema reactivo. Esto también indica la simultaneidad de fenómenos de adsorción superficial y absorción dentro de la estructura del polímero, dificultando la interpretación de la adsorción a través de modelos teóricos (múltiples capas sobre la superficie).
Después de analizar los modelos utilizados para la evaluación de los parámetros de adsorción, se seleccionó el formalismo de Kippling, debido a que este considera la competitividad de los solventes por la superficie libre. El procedimiento experimental utilizado corresponde al seguido por Song en la determinación de la adsorción binaria en el sistema de acetato de metilo, utilizando el modelo de ley de acción de masas.
En general, los sistemas reactivos de esterificación involucran compuestos de naturaleza fisico-química bien diferentes y las mezclas que forman presentan un comportamiento no ideal (Venimadhavan et al., 1999; Zhicai et al., 1998; Bevia et al., 1984; Esquivel, 1990; Gangadwala et al., 2003; Löning et al., 2000). Por tal razón se incluyó un modelo termodinámico (UNIQUAC) para representar el equilibrio de fases del sistema, el cual permitió calcular los coeficientes de actividad del sistema. Se utilizaron los parámetros de interacción reportados por Venimadhavan.
En cada ensayo se utilizó una concentración de catalizador de 10% peso a volumen respecto a la carga inicial, que corresponde aproximadamente a las concentraciones de catalizador utilizadas en los ensayos de reacción (Orjuela et al., 2003, 2004). Cada mezcla binaria se preparó con un volumen inicial de 100 ml y una composición de 5% molar del componente más fuertemente adsorbido por la resina. La mezcla se precalentó en el reactor agitado a una temperatura de 80°C por una hora, después de la cual se adicionó la cantidad de catalizador especificada. El sistema se dejó estabilizar por una hora, después de la cual se tomó una muestra del líquido sobrenadante y se evaluaron las concentraciones por cromatografía de gases. Los siguientes datos fueron obtenidos por adiciones sucesivas del componente más fuertemente adsorbido para estudiar el comportamiento en todo el intervalo de concentraciones. Para evitar la acumulación de error debida al retiro de muestras y a la disminución de la relación sólido/líquido, el ensayo se detuvo cuando el volumen total de líquido fue de 300 ml. El análisis complementario de cada curva se reinició lo más cerca posible de las concentraciones del ensayo previo, hasta evaluar todo el intervalo de composiciones (Figura 2). Los datos obtenidos se correlacionaron con el modelo teórico (ecuación 26) a través de una estrategia de regresión no lineal, con el método de los mínimos cuadrados (implementada sobre EXCEL®).
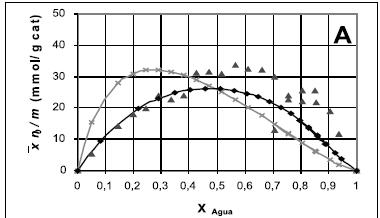
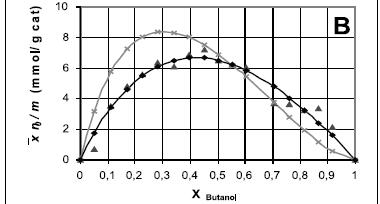
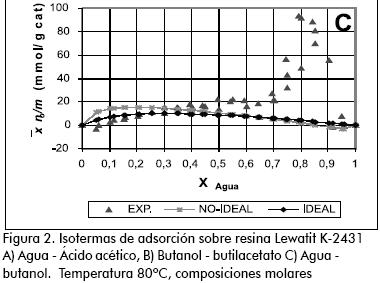
Se utilizó como función objetivo la diferencia entre los valores del parámetro de absorción medido experimentalmente en cada muestra p, y el calculado por evaluación con modelo ideal (en término de composiciones) y no ideal (en término de actividades). En la figuras 2A y 2B se observa que la introducción del componente que presenta mayor afinidad por la resina produce un aumento de las moles adsorbidas. Esta adsorción disminuye al sobrepasar fracciones molares superiores al 0,5, lo que indica un proceso paulatino de saturación de la superficie. En el caso del sistema agua-butanol (Figura 2C), a bajas concentraciones de agua la adsorción sobre el catalizador aumenta levemente hasta una fracción molar alrededor de 0,5, pero por encima de 0,7 se observa una aumento súbito, alcanzando la saturación por encima de concentraciones de agua superiores al 0,8. Este comportamiento puede ser causado por la resistencia que genera el butanol presente inicialmente en la resina para el acceso del agua debido a la inmiscibilidad de los componentes. Al aumentar el contenido de agua en el medio, la resina la adsorbe selectivamente desplazando al butanol, lo que genera el hinchamiento súbito observado.

Los parámetros obtenidos para el modelo no ideal se presentan en la Tabla 5. Se puede observar una gran divergencia entre los datos experimentales y los obtenidos por evaluación de los dos modelos. El número total de sitios ocupados nS calculados para los tres ensayos es bien diferente, y la relación entre las constantes de equilibrio no corresponde con el hinchamiento selectivo observado en el sólido. Todo lo anterior indica que el modelo no representa bien el comportamiento fisico-químico del sistema, principalmente por la existencia de absorción selectiva, la simultaneidad de los fenómenos adsorción y absorción, la interacción entre los compuestos dentro de la resina, y el carácter iónico y elástico de la matriz polimérica, que lo alejan de la concepción de sólido ideal.
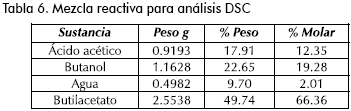
Debido a la imposibilidad de obtener datos confiables a través de los ensayos de adsorción binaria, se realizó la evaluación de la adsorción por medio de ensayos calorimétricos (Zimehl, 1998; Ruffmanna et al., 1999) tanto de los compuestos puros como de la mezcla reactiva (las composiciones se presentan en la Tabla 6). Las muestras de catalizador (1 g), se dejaron sumergidas en 5 ml de solvente por 48 horas a temperatura ambiente. La concentración de la mezcla reactiva se preparó en condiciones cercanas al equilibrio químico de la reacción equimolar, según lo establecido en ensayos preliminares (Orjuela, 2003).
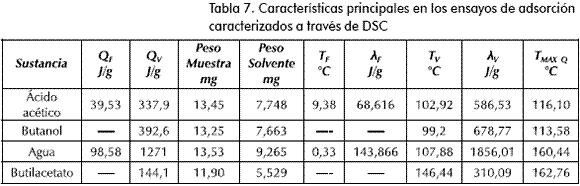
Antes del análisis calorimétrico, los sólidos fueron filtrados y se les retiró el exceso de solvente con un papel adsorbente. En la Figura 3 se presentan algunos perfiles calorimétricos, y en la Tabla 7 se resumen las características obtenidas de estos ensayos.
En el caso del la resina saturada con butanol, se observan dos picos ubicados alrededor de las temperaturas de ebullición del alcohol puro, lo que indica algún tipo de interacción con la estructura de la resina polimérica o sus grupos activos (Dhanuka, 1997; reportó la formación de enlaces químicos seudoestables entre el butanol y los grupos sulfónicos).
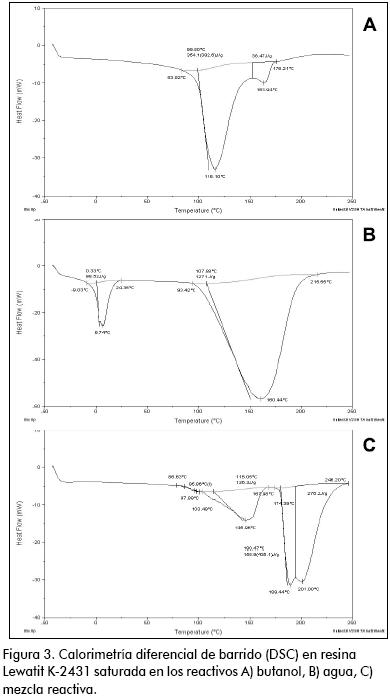
La muestra saturada con agua presenta un hombro en el pico de baja temperatura (fusión). Este comportamiento es similar al presentado en algunos sólidos que contienen agua libre (hinchamiento) y agua ligada (quimiadsorbida o de la estructura polimérica). Esto se explica considerando la alta afinidad de los grupos sulfónicos de la resina por el agua. Para la mezcla multicomponente se observa que los picos asociados a las diferentes sustancias se superponen, y los fenómenos calóricos quedan enmascarados. Hay indicios de interacciones entre los componentes de la mezcla, ya que se presenta una variación en las temperaturas máximas de los picos, respecto de los análisis realizados sobre los componentes puros.
Para el cálculo de las entalpías de fusión y vaporización se supuso inicialmente que la resina se saturó en los diferentes componentes (estado de equilibrio de adsorción evaluado en los ensayos de hinchamiento) y que todo el calor correspondiente a cambios de fase afectó solamente al líquido adsorbido y no a la fase polimérica.
Analizando las temperaturas asociadas a los cambios de fase en los diferentes ensayos (puntos de fusión y ebullición) a la presión del sistema; o la temperatura a la que la mayor parte del calor durante la ebullición fue transferido TMAX Q (asociada a la mayor cantidad de masa vaporizada), se encuentra una discrepancia respecto de las temperaturas reportadas para los componentes puros (Venimadhavan et al., 1999; Wasylkiewicz, 2000). Esto se puede explicar considerando que el líquido en la superficie exterior del catalizador cambia de fase más rápidamente que el adsorbido dentro de la matriz polimérica (resistencia a la transferencia de calor intrapartícula).
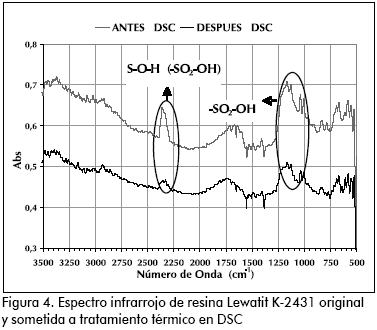
Si se consideran los calores latentes asociados a los cambios de fase, tampoco hay correspondencia con los datos de la literatura. Si la suposición de equilibrio de adsorción es válida (el catalizador fue sometido a condiciones similares a las utilizadas en los ensayos de hinchamiento), esto puede ser causado por dos fenómenos. Como se indicó anteriormente, puede existir una interacción fisico-química entre la resina y los diferentes componentes, o por otro lado, un cambio en la estructura del catalizador durante el tratamiento térmico (transiciones en la fase polimérica, reacciones químicas). Seguramente esto último se propició, pues la resina seca sometida al mismo ensayo resultaba con una coloración oscura muy diferente a la del material original. Para confirmar la naturaleza de la modificación en el sólido resultante se efectuó un análisis de infrarrojo sobre el catalizador seco original y la muestra resultante del ensayo de DSC, el cual se presenta en la Figura 4.
Comparando los perfiles de la muestra tratada térmicamente con la original, se observa una reducción en la absorbancia alrededor de una banda entre 2280 – 2380 cm-1, con una reducción en el pico máximo ubicado en 2350 cm-1. Según lo reportado en la literatura (CRC, 1974), estas bandas corresponden a la absorción del enlace OH dentro de grupos sulfónicos (-SO2-OH), ligados a cadenas carbonadas. Otra ligera reducción se observa entre 1.100-1.200 cm-1 lugares característicos de las bandas de adsorción de los enlaces SO2. La degradación de la matriz sulfonada se debe a la baja estabilidad química de la resina a temperaturas superiores por encima de 130°C (Bayer, A.G., 2001; Coutinho et al., 2004; Patel, 1965). Lo anterior permite concluir que los métodos calorimétricos no son adecuados para cuantificar la adsorción en matrices poliméricas como las estudiadas, debido a que no permiten diferenciar entre las energías asociadas a los cambios de fase de los diferentes compuestos y aquellas generadas por los cambios químicos del sólido, así como las interacciones de este con los solventes y de estos entre sí.
Conclusiones y resultados
En el presente trabajo se realizó un reconocimiento preliminar sobre algunos de los modelos comúnmente utilizados para evaluar la adsorción sobre matrices sólidas. Como resultado de dicho análisis se desarrolló un estudio experimental para evaluar los parámetros de adsorción del modelo de Kippling, asociado a la de ley de acción de masas, en el sistema reactivo ácido acético – butanol – agua– acetato de butilo, sobre una resina de intercambio Lewatit K-2431. Se pudo corroborar la adsorción selectiva de la matriz polimérica en el orden: agua >> butanol ≈ ácido >> acetato; y se apreció un notable aumento de volumen de la resina (hinchamiento de 2,2 a 3,8 veces), lo que indica la coexistencia de los fenómenos de adsorción y absorción.
Se determinaron las limitantes del modelo de adsorción compuesta para ajustar los datos obtenidos experimentalmente en el sistema en estudio, lo que sugiere la imposibilidad de correlacionar el fenómeno de absorción en sistemas altamente no ideales, a través de modelos teóricos simples. La existencia de interacciones entre el sólido y los componentes adsorbidos, así como entre estos últimos, se demostró a través de los ensayos de DSC, lo que confirma que buena parte de las suposiciones sobre las que se fundamentan los modelos teóricos no son válidas para sistemas como el estudiado.
Finalmente, se logró demostrar la imposibilidad de obtener parámetros de adsorción a través de análisis calorimétrico, debido no solo a las interacciones fisicoquímicas en el medio, sino también a la inestabilidad térmica de la estructura polimérica (pérdida de grupos sulfónicos), reconocida a través del análisis infrarrojo del sólido. Este estudio permitió establecer la necesidad de desarrollar e incorporar modelos más elaborados, o el uso de expresiones semi empíricas para la evaluación de los parámetros de adsorción sobre catalizadores poliméricos, y sugiere su estudio directamente asociado con ensayos cinéticos de reacción.
Agradecimientos
Este trabajo fue posible gracias a la colaboración de Colciencias y la Universidad Nacional de Colombia, quienes financiaron la investigación bajo el proyecto Ref: 1101-05-035-99.
Bibliografía
Anasthas, H., and Gaikar, V., Removal of acetic acid impurities from ethyl acetate by adsorption on ion exchange resins. Separation Science and Technology, 36(12), pp. 2623-2646, 2001. [ Links ]
Anasthas, H., and Gaikar, V. Adsorption of acetic acid on ion-exchange resins in non-aqueous conditions. Reactive and Funct. Polymers. 47, pp. 23-35, 2001. [ Links ]
Bayer, A.G. Catalysis and chemical processing with Lewatit®, Technical Information, Leverkusen, Germany, 2001. [ Links ]
Bayer, A.G. Bayer Catalyst K 2431 Product Information, Leverkusen, Germany, 2001. [ Links ]
Bevia, F. et al., Quaternary liquid-liquid equilibrium: water – acetic acid – butanol – n-butyacetate at 25°C., Fluid Phase Equilibria, 18, pp. 171-183, 1984. [ Links ]
Condon, J., Calculations of microporosity and mesoporosity by the chi theory method, Micro. and Meso. Mat, 55, pp.15-30, 2002. [ Links ]
Corain, B., et al. Catalysis and polymer networks - the role of morphology and molecular accessibility, Journal of Molecular Catalysis A: Chemical, 177: pp.3-20, 2001. [ Links ]
Coutinho, F. et al. Synthesis, characterization and evaluation of sulfonic resins as catalysts. European Polymer Journal, 40, pp. 1525-1532, 2004. [ Links ]
CRC Handbook of Spectroscopy, CRC Press. Cleveland, USA, pp. 999-1006, 2004. [ Links ]
Dhanuka, V. R. et al., Kinetics of liquid phase esterification of carboxylic acid with alcohols in the presence of acid catalysts, Chem. Eng. Sci, Vol. 32, pp. 551-556, 1977. [ Links ]
Esquivel, M., and Bernardo-Gil, M. Liquid-liquid equilibria for the systems water – alcohols - acetic acid, Fluid Phase Equilibria, 57, pp. 307-316, 1990. [ Links ]
Favre, E. et al., Application of Flory-Huggins Theory to ternary Polymer-Solvent Equilibria: A Case Study, Eur. Polym. J., Vol. 32, pp. 303-309, 1996. [ Links ]
Gangadwala, J. et al. Esterification of Acetic Acid with Butanol in the presence of Ion-exchange resins as Catalysts. Ind. Eng. Chem, Res. Vol. 42, pp. 2146-2155, 2003. [ Links ]
Gangadwala, J. et al. Production of Butyl Acetate By Catalytic Distillation: Process Design Studies. Ind. Eng. Chem. Res., Vol. 43, pp. 136-143, 2004. [ Links ]
Hanika, J. et al. Multi-functional trickle bed reactor for Butylacetate Synthesis. Catalysis Today, Vol. 79-80, pp. 83-87, 2003. [ Links ]
Hanika, J., Kolena, J., and Smejkal, Q. Butylacetate via reactive distillation - modelling and experiment. Chem. Eng. Sci., Vol. 54, pp. 5205-5209, 1999. [ Links ]
Harmer, M., and Sun, Q. Solid acid catalysis using ion-exchange resins. Appl. Catalysis A: General, 221. pp. 45-62, 2001. [ Links ]
Kanazawa, N. et al., Adsorption equilibrium equation of carboxylic acids on anion-exchange resins in water. Journal of Colloid and Interface Science, 238, pp. 196-202, 2001. [ Links ]
Kawase, M. et al. Increased esterification conversion by application of the simulated moving-bed reactor. Chem. Eng. Sci., Vol. 51, No. 11, pp. 2971-2976, 1996. [ Links ]
Kippling, J. J. Adsortion from solutions of non-electrolytes. Academic Press: New York, 1965, pp. 23-69, 1965. [ Links ]
Liu, O. et al. Study on the coupling of esterification with pervaporation. Journal of Membrane Science, 182, pp. 173-181, 2001. [ Links ]
Löning S. et al. Theorical Investigation on the quaternary system n-butanol, butyl acetate, acetic acid and water. Chem. Eng. Tech., Vol. 23, No. 9, pp. 789-793, 2000. [ Links ]
Matatov, Y., and Sheintuch, M. Catalytic fibers and cloths, Review. Appl. Catalysis A: General, 231, pp. 1-16, 2002. [ Links ]
Mazzotti, et al. Kinetics of Liquid-Phase Esterification Catalyzed by Acidic Resins, Ind. Eng. Chem. Res, Vol. 36, pp.3-10, 1997. [ Links ]
Orjuela, A. et al. Estudio de la síntesis de acetato de butilo – 1. Selección del Catalizador, En Revista: Ingeniería e Investigación, Publ. Fac. Ing. Universidad Nacional de Colombia, Bogotá, Vol. 55, pp. 50-60, 2004. [ Links ]
Orjuela, A. et al., Estudio de la síntesis de acetato de butilo – 2. análisis de las condiciones del equilibrio químico, Ingeniería e Investigación, Publ. Fac. Ing., Universidad Nacional de Colombia, Bogotá, Vol. 25, No. 3, pp. 13-21, Dic 2005. [ Links ]
Orjuela, A. Evaluación de un sistema de destilación reactiva a nivel de planta piloto en reacciones de esterificación. Proyecto de grado de maestría en Ing. Química, Universidad Nacional de Colombia, Bogotá, 2003. [ Links ]
Patel, D. and Bafna, S., Molecular sorption on ion exchange resins, Ind. & Eng. Chem. Prod. Res. and Dev, Vol. 4, No. 1, pp. 1-4, 1965. [ Links ]
Rhodes, C. N. et al. Sulphonated polystyrene resins: acidities and catalytic activities, Reactive and Funct. Polymers, Vol. 40, pp. 187-193, 1999. [ Links ]
Romero, C. and Blanco, L. Tópicos en química básica, experimentos de laboratorio, Academia Colombiana de Ciencias Exactas, Físicas y Naturales, Bogotá, Colombia. pp. 193-211, 1996. [ Links ]
Ruffmanna, B. et al. Characterisation of surface modified polystyrene particles by microcalorimetry and liquid sorption, Thermochimica Acta, 337, pp. 55-63, 1999. [ Links ]
Sainio, T., et al. Phase Equilibria in Solvent Mixture-ion Exchange Resin Catalyst System, Fluid Phase Equilibria, 218, pp. 269-283, 2004. [ Links ]
Steinigeweg, S. and Gmehling, J. n-Butyl Acetate Synthesis via Reactive Distillation: Thermodynamic Aspects, Reaction Kinetics, Pilot-Plant Experiments, and Simulation Studies. Ind. Eng. Chem. Res., 41, pp. 5483-5490, 2002. [ Links ]
Song, W. et al. Measurement of Residue Curve Maps and Heterogeneous Kinetics in Methyl Acetate Synthesis. Ind. Eng. Chem. Res, Vol. 37, pp. 1917-1928, 1998. [ Links ]
Tamura, H. et al. Polyfunctionality of carboxyl sites on IRC-50, an MR-type ion exchange resin, evaluated by modeling with the Frumkin isotherm, Reactive and Funct. Polymers 38, pp. 177-181, 1998. [ Links ]
Tao, Z. et al. Comparative study of adsorption isotherms of BSA on DEAE- and CM-dextran-type ion exchangers, Reactive and Funct. Polymers, 32, pp. 257-262, 1997. [ Links ]
Venimadhavan, G. et al., A novel distillate policy for batch reactive distillation with application to the production of butyl acetate. Ind. Eng. Chem. Res, Vol. 38, pp. 714-722, 1999. [ Links ]
Wang, S. et al. Control of a Reactive Distillation Column in the Kinetic Regime for the Synthesis of n-butyl Acetate, Ind. Eng. Chem. Res, Vol. 42, pp. 5182-5194, 2003. [ Links ]
Wasylkiewicz, S. and Ung, S., Global phase stability analysis for heterogeneous reactive mixtures and calculation of reactive liquid-liquid and vapor-liquid-liquid equilibria, Fluid Phase Equilibria, 175, No. 1-2, pp. 253-272, 2000. [ Links ]
Xu, Z. and Chuang, K., Kinetics of Acetic Acid Esterification over Ion Exchange Catalysts, The Canadian Jour of Chem. Eng, Vol 74, pp. 493-500, 1996. [ Links ]
Zhicai, Y.; et al. Esterification-Distillation of Butanol and Acetic Acid, Chem. Eng. Sci, Vol. 53, pp. 2081-2088, 1998. [ Links ]
Zimehl, R., Flow microcalorimetry and competitive sorption II. Liquid sorption and wetting on macroreticular hydrophilic / hydrophobic networks, Thermochimica Acta, 310, pp. 207-215, 1998. [ Links ]














