Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.26 no.2 Bogotá May/Aug. 2006
Óscar Javier Suárez García1
1 Ingeniero químico, Universidad Nacional de Colombia, Bogotá, Ingeniero de producción de Alfacrom Ltda. ojsgiq@yahoo.com
RESUMEN
El presente trabajo tiene como objetivo evaluar de forma cualitativa, a escala de laboratorio, diferentes alternativas para el montaje y operación de un baño de cromo trivalente para obtener recubrimientos de cromo decorativo. Fueron empleadas soluciones de diferentes concentraciones de cromo y diversos agentes formadores de complejos. Este análisis arrojó como resultado inicial que de las soluciones compuestas de cloruros, formiatos y acetatos se obtienen los mejores resultados. Se evaluaron las condiciones de preparación de la soluciones: temperatura y tiempo de formación del complejo de cromo III; también la operación durante proceso de recubrimiento: pH y temperatura. El trabajo experimental fue desarrollado en la empresa Alfacrom Ltda., los parámetros de evaluación fueron: apariencia del depósito de cromo y densidad mínima de corriente a la que aparece el mismo. Se evaluó la resistencia a la corrosión en cámara salina, tomando como referencia un recubrimiento de cromo hexavalente convencional; este ensayo se realizó en el laboratorio de Ingeniería Química de la Universidad Nacional de Colombia. Se concluyó que el recubrimiento con soluciones de cromo trivalente puede ser una alternativa viable técnica y económicamente para cambiar los procesos de cromado convencionales que son altamente tóxicos y contaminantes; sin embargo, se debe continuar la investigación para encontrar las condiciones óptimas del proceso.
Palabras clave: recubrimiento, cromo trivalente, complejos, procesos galvánicos.
ABSTRACT
The present work was aimed at a qualitative evaluation, in the laboratory, of different alternatives for assembling and operating a trivalent chromium bath for decorative chromium plating. Different chromium concentration solutions and different complexing agents were used. The initial result of this analysis was that chloride, formate and acetate solutions produced the best results. Solution preparation conditions were evaluated: temperature, chromium III complex formation time and also operation during the plating process: pH and temperature. The experimental work was done in the Alfacrom Ltda company; the parameters evaluated consisted of the appearance of chromium deposit and the minimum current density at which it appeared. Resistance to corrosion was tested in a saline-spray chamber, taking conventional hexavalent chromium plating as reference. This assay was done in the Universidad Nacional de Colombia’s Chemical Engineering Laboratory. It was concluded that trivalent chromium plating may represent a technical and economic alternative to conventional hexavalent chromium plating, this being a highly toxic and contaminant process. However, research should be continued into finding optimal process conditions.
Keywords: plating, trivalent chromium, complexing, galvanising.
Recibido: abril 17 de 2006
Aceptado: junio 7 de 2006
Introducción
La galvanotecnia es una técnica que consiste en la electrodeposición de un recubrimiento metálico sobre una superficie que puede ser o no metálica. Se recomienda cuando por costos o por razones estructurales es necesario modificar las características del material base, principalmente resistencia a la corrosión, dureza, apariencia, conductividad eléctrica y rozamiento (Acercar, 2003).
Los recubrimientos pueden ser anódicos o catódicos, dependiendo de la posición de la pieza en el terminal anódico o catódico del circuito. Los recubrimientos de cromo decorativo son catódicos y se utilizan para mejorar la apariencia del material base y brindar resistencia a la corrosión en ambientes moderados. Aunque existen diferentes teorías sobre el mecanismo de reacción para la deposición del cromo hexavalente, este se puede resumir en los siguientes pasos (Snyder y Jones, 2004:.
Reacción de deposición de cromo
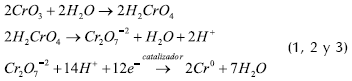
Reacción colateral

En Bogotá, existen aproximadamente 400 plantas galvánicas, el 13% se dedica a procesos de anodizado y preparación de superficies, las restantes realizan procesos de recubrimientos, entre ellos el cromado (Acercar, 2003).
En Colombia estos recubrimientos se emplean principalmente en autopartes, herramientas agrícolas, grifería, muebles, artefactos a gas, entre otros. El proceso convencional de cromado se presenta en la Figura 1.
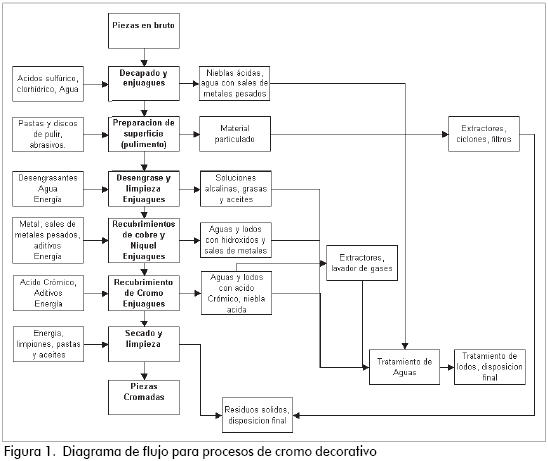
Entre cada operación se tienen tanques con agua para lavar las piezas, así se evita contaminar la solución de la siguiente etapa; las aguas de enjuague son descartadas periódicamente, y debido a que tienen contenido de metales pesados, ácidos, álcalis y otras sustancias peligrosas, deben ser llevadas a una planta depuradora antes de ser vertidas al alcantarillado. El cromado convencional se realiza en soluciones de cromo hexavalente, que contienen entre 200–250 g/L de acido crómico (CrO3) y 1-2 g/L de ácido sulfúrico y fluoro. Silicatos como catalizadores; estas soluciones son altamente corrosivas y presentan gran riesgo para la salud y el ambiente. Debido a la alta concentración de cromo en la solución, se pierden por arrastre en los enjuagues entre 50 y 100 mL de solución por cada m2 de material procesado; además, por la reacción de producción de hidrogeno (ecuación 4) se obtiene una niebla ácida con contenido de material particulado de Cr+6. Las ventajas y desventajas del proceso convencional de cromado se resumen en la Tabla 1.

Los baños de cromo trivalente se desarrollaron a partir de los años setenta como una alternativa para solucionar los problemas asociados al cromado tradicional (Snyder y Jones, 2004). En el medio industrial colombiano los procesos basados en Cr+3 no son utilizados, principalmente por desconocimiento de tecnologías alternativas, lo que dificulta y encarece la implementación de procesos que pueden ser más eficientes y que reducen la generación de residuos y peligros para el medio ambiente y la salud de los trabajadores. El presente trabajo tiene como objetivo evaluar de forma cualitativa y a escala de laboratorio, diferentes alternativas para el montaje y operación de un baño de cromo trivalente para recubrimientos de cromo decorativo, y de esta manera tener un primer acercamiento a esta tecnología con fines de una posible aplicación industrial.
Características de procesos de cromo trivalente
Las principales ventajas de los recubrimientos a partir de cromo trivalente son: 1) baja viscosidad por una menor concentración de cromo, lo que disminuye pérdidas por arrastre de materia prima, 2) menor toxicidad del proceso, 3) el peso equivalente es el doble que el del ión Cr+6, es decir, se obtiene mayor eficiencia catódica, 4) la microestructura del depósito que se obtiene da mayor resistencia a la corrosión y 5) es completamente tolerante a interrupciones de corriente durante el proceso (Dahlhaus , 2005; Snyder y Jones, 2004; Song y Chin, 2002). Sin embargo, el cromo metálico no se puede obtener directamente a partir de una solución de sulfato o cloruro de cromo III, ya que el cromo forma complejos estables e inertes con los iones OH- y Cl-, y también óxidos que interfieren en la reacción catódica, el cromo debe formar un complejo con un compuesto que libere fácilmente el Ion Cr+3 y de esta manera se produzca la reducción a Cr0 (Song y Chin, 2002).
Los formadores de complejos de cromo trivalente comúnmente empleados son: hipofosfito de sodio y glicina, también otros quelantes como ácidos carboxílicos o sus sales, urea, tiourea, tiocianatos y dimetilformamida, entre otros (Barclay, 1977; Barelay, 1981; Benahen, 1986; Bernard y Barnes, 1977; Ward y Barnes, 1979); la formación de los complejos de cromo trivalente no ocurre de manera instantánea, sino que se debe dar un tiempo de reacción hasta lograr el equilibrio; la formación del complejo y por tanto la calidad del recubrimiento de cromo, dependen del pH, temperatura y tiempo de la reacción de complejación. El pH de la solución debe estar entre 2-4 unidades (Bernard y Barnes, 1977), a bajas temperaturas la reacción puede tardar hasta dos meses en llegar al equilibrio (Szyncarzuk et al., 1988 y Szyncarzuk, Drella, y Kubicki, 1989), mientras que a temperaturas más altas, del orden de 90°C o más, el tiempo se puede reducir considerablemente (Bernard y Barnes, 1977).
Bernard y Barnes (1977) han estudiado baños de cromo trivalente con sulfatos o cloruros, con una concentración de 200-250 g/L de sal de cromo y 100 g/L de hipofosfito de sodio de los que se obtuvo recubrimiento brillante en el intervalo de 1.2-35 A/dm2, y con 100g/L de urea el depósito brillante aparece de 8-40 A/dm2. Por su parte, Song y Chin (2002) han empleado soluciones más diluidas de 60 g/L de Cloruro de cromo (III), empleando 28 g/L de formiatos y 12g/L de acetatos, obteniendo también superficies cromadas, y se ha comprobado experimentalmente que los agentes formadores de complejo participan activamente en las reacciones de reducción de Cr+3 (Song y Chin, 2002; Szyncarzuk et al., 1988, y Szyncarzuk, Drella, y Kubicki, 1989) según el siguiente mecanismo:
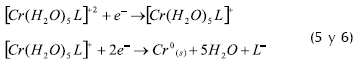
En estas soluciones se deben adicionar otros componentes para mejorar propiedades como estabilidad, conductividad, tensión superficial, entre otras (Barclay, 1977; Barelay, 1981; Benahen, 1986; Bernard y Barnes, 1977; Ward y Barnes, 1979).
Resistencia a la corrosión
Los depósitos de cromo a partir de soluciones de Cr+3 poseen una estructura microporosa (Dahlhaus, 2005 y Snyder y Jones, 2004) que aumenta la resistencia a la corrosión al disminuir la relación área catódica / área anódica en los pares galvánicos Cr/Ni, Cr/Fe, y Ni/Fe que se presentan en una superficie cromada y que son en gran medida responsables de la aparición de manchas de óxido.
Los depósitos de cromo hexavalente pueden ser también microporosos, pero con un tratamiento previo de la superficie durante el niquelado que puede incluir dos o más capas de níquel, con aditivos que permiten la aparición de la estructura (Dahlhaus, 2005), sin embargo, este proceso implica el montaje de instalaciones extras que aumentan los costos de producción.
Cromo trivalente en el mercado
En el mercado internacional existen empresas que distribuyen actualmente productos para el montaje de baños de cromo trivalente; las condiciones varían según el tipo de piezas y el uso de las mismas. Los intervalos de operación son (Atotech, 2004; Enthone Inc., 2003, y Mc Dermid, 2004):
Temperatura: 25-45°C
Densidad: 1.16-1.21 g/cm3 (20-25°Be)
Corriente catódica: 3-20 A/dm2
Relación Ánodo: cátodo = 2:1
pH: 2.5-3.4
Cromo trivalente: 4.5-25 g/L
Tiempo de proceso: 30 segundos a 6 minutos
Agitación: con aire o mecánica
Para velocidades de reacción altas se recomiendan grandes temperaturas, para cromado en bajas densidades de corriente se prefieren valores altos de pH (Atotech, 2004 y Enthone, 2003). Los productos para el montaje y la asesoría para la operación de estos baños se deben importar, el costo comparativo para un tanque de 1500 Litros se presenta en la Tabla 2.

Por los elevados costos de la implementación de esta tecnología con materias primas importadas se presenta la necesidad de experimentar con procesos de cromo III que reúnan las características de calidad, protección y costo para competir en el mercado nacional de los recubrimientos decorativos.
Desarrollo experimental
Debido a la posibilidad de variar componentes en los baños de Cr+3 a evaluar se estableció un procedimiento experimental (ver Figura 2) general en el cual se pudieran cambiar los diferentes insumos y descartar alternativas que no cumplen con los requisitos determinados para cada etapa.
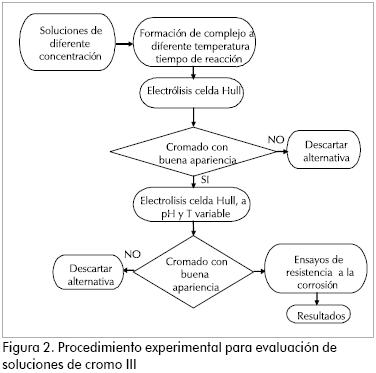
Para la preparación de soluciones se emplearon reactivos grado técnico (ver Tabla 3) de uso industrial común y de fácil consecución en almacenes de productos químicos.

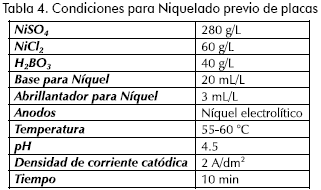
Los ensayos se realizaron en una celda Hull de 277 mL con control de temperatura, un rectificador de corriente con capacidad para 20 amperios y 10 voltios. Los cátodos fueron placas de acero HR con una superficie sumergida de 0.5dm2. Estas fueron previamente niqueladas en un baño tipo Watts, bajo las condiciones presentadas en la Tabla 4.
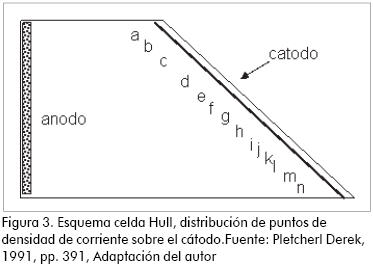
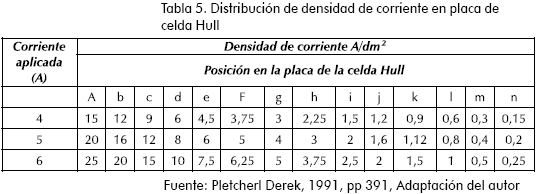
Debido a que en la celda de Hull la densidad de corriente en el cátodo varía con la distancia al ánodo, la determinación de densidad en que se obtiene el recubrimiento de cromo se realizó basándose en las convenciones de la Figura 3 y la Tabla 5.
Preparación de cloruro de cromo
Se preparó una solución de 330 g/L de sulfato básico de cromo, el pH se ajustó a un valor de 7,0, al que se precipitó el cromo como hidróxido; el sólido se separó por sedimentación y se lavó varias veces hasta que la densidad del agua de lavado fue de 1.02 g/mL; por último, se adicionó ácido clorhídrico al 37% p/v, hasta disolución total del hidróxido. Se obtuvo una solución de cloruro de cromo de densidad 1.10 g/mL que corresponde a una concentración aproximada de 110 g/L de CrCl3 (Perry, Chemical Engeneering´s Handbook, pp 2-100).
Soluciones de cromo III
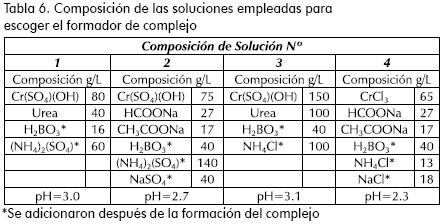
Se prepararon soluciones de diferente composición (ver Tabla 6); en esta etapa se buscó seleccionar la solución de la cual se obtuviera el recubrimiento de mejor apariencia.
Formación de complejos
Para cada tipo de solución se probaron diferentes tiempos y temperaturas de formación de complejos (ver Tabla 7) para su evaluación. Se prepararon volúmenes de 300mL, se ajustó la temperatura, y en ese momento se adicionó el formador de complejo; la temperatura se mantuvo en un intervalo de +-5°C con agitación intermitente. Después de finalizado el tiempo de reacción determinado para cada una, se adicionaron los demás componentes.

Electrólisis
La deposición de cromo se realizó inicialmente a 40°C con una densidad de corriente catódica promedio de 10A/dm2 durante 30 segundos, sin modificar el pH de cada solución. Como ánodo se empleo grafito.
Estudio de condiciones para cromado
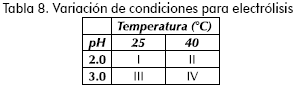
Después de escoger la solución y mejores condiciones de formación de complejo, se preparó solución nueva y se variaron las condiciones de pH y temperatura para la electrólisis de cromo como se muestra en la Tabla 8, la densidad de corriente se mantuvo en 10A/dm2.
Resistencia a la corrosión
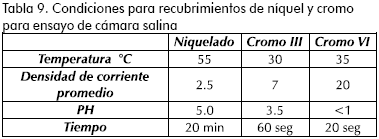
A fin de comparar la resistencia del cromado convencional con el cromado en estudio, se escogieron las mejores condiciones para preparar un baño de 20 litros, se cromaron placas de 10x10 cm en las condiciones de operación presentadas en la Tabla 9 y se realizó la evaluación de la resistencia a la corrosión en cámara salina (prueba realizada por el Laboratorio de Electroquímica y Corrosión de la Facultad de Ingeniería de la Universidad Nacional de Colombia).
Resultados y análisis
Formación de complejos
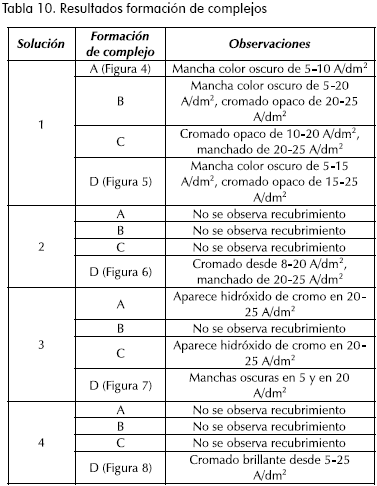
Los resultados se presentan en la Tabla 10. A temperaturas de 60°C y 180 minutos de reacción se obtuvieron los mejores resultados para cada una de las soluciones. A tiempos cortos y bajas temperaturas únicamente se obtuvieron depósitos manchados para la solución 1 (Figura 4). Para las soluciones 2, 3 y 4 no hubo superficie cromada a estas condiciones, lo que evidencia la estabilidad de los complejos inorgánicos, en especial en soluciones con contenido de cloruros (solución 3D, Figura 7).
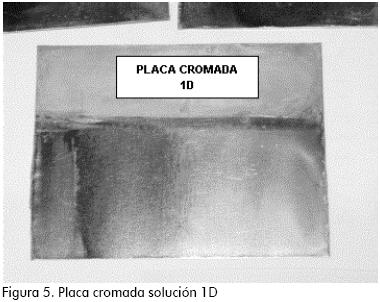
El depósito de cromo se observa manchado para todas las soluciones con contenido de urea (figuras 5 y 6); estas manchas pueden deberse a la deposición de óxidos de Cr+2 y Cr+3 , o por la presencia de Cromo+3 sin acomplejar; para la solución 2D que contiene sulfatos, formiato y acetato (Figura 6) se observa la presencia de un recubrimiento pero únicamente en zonas de alta densidad de corriente (>8A/dm2), lo que disminuye la posibilidad de su uso en una aplicación industrial ya que restringe el uso a piezas con geometrías regulares. Para la solución 4D que contiene cloruros, formiato y acetato (Figura 8) se obtuvo el mejor recubrimiento, este aparece desde zonas de media densidad de corriente (5 A/dm2) y no presenta manchas en la alta densidad de corriente. Se optó entonces por emplear esta solución para el estudio de las condiciones de cromado.








Efecto del pH y temperatura
Los resultados se presentan en la Tabla 11. Se encontró que para las soluciones 4D I y 4D II (figuras 9 y 10), que tienen los valores más bajos de pH, el área de superficie cromada se restringe a los valores de alta densidad de corriente (>8 A/dm2), mientras que a valores altos de pH se el área cromada aumenta (figuras 11 y 12); esto coincide con lo reportado en la literatura, sin embargo, el aumentar la temperatura no presenta ventajas ya que el intervalo de cromado disminuye levemente y el recubrimiento se presenta manchado en la alta densidad de corriente (Figura 12). Se escogieron las condiciones de baja temperatura y alto pH para realizar el ensayo de resistencia a la corrosión.

Resistencia a la corrosión
Los resultados se presentan en la Tabla 12; se observa un mayor deterioro del recubrimiento obtenido a partir de cromo trivalente (Figura 13), este resultado no concuerda con lo reportado en la literatura lo cual quiere decir que aunque se obtienen recubrimientos de buena apariencia, las condiciones no son las óptimas para obtener la máxima resistencia a la corrosión.
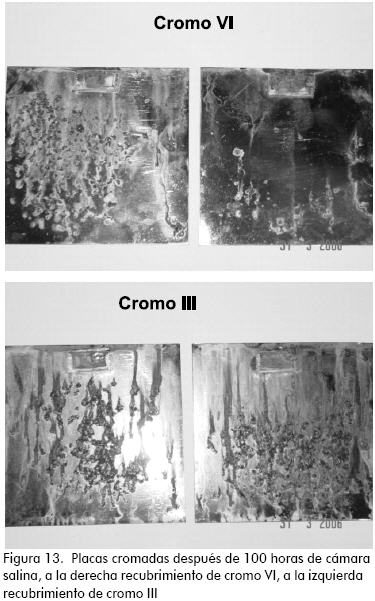
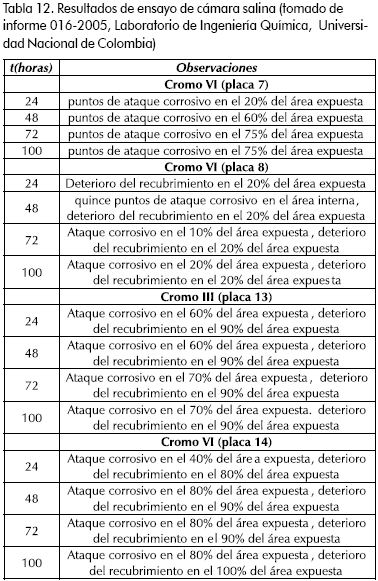
Conclusiones y trabajos futuros
Se obtuvieron recubrimientos de cromo decorativo a partir de soluciones de cromo trivalente, lo cual indica que esta tecnología es una alternativa para mejorar los problemas asociados al proceso de cromado tradicional; el cloruro de cromo acomplejado con formiato y acetato de sodio aparece como la mejor alternativa pues permite obtener recubrimientos brillantes en un intervalo amplio de corriente, con bajas densidades de corriente y con una baja concentración de cromo metálico en la solución, esto es importante para disminuir la pérdida de materia prima por arrastre a los enjuagues; de igual manera, se disminuye la generación de residuos y el consumo de energía en comparación al proceso de cromo hexavalente.
En estos baños a valores bajos de pH se reduce el intervalo de cromado, mientras que a alta temperatura el recubrimiento aparece defectuoso. Las mejores características de apariencia del recubrimiento se obtuvieron a valores altos de pH (3,0 unidades) y temperatura de 30°C, lo cual es un indicio para una futura evaluación de las condiciones óptimas en una aplicación industrial, ya que es necesario continuar la investigación para optimizar el proceso. Los recubrimientos obtenidos a partir de soluciones de sulfatos o urea no tienen buenas características, ya que aparecen manchados y en restringidos intervalos de densidad de corriente.
El recubrimiento de cromo convencional presentó mayor resistencia a la corrosión en cámara salina, lo que indica que las condiciones de trabajo del baño de cromo trivalente en estudio, ya sea formación de complejo, concentración de componentes o condiciones durante el cromado, no son las óptimas para alcanzar la máxima efectividad del recubrimiento.
Los costos de insumos químicos para un baño de 1 500 litros con la formulación escogida son de $1.500.000 aproximadamente, siendo menor que el costo de un baño de cromo hexavalente del mismo tamaño, y aunque no se han determinado las adiciones de materia prima para una producción dada, se estima que el costo no debe ser tan elevado como el presentado para una solución de Cr+3 importada; esto, junto con una disminución en el costo de tratamiento de residuos, hace económicamente viable la alternativa de cambio al proceso de cromo trivalente.
Se recomienda profundizar en esta investigación empleando técnicas como voltametría, coulometría o espectrometría de impedancia, para evaluar las propiedades del recubrimiento a diferentes condiciones de obtención (concentración, formación de complejo y cromado). Es además recomendable determinar las adiciones de insumos químicos según la producción, así como el costo de tratamiento de los residuos producidos por este proceso, para poder realizar un análisis de costos completo y hacer una evaluación de factibilidad económica para el cambio de proceso.
Agradecimientos
El autor expresa sus agradecimientos al ingeniero Alfonso Leyva Santacoloma, gerente general de Alfacrom Ltda.; al ingeniero Diego Camilo Mancipe, Msc. Universidad de Salamanca; y a todo el personal de Alfacrom Ltda.
Bibliografía
ACERCAR Industria, Planes de acción para mejoramiento ambiental GALVANOTECNIA., 2003. [ Links ]
Atotech USA Inc., Tri-chrome PLUS, Trivalent chromium plating process., Technical data sheet., 2004. [ Links ]
Barclay, D. J. y Morgan, W., Electrodeposition of Chromium., United States Patent 4 062 737, Diciembre ,1977. [ Links ]
Barclay, D. J., Vigar J. M.L., Low concentration trivalent chromium electroplating solution and process., United States Patent 4 278 512., Julio 1981. [ Links ]
Benahen, P., y Tardy, R., Chromium electroplating trivalent chromium bath therefore and method of making such bath., United States Patent 4 612 091, Septiembre 1986. [ Links ]
Bernard, J. J. y Barnes C., Trivalent chromium plating bath., Patent Specification 1 488 381, Londres, 12 Octubre, 1977. [ Links ]
Dahlhaus, M., Calculating Corrosion., Products finishing, ENTHONE Germany, 2005. [ Links ]
Denis, A. J., Principles and Prevention of Corrosion., Mc Millan Publishing company, 1992. [ Links ]
Dubpernell, G., Chromium modern electroplating., Jhon Wiley & Son Inc, 1974. [ Links ]
ENTHONE Inc., .Triclolyte IV, Trivalent Chromium Process., Technical data sheet, 2003. [ Links ]
Mc Dermid Inc., .Trimac Envirochrome III, Decorative trivalent chromium., Technical data sheet, 2004. [ Links ]
Perry., Chemical Engeneering´s Handbook., 7 ed, Mc Graw Hill,1999. [ Links ]
Pletcher, D., Industrial Electrochemistry., Chapman and Hall., 1991. [ Links ]
Shanin, G. E., Functional plating from solutions containing trivalent chromium ion., United States Patent 5 294 326., Marzo, 1994. [ Links ]
Snyder, D. y Jones, R., Decorative and Functional Trivalent Chromium electroplating., Atotech USA, Suffice Finished, 2004. [ Links ]
Song, Y. B., Chin, D.T., Current efficiency and polarization behavior of trivalent chromium electrodeposition process., Electrochimica Acta, Vol 48, 2002, pp 349-356. [ Links ]
Szyncarzuk, J., Drella, I. y Kubicki J., Electrochemical behaviour of chromium III in the presence of formica acid –I., Electrochimica Acta, vol 34, No 3, 1989, pp 399-403. [ Links ]
Szyncarzuk, J., Drella, I., Kubicki J., Electroreduction of chromium (III)-acetate complex to metallic chromium on the copper electrode., Electrochimica Acta, vol 33, No 4, 1988, pp 589-592. [ Links ]
Ward, J. y Barnes C., Trivalent chromium plating baths., United States Patent 4 157 945, Junio, 1979. [ Links ]














