Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.27 no.1 Bogotá Jan./Apr. 2007
José Daniel Del Río,1 Gustavo Andrés Durán,2 Álvaro Orjuela Londoño,3 Francisco José Sánchez,4 Carlos Alberto Guerrero Fajardo5
1 Ingeniero Químico. Estudiante M.Sc., Departamento de Ingeniería Química, Universidad Nacional de Colombia, Bogotá, correo electrónico: ejddelrioc@unal.edu.co
2 Ingeniero Químico, Universidad Nacional de Colombia, Bogotá, correo electrónico: gadurand@unal.edu.co.
3 Ingeniero químico. M.Sc., profesor, Departamento de Ingeniería Química, Universidad Nacional de Colombia, Bogotá, correo electrónico: aorjuelal@unal.edu.co
4 Ingeniero Químico, M.Sc, Dr. Sc., profesor, Departamento de Ingeniería Química, Universidad Nacional de Colombia, Bogotá, correo electrónico: fjsancezc@unal.edu.co
5 Químico. Ph.D., Ingeniería Química, profesor, Departamento de Química, Universidad Nacional de Colombia, Bogotá, correo electrónico: caguerrerofa@unal.edu.co
RESUMEN
Uno de los grandes retos para la catálisis ha sido la conversión directa de metano en productos químicos útiles a la industria tales como metanol y formaldehído. Actualmente el formaldehído es producido en un proceso que involucra tres pasos con gas de síntesis y metanol como productos intermedios. En este trabajo se emplearon catalizadores de MoO3, Fe2O3 y Fe2(MoO4)3 en cuatro proporciones Mo/Fe diferentes (0.5, 1, 1.5, 2). El catalizador de ferromolibdeno fue preparado por coprecipitación. Los óxidos puros presentan mayor actividad; sin embargo, no son selectivos a formaldehído, siendo los óxidos de carbono (CO, CO2) los principales productos. Los catalizadores de ferromolibdeno mejoran la selectividad a HCHO en detrimento del grado de conversión; el contenido de molibdeno no muestra incrementos en la actividad catalítica. El aumento en la temperatura de reacción no genera un aumento en la selectividad a formaldehído.
Palabras clave: formaldehído, metano, ferromolibdeno, óxido férrico, óxido de molibdeno, oxidación parcial.
ABSTRACT
One of the main challenges for catalysis has been direct methane conversion to useful products such as methanol and formaldehyde. Formaldehyde is currently produced by a three-step industrial process with syngas and methanol as intermediate products. MoO3, Fe2O3 and Fe2(MoO4)3 catalysts were used with four different Mo/Fe molar ratios (0.5, 1, 1.5, 2) in this work. The ferromolybdenum catalyst was prepared by coprecipitation. Pure oxides are more active; however they are not formaldehyde selective, but carbon oxide (CO, CO2) selective. The ferromolybdenum catalysts showed better HCHO selectivity at low conversions; the molybdenum oxide content did not show increased in catalytic activity. Increased reaction temperature did not increase formaldehyde selectivity.
Keywords: formaldehyde, methane, ferromolybdenum, ferric oxide, molybdenum oxide, partial oxidation.
Recibido: marzo 21 de 2006
Aceptado: septiembre 4 de 2006
Introducción
Dados los problemas ambientales generados en las últimas décadas por causa de la emisión de gases de efecto invernadero como el CO2 y CH4 entre otros, y paralelo a esto la rápida disminución de reservas de petróleo así como su disminución en calidad, que conlleva a incrementos en los costos de refinación, se ha visto la necesidad de aprovechar este tipo de sustancias de mejor manera. En el caso del metano, se busca su transformación en sustancias de mayor peso molecular y la adición de grupos funcionales.
Hasta ahora no hay planes claros para el aprovechamiento a nivel macrosectorial de estos gases ricos en metano, exceptuando la producción de energía por medio de su combustión. Con tal propósito se han realizado investigaciones orientadas hacia la oxidación parcial, directa y selectiva de metano a productos como metanol y formaldehído (Arena, 2002; Lunsford, 2000; Otsuka, 2001; Parmaliana, 1998; Takemoto, 2001; Zhang, 2003), proceso que genera una reducción en los costos de producción de estos compuestos químicos comparado con los procesos actuales. En este momento existe un proceso que involucra dos etapas para la obtención de metanol. Consiste en generar gas de síntesis (H2 y CO) y posteriormente la hidrogenación del CO para la obtención del metanol y luego se realiza una oxidación directa del metanol.
Hasta ahora las investigaciones realizadas con el fin de llevar a cabo una oxidación parcial y selectiva del metano a productos oxigenados (metanol y formaldehído, específicamente) en un solo paso, no han logrado encontrar un sistema catalítico capaz de competir con el proceso de dos etapas; sin embargo, se han obtenido resultados positivos y cada vez más alentadores (Herman, 1997).
Muchos de los estudios realizados han encontrado condiciones de operación que permiten que este proceso sea cada vez más factible (Arena, 2000; Arena, 2005; Parmaliana, 2002; Parmaliana, 1996). Dentro de las variables que se han estudiado se encuentran: la relación metano/oxígeno, el agente oxidante, la temperatura de reacción, la relación de recirculación y la adición de vapor de agua al alimento.
En este artículo se resalta la importancia en la investigación de la oxidación parcial de metano y se muestran los resultados obtenidos en los ensayos realizados, haciendo una breve discusión de los mismos.
Desarrollo experimental
Preparación de los catalizadores
Los catalizadores de ferromolibdeno se prepararon por coprecipitación (Sánchez, 1989), utilizando soluciones acuosas de Fe(NO3)39H2O (Merck, > 99,0%) y (NH4)6Mo7O24 (Merck > 99,0%) como precursores de hierro y molibdeno. A la solución de Fe(NO3)39H2O se le adicionó HNO3 y posteriormente se agregó la solución de (NH4)6Mo7O24,. Este procedimiento se realizó bajo una agitación vigorosa. La solución final se concentró a 353 K por cuatro horas para generar una espuma rígida, la cual se calcinó durante ocho horas a 573 K y posteriormente a 773 K por ocho horas más. Mediante este procedimiento se prepararon cuatro catalizadores de ferromolibdeno en proporciones molares Mo/Fe = 0,5, 1, 1,5 y 2.
Los catalizadores de Fe2O3 y MoO3 se prepararon por calcinación de Fe(NO3)3 9H2O y de (NH4)6Mo7O24 a 773 K durante 17 horas (Del Río, 2005).
Caracterización de los catalizadores
La superficie específica de los catalizadores se determinó mediante fisisorción de nitrógeno a 77°K y el área correspondiente se evaluó por el método BET en un sortómetro Coulter SA 3100. Los patrones de difracción de rayos X (XRD) se tomaron con un difractómetro Siemens D5000 equipado de un anticátodo de cobalto (Co Kα = 1,7890 Å). La estructura superficial de los catalizadores se determinó empleando un microscopio E600 equipado con una cámara Coolpix 995 y objetivos de 10, 20 y 40X utilizando campo oscuro.
Ensayos catalíticos
La mezcla reaccionante consistió en CH4, O2 y He como diluyente en relación volumétrica de 3/1/4, respectivamente, con un flujo total de 20 ml/s. El flujo alimentado al sistema de reacción fue medido con válvulas de precisión Brooks Instruments.
Los ensayos catalíticos fueron realizados en un reactor diferencial de cuarzo (forma de U alargada) a presión atmosférica y utilizando temperaturas de 473, 573, 673, 773 K con cada catalizador. Para cada temperatura evaluada se empleó 0.1g de catalizador. Los productos de reacción fueron conducidos por una línea hasta un cromatógrafo de gases. Esta línea se mantuvo a una temperatura de 373 K para evitar la condensación de productos y la polimerización del formaldehído. En la Tabla 1 se muestran las características del método cromatográfico empleado para el análisis de los productos.

Resultados y discusión
Caracterización de los catalizadores
En la Tabla 2 se muestran los resultados del área superficial SBET de los catalizadores preparados. A diferencia de los resultados obtenidos por Soares et al. (Soares, 2001), en los cuales el área BET aumenta con el contenido de molibdeno, en los obtenidos en esta investigación se encuentra una disminución en su valor al aumentar el contenido de molibdeno, excepto en el catalizador de ferromolibdeno Mo/Fe = 1,5.

Las diferencias se pueden atribuir a factores del método de preparación o a la incertidumbre que tiene dicho método.
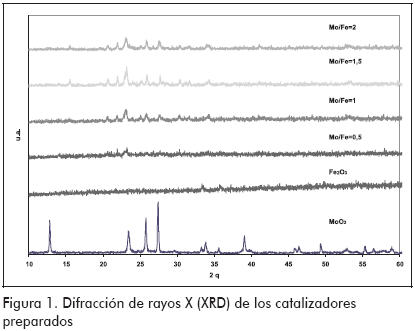
En la Figura 1 se muestra la difracción de rayos X (XRD) de los catalizadores preparados. El MoO3 presenta una alta cristalinidad, comparada con los demás catalizadores. El Fe2O3 no presenta ningún tipo de pico característico, lo que indica que el material es amorfo. El ferromolibdeno presenta picos característicos de la fase ferromolibdeno en las cuatro proporciones Mo/Fe.
En la Figura 2 se muestran las micrografías de la superficie de los catalizadores preparados. Se puede apreciar que los catalizadores con menor contenido de molibdeno (relaciones Mo/Fe = 0,5, 1) presentan pequeños conglomerados de color blanco en la superficie, observando como base el óxido férrico. Estos conglomerados pueden atribuirse a ferromolibdeno, lo que concuerda con los resultados de los difractogramas obtenidos de estos dos catalizadores, en los cuales no existe la presencia de algunos picos que sí son identificables en los catalizadores con mayores contenidos de molibdeno.
El catalizador de ferromolibdeno Mo/Fe = 1,5 muestra algunos puntos de color rojizo, los cuales pueden ser de oxido férrico que no están dentro de la estructura; sin embargo, el mayor porcentaje del sólido muestra una homogeneidad en su estructura, siendo esto indicio de la formación del ferromolibdeno en relación estequiométrica.
El catalizador de ferromolibdeno Mo/Fe = 2 presenta una coloración similar a la del óxido de molibdeno, no obstante, en su estructura se presentan pequeños puntos rojizos que pueden ser estructuras de óxido férrico.
El oxido férrico revela una estructura similar a la de una esponja, mientras que el óxido de molibdeno luce una estructura más definida y una coloración blanca.

Evaluación catalítica
Blancos
En los ensayos realizados sin carga de catalizador se emplearon las mismas condiciones utilizadas en las pruebas catalíticas. Estas permitieron cuantificar los efectos de las paredes del reactor y de las líneas de transporte sobre la reacción.
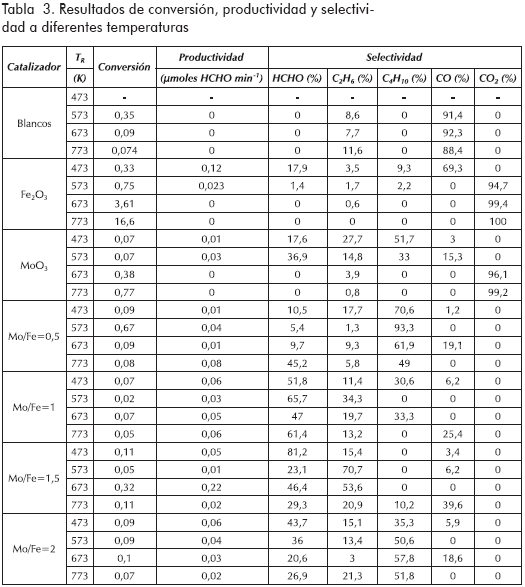
En el ensayo realizado a 573 K se observa la presencia de etano y CO con una conversión de metano de 0,35% y una selectividad de 7,7% y 92,3%, respectivamente. Los resultados de los ensayos realizados se presentan en la Tabla 3.
Para los ensayos realizados a 673 y 773 K se presenta de igual manera la presencia de CO y etano con conversiones de metano de 0,09 y 0,07%. Es extraño el comportamiento presentado con la temperatura de 573 K, en el cual se obtiene una conversión más alta; esto es de esperarse con las temperaturas de 673 y 773K ya que estas favorecerían las reacciones en fase gaseosa; más a 773 K aún no es común encontrar este tipo de reacciones (Arena, 1997).
Fe2O3
Se observó la producción de formaldehído en los ensayos realizados a 473 y 573 K, la cual desaparece por completo en los ensayos de 673 y 773 K, mientras que la producción de CO2 es alta en el transcurso de los ensayos de
Como se esperaba, el óxido férrico promovió la oxidación total de los productos, al aumentar la temperatura de reacción, ya que este es un catalizador que posee una alta actividad y disposición a liberar oxígeno (semiconductor tipo n), lo que le permite actuar como un agente deshidrogenante del metano.
Con este catalizador se logran las conversiones más altas encontradas en todos los ensayos realizados, aunque la selectividad hacia formaldehído decrece sustancialmente con el aumento en la temperatura.
Con estos resultados se puede afirmar que a menores temperaturas existe una mayor probabilidad de encontrar productos parcialmente oxidados, como es el caso del formaldehído, pero esto implica obtener conversiones bajas.
Se puede pensar que el dióxido de carbono logra producirse por dos rutas paralelas; una, en la que el metano sufre una deshidrogenación total permitiendo su paso de manera directa a CO2, mientras que una segunda ruta sería la de la oxidación del CO producido a partir de la oxidación del formaldehído. La primera ruta, de acuerdo con lo expuesto por Herman et al. (Herman, 1997), en la cual el metano se oxida directamente a CO2; de igual manera, la segunda ruta propuesta corresponde al mecanismo planteado por Arena, Fusteri y Parmaliana (Arena, 2002), en el cual el formaldehído se oxida a CO.
MoO3
A las temperaturas de 473 y 573 K se encuentra una amplia distribución de productos, mientras que para las de 673 y 773 K el dióxido de carbono y las trazas de etano son los únicos productos presentes. Se aprecia que a menores temperaturas existe la producción de formaldehído, lo que indica que los oxigenados de interés sufren una oxidación profunda a causa de los efectos térmicos; este comportamiento corresponde a los modelos cinéticos expuestos por Pereira et al. (Spencer, 1991), en los cuales el CO y CO2 provienen de HCHO y CH4, respectivamente. Es de notarse que según estos modelos cinéticos algunas especies activas o los productos originados son capaces de generar otros en su paso sobre el catalizador, en detrimento del producto de interés, lo que ocurre con el CO y el butano, los cuales provienen del HCHO y el etano.
Es notorio que las conversiones alcanzadas por el metano sobre el óxido de molibdeno no superan el 0,5%, las cuales al ser comparadas con las alcanzadas por el óxido de hierro indican que el MoO3 no es un compuesto eficaz para la activación del metano aún a altas temperaturas. Este óxido tiene la capacidad de almacenar oxígeno en su estructura (semiconductor tipo P), lo cual da una idea del por qué genera de manera selectiva productos parcialmente oxidados y no totalmente oxidados, por lo menos a las temperaturas bajas.
Ferromolibdeno
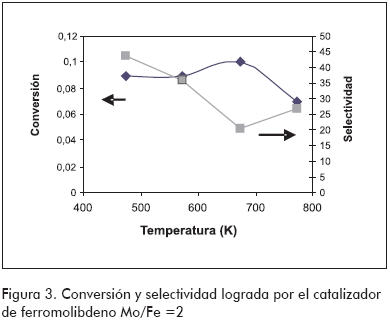
El catalizador con composición Mo/Fe =2 presentó la producción de formaldehído en todo el intervalo de temperaturas, siendo muestra de que es selectivo a este producto, así mismo es notorio que no hay presencia de CO2 en los ensayos realizados con las temperaturas más altas, lo que indica que este catalizador no permite que se presente una oxidación total del metano.
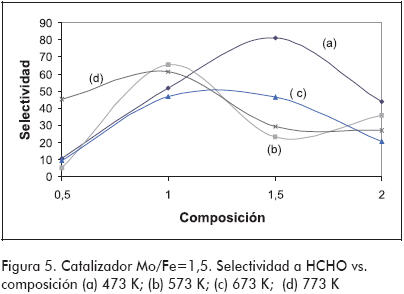
No se pudo apreciar algún tipo de tendencia en la conversión y la selectividad respecto a la temperatura; no obstante, como lo muestra la Figura 3, se ve que los puntos de máxima conversión presentan los de mínima selectividad. Para el catalizador de ferromolibdeno en composición Mo/Fe =1,5 se presentó un comportamiento singular, ya que los puntos de mayor conversión también son los de mayor selectividad. Esto se puede atribuir a que existe, además de la producción de formaldehído, la de etano y CO, el cual genera una mayor conversión del metano. En las figuras 4 y 5 se puede apreciar que este catalizador es uno de los que presentan mejores conversiones y selectividades.
Con el catalizador de ferromolibdeno en composición Mo/Fe = 1 se observó la presencia de formaldehído en todo el intervalo de temperaturas, no se presentó CO2, pero sí hay formación de etano y butano. Al observar los resultados dados en la Tabla 2 es fácil ver que los puntos de máxima conversión son lo de mínima selectividad a formaldehído.
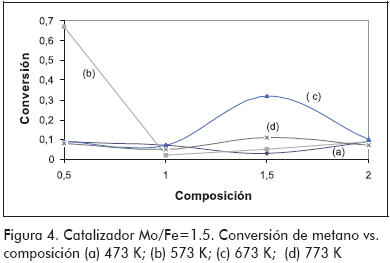
Por último, el catalizador preparado con una composición Mo/Fe=0,5 mostró nuevamente que los puntos de mayor conversión son los de menor selectividad. En la Figura 4 se puede apreciar que a una temperatura de 573 K se dio el máximo valor de conversión, lo cual no es común ya que esto se esperaría con temperaturas más altas. El catalizador de ferromolibdeno Mo/Fe =1,5 mostró una conversión bastante buena con una temperatura de 673 K. Los demás catalizadores indicaron un comportamiento muy estable, en el cual no se observó una influencia marcada por la temperatura; así mismo, no se encontraron diferencias causadas por el contenido de molibdeno. En la Figura 5 se nota que se obtienen mejores selectividades a formaldehído utilizando menores temperaturas de reacción. No se observó una influencia marcada de la composición en cuanto a la selectividad; sin embargo, los catalizadores con relación Mo/Fe de 1 y 1,5 son los que presentan los valores más altos en todo el intervalo de temperaturas.
Conclusiones
Estos resultados permiten afirmar que a menores temperaturas existe una mayor probabilidad de encontrar productos parcialmente oxidados, como es el caso del formaldehído, pero esto implica obtener conversiones bajas.
Existe una interacción entre los reactantes y productos con las paredes del reactor o con las tuberías de acero inoxidable que los transportan, generando productos tales como CO y etano.
El butano y el etano son productos que presentan mayor estabilidad termodinámica que el formaldehído, razón por la que su probabilidad de ocurrencia es mayor bajo las condiciones de reacción utilizadas.
La temperatura es un factor determinante en la obtención de formaldehído a partir de la oxidación de metano, y se puede apreciar que a menores temperaturas de reacción se ve favorecida su producción, aunque la conversión sí se ve notablemente reducida.
Es clara la relación inversamente proporcional entre la selectividad y la conversión. Siendo la temperatura la principal variable a analizar, se encuentra que al incrementar su magnitud aumenta la conversión de los reactantes, mientras que la selectividad disminuye.
Los óxidos Fe2O3 y MoO3 presentaron conversiones considerables a temperaturas elevadas, mientras que los catalizadores de ferromolibdeno generaron conversiones bajas a altas temperaturas a pesar que las micrografías indican que se trata de mezcla de fases de ferromolibdeno, MoO3 o Fe203. Esto se debe probablemente a la mayor presencia de la fase ferromolibdeno o a que los agregados atómicos de los óxidos puros se encuentran en lugares inaccesibles para los reactantes.
Los catalizadores de ferromolibdeno presentan mejores selectividades hacia formaldehído comparados con los óxidos puros, ya que no permiten la oxidación total de los reactivos (formación de CO2), si bien sí permiten la generación de CO.
Agradecimientos
Los autores expresan su agradecimiento a la Dirección de Investigaciones de la sede Bogotá (DIB) de la Universidad Nacional de Colombia, que financió la investigación a través del proyecto 8008010 (Transformación de metano en productos de mayor valor agregado), y en especial al Laboratorio de materiales, polímeros y superficies catalíticas de la Universidad Louis Pasteur, en la ciudad de Estrasburgo, Francia.
Bibliografía
Arena, F., Frusteri, F. and Parmaliana, A., Partial Oxidation of Methane to Formaldehyde A Theoretic-Experimental approach to process design and catalyst development., Journal of Catalysis 207, 2002, pp. 232-236. [ Links ]
Lunsford, J. H., Catalytic conversion of methane to more useful chemicals and fuels a challenge for the 21st century., Catalysis Today 63, 2000, pp. 165-174. [ Links ]
Otsuka, K. and Wang, Y., Direct conversion of methane into oxygenates., Applied Catalysis 222, 2001, pp. 145-161. [ Links ]
Sokolovskii, V. D., Coville, N. J., Parmaliana, A., Eskendirov, I. and Makoa, M., Methane partial oxidation. Challenge and perspective., Catalysis Today 42, 1998, pp. 191-195. [ Links ]
Takemoto, T.,Tabata, K., Teng, Y., Lian-Xin Dai, L. X. and Suzuki, E., Selective oxidation of methane in CH4 – O2 – NO2 over MoO 3., Catalysis Today 71, 2001, pp. 5-13. [ Links ]
Zhang, Q., He, D. and Zhu, Q., Recent Progress in Direct Partial Oxidation of Methane to methanol., Journal of Natural Gas Chemistry 12, 2003, pp. 81-89. [ Links ]
Herman, R.G., Sun, Q., Shi, C., Klier, K., Wang, C. B., Hu, H., Wachs, I. E. and Bhasin M. M., Development of active catalysts for the direct oxidation of the methane to formaldehyde., Catalysis Today 37, 1997, pp. 1-14. [ Links ]
Arena,F., Frusteri, F. and Parmaliana, A., Modeling the Partial oxidation of methane to formaldehyde on silica catalyst., Applied Catalysis 197, 2000, pp. 232-236. [ Links ]
Arena, F. and Parmaliana, A., Working Mechanism of Oxide Catalysts in the Partial Oxidation of Methane to Formaldehyde., Journal of catalysis 167, 1997, pp. 57-65. [ Links ]
Arena, F., Gatti, G., Martra, G., Coluccia, S., Stievano, L., Spadaro, L., Famulari, P. and Parmaliana, A., Structure and reactivity in the selective oxidation of methane to formaldehyde of low-loaded FeO X/SiO2 catalysts., Journal of catalysis 231, 2005, pp. 365-380. [ Links ]
Parmaliana, A., Effect of Fe-addition on the catalytic activity of silicas in the partial oxidation of methane to formaldehyde., Applied Catalysis 226, 2002, pp. 163-174. [ Links ]
Parmaliana, A., Arena, F., Sokolovskii, V., Frusteri, F., Giordano, N., A comparative study of the partial oxidation of methane to formaldehyde on bulk and silica supported MoO3 and V2O5 catalyst., Catalysis Today 28, 1996, pp. 363-371. [ Links ]
Sánchez, F., Estudio de catalizadores y cinética para la oxidación selectiva de etanol a acetaldehído., Tesis presentada a la Universidad Nacional de Colombia, Facultad de Ingeniería, para optar al grado de Magister Science en Ingeniería Química, Bogotá, 1989. [ Links ]
Del Río, J.D. y Durán, G.A., Oxidación Parcial de Metano a Formaldehído empleando un Catalizador de Ferromolibdeno., Tesis presentada a la Universidad Nacional de Colombia. Facultad de Ingeniería, para optar al título de Ingeniero Químico, Bogotá, 2005. [ Links ]
Soares, A. P. V., Portela, M. F., Kiennemann, A., Hilaire, L. and Millet, J. M. M., Iron molybdate catalysts for methanol to formaldehyde oxidation: effects of Mo excess on catalytic behavior., Applied Catalysis 206, 2001, pp. 221-229. [ Links ]
Amiridis, M. D., Rekoske, J. E., Dumesic, J. A., Rudd, D. F., Spencer, N. D. and Pereira, C.J., Simulation of methane partial oxidation over silica-supported MoO3 and V2O5., AiChE Journal, January, Vol. 37, No. 1, 1991. [ Links ]














