Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.27 no.3 Bogotá Sep./Dec. 2007
Alba Nelly Ardila Arias1 y Consuelo Montes de Correa2
1 Licenciada en educación biológica y química. Especialista en didáctica de las ciencias con énfasis en matemáticas y física. M. Sc., Ciencias Químicas, Universidad de Antioquia.. Docente Politécnico Colombiano Jaime Isaza Cadavid, Medellín-Colombia. albanellya@gmail.com
2 Ph.D., en ingeniería química Profesora en el Departamento de Ingeniería Química, Universidad de Antioquia, Medellín, Colombia. cmontes@udea.edu.co
RESUMEN
Se presenta una visión general de la problemática actual de las emisiones de compuestos organoclorados ligeros, y las principales características y ventajas de la hidrodecloración catalítica en fase líquida. Se describen los mas importantes catalizadores utilizados en el proceso de hidrodecloración, haciendo énfasis en los de paladio; su naturaleza, actividad y desactivación. Se explica detalladamente el efecto de varios parámetros, tales como: HCl producido, solvente, base y agente reductor utilizados en el proceso de hidrodecloración. Finalmente, se muestran los principales resultados de estudios cinéticos, el tipo de reactores usados, y se resumen los aspectos más relevantes de la revisión bibliográfica.
Palabras clave: compuestos organoclorados ligeros, diclorometano, cloroformo, tetracloroetileno, hidrodecloración catalítica en fase líquida, catalizadores de paladio, HCl producido, agentes reductores utilizados, bases utilizadas, solventes usados, estudios cinéticos.
ABSTRACT
This survey was aimed at introducing the effect of light organochlorinated compound emissions on the environment, particularly on water, air, soil, biota and human beings. The characteristics and advantages of liquid phase catalytic hydrodechlorination as a technology for degrading these chlorinated compounds is also outlined and the main catalysts used in the hydrodechlorination process are described. Special emphasis is placed on palladium catalysts, their activity, the nature of active species and deactivation. The effect of several parameters is introduced, such as HCl, solvent, base addition and type of reducing agent used. The main results of kinetic studies, reactors used and the most important survey conclusions are presented.
Keywords: light organochlorinated compound, liquid phase catalytic hydrodechlorinarion, palladium catalyst, HCl produced, reducing agent, base, solvent, kinetic study.
Recibido: mayo 18 de 2007
Aceptado: octubre 16 de 2007
Introducción
Los solventes clorados volátiles son compuestos que contienen principalmente de uno a seis átomos de carbono, uno o más átomos de cloro en su estructura, y generalmente sus puntos de ebullición están comprendidos entre 20 y 220 °C. La capacidad de estos compuestos para desplazarse a cualquier parte del planeta; ha causado contaminación no solo en áreas cercanas a las fuentes de origen, sino también en lugares recónditos del planeta, ya que pueden depositarse en la biota, sedimentos, suelo, aire y agua por varios mecanismos como volatilización, sedimentación, vaporización, escurrimiento o dispersión global. Los compuestos organoclorados constituyen uno de los tipos de contaminantes atmosféricos que más preocupación han despertado en las últimas décadas, pues incluyen una gran cantidad de productos tóxicos para el ser humano, cuya velocidad de degradación en suelos y aguas es baja, lo que agrava sus efectos. Asimismo, estos compuestos son capaces de generar radicales libres en la atmósfera, dañando de este modo la capa de ozono (López et al., 2006; Orth et al., 1996; Fernández, 2003).
Dada la toxicidad de estos compuestos, el método de tratamiento más adecuado es la destrucción química. Con la hidrodecloración catalítica en fase líquida se han obtenido buenos resultados, lográndose degradar completamente dichos contaminantes. Este método consiste en hacer reaccionar el compuesto organoclorado con hidrógeno, produciéndose hidrocarburos ligeros (aprovechables por combustión o como materia prima) y cloruro de hidrógeno, fácilmente eliminable por absorción con álcalis. Para que esta técnica sea aplicable se debe disponer de un catalizador muy activo y resistente al envenenamiento por HCl, además de diseñar el equipo para que el aprovechamiento de hidrógeno sea máximo, evitando así el encarecimiento del proceso. En la hidrodecloración catalítica de compuestos organoclorados se usan fundamentalmente catalizadores de metales nobles como Pd, Pt y Rh, soportados usualmente en alúmina, carbón activo y titania. El catalizador de paladio soportado se ha reportado como el más activo y selectivo, sin embargo, se ha observado que se desactiva rápidamente (López et al., 2006; Miranda et al., 2006; Golubina et al., 2003; Martino et al., 1999; Keane, 2004; Aristizàbal et al., 2004). Dada la problemática ambiental que generan los compuestos organoclorados, en este documento se presenta una revisión bibliográfica sobre la hidrodecloración catalítica en fase líquida, la cual se ha vislumbrado como una opción sencilla, económica, efectiva y eficaz para el tratamiento de compuestos organoclorados volátiles.
Problemática
Los compuestos clorados ligeros se usan industrialmente en los sectores de pinturas, limpieza de metales, farmacéuticos, lavanderías e imprentas. Por ejemplo, el diclorometano y el 1,1,1-tricloroetano se utilizan como aditivos de pinturas y adhesivos; el tricloroetileno, tetracloroetileno y el 1,1,1-tricloroetano, como agentes de limpieza en seco y desengrasantes de superficies de metales, pieles, cueros y textiles; el diclorometano, el cloroformo y el 1,1,1-tricloroetano, como agentes extractantes químicos; y el diclorometano y el tetracloruro de carbono como materias primas en síntesis de fármacos, polímeros, fabricación de tintas y disolventes para reacciones químicas (Martino et al., 1999; Ordóñez et al., 2000; López et al., 2003; Calvo et al., 2004).
Las descargas y emisiones de estos compuestos al ambiente son especialmente peligrosas debido a la gran capacidad de distribución que logran en el agua y al alto grado de dispersión que alcanzan en la atmósfera. La toxicidad de dichas sustancias es el resultado de su estructura molecular y el tipo de átomos que las constituyen, pues cabe destacar lo extraordinariamente nocivo que es el cloro orgánico y su efecto devastador que tiene al incorporarse en la cadena alimenticia de los ecosistemas. Por dichas razones, estos solventes hacen parte de las listas de contaminantes prioritarios que presentan riesgos para los ecosistemas y para la salud humana (Ordóñez y Díez, 1999; Ordóñez et al., 1997).
Aunque se han hecho esfuerzos en la búsqueda de alternativas para su reemplazo, los solventes clorados se continúan usando a pesar de su toxicidad. Actualmente su aplicación y demanda sigue siendo alta, lo que conlleva a un elevado volumen de producción y vertido, trayendo como consecuencia la contaminación de suelos, sedimentos y aguas subterráneas y superficiales. Los efluentes que contienen esta clase de compuestos clorados son generalmente de dos tipos: corrientes líquidas acuosas o corrientes líquidas orgánicas. Las primeras pueden ser efluentes industriales, como aguas de proceso de plantas que trabajan con compuestos clorados, se caracterizan por tener una concentración muy baja de estos compuestos dada su baja solubilidad en agua. Sin embargo, tienen un gran poder contaminante debido a la gran capacidad de extensión del compuesto organoclorado en el ciclo hidrológico, llegando a hacer parte de corrientes acuosas naturales e introduciéndose así en la cadena trófica de los seres vivos. Las segundas contienen concentraciones de organoclorados relativamente más altas en comparación con los efluentes acuosos. Estos efluentes son residuos clorados mezclados con otros compuestos orgánicos, polvo, grasas o aceites, que pueden ser producto de corrientes residuales de la industria textil, lavado en seco, procesos de tratamiento de emisiones gaseosas de organoclorados con disolventes o de procesos de adsorción-desorción de efluentes acuosos, entre otros (Ordóñez et al., 1997; Padilla et al., 2005; Ordóñez et al., 2001).
Los solventes clorados contenidos en estos efluentes (por ejemplo, aguas subterráneas poco profundas) se vaporizan y avanzan hacia la atmósfera. Tal tipo de vertidos son emisiones gaseosas descontroladas, de poco volumen y con muchos focos. Una vez en la atmósfera, estos compuestos contribuyen a la degradación de la capa de ozono estratosférico, al calentamiento global del planeta y a la formación del smog fotoquímico, además de efectos directos sobre la salud de los seres vivos (Padilla et al., 2001; et al., 2005). Aunque se cree que la mayor parte de los solventes presentes en los efluentes líquidos acuosos y orgánicos se evaporan fácilmente, su densidad es relativamente mayor que la del agua y llegan a sedimentarse. De esta manera, pueden mantenerse en los sedimentos, suelo y aguas subterráneas por tiempos prolongados. Además, dicho fenómeno facilita la asociación de los residuos clorados a las partículas de suelo, el cual se convierte en fuente contaminante de los cuerpos de agua, principalmente en época de lluvias, afectando la calidad de las aguas de corrientes naturales. Es importante tener en cuenta que aunque la solubilidad de estos compuestos en agua es baja, si un cosolvente completamente miscible con la fase acuosa está presente en el efluente contaminado la solubilidad de los compuestos organoclorados se puede incrementar considerablemente. Esto puede ocurrir normalmente con las descargas de residuos industriales contaminados con solventes organoclorados (Ordóñez et al., 2001).
Los compuestos organoclorados presentes en las aguas suponen un grave riesgo para la salud humana. La mayoría de estas sustancias son muy estables y difícilmente biodegradables, permaneciendo en el medio durante cientos de años, de ahí su denominación de compuestos orgánicos persistentes (COP). Estas sustancias son lipofílicas, por lo tanto, se bioacumulan en el tejido adiposo de los animales y el hombre a lo largo de sus vidas, y sus niveles aumentan de un nivel trófico a otro por un proceso de biomagnificación. De esta manera, los productos agropecuarios (carne, leche y derivados, que son de uso frecuente en la dieta humana) tienen una alta probabilidad de contaminarse y como consecuencia, pueden conducir a intoxicaciones. Asimismo, en las últimas décadas, debido tanto a la explosión demográfica como al desarrollo industrial y agrícola se ha incrementado la demanda de agua, lo que conlleva también riesgos de intoxicación por ingestión de aguas contaminadas (Padilla et al., 2005; Ordóñez, 2000).
La toxicidad de estos compuestos se ha confirmado en diferentes estudios, especialmente con animales, en los que se ha encontrado que inducen actividades enzimáticas mediante radicales libres, afectan los procesos reproductivos, alteran el metabolismo lipídico, trastornan la respuesta inmunológica, el transporte de vitaminas y de glucosa. Además, algunos son considerados mutagénicos, teratogénicos o carcinogénicos, con diferente nivel de sensibilidad no solo en la especie humana, sino también en las comunidades bióticas. Por estas razones, las autoridades competentes han impuesto políticas de minimización y control riguroso en cuanto al uso y descarga de efluentes contaminados con solventes organoclorados, estableciendo límites máximos permisibles de estos contaminantes en las descargas de aguas residuales y bienes nacionales. Además, se han desarrollado varios métodos analíticos para su detección y cuantificación de tal manera que la detección de niveles de solventes organoclorados presentes en aguas superficiales y subterráneas se ha convertido en un tema de interés social debido a su impacto medioambiental negativo. Ello genera la necesidad de tecnologías capaces de degradar estos compuestos con una alta efectividad (International Agency for Research on Cancer World Health Organization, 1995).
Generalmente para el tratamiento de residuos líquidos contaminados con solventes organoclorados se han aplicado métodos no destructivos cuyo objetivo es la recuperación de los compuestos organoclorados para su posterior utilización o para su degradación. Entre estos métodos, los más utilizados para el tratamiento de aguas residuales y la remoción de solventes organoclorados desde los efluentes, están: la adsorción con carbón activado, el arrastre con vapor, tratamientos biológicos, tratamientos con lodos activados, lagunas aireadas y filtros percoladores, entre otros. Sin embargo, dichas técnicas no destructivas requieren de procesos posteriores de tratamiento, lo que en muchos casos las hace complementarias a la eliminación definitiva. Por ejemplo, las industrias, con la intención de minimizar el impacto ambiental de tales productos y a la vez reducir el consumo de estos disolventes, han diseñado equipos en los que estos disolventes circulan en circuitos cerrados. En ellos se separa el disolvente clorado de las grasas e impurezas adquiridas en el proceso de limpieza, extracción, etc., mediante un sistema de evaporación y condensación. Sin embargo, en cada ciclo de este proceso el disolvente se va contaminando progresivamente, con lo que el número de ciclos es limitado, y al final siempre se obtiene una mezcla no utilizable de disolventes contaminados con organoclorados. Además, los residuos de solventes que no se recuperan, sea por razones económicas o por falta de oportunidad técnica, deben ser dispuestos de manera adecuada, aunque en la mayoría de los casos pasan a hacer parte del ciclo hidrológico. Este tipo de residuos de solventes clorados constituyen una fracción importante de los desechos de solventes peligrosos producidos por la industria (Ordóñez y Díez, 1999; Ordóñez et al., 1997; Blanco et al., 1998).
Entre los métodos destructivos para el tratamiento de efluentes clorados, los más utilizados son la incineración térmica, la oxidación catalítica y la reducción con hierro. Sin embargo, con estas técnicas se han presentado inconvenientes como la poca posibilidad de reutilizar los productos obtenidos, la formación de otras sustancias más tóxicas que las de partida, los altos costos de operación y la posibilidad de aumentar la contaminación por el transporte de los residuos del lugar de origen al de tratamiento. El uso de hierro metálico para la decloración reductiva de compuestos organoclorados ha sido el método más utilizado para el tratamiento de los efluentes acuosos. Desafortunadamente esta reacción tiene ciertas limitaciones: las velocidades de decloración son muy lentas, lo que conduce a la acumulación de productos tóxicos en algunos casos, por ejemplo, el tetracloruro de carbono se convierte a cloroformo y más lentamente a cloruro de metileno, acumulándose esencialmente en esta forma. Además, la reacción fracasa para declorar algunos compuestos aromáticos y alifáticos clorados de relevancia ambiental, como el diclorometano y el 1,2-dicloroetano. Asimismo, se presenta el problema de la formación de iones metálicos pesados, que deben ser eliminados en procesos posteriores (Blanco et al., 1998; Aikawa et al., 2003; Padilla et al., 1999; González et al., 1998; Matatov y Sheintuch, 2002; Brink y Louw, 2002; Brink et al., 2000; Criddle y MaCart, 1991; Scott W y Gillham, 1996).
Actualmente se están investigando nuevas tecnologías para el tratamiento de estos efluentes, que sean aplicables a todo tipo de residuos y corrientes acuosas contaminadas con compuestos clorados. En los últimos años la hidrodecloración catalítica en fase líquida catalizada con catalizadores de metales preciosos, se ha vislumbrado como la técnica más adecuada para la degradación de una amplia gama de compuestos clorados contenidos en cualquier matriz, obteniéndose resultados muy satisfactorios. Sin embargo, la tecnología generalmente se ha aplicado a compuestos clorados semivolátiles y de peso molecular apreciable como los clorobencenos, clorofenoles, dioxinas, furanos y bifenilos policlorados, entre otros, los cuales han sido degradados por completo (Hoke et al., 1992; Ukisu et al., 2000; Ukisu y Miyadera, 1997; Mori et al., 2004; Nishijima et al., 2004; Janiak y Blazejowski, 2004; Murena y Gioia, 2004; Yuan y Keane, 2003; Gopinath et al., 2004; Yuan y Keane, 2004; Ukisu y Miyadera 2003 y 2004). De esta manera, la hidrodecloración catalítica usando metales preciosos como catalizadores se considera actualmente como la tecnología más viable para el tratamiento de este tipo de residuos, ya que, además de ser ambientalmente amigable, puede ser incluso competitiva desde el punto de vista económico con respecto a los demás métodos, y aunque se han realizado numerosos estudios aplicando la técnica a matrices gaseosas, en los pocos estudios en los que se ha aplicado a efluentes acuosos se han obtenido excelentes resultados.
Hidrodecloración catalítica en fase líquida
La hidrodecloración catalítica de compuestos organoclorados en fase líquida es un método sencillo, económico y seguro para destruir este tipo de contaminantes. También se ha denominado hidrogenólisis catalítica por el rompimiento del enlace C-Cl o hidrodehalogenación catalítica por el reemplazo de un halógeno por el hidrógeno. En la hidrodecloración catalítica el compuesto organoclorado reacciona con el hidrógeno proveniente de un agente reductor para formar cloruro de hidrógeno fácilmente absorbido con álcalis, y los respectivos hidrocarburos, que son menos tóxicos que los compuestos de partida, los cuales se pueden aprovechar por combustión o como materia prima. Aunque las reacciones de hidrodecloración son exotérmicas, no ocurren en ausencia de catalizador, salvo a altas temperaturas y en presencia de radicales libres. Esto se debe a que la molécula de hidrógeno es muy estable y necesita de un catalizador que la quimiabsorba (Xia et al., 2004; Aramendía et al., 2001; Schüth y Reinhard, 1998; y Ordóñez et al., 2001). La ecuación típica de una reacción de hidrodecloración catalítica es la siguiente:

Esta tecnología tiene las siguientes ventajas frente a otras técnicas utilizadas para el tratamiento de efluentes contaminados con compuestos organoclorados:
- Las instalaciones son bastante sencillas, lo que permite la construcción de pequeñas unidades de tratamiento cercanas a los lugares de producción de los residuos organoclorados, es decir, el tratamiento de los contaminantes in situ, evitándose así el transporte de los contaminantes de un lugar a otro (Calvo et al., 2004; Padilla; Ordóñez, 2006).
- Es efectiva para declorar una amplia variedad de compuestos clorados presentes en cualquier matriz: acuosa, orgánica o gaseosa (Ordóñez, 2006; Ukisu y Miyadera, 2004).
- Se puede realizar bajo condiciones de presión y temperatura mucho más suaves, como temperatura ambiente y presión atmosférica, con lo cual se impide la deposición de materiales carbonosos sobre el catalizador. Además, los problemas de puntos locales de calentamiento en el catalizador son menos agudos (Ukisu y Miyadera, 2004; Bae et al., 2003).
- Es ambientalmente más amigable, ya que las condiciones de trabajo utilizadas impiden la formación de otros contaminantes como COX, NOX, fosgeno, dioxinas y furanos, entre otros. Estas sustancias se caracterizan porque precisan de altas temperaturas y presencia de oxígeno para formarse, condiciones que no se presentan en la hidrodecloración catalítica (Ordóñez et al., 2001; Yuan y Keane, 2003).
- Entre los productos de reacción se encuentran los hidrocarburos directamente reutilizables, ya que se pueden aprovechar por combustión o como materia prima (Martino, 1999; Ordóñez, 2000).
- Se pueden utilizar otros donadores de hidrógeno diferentes al hidrógeno molecular, lo que hace el proceso menos peligroso y más económico y viable a nivel industrial (Martino, 1999; Ukisu y Miyadera, 2003).
- Las condiciones de reacción suaves utilizadas en los procesos de hidrodecloración hacen que esta tecnología sea más económica y competitiva que otros métodos de degradación aplicados actualmente.
Catalizadores de hidrodecloración catalítica en fase líquida
En la hidrodecloración catalítica de compuestos organoclorados se usan principalmente catalizadores de metales preciosos soportados, como paladio, platino, níquel, rodio o rutenio sobre alúmina, sílice, titania o carbón activado. Con estos catalizadores se logran altas conversiones bajo las condiciones de presión y temperatura utilizadas en la hidrodecloración catalítica. Además, debido a las bajas concentraciones con que se opera, los catalizadores tienen un periodo de vida muy largo. Sin embargo, se ha demostrado que se desactivan rápidamente y son muy sensibles a fenómenos de envenenamiento. La mayoría de estudios coinciden en que la actividad de los metales del grupo VIIIB en la hidrodecloración en fase líquida de compuestos organoclorados sigue el orden: Pd >> Pt > Rh > Ru > Ni, considerándose el Pd como el metal más activo y selectivo hacia el hidrógeno y los compuestos organoclorados (Wu et al., 2005; Chang y Thornton, 2000; López et al., 2003; Ukisu et al., 2000).
El paladio se prefiere en las reacciones de hidrodecloración por varias razones. Las fuerzas de los enlaces entre la superficie metálica y el hidrógeno son relativamente altas, principalmente por la presencia de sus orbitales d vacíos. No obstante, la máxima actividad catalítica no se puede conseguir si los enlaces son demasiado fuertes, pues los productos no se liberarían fácilmente. El paladio tiene alta capacidad de adsorber compuestos organoclorados; no obstante, los enlaces entre el cloro y las especies de Pd no son demasiado fuertes. El orden de afinidad de los metales preciosos por el cloruro es Ru >> Rh >> Pt > Pd. Como consecuencia, el Pd presenta cierta resistencia al HCl producido, en comparación con los otros metales utilizados. Así mismo, el paladio tiene la capacidad de operar a condiciones menos drásticas de presión y temperatura (presión atmosférica y temperaturas entre 25 – 200°C). Específicamente, en las reacciones de hidrodecloración el paladio presenta alta actividad para remplazar múltiples átomos de cloro enlazados a un mismo carbono como C2Cl4, CH2Cl2 y CHCl3 (Ukisu et al., 2000: López et al., 2003).
Actividad y desactivación de los catalizadores de paladio
Gran parte de las publicaciones realizadas sobre hidrodecloración catalítica en fase líquida han reportado que el Pd se puede desactivar durante el curso de la reacción, lo cual se ha atribuido principalmente a las especies de paladio presentes, a la dispersión del metal, a las variables de preparación del catalizador (sal precursora y carga del metal, tipo y naturaleza del soporte, temperaturas de tratamiento) y a la presencia de otras sustancias en el medio de reacción como el HCl producido o las sales formadas por la adición de bases, entre otras (Nishijima et al., 2004; Gopinath et al., 2004; Ukisu y Miyadera, 2004; Aramendía et al., 2001; Schüth et al., 1998; Yuan y Keane, 2003; Wu et al., 2005; Chang y Thornton, 2000; López et al., 2003; Mackenzie et al., 2006).
Especies de paladio
En la mayoría de estudios sobre hidrodecloración catalítica en fase líquida con paladio, se ha encontrado que los catalizadores que contienen ambas especies, Pd0 y Pdn+, son activos y selectivos a los compuestos organoclorados. Además, se ha comprobado que los catalizadores que contenían solamente una de estas especies eran inactivos. Se ha propuesto que los sitios activos de paladio tienen una naturaleza dual constituida por la asociación de dos especies; una electrodeficiente en electrones y una de paladio metálico [Pd0⋅⋅⋅⋅Pdn+]. De esta manera, la actividad para la hidrodecloración en fase líquida con paladio está relacionada con la relación Pdn+/Pd0, y la máxima actividad corresponde a una relación Pdn+/Pd0 ≈ 1 (Bae et al., 2003; Yuan y Keane, 2003; Alonso et al., 2002; Aramendía et al., 2002).
Dispersión metálica y sensibilidad a la estructura (structure sensitive)
En general no hay un consenso acerca de si la reacción de hidrodecloración catalizada con paladio es sensible a la estructura o no. Algunos autores presentan datos que permiten asociar el incremento de la dispersión con la disminución de la actividad, pero otros autores reportan lo contrario. Además, los resultados que se presentan en la literatura son difíciles de comparar, ya que las condiciones de reacción, el soporte catalítico, los reactivos usados y las variables de preparación del catalizador, varían mucho de un estudio a otro, haciendo difícil establecer un esquema general o unificado de la química implicada en la reacción de hidrodecloración (Bae et al., 2003; Yuan y Keane, 2003; Alonso et al., 2002; Aramendía et al., 2002).
Precursor del metal
Se ha demostrado que la correcta elección del precursor metálico (libre de iones cloro) es crucial para el óptimo desempeño del sólido final, ya que es posible que el efecto de los iones cloro provenientes del precursor contribuya al auto-envenenamiento del catalizador. Sin embargo, el efecto del precursor del metal no depende solamente de este parámetro. En varias publicaciones (Aramendía et al., 2001; Aramendía et al., 2002; Aramendía et al., 1999) sobre hidrodecloración catalítica de clorobenceno, dicho efecto lo relacionan con la dispersión del metal, encontrándose que al utilizar cloruro de paladio el catalizador exhibe mayor dispersión que el sintetizado a partir del acetilacetonato de paladio, asociando así el incremento de la dispersión con la disminución de la actividad inicial en la hidrogenólisis del clorobenceno. Sin embargo, esta diferencia en la dispersión no es suficiente para explicar la gran disparidad observada en la actividad inicial y en la conversión residual. Es importante tener presente que el efecto del precursor no se debe relacionar en forma aislada, sino también con otras variables sintéticas, por ejemplo, si el soporte está o no dopado. Al evaluar este parámetro, el catalizador cuyo precursor fue cloruro de paladio exhibió la más baja dispersión y la más alta actividad catalítica inicial. En este caso, los iones cloro del precursor de paladio no desactivaron el catalizador, ya que se asociaron con los átomos de sodio contenidos en el soporte del catalizador (Aramendía et al., 2001; Ordóñez et al., 2001; Bae et al., 2003; Mackenzie et al., 2006; Alonso et al., 2001).
Naturaleza del soporte
La elección del soporte y su método de síntesis también son parámetros importantes en el momento de explicar la reactividad del paladio (Aramendía et al., 2001; Ordóñez et al., 2001; Bae et al., 2003; Mackenzie et al., 2006; Alonso et al., 2001). El papel del soporte del catalizador en la hidrodecloración de compuestos organoclorados se ha explicado desde varios puntos de vista, como por ejemplo, las propiedades morfológicas, texturales y ácido-base del soporte y la interacción metal-soporte, entre otras (Aramendía et al., 2001; Ordóñez et al., 2001; Bae et al., 2003; Mackenzie et al., 2006; Alonso et al., 2001; Bae et al., 2003; Yuan y Keane, 2003; Alonso et al., 2002; Aramendía et al., 2002; Ma et al., 2002 y Aramendía et al., 2001). Los estudios cinéticos de las reacciones de hidrodecloración han demostrado la importancia de la naturaleza química del soporte en la velocidad de conversión de los hidrocarburos clorados. La desactivación detectada en algunos catalizadores se ha atribuido al soporte y no a la fase activa. Uno de los soportes sobre los que más se ha profundizado en los trabajos de hidrodecloración catalítica en fase líquida es el carbón activado, ya que posee alta área superficial, permite una adecuada distribución de la fase activa y confiere gran estabilidad térmica, razones por las que se considera un soporte de referencia en los estudios de hidrodecloración en fase líquida. No obstante, últimamente se ha encontrado que la alúmina y la titania son materiales interesantes como soportes del Pd en la hidrodecloración catalítica, debido a su estabilidad térmica y a sus propiedades superficiales básicas, ácidas, reductoras y oxidantes (Nishijima et al., 2004; Murena et al., 2004; Gopinath et al., 2004). La mayoría de investigaciones coinciden en que la actividad catalítica depende de la cantidad de metal expuesto, por lo tanto, el papel primario del soporte es dispersar el paladio metálico, lo cual depende generalmente del área superficial y la fuerte habilidad de adsorción del soporte. A mayor área superficial mayor cantidad de metal activo estará expuesto para la reacción.
Los reportes en cuanto a las propiedades ácido-base del soporte sugieren que estas pueden contribuir a la adsorción o disolución de ciertas sustancias presentes en el medio de reacción. Por ejemplo, en la hidrodecloración catalítica en fase líquida de cloroaromáticos se evaluaron dos soportes de dispersión metálica similar para minimizar el efecto del tamaño de partícula; los sólidos analizados fueron, MgO (esencialmente básico) y ZrO2 (de naturaleza anfotérica, es decir, moderadamente ácido y básico). En el estudio se encontró que el MgO se disolvió con el HCl producido después de cierto tiempo de reacción a valores de pH muy bajos. El soporte ZrO2 puede capturar especies cloruro, por lo tanto, permitió que la reacción finalizara en un tiempo corto. No obstante, en otro estudio sobre la hidrodecloración de dioxinas y furanos utilizando catalizadores de Pd/Al2O3 con diferentes propiedades ácido-base, se halló que los soportes básicos mostraban un incremento en la actividad catalítica. Esto se explicó teniendo en cuenta que los átomos de cloro son capturados por los sitios básicos de la alúmina, favoreciendo así su remoción de la molécula orgánica (Xia et al., 2004; Chang et al., 2000; Aramendía at al., 1999). En otras investigaciones sobre la hidrodecloración catalítica de etilenos clorados, dioxinas y furanos, se evidenció que los soportes hidrofóbicos, tales como el carbón activado, tienen un efecto favorable en este tipo de reacción por la fácil adsorción de los haluros orgánicos hidrofóbicos. El efecto del soporte también se ha analizado en términos de la interfase metal soporte; por ejemplo, en un estudio usando Pd/Al2O3 se sugirió que las especies cloruro desde el metal a la interfase forman especies halogenadas con el soporte, impidiendo así el envenenamiento gradual del catalizador (Nishijima et al., 2004; Aramendía et al., 1999).
HCl producido
Cuando las reacciones de hidrodecloración catalítica se llevan a cabo en fase líquida, el HCl producido durante la reacción aumenta con el progreso de la reacción. Por lo tanto, muchos estudios atribuyen la desactivación del catalizador al envenenamiento de la superficie del mismo por la deposición de HCl. Esto se puede explicar por la habilidad del HCl para clorar los sitios metálicos activos y transformarlos en cloruros estables en la superficie del catalizador, bloqueando los sitios activos disponibles para la conversión del organoclorado. El efecto es más pronunciado a medida que transcurre la reacción, disminuyendo las interacciones entre los compuestos organoclorados y el catalizador. Por lo tanto, el HCl y el organoclorado pueden competir por los mismos sitios activos del catalizador. Además, el medio corrosivo producido por el ácido clorhídrico puede degradar el catalizador (tanto el metal como el soporte), dependiendo especialmente de las propiedades ácido-base del soporte (Aramendía et al., 2002; ángel y Benítez, 2001; Gómez et al., 2004).
Adición de base
Una forma de desvanecer o disminuir el efecto negativo del HCl es adicionando una base al medio de reacción, la cual tiene como función evitar la desactivación del catalizador por deposición del HCl en la superficie. Los hidróxidos que se han utilizado en este tipo de reacciones son NaOH, KOH, NH4OH, RbOH, CsOH y LiOH (Nishijima et al., 2004; Yuan y Keane, 2004; Ukisu y Miyadera, 2003). La efectividad de la base depende de las entalpías de adsorción y su relación con el soporte y el organoclorado para una superficie cargada negativamente. Es importante anotar que no todas las bases utilizadas en las reacciones de hidrodecloración son efectivas. Esto implica que el rol de la base no es solamente neutralizar el HCl. Algunos estudios sugieren que la base facilita la deshalogenación catalítica del compuesto clorado de alguna manera. En casi la totalidad de estudios realizados sobre hidrodecloración catalítica en fase líquida se ha utilizado NaOH como base, pero no se tiene un criterio definitivo para describir el efecto del compuesto básico en este tipo de reacciones, pues la reacción con o sin base depende del tipo de compuesto a hidrodeclorar, de las condiciones de reacción y del catalizador que se utiliza. Algunos autores han encontrado que la reacción de hidrodecloración no se lleva a cabo sin la presencia de un hidróxido, en cambio, otros han degradado el compuesto organoclorado sin una base presente en el medio de reacción. Sin embargo, todos confirman que la adición de una base sirve para limitar el envenenamiento del catalizador con HCl (Nishijima et al., 2004; Yuan y Keane, 2004; Ukisu y Miyadera, 2003; Xia et al., 2004).
Es muy importante tener en cuenta que la cantidad de base adicionada es también un parámetro que debe tenerse presente, ya que esta podría envenenar el catalizador por la deposición de la sal formada (por ejemplo, NaCl) en la superficie del mismo, bloqueando o taponando los poros del soporte e impidiendo el curso de la reacción de hidrodecloración. La mayoría de las investigaciones reportan que la relación base adicionada / ácido clorhídrico liberado debe ser mayor a uno para neutralizar todo el HCl producido durante la reacción. Sin embargo, es primordial tener presente que una concentración de base muy alta no es conveniente, ya que un medio fuertemente alcalino también podría destruir los poros del soporte catalítico y disolver el metal soportado (Ukisu y Miyadera, 2003; Aramendía et al., 2002).
Reactivación del catalizador
Se han desarrollado varios procesos de regeneración de catalizadores desactivados durante el proceso de hidrodecloración, como la extracción de los cloruros quimiabsorbidos sobre el metal precioso mediante disoluciones diluidas de amoníaco-agua, o procesos sucesivos de oxidación con oxígeno a alta presión y temperatura y posterior reducción. El fenómeno de desactivación, regeneración de catalizadores desactivados y el desarrollo de sistemas catalíticos resistentes al envenenamiento son temas que actualmente tienen un alto significado para las reacciones de hidrodecloración catalítica en fase líquida y apenas están en estudio (Ukisu y Miyadera, 2003; Aramendía et al., 2002).
Disolventes utilizados en las reacciones de hidrodecloración catalítica en fase líquida
Varios estudios de hidrodecloración catalítica en fase líquida de compuestos organoclorados han mostrado que la elección del solvente es un factor importante que se debe tener en cuenta para la actividad catalítica, ya que el poder de solvatación depende de la constante dieléctrica, además, de los efectos intrínsecos de los solventes (Ordóñez et al., 2001; Ordóñez, 2000; Scott y Gillham, 1996; ángel, 2001). Varios solventes orgánicos se han evaluado para la decloración catalítica de compuestos organoclorados en fase líquida, entre los cuales, los más utilizados son: n-hexano, tolueno, n-heptano y algunos alcoholes como etanol, metanol e isopropanol (Mori et al., 2004; Janiak y Blazejowski, 2004; Aramendía et al., 2001). Sin embargo, se ha llegado a la conclusión de que los alcoholes secundarios son los mejores disolventes para esta reacción, ya que dichos alcoholes pueden donar el α-hidrógeno durante la reacción de hidrodecloración (Xia y et al., 2004; Yuan y Keane, 2003; Urbano et al., 2001; Yakovlev et al., 2000; Schreier y Reinhard, 1995). Por otro lado, la adición de agua a los alcoholes mejora la degradación de los compuestos clorados y, aunque no hay un consenso en cuanto a cuál es la mejor proporción, la mayoría de estudios coinciden en que los mejores resultados se logran con mezclas 50/50 y 20/80 (v/v) agua-alcohol. El incremento de las velocidades de decloración de los organoclorados debido al aumento en el contenido de agua, se explica principalmente por la naturaleza del catalizador. Así por ejemplo, cuando se utilizan catalizadores de Pd/C, el incremento en la cantidad de agua en el sistema de reacción está relacionado con la adsorción del compuesto organoclorado a la superficie del catalizador, ya que la adsorción de un soluto sobre carbón activo incrementa cuando su solubilidad en el solvente disminuye, propiedad característica de los compuestos organoclorados en el agua.
Existen varias ventajas en cuanto a la adición de agua a los solventes orgánicos, las más obvias son las siguientes (Miyadera, 1997; Janiak y Blazejowski, 2004; Aramendía et al., 2001; Gómez et al., 2004):
- Se evitarían otros solventes que podrían aumentar o empeorar el problema de la contaminación.
- Trabajar con agua es más económico y seguro.
- La mayoría de contaminantes clorados se encuentran mezclados con agua, lo que permite evaluar la actividad del catalizador en un mezcla más parecida a la que se encuentra en condiciones prácticas.
- Los catalizadores de paladio son tolerantes al agua, además, estos se pueden lavar también con agua.
- La utilización de agua produce una mejor ionización de algunas bases, por ejemplo, NaOH, mejorando así su habilidad para neutralizar el HCl producido en la reacción.
- El agua provee una mejor remoción de los productos de reacción adsorbidos en la superficie del catalizador, especialmente sales como el NaCl.
- Un aspecto importante que se debe tener en cuenta cuando se usa un agente reductor y alcoholes secundarios como solventes es considerar que existen dos fuentes competitivas de hidrógeno para la hidrogenólisis del enlace C-Cl, ya que estos pueden actuar como solventes y como donadores de hidrógeno a la vez. Esa es otra ventaja de la utilización de alcoholes como solventes (Gómez et al., 2004).
Agentes reductores utilizados en las reacciones de hidrodecloración catalítica en fase líquida
Hidrógeno molecular. En la mayoría de estudios realizados sobre hidrodecloración catalítica de compuestos organoclorados en fase líquida se ha utilizado el hidrógeno molecular como agente reductor, el cual se oxida formando protones. El hidrógeno ha sido un agente reductor de gran interés, además no forma productos ajenos al sistema que sea necesario eliminar en etapas posteriores (Aramendía et al., 2002; Kopinke et al., 2003 y 2004). Sin embargo, aunque la reducción con hidrógeno está termodinámicamente favorecida, la alta inercia química de esta molécula hace que la reacción no se produzca en ausencia de un catalizador que sea capaz de activarla. El paladio es el catalizador preferido para este tipo de reacciones. Una cuestión importante que se debe considerar al trabajar con hidrógeno molecular, es su baja solubilidad en agua. A 15°C es 0,84 mM a una presión de hidrógeno igual a 100 kPa. Esto puede no ser suficiente para el tratamiento de aguas o residuos altamente contaminados. Por otro lado, las dosis repetidas in situ de este gas dentro del contaminante acuoso puede ser un procedimiento difícil. Adicionalmente, el hidrógeno es un donante de electrones muy digerible para los microorganismos que pueden estar presentes en las corrientes a hidrodeclorar. Igualmente, el trabajo con hidrógeno a escala industrial presenta riesgos, y su costo, comparado con el de otros agentes reductores, puede ser sensiblemente más alto. Otras alternativas al hidrógeno molecular como la hidracina, el ácido fórmico y el isopropanol, que son solubles en agua, se han propuesto para este tipo de reacciones. La solubilidad en agua de estos donantes de hidrógeno puede hacer más factible la inyección de la sustancia pura o en soluciones acuosas altamente concentradas (Ordóñez, 2000; Brink et al., 2000; Ukisu y Miyadera, 2004; Xia et al., 2004; Kopinke et al., 2003).
Hidracina. Se ha demostrado que en ausencia de oxidantes la hidrazina no se descompone espontáneamente en suspensiones acuosas. Sin embargo, la inyección de oxidantes como el oxígeno inician una liberación momentánea de pequeñas cantidades de hidrógeno molecular, el cual se consume rápidamente. En otro estudio se encontró que la hidracina dona efectivamente el hidrógeno para la hidrodecloración catalítica, solamente bajo condiciones alcalinas. Sin embargo, la reacción es más lenta que con hidrógeno molecular en un factor de 30 (Kopinke et al., 2003; Roy et al., 2004).
ácido fórmico. Aunque el ácido fórmico se conoce como un poderoso agente reductor, son pocas las investigaciones en las que se ha evaluado la propiedad de este compuesto como donante de hidrógeno en las reacciones de hidrodecloración catalítica en fase líquida. Sin embargo, estudios sobre hidrodecloración catalítica en fase líquida demuestran que el ácido fórmico es tan buen agente reductor como el hidrógeno molecular bajo condiciones ácidas y neutras, pero menos reactivo bajo condiciones alcalinas. Además, algunos consumidores de hidrógeno como los compuestos clorados y el oxígeno estimulan fuertemente la descomposición del ácido fórmico. Por lo tanto, el ácido fórmico se considera un sustituto promisorio del hidrógeno, desde los puntos de vista químico, técnico y económico (Kopinke et al., 2003; Roy et al., 2004; Aristizàbal, 2003).
Isopropanol. El isopropanol se ha catalogado como el representante más activo del grupo de alcoholes como agente reductor. El isopropanol se ha utilizado en las reacciones de hidrodecloración de algunos solventes clorados, compuestos aromáticos clorados, dioxinas y furanos. Sin embargo, se ha reportado que el isopropanol es alrededor de 5 veces menos reactivo que el hidrógeno, y la velocidad de decloración no varió al aumentar la concentración de isopropanol (en un factor de 10) o el valor del pH de la suspensión acuosa (de 4 a 10) (Mori et al., 2004; Yuan y Keane, 2003; Xia et al., 2004; Kopinke et al., 2003). El isopropanol pertenece a los alcoholes secundarios, los cuales se conocen como los mejores donantes de hidrógeno, ya que el hidrógeno α se libera en las reacciones de hidrodecloración catalítica como especies de hidruro para transformar al sustrato. Cuando los alcoholes primarios tales como el 1-propanol y el etanol se usan como agentes reductores, en muchos casos no se da la degradación del organoclorado, y en otros es muy lenta; mientras que cuando se usan alcoholes secundarios como el 3-butanol y el 2-propanol la actividad es apreciable. Esto confirma que los alcoholes más recomendados como donantes de hidrógeno en las reacciones de hidrodecloración catalítica son indudablemente los secundarios (Aramendía et al., 2002).
Degradación de compuestos organoclorados por hidrodecloración catalítica
Los clorofenoles, clorobencenos, bifenilos policlorados, dioxinas y furanos son los compuestos organoclorados más tratados en las reacciones de hidrodecloración catalítica en fase líquida. Estos compuestos tienen en común un peso molecular apreciable y una estructura carbonada aromática, lo que los hace diferentes a los compuestos organoclorados ligeros. Sin embargo, los mecanismos y datos cinéticos reportados en la literatura sobre estos compuestos han sido muy útiles al tratar otros organoclorados de bajo peso molecular. El compuesto organoclorado de bajo peso molecular más estudiado en reacciones de hidrodecloración catalítica en fase líquida ha sido el tetracloruro de carbono (CCl4). No obstante, se han realizado otras investigaciones menos numerosas con muy buenos resultados, usando tetracloroetileno; (C2Cl4), cloruro de metileno; (CH2Cl2), tricloroetileno; (C2HCl3), cloroformo; (CHCl3) y tetracloroetano; (C2H2Cl4) (Tabla 1). En la gran mayoría de estudios sobre hidrodecloración catalítica, tanto en fase líquida como gaseosa, se han tratado compuestos organoclorados aislados. En la práctica, los compuestos organoclorados se encuentran mezclados. Desafortunadamente, las escasas investigaciones que se han efectuado sobre hidrodecloración de organoclorados mezclados no han sido exitosas a causa de las reacciones competitivas que se pueden presentar entre los componentes, las cuales inhiben los catalizadores (Bustamante, 2006; Santamaría, 2006; González, 2006; Rosy et al., 1995; Roberts et al., 1983; Lowry y Reinhard, 1999; Matheson y Tratnyek, 1994; Siantar et al., 1996; Ordóñez et al., 2003; Filippis et al., 1999; Schüth et al., 2000 y 2004; Mackenzie et al., 2005; Tavoularis et al., 1999; Aristazábal et al., 2004; Fogler, 2001; Lui et al., 2006).
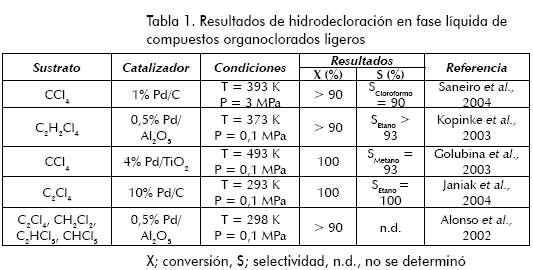
En los estudios realizados sobre hidrodecloración catalítica en fase líquida de solventes organoclorados volátiles se ha llegado a las siguientes conclusiones con respecto a su reactividad:
- En general la velocidad de reacción en la hidrodecloración es inversamente proporcional al número de átomos de cloro en la molécula; los compuestos clorados alifáticos son la excepción, ya que los compuestos con más átomos de cloro se hidrodecloran mejor, siendo el tetracloruro de carbono una de las moléculas cloradas más activas y el diclorometano uno de los compuestos más refractarios a la hidrodecloración. La diferencia en la reactividad de los compuestos alifáticos como diclorometano, triclorometano y los compuestos olefínicos como tricloroetileno y tetracloroetileno se ha explicado mediante mecanismos de radicales libres, donde los enlaces hidrógeno-hidrógeno de la molécula de hidrógeno y los enlaces carbono-cloro en el compuesto organoclorado son activados por el catalizador, teniendo lugar la reacción.
- El diferente grado de reactividad de los organoclorados se ha explicado en los trabajos de hidrodecloración existentes, mediante diferentes mecanismos de reacción basados en varias hipótesis donde se registran diversos fenómenos relacionados con la estructura del compuesto, sugiriéndose por ejemplo la formación de radiales libres, sustancias de naturaleza iónica o presencia de tautómeros durante la interacción de los organoclorados con los catalizadores. Igualmente, se ha discutido la naturaleza del compuesto en cuanto al número de átomos de cloro o de enlaces presentes, y la posibilidad de efectos resonantes, inductivos y estéricos. Todo esto lleva a la obtención de diferentes datos cinéticos de acuerdo no sólo al catalizador, sino también de acuerdo al compuesto modelado, razón por la cual es necesario analizar cada compuesto organoclorado, ya que no existe la posibilidad de extender unos resultados cinéticos para predecir los de otros sistemas con características diferentes (Bustamante, 2006; Santamaría, 2006; González, 2006; Rosy et al., 1995; Roberts et al., 1983; Lowry y Reinhard, 1999; Matheson y Tratnyek, 1994; Siantar et al., 1996; Ordóñez et al., 2003; 1996; Filippis et al., 1999; Schüth et al., 2000 y 2004; Mackenzie et al., 2005; Tavoularis et al., 1999; Aristazábal et al., 2004; Fogler, 2001; Lui et al., 2006).
- Se ha demostrado que el número de cloros afecta el desempeño catalítico para la reacción de hidrodecloración. El estudio de este parámetro es decisivo para evaluar el efecto de un sistema catalítico cuando se usan mezclas de varios organoclorados.
Aspectos relacionados con los reactores utilizados en las reacciones de hidrodecloración catalítica en fase líquida
La parte central del proceso de hidrodecloración es el reactor catalítico, en cuyo diseño se deben tener en cuenta dos factores importantes: por un lado, el reactor ha de permitir enfriamientos rápidos de la mezcla reactiva. Por tratarse de una reacción catalítica exotérmica, los incrementos bruscos de temperatura pueden dañar el catalizador, además de suponer un peligro para la operación de la planta. En segundo lugar, el catalizador puede desactivarse. Las disposiciones de reactores usados son de lecho fijo, tanto en multietapa como en bancada de tubos. Aunque con los primeros la operación es más fácil, se consigue mejorar el proceso con los de bancada de tubos. En los reactores de lecho fijo generalmente se opera en forma trifásica, donde el compuesto organoclorado está en fase líquida, con lo que el reactor se considera de goteo (Ordóñez y Díez, 1997 y 1999; Padilla et al., 2005; Ordóñez et al., 2001; Ordóñez, 2000).
En cuanto a la disposición del reactor donde se llevan a cabo las reacciones de hidrodecloración catalítica en fase líquida, hay tres disposiciones básicas:
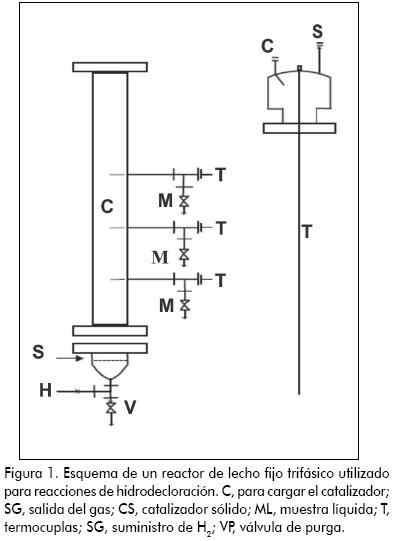
Reactor de lecho fijo trifásico: el compuesto organoclorado está en la fase líquida, bien sea puro o disuelto en un disolvente orgánico, con lo que el reactor se considera de goteo (Figura 1). El control de la reacción es más fácil, pero hay que tener en cuenta los fenómenos de mojado del catalizador.
Reactor de lecho fijo bifásico: utilizado principalmente para efluentes líquidos muy volátiles.
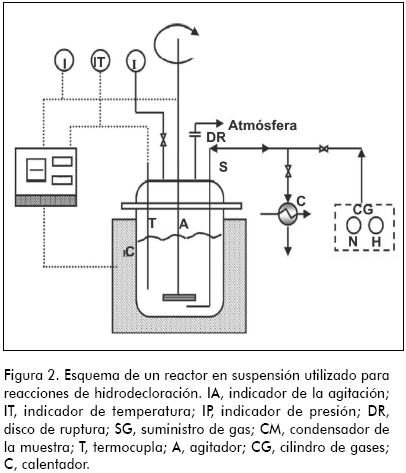
Reactor en suspensión: el catalizador muy finamente dividido se mantiene en suspensión dentro de la masa líquida que contiene el compuesto organoclorado (Figura 2). El volumen de reacción está contenido en un reactor bajo presión de hidrógeno cuando se usa como donante. Estos son menos utilizados a nivel industrial debido a que la separación del catalizador de la fase líquida es difícil.
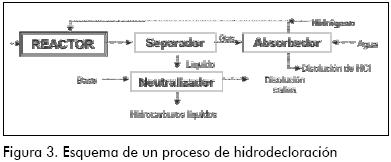
Además del reactor propiamente dicho, el equipo de hidrodecloración en fase líquida debe constar de un absorbedor donde se separe con agua el cloruro de hidrógeno gaseoso formado, obteniendo una disolución acuosa de ácido clorhídrico. Para el HCl disuelto en la fase orgánica, se le añade una disolución acuosa alcalina. Del separador sale una corriente líquida orgánica que contiene el disolvente orgánico e hidrocarburos no clorados, una solución salina inocua que contiene los cloruros formados en la neutralización, y una corriente gaseosa que contiene el hidrógeno sobrante e hidrocarburos de bajo peso molecular. Esta corriente se recircula al reactor, previa purga para la eliminación de hidrocarburos ligeros (Figura 3). Es importante tener en cuenta que la eficacia en la separación y el reciclado del hidrógeno es el factor clave en la economía del proceso (Ordóñez y Díez, 1997 y 1999; Padilla et al., 2005; Ordóñez et al., 2001; Ordóñez, 2000).
Conclusiones
Los compuestos organoclorados constituyen uno de los tipos de contaminantes que más preocupación ha despertado en las últimas décadas, pues incluye una gran cantidad de productos tóxicos para los seres vivos y el medio ambiente.
La destrucción completa de los compuestos organoclorados actualmente es una necesidad inminente, ya que la emisión no controlada de estos compuestos trae consigo una problemática que afecta a cada una de las personas y a las familias como núcleo integrador de la sociedad. Diferentes entidades como las industrias, microempresas, los floricultores, las incineradoras, los químicos farmacéuticos y los cultivadores, entre otros, son los principales responsables en gran medida de dicha problemática, razón por la cual estamos expuestos a los compuestos organoclorados en nuestra vida cotidiana, ya que pasan a hacer parte del agua que tomamos, los alimentos que consumimos y el aire que respiramos, provocando impactos locales y globales de tipo económico, ambiental, científico, tecnológico, social y familiar.
La hidrodecloración catalítica en fase líquida catalizada con paladio es una tecnología viable, económica y ambientalmente amigable para el tratamiento eficiente y eficaz de trazas de compuestos organoclorados ligeros y de peso molecular apreciable presentes en aguas contaminadas y efluentes industriales.
La hidrodecloración catalítica es una tecnología que consiste en poner a reaccionar el compuesto organoclorado con el hidrógeno proveniente de un agente reductor, para formar cloruro de hidrógeno fácilmente absorbido con álcalis, y los respectivos hidrocarburos menos tóxicos que los compuestos de partida, los cuales se pueden aprovechar por combustión o como materia prima. Aunque las reacciones de hidrodecloración son exotérmicas, no ocurren en ausencia de catalizador, salvo a altas temperaturas y en presencia de radicales libres. Asimismo, para que esta técnica sea aplicable debe disponerse de un catalizador muy activo y resistente al envenenamiento por HCl, además de diseñar el equipo para que el aprovechamiento de hidrógeno sea máximo, evitando así el encarecimiento del proceso.
En la hidrodecloración catalítica de compuestos organoclorados se han usado fundamentalmente catalizadores de metales nobles como Pd, Pt y Rh, soportados usualmente en alúmina, carbón activado o titania. El catalizador de paladio soportado se ha reportado como el más activo y selectivo. Sin embargo, se desactiva rápidamente.
Aunque las investigaciones de hidrodecloración catalítica orientadas al tratamiento de compuestos orgánicos clorados contenidos en una matriz líquida son poco numerosas, los resultados obtenidos son muy exitosos. Lo que sí es claro es que todas las investigaciones de hidrodecloración catalítica en fase líquida buscan desarrollar un catalizador activo, selectivo y resistente. Para tal fin, se ha determinado la relación entre las variables de síntesis del catalizador, el HCl producido, la adición de base, la naturaleza del solvente y el tipo de agente reductor, con las velocidades de detoxificación de los compuestos organoclorados, la selectividad y la resistencia del catalizador.
Bibliografía
Aikawa, B.; Buró, R.C.; Sitholé, B.B, Catalytic Hydrodechlorination of 1-Chlorooctadecane, 9,10-Dichlorostearic Acid, and 12,14-Dichlorodehydroabietic Acid in Supercritical Carbon Dioxide., en Applied Catalysis B: Environmental, Vol. 43, 2003, pp. 371-387. [ Links ]
Alonso, F.; Beletskaya, I.P.; Yus, M., Metal-, Mediated Reductive Hydrodehalogenation of Organic Halides., en Chemical Review, Vol. 102, 2002, pp. 4009-4091. [ Links ]
ángel, G.A.; Benítez, J.L., Effect of HCl Acid on the Hydrodechlorination of Chlorobenzene over Palladium Supported Catalysts., en Journal of Molecular Catalysis A: Chemical, Vol., 165, 2001, pp. 9-13. [ Links ]
Aramendía, M. A.; Burch, R.; García, I. M.; Marinas, A.; Marinas, J. M.; Southward, B.; Urbano, F. J., The effect of the Addition of Sodium Compounds in the Liquid Phase Hydrodechlorination of Chlorobenzene Over Palladium Catalysts., en Applied Catalysis B: Environmental, Vol., 31, 2001, pp. 163-171. [ Links ]
Aramendía, M.A.; Boráu, V.; García, I.M.; Jimènez, C; Lafont, F.; Marinas, A.; Marinas, J. M.; Urbano F. J., Influence of the Reaction Conditions and Catalytic Properties on the Liquid-Phase Hydrodechlorination of Chlorobenzene Over Palladium-Supported Catalysts: Activity and Deactivation., en Journal of Catalysis, Vol. 187, 1999, pp. 392-399. [ Links ]
Aramendía, M.A.; Boráu, V.; García, I.M.; Jimènez, C.; Lafont F.; Marinas A.; Marinas J. M.; Urbano F. J., Liquid-phase Hydrodechlorination of Chlorobenzene Over Palladium-Suppoted Catalysts: Influence of HCl Formation and NaOH Addition., en Journal of Molecular Catalysis A: Chemical, Vol.184, 2002, pp. 237-245. [ Links ]
Aristizábal, B.; González, C. A.; Barrio, I.; Montes, M.; Montes de Correa, C., Screening of Pd and Ni Supported on Sol-Gel Derived Oxides for Dichloromethane Hydrodechlorination., Journal of Molecular Catalysis A: Chemical, Vol. 222, 2004, pp. 189-198. [ Links ]
Aristizàbal, Z. B., Hidrodecloración catalítica en fase gaseosa de compuestos organoclorados sobre catalizadores Sol-Gel., tesis presentada a la Universidad de Antioquia, Facultad de Ciencias Exactas y Naturales, para optar por el titulo de Magíster en Ciencias Químicas, Medellín, Colombia, 2003. [ Links ]
Bae, J. W.; Jang, E. J.; Hyun Jo, D., Lee, J.S.; Lee, K. H., Liquid-Phase Hydrodechlorination of CCl4 in a Medium of Ethanol with Co-production of Acetal and Diethyl Carbonate., en Journal of Molecular Catalysis A: Chemical, Vol. 206, 2003, pp. 225-238. [ Links ]
Blanco, J.; álvarez, E.; Knapp, C., en Adsorción y catálisis para reducir la contaminación por compuestos organoclorados, ecología y residuos, s.v., s.n, Madrid, 1998, s.p. [ Links ]
Brink, R.; Mulder, P.; Louw, R., Catalytic Combustion of Chlorobenzene on Pt/g-Al2O3 in the Presence of Aliphatic Hydrocarbons., en Catalysis Today, Vol. 54, 2002, pp. 101-106. [ Links ][/oiserial][/ocitat]
Brink, R.W.; Mulder, P.; Louw, R., Increased Combustion Rate of Chlorobenzene on Pt/g-Al2O3 in Binary Mixtures with Hydrocarbons and with Carbon Monoxide., en Applied Catalysis B: Environmental, Vol. 25, 2000, pp. 229-237. [ Links ] Bustamante, G.A., Hidrodecloración catalítica de diclorometano con catalizadores Pd/TiO2 Sol-Gel., proyecto de grado presentado a la Universidad de Antioquia para optar por el título de ingeniero químico, Medellín, Colombia, 2006. [ Links ] Calvo, L.; Mohedano, A.F.; Casas, J.A.; Gilarranz, M.A.; Rodríguez, J. J., Treatment of Chlorophenols-bearing Wastewaters Through Hydrodechlorination Using Pd/activated Carbon Catalysts., en Carbon, Vol. 42, 2004, pp. 1377-1381. [ Links ] Chang, Z.; Thornton, G., Effect of Pd on the Interaction of Formic Acid with TiO2 (110)., en Surface Science, Vol. 459, 2000, pp. 303-309. [ Links ] Concibido, N.; Okuda, T.; Nakano, Y.; Nishijima, W.; Okada, M., Enhancement of the Catalytic Hydrodechlorination of Tetrachloroetilene in Metanol at Mild Conditions by Water Addition., en Tetrahedron Letter, Vol. 46, 2005, pp. 3613-3617. [ Links ] Criddle, C.S.; MaCart, y P.R., Electrolytic Model System for Reductive Dehalogenation in Aqueous Environments., en Environmental Science Technology, Vol. 25, 1991, pp. 973-978. [ Links ] Fernández, P.; Carrera, G.; Grimalt, J.; Ventura, M., Camaero, L.; Catalan, J.; Nickus, U.; Thies, H.; Psenner, R., Factors Governing the Atmospheric Deposition of Polycyclic Aromatic Hydrocarbons to Remote Areas., Environmental Science Technology, Vol. 37, 2003, pp. 3261-3267. [ Links ] Filippis, P.; Scarsella, M., Pochetti, F.; Dechlorination of Polychlorinated Biphenyls: A Kinetic Study of Removal of PCBs from Mineral Oils., en Industrial Engineering Chemical Research, Vol. 38, 1999, pp. 380-384. [ Links ] Fogler, H. S., Elementos de ingeniería de las reacciones químicas, 3ª. Ed, Prentice-Hall, EE. UU., 2001, pp. 223-281. [ Links ] Golubina, E.V.; Lokteba, E.S.; Lunin, V.V.; Turakulova, A.O.; Simagina, V.I.; Stoyanova, I.V.; Modification of the Supported Palladium Catalysts Surface During Hydrodechlorination of Carbon Tetrachloride., en Applied Catalysis A: General, Vol. 241, 2003, pp. 123-132. [ Links ] Gómez, S. L; Seoane, X.L.; Fierro, J. L.;Arcoya, A., Liquid-Phase Hydrodechlorination of CCl4 to CHCl3 on Pd/Carbon Catalysts: Nature and Role of Active Species., en Journal of Catalysis, Vol. 209, 2002, pp. 279-288. [ Links ] Gómez, S. L.; Seoane, X.L.; Arcoya, A., Hydrodeclorination of Carbon Tetrachloride in the Liquid Phase on a Pd/Carbon Catalyst: Kinetic and Mechanistic Studies., en Applied Catalysis B: Environmental, Vol. 53, 2004, pp. 101-110. [ Links ] González, C. A., Hidrodecloración catalítica de diclorometano en presencia de cloroformo o tetracloroetileno. Estudio cinético., tesis presentada a la Universidad de Antioquia para optar por el título de magíster en ingeniería química, Medellín, Colombia, 2006. [ Links ] González, V. J.; Aranzábal, A.; Gutiérrez, O. J.; Lòpez, F. R.; Gutiérrez, O. M., Activity and Product Distribution of Alumina Supported Platinum and Palladium Catalysts in the Gas-Phase Oxidative Decomposition of Chlorinated Hydrocarbons., en Applied Catalysis B: Environmental, Vol. 19, 1998, pp. 189-197. [ Links ] González, C.A.; Bustamante, F.; Montes de Correa, C., Hidrodecloración catalítica de diclorometano, cloroformo y tetracloroetileno., Revista Facultad de Ingeniería, s.v., No. 38, 2006, pp. 73-87. [ Links ] Gopinath, R.; Lingaiah, N.; Babu, N.; Suryanarayana, I.; Prasad, P.; Obuchi, A., A Highly Active Low Pd Content Catalyst Synthesized by Deposition–Precipitation Method for Hydrodechlorination of Chlorobenzene., Journal of Molecular Catalysis A: Chemical, Vol. 223, 2004, pp. 289-293. [ Links ] Hoke, J. B.; Gramiccioni, G.A.; Balko, E. N., Catalytic Hidrodechlorination of Chlorophenols., Applied Catalysis B: Environmental, Vol.1, 1992, pp. 285-296. [ Links ] International Agency for Research on Cancer World Heald Organization, Larc Monographs on the Evaluation of carcinogenic Risks to Humans, Vol. 63, 1995. [ Links ] Janiak, T.; Blazejowski, J.; Kinetics of 10% Pd/C-Catalysed Hydrogenolysis of Chlorobenzene Dissolved in n-Heptane by Gaseous Hydrogen in Contact with Aqueous NaOH or Water., en Applied Catalysis A: General, Vol. 271, 2004, pp.103-108. [ Links ] Keane, M.A., Hydrodehalogenation of Haloarenes Over Silica Supported Pd and Ni: A Consideration of Catalytic Activity/Selectivity and Haloarene Reactivity., en Applied Catalysis A: General, Vol. 271, 2004, pp. 109-118. [ Links ] Kopinke, F.D.; Mackenzie, K.; Köhler, R., Catalytic Hydrodechlorination of Groundwater Contaminants in Water and in the Gas Phase Using Pd/g-alumina., en Applied Catalysis B: Environmental, Vol. 44, 2003, pp. 15-24. [ Links ] Kopinker, F. D.; Mackenzie, K.; Koehler, R.; Georgi, Anetty, Alternative Sources of Hydrogen for Hydrodechlorination of Chlorinated Organic Compounds in Water on Pd Catalysts., en Applied Catalysis A: General, Vol. 271, 2004, pp.119-128. [ Links ] Lòpez, E.; Ordóñez, S.; Sastre, H.; Díez, F., Kinetic Study of the Gas-Phase Hydrogenation of Aromatic and Aliphatic Organochlorinated Compounds Using a Pd/Al2O3 Catalysts., en Journal of Hazardous Materials, Vol. B97, 2003, pp. 281-294. [ Links ] Lòpez, E.; Ordóñez, S., Dìez, F.; Deactivation of a Pd/Al2O3 Catalyst Used in Hydrodechlorination Reactions: Influence of the Nature of Organochlorinated Compound and Hydrogen Chloride., en Applied Catalysis B: Environmental, Vol. 62, 2006, pp. 57-65. [ Links ] López, E.; Ordóñez, S.; Díez, F., Inhibition Effects of Organosulfphur Compounds on the Hydrodechlorination of Tetrachloroethylene Over Pd/Al2O3 Catalysts., en Catalysis Today, Vol. 84, 2003, pp. 121-127. [ Links ] López, E.; Ordóñez, S.; Sastre, H.; Díez, F.V., Kinetic Study of the Gas-phase Hydrogenation of Aromatic and Aliphatic Organochlorinated Compounds Using a Pd/Al2O3 Catalyst., en Journal of Hazardous Materials, Vol. B97, 2003, pp. 281-294. [ Links ] Lowry, G.; Reinhard, M., Hydrodehalogenation of 1-to3-Carbon Halogenated Organic Compouds in Water Using a Palladium Catalyst and Hydrogen Gas., en Environmental Science Technology, Vol. 33, 1999, pp.1905-1910. [ Links ] Lui, X.; Lu, G.; Guo, Y.; Wang, Y.; Wang, X., Catalytic Transfer Hydrogenolysis of 2-phenyl-2-propanol Over Palladium Supported on Activated Carbon., en Journal of Molecular Catalysis A: Chemical, Vol. 252, 2006, pp. 176-180. [ Links ] Mackenzie, K.; Frenzel, H.; Kopinke,F.; Hydrodehalogenation of Halogenated Hydrocarbons in Water with Pd Catalysts: Reactions Rates and Surfaces Competition., en Applied Catalysis B: Environmental, 63, 2006, pp. 161-167. [ Links ] Martino, M.; Rosal, R.; Sastre, H.; Díez, H., Hydrodechlorination of Dichloromethane, Trichloroethane, Trichloroethylene and Tetrachloroethylene over a Sulfided Ni/Mo-g-Alumina Catalysts., en Applied Catalysis B: Environmental, Vol. 20, 1999, pp. 301-307. [ Links ] Matatov, M. Y.; Sheintuch, M., Hydrotreating Processes for Catalytic Abatement of Water Pollutants., en Catalysis Today, Vol. 75, 2002, pp. 63-67. [ Links ] Matheson, L.J.; Tratnyek, P.G.; Reductive Dehalogenation of Chlorinated Methanes by Iron Metal., en Environmental Science Technology, Vol. 28, 1994, pp. 2045-2053. [ Links ] Miranda, B.; Díaz, E.; Ordòñez, S.; Vega, A.; Díez, F., Performance of Alumina-Supported Noble Metal Catalysts for the Combustion of Trichloroethene at Dry and Wet Conditions., en Applied Catalysis B: Environmetal, Vol. 64, 2006, pp. 262-271. [ Links ] Mori, T., Kubo, J.; Morikawa, Y., Hydrodechlorination of 1,1,1-Trichloroethane over Silica-Supported Palladium Catalysts., en Applied Catalysis A: General, Vol. 271, 2004, pp. 69-76. [ Links ] Murena, F.; Gioia, F., Diffusional Kinetics in the Catalytic Hydrodechlorination of Chlorobenzene in Multiphase Aqueous Mixtures., en Applied. Catalysis A: General, Vol. 271, 2004, pp. 145-151. [ Links ] Nishijima, W.; Ochi, Y.; Tsai, T.; Nakano, Y.; Okada, M.., Catalytic Hydrodechlorination of Chlorinated Ethylenes in Organic Solvents at Room Temperature and Atmospheric Pressure., en AppIied Catalysis B, Vol. 51, 2004, pp. 135-140. [ Links ] Ordóñez, G. S., Hidrodecloración catalítica de compuestos alifáticos clorados., tesis presentada a la Universidad de Oviedo para optar por el título de doctor en ingeniería química, Oviedo, España, 2000. [ Links ] Ordóñez, G. S.; Díez, S. F.; Sastre, A., Emisiones de disolventes clorados ligeros: problemática medioambiental y tratamiento., en Ingeniería Química, Vol. 29, No. 331, 1997, pp. 185-192. [ Links ] Ordóñez, G. S.; Díez, S.F.; Sastre, H., Tratamiento de efluentes orgánicos contaminados por compuestos clorados ligeros., en Retema, s.v., s.n., 1999, pp. 9-23. [ Links ] Ordóñez, S.; Sastre, H.; Díez, F. V., Characterization and Activation Studies of Sulfided Red Mud Used as Catalysts for the Hydrodechlorination of Tetrachloroethylene., en Applied Catalysis.B: Environmental, Vol. 29, 2001, pp. 263-273. [ Links ] Ordóñez, S.; Sastre, H.; Díez, F., Catalytic Hydrodechlorination of Tetrachloroethylene over Red Mud., en Journal of Hazardous Materials., Vol. B81, 2001, pp. 103-114. [ Links ] Ordóñez, S.; Sastre, H.; Díez, F.; Hydrodechlorination of Aliphatic Organochlorinated Compounds Over Commercial Hydrogenation Catalysts., en Applied Catalysis B: Environmental, Vol. 25, 2000, pp. 49-58. [ Links ] Ordóñez, S.; Sastre, H.; Díez, F.V., Hydrodechlorination of Tetrachloroethylene over Pd/Al2O3: Influence of Process Conditions on Catalyst Performance and Stability., en Applied Catalysis B: Environmental, Vol. 40, 2003, pp. 119-130. [ Links ] Orth, W.S.; Gillham, R.W., Dechlorination of Trichloroethene in Aqueous Solution Using Fe0., en Environmental Science Technology, Vol. 30, 1996, pp. 66-71. [ Links ] Padilla, A.M., Corella, J.; Toledo, J.M., Total Oxidation of Some Chlorinated Hydrocarbons with Commercial Chromia Based Catalysts., en Applied Catalysis B: Environmental, Vol. 22, 1999, pp. 107-121. [ Links ] Padilla, B.V.; Díez, S.F.; Ordóñez, G.S., Tratamiento de efluentes acuosos contaminados con compuestos organoclorados., en Ingeniería del Agua, Vol. 12, No. 4, 2005, pp. 361-375. [ Links ] Roberts, P.V.; Dändllker, P.G., Mass Transfer of Volatile Organic Contaminants from Aqueous Solution to the Atmosphere During Surface Aeration., en Environmental, Science, Technology, Vol. 17, 1983, pp. 484-489. [ Links ] Rosy, M.;Quintus, F.; Nic, K., A Method for the Rapid Dechlorination of Low Molecular Weight Chlorinated Hydrocarbons in Water., en Water Research, Vol. 29, 1995, pp. 2434-2439. [ Links ] Roy, H.; Wai, C.; Yuan, T.; Kim, J., Marshall, W., Catalytic Hydrodechlorination of Chlorophenols in Aqueous Solution Under Mild Conditions., en Applied Catalysis A: General, Vol. 271, 2004, pp.137-143. [ Links ] Santamaría, D.C., Efecto de las condiciones de pretratamiento de los catalizadores de paladio soportados en alúmina Sol-Gel en la actividad de Pd/Al2O3 para la hidrodecloración catalítica de diclorometano gaseoso., tesis de pregrado presentada a la Universidad de Antioquia para optar por el título de ingeniero químico, Medellín, Colombia, 2006. [ Links ] Schreier, C.G.; Reinhard, M., Catalytic Hydrodehalogenation of Chlorinated Ethylenes Using Palladium and Hydrogen for the Treamentd of Contaminated Water., en Chemosphere, Vol. 31, 1995, pp. 3475-3487. [ Links ] Schüth, C.; Disser, S.; Schüth, F.; Reinhard, M., Tailoring Catalysts for Hydrodechlorinating Chlorinated Hydrocarbon Contaminants in Groundwater., en Applied Catalysis B: Environmental, Vol. 28, 2000, pp. 147-152. [ Links ] Schüth, C.; Kummer, N.; Weidenthaler, C.; Schad, H., Field Application of a Tailored Catalyst for Hydrodechlorinating Chlorinated Hydrocarbon Contaminants in Groundwater., en Applied Catalysis B: Environmental, Vol. 52, 2004, pp. 197-203. [ Links ] Schüth, C.; Reinhard, M., Hydrodechlorination and Hydrogenation of Aromatics Compounds Over Palladium on Alumina in Hydrogen-saturated Water., en Applied Catalysis B: Environmental, Vol. 18, 1998, pp. 215-221. [ Links ] Siantar, D.; Schreier, C.; Chou, C.; Reinhard, M., Treament of 1,2-dicromo-3-Chloropropane and Nitrate-contaminated Water with Zero-valent Iron or Hydrogen/palladium Catalysts., en Water Research, Vol. 30, 1996, pp. 2315-2322. [ Links ] Tavoularis, G.; Keane, M.A., Gas Phase Catalytic Dehydrochlorination and Hydrodechlorination of Aliphatic and Aromatic Systems., en Journal of Molecular Catalysis A: Chemical, Vol. 142, 1999, pp. 187-199. [ Links ] Ukisu, Y.; Kameoka, S., Miyadera, T., Catalytic Dechlorination of Aromatic Chlorides with Noble-Metal Catalysts Under Mild Condictions: Approach to Practical Use., en Applied Catalysis B: Environmental, Vol. 27, 2000, pp. 97-104. [ Links ] Ukisu, Y.; Miyadera, T., Dechlorination of Dioxins with Supported Palladium Catalysts in 2-Propanol Solution., en Applied Catalysis A: General, Vol. 271, 2004, pp.165-170. [ Links ] Ukisu, Y.; Miyadera, T., Hydrogen-Transfer Hydrodehalogenation of Aromatic Halides with Alcohols in the Presence of Noble Metal Catalysts., en Journal of Molecular Catalysis A: Chemical, Vol. 125, 1997, pp. 135-142. [ Links ] Ukisu, Y.; Miyadera, T., Hydrogen-Transfer Hydrodechlorination of Polychlorinated Dibenzo-p-dioxins and Dibenzofurans Catalyzed by Supported Palladium Catalysts., en Catalysis B: Environmental, Vol. 40, 2003, pp. 141-149. [ Links ] Urbano, F.J.;Marinas, J.M., Hydrogenolysis of Organohalogen Compounds Over Palladium Supported Catalysts., en Journal of Molecular Catalysis A: Chemical, Vol. 173, 2001, pp. 329-345. [ Links ] Wu, W.; Xu, J.; Ohnishi, R., Complete Hydrodechlorination of Chlorobenzene and its Derivatives over Supported Nickel Catalysts Under Liquid Phase Conditions., en Applied Catalysis B: Environmental, Vol. 60, 2005, pp. 129-137. [ Links ] Xia, C.; Xu, J.; Wu, W.; Liang, X., Pd/C-Catalized Hidrodehalogenation of Aromatic Halides in Aqueous Solutions at Room Temperature Under Normal Pressure., en Catalysis Communications, Vol. 5, 2004, pp. 383-386. [ Links ] Yakovlev, V.A.; Terskikh, V.V.; Simagina, V.I.; Likholobov, V.A., Liquid Phase Catalytic Hydrodecholorination of Chlorobenzene Over Supported Nickel and Palladium Catalyst: an NMR Insight Into Solvent Function., en Journal of Molecular Catalysis A: Chemical, Vol. 153, 2000, pp. 231-236. [ Links ] Yuan, G.; Keane, M. A., Catalysts Deactivation During the Liquid Phase Hydrodechlorination of 2,4-Dichlorophenol over Supported Pd: Influence of the Support., en Catalysis Today, Vol. 88, 2003, pp. 27-36. [ Links ] Yuan, G.; Keane, M., Liquid Phase Catalytic Hydrodechlorination of 2, 4-Dichlophenol over Carbon Supported Palladium: An Evaluation of Transport Limitations., en Chemical. Engineering Science, Vol., 58, 2003, pp. 257-267. [ Links ] Yuan, G.; Keane, M.A. Role of Base Addition in the Liquid-Phase Hydrodechlorination of 2,4-Dichlorophenol over Pd/Al2O3 and Pd/C., en Journal Catalysis, Vol. 225, 2004, pp. 510-522. [ Links ]














