Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.28 no.2 Bogotá May/Aug. 2008
Mahacine Amrani1
1 Ingénieur Génie des Procédés, Département de Génie Chimique, Marruecos. Ingeniero especializado en procesos industriales, Ecole Mohammadia dIngénieurs de Rabat, Marruecos. Ph.D., Génie des Procédés Industriels, Faculté des Sciences et Techniques de Tanger, Marruecos. amrani.mahacine@menara.ma, mahacine.amrani@gmail.co
RÉSUMÉ
La récupération et la purification des solvants organiques lors des synthèses chimiques et pharmaceutiques savèrent dune grande importance économique et environnementale. La séparation des mélanges eau/alcool par le procédé de pervaporation a été effectuée préférentiellement à travers des membranes hydrophobes. Ce travail se réfère à létude des performances des membranes élaborées en polydimethylsiloxane (PDMS), pour la déshydratation du mélange eau/ propanol par le procédé de pervaporation. Le PDMS est recon pour présenter une permsélective préférentielle aux alcools lors de la pervaporation des mélanges eau/ alcool, néanmoins, on observe aussi une perméation de leau à travers la membrane hydrophobe. Une unité de pervaporation a été utilisée pour étudier des caractéristiques de séparation de cette membrane en termes de flux de pervaporation et de sélectivité pour des charges contenant jusquà en masse deau et pour des températures de 30 à 50°C. Cette différence devient plus importante à mesure que la température de fonctionnement augmente. Bien que le PDMS ait présenté de bonnes caractéristiques pour la séparation des mélanges eau/propanol, le facteur de séparation et le flux de pervaporation diminuent à mesure que la teneur en eau dans la charge à traiter augmente. On observe que la membrane choisie sest avérée plus efficace pour des teneurs en eau inférieures à 0.3, ce qui correspond à un flux de transfert total maximum.
Mots-clés: pervaporation, membrane en PDMS, solvants organiques, eau /propanol, déshydratation.
RESUMEN
La recuperación y purificación de disolventes orgánicos en la química farmacéutica resulta de gran importancia para la economía y el medio ambiente. La separación de mezclas de agua/alcohol por el proceso de pervaporación se llevó a cabo a través de membranas hidrofóbicas. En este trabajo se estudia el rendimiento de las membranas de polidimetilsiloxano (PDMS) para la deshidratación de mezclas agua/propanol por el proceso de preevaporación. El PDMS es reconocido por su selectividad de permeabilidad al alcohol preferentemente en mezclas de agua/alcohol durante el preevaporación debido a su tamaño molecular, aunque aún se presente penetración de agua a través de la membrana hidrofóbica. Se utilizó una unidad de preevaporación a escala de laboratorio para el estudio de esta membrana de separación evaluando características en términos de pervaporación como el flujo y la selectividad de los canales con un contenido máximo de masa de agua y de 30 °C a 50 °C. El flujo de propanol/agua fue observado al variar la temperatura. A pesar que el PDMS presentó buenas características para la separación de mezclas de agua/propanol, el factor de separación y el flujo de pervaporación disminuyen a medida que el contenido de agua en la carga aumenta. La membrana PDMS resultó ser muy eficiente para concentraciones de agua de menos de 0.3, lo que corresponde al total del flujo de transferencia máxima.
Palabras clave: pervaporation, membrane en PDMS, solvants organiques, eau /propanol, déshydratation.
ABSTRACT
Recovering and purifying organic solvents during chemical and pharmaceutical synthesis has great economic and environmental importance. Water-alcohol mixture pervaporation was investigated using a pervaporation cell and hydrophobic membranes. This work studied polydimethylsiloxane (PDMS) membrane performance and hydrophobic membranes for removing propanol from aqueous mixtures. PDMS is recognised as being alcohol permselective during pervaporation. It was also observed that water was transferred through a hydrophobic membrane as waters molecular size is smaller than that of propanol. A laboratory-scale pervaporation unit was used for studying this membranes separation characteristics in terms of pervaporation flux and selectivity for feeds containing up to water mass and 30°C-50°C. Total propanol/water flux was observed to vary as operating temperature increased. Although PDMS membranes presented good characteristics for separating water/propanol mixtures, the separation factor and pervaporation flow decreased as water content in the feed increased. The tested membrane was found to be very efficient for water concentrations of less than 0.3, corresponding to total flux transfer maximum.
Keywords: pervaporation, organic solvent, PDMS membrane, dehydration, water/propanol mixture.
Recibido: diciembre 12 de 2007
Aceptado: abril 25 de 2008
Introduction
La pervaporation est un procédé de fractionnement complexe à travers des membranes en polymères où les caractéristiques de séparation peuvent être influencées par la composition du mélange à traiter. Ce procédé est communément utilisé pour enlever un contaminant dun mélange liquide. Il savère très attractif quand il sagit de contourner la composition azéotropique. Pour améliorer le flux de transfert, il est préférable de choisir une membrane en polymères à létat viscoélastique car ceci permet dobtenir une plus grande solubilité des impuretés à séparer. Contrairement à la séparation de mélanges gazeux ou les membranes utilisées sont dans un état cristallin ou semi cristallin (Mulder, 1996). Le mécanisme de dissolution- diffusion est généralement adopté pour expliquer le phénomène de pervaporation, en particulier lors du fractionnement des mélanges dhydrocarbures ou dhydrocarbures halogénés. La pervaporation des mélanges liquides diffère de la perméation à constituant unique puisque la solubilité et la diffusivité dun constituant du mélange peuvent être affectées significativement par la perméation des autres constituants; comme cest le cas observé pour la séparation du mélange benzène/hexane/polyéthylène, qui pervapore considérablement plus vite que chacun des constituants seuls (Huang and Lin, 1968). Ces résultats imprévus de perméation sont dus à laugmentation de la vitesse de diffusion des espèces lentes retenues par la présence des espèces coexistantes. Des conclusions similaires sur laccouplement des flux de pervaporation ont été rencontrées dans des études récentes (Fels et Huang, 1971; Heintz et Stephan, 1994). Le principe de séparation est considéré comme un mécanisme de dissolution-diffusion, contrôlé principalement par les interactions complexes existant entre les différentes molécules du mélange à traiter et de la membrane polymérique utilisée. La pervaporation est fréquemment considérée comme un procédé de distillation extractive dans lequel la membrane joue le rôle du troisième constituant (Zhang and Drioli, 1995). Contrairement à la distillation classique, le pervaporation peut être utilisée pour la séparation de certains mélanges particuliers tels les mélanges azéotropiques, les isomères, ainsi que les matériaux thermosensibles (Neel et Aptel, 1985). Cest un procédé membranaire qui permet la séparation de composés en phase liquide par valorisation préférentielle de certains composés à travers la membrane. Le principe de la séparation repose essentiellement sur la différence de laffinité chimique du matériau des membranes envers les divers constituants du mélange à pervaporer.
Cependant elle nest pas basée sur léquilibre du système liquide-vapeur mais sur la différence des coefficients de diffusivité et de solubilité des constituants du mélange à pervaporer à travers la couche sélective de la membrane utilisée. Léquilibre liquide- vapeur agit directement sur la force motrice du processus et par conséquent sur les caractéristiques pervaporatives de celuici (Brun, 1981). Outre la grande pureté des produits obtenus, la faible consommation dénergie lors de la pervaporation élargit son application à dautres domaines industriels (Krug, 1989). Cest un procédé membranaire qui permet la séparation de composés en phase liquide par vaporisation préférentielle de certains composés à travers la membrane. Le principe de séparation repose sur une différence d'affinité chimique du matériau des membranes envers les divers constituants du mélange à traiter (Binning et James, 1958). La séparation et la purification des mélanges organiques savére dune grande utilité économique et environnementale. Les alcools à chaînes courtes, tel le propanol, sont communément utilisés dans les synthèses chimiques et pharmaceutiques. Cependant, beaucoup de ces composés organiques forment des azéotropes avec leau. Ce qui rend le procédé de séparation plus délicat. La pervaporation savère donc une technique de séparation particulièrement recommandée pour ce type de mélanges. Les membranes de pervaporation sont des membranes organiques denses. Elles sont essentiellement de deux types: hydrophiles ou organophiles. Les membranes hydrophiles ont une forte affinité pour l'eau qui les traverse bien plus facilement que les matières organiques préférentiellement retenues. Elles sont donc utilisées pour déshydrater des solvants organiques. Les membranes organophiles ont une affinité plus prononcée envers les molécules organiques que pour l'eau, qui dans ce cas, est majoritairement retenue. Elles sont donc plus utilisées pour éliminer les composés organiques de leau (Van Veen et al., 2001; Tatiana et al., 2002). Le propanol est un alcool souvent utilisé comme solvant dans les synthèses chimiques et pharmaceutiques. Bien que beaucoup d'études décrivent la récupération de léthanol (Takegami et al., 1992), du n-buta-nol, (Favre et al., 1996) et 2-butanol (Boddeker et al., 1990) à partir des milieux de fermentation (Qureshi et al., 2003; Fadeev et al., 2000) par pervaporation sur diverses membranes, peu de données sont fournies sur la récupération du propanol (Huang and Feng, 1993). Les matériaux polymères sont dune grande utilité pour la séparation des mélanges eau -alcools. Le poly(1-triméthylsilyl-1-propyne) PTPMSP est un polymère de choix pour la pervaporation du mélange eau –éthanol (Takegami et al., 1992) avec des facteurs de séparation et des flux de pervaporation voisins de ceux obtenus en utilisant le (poly-diméthylsiloxane) PDMS (Masuda et al., 1986, 1990). Le PDMS présente des propriétés mécaniques et une capacité filmogène assez faible, ce qui rend délicat la préparation de membranes de faible épaisseur (Liang et Ruckenstein, 1996). Néanmoins, le flux de pervaporation est indépendant de lépaisseur de la membrane quand celleci est inférieure à 150 µm(Mazuda et al., 1990). L'objectif de cette recherche consiste à étudier la déshydratation du propanol sur des membranes en PDMS et d'établir les performances de cellesci sous différentes conditions opératoires.
Matériel et méthode
La solution à pervaporer a été obtenue par mélange du propanol, de qualité analytique (Merck) utilisé sans aucune purification préalable. Un mélange binaire deau/ propanol dune teneur variant de 0% à 80% en masse deau a été utilisé pour alimenter linstallation de pervaporation (Figure 1). Les membranes testées ont été élaborées à partir du PDMS (Amrani, 2006a, 2007). La température de fonctionnement à été fixée successivement à 30, 35, 40, 45 et 50 °C.
Les films membranaires ont été placés dans la cellule de pervaporation sur un support en acier inoxydable. Cette cellule est divisée en deux compartiments séparés par la membrane organique. Le compartiment amont est sous agitation grâce à la circulation de la charge, assurée par une pompe mécanique. Le compartiment aval est maintenu sous vide (3 millibars). Le pervaporat est récupéré alternativement dans les pièges refroidis à lair liquide. La température de la charge est contrôlée à laide dun bain thermo staté. Les membranes étudiées sont caractérisées essentiellement par le flux de pervaporation Jp(kg/h.m2) et le facteur de séparation α définis comme suit: une masse de pervaporat est recueillie dans le piège pendant le temps t, le flux de pervaporation est donné par 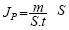 étant la section effective de la membrane. Le pervaporat est pesé puis analysé par chromatographie en phase gazeuse pour déterminer sa teneur en eau et en t-butanol. Le coefficient de séparation α est donné par
étant la section effective de la membrane. Le pervaporat est pesé puis analysé par chromatographie en phase gazeuse pour déterminer sa teneur en eau et en t-butanol. Le coefficient de séparation α est donné par 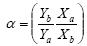 ou X et Y représentent respectivement la concentration dans la charge et la concentration dans le pervaporat des espèces A et B. Les échantillons prélevés sont pesés à laide dune balance Mettler Toledo, puis analysés par chromatographie en phase gazeuse à laide dun chromatographe HP6890.
ou X et Y représentent respectivement la concentration dans la charge et la concentration dans le pervaporat des espèces A et B. Les échantillons prélevés sont pesés à laide dune balance Mettler Toledo, puis analysés par chromatographie en phase gazeuse à laide dun chromatographe HP6890.
Résultats et discussions
Effet de la teneur en eau dans la charge
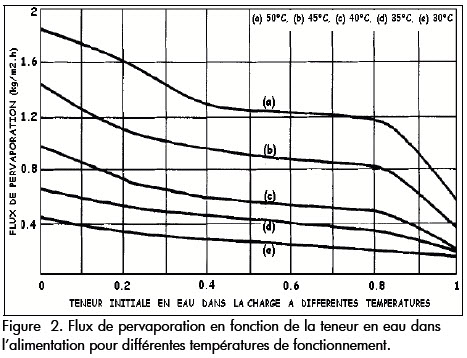
Lors de la pervaporation du mélange eau/ propanol à travers la membrane élaborée en PDMS, on observe une diminution rapide du flux de transfert jusquà une teneur en eau de 0.3. Une faible variation est observée pour des teneurs en eau de 0.3 à 0.8 (Figure 2).
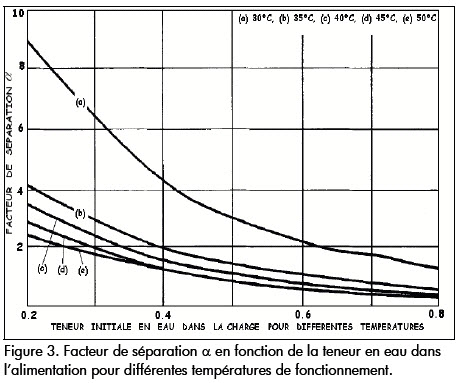
Le facteur de séparation α diminue de façon uniforme en fonction de la teneur en eau, comme lillustre la Figure 3, et ceci pour les différentes températures adoptées. Ce phénomène peut être expliqué par le fait que la membrane étant hydrophobe, cest à dire quelle présente plus daffinité envers le propanol que pour leau, il existe de moins en mois dinteractions entre les molécules de la membrane et le propanol à mesure que la teneur en eau dans la charge augmente. En effet, la très grande solvatation des molécules organiques dans la membrane hydrophobe rend bien compte de la grande sélectivité de ces membranes pour le transfert de ces molécules organiques: la sorption de leau dans ces élastomères y compris pour des mélanges titrant plus de 99% deau reste souvent inférieur à 1%. Ce pendant le transfert de leau nest pas négligeable et sexplique par la mobilité de cette molécule (Huang, 1991).
La Figure 4 illustre le transfert sélectif de leau à travers le membrane, en fonction de la teneur en eau dans le mélange à traiter. Ce flux de transfert a été calculé daprès lexpression suivante (Amrani, 2006b): 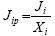 où Ji est le flux de transfert du constituant i pur à travers la membrane considérée. Xi est la fraction massique du constituant i dans lalimentation, et Jip est le flux de transfert du constituant i dun mélange binaire ou multi constitué à travers la membrane.
où Ji est le flux de transfert du constituant i pur à travers la membrane considérée. Xi est la fraction massique du constituant i dans lalimentation, et Jip est le flux de transfert du constituant i dun mélange binaire ou multi constitué à travers la membrane.
On observe une augmentation rapide du flux de transfert en eau pour des teneurs jusquà 0.3, puis une stabilisation sur lintervalle des teneurs 0.3 à 0.8. Ceci est valable pour toutes les températures opératoires étudiées. Bien que le PDMS soit connu pour présenter une perméation préférentielle du propanol lors de la pervaporation des mélanges eau/propanol, la perm sélectivité de ce matériel est liée à l'existence dun volume libre et à lhydrophobicité de la surface de membrane. Cest pour cette raison que la plupart des membranes en polymères sont perméables à l'eau vu que la taille moléculaire de l'eau est plus petite que celle des molécules organiques (éthanol, butanol, propanol, ).
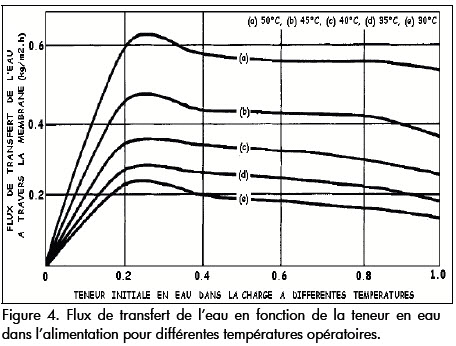
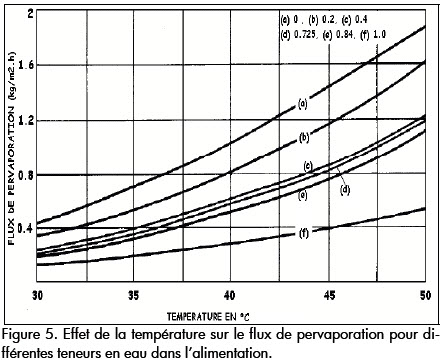
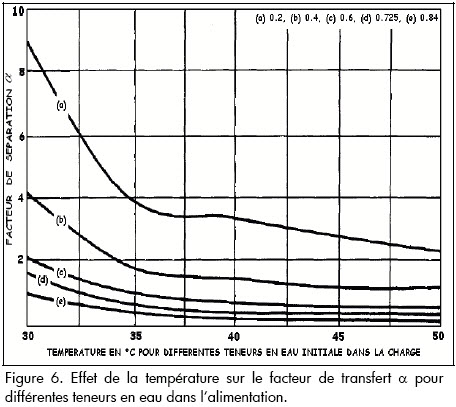
Effet de la température
Lorsque la température varie de 30 à 50 °C, on observe une augmentation du flux de pervaporation et une diminution du coefficient de séparation de la membrane (Figure 5 et Figure 6). Ceci peut être expliqué par le fait que lorsque la température augmente, le mouvement des chaînes de PDMS devient plus violent, induisant ainsi une plus grande part de volume libre dans la structure de la membrane. En outre le mouvement des molécules constituant le mélange, diffusent plus rapidement à travers les volumes libres de la membrane. Ce qui implique une augmentation considérable du flux de pervaporation, en particulier pour la température de 50 °C. accompagnée dune diminution de la sélectivité de la membrane. En pervaporation, leffet de la température sur les performances des membranes dépend du facteur principal qui régit la sélectivité de transfert à travers la membrane. S'il est principalement dû à l'étape de sorption, la variation de la sélectivité dépendra de la chaleur de la sorption des composés dans la membrane. S'il est dû à une différence dans des vitesses de diffusion, alors la variation de la sélectivité dépendra de l'énergie d'activation pour la diffusion de chaque constituant. Une énergie d'activation plus élevée de la diffusion du composant qui imprègne préférentiellement devrait mener à une augmentation de sélectivité avec la température (Yildirim et al., 2001).
Conclusion
Dans ce travail, nous nous sommes intéressés à létude de la pervaporation du mélange eau/propanol à travers des membranes en PDMS dans un intervalle de températures allant de 30 à 50 °C. On observe que la membrane choisie sest avérée plus efficace pour des teneurs en eau inférieures à 0.3, ce qui correspond à un flux de transfert total maximum. Les résultats montrent que le facteur de séparation et le flux de pervaporation augmentent lorsque la température augmente. La séparation est dautant plus efficace notamment à la température de 50 °C en raison de laffaiblissement des liaisons hydrogène.
Bien que le PDMS ait présenté de bonnes caractéristiques pour la séparation des mélanges eau/propanol, le facteur de séparation et le flux de pervaporation diminuent à mesure que la teneur en eau dans la charge à traiter augmente. On observe même une stabilisation du flux de transfert total pour des teneur en eau de 0.3 à 0.8. Ceci est probablement dû à un processus de gonflement de la membrane.
Bibliografía
Amrani, M., Pervaporation du mélange eau-éthanol à travers des membranes en alcool polyvinylique., Revista Digital Cientifica y Technologica e-Gnosis [online], Vol.4, Art.14., 2006a. [ Links ]
Amrani, M., Approche thermodynamique appliquée au choix de membranes pervaporatives., Revista Ing. Investig., Vol. 26, No. 3, 2006b, pp. 42-49. [ Links ]
Amrani, M., Analyse des membranes de déshydratation du mélange eau-t-butanol par procédé de pervaporation., Revista Digital Cientifica y Technologica e-Gnosis [online], Vol.5, Art. 7, 2007. [ Links ]
Binning, R. L., James, F. E., Permation a new commercial separation tool., Petrolum Refiner, Vol.39, No.214, 1958. [ Links ]
Boddeker, K. W., Bengston, G., Pingel, H., Pervaporation of isomeric butanols., Journal of Membrane Science, Vol.54, No. 1-2, 1990, pp.1-12. [ Links ]
Brun, J. P., Etude thermodynamique du transfert sélectif par pervaporation à travers les membranes délastomère des-pèces organiques dissoutes en milieu aqueux, Thèse de Doctorat, Paris, 1981. [ Links ]
Fadeev, A. G., Meagher, M. M., Kelley, S. S., Volkov, V.V., Fouling of poly[-1-(trimethylsilyl)-1-propyne] membranes in pervaporative recovery of butanol from aqueous solutions and ABE fermentation broth., J. Membr. Sci., 173, 2000, pp. 133-144. [ Links ]
Favre, E., Nguyen, Q. T., Bruneau, S,. Extraction of 1-Butanolfrom aqueous solutions by pervaporation., Journal of chemical Technology and Biotechnology, Vol 65, Issue 3, 1996, pp.211-302. [ Links ]
Fels, M., Huang, R. Y. M., Theoretical interpretation of the effect of mixture composition on separation of liquids in polymers, J. Macromol. Sci. Phys.B, 5(1), 1971, pp. 89-110. [ Links ]
Heintz, A., Stephan, W. J., A generalized solutiondiffusion model of the pervaporation process through composite membranes Part I. Prediction of mixture solubilities in the dense active layer using the UNIQUAC model., J. Membrane Sci., 89, 1994, pp.143-151. [ Links ]
Huang, R.Y. & V.J.C., Lin, Separation of liquid mixtures by using polymer membranes. I. Permeation of binary organic liquid mixtures through polyethylene, J.Appl. Polym.Sci, 12, 1968, pp. 2615-2631. [ Links ]
Huang, R. Y. M., Pervaporation membrane separation processes., Ed. Elsevier, Amsterdam, Oxford, New York, Tokyo, 1991. [ Links ]
Huang, R. Y. M., Feng, X. S., Dehydration of isopropanol by pervaporation using aromatic polyetherimide membranes., Sep. Sci. Tech., 28, 1993, pp. 2035–2048. [ Links ]
Krug, J., Principal possibilities, practical difficulties of the use of pervaporationprocesses in the chemical industry., Fort Lauderdale, Ed. Bakish Materials Corp., New Jersey, USA, 1989, pp. 297-303. [ Links ]
Liang, L., Ruckenstein, E., Pervaporation of ethanol-water mixtures through polydimethylsiloxanepolystyrene interpenetrating polymer network supported membranes., J. Membr. Sci., 114, 1996, pp. 227–234. [ Links ]
Masuda, T., Tang, B-Z., Higashimura, T., Ethanol-water separation by pervaporation through substitutedpolyace-tylene membranes., Polym. J., Vol.18, No.7, 1986, pp. 565–567. [ Links ]
Masuda, T., Higashimura, T., Synthesis and properties of silicon-containing polyacetylenes., Adv. Chem. Ser., 224, 1990, pp. 641–661. [ Links ]
Masuda, T., Takatsuda, M., Tang, B-Z., Higashimura, T., Pervaporation of organic liquid-water mixtures through substituted polyacetylene membranes., J. Membr. Sci., 49, 1990, pp. 69–83. [ Links ]
Mulder, M. V. H., Basic Principles of Membrane Technology., 2nd Edition, Kluwer Academic Publishers, 1996, pp. 584. [ Links ]
Neel, J., Aptel, P., La pervaporation 1ère partie: principe de la technique, Entropie, No.104.5, 1985. [ Links ]
Qureshi, N., Dien, B. S., Saha, B. C., Ezeji, T. C., Blaschek, H. P., Cotta, M. A., Separation of butanol from fermentation broths by pervaporation: mass flux and energy balance., American Institute of chemical Engineers. No. 162.B, 2003. [ Links ]
Tatiana, G. L., Edwards, E., Lobiundo, G., Santos, L. F., Dehydration of water/t-butanol mixtures by pervaporation: comparative study of commercially available polymeric., microporous silica and zeolithe membranes, J. Membr. Sci., 197, 2002, pp. 309-319. [ Links ]
Takegami, S., Yamada, H., Tsujii, S., Dehydration of water/ ethanol mixtures by pervaporation using modified poly (vinyl alcohol) membrane, Polym. J., Vol.24, No. 11, 1992, pp. 1239-1250. [ Links ]
Van Veen, H. M., Van Delft, Y. C., Engelen, C. W. R., Pexp, P. A. C., Dewatering of organics by pervaporation with silica membranes., Separation and Purification Technology Journal, Elsevier Science, Vol.22-23, No. 1-3, 2001, pp. 361-366. [ Links ]
Yildirim, A. E., Hilmioglu, N. D., Tulbentci, S., Pervaporation separation of benzene/cyclohexane mixtures by poly(vinyl chloride) membranes., Chem. Eng. Technol., 24, 2001, pp. 275–279. [ Links ]
Zhang, S. M., Drioli, E., Pervaporation Membranes (review)., Separation Science and Technology, 30, 1995, pp. 1-31. [ Links ]














