Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Ingeniería e Investigación
versão impressa ISSN 0120-5609
Ing. Investig. v.29 n.3 Bogotá set./dez. 2009
Rolando Barrera Zapata1 , Aída Luz Villa de P.2 y Consuelo Montes de Corrrea3
1 Ingeniero químico, M.Sc., en Ciencias Químicas y Estudiante Ph.D., en Ingeniería, Universidad de Antioquia, Colombia. rolando@udea.edu.co
2 Ingeniera química y M.Sc., en Ciencias Químicas, Universidad de Antioquia, Colombia. Ph.D., en Ciencias Biológicas Aplicadas, Katholieke Universiteit Leuven, Bélgica. Profesora asociada, Departamento de Ingeniería Química, Universidad de Antioquia, Colombia. alvilla@udea.edu.co.
3 Ingeniera química, Universidad de Antioquia, Colombia. Ph.D., en Ingeniería Química, Virginia Polytechnic Institute And State University, Estados Unidos. Postdoctorado, Katholieke Universiteit Leuven, Bélgica. Profesora titular, Departamento de Ingeniería Química, Universidad de Antioquia, Colombia. cmontes@udea.edu.co.
RESUMEN
El catalizador PW-Amberlita es activo para la epoxidación de limoneno en condiciones trifásicas, pero se desactiva durante la reacción. En esta contribución se evaluó la estabilidad del catalizador en la reacción y la recuperación de la actividad catalítica al tratarlo con varios solventes. Se encontró que el catalizador recupera el 99% de su actividad inicial cuando se lavó con tolueno y que la recuperación fue de 95 y 97% cuando se utilizaron etanol o acetona como solventes de lavado, respectivamente. Las pruebas de lixiviación mostraron que la reacción no continuaba al separar el catalizador de la mezcla de reacción, confirmando la ausencia de lixiviación de la fase activa del catalizador. Mediante análisis FTIR se evidenció que las especies características del complejo fosfotungstato no se modificaron con reutilizaciones sucesivas del catalizador.
Palabras clave: PW-Amberlita, estabilidad del catalizador, regeneración del catalizador, epoxidación de limoneno.
ABSTRACT
The PW-Amberlite catalyst is active for limonene epoxidation in triphasic conditions; it becomes deactivated in reaction conditions. Catalyst stability during the reaction and recovery of catalyst activity when it was treated with several solvents were evaluated. It was found that the catalyst recovered 99% of its initial activity when it was washed with toluene and that the recovery was 95% and 97% when ethanol or acetone were used as washing solvents, respectively. Leaching tests showed that the reaction did not continue when the catalyst was removed from the reaction mixture, confirming the absence of leaching during the catalyst's active phase. FTIR analysis revealed that the characteristic species of the phosphotungstate complex did not vary with successive reusing of the catalyst.
Keywords: PW-Amberlite, stability, catalyst regeneration, limonene epoxidation.
Recibido: enero 30 de 2008
Aceptado: junio 16 de 2009
Introducción
El epóxido de limoneno se utiliza como materia prima en la síntesis de precursores para fragancias, saborizantes, drogas y agro-químicos. Se obtienen rendimientos al epóxido de limoneno superiores al 70% (24 h, 38°C) con el catalizador PW-Amberlita, peróxido de hidrógeno acuoso como oxidante y acetonitrilo como solvente (Villa et al., 1999). El catalizador PW-Amberlita se obtiene por inmovilización del complejo {PO4[WO(O2)2]4}3- (PW) en la resina macrorreticular de intercambio iónico Amberlita IRA 900. Como especie activa, en la epoxidación de limoneno con este catalizador se propuso el poliperoxofosfotungstato que se forma por la interacción del oxidante con el complejo PW (Villa et al., 2002). La cinética de la reacción con este sistema se ha estudiado en condiciones bifásicas (Villa et al., 2002) y trifásicas (Barrera et al., 2006); encontrándose que la energía de activación aparente para la epoxidación de limoneno es de 75 KJ/mol en el sistema bifásico (Villa et al., 2002) y de 25 KJ/mol en el trifásico (Barrera et al., 2006).
Tanto en condiciones bifásicas como trifásicas se ha encontrado que aunque el catalizador se desactiva y su velocidad de reacción disminuye en presencia de epóxido de limoneno, éste recupera alrededor del 97% de su actividad inicial después de ser lavado con acetona (Villa et al., 2002; Barrera et al., 2006). Teniendo en cuenta la desactivación del catalizador, la expresión de velocidad de reacción para el sistema trifásico se modificó con un factor de desactivación, obteniéndose un excelente ajuste del modelo con los datos de conversión experimental a diferentes tiempos (Barrera et al., 2007). Esta ecuación cinética modificada se utilizó para proponer la ecuación de diseño de un reactor batch donde se lleve a cabo la epoxidación de limoneno con PW-Amberlita bajo condiciones trifásicas, ecuación (1).
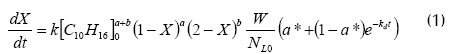
Con: k, pseudoconstante de reacción; [C10H16]0, concentración inicial de limoneno; a y b, órdenes de reacción; W, masa de catalizador; NLo, moles iniciales de limoneno; a*, actividad residual (Fuentes, 1985; Sandelin et al., 2006;); kd, constante de desactivación y t tiempo.
Con el fin de conocer mejor el fenómeno de desactivación del catalizador PW-Amberlita en la epoxidación de limoneno en condiciones trifásicas, se comparó la actividad del catalizador fresco y reutilizado después de lavarlo con solventes de diferente polaridad (tolueno, etanol y acetona), al reutilizarlo cuatro veces, y al adicionar epóxido de limoneno al comienzo de la reacción. La heterogeneidad del catalizador se evidenció mediante pruebas de lixiviación de las especies activas. Adicionalmente, el sólido fresco y después de reacción se analizó por FTIR.
Desarrollo experimental
Síntesis del catalizador, pruebas catalíticas y análisis de los productos de reacción
El catalizador se sintetizó mediante procedimientos previamente descritos (Barrera et al., 2006). En una reacción típica la mezcla de reacción se preparó con 0,5 g de limoneno, 3,2 g de acetonitrilo, 0,83 g de peróxido de hidrógeno acuoso al 30% y 0,1 g de catalizador PW-Amberlita con tamaño de partícula menor a 0,425 µm. La reacción se llevó a cabo en viales de 8 mL agitados magnéticamente (1.000 rpm) e inmersos en un baño de aceite (33 ± 0,5 °C). Muestras de reacción (2 µL) de diversos tiempos (0–24 h) se analizaron 3 veces por cromatografía de gases, utilizando decano (0,125 M) como estándar. Para los análisis cromatográficos se utilizó un equipo Varian Star 3400 equipado con una columna capilar DB-1 de 50 m, la temperatura del horno se incrementó de 135 a 195 °C con una velocidad de calentamiento de 15 °C/min. La temperatura del inyector fue de 200°C y la del detector FID de 280°C. La relación de venteo utilizada fue de 10,8 con nitrógeno como gas de arrastre. Los tiempos típicos de retención fueron: decano 6,75 min, limoneno 7,35 min y epóxido de limoneno 8,71 min.
Reutilización del catalizador PW-Amberlita
Después de cada reacción el catalizador se recuperó por filtración, se lavó con aproximadamente 15 mL del solvente de lavado, se agitó durante 20 minutos en 30 mL del solvente, y se filtró y lavó nuevamente. El sólido se secó a temperatura ambiente, almacenándose aproximadamente a 15°C antes de su reutilización bajo las mismas condiciones utilizadas con el material fresco.
El catalizador se reutilizó hasta cuatro veces, utilizando acetona como solvente de lavado. La incertidumbre estimada para la conversión de limoneno, asumiendo un intervalo de confianza del 95% y una distribución normal de los datos (Chirico et al., 2003), fue de ± 0,012 (1,2%).
Efecto del solvente de lavado en la actividad catalítica
El catalizador se lavó con un solvente apolar (tolueno), polar prótico (etanol) y aprótico (acetona).
Prueba de lixiviación
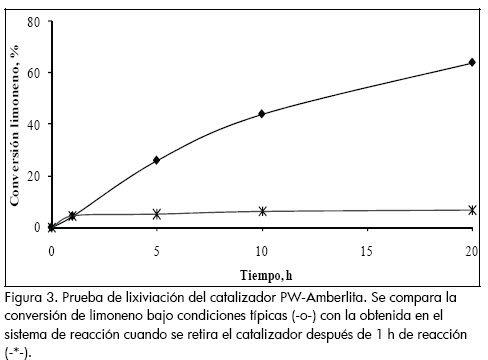
Se llevó a cabo una reacción típica y el catalizador se separó del medio de reacción por filtración a una conversión menor al 5%. La reacción se continuó sin catalizador durante 19 h más y la conversión obtenida se comparó con la alcanzada bajo condiciones típicas de reacción.
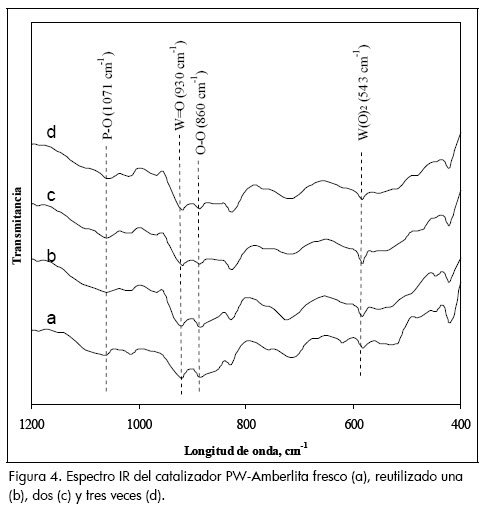
Análisis IR del catalizador fresco y reutilizado. Tanto el catalizador fresco como el reutilizado se analizaron por espectroscopía IR. Cada muestra se diluyó en bromuro de potasio para obtener una mezcla de aproximadamente 3% p/p de catalizador. Se utilizó un equipo FT-IR marca Nicolet Avatar 330 con celda dispersiva, analizándose en el rango de 400 a 1.200 cm-1.
Desactivación del catalizador PW-Amberlita en el transcurso de la reacción
Para verificar el efecto del epóxido de limoneno en la desactivación del catalizador se comparó la actividad del catalizador i) al lavarlo con acetona antes de reutilizarlo y sin lavarlo; ii) cuando se adicionaba epóxido de limoneno (0,42 g) al comienzo de la reacción y bajo condiciones típicas de reacción.
Resultados y discusión
Reutilización del catalizador
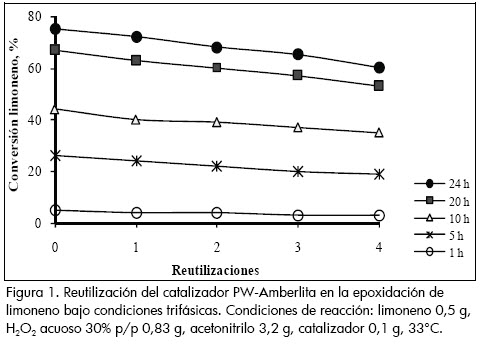
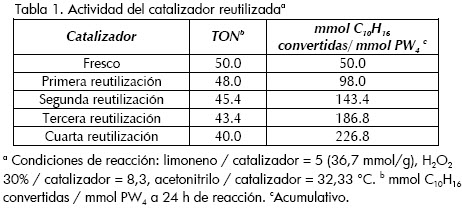
La figura 1 muestra que para tiempos cortos de reacción (< 5 h) la conversión de limoneno no presenta diferencias significativas si el catalizador es fresco o reutilizado. Sin embargo, a tiempo mayor esta diferencia es cercana al 3% en cada reutilización. En la tabla 1 se compara la actividad del catalizador en términos del TON (del inglés Turn Over Number, mmol limoneno transformado por mmol de complejo activo) para diferentes tiempos de reacción, teniendo en cuenta que en el catalizador hay 0,55 mmol de PW4 /g PW-Amberlita (Villa et al., 2002). En la cuarta reutilización cerca de 227 mmoles de limoneno se convierten a partir del mismo lote de catalizador. Si el catalizador no se pudiera reutilizar, se requerirían aproximadamente 4,5 lotes de catalizador fresco para transformar la misma cantidad de limoneno (tabla 1).
Efecto del solvente de lavado
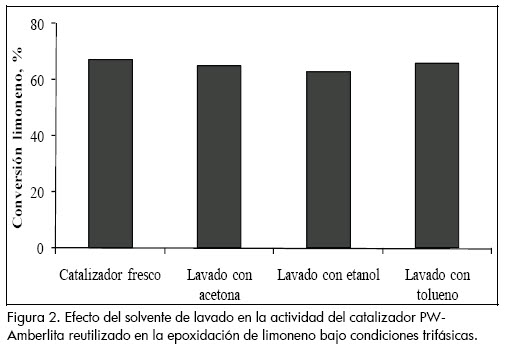
La figura 2 muestra el efecto del solvente de lavado en la actividad del catalizador reutilizado. Se observa que al utilizar un solvente apolar como el tolueno el catalizador recupera aproximadamente el 99% de su actividad catalítica. El lavado con solventes polares como etanol o acetona es menos efectivo para remover los compuestos orgánicos que posiblemente están envenenando el catalizador, recuperándose el 95 y 97% de la actividad catalítica inicial, respectivamente.
Pruebas de lixiviación y análisis IR
Ya que la reacción se inhibe cuando el catalizador se extrae de la mezcla de reacción, figura 3, puede concluirse que no hay lixiviación del catalizador de la fase activa durante la reacción. El catalizador fresco y el reutilizado presentan las bandas del infrarrojo características de los tungstofosfatos, figura 4 (Villa, 2000): vibraciones oxometálicas, P-O (≈1071 cm-1), W=O (≈930 cm-1); la banda correspondiente a las vibraciones O-O (≈860 cm-1) y a las vibraciones peroxometálicas, W(O)2, (≈543 cm-1). Estos resultados muestran que la estructura peroxo PW no se modifica durante la reacción.
Desactivación del catalizador
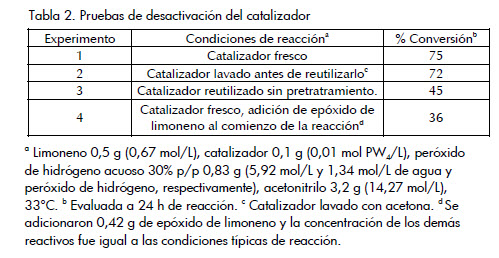
La tabla 2 despliega las pruebas de desactivación del catalizador. Cuando el catalizador se lava con acetona (experimento 2), recupera alrededor del 97% de su actividad inicial (Villa et al., 2002; Barrera et al., 2006). Si el catalizador no se lava antes de reutilizarse (experimento 3), se pierde cerca del 40% de la actividad catalítica, lo cual sugiere que los compuestos orgánicos se adsorben fuertemente en la superficie del catalizador. Esta conclusión se prueba con lo observado en el experimento 4, donde la conversión de limoneno decrece más del 50% al adicionar epóxido de limoneno a la mezcla inicial de reacción. Estos resultados sugieren que efectivamente la desactivación del catalizador se debe al epóxido de limoneno formado en la reacción, justificándose además la inclusión del término de desactivación en la expresión cinética, ecuación 1.
Conclusiones
El catalizador PW-Amberlita es un material activo para la epoxidación de limoneno que aunque se desactiva con el epóxido de limoneno formado puede recuperar el 95, 97 ó 99% de su actividad inicial si se lava con etanol, acetona o tolueno, respectivamente. Adicionalmente, las especies activas del catalizador no se lixivian ni se modifican durante la reacción. El sistema catalítico PW-Amberlita/H2O2/acetonitrilo, es entonces un sistema promisorio para la obtención de epóxido de limoneno a mayor escala, por utilizar un oxidante limpio y por la posibilidad de regenerar y reutilizar el catalizador.
Agradecimientos
Los autores agradecen el apoyo financiero de Colciencias mediante Cenivam RC No. 432. R.B. y la beca doctoral.
Bibliografía
Barrera R., Villa, A.L. y Montes de Correa, C., Limonene epoxydation: Diffusion and reaction over PW-Amberlite in a triphasic system., Industrial and Engineering Chemical Research, Vol. 45, 2006, pp. 4589-4596. [ Links ]
Barrera, R., Villa, A. L., Montes de Correa, C., Modelado de la epoxidación de limoneno con PW-Amberlita., Scientia et Technica, Año XIII, No. 33, 2007, pp. 451-454. [ Links ]
Chirico, R. D., Frenkel, M., Diky, V. V., Marsh, N. K., Wilhoit, R. C., ThermoML-An XML-Based Approach for Storage and Exchange of Experimental and Critically Evaluated Thermophysical and Thermochemical Property Data. 2. Uncertainties., Journal of Chemical Engineering Data, Vol. 48, 2003, pp. 1344-1359. [ Links ]
Fuentes, G., Catalyst deactivation and steady-state activity: a generalized power-law equation model., Applied Catalysis, Vol. 15, 1985, pp. 33-40. [ Links ]
Sandelin, F., Oinas, P., Salmi, T., Paloniemi, J., Haairo, H., Dynamic modelling of catalytic liquid-phase reactions in fixed bedskinetics and catalyst deactivation in the recovery of anthraquinones., Chemical Engineering Science, Vol. 61, 2006, pp. 4528-4539. [ Links ]
Villa, A. L., Sels, B. F., De Vos, D. E., Jacobs, P. A., A heterogeneous tungsten catalyst for epoxidation of terpenes and tungsten-catalyzed synthesis of acidsensitive terpene epoxides., Journal of Organic Chemistry, Vol. 64, 1999, pp. 7267-7270. [ Links ]
Villa, A. L., Epoxidation of Monoterpenes by Homogeneous and Heterogeneous Catalytic Systems., tesis presentada a la Universidad de Leuven, Bélgica, para optar al grado de Doctor en Ciencias Biológicas Aplicadas, 2000. [ Links ]
Villa, A. L., Taborda, F., Montes de Correa, C., Kinetics of limonene epoxidation by hydrogen peroxide on PW-Amberlite., Journal of Molecular Catalysis A: Chemical, Vol. 185, 2002, pp. 269-277. [ Links ]














