Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería e Investigación
Print version ISSN 0120-5609
Ing. Investig. vol.30 no.1 Bogotá Apr. 2010
Andrés Felipe Rojas González 1 Erika Girón Gallego 2 y Harlen Gerardo Torres Castañeda3
1 Ingeniero químico, Universidad Nacional de Colombia, Manizales. M.Sc., en Ingeniería Química y Ph.D., en Ingeniería, Universidad del Valle, Colombia. Profesor Asociado, Departamento de Ingeniería Química, Facultad de Ingeniería y Arquitectura, Universidad Nacional de Colombia, Manizales.afrojasgo@unal.edu.co 2 Ingeniera agroindustrial, Universidad Nacional de Colombia, Palmira. Ingeniero Auxiliar de Despacho, Ingenio Manuelita. erika.giron@manuelita.com 3 Químico. M.Sc., en Ciencias Químicas, Universidad del Valle, Colombia. Profesor Asistente, Departamento de Ciencias Básicas, Facultad de Ingeniería y Administración, Universidad Nacional de Colombia, Palmira. hgtorresc@palmira.unla.edu.co
RESUMEN
En este artículo se presentan los resultados de la revisión bibliográfica sobre la influencia de variables tales como temperatura y tiempo de reacción, tipo de alcohol, concentración molar alcohol:aceite vegetal, tipo y concentración de biocatalizador, solvente, intensidad del mezclado, pureza de los reactivos, y concentración de ácidos grasos libres y humedad, sobre el rendimiento en la producción de biodiesel por transesterificación enzimática de aceites vegetales. En la catálisis enzimática de aceites vegetales se pueden alcanzar rendimientos superiores al 90%, utilizando temperaturas entre 35-50 °C, tiempos largos de reacción (7-90h) y una relación molar alcohol:aceite vegetal de 3:1; sin embargo, dichos valores dependerán intrínsecamente del tipo de lipasa y aceites utilizados. Además, se encontró que el contenido de ácidos grasos y de humedad no son parámetros que requieran un control riguroso debido a la alta especificidad de las enzimas. Las lipasas inmovilizadas de la bacteria Pseudomonas cepacia y del hongo Rhizopus orizae son las más utilizadas en la transesterificación enzimática de aceites vegetales.
Palabras clave: transesterificación, condiciones de operación, biodiesel, aceites vegetales, enzimas.
ABSTRACT
This paper presents the results of a literature review regarding how operating conditions influence vegetable oil enzymatic transesterification yield. The following parameters were studied: temperature and time reaction, alcohol:oil molar ratio, alcohol type, biocatalyst type and concentration, solvent, mixed intensity, reagent purity and free fatty acid and moisture concentration. Yields greater than 90% can be achieved in the enzymatic catalyst of vegetable oil using 35-50°C temperatures, long time reactions (790h) and a 3:1alcohol:vegetable oil molar ratio; however, such values would intrinsically depend on the type of lipase and oil used. It was also found that free fatty acid and moisture concentration were parameters which did not require rigorous control due to high enzyme specificity. Lipases immobilisedfrom Pseudomona cepacia bacteria and Rhizopus orizae fungi were most used in vegetable oil enzymatic transesterification.
Keywords: Transesterification, operating conditions, biodiesel, vegetable oil, enzyme.
Recibido: noviembre 11 de 2008 Aceptado: noviembre 3 de 2009
Introducción
El uso de aceites vegetales como combustible se registra desde los orígenes del motor diesel, pero ha tomado fuerza a partir de la crisis energética de 1970. Desde entonces, y debido a los problemas generados en el motor al utilizar directamente aceite vegetal, se han desarrollado procesos para modificarlo químicamente, de tal manera que los triglicéridos se transforman en sus correspondientes ésteres grasos. A esta conversión química del aceite se la conoce como proceso de transesterificación, y los ésteres grasos son llamados biodiesel. El biodiesel es un biocombustible líquido sintético que se obtiene de aceites vegetales o de grasas animales y se caracteriza porque en el proceso de combustión es entre el 40% y el 80% menos contaminante que el petrodiesel pues en su molécula contiene átomos de oxígeno que ayudan a una combustión más limpia. No es tóxico, ya que no emite óxidos de azufre ni sustancias nocivas, y es completamente biodegradable. Este biocombustible ofrece ventajas medioambientales, energéticas (aporta el triple de energía de la que se necesita para su producción) y eco-nómicas frente a los combustibles tradicionales, y se considera in-dispensable en la lucha contra el cambio climático (Alcántara, 2000; Zhang, 2003a, b). El propósito principal del proceso de transesterificación es el de reducir la viscosidad del aceite para mejorar sus características carburantes (Ma, 1999a) y de flujo (Meka, 2007; Refaat, 2008).
ón de aceites vegetales se puede llevar a cabo con catalizadores homogéneos como NaOH, KOH o H2SO4, o en presencia de catalizadores heterogéneos como los óxidos metálicos, carbonatos o enzimas (Schuchardt, 1998; Vicente, 2007). De los anteriores procesos la catálisis enzimática se caracteriza porque los productos son más puros, no hay formación de jabón, no se emplean catalizadores químicos que afectan el medio ambiente, se evita la neutralización ácida y la recuperación del catalizador es fácil (Lin, 2006). En este proceso se emplean enzimas como Rhizomucor miehei (Veena, 2007), Pseudomonas cepacia (Kaieda, 2001; Veena, 2007), Rhizopus orizae (Ban, 2001; Li, 2007), Candi-da antarctica (Köse, 2002) y Candida rugosa (Kaieda, 2001). Estas enzimas se utilizan en forma libre o inmovilizada en la transesterificación. Las enzimas libres se agregan directamente al medio reactante, pero debido al contacto directo con el alcohol se reduce su actividad catalítica y se dificulta su recuperación al final del proceso. Las enzimas inmovilizadas hacen referencia a las lipasas que se adhieren o confinan en partículas sólidas (soportes de inmovilización), con el propósito de mantener su actividad catalítica y posibilitar su reutilización. Entre los soportes de inmovilización más utilizados se encuentran: espumas de poliuretano reticulado (Ban, 2001; Hama, 2004], celita (Shweta, 2004), soportes de polipropileno (Veena, 2007), resinas de intercambio iónico (Fukuda, 2001), y filosilicato sol-gel (Hsu, 2001).
El objetivo de este artículo es el de mostrar la influencia de la temperatura y tiempo de reacción, tipo de alcohol, concentración molar alcohol:aceite vegetal, tipo y concentración de biocatalizador (enzima), solvente, intensidad del mezclado, pureza de los reactivos y concentración de ácidos grasos libres y humedad, sobre el rendimiento en la producción de biodiesel de aceites vegetales empleando catálisis enzimática, a través del estudio de trabajos desarrollados y reportados en la literatura en los últimos veinte años.
Proceso de manufactura del biodiesel
El biodiesel obtenido mediante la transesterificación o alcoholisis (Gerpen, 2005, 2006; Vicente, 2006] de aceites vegetales utilizando enzimas como catalizadores, es igual al obtenido por los procesos convencionales a través de catálisis inorgánica. Las características de este biocombustible son similares a las del petrodiesel, y se puede mezclar con gasóleo en cualquier proporción (Demirbas, 2002; Zhang, 2003a). En la transesterificación intervienen un mol de triglicérido y tres moles de alcohol para producir uno de glicerina y tres de alquil-éster (biodiesel). La reacción de transesterificación enzimática de triglicéridos es:
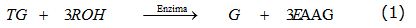
donde TG: triglicérido, ROH: alcohol, G: glicerol y EAAG: ésteres alquílicos de ácidos grasos. El alcohol empleado en esta reacción es preferiblemente de cadena corta para evitar la formación de una emulsión estable entre la glicerina y el biodiesel al finalizar la reacción (Schuchardt, 1998; Demirbas, 2006; Marchetti, 2007). La mayor parte del biodiesel que se comercializa en el mundo se produce empleando metanol, pero se han realizado trabajos donde se utiliza etanol, propanol y butanol (Lang, 2001; Gerpen, 2005; Benjumea, 2007).
Factores que afectan el proceso de transesterificación
La alcoholisis de aceites vegetales depende de la temperatura y tiempo de reacción, relación molar alcohol:aceite vegetal, tipo de alcohol, tipo y concentración de catalizador, intensidad del mezclado y contenido de ácidos grasos libres (AGL) y humedad (Ma, 1999a, b; Hernández, 2008; Sharma, 2008). Sin embargo, cuando se utilizan lipasas se deben considerar otras variables como: tipo de solvente, pH del medio reactante, microorganismo que genera la enzima y estado libre o inmovilizado de la enzima (Demirbas, 2008). A continuación se analizan los efectos de las condiciones de operación en la transesterificación de aceites vegetales sobre el rendimiento de la reacción, reportados en la literatura.
Temperatura de reacción. En los procesos biocatalíticos la tempera-tura de reacción es más baja que la utilizada en catálisis inorgánica, debido a que las altas temperaturas desnaturalizan las enzimas, evaporan el solvente cuando éste es utilizado en la reacción (Lu, 2007) y favorece la reacción de hidrólisis (Noureddini, 2005). El rango de temperatura más utilizado en la catálisis enzimática está entre 35-50 °C. Sin embargo, Köse (2002) reportó un rendimiento del 90% utilizando una temperatura de 60 °C al transesterificar a-ceite de semillas de algodón con Candida antarctica en estado libre. Soumanou (2003)encontró que el rendimiento al transesterificar aceite de girasol con R. miehei, a temperaturas de 35, 40 y 45°C, alcanzó valores de 37, 43 y 63%, respectivamente. Esto muestra que al aumentar la temperatura de reacción, dentro del rango limitado por la enzima, el rendimiento aumenta.
Relación molar alcohol:aceite vegetal. Por la estequiometría de la reacción se requiere una relación molar alcohol:aceite de 3:1, la cual se debe mantener en la catálisis enzimática, pero como la alcoholisis es reversible, se necesita alimentar un exceso de alcohol para favorecer la reacción directa. Se ha reportado (Tamalampudi, 2008) que aun con la cantidad estequiométrica de alcohol, la enzima se inhibe así esté inmovilizada. Hay enzimas que soportan mayor concentración de alcohol que otras, como la P. fluorescens, quemantiene su actividad hasta una relación de 4.5:1 (Soumanou, 2003). Eso se debe a que en algunas cepas de la Pseudomona los ácidos grasos insaturados de la membrana celular se isomerizan de cis a trans haciéndola más tolerante a solventes orgánicos (Heipieper, 1994). Para evitar la inhibición de las enzimas por el alcohol, éste se adiciona a diversos tiempos durante la reacción, como es el caso donde se realizan tres adiciones sucesivas de 1/3 del equivalente molar del alcohol (Lu, 2007).
Tipo de alcohol. El rendimiento de la reacción depende del alcohol y la lipasa utilizada (Nelson, 1996). Se ha reportado [Nelson, 1996] que la lipasa de M. miehei es más eficiente con alcoholes primarios, mientras que la lipasa de C. antarctica lo es con alcoholes secundarios. También se ha encontrado (Noureddini, 2005) que en la etanólisis de aceite de soya con P. cepacia inmovilizada el rendimiento es del 65% y con metanol del 47%. Resultados similares se lograron con aceite de soya y M. miehei (Nelson, 1996), y aceite de girasol y P. cepacia (Mittelbach, 1990). Esto se debe a que algunas lipasas son más eficientes con alcoholes de cadena larga que con alcoholes de cadena corta (Fukuda, 2001). Sin embargo, se ha establecido (Tamalampudi, 2008) que el rendimiento de la alcoholisis de aceite de jatrofa con R. orizae inmovilizada es mayor con metanol que con etanol. Esto se atribuye al bajo peso molecular y la alta polaridad del metanol, pues estas características permiten un mayor contacto con la enzima debido al aumento en la velocidad de difusión a través de la membrana celular (Hama, 2004).
Solvente. En la catálisis enzimática se presentan dificultades como la baja solubilidad del alcohol con los demás componentes de la reacción y el recubrimiento de la enzima por la glicerina (Royon, 2006). Para evitar estos inconvenientes se utilizan solventes como hexano, terbutanol, octano, acetona y éter de petróleo (Soumanou, 2003). En la alcoholisis de aceite de Madhuca indica con P. cepacia libre utilizando octano como solvente se alcanzó un rendimiento del 84%, mientras que sin solvente fue del 80% (Veena, 2007). Soumanou (2003) evaluó el rendimiento al transesterificar aceite de girasol con R. miehei, utilizando diversos tipos de solventes, y encontró que al utilizar enzimas inmovilizadas se obtienen mayores rendimientos con solventes no polares, lo cual se debe a que dichos solventes no retiran el agua esencial de las enzimas, prolongando su actividad catalítica (Lu, 2007). Algunas lipasas, como la R. miehei, T. lanuginosa y P. flourescens, se ven inhibidas al utilizar solventes orgánicos polares, como la acetona (Soumanou, 2003). Aunque el rendimiento de la alcoholisis aumenta al utilizar solventes, también lo hacen los costos de producción al recuperar y purificar el solvente.
Tipo de biocatalizador. Las lipasas utilizadas se producen de forma extra o intracelular. Las primeras requieren de métodos de purificación para su obtención, elevando sus costos en el mercado (Fukuda, 2001). Debido a esto, se han desarrollado métodos para su inmovilización, incrementando su eficiencia y reutilización en nuevas reacciones (Yahya, 1998; Ranganathan, 2008). Se ha encontrado (Shweta, 2007) que en la alcoholisis de aceite de jatrofa con P. cepacia se alcanzan rendimientos del 63 y 79% en 24 h, mientras que en la metanólisis de aceite de soya, con esta misma lipasa, las conversiones son de 41 y 65% mol en 1 h cuando la lipasa se encuentra libre e inmovilizada, respectivamente (Noureddini, 2005). Esto quiere decir que el rendimiento de la reacción aumenta al inmovilizar la enzima debido a la protección que brinda el soporte a los cambios del microambiente de la reacción (Ghamgui, 2007).
Concentración de biocatalizador. Cuando se usan enzimas existe un rango de concentración en el cual se deben agregar, y depende de la lipasa y las condiciones del proceso. Noureddini agregó 300, 550 y 3000 mg de lipasa inmovilizada de P. cepacia en la metanólisis de aceite de soya en 1h y encontró rendimientos de 61, 65 y 47% mol, respectivamente. Para el mismo aceite con lipasa libre de C. viscosum agregando 10, 50, 75 y 100 mgde la lipasa se obtuvo rendimientos de 50, 61, 69 y 48%, en 8 h (Shweta, 2004). Esto indica que una cantidad elevada de biocatalizador limita el rendimiento, lo cual se debe a que la viscosidad del medio aumenta, dificultando el contacto entre los componentes (Shweta, 2004). Aunque el aumento en la cantidad de lipasa mejora el ren-dimiento (Noureddini, 2005), éste no es muy significativo, pero sí los costos del proceso, debido a la cantidad de enzima adicionada.
Tiempo de reacción. En la catálisis enzimática este parámetro puede ser mayor que el utilizado en la catálisis química, como lo reportó Tamalampudi (2008) cuando transesterificó aceite de jatrofa con R. oryzae durante 60 h y obtuvo un rendimiento del 80%, utilizando una relación molar metanol:aceite del 3:1 y un contenido de humedad del 5%. Sin embargo, Noureddini (2005) reportó que al transesterificar aceite de soya con Pseudomona cepacia utilizando una relación molar etanol:aceite de 9.5:1 y un porcentaje de agua del 3%, obtuvo un rendimiento del 63% mol al cabo de 1 h, y a las mismas condiciones pero a un tiempo de 5 h halló que el rendimiento aumentó sólo hasta el 67%.
Intensidad del mezclado. En la catálisis enzimática no sólo es importante agitar al comienzo de la reacción, sino también, durante el transcurso de ella, ya que una vez alimentados los reactivos se forma un sistema de tres fases inmiscibles entre el aceite, el metanol y la enzima (Anjana, 2000; Meher, 2006). Al final de la reacción no se requiere agitación, ya que se busca desestabilizar la emulsión formada y dar paso a la separación de las fases (biodiesel/glicerina/enzima). Es de anotar que el efecto del mezclado en la cinética de la transesterificación es la base para el escalado y diseño del proceso (Barnwal, 2005). En este tipo de catálisis se aconseja una velocidad de agitación entre 150-200 r. p. m. para no afectar la estructura de la lipasa. Sin embargo, se han reportado (Hsu, 2001) velocidades de agitación de 500 y 700 rpm, sin efec-tos importante durante la reacción. Cuando la lipasa se encuentra inmovilizada en un soporte sólido, se requiere mayor velocidad de agitación para aumentar la transferencia de masa en el soporte y disminuir la saturación de los poros del soporte con la glicerina (Shimada, 2002).
Contenido de ácidos grasos libres (AGL) y humedad. Se ha encontrado (Freedman, 1984; Recinos, 2005) que en la catálisis inorgánica altos contenidos de AGL y humedad favorecen el proceso desaponificación. En la catálisis biológica altos valores de estos parámetros no promueven la reacción de saponificación debido a la alta especificidad de las enzimas (Li, 2007; Watanabe, 2001). Se encontró (Li, 2007) que células inmovilizadas de R. oryzae sintetizan biodiesel a partir de aceites de colza con alto grado de acidez. Tamalampudi (2008) reporta que con humedades de 0,5 y 10% en la transesterificación de aceite de jatrofa con la lipasa inmovilizada del R. Orizae se alcanzaron rendimientos de 50, 80 y 60%, respectivamente. Resultados similares se reportaron cuando se transesterificó aceite de jatrofa (Shweta, 2007) y aceite de soya con P. cepacia (Noureddini, 2005), lo cual indica que el rendimiento aumenta hasta un valor límite cuando se incrementa el contenido de agua. Este aumento se explica debido a que algunas lipasas requieren de la interfase agua-aceite para iniciar su actividad catalítica (Lu, 2007). Sin embargo, un incremento en el contenido de agua por encima del valor límite reduce la formación de ésteres debido a que las lipasas en medios muy acuosos favorecen la reacción de hidrólisis (Noureddini, 2005).
En la Tabla 1 se resumen las condiciones de operación, encontradas en la literatura, del proceso de síntesis de biodiesel con lipasas como biocatalizadores. En la tabla se muestra que las lipasas más utilizadas provienen de la bacteria P. cepacia y del hongo R. orizae debido a su facilidad de manejo, así como también a su resistencia frente a condiciones precarias de la reacción. También se observa que la forma más conveniente de adicionar la lipasa a la reacción es inmovilizándola en un soporte sólido, con el fin de obtener mayor rendimiento y garantizar su reutilización en nuevas reacciones sin perder su actividad catalítica. Este método se lleva a cabo a bajas temperaturas (35-50 °C), y no requiere un control rigurosamente del contenido de humedad (0-30%) y de AGL. Además, se observa que sólo se requiere la cantidad estequiométrica de alcohol para efectuar la transesterificación: esto repercute en economía para el proceso. Se pueden alcanzar rendimientos hasta del 69% mol utilizando tiempos de reacción de 1 h, mientras que rendimientos mayores al 80% se obtienen a las 7-90 h. La información presentada en la Tabla 1 complementa lo reportado por Fukuda ( 2001), Shimada (2002) y Ranganathan (2008).
Conclusiones
Para alcanzar rendimientos altos (>90%) en biocatálisis se recomienda: inmovilizar enzimas provenientes de la bacteria P.cepacia y del hongo R. orizae, en un soporte muy poroso; mante-ner una velocidad de agitación alrededor de 600 r. p. m. para no afectar la estructura de la lipasa; utilizar aceites con humedad me-nor al 25%; solventes no polares; alcoholes de cadena larga (se su-giere bioetanol anhidro por su carácter renovable) adicionado por etapas; una relación molar alcohol: aceite igual a la estequiométrica; y una temperatura de reacción y concentración de biocatalizador adecuados a la enzima utilizada, ya que éstas dos variables, al igual que el tipo de alcohol, dependen intrínsecamente del tipo de lipasa.
La transesterificación biológica tiene gran impacto en el desarrollo de una tecnología verdaderamente sostenible en la producción de biocombustibles, dado que la reacción se lleva a cabo a menor temperatura (35-50 °C, menor consumo de energía) que en la catálisis química (65-90 °C), se emplea etanol en lugar de metanol y no se requiere catalizadores químicos que afecten el ambiente.
Se plantea como trabajo futuro transesterificar aceites de fritura usados con lipasas del páncreas del pollo y de semillas de zapallo, en forma libre e inmovilizada en quitosan, colágeno extraído de la pata de la res, y una mezcla quitosan/colágeno.
Bibliografía
AENOR., Documentación: recopilación de normas UNE/ AENOR., 2ª ed. Madrid: AENOR, 1997. [ Links ]
Arocena, R., Sutz, J., Latin American Universities: From an original revolution to an uncertain transition., Higher Education 50, 2005, pp. 573-592. [ Links ]
Carreras, A., Granjel, M., Gutiérrez, B. M., Rodríguez, J. A., Guía práctica para la elaboración de un trabajo científico., Cita. Bilbao, 1994, 263 pp. [ Links ]
Crespo García, F., El artículo científico: ¿rutina o método?., La Haban, Ediciones CENSA, 1987, 323 p. [ Links ]
Day, R., Cómo escribir y publicar trabajos científicos., Washington: Organización Panamericana de la Salud, 1990. [ Links ]
Eco, H., Cómo se hace una tesis. Técnicas y procedimientos de investigación, estudio y escritura., Barcelona, GEDISA, 1982, 267 p. [ Links ]
Etzkowitz, H., Research groups as quasi-firms: the invention of the entrepreneurial university., Research Policy 32, 2003, pp. 109-121. [ Links ]
Etzkowitz, H., Leydesdorff, L., The dynamics of innovation: from National Systems and Mode 2 to a Triple Helix of university-industry-government relations., Research Policy 29, 2000, pp. 109-123. [ Links ]
Geuna, A., The internationalization of European universities: a return to medieval roots., Minerva XXXVI (3), 1998, pp. 253-270. [ Links ]
Geuna, A., European Universities: An Interpretive History., MERIT, University of Limburg, 1996, 56 p. [ Links ]
Hernández, S. R., Metodología de la investigación., Tomo 2. La Habana, Editorial Félix Varela, 2003, 475 p. [ Links ]
Kendall, K. E., Kendall, J. E., Análisis y Diseño de Sistemas., México, Prentice Hall,1997, 913 p. [ Links ]
Rudy, W., The university of Europe, 1100-1914., A. History, Cranbury, Associated University Press, 1984. [ Links ]
Wittrock, B., The Modern University: The Three Transformations., in S.Rothblatt, and B. Wittrock (eds.), 1993. ` [ Links ]
UNESCO., Guía para la redacción de artículos científicos destinados a la publicación., 2 ed., París, UNESCO, 1983. [ Links ]














